文档内容
2022 学年第一学期高三化学教学质量调研试卷
相对原子质量:H-1 O-16 S-32 P-31 Cl-35.5 C-12 N-14 Na-23
一、选择题(共40分,每小题2分,每小题只有一个正确选项)
1. 生活中处处有化学,下列叙述正确的是
A. HB铅笔芯的成分为二氧化铅 B. 碳酸氢钠可做食品膨松剂
C. 青铜和黄铜是不同结构的单质铜 D. 焰火中红色来源于钠盐灼烧
2. 下列变化需要加入氧化剂才能实现的转化是
A. 浓HSO →SO B. KClO→O C. HS→SO D. →CO
2 4 2 3 2 2 2 2
3. 能用于比较硫、氯两种元素非金属性强弱的是
A. 熔点:S > Cl B. 酸性:HClO > H SO
2 4 2 4
C. 相对原子质量:Cl > S D. 氧化性:HClO>HSO
2 3
4. 关于乙烯的说法正确的是
A. 等摩尔乙烷和乙烯中,化学键数相同 B. 所有原子在一直线上
C. 既有极性键又有非极性键 D. 属于极性分子
的
5. 下列化学用语正确 是
A. 碳原子的核外电子轨道表示式:
B. 的电子式:
C. 丙烷的比例模型:
D. 原子核内有6个中子的碳原子:
6. 过氧化氢溶液是一种常见的消毒剂,以下对其描述不符合事实的是
A. 外用消毒剂 B. 有漂白作用 C. 需密封保存 D. 有强氧化性,无还原性
7. 在醋酸溶液中,CHCOOH电离达到平衡的标志是
3
A. 溶液显电中性 B. 氢离子浓度恒定不变
C. c(H+) = c(CHCOO¯) D. 溶液中检测不出CHCOOH分子存在
3 3
8. 能用分液漏斗分离的一组物质是
A. AgCl 和NaCl 溶液 B. 苯和水C. 溴和四氯化碳 D. 乙酸和乙酸乙酯
9. 下列生产中,水没有参与化学反应的是
A. 氯碱工业 B. 侯氏制碱 C. 湿法炼铜 D. 接触法制硫酸
10. 加油站有不同型号的汽油,下列说法正确的是
A. 汽油属于纯净物 B. 煤通过干馏可以转化为汽油
C. 石油分馏可以获得汽油 D. 重油的裂解可以提高汽油的产量
11. FeS 与酸反应时生成HS,HS 与HO 相似,易分解。实验室用过量稀硫酸与FeS 颗粒混合,不可能
2 2 2 2 2 2 2 2
生成的物质是
A. HS B. S C. FeS D. FeSO
2 4
12. 海水提溴常用 达到富集目的,此反应相关物质的叙述正确的是
A. 在常温常压下是红棕色的气体 B. 属于离子化合物
C. 属于非电解质的只有 D. HO分子的空间构型是直线型
2
13. 有关水处理的方法错误的是
A. 用可溶性的铝盐、铁盐处理水中悬浮物
B. 用氯气处理水中的Cu2+、Hg2+等重金属离子
C. 用石灰、纯碱等碱性物质处理废水中的酸
D. 用烧碱处理含高浓度 的废水并回收利用氨
14. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. c(H+)/c(OH-)=1×10-14的溶液:Ca2+、Na+、 、
B. 0.1 mol·L-1 KOH溶液: 、Na+、I-、
C. 能使pH试纸显深红色的溶液:Fe3+、Cl-、Ba2+、SCN-
D. 0.1 mol·L-1NaClO溶液:HS-、Na+、Cl-、
15. 测定CuSO •xH O中水的含量,如果实验值偏低,可能的原因是
4 2
A. 盛晶体的坩埚未完全干燥
B. 加热后白色粉末在空气中冷却
C. 加热后有少量黑色固体产生
D. 加热时有少量晶体溅出
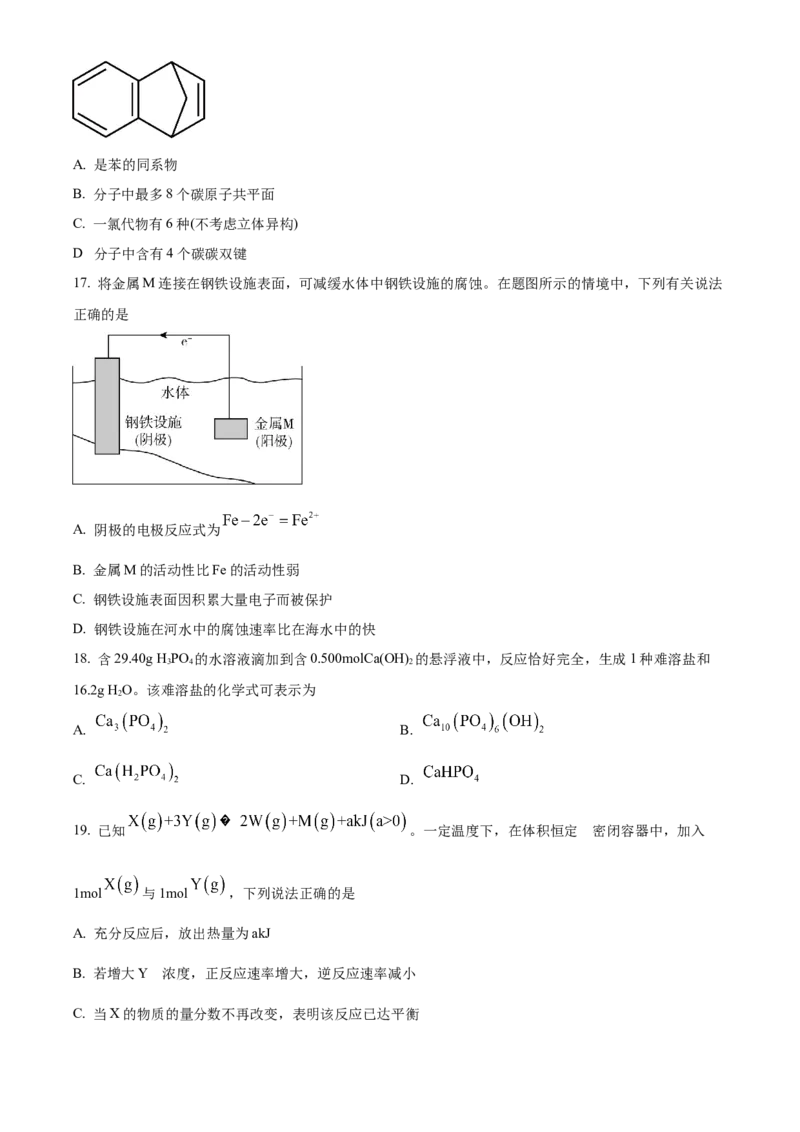
16. 苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合物,下列说法正确的是A. 是苯的同系物
B. 分子中最多8个碳原子共平面
C. 一氯代物有6种(不考虑立体异构)
.
D 分子中含有4个碳碳双键
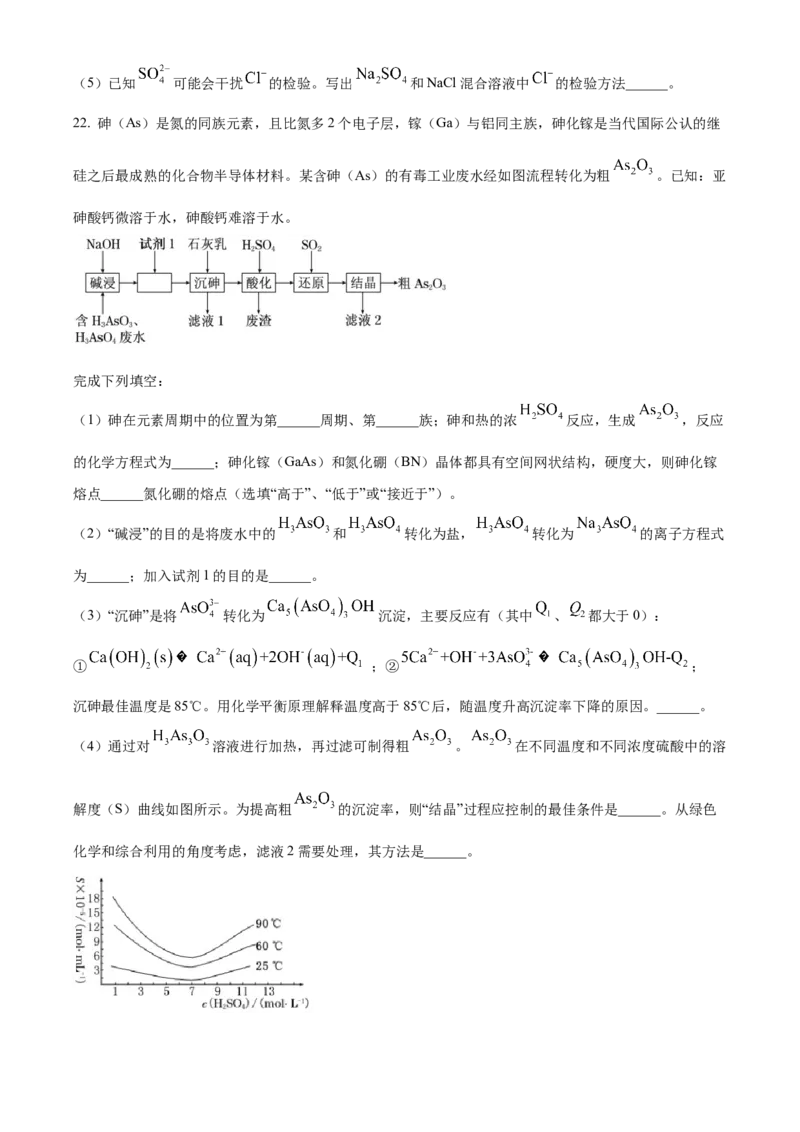
17. 将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境中,下列有关说法
正确的是
A. 阴极的电极反应式为
B. 金属M的活动性比Fe的活动性弱
C. 钢铁设施表面因积累大量电子而被保护
D. 钢铁设施在河水中的腐蚀速率比在海水中的快
18. 含29.40g HPO 的水溶液滴加到含0.500molCa(OH) 的悬浮液中,反应恰好完全,生成1种难溶盐和
3 4 2
16.2g HO。该难溶盐的化学式可表示为
2
A. B.
C. D.
19. 已知 。一定温度下,在体积恒定 的密闭容器中,加入
1mol 与1mol ,下列说法正确的是
A. 充分反应后,放出热量为akJ
的
B. 若增大Y 浓度,正反应速率增大,逆反应速率减小
C. 当X的物质的量分数不再改变,表明该反应已达平衡D. 当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
20. 室温下,反应 的平衡常数 。将 溶液和氨水按一
定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒
物质的量浓度关系正确的是
A. 0.2mol/L氨水:
B. 溶液( ):
C. 0.2mol/L氨水和 溶液等体积混合:
D. 氨水和 溶液等体积混合:
二、综合题(共60分)
21. 硫及其化合物在生产、生活中有广泛应用。
(1)硫原子最外层有______种不同运动状态的电子,其中能量最高的电子所占电子亚层符号为______。
(2)硫与同主族 的氧元素相比,两者各自形成气态氢化物稳定性 ______ (选填“>”、“<”或“=”
下同),分别与氢元素形成化学键键能大小关系为H—O______H—S。
(3)正交硫和单斜硫是硫常见的两种单质,它们互为______。已知: (正交)= (单斜)―2.64kJ。
正交硫与单斜硫相比,相对比较稳定的是______。已知通常状况下4g硫粉完全燃烧放出37kJ的热量,写
出该反应的热化学方程式______。
(4)同温同浓度的 、 、 三种溶液, 最大的是______;经测定
溶液中 ,则 溶液呈______(填“酸”或“碱”)性;等物质的量浓
度的下列四种溶液:① ② ③ ④ ,溶液中水的电离程度由大到小排
列顺序为______。(5)已知 可能会干扰 的检验。写出 和NaCl混合溶液中 的检验方法______。
22. 砷(As)是氮的同族元素,且比氮多2个电子层,镓(Ga)与铝同主族,砷化镓是当代国际公认的继
硅之后最成熟的化合物半导体材料。某含砷(As)的有毒工业废水经如图流程转化为粗 。已知:亚
砷酸钙微溶于水,砷酸钙难溶于水。
完成下列填空:
(1)砷在元素周期中的位置为第______周期、第______族;砷和热的浓 反应,生成 ,反应
的化学方程式为______;砷化镓(GaAs)和氮化硼(BN)晶体都具有空间网状结构,硬度大,则砷化镓
熔点______氮化硼的熔点(选填“高于”、“低于”或“接近于”)。
(2)“碱浸”的目的是将废水中的 和 转化为盐, 转化为 的离子方程式
为______;加入试剂1的目的是______。
(3)“沉砷”是将 转化为 沉淀,主要反应有(其中 、 都大于0):
① ;② ;
沉砷最佳温度是85℃。用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因。______。
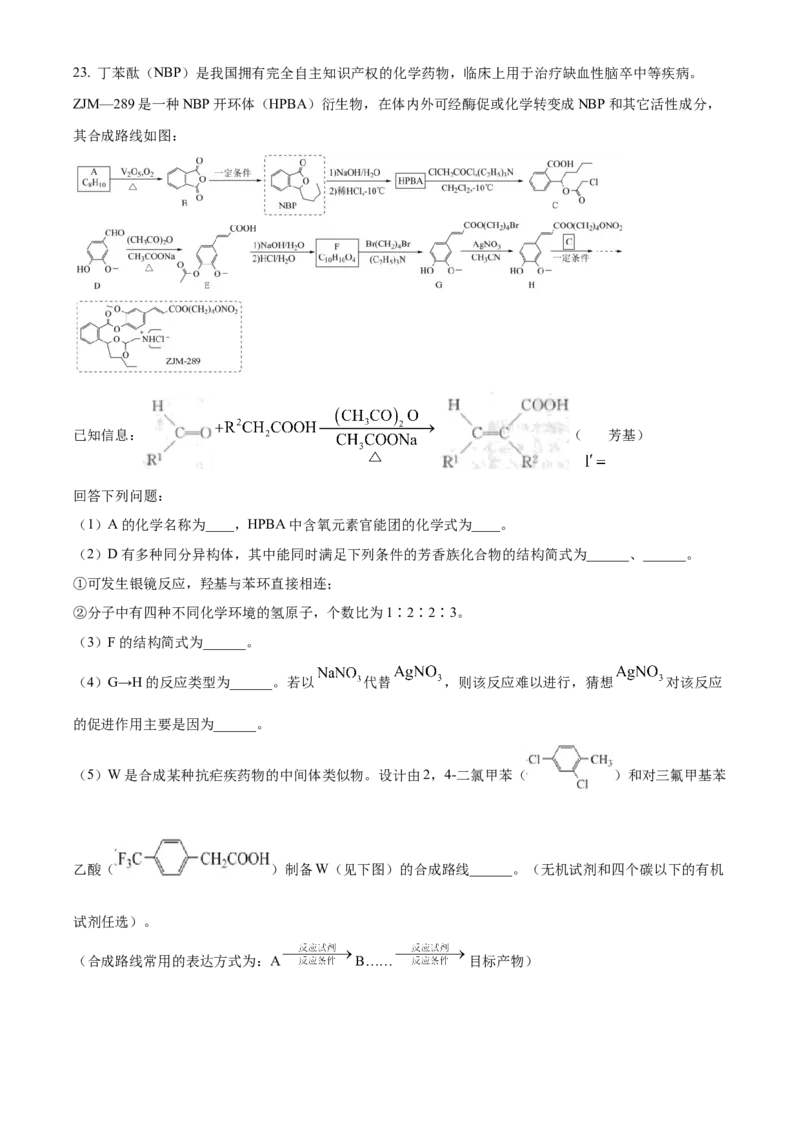
(4)通过对 溶液进行加热,再过滤可制得粗 。 在不同温度和不同浓度硫酸中的溶
解度(S)曲线如图所示。为提高粗 的沉淀率,则“结晶”过程应控制的最佳条件是______。从绿色
化学和综合利用的角度考虑,滤液2需要处理,其方法是______。23. 丁苯酞(NBP)是我国拥有完全自主知识产权的化学药物,临床上用于治疗缺血性脑卒中等疾病。
ZJM—289是一种NBP开环体(HPBA)衍生物,在体内外可经酶促或化学转变成NBP和其它活性成分,
其合成路线如图:
已知信息: ( 芳基)
回答下列问题:
(1)A的化学名称为____,HPBA中含氧元素官能团的化学式为____。
(2)D有多种同分异构体,其中能同时满足下列条件的芳香族化合物的结构简式为______、______。
①可发生银镜反应,羟基与苯环直接相连;
②分子中有四种不同化学环境的氢原子,个数比为1∶2∶2∶3。
(3)F的结构简式为______。
(4)G→H的反应类型为______。若以 代替 ,则该反应难以进行,猜想 对该反应
的促进作用主要是因为______。
(5)W是合成某种抗疟疾药物的中间体类似物。设计由2,4-二氯甲苯( )和对三氟甲基苯
乙酸( )制备W(见下图)的合成路线______。(无机试剂和四个碳以下的有机
试剂任选)。
(合成路线常用的表达方式为:A B…… 目标产物)24. Ⅰ.次氯酸钠溶液和二氯异氰尿酸钠( )都是常用的杀菌消毒剂。NaClO可用于制备二
氯异氰尿酸钠。
(1)NaClO溶液可由低温下将 缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为______;
用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用
减弱,其原因是______。
(2)有研究显示,南极臭氧空洞中的污染物硝酸氯( )与次氯酸钠在结构上有类似之处。下列
推测有一项不合理,该选项是______。
A. 具有强氧化性 B. 与NaOH溶液反应可生成两种钠盐
C. 与盐酸作用能产生氯气 D. 水解生成盐酸和硝酸
Ⅱ.二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标
准。实验检测原理为: ; ;
。
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸
和过量KI溶液,密封在暗处静置5min;用 标准溶液滴定至溶液呈微黄色,加入
淀粉指示剂继续滴定至终点,消耗 溶液20.00mL。
(3)滴定达到终点的现象为:溶液由______色变______色,且半分钟内不再改变。
(4)通过计算判断该样品是否为优质品______。(写出计算过程)
该样品的有效氯= ×100%
(5)若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值______(填“偏高”或“偏低”)。