文档内容
专练 10 氧化还原反应规律
1.[2021·浙江卷6月]关于反应KHIO +9HI===2KI+4I +6HO,下列说法正确的是(
2 3 6 2 2
)
A.KHIO 发生氧化反应
2 3 6
B.KI是还原产物
C.生成12.7 g I 时,转移0.1 mol电子
2
D.还原剂与氧化剂的物质的量之比为7∶1
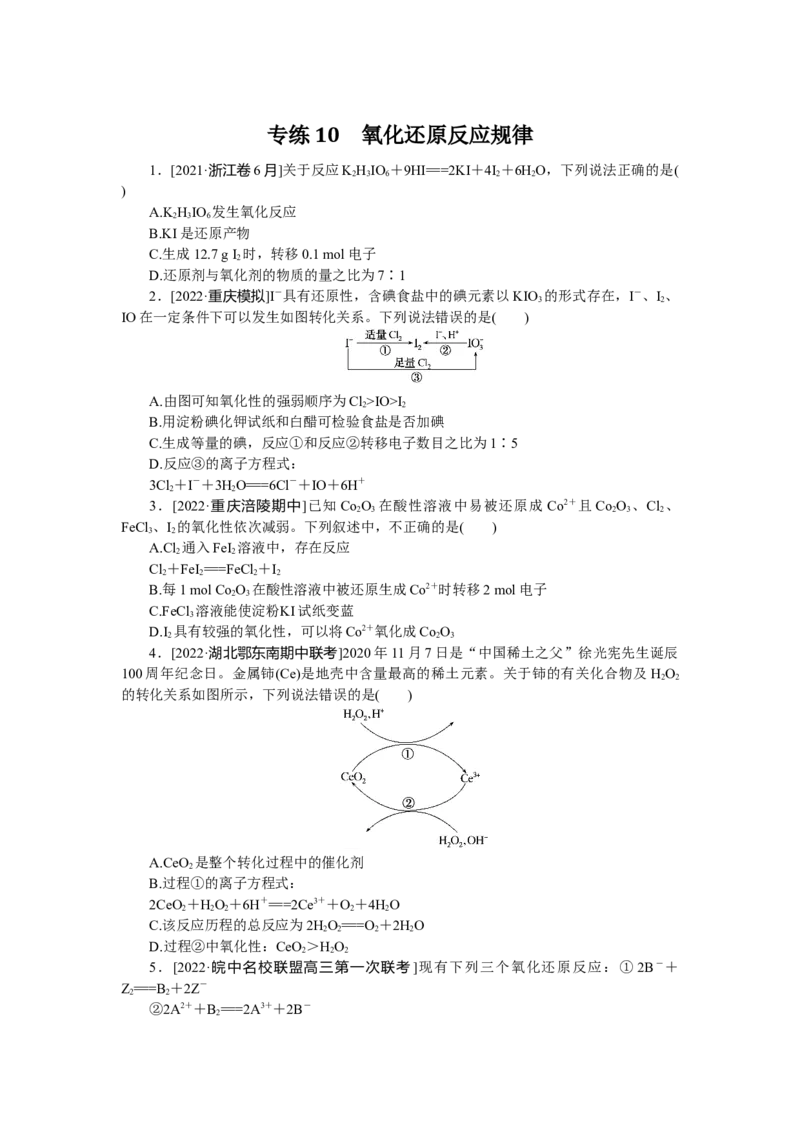
2.[2022·重庆模拟]I-具有还原性,含碘食盐中的碘元素以KIO 的形式存在,I-、I 、
3 2
IO在一定条件下可以发生如图转化关系。下列说法错误的是( )
A.由图可知氧化性的强弱顺序为Cl>IO>I
2 2
B.用淀粉碘化钾试纸和白醋可检验食盐是否加碘
C.生成等量的碘,反应①和反应②转移电子数目之比为1∶5
D.反应③的离子方程式:
3Cl+I-+3HO===6Cl-+IO+6H+
2 2
3.[2022·重庆涪陵期中]已知Co O 在酸性溶液中易被还原成 Co2+且Co O 、Cl 、
2 3 2 3 2
FeCl 、I 的氧化性依次减弱。下列叙述中,不正确的是( )
3 2
A.Cl 通入FeI 溶液中,存在反应
2 2
Cl+FeI===FeCl +I
2 2 2 2
B.每1 mol Co O 在酸性溶液中被还原生成Co2+时转移2 mol电子
2 3
C.FeCl 溶液能使淀粉KI试纸变蓝
3
D.I 具有较强的氧化性,可以将Co2+氧化成Co O
2 2 3
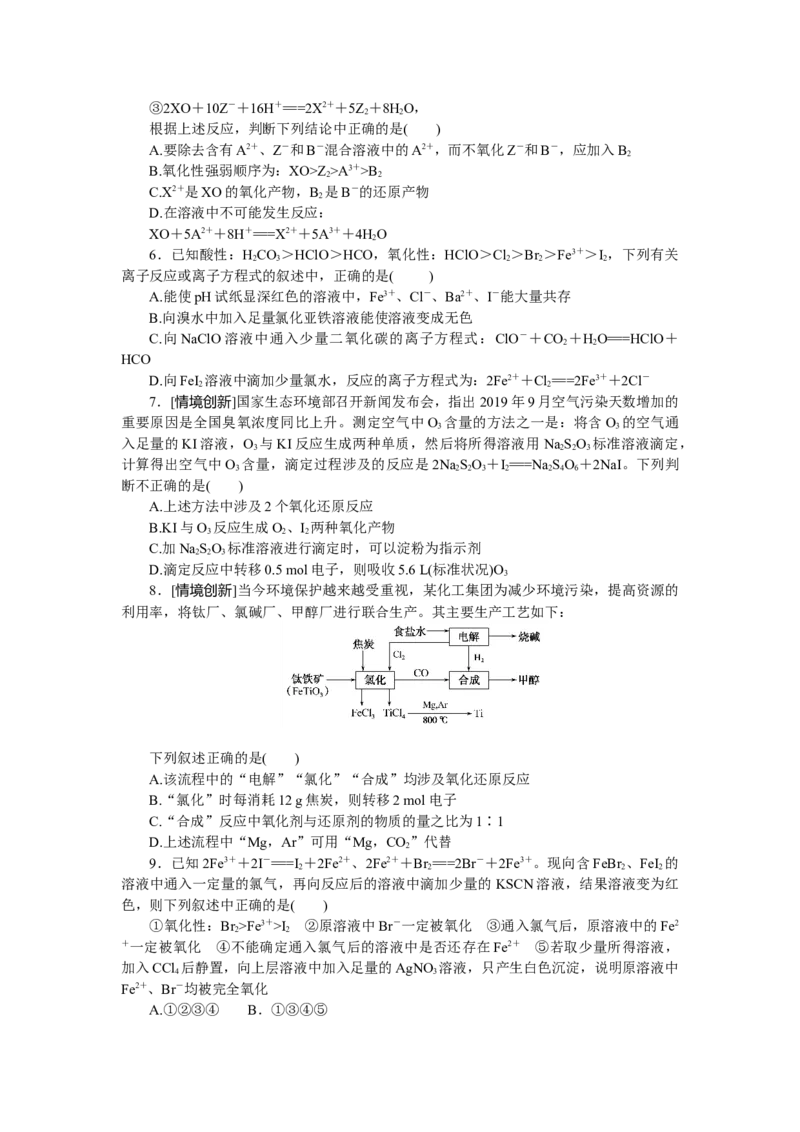
4.[2022·湖北鄂东南期中联考]2020年11月7日是“中国稀土之父”徐光宪先生诞辰
100周年纪念日。金属铈(Ce)是地壳中含量最高的稀土元素。关于铈的有关化合物及HO
2 2
的转化关系如图所示,下列说法错误的是( )
A.CeO 是整个转化过程中的催化剂
2
B.过程①的离子方程式:
2CeO+HO+6H+===2Ce3++O+4HO
2 2 2 2 2
C.该反应历程的总反应为2HO===O +2HO
2 2 2 2
D.过程②中氧化性:CeO>HO
2 2 2
5.[2022·皖中名校联盟高三第一次联考]现有下列三个氧化还原反应:① 2B-+
Z===B +2Z-
2 2
②2A2++B ===2A3++2B-
2③2XO+10Z-+16H+===2X2++5Z+8HO,
2 2
根据上述反应,判断下列结论中正确的是( )
A.要除去含有A2+、Z-和B-混合溶液中的A2+,而不氧化Z-和B-,应加入B
2
B.氧化性强弱顺序为:XO>Z >A3+>B
2 2
C.X2+是XO的氧化产物,B 是B-的还原产物
2
D.在溶液中不可能发生反应:
XO+5A2++8H+===X2++5A3++4HO
2
6.已知酸性:HCO >HClO>HCO,氧化性:HClO>Cl >Br >Fe3+>I ,下列有关
2 3 2 2 2
离子反应或离子方程式的叙述中,正确的是( )
A.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、I-能大量共存
B.向溴水中加入足量氯化亚铁溶液能使溶液变成无色
C.向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO +HO===HClO+
2 2
HCO
D.向FeI 溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl===2Fe3++2Cl-
2 2
7.[情境创新]国家生态环境部召开新闻发布会,指出2019年9月空气污染天数增加的
重要原因是全国臭氧浓度同比上升。测定空气中O 含量的方法之一是:将含O 的空气通
3 3
入足量的KI溶液,O 与KI反应生成两种单质,然后将所得溶液用NaSO 标准溶液滴定,
3 2 2 3
计算得出空气中O 含量,滴定过程涉及的反应是2NaSO +I===Na SO +2NaI。下列判
3 2 2 3 2 2 4 6
断不正确的是( )
A.上述方法中涉及2个氧化还原反应
B.KI与O 反应生成O、I 两种氧化产物
3 2 2
C.加NaSO 标准溶液进行滴定时,可以淀粉为指示剂
2 2 3
D.滴定反应中转移0.5 mol电子,则吸收5.6 L(标准状况)O
3
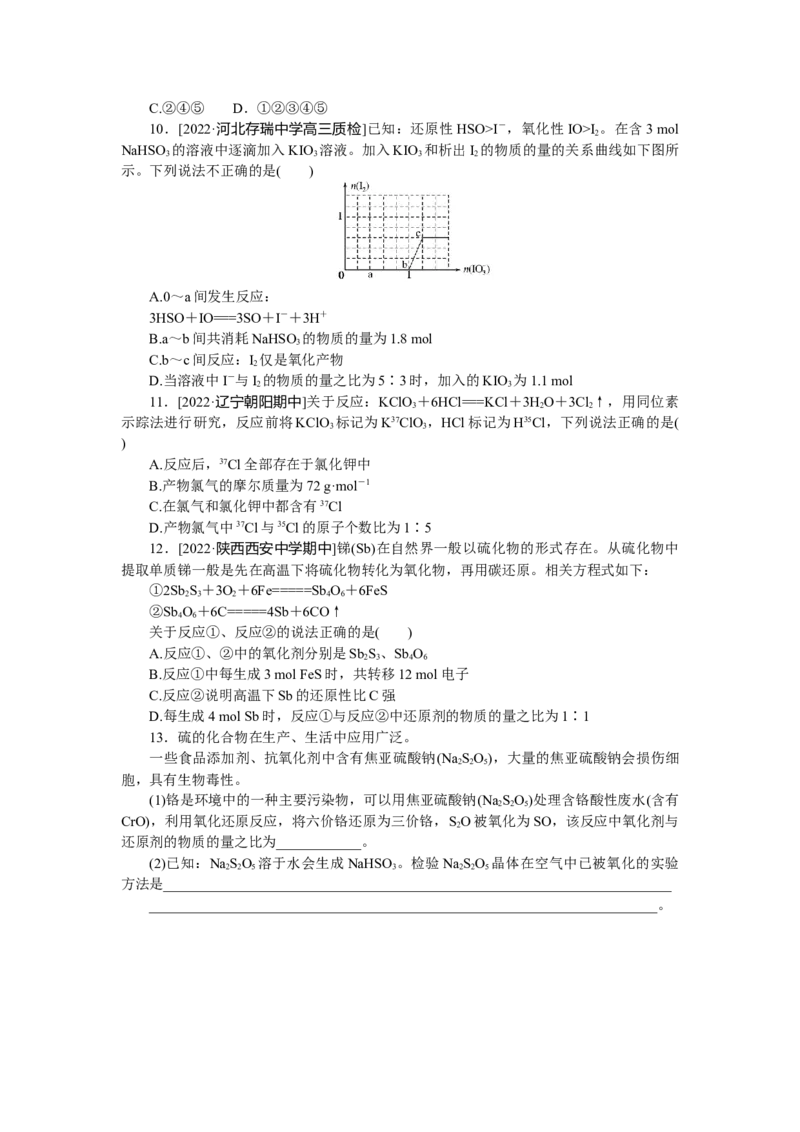
8.[情境创新]当今环境保护越来越受重视,某化工集团为减少环境污染,提高资源的
利用率,将钛厂、氯碱厂、甲醇厂进行联合生产。其主要生产工艺如下:
下列叙述正确的是( )
A.该流程中的“电解”“氯化”“合成”均涉及氧化还原反应
B.“氯化”时每消耗12 g焦炭,则转移2 mol电子
C.“合成”反应中氧化剂与还原剂的物质的量之比为1∶1
D.上述流程中“Mg,Ar”可用“Mg,CO”代替
2
9.已知2Fe3++2I-===I +2Fe2+、2Fe2++Br ===2Br-+2Fe3+。现向含FeBr 、FeI 的
2 2 2 2
溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 KSCN溶液,结果溶液变为红
色,则下列叙述中正确的是( )
①氧化性:Br >Fe3+>I ②原溶液中Br-一定被氧化 ③通入氯气后,原溶液中的Fe2
2 2
+一定被氧化 ④不能确定通入氯气后的溶液中是否还存在Fe2+ ⑤若取少量所得溶液,
加入CCl 后静置,向上层溶液中加入足量的AgNO 溶液,只产生白色沉淀,说明原溶液中
4 3
Fe2+、Br-均被完全氧化
A.①②③④ B.①③④⑤C.②④⑤ D.①②③④⑤
10.[2022·河北存瑞中学高三质检]已知:还原性HSO>I-,氧化性IO>I 。在含3 mol
2
NaHSO 的溶液中逐滴加入KIO 溶液。加入KIO 和析出I 的物质的量的关系曲线如下图所
3 3 3 2
示。下列说法不正确的是( )
A.0~a间发生反应:
3HSO+IO===3SO+I-+3H+
B.a~b间共消耗NaHSO 的物质的量为1.8 mol
3
C.b~c间反应:I 仅是氧化产物
2
D.当溶液中I-与I 的物质的量之比为5∶3时,加入的KIO 为1.1 mol
2 3
11.[2022·辽宁朝阳期中]关于反应:KClO +6HCl===KCl+3HO+3Cl↑,用同位素
3 2 2
示踪法进行研究,反应前将KClO 标记为K37ClO ,HCl标记为H35Cl,下列说法正确的是(
3 3
)
A.反应后,37Cl全部存在于氯化钾中
B.产物氯气的摩尔质量为72 g·mol-1
C.在氯气和氯化钾中都含有37Cl
D.产物氯气中37Cl与35Cl的原子个数比为1∶5
12.[2022·陕西西安中学期中]锑(Sb)在自然界一般以硫化物的形式存在。从硫化物中
提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原。相关方程式如下:
①2Sb S+3O+6Fe=====Sb O+6FeS
2 3 2 4 6
②Sb O+6C=====4Sb+6CO↑
4 6
关于反应①、反应②的说法正确的是( )
A.反应①、②中的氧化剂分别是Sb S、Sb O
2 3 4 6
B.反应①中每生成3 mol FeS时,共转移12 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4 mol Sb时,反应①与反应②中还原剂的物质的量之比为1∶1
13.硫的化合物在生产、生活中应用广泛。
一些食品添加剂、抗氧化剂中含有焦亚硫酸钠(Na SO),大量的焦亚硫酸钠会损伤细
2 2 5
胞,具有生物毒性。
(1)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(Na SO)处理含铬酸性废水(含有
2 2 5
CrO),利用氧化还原反应,将六价铬还原为三价铬,SO被氧化为SO,该反应中氧化剂与
2
还原剂的物质的量之比为____________。
(2)已知:NaSO 溶于水会生成NaHSO 。检验NaSO 晶体在空气中已被氧化的实验
2 2 5 3 2 2 5
方法是________________________________________________________________________
________________________________________________________________________。