文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练11 14道选择题+主观原理题
完卷时间:40分钟
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案
可能用到的相对原子质量:C-12 Fe-56
一、选择题(共42分,只有1个正确选项)
1.化学与生产、生活、密切相关,下列说法不正确的是
A.北京冬奥会吉祥物“冰墩墩”使用的聚乙烯属于有机高分子材料
B.“墨子号”卫星的成功发射实现了光纤量子通信,光纤的主要成分为二氧化硅
C.制造5G芯片的氮化铝晶圆属于无机非金属材料
D.焰火中的红色来源于钠盐灼烧
2.当将钼酸铵和磷酸盐的溶液进行酸化时,得到一种黄色沉淀12-磷钼酸铵,可利用该原
理进行磷酸盐的定量测定,反应为
。下列有关说法错误的
是
A.电负性:O>N>P>H
B. 与Cr同族,基态Mo原子的价层电子表示式为
C. 中H-N-H的键角比 中H-N-H的键角大
D. 和 的空间结构均为正四面体形
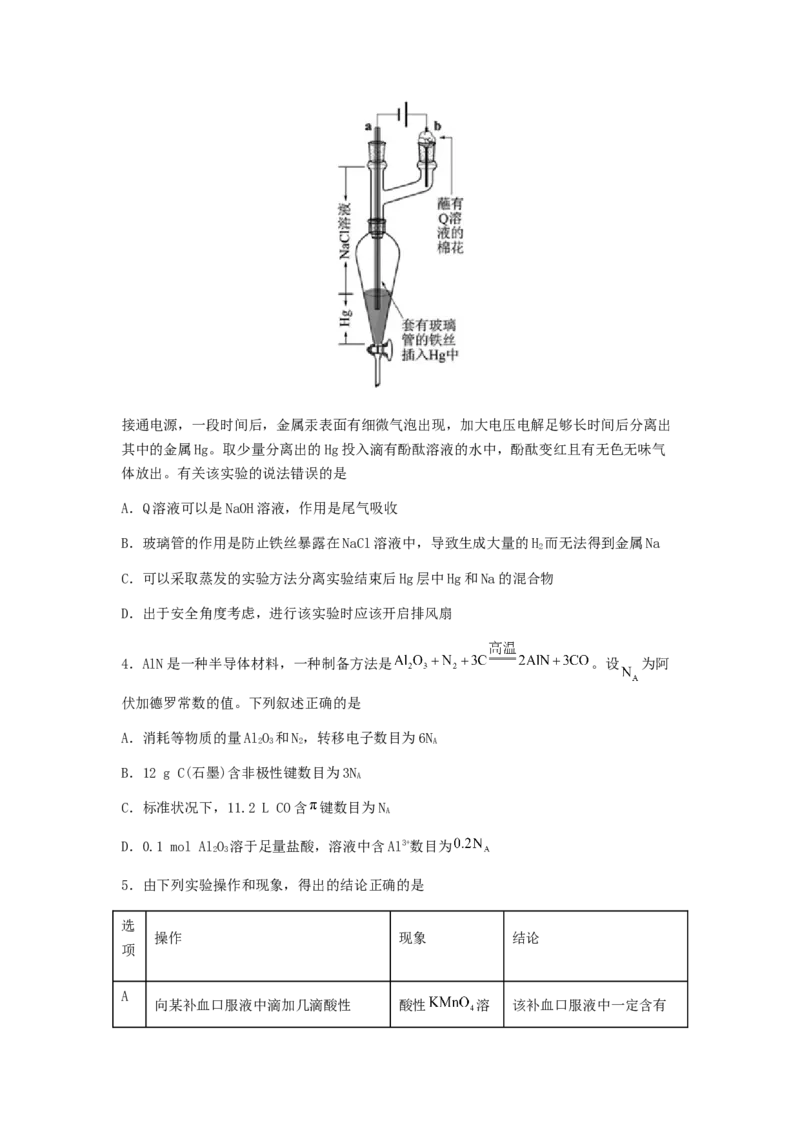
3.某同学查阅资料发现电解饱和食盐水也可以获得金属Na,但必须改进实验装置,装置
图和实验现象记录如下:接通电源,一段时间后,金属汞表面有细微气泡出现,加大电压电解足够长时间后分离出
其中的金属Hg。取少量分离出的Hg投入滴有酚酞溶液的水中,酚酞变红且有无色无味气
体放出。有关该实验的说法错误的是
A.Q溶液可以是NaOH溶液,作用是尾气吸收
B.玻璃管的作用是防止铁丝暴露在NaCl溶液中,导致生成大量的H 而无法得到金属Na
2
C.可以采取蒸发的实验方法分离实验结束后Hg层中Hg和Na的混合物
D.出于安全角度考虑,进行该实验时应该开启排风扇
4.AlN是一种半导体材料,一种制备方法是 。设 为阿
伏加德罗常数的值。下列叙述正确的是
A.消耗等物质的量AlO 和N,转移电子数目为6N
2 3 2 A
B.12 g C(石墨)含非极性键数目为3N
A
C.标准状况下,11.2 L CO含 键数目为N
A
D.0.1 mol AlO 溶于足量盐酸,溶液中含Al3+数目为
2 3
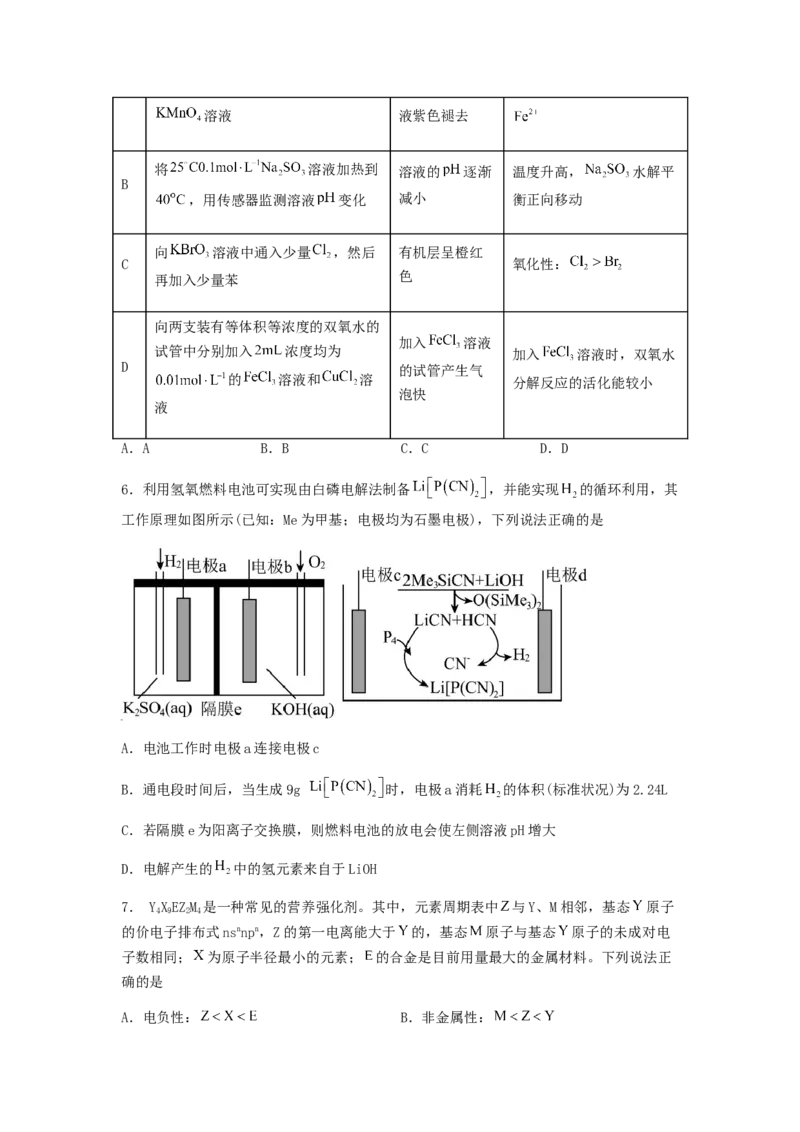
5.由下列实验操作和现象,得出的结论正确的是
选
操作 现象 结论
项
A
向某补血口服液中滴加几滴酸性 酸性 溶 该补血口服液中一定含有溶液 液紫色褪去
将 溶液加热到 溶液的 逐渐 温度升高, 水解平
B
,用传感器监测溶液 变化 减小 衡正向移动
向 溶液中通入少量 ,然后 有机层呈橙红
C 氧化性:
再加入少量苯 色
向两支装有等体积等浓度的双氧水的
加入 溶液
试管中分别加入 浓度均为 加入 溶液时,双氧水
D 的试管产生气
的 溶液和 溶 分解反应的活化能较小
泡快
液
A.A B.B C.C D.D
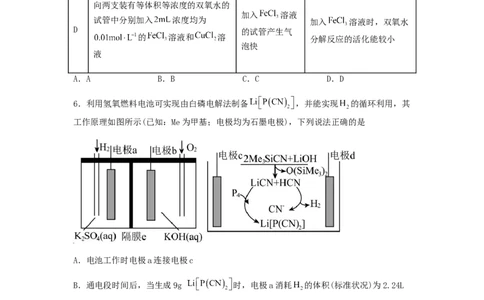
6.利用氢氧燃料电池可实现由白磷电解法制备 ,并能实现 的循环利用,其
工作原理如图所示(已知:Me为甲基;电极均为石墨电极),下列说法正确的是
A.电池工作时电极a连接电极c
B.通电段时间后,当生成9g 时,电极a消耗 的体积(标准状况)为2.24L
C.若隔膜e为阳离子交换膜,则燃料电池的放电会使左侧溶液pH增大
D.电解产生的 中的氢元素来自于LiOH
7. YXEZM 是一种常见的营养强化剂。其中,元素周期表中 与Y、M相邻,基态 原子
4 9 2 4
的价电子排布式nsnnpn,Z的第一电离能大于 的,基态 原子与基态 原子的未成对电
子数相同; 为原子半径最小的元素; 的合金是目前用量最大的金属材料。下列说法正
确的是
A.电负性: B.非金属性:C.简单氢化物的沸点: D.高温下, 的单质与 反应得到
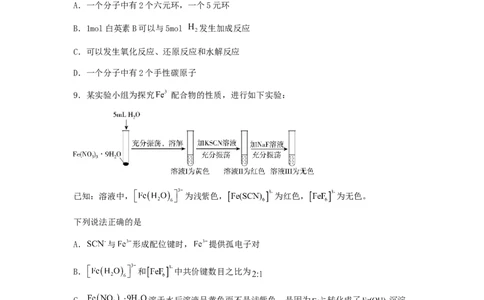
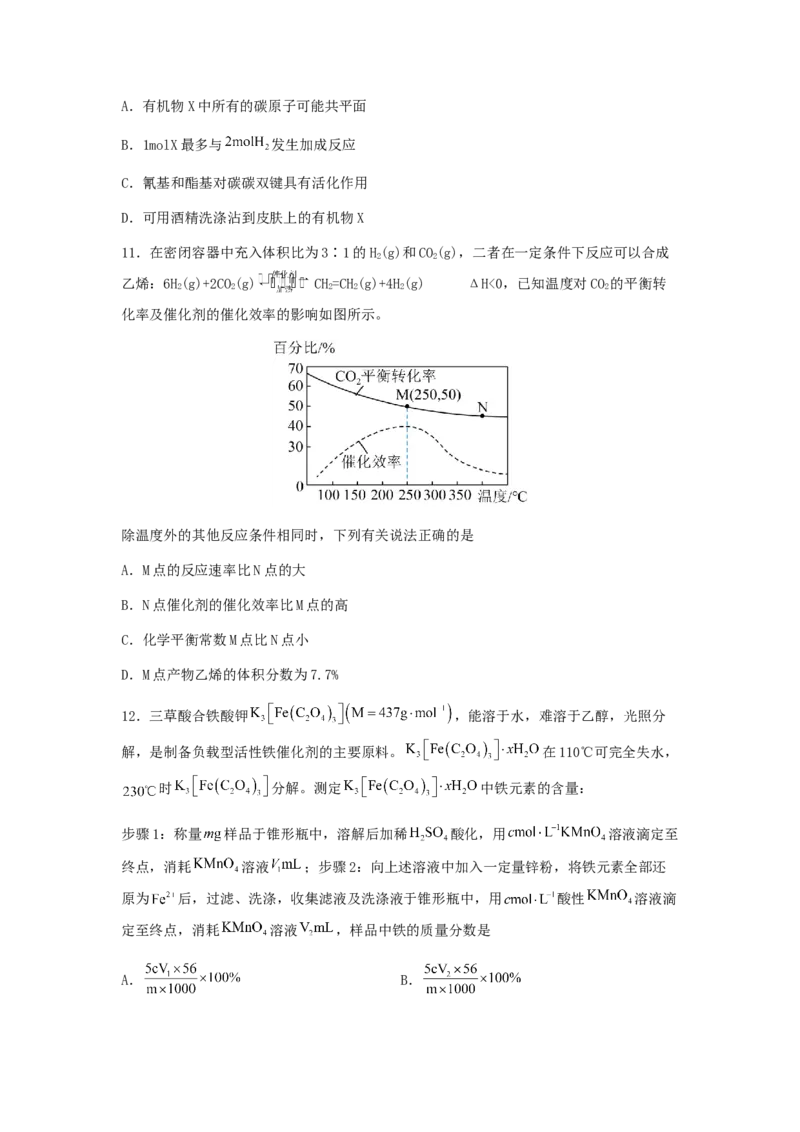
8.青杞始载于《新修本草》,有清热解毒的功效。青杞中含有白英素B,其结构简式如图
所示。下列有关白英素B的叙述正确的是
A.一个分子中有2个六元环,一个5元环
B.1mol白英素B可以与5mol 发生加成反应
C.可以发生氧化反应、还原反应和水解反应
D.一个分子中有2个手性碳原子
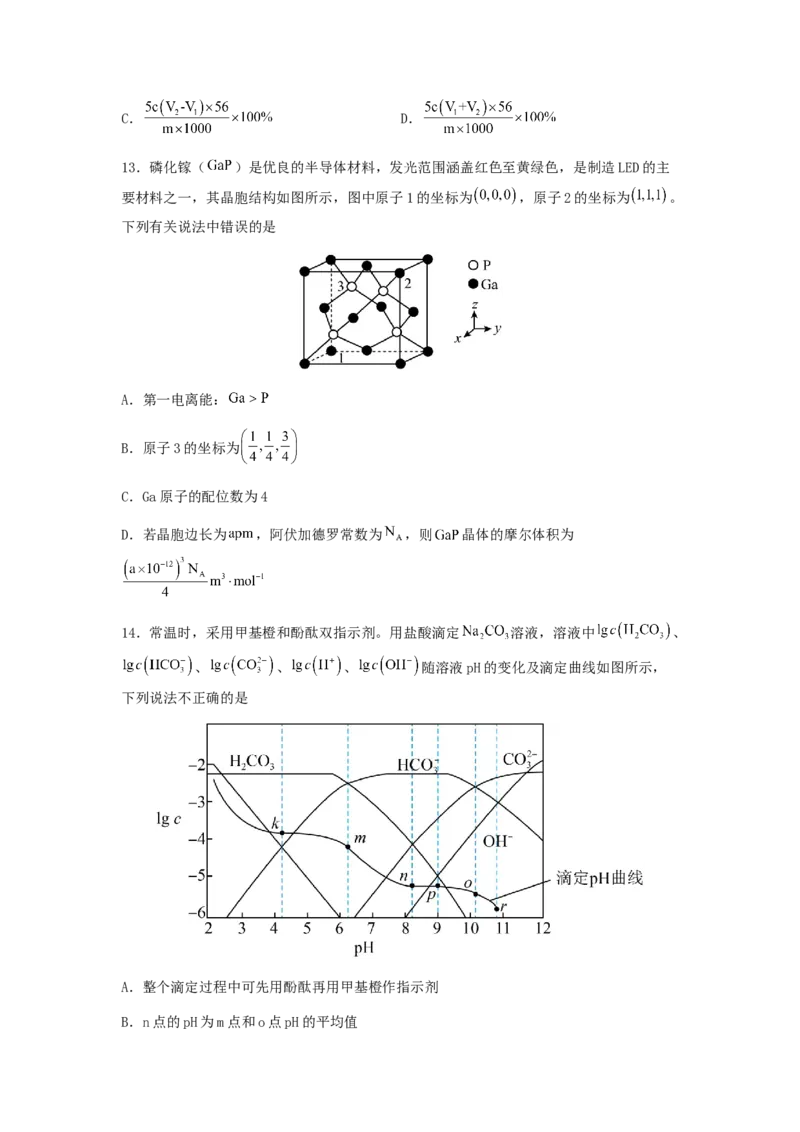
9.某实验小组为探究 配合物的性质,进行如下实验:
已知:溶液中, 为浅紫色, 为红色, 为无色。
下列说法正确的是
A. 与 形成配位键时, 提供孤电子对
B. 和 中共价键数目之比为
C. 溶于水后溶液呈黄色而不是浅紫色,是因为 转化成了 沉淀
D.上述实验说明 与 配位键强度弱于 与 配位键强度
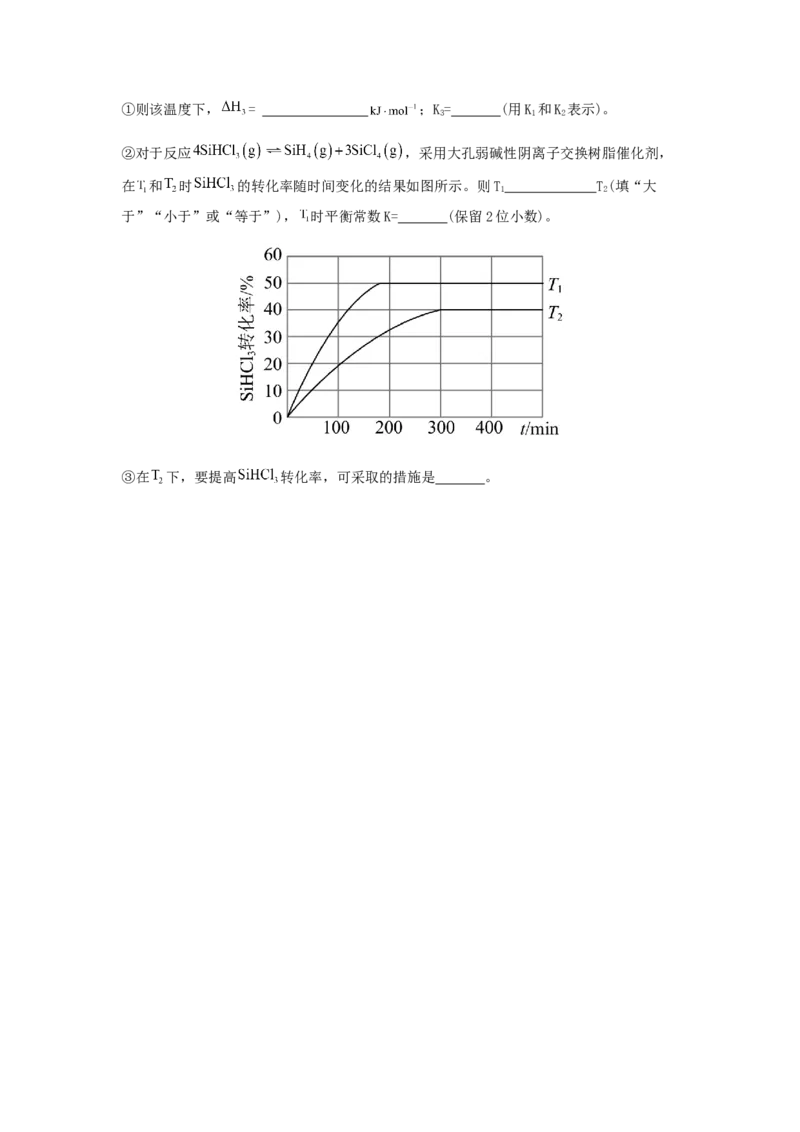
10.有机物X是一种瞬干胶﹐在常温、常压下受水的引发可快速聚合实现黏合,其原理如
下图所示。下列说法错误的是A.有机物X中所有的碳原子可能共平面
B.1molX最多与 发生加成反应
C.氰基和酯基对碳碳双键具有活化作用
D.可用酒精洗涤沾到皮肤上的有机物X
11.在密闭容器中充入体积比为3∶1的H(g)和CO(g),二者在一定条件下反应可以合成
2 2
乙烯:6H(g)+2CO(g) CH=CH(g)+4H(g) ΔH<0,已知温度对CO 的平衡转
2 2 2 2 2 2
化率及催化剂的催化效率的影响如图所示。
除温度外的其他反应条件相同时,下列有关说法正确的是
A.M点的反应速率比N点的大
B.N点催化剂的催化效率比M点的高
C.化学平衡常数M点比N点小
D.M点产物乙烯的体积分数为7.7%
12.三草酸合铁酸钾 ,能溶于水,难溶于乙醇,光照分
解,是制备负载型活性铁催化剂的主要原料。 在110℃可完全失水,
时 分解。测定 中铁元素的含量:
步骤1:称量 样品于锥形瓶中,溶解后加稀 酸化,用 溶液滴定至
终点,消耗 溶液 ;步骤2:向上述溶液中加入一定量锌粉,将铁元素全部还
原为 后,过滤、洗涤,收集滤液及洗涤液于锥形瓶中,用 酸性 溶液滴
定至终点,消耗 溶液 ,样品中铁的质量分数是
A. B.C. D.
13.磷化镓( )是优良的半导体材料,发光范围涵盖红色至黄绿色,是制造LED的主
要材料之一,其晶胞结构如图所示,图中原子1的坐标为 ,原子2的坐标为 。
下列有关说法中错误的是
A.第一电离能:
B.原子3的坐标为
C.Ga原子的配位数为4
D.若晶胞边长为 ,阿伏加德罗常数为 ,则 晶体的摩尔体积为
14.常温时,采用甲基橙和酚酞双指示剂。用盐酸滴定 溶液,溶液中 、
、 、 、 随溶液pH的变化及滴定曲线如图所示,
下列说法不正确的是
A.整个滴定过程中可先用酚酞再用甲基橙作指示剂
B.n点的pH为m点和o点pH的平均值C.r点溶液中:
D.r点到k点对应的变化过程中,溶液中水的电离程度一直减小
二、主观题
17.(15分)硅是信息产业、太阳能电池光电转化的基础材料。
(1)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
化学键
键能 356 413 226 318
硅与碳同族,但硅烷在种类和数量上都远不如烷烃多,原因是 。
(2)锌还原四氯化硅是一种有着良好应用前景的制备硅的方法。 还原 的反应如下:
反应1: ,
反应2:
反应3:
①对于上述三个反应,下列说法合理的是 。
a.升高温度会提高 的转化率 b.还原过程需在无氧的气氛中进行
c. d.Na、Mg可以代替 还原
②实际制备过程选择“反应3”,选择的理由是 。
(3)工业上也可用 制备高纯硅。 时, 相关反应的热化学方程式和平衡常
数如表:
热化学方程式 平衡常数
K
1
K
2
K
3①则该温度下, = ;K= (用K 和K 表示)。
3 1 2
②对于反应 ,采用大孔弱碱性阴离子交换树脂催化剂,
在 和 时 的转化率随时间变化的结果如图所示。则T T(填“大
1 2
于”“小于”或“等于”), 时平衡常数K= (保留2位小数)。
③在 下,要提高 转化率,可采取的措施是 。