文档内容
专练 17 氯、溴、碘及其化合物
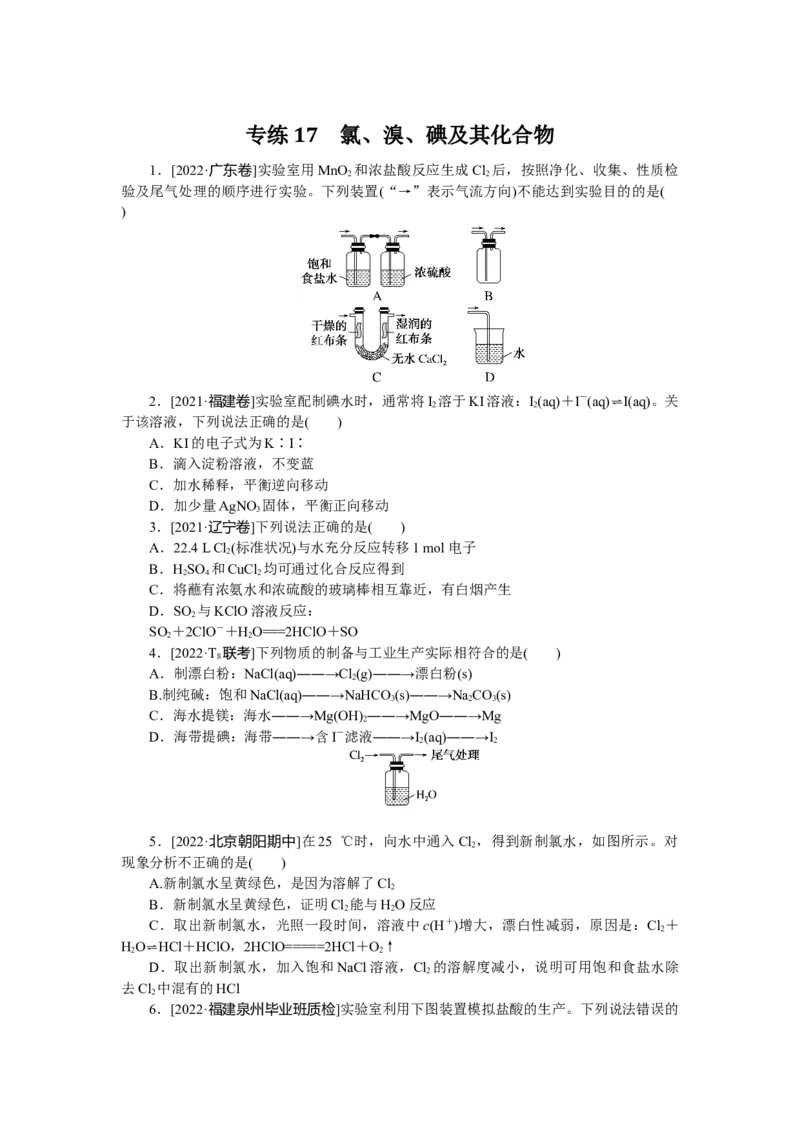
1.[2022·广东卷]实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检
2 2
验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是(
)
2.[2021·福建卷]实验室配制碘水时,通常将I
2
溶于KI溶液:I
2
(aq)+I-(aq)⇌I(aq)。关
于该溶液,下列说法正确的是( )
A.KI的电子式为K∶I∶
B.滴入淀粉溶液,不变蓝
C.加水稀释,平衡逆向移动
D.加少量AgNO 固体,平衡正向移动
3
3.[2021·辽宁卷]下列说法正确的是( )
A.22.4 L Cl (标准状况)与水充分反应转移1 mol电子
2
B.HSO 和CuCl 均可通过化合反应得到
2 4 2
C.将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D.SO 与KClO溶液反应:
2
SO +2ClO-+HO===2HClO+SO
2 2
4.[2022·T 联考]下列物质的制备与工业生产实际相符合的是( )
8
A.制漂白粉:NaCl(aq)――→Cl(g)――→漂白粉(s)
2
B.制纯碱:饱和NaCl(aq)――→NaHCO (s)――→NaCO(s)
3 2 3
C.海水提镁:海水――→Mg(OH) ――→MgO――→Mg
2
D.海带提碘:海带――→含I-滤液――→I(aq)――→I
2 2
5.[2022·北京朝阳期中]在25 ℃时,向水中通入Cl ,得到新制氯水,如图所示。对
2
现象分析不正确的是( )
A.新制氯水呈黄绿色,是因为溶解了Cl
2
B.新制氯水呈黄绿色,证明Cl 能与HO反应
2 2
C.取出新制氯水,光照一段时间,溶液中c(H+)增大,漂白性减弱,原因是:Cl +
2
H
2
O⇌HCl+HClO,2HClO=====2HCl+O
2
↑
D.取出新制氯水,加入饱和NaCl溶液,Cl 的溶解度减小,说明可用饱和食盐水除
2
去Cl 中混有的HCl
2
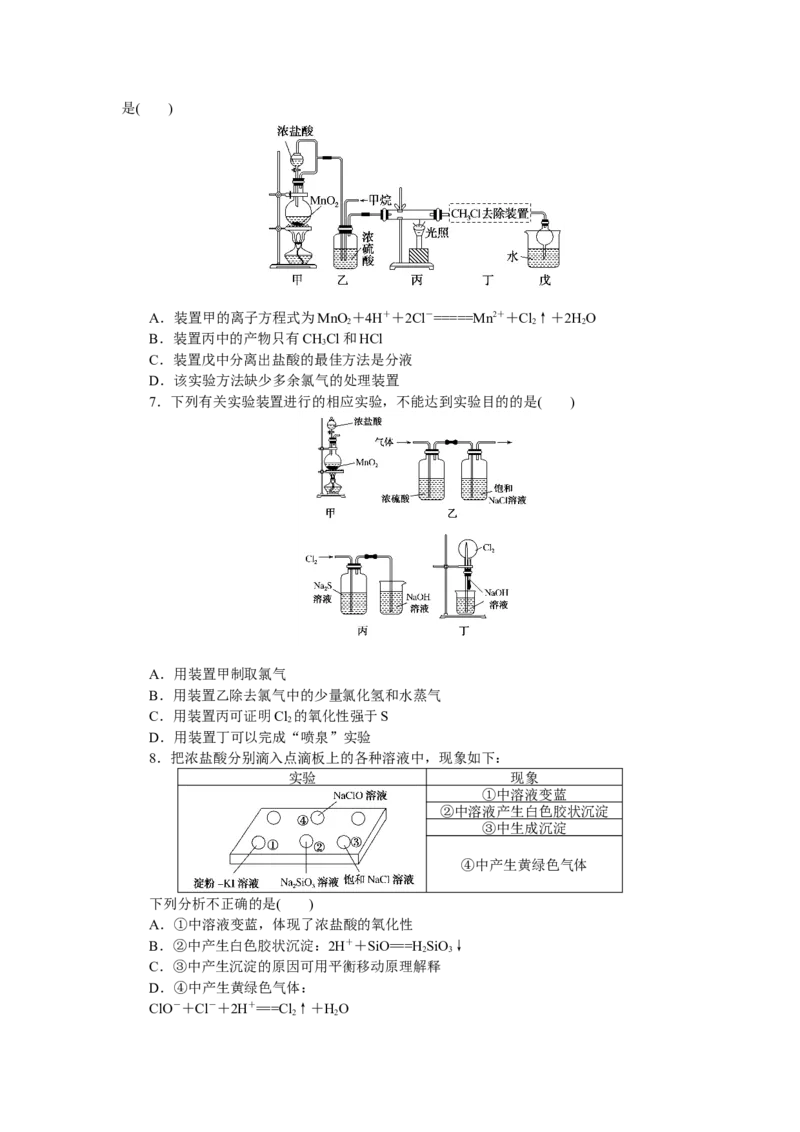
6.[2022·福建泉州毕业班质检]实验室利用下图装置模拟盐酸的生产。下列说法错误的是( )
A.装置甲的离子方程式为MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
B.装置丙中的产物只有CHCl和HCl
3
C.装置戊中分离出盐酸的最佳方法是分液
D.该实验方法缺少多余氯气的处理装置
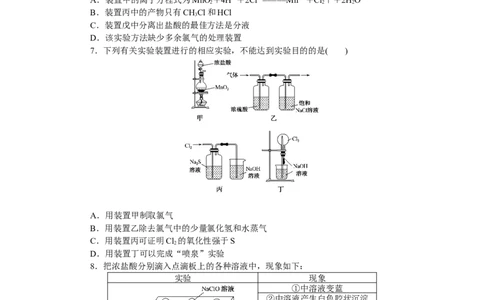
7.下列有关实验装置进行的相应实验,不能达到实验目的的是( )
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢和水蒸气
C.用装置丙可证明Cl 的氧化性强于S
2
D.用装置丁可以完成“喷泉”实验
8.把浓盐酸分别滴入点滴板上的各种溶液中,现象如下:
实验 现象
①中溶液变蓝
②中溶液产生白色胶状沉淀
③中生成沉淀
④中产生黄绿色气体
下列分析不正确的是( )
A.①中溶液变蓝,体现了浓盐酸的氧化性
B.②中产生白色胶状沉淀:2H++SiO===H SiO↓
2 3
C.③中产生沉淀的原因可用平衡移动原理解释
D.④中产生黄绿色气体:
ClO-+Cl-+2H+===Cl↑+HO
2 29.[2022·龙岩联考] 中学常见的某反应化学方程式为X+Y―→M+N+HO(未配平,
2
反应条件已略去),下列叙述错误的是( )
A.若X、Y的物质的量之比为1∶4,且N是黄绿色气体,则该反应的离子方程式为
MnO +4H++2Cl-===Mn2++Cl↑+2HO
2 2 2
B.当N为氯碱工业的主要原料,M是造成温室效应的主要气体,则上述反应的离子
方程式一定为:CO+2H+===CO ↑+HO
2 2
C.若X是铁,Y是稀硝酸(过量),则X 与Y 反应的离子方程式为
Fe+4H++NO===Fe3++NO↑+2HO
2
D.若M、N为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙
色褪色,橙色褪色过程的离子方程式为SO +Br +2HO===4H++SO+2Br-
2 2 2
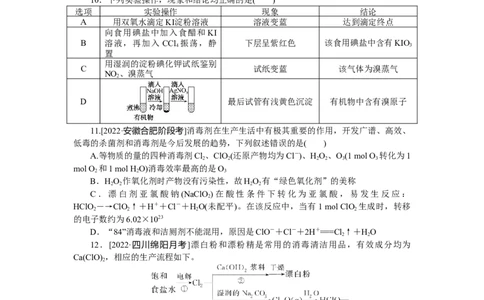
10.下列实验操作,现象和结论均正确的是( )
选项 实验操作 现象 结论
A 用双氧水滴定KI淀粉溶液 溶液变蓝 达到滴定终点
向食用碘盐中加入食醋和 KI
B 溶液,再加入 CCl 振荡,静 下层呈紫红色 该食用碘盐中含有KIO
4 3
置
用湿润的淀粉碘化钾试纸鉴别
C 试纸变蓝 该气体为溴蒸气
NO 、溴蒸气
2
D 最后试管有浅黄色沉淀 有机物中含有溴原子
11.[2022·安徽合肥阶段考]消毒剂在生产生活中有极其重要的作用,开发广谱、高效、
低毒的杀菌剂和消毒剂是今后发展的趋势,下列叙述错误的是( )
A.等物质的量的四种消毒剂Cl、ClO (还原产物均为Cl-)、HO、O(1 mol O 转化为1
2 2 2 2 3 3
mol O 和1 mol H O)消毒效率最高的是O
2 2 3
B.HO 作氧化剂时产物没有污染性,故HO 有“绿色氧化剂”的美称
2 2 2 2
C.漂白剂亚氯酸钠(NaClO)在酸性条件下转化为亚氯酸,易发生反应:
2
HClO―→ClO ↑+H++Cl-+HO(未配平)。在该反应中,当有1 mol ClO 生成时,转移
2 2 2 2
的电子数约为6.02×1023
D.“84”消毒液和洁厕剂不能混用,原因是ClO-+Cl-+2H+===Cl↑+HO
2 2
12.[2022·四川绵阳月考]漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为
Ca(ClO) ,相应的生产流程如下。
2
下列说法不正确的是( )
A.①中阳极的电极反应式为2Cl--2e-===Cl↑
2
B.②中反应的化学方程式为2Cl+2Ca(OH) ===Ca(ClO) +CaCl +2HO
2 2 2 2 2
C.上述过程涉及氧化还原反应、化合反应、复分解反应
D.制备漂粉精过程中,Cl 转化为Ca(ClO) 时,Cl原子的利用率为100%
2 2
13.[2021·广东卷(节选)]含氯物质在生产生活中有重要作用。1774年,舍勒在研究软
锰矿(主要成分是MnO )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810
2年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
(1) 实 验 室 沿 用 舍 勒 的 方 法 制 取 Cl 的 化 学 方 程 式 为
2
________________________________________________________________________。
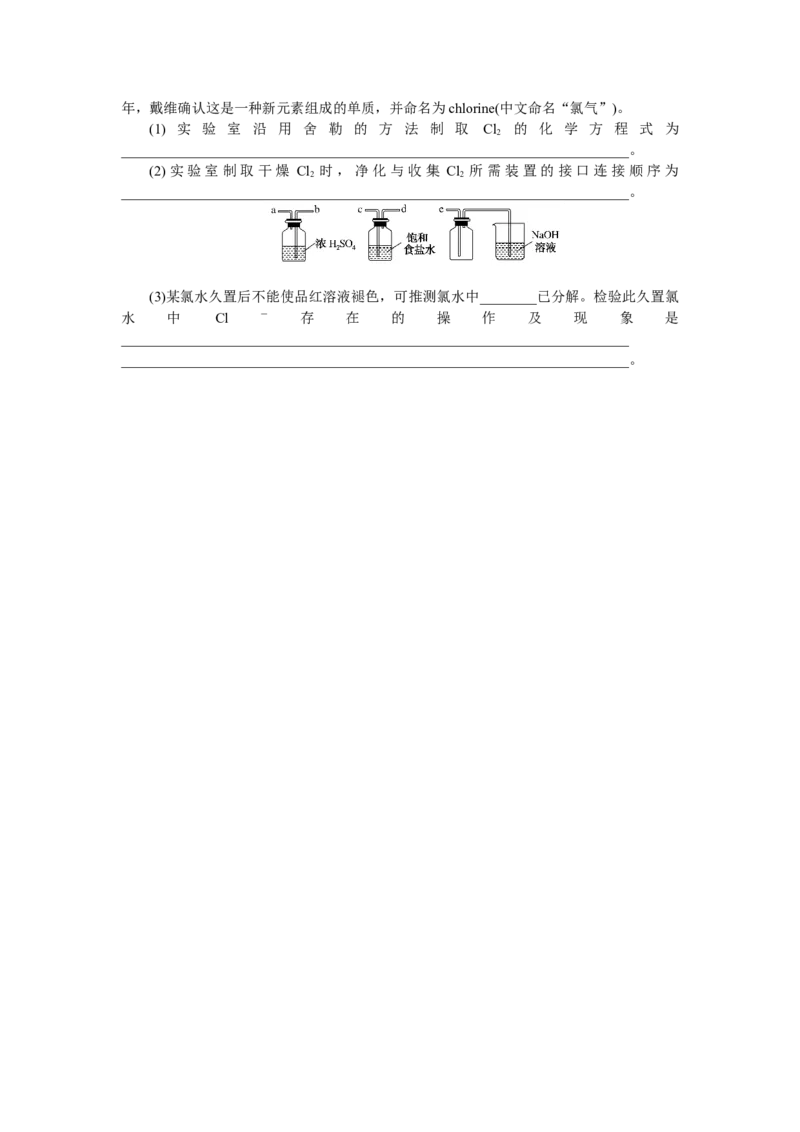
(2)实验室制取干燥 Cl 时,净化与收集 Cl 所需装置的接口连接顺序为
2 2
________________________________________________________________________。
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中________已分解。检验此久置氯
水 中 Cl - 存 在 的 操 作 及 现 象 是
________________________________________________________________________
________________________________________________________________________。