文档内容
专练 17 氯、溴、碘及其化合物
一、单项选择题
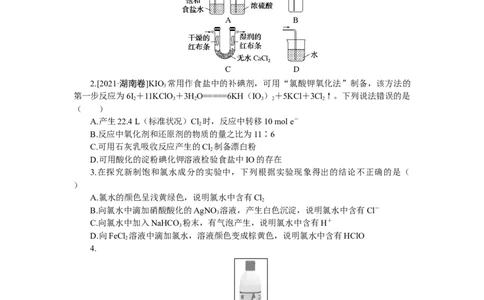
1.[2022·广东卷]实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验
2 2
及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是(
)
2.[2021·湖南卷]KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的
3
第一步反应为6I+11KClO+3HO=====6KH(IO )+5KCl+3Cl↑。下列说法错误的是
2 3 2 3 2 2
( )
A.产生22.4 L(标准状况)Cl 时,反应中转移10 mol e-
2
B.反应中氧化剂和还原剂的物质的量之比为11∶6
C.可用石灰乳吸收反应产生的Cl 制备漂白粉
2
D.可用酸化的淀粉碘化钾溶液检验食盐中IO的存在
3.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是(
)
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl
2
B.向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,说明氯水中含有Cl-
3
C.向氯水中加入NaHCO 粉末,有气泡产生,说明氯水中含有H+
3
D.向FeCl 溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
2
4.
[2022·北京海淀期末]下列说法不正确的是( )
A.“84消毒液”的有效成分是NaClO
B.“84消毒液”能漂白棉、麻、纸张
C.“84消毒液”与酸性洁厕剂混用会产生Cl
2
D.“84消毒液”久置失效,只涉及氧化还原反应
5.如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含氯气的气体经过甲瓶后,通入乙瓶,
布条不褪色;若关闭Ⅱ阀,打开Ⅰ阀,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )
①浓硫酸 ②饱和氯化钠溶液 ③亚硫酸钠溶液 ④饱和碳酸氢钠溶液
A.①②③ B.②③④ C.①②④ D.①③④
6.把浓盐酸分别滴入点滴板上的各种溶液中,现象如下:
实验 现象
①中溶液变蓝
②中溶液产生白色胶
状沉淀
③中生成沉淀
④中产生黄绿色气体
下列分析不正确的是( )
A.①中溶液变蓝,体现了浓盐酸的氧化性
B.②中产生白色胶状沉淀:
2H++SiO===H SiO↓
2 3
C.③中产生沉淀的原因可用平衡移动原理解释
D.④中产生黄绿色气体:
ClO-+Cl-+2H+===Cl↑+HO
2 2
7.[2022·河北石家庄外国语学校月考]下列实验操作对应的实验现象、实验结论均正确
且有逻辑关系的是( )
选项 实验操作 实验现象 实验结论
常温下,用pH计测定0.1
A mol·L-1 NaHRO 溶液的 溶液的pH=3.71 HRO 为二元酸
3 2 3
pH
将过量干燥的氯气通入装
B 红色鲜花颜色无变化 干燥的氯气不具有漂白性
有红色鲜花的集气瓶中
分别将乙烯和SO 通入溴 两种气体使溴水褪色的原
C 2 溴水均褪色
水中 理完全相同
向湿润的KI-淀粉试纸上 该黄色溶液中一定含有
D KI-淀粉试纸变蓝
滴2滴某黄色溶液 Fe3+
8.[2022·重庆七中四模]实验小组同学制备KClO 并探究其性质,过程如图:
3
下列说法不正确的是( )
A.可用饱和NaCl溶液净化氯气
B.生成KClO 的离子方程式为
3
3Cl+6OH-=====ClO+5Cl-+3HO
2 2C.若取少量无色溶液a于试管中,滴加稀HSO 后,溶液仍为无色
2 4
D.上述实验说明碱性条件下氧化性:Cl>KCl ,酸性条件下氧化性:Cl<KClO
2 3 2 3
二、不定项选择题
9.[2022·龙岩联考] 中学常见的某反应化学方程式为X+Y―→M+N+HO(未配平,
2
反应条件已略去),下列叙述错误的是( )
A.若X、Y的物质的量之比为1∶4,且N是黄绿色气体,则该反应的离子方程式为
MnO +4H++2Cl-===Mn2++Cl↑+2HO
2 2 2
B.当N为氯碱工业的主要原料,M是造成温室效应的主要气体,则上述反应的离子
方程式一定为:CO+2H+===CO ↑+HO
2 2
C.若X是铁,Y是稀硝酸(过量),则X 与Y 反应的离子方程式为Fe+4H++
NO===Fe3++NO↑+2HO
2
D.若M、N为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙
色褪色,橙色褪色过程的离子方程式为SO +Br +2HO===4H++SO+2Br-
2 2 2
10.南海是一个巨大的资源宝库,海水开发利用的部分过程如图所示。下列有关说法正
确的是( )
A.第①步中除去粗盐中的SO、Ca2+、Mg2+等杂质,加入药品的顺序为:NaCO 溶液、
2 3
NaOH溶液、BaCl 溶液、过滤后加盐酸
2
B.第②步的关键要低温小火烘干
C.氯碱工业的阴极产物是H
2
D.第③步到第⑤步的目的是为了富集溴元素
11.已知:反应ⅰ:4KI+O +2HO===4KOH+2I 反应ⅱ:3I +6OH-===IO+5I-+
2 2 2 2
3HO。某同学进行如下实验: ①取久置的KI固体(呈黄色)溶于水配成溶液; ②立即
2
向上述溶液中滴加淀粉溶液,溶液无明显变化;滴加酚酞后,溶液变红; ③继续向溶液中
滴加硫酸,溶液立即变蓝。下列分析合理的是( )
A.②说明久置的KI固体中不含有I
2
B.③中溶液变蓝的可能原因:
IO+5I-+6H+===3I +3HO
2 2
C.碱性条件下, I 与淀粉显色的速率慢于其与OH-反应的速率
2
D.若向淀粉KI试纸上滴加硫酸,一段时间后试纸变蓝,则证实该试纸上存在IO
12.[2022·河北邯郸质检]ClO 是一种黄绿色、易溶于水的气体,是高效、低毒的消毒剂。
2
实验室以NH Cl溶液、盐酸和NaClO 溶液为原料,按照以下流程制取ClO ,下列说法正
4 2 2
确的是( )
A.电解时,阳极反应式为NH+3Cl--6e-===NCl +4H+
3
B.电解过程中,混合溶液的pH逐渐减小
C.可用碱石灰除去ClO 中的NH
2 3
D.向溶液X中滴加AgNO 溶液,观察到沉淀生成,说明X中含有Cl-
3