文档内容
第四篇 化学反应速率与化学平衡
专项 26 化学速率常数
运用题给陌生的原理和规律进行解题是近几年高考的一大热点,主要考查考生的迁移运用能力,得分
率极低。化学速率常数备受命题者青睐。
速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同的浓度条件下,可
用速率常数大小来比较化学反应的反应速率。化学反应速率与反应物浓度(或浓度的次方)成正比,而速率
常数是其比例常数,在恒温条件下,速率常数不随反应物浓度的变化而改变。因此,可以应用速率方程求
出该温度下任意浓度时的反应速率。
速率方程,一定温度下,化学反应速率与反应物浓度以其计量数为指数的幂的乘积成正比。对于反应:
aA(g)+bB(g) gG(g)+hH(g),则 v =k ca(A)·cb(B)(其中 k 为正反应的速率常数),v =k
正 正 正 逆 逆
·cg(G)·ch(H)(其中k 为逆反应的速率常数)。如反应2NO (g) 2NO(g)+O(g),v =k ·c2(NO ),v =
逆 2 2 正 正 2 逆
k ·c2(NO)·c(O)。
逆 2
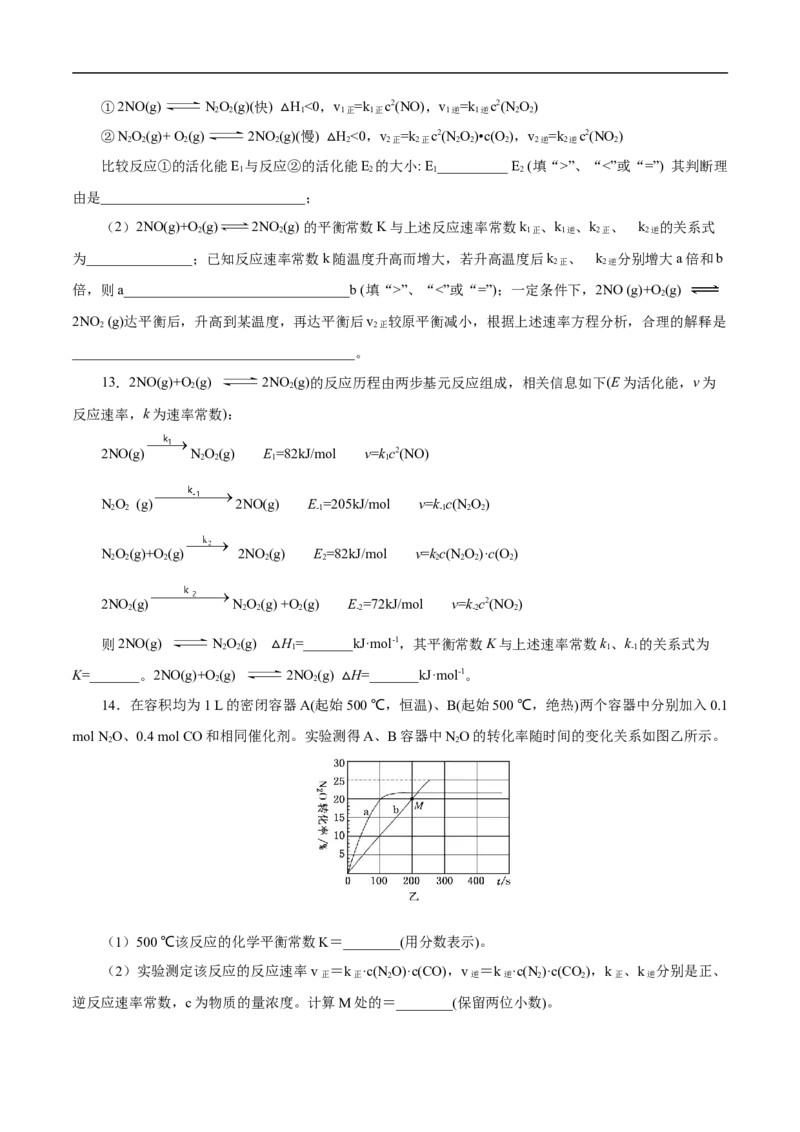
1.(2021•河北选择性考试)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、
1 1 2 2 1
k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
2
A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
【答案】A
【解析】A项,由图中数据可知,30 min时,M、Z的浓度分别为0.300 mol•L-1和0.125 mol•L-1,则M
的变化量为0.5 mol•L-1-0.300 mol•L-1=0.200 mol•L-1,其中转化为Y的变化量为0.200 mol•L-1-0.125
mol•L-1=0.075 mol•L-1。因此,0~30 min时间段内,Y的平均反应速率为
,A不正确;B项,由题中信息可知,反应①和反应②的速率之比为 ,Y和Z分别为反
应①和反应②的产物,且两者与M的化学计量数相同(化学计量数均为1),因此反应开始后,体系中Y和
Z的浓度之比等于 ,由于k、k 为速率常数,故该比值保持不变,B正确; C项,结合A、B的分析
1 2
可知因此反应开始后,在相同的时间内体系中Y和Z的浓度之比等于 = ,因此,如
果反应能进行到底,反应结束时有 的M转化为Z,即62.5%的M转化为Z,C正确;D项,由以上分析
可知,在相同的时间内生成Z较多、生成Y较少,因此,反应①的化学反应速率较小,在同一体系中,活
化能较小的化学反应速率较快,故反应①的活化能比反应②的活化能大,D说法正确。故选A。
2.(2022•河北省选择性考试)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为
①X Y;②Y Z。反应①的速率 ,反应②的速率 ,式中 为速率常数。
图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是(
)A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
1
【答案】AB
【解析】由图中的信息可知,浓度随时间变化逐渐减小的代表的是X,浓度随时间变化逐渐增大的代
表的是Z,浓度随时间变化先增大后减小的代表的是Y;由图乙中的信息可知,反应①的速率常数随温度
升高增大的幅度小于反应②的。A项,由图甲中的信息可知,随c(X)的减小,c(Y) 先增大后减小,c(Z)增
大,因此,反应①的速率随c(X)的减小而减小,而反应②的速率先增大后减小,A错误;B项,根据体系
中发生的反应可知,在Y的浓度达到最大值之前,单位时间内X的减少量等于Y和Z的增加量,因此,v
(X)= v (Y) +v(Z),但是,在Y的浓度达到最大值之后,单位时间内Z的增加量等于Y和X的减少量,故v
(X) + v (Y) = v(Z),B错误;C项,升高温度可以可以加快反应①的速率,但是反应①的速率常数随温度
升高增大的幅度小于反应②的,且反应②的的速率随着Y的浓度的增大而增大,因此,欲提高Y的产率,
需提高反应温度且控制反应时间,C正确;D项,由图乙信息可知,温度低于T时,k>k,反应②为慢反
1 2
应,因此,总反应速率由反应②决定,D正确;故选AB。
3.(2022•辽宁省选择性考试节选)某合成氨速率方程为: ,根据表中数据,
___________;
实
验
1 m n p q
2 n p3 m n
4 m p
在合成氨过程中,需要不断分离出氨的原因为___________。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
【答案】 -1 a
【解析】将实验1、3中数据分别代入合成氨的速率方程可得:① ,③
,可得 。合成氨过程中,不断分离出氨,即降低体系中c(NH ),生成物浓度
3
下降,平衡向正反应方向移动,但不会提高正反应速率,a正确,c错误;反应主产物即氨不能使催化剂中
毒,b错误。
4.(2020•新课标Ⅰ卷节选)研究表明,SO 催化氧化的反应速率方程为:v=k( −1)0.8(1−nα')。式中:k
2
为反应速率常数,随温度t升高而增大;α为SO 平衡转化率,α'为某时刻SO 转化率,n为常数。在
2 2
α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度t 。tt 后,v逐渐下
m m m
降。原因是__________________________。
【答案】升高温度,k增大使v逐渐提高,但α降低使v逐渐下降。当t<t ,k增大对v的提高大于α
m
引起的降低;当t>t ,k增大对v的提高小于α引起的降低
m
【解析】 由于该反应是放热反应,温度升高后α降低。由题中信息可知,v= ,
升高温度,k增大使v逐渐提高,但α降低使v逐渐下降。当t<t ,k增大对v的提高大于α引起的降低;
m
当t>t ,k增大对v的提高小于α引起的降低。
m
1.速率常数的影响因素温度对化学反应速率的影响是显著的,速率常数是温度的函数,同一反应,温度不同,速率常数将有
不同的值,但浓度不影响速率常数。
2.速率常数与化学平衡常数之间的关系
一定温度下,可逆反应:aA(g)+bB(g) gG(g)+hH(g),达到平衡状态时,v =k ·ca(A)·cb(B),v
正 正
=k ·cg(G)·ch(H),因平衡时v =v ,则k ·ca(A)·cb(B)=k ·cg(G)·ch(H),==K。
逆 逆 正 逆 正 逆
1.(2022·河北省张家口市高三联考)在一定温度下的可逆反应X(g) 2Y(g) ΔH>0,v =k
正
·c(X),v =k ·c2(Y),若该温度下的平衡常数K=10,下列说法错误的是( )
正 逆 逆
A.该温度下k =10 k
正 逆
B.升高温度,k 增大的倍数大于k 增大的倍数
正 逆
C.有利于测定X的相对分子质量的条件为低温高压
D.恒压条件下,向平衡体系中充入惰性气体He,X的转化率减小
2.氨气去除NO的反应原理为:4NH (g)+6NO(g) 5N(g)+6HO(g) ΔH<0,反应速率与浓度之间
3 2 2
存在如下关系:v =k ·c4(NH )·c6(NO),v =k ·c5(N )·c6(H O),k 、k 为速率常数,只受温度影响。
正 正 3 逆 逆 2 2 正 逆
350℃时,在2L恒容密闭容器中,通入0.9molNH (g)和1.2molNO(g)发生反应,保持温度不变,5min后反
3
应达平衡,NO的转化率为50%。下列说法正确的是( )
A.用NH 表示的化学反应速率为0.06mol·L-1·min-1
3
B.350℃时,该反应的平衡常数为0.5
C.其他条件不变,往反应后的容器中再通入0.9molNH (g)和1.2molNO(g),重新达平衡时NO的体积
3
分数增大
D.当温度改变为T°C时,若k =k ,则T>350
正 逆
3.(2022·北京市人大附中三模)某温度时两个恒容密闭容器中仅发生反应2NO(g)+O (g)
2
2NO (g) ΔH>0。实验测得: , , 、 为速率常数,
2
只受温度影响。
起始浓度 (mol/L) 平衡浓度(mol/L)
容器编号
c(NO ) c(NO) c(O) c(O)
2 2 2
Ⅰ 0.6 0 0 0.2Ⅱ 0.6 0.1 0
下列说法不正确的是( )
A.升高温度,该反应的化学平衡常数增大 B.Ⅰ中NO 的平衡转化率约为66.7%
2
C.Ⅱ中达到平衡状态时,c(O)>0.2 mol·L−1 D.该反应的化学平衡常数可表示为
2
4.已知反应2NO(g)+2H(g)===N (g)+2HO(g)生成N 的初始速率与NO、H 的初始浓度的关系为v=
2 2 2 2 2
kcx(NO)·cy(H ),k为速率常数。在800 ℃时测得的相关数据如下表所示。
2
初始浓度
实验数据 生成N 的初始速率/mol·L-1·s-1
2
c(NO)/ mol·L-1 c(H )/ mol·L-1
2
1 2.00×10-3 6.00×10-3 1.92×10-3
2 1.00×10-3 6.00×10-3 4.80×10-4
3 2.00×10-3 3.00×10-3 9.60×10-4
下列说法中不正确的是( )
A.关系式中x=1,y=2
B.800 ℃时,k值为8×104
C.若800 ℃时,初始浓度c(NO)=c(H )=4.00×10-3 mol·L-1,则生成N 的初始速率为5.12×10-3
2 2
mol·L-1·s-1
D.当其他条件不变时,升高温度,速率常数将增大
5.某反应A(g)+ B(g) →C (g)+ D(g)的速率方程为 ,其半衰期(当剩余反应物恰
好是起始的一半时所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示:
c(A)/( mol·L-1) c(B)/( mol·L-1) v/(10-3mol·L-1·min-1)
0.25 0.050 1.4
0.50 0.050 2.8
1.00 0.050 5.6
0.50 0.100 2.8
下列说法正确的是
A.速率方程中的 、
B.该反应的速率常数k=2.8×10-3min-1C.增大反应物浓度,k增大导致反应的瞬时速率加快
D.在过量的B存在时,反应掉87.5%的A所需的时间是375min
6.温度为T 时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO (g) 2NO(g)+O (g)
1 2 2
(正反应吸热)。实验测得:v =v(NO ) =k ·c2(NO ),v =v(NO) =2v(O ) =k ·c2(NO)·c(O ),k 、k 为
正 2 消耗 正 2 逆 消耗 2 消耗 逆 2 正 逆
速率常数,受温度影响。下列说法正确的是( )
容器 物质的起始浓度(mol·L-1) 物质的平衡浓度(mol·L-1)
编号 c(NO ) c(NO) c(O ) c(O )
2 2 2
Ⅰ 0.6 0 0 0.2
Ⅱ 0.3 0.5 0.2
Ⅲ 0 0.5 0.35
k
A.设K为该反应的化学平衡常数,则有K= 逆
k
正
B.达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比为20∶17
C.容器Ⅱ中起始时平衡正向移动,达到平衡时,容器Ⅱ中NO 的转化率比容器Ⅰ中的小
2
D.若改变温度为T,且T>T ,则k ∶k <0.8
2 2 1 正 逆
7.(2022·浙江省镇海市高三选考模拟)硫酸工业中,将SO 氧化为SO 是生产工艺中的重要环节。在温
2 3
度为T 条件下,在三个容积均为1L的恒容密闭容器中仅发生反应:2SO (g)+O(g) 2SO (g)ΔH<0,实
1 2 2 3
验测得:v =k ·c2(SO )·c(O),v =k ·c2(SO )。
正 正 2 2 逆 逆 3
起始浓度/(mol·L-1) 平衡浓度/(mol·L-1)
容器编号
c(SO ) c(O) C(SO ) c(O)
2 2 3 2
I 0.6 0.3 0 0.2
II 0.5 x 0.3
III 0.3 0.25 0.2
已知:k 、k 为速率常数,仅受温度的影响。
正 逆
下列说法错误的是( )
A.达到平衡时,平衡常数和速率常数的关系:
B.若容器II中达到平衡时 =1,则x=0.85
C.容器III中达到平衡时,c(O)<0.25mol·L-1
2D.当温度升高为T 时,k 、k 分别增大m倍和n倍,则m0 中,v =k c(NO),v =k
2 4 2 正 正 2 4 逆 逆
c2(NO )(k 、k 只是温度的函数)。若该温度下的平衡常数K=10,则k =________k 。升高温度,k 增
2 正 逆 正 逆 正
大的倍数________(填“大于”“小于”或“等于”)k 增大的倍数。
逆
10.对于基元反应,如aA+bB cC+dD,反应速率v =k ·ca(A)·cb(B),v =k ·cc(C)·cd(D),
正 正 逆 逆
其中k 、k 是取决于温度的速率常数。
正 逆
对于基元反应2NO(g)+O(g) 2NO (g),在653 K时,速率常数k =2.6×103 L2·mol-2·s-1,k
2 2 正 逆
=4.1×103 L·mol-1·s-1。
(1)计算653 K时的平衡常数K=________。
(2)653 K时,若NO的浓度为0.006 mol·L-1,O 的浓度为0.290 mol·L-1,则正反应速率为________
2
mol·L-1·s-1。
11.利用“合成气”合成甲醇后,甲醇脱水制得二甲醚的反应为:
2CHOH(g) CHOCH (g) + H O(g) ΔH,其速率方程式为:v =k ·c2(CHOH),v
3 3 3 2 正 正 3
=k ·c(CHOCH )·c(HO),k 、k 为速率常数且只与温度有关。经查阅资料,上述反应平衡状态下
逆 逆 3 3 2 正 逆
存在计算式:lnKc = −2.205+ (Kc为化学平衡常数;T 为热力学温度,单位为K)。
反应达到平衡后,仅升高温度,k 增大的倍数_________ k 增大的倍数(填“>”、“<”或
正 逆
“=”)。
12.(1)已知2NO(g)+O (g) 2NO (g) H的反应历程分两步:
2 2
△①2NO(g) NO(g)(快) H<0,v =k c2(NO),v =k c2(N O)
2 2 1 1正 1正 1逆 1逆 2 2
②N
2
O
2
(g)+ O
2
(g) 2NO
2
(△g)(慢) H
2
<0,v
2正
=k
2正
c2(N
2
O
2
)•c(O
2
),v
2逆
=k
2逆
c2(NO
2
)
比较反应①的活化能E
1
与反应②的活△化能E
2
的大小: E
1
__________ E
2
(填“>”、“<”或“=”) 其判断理
由是_____________________________;
(2)2NO(g)+O (g) 2NO (g) 的平衡常数K与上述反应速率常数k 、k 、k 、 k 的关系式
2 2 1正 1逆 2正 2逆
为_______________;已知反应速率常数k随温度升高而增大,若升高温度后k 、 k 分别增大a倍和b
2正 2逆
倍,则a________________________________b (填“>”、“<”或“=”);一定条件下,2NO (g)+O(g)
2
2NO (g)达平衡后,升高到某温度,再达平衡后v 较原平衡减小,根据上述速率方程分析,合理的解释是
2 2正
________________________________________。
13.2NO(g)+O (g) 2NO (g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为
2 2
反应速率,k为速率常数):
2NO(g) NO(g) E=82kJ/mol v=kc2(NO)
2 2 1 1
NO (g) 2NO(g) E =205kJ/mol v=k c(N O)
2 2 -1 -1 2 2
NO(g)+O(g) 2NO (g) E=82kJ/mol v=kc(N O)·c(O )
2 2 2 2 2 2 2 2 2
2NO (g) NO(g) +O (g) E =72kJ/mol v=k c2(NO )
2 2 2 2 -2 -2 2
则2NO(g) NO(g) H=_______kJ·mol-1,其平衡常数K与上述速率常数k、k 的关系式为
2 2 1 1 -1
K=_______。2NO(g)+O (g) △ 2NO (g) H=_______kJ·mol-1。
2 2
14.在容积均为1 L的密闭容器A(起始△500 ℃,恒温)、B(起始500 ℃,绝热)两个容器中分别加入0.1
mol NO、0.4 mol CO和相同催化剂。实验测得A、B容器中NO的转化率随时间的变化关系如图乙所示。
2 2
(1)500 ℃该反应的化学平衡常数K=________(用分数表示)。
(2)实验测定该反应的反应速率v =k ·c(NO)·c(CO),v =k ·c(N)·c(CO),k 、k 分别是正、
正 正 2 逆 逆 2 2 正 逆
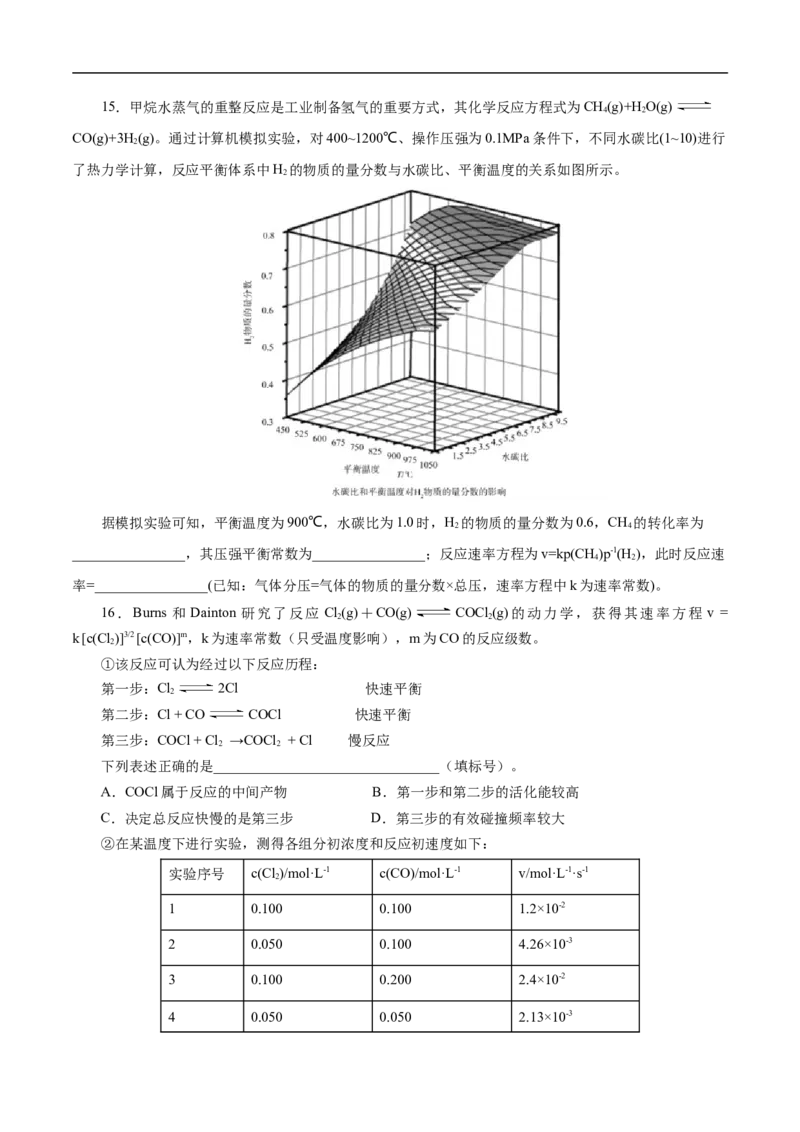
逆反应速率常数,c为物质的量浓度。计算M处的=________(保留两位小数)。15.甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH(g)+HO(g)
4 2
CO(g)+3H(g)。通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行
2
了热力学计算,反应平衡体系中H 的物质的量分数与水碳比、平衡温度的关系如图所示。
2
据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H 的物质的量分数为0.6,CH 的转化率为
2 4
________________,其压强平衡常数为________________;反应速率方程为v=kp(CH )p-1(H ),此时反应速
4 2
率=________________(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
16.Burns 和 Dainton 研究了反应 Cl(g)+CO(g) COCl (g)的动力学,获得其速率方程 v =
2 2
k[c(Cl )]3/2 [c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。
2
①该反应可认为经过以下反应历程:
第一步:Cl 2Cl 快速平衡
2
第二步:Cl + CO COCl 快速平衡
第三步:COCl + Cl →COCl + Cl 慢反应
2 2
下列表述正确的是________________________________(填标号)。
A.COCl属于反应的中间产物 B.第一步和第二步的活化能较高
C.决定总反应快慢的是第三步 D.第三步的有效碰撞频率较大
②在某温度下进行实验,测得各组分初浓度和反应初速度如下:
实验序号 c(Cl )/mol·L-1 c(CO)/mol·L-1 v/mol·L-1·s-1
2
1 0.100 0.100 1.2×10-2
2 0.050 0.100 4.26×10-3
3 0.100 0.200 2.4×10-2
4 0.050 0.050 2.13×10-3CO的反应级数m =_________________,当实验4进行到某时刻,测得c(Cl ) = 0.010 mol·L-1,则此时
2
的反应速率v =_________________mol·L-1·s-1(已知: ≈ 0.32)。
17.升高温度绝大多数的化学反应速率增大,但是2NO(g)+O(g) 2NO (g)的速率却随温度的升
2 2
高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O(g) 2NO (g)的反应历
2 2
程分两步:
i:2NO(g) NO(g)(快),v =k c2(NO) v =k c(NO) ΔH<0
2 2 1正 1正 1逆 1逆 2 2 1
ii:NO(g)+O(g) 2NO (g)(慢),v =k c(NO)c(O) v =k c2(NO ) ΔH<0
2 2 2 2 2正 2正 2 2 2 2逆 2逆 2 2
请回答下列问题:
①一定温度下,反应2NO(g)+O(g) 2NO (g)达到衡状态,请写出用k 、k 、k 、k 表示的
2 2 1正 1逆 2正 2逆
平衡常数表达式K=_______________
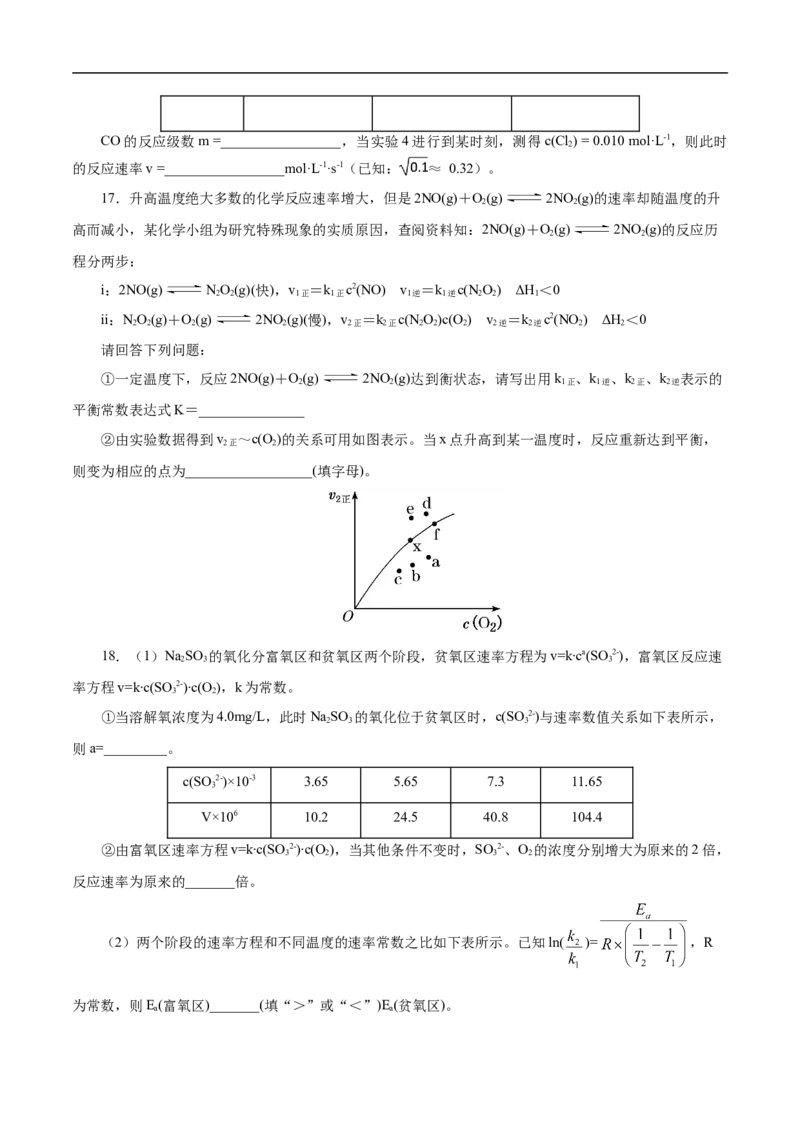
②由实验数据得到v ~c(O)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,
2正 2
则变为相应的点为__________________(填字母)。
18.(1)NaSO 的氧化分富氧区和贫氧区两个阶段,贫氧区速率方程为v=k∙ca(SO 2-),富氧区反应速
2 3 3
率方程v=k∙c(SO 2-)∙c(O),k为常数。
3 2
①当溶解氧浓度为4.0mg/L,此时NaSO 的氧化位于贫氧区时,c(SO 2-)与速率数值关系如下表所示,
2 3 3
则a=_________。
c(SO 2-)×10-3 3.65 5.65 7.3 11.65
3
V×106 10.2 24.5 40.8 104.4
②由富氧区速率方程v=k∙c(SO 2-)∙c(O),当其他条件不变时,SO 2-、O 的浓度分别增大为原来的2倍,
3 2 3 2
反应速率为原来的_______倍。
(2)两个阶段的速率方程和不同温度的速率常数之比如下表所示。已知ln( )= ,R
为常数,则E(富氧区)_______(填“>”或“<”)E(贫氧区)。
a a反应阶
速率方程 k(297.9K)/k(291.5K)
段
富氧区 v=k∙c(SO 2-)∙c(O) 1.47
3 2
贫氧区 v=k∙ca(SO2-)∙cb(O) 2.59
3 2
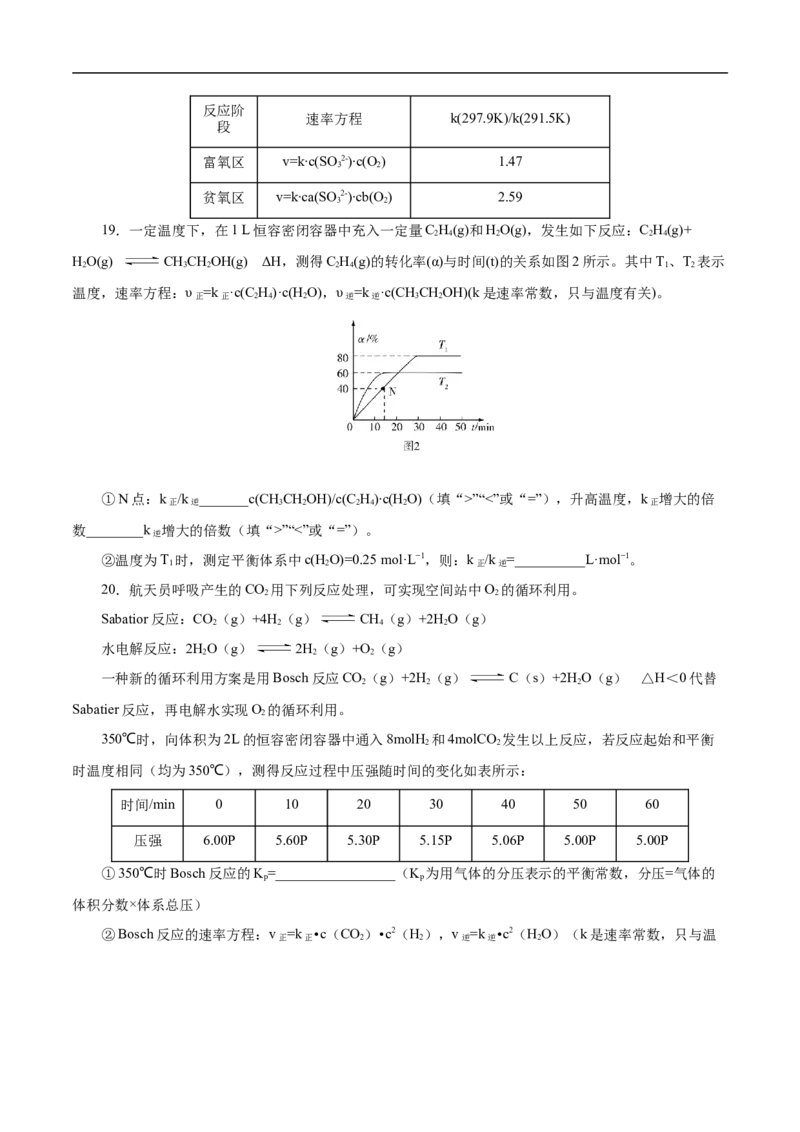
19.一定温度下,在1 L恒容密闭容器中充入一定量C H(g)和HO(g),发生如下反应:C H(g)+
2 4 2 2 4
HO(g) CHCHOH(g) ΔH,测得C H(g)的转化率(α)与时间(t)的关系如图2所示。其中T、T 表示
2 3 2 2 4 1 2
温度,速率方程:υ =k ·c(C H)·c(HO),υ =k ·c(CHCHOH)(k是速率常数,只与温度有关)。
正 正 2 4 2 逆 逆 3 2
①N点:k /k _______c(CHCHOH)/c(C H)∙c(HO)(填“>”“<”或“=”),升高温度,k 增大的倍
正 逆 3 2 2 4 2 正
数________k 增大的倍数(填“>”“<”或“=”)。
逆
②温度为T 时,测定平衡体系中c(HO)=0.25 mol·L−1,则:k /k =__________L·mol−1。
1 2 正 逆
20.航天员呼吸产生的CO 用下列反应处理,可实现空间站中O 的循环利用。
2 2
Sabatior反应:CO(g)+4H (g) CH(g)+2H O(g)
2 2 4 2
水电解反应:2HO(g) 2H(g)+O (g)
2 2 2
一种新的循环利用方案是用Bosch反应CO(g)+2H (g) C(s)+2H O(g) △H<0代替
2 2 2
Sabatier反应,再电解水实现O 的循环利用。
2
350℃时,向体积为2L的恒容密闭容器中通入8molH 和4molCO 发生以上反应,若反应起始和平衡
2 2
时温度相同(均为350℃),测得反应过程中压强随时间的变化如表所示:
时间/min 0 10 20 30 40 50 60
压强 6.00P 5.60P 5.30P 5.15P 5.06P 5.00P 5.00P
①350℃时Bosch反应的K=_________________(K 为用气体的分压表示的平衡常数,分压=气体的
p p
体积分数×体系总压)
②Bosch反应的速率方程:v =k •c(CO)•c2(H),v =k •c2(HO)(k是速率常数,只与温
正 正 2 2 逆 逆 2度有关)。30min时, _________________ (填“>”“<”或“=”);升高温度,k
增大的倍数_________________k 增大的倍数。(填“>”“<”或“=”)
正 逆
21.(1)一步完成的反应称为基元反应,只由基元反应构成的化学反应称为简单反应,两个及以上
基元反应构成的化学反应称为复杂反应,复杂反应的速率取决(等)于慢的基元反应速率。基元反应
aA+bB=cC+dD的速率方程为v=k·ca(A)·cb(B),其中k为速率常数。已知反应NO +CO=NO+CO ,在不同
2 2
温度下反应机理不同。
①温度高于490K时,上述反应为简单反应,请写出其速率方程_______________。
②温度高于520K时,该反应是由两个基元反应构成的复杂反应,其速率方程v=k·c2(NO ),已知慢的
2
基元反应的反应物和产物为NO、NO 、NO ,用方程式表示反应历程。
2 3
第一步:__________________________________(慢反应)。
第二步:_____________________________________(快反应)。
(2)NO(g) 2NO (g) ΔH =+57 kJ·mol-1 该反应是高中和大学化学学习的经典素材。
2 4 2
②TK时,向1L真空容器中加入1molN O ,达到平衡时NO 的平衡产率为20%,则该温度下的平衡
1 2 4 2
常数K=________,达到平衡时吸收的热量为______kJ。某温度下,该反应达到平衡,NO 与NO 的混合气
2 2 4
体总压强为100KPa,密度为同状态下氢气密度的34.5倍,平衡常数K =__________KPa(用平衡分压代替
P
平衡浓度计算)。
③若v(N O)=k ·c(NO) v(NO )=k ·c(NO ),T 温度下,若k=k ,则T_______________T(填“高
2 4 1 2 4 2 2 2 2 1 2 2 1
于”或“低于”)。
(3)复杂反应2NO(g)+O (g)=2NO (g)由两个基元反应构成,2NO(g)=N O(g)(快速平衡)NO(g)
2 2 2 2 2 2
+O (g)=2NO (g)(慢反应),已知快反应为放热反应,其正、逆反应速率常数分别为k 和k 慢反应正、逆
2 2 1 2
反应速率常数分别为k 和k。若v =k·c2(NO)·c(O) 则k=__________________________________(用k
3 4 正 2 1、
k k 表示)。
2、 3