文档内容
第六篇 物质结构与性质
专项 39 杂化与空间结构
在选择性必修二《物质结构与性质》中,ABn型物质中心原子的杂化方式、分子或离子的空间构型是
高考热点题型之一,要求运用杂化轨道理论和价层电子对互斥模型进行解释和预测分子空间结构。通过杂
化轨道理论对分子空间结构及原子间成键情况解释的探究学习,强化宏观辨识与微观探析素养,借助价层
电子对互斥模型对分子空间结构的预测,建立分子空间结构分析的思维模型,强化模型意识。
在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这
个过程叫做轨道的杂化,产生的新轨道叫杂化轨道。杂化轨道在角度分布上比单纯的 s或p轨道在某一方
向上更集中,从而使它与其它原子的原子轨道重叠的程度更大,形成的共价键更牢固。中心原子价层电子
对数、杂化轨道类型与粒子的立体构型(A 型)如下:
Bm±
n
价层电子对数
2 3 4
(杂化轨道数)
杂化轨道类型 sp sp2 sp3
价层电子对模
直线形 三角形 四面体形
型(VSEPR)
粒子组成形式 AB 2 : AB 2 : AB 3 : AB 2 : AB 3 : AB 4 :(正)
与构型
直线形 V形 三角形 V形 三角锥形 四面体形
当中心原子无孤电子对时,分子构型与价层电子对模型一致;当有孤电子对时,分子的
规律 构型为去掉孤电子对后剩余部分的立体构型,且孤电子对会对分子构型产生“挤压”效
果,使键角变小
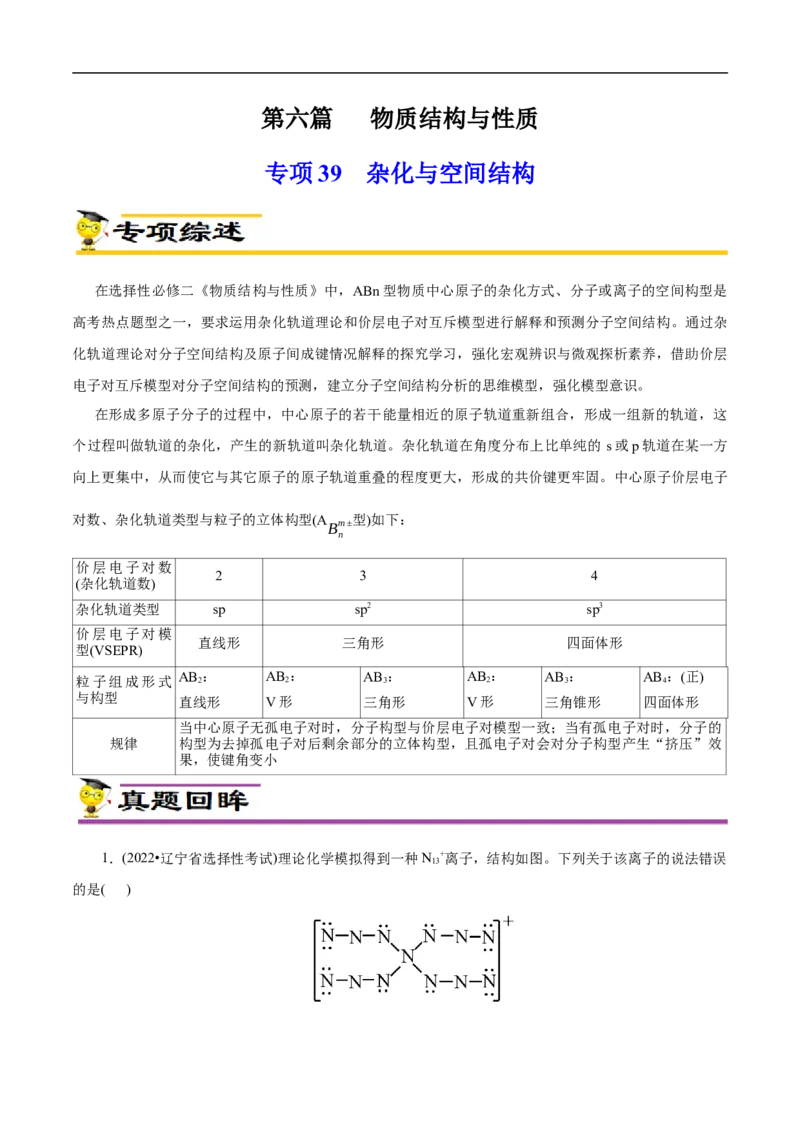
1.(2022•辽宁省选择性考试)理论化学模拟得到一种N +离子,结构如图。下列关于该离子的说法错误
13
的是( )A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
【答案】B
【解析】A项,由N +的结构式可知,所有N原子均满足8电子稳定结构,A正确;B项,中心N原
13
子为sp3杂化,与中心N原子直接相连的N原子为sp2杂化,与端位N原子直接相连的N原子为sp杂化,
端位N原子为sp2杂化,则N原子的杂化方式有3种,B错误;C项,中心N原子为sp3杂化,则其空间结
构为四面体形,C正确;D项,N +中含叠氨结构( ),常温下不稳定,D正确;故选B。
13
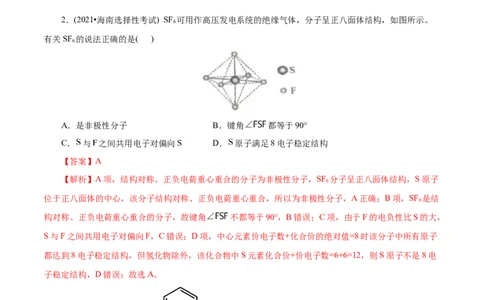
2.(2021•海南选择性考试) SF 可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。
6
有关SF 的说法正确的是( )
6
A.是非极性分子 B.键角 都等于90°
C. 与 之间共用电子对偏向S D. 原子满足8电子稳定结构
【答案】A
【解析】A项,结构对称、正负电荷重心重合的分子为非极性分子,SF 分子呈正八面体结构,S 原子
6
位于正八面体的中心,该分子结构对称、正负电荷重心重合,所以为非极性分子,A正确;B项,SF 是结
6
构对称、正负电荷重心重合的分子,故键角 不都等于90°,B错误;C项,由于F的电负性比S的大,
S与F之间共用电子对偏向F,C错误;D项,中心元素价电子数+化合价的绝对值=8时该分子中所有原子
都达到8电子稳定结构,但氢化物除外,该化合物中S元素化合价+价电子数=6+6=12,则S原子不是8电
子稳定结构,D错误;故选A。
3.(2022•山东卷节选)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似
的π 6大π键、则吡啶中N原子的价层孤电子对占据_______(填标号)。
6
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
【答案】D【解析】吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的π 6大π键,则
6
说明吡啶中N原子也是采用sp2杂化,杂化轨道只用于形成σ键和存在孤电子对,则吡啶中N原子的价层
孤电子对占据sp2杂化轨道,故选D。
4.(2022•北京卷节选)比较SO 2-和HO分子中的键角大小并给出相应解释:___________。
4 2
【答案】SO 2-的键角大于HO,SO 2-中S原子的价层电子对数为4、孤对电子对数为0,离子的空间构
4 2 4
型为正四面体形,HO分子中O原子的价层电子对数为4、孤对电子对数为2,分子的空间构型为V形
2
【解析】硫酸根离子中硫原子的价层电子对数为4、孤对电子对数为0,离子的空间型为正四面体形,
水分子中氧原子的价层电子对数为4、孤对电子对数为2,分子的空间构型为V形,所以硫酸根离子的键
角大于水分子。
5.(2022•河北省选择性考试节选)SnCl -的几何构型为_______,其中心离子杂化方式为_______。
3
【答案】三角锥形 sp3杂化
【解析】Sn是ⅣA族元素,SnCl -的中心离子Sn2+价层电子对数为3+ ,有1对孤电子对,
3
中心离子是sp3杂化,SnCl -的几何构型是三角锥形。
3
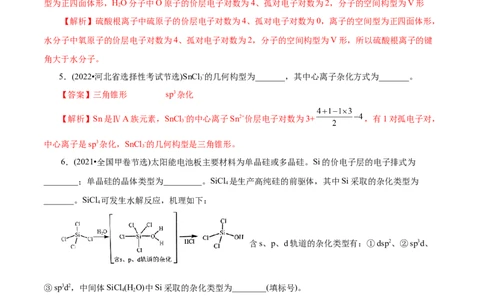
6.(2021•全国甲卷节选)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排式为
________;单晶硅的晶体类型为_________。SiCl 是生产高纯硅的前驱体,其中Si采取的杂化类型为
4
_______。SiCl 可发生水解反应,机理如下:
4
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、
③sp3d2,中间体SiCl (H O)中Si采取的杂化类型为________(填标号)。
4 2
【答案】(1)3s23p2 原子晶体(共价晶体) sp3 ②
【解析】(1)基态Si原子的核外电子排布式为1s22s22p63s23p2,因此Si的价电子层的电子排式为
3s23p2;晶体硅中Si原子与Si原子之间通过共价键相互结合,整块晶体是一个三维的共价键网状结构,因
此晶体硅为原子晶体;SiCl 中Si原子价层电子对数为4+ =4,因此Si原子采取sp3杂化;由图可知,
4
SiCl (H O)中Si原子的δ键数为5,说明Si原子的杂化轨道数为5,由此可知Si原子的杂化类型为sp3d。
4 27.(2021•全国乙卷节选) [Cr(NH )(H O) Cl]2+中配体分子NH 、HO以及分子PH 的空间结构和相应
3 3 2 2 3 2 3
的键角如图所示。
PH 中P的杂化类型是_______。NH 的沸点比PH 的_______,原因是_______,HO的键角小于NH
3 3 3 2 3
的,分析原因_______。
【答案】sp3 高 NH 存在分子间氢键 NH 含有一对孤对电子,而HO含有两对孤对电子,
3 3 2
HO中的孤对电子对成键电子对的排斥作用较大
2
【解析】PH 的价层电子对为3+1=4,故PH 中P的杂化类型是sp3; N原子电负性较强,NH 分子之
3 3 3
间存在分子间氢键,因此NH 的沸点比PH 的高;HO的键角小于NH 的,原因是:NH 含有一对孤对电
3 3 2 3 3
子,而HO含有两对孤对电子,HO中的孤对电子对成键电子对的排斥作用较大。
2 2
1.判断分子中中心原子的杂化轨道类型的方法
(1)根据分子或离子中有无π键及π键数目判断。没有π键的为sp3杂化,如CH 中的C原子;含1个π
4
键的为sp2杂化,如HCHO中的C原子;含2个π键的为sp杂化,如二氧化碳分子和乙炔分子中的碳原子。
(2)根据VSEPR模型、中尽原子价层电子对数判断。如ABn型中心原子的价层电子对数为4,中心原
子的杂化轨道类型为sp3杂化;价层电子对数为3,中心原子的杂化轨道类型为sp2杂化;价层电子对数为
2,中心原子的杂化轨道类型为sp杂化;
2.分子的立体结构的判断
(1)三种杂化轨道的轨道形状,sp杂化夹角为180°的直线型杂化轨道,例如BeCl 、C H ;sp2 杂化轨
2 2 2
道为120°的平面三角形,例如BF、C H;sp3杂化轨道为109°28′的正四面体构型,例如CH、CCl 。
3 2 4 4 4
(2)根据价层电子对互斥理论确定中心原子杂化类型,价层电子对数n= ,
(氧族元素原子做中心原子提供6个价电子,做配位原子不提供价电子,卤族元素原子做中心原子提供7个
价电子,做配位原子提供1个价电子),一般n=2,采取sp杂化,n=3采取sp2杂化,n=4采取sp3杂化,
据此判断。
3.预测分子或离子空间结构的步骤。第一步:确定中心原子上的价层电子对数
a为中心原子的价电子数(若为离子则应加上或减去相应的电荷数),x为与中心原子结合的原子数,b
为与中心原子结合的原子最多能接受的电子数。如NH + 的中心原子为N,a=5-1=4,b=1,x=4,所以中心
4
1 1
原子上的孤电子对数= (a-xb)= ×(4-4×1)=0。
2 2
第二步:确定价层电子对的VSEPR模型
由于价层电子对之间的相互排斥作用,它们趋向于尽可能地相互远离,这样已知价层电子对的数目,
就可以确定价层电子对的VSEPR模型。
第三步:分子空间结构的确定。价层电子对有成键电子对和孤电子对之分,价层电子对的总数减去成
键电子对数,得孤电子对数。根据成键电子对数和孤电子对数,可以确定相应的较稳定的分子空间结构。
注意:(1)若AB 型分子中,A与B之间通过两对或三对电子(即通过双键或三键)结合而成,则价层电
n
子对互斥理论把双键或三键作为一对电子对看待。
(2)价层电子对之间相互排斥作用大小的一般规律:孤电子对-孤电子对>孤电子对-成键电子对>成键电
子对-成键电子对。随着孤电子对数目的增多,斥力增大,键角减小。如CH 、NH 和HO分子中的键角依
4 3 2
次减小。
4.比较键角大小的思维模型1.(2023届·北京市第十一中学高三摸底考试)下列粒子的空间构型不同于其他三个的是( )
A.气态SeO B.气态SO C.SO 2- D.NO -
3 3 3 3
2.推理是学习化学知识的一种重要方法。下列推理合理的是( )
A.SO 中硫原子采取sp2杂化,则CO 中碳原子也采取sp2杂化
2 2
B.NH 分子的空间结构是三角锥形,则NCl 分子的空间结构也是三角锥形
3 3
C.HO分子的键角是105°,则HS分子的键角也是105°
2 2
D.PCl 分子中每个原子最外层达到8电子稳定结构,则BF 分子中每个原子最外层也能达到8电子稳
3 3
定结构
3.下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.PCl 中P原子sp3杂化,为三角锥形 B.BCl 中B原子sp2杂化,为平面三角形
3 3
C.CS 中C原子sp杂化,为直线形 D.HS分子中,S为sp杂化,为直线形
2 2
4.(2022·江苏省木渎苏苑高三联合适应性检测)下列有关SO 、SO 、SO 2-和SO 2-的说法正确的是
2 3 3 4
( )
A.SO 2-中S原子的杂化方式为sp2 B.SO 2-的空间构型为平面正方形
3 4
C.SO 分子中的键角小于SO 分子中的键角 D.SO 分子是极性分子
2 3 3
5.(2022·江苏省泰州市第四次调研测试)催化剂作用下,SO 与Cl 反应生成SO Cl;对SO 水溶液的
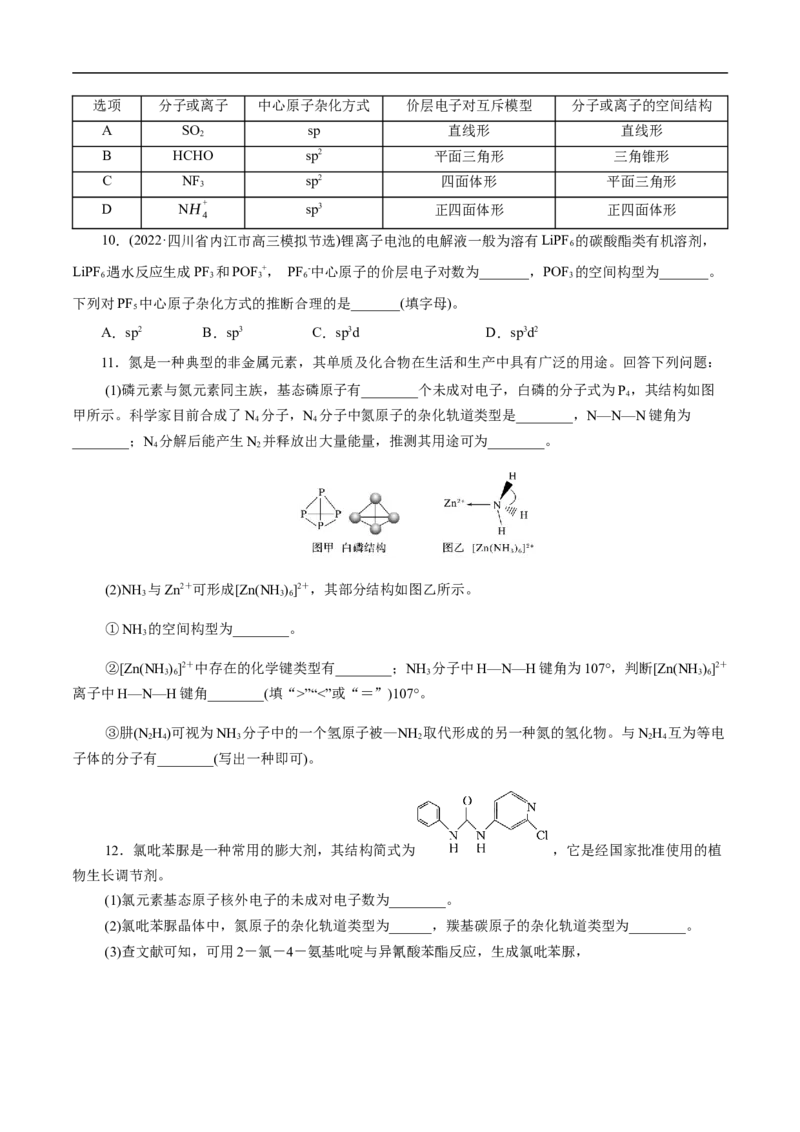
2 2 2 2 2光谱分析可以检测到HSO -、SO2-和痕量的SO 2-,三氧化硫在液态时有单分子SO 和三聚的(SO )(结构如
3 2 3 3 3 3 3
下图所示)两种形式,在高温时能将HBr氧化为Br 。关于说法正确的是( )
2
A.SO 、SO 都是非极性分子
2 3
B.SO Cl 为正四面体结构
2 2
C.SO 、SO 2-中S原子都是sp2杂化
3 3
D.1 mol (SO ) 分子中含有12 mol σ键
3 3
6.(2022·江苏省平潮高级中学等五校临门一脚)氨是一种重要的化工原料,主要用于化肥工业,也广
泛用于硝酸、纯碱、制药等工业;合成氨反应为N(g)+3H(g) 2NH (g)ΔH=-92.4kJ·mol-1。实验室用加
2 2 3
热NH Cl和Ca(OH) 固体混合物的方法制取少量氨气;侯氏制碱法用氨气、二氧化碳,与饱和食盐水制备
4 2
纯碱碳酸钠。下列有关NH 、NF 、NH +、NO -、NO -等含氮粒子的说法正确的是( )
3 3 4 2 3
A.NH 中N-H键角比NH +中N-H键角大
3 4
B.NH 极易溶于水,主要原因是NH 分子间能形成氢键
3 3
C.NH 的水溶液能导电,但一水合氨不能完全电离,因此NH 属于弱电解质
3 3
D.NH 、NF 的空间构型都是三角锥型,NO -、NO -中的N都是sp2杂化
3 3 2 3
7.有几种阴离子的信息如下:
阴离子 ClO - ClO - M ClO-
4 3
中心元素化合价 +5 +3 +1
中心原子杂化类型 sp3 sp3
下列推断不正确的是( )
A.ClO -和CO2-的价电子总数相同 B.M的化学式为ClO -
3 3 2
C.ClO -、ClO-中氯原子的杂化类型都为sp3 D.M的空间结构为V形
3
8.短周期元素X、Y、Z原子序数依次增大,X元素基态原子有2个未成对电子,Y元素基态原子的
核外p电子数比s电子数少1个,Z的一种“超原子”(Z -)具有40个价电子,下列说法错误的是( )
13
A.简单离子半径:Y<Z B.XO 2-的空间构型为平面三角形
3
C.YO -中心原子的杂化方式为sp2杂化 D.X、Y、Z的电负性:Y>X>Z
3
9.根据杂化轨道理论和价层电子对互斥模型,判断下列分子或离子的空间结构正确的是( )选项 分子或离子 中心原子杂化方式 价层电子对互斥模型 分子或离子的空间结构
A SO sp 直线形 直线形
2
B HCHO sp2 平面三角形 三角锥形
C NF sp2 四面体形 平面三角形
3
D NH+ sp3 正四面体形 正四面体形
4
10.(2022·四川省内江市高三模拟节选)锂离子电池的电解液一般为溶有LiPF 的碳酸酯类有机溶剂,
6
LiPF 遇水反应生成PF 和POF +, PF -中心原子的价层电子对数为_______,POF 的空间构型为_______。
6 3 3 6 3
下列对PF 中心原子杂化方式的推断合理的是_______(填字母)。
5
A.sp2 B.sp3 C.sp3d D.sp3d2
11.氮是一种典型的非金属元素,其单质及化合物在生活和生产中具有广泛的用途。回答下列问题:
(1)磷元素与氮元素同主族,基态磷原子有________个未成对电子,白磷的分子式为P,其结构如图
4
甲所示。科学家目前合成了N 分子,N 分子中氮原子的杂化轨道类型是________,N—N—N键角为
4 4
________;N 分解后能产生N 并释放出大量能量,推测其用途可为________。
4 2
(2)NH 与Zn2+可形成[Zn(NH )]2+,其部分结构如图乙所示。
3 3 6
①NH 的空间构型为________。
3
②[Zn(NH )]2+中存在的化学键类型有________;NH 分子中H—N—H键角为107°,判断[Zn(NH )]2+
3 6 3 3 6
离子中H—N—H键角________(填“>”“<”或“=”)107°。
③肼(N H)可视为NH 分子中的一个氢原子被—NH 取代形成的另一种氮的氢化物。与NH 互为等电
2 4 3 2 2 4
子体的分子有________(写出一种即可)。
12.氯吡苯脲是一种常用的膨大剂,其结构简式为 ,它是经国家批准使用的植
物生长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为________。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为______,羰基碳原子的杂化轨道类型为________。
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲,反应过程中,每生成1 mol氯吡苯脲,断裂________个σ键,断裂________个π键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有HO、NH 、CO 等。
2 3 2
①请用共价键知识解释HO分子比NH 分子稳定的原因:________________________。
2 3
②HO、NH 、CO 分子的空间构型分别是__________________,中心原子的杂化类型分别是
2 3 2
______________________________。