文档内容
第六篇 物质结构与性质
专项 43 坐标参数与投影图
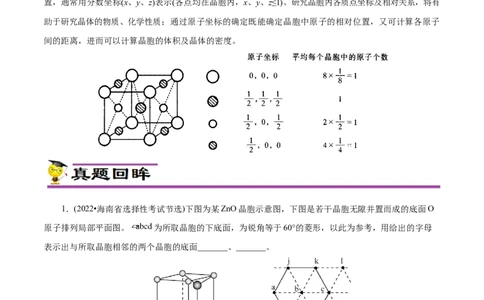
原子坐标参数是晶胞的基本要素之一,用于表示晶胞内部各原子的相对位置。晶胞中各原子的坐标位
置,通常用分数坐标(x、y、z)表示(各点均在晶胞内,x、y、z≤1)。研究晶胞内各质点坐标及相对关系,将有
助于研究晶体的物质、化学性质;通过原子坐标的确定既能确定晶胞中原子的相对位置,又可计算各原子
间的距离,进而可以计算晶胞的体积及晶体的密度。
1.(2022•海南省选择性考试节选)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O
原子排列局部平面图。 为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母
表示出与所取晶胞相邻的两个晶胞的底面_______、_______。
【答案】 ▱cdhi ▱bcek
【解析】根据晶胞示意图,一个晶胞中8个O原子位于晶胞的顶点,1个O原子位于晶胞体内,4个
Zn原子位于晶胞的棱上,1个Zn原子位于晶胞体内,棱上的3个Zn原子和体内的Zn原子、O原子形成四
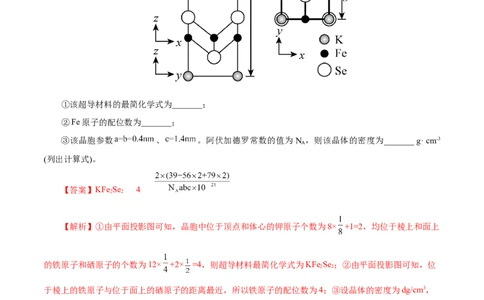
面体结构,则于其相邻的晶胞与该晶胞共用bc和cd,则相邻的两个晶胞的底面为▱cdhi和▱bcek。2.(2022•湖南选择性考试节选)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分
别如图所示:
①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数 、 。阿伏加德罗常数的值为N ,则该晶体的密度为_______ g· cm-3
A
(列出计算式)。
【答案】KFe Se 4
2 2
【解析】①由平面投影图可知,晶胞中位于顶点和体心的钾原子个数为8× +1=2,均位于棱上和面上
的铁原子和硒原子的个数为12× +2× =4,则超导材料最简化学式为KFe Se ;②由平面投影图可知,位
2 2
于棱上的铁原子与位于面上的硒原子的距离最近,所以铁原子的配位数为4;③设晶体的密度为dg/cm3,
由晶胞的质量公式可得: =abc×10—21×d,解得d= 。
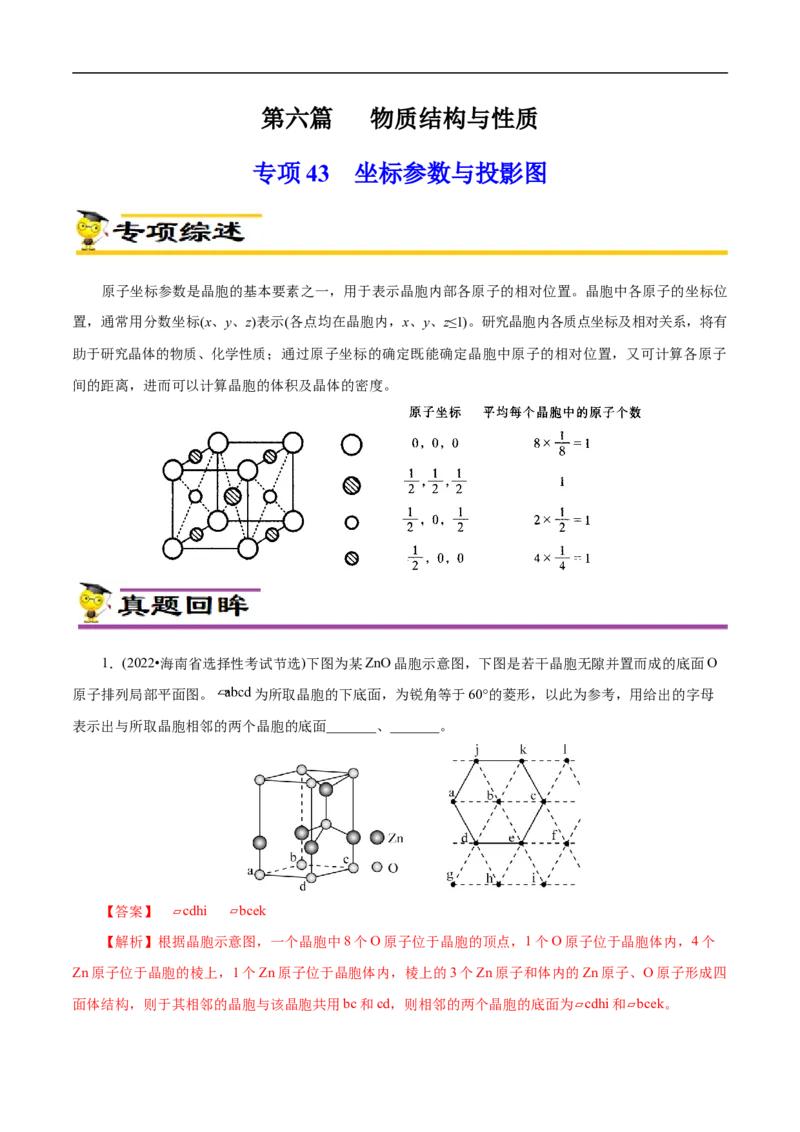
3.(2022•广东选择性考试节选)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预
测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材
料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______ (列
出计算式,N 为阿伏加德罗常数的值)。
A
【答案】KSeBr
2 6
【解析】①根据晶胞结构得到K有8个, 有 ,则X的化学式为
KSeBr ;②设X的最简式的式量为 ,晶体密度为 ,设晶胞参数为anm,得到
2 6
,解得 ,X中相邻K之间的最短距离为晶胞参数的一半即
。
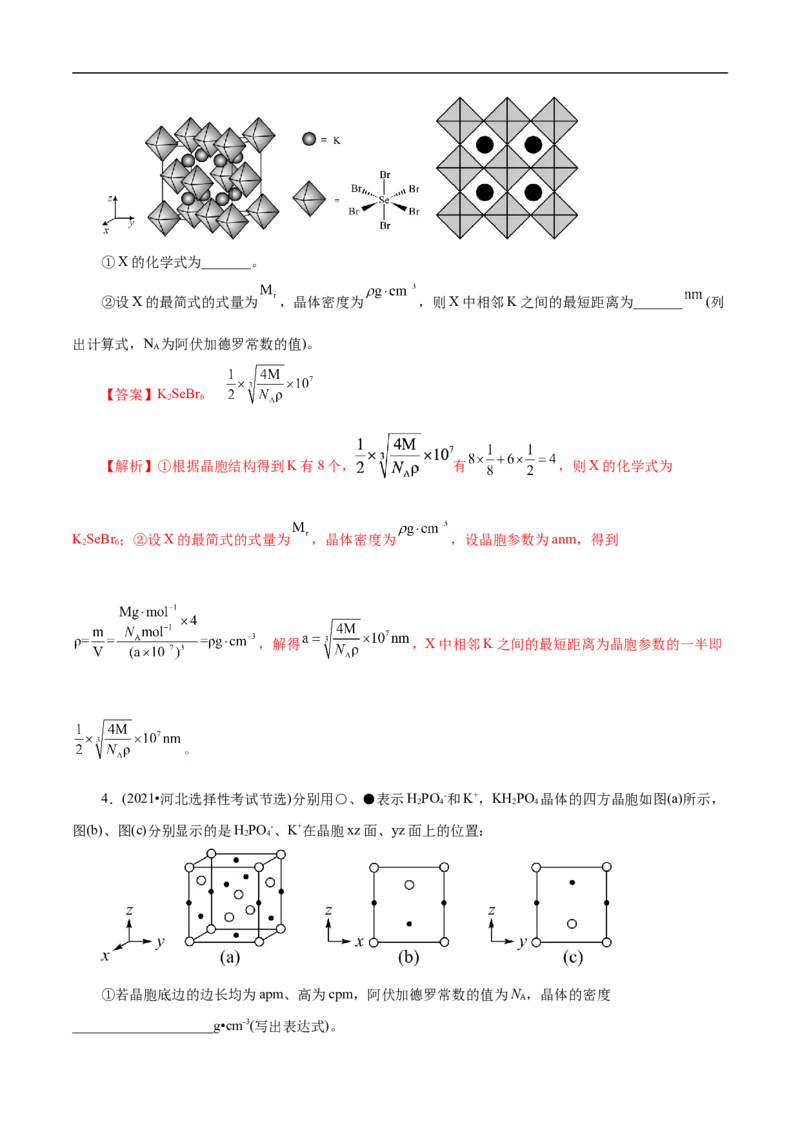
4.(2021•河北选择性考试节选)分别用○、●表示HPO -和K+,KH PO 晶体的四方晶胞如图(a)所示,
2 4 2 4
图(b)、图(c)分别显示的是HPO -、K+在晶胞xz面、yz面上的位置:
2 4
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为N ,晶体的密度
A
____________________g•cm-3(写出表达式)。②晶胞在x轴方向的投影图为_________ (填标号)。
【答案】① ②B
【解析】①由晶胞结构可知,HPO -位于晶胞的顶点、面上和体心,顶点上有8个、面上有4个,体
2 4
心有1个,故晶胞中HPO -的数目为 ;K+位于面上和棱上,面上有6个,棱上4个,
2 4
故晶胞中K+的数目为 。因此,平均每个晶胞中占有的HPO -和K+的数目均为4,若晶胞
2 4
底边的边长均为apm、高为cpm,则晶胞的体积为10-30a2c cm3,阿伏加德罗常数的值为N ,晶体的密度为
A
。②由图(a)、(b)、(c)可知,晶胞在x轴方向的投影图为 ,选B。
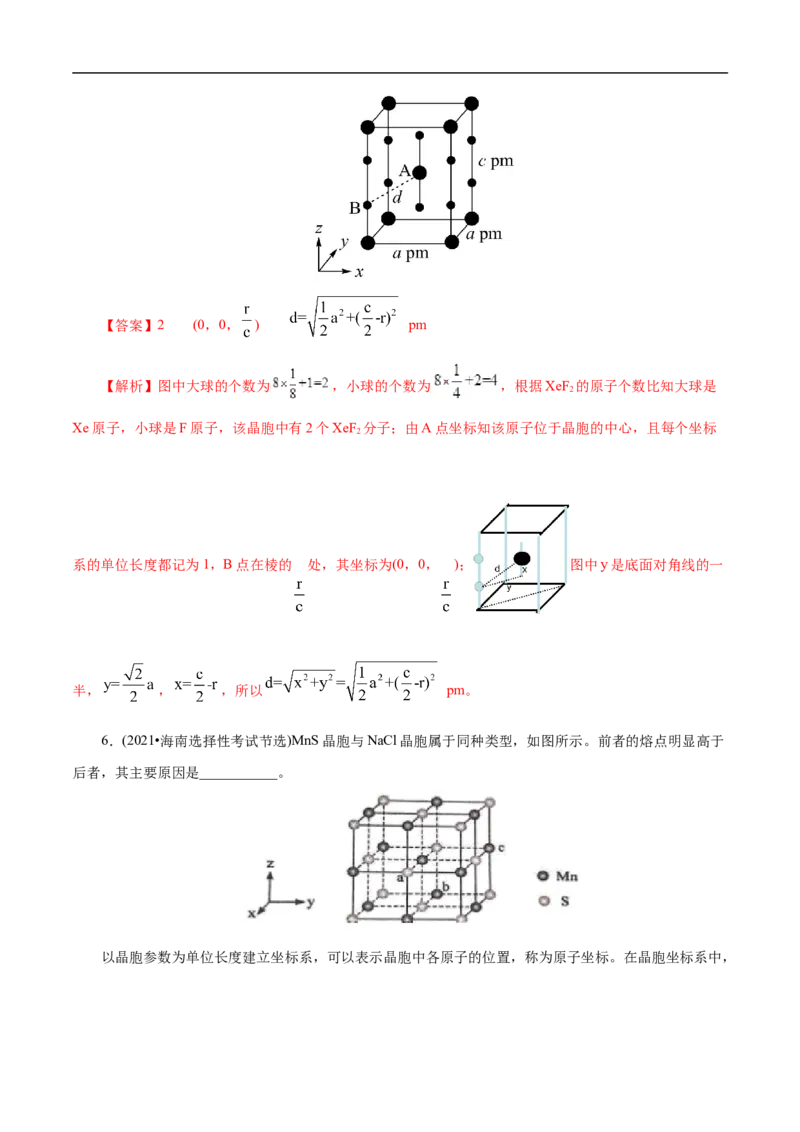
5.(2021•山东卷节选)XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
2
_____个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数
2
坐标,如A点原子的分数坐标为( , , )。已知Xe—F键长为rpm,则B点原子的分数坐标为
________;晶胞中A、B间距离d=_______________pm。【答案】2 (0,0, ) pm
【解析】图中大球的个数为 ,小球的个数为 ,根据XeF 的原子个数比知大球是
2
Xe原子,小球是F原子,该晶胞中有2个XeF 分子;由A点坐标知该原子位于晶胞的中心,且每个坐标
2
系的单位长度都记为1,B点在棱的 处,其坐标为(0,0, ); 图中y是底面对角线的一
半, , ,所以 pm。
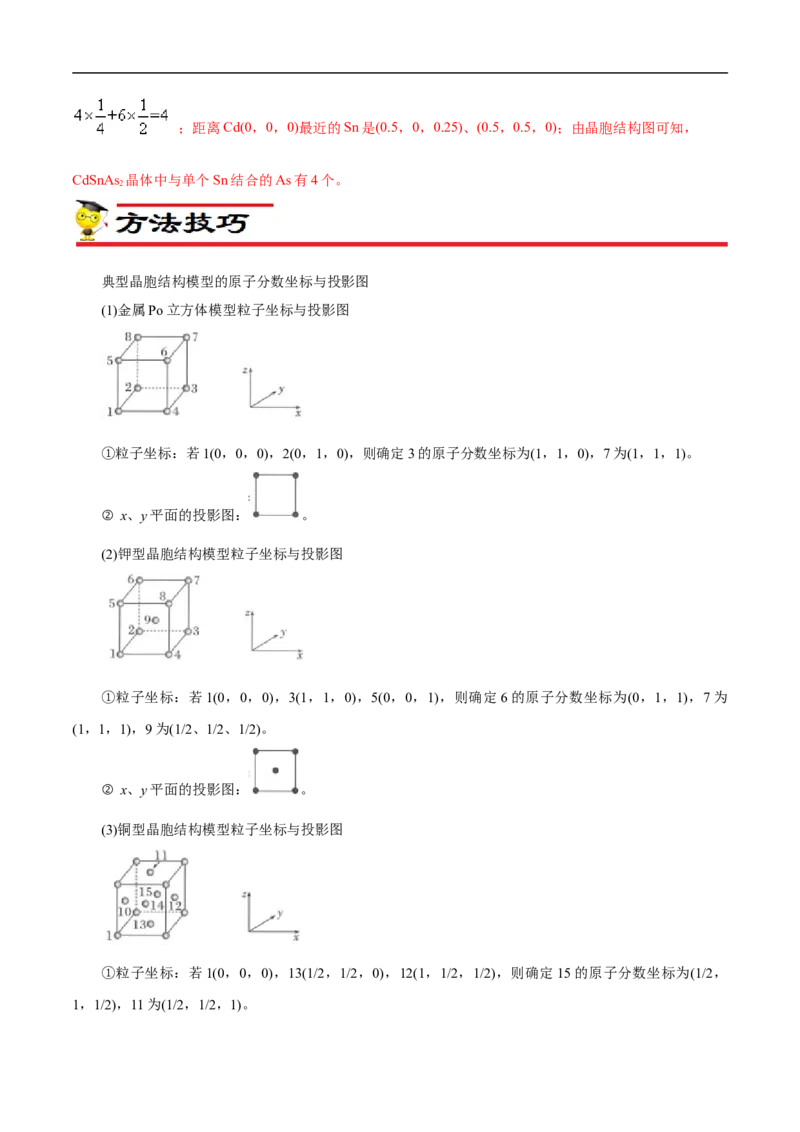
6.(2021•海南选择性考试节选)MnS晶胞与NaCl晶胞属于同种类型,如图所示。前者的熔点明显高于
后者,其主要原因是___________。
以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在晶胞坐标系中,a点硫原子坐标为 ,b点锰原子坐标为 ,则c点锰原子坐标为___________。
【答案】MnS中阴阳离子所带电荷数比NaCl的多,离子键强度更大 (0,1,1/2)
【解析】①离子晶体熔沸点高低不光与晶体结构有关,也与离子带电荷量有关,MnS晶体中每个离子
都带2个单位电荷(正或负),而NaCl晶体中,每个离子只带1个单位电荷,所以本问第一空应填“MnS中
阴阳离子所带电荷数比NaCl的多,离子键强度更大”;②根据题目所给信息,依据a、b两点原子的三维
坐标推得,MnS晶胞的三维坐标关系是以b点左侧y轴上同一高度的S原子中心为三维坐标中心,轴向上
每两个最近的S原子(或Mn原子)间距为单位长度,那么c点Mn原子的坐标为(0,1,1/2)。
7.(2020•山东卷节选)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的
分数坐标。四方晶系CdSnAs 的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标
2
如下表所示。
坐标原子 x y z
Cd 0 0 0
Sn 0 0 0.5
As 0.25 0.25 0.125
一个晶胞中有_________个Sn,找出距离Cd(0,0,0)最近的Sn_________(用分数坐标表示)。CdSnAs
2
晶体中与单个Sn键合的As有___________个。
【答案】4 (0.5,0,0.25)、(0.5,0.5,0) 4
【解析】由部分Cd原子的分数坐标为(0,0,0),可知8个Cd在晶胞的顶点,4个Cd在晶胞的面心,1
个在晶胞的体心;部分Sn原子的分数坐标为(0,0,0.5),4个Sn在晶胞的棱上,6个Sn在晶胞的面心;
部分As原子的分数坐标为(0.25,0.25,0.125),8个As在晶胞的体心;所以1个晶胞中Sn的个数为;距离Cd(0,0,0)最近的Sn是(0.5,0,0.25)、(0.5,0.5,0);由晶胞结构图可知,
CdSnAs 晶体中与单个Sn结合的As有4个。
2
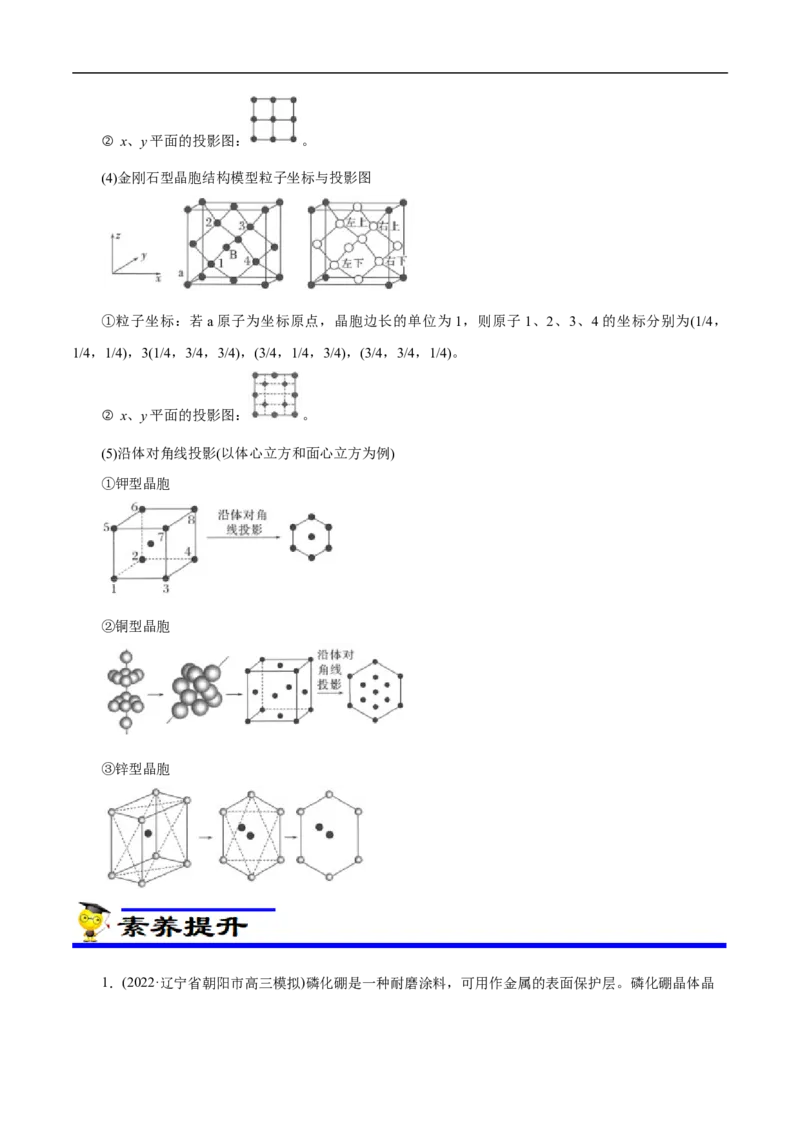
典型晶胞结构模型的原子分数坐标与投影图
(1)金属Po立方体模型粒子坐标与投影图
①粒子坐标:若1(0,0,0),2(0,1,0),则确定3的原子分数坐标为(1,1,0),7为(1,1,1)。
② x、y平面的投影图: 。
(2)钾型晶胞结构模型粒子坐标与投影图
①粒子坐标:若1(0,0,0),3(1,1,0),5(0,0,1),则确定6的原子分数坐标为(0,1,1),7为
(1,1,1),9为(1/2、1/2、1/2)。
② x、y平面的投影图: 。
(3)铜型晶胞结构模型粒子坐标与投影图
①粒子坐标:若1(0,0,0),13(1/2,1/2,0),12(1,1/2,1/2),则确定15的原子分数坐标为(1/2,
1,1/2),11为(1/2,1/2,1)。② x、y平面的投影图: 。
(4)金刚石型晶胞结构模型粒子坐标与投影图
①粒子坐标:若a原子为坐标原点,晶胞边长的单位为1,则原子1、2、3、4的坐标分别为(1/4,
1/4,1/4),3(1/4,3/4,3/4),(3/4,1/4,3/4),(3/4,3/4,1/4)。
② x、y平面的投影图: 。
(5)沿体对角线投影(以体心立方和面心立方为例)
①钾型晶胞
②铜型晶胞
③锌型晶胞
1.(2022·辽宁省朝阳市高三模拟)磷化硼是一种耐磨涂料,可用作金属的表面保护层。磷化硼晶体晶胞(立方体)如图所示。已知原子坐标 为 , 为 ,晶胞的密度为 ,阿伏加德罗常数的
值用 表示。下列说法中正确的是( )
A.磷原子的配位数为12 B.图中a原子的坐标是
C.磷化硼晶体的晶胞边长为 D.电负性:
【答案】C
【解析】A项,以上底面面心P原子为研究对象,与之距离最近且相等的硼原子为该晶胞内部上层2
个B原子,还有上层晶胞内部下层2个B原子,即磷原子的配位数为4,A错误;B项,图中a原子处于上
层、左侧、后方 晶胞体心位置,可知a左侧面距离为晶胞棱长的 ,即 ,到前平面、下底面距离均
为晶胞棱长的 ,则坐标参数 ,则a原子的坐标为 ,B错误;C项,根据均摊法一个晶
胞中含有P个数为 ,含有B个数为4,设晶胞边长为xcm,则
,C正确;D项,电负性P大于B,D错误;故选C。
2.(2022·宁夏银川一中高三模拟节选)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为
_______;其中原子坐标参数A为(0,0,0),B为(0, , ),则晶胞中氮原子的坐标参数为_______。【答案】MnZnN ( , , )
3
【解析】(4)某种含锰特殊材料的晶胞结构如图所示,根据晶胞结构分析N有1个,Zn有 ,Mn
有 ,则该晶体的化学式为MnZnN;其中原子坐标参数A为(0,0,0),B为(0, , ),氮原子
3
在体心,因此晶胞中氮原子的坐标参数为( , , )。
3.(2022·四川省内江市高三模拟节选)链化锂被认为是很有潜力的正极材料,晶胞结构如图所示。
(1)晶施可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体
的化学式为_______。
(2)图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为_______,Bi与Li(1)和Li(2)之
间的最短距离的比值为_______。
【答案】(1)BiLi (2)(0.25,0.75,0.25)
3
【解析】Bi位于顶点和面心,个数为 =4,Li(1)位于棱上和体心,个数为 ,
Li(2)位于体内,个数为8,Bi、Li个数比为4:(4+8)=1:3,则晶体的化学式为BiLi ;故答案为:BiLi 或者
3 3
LiBi;根据图示找到C的坐标为(0.25,0.75,0.25);设晶胞棱长为a,Bi 与Li(1)之间的最短距离为棱长的
3
一半即 ,Bi 与Li(2)之间的最短距离为体对角线的 ,即为 ,则Bi与Li(1)和Li(2)之间的最短距离的比值为 。
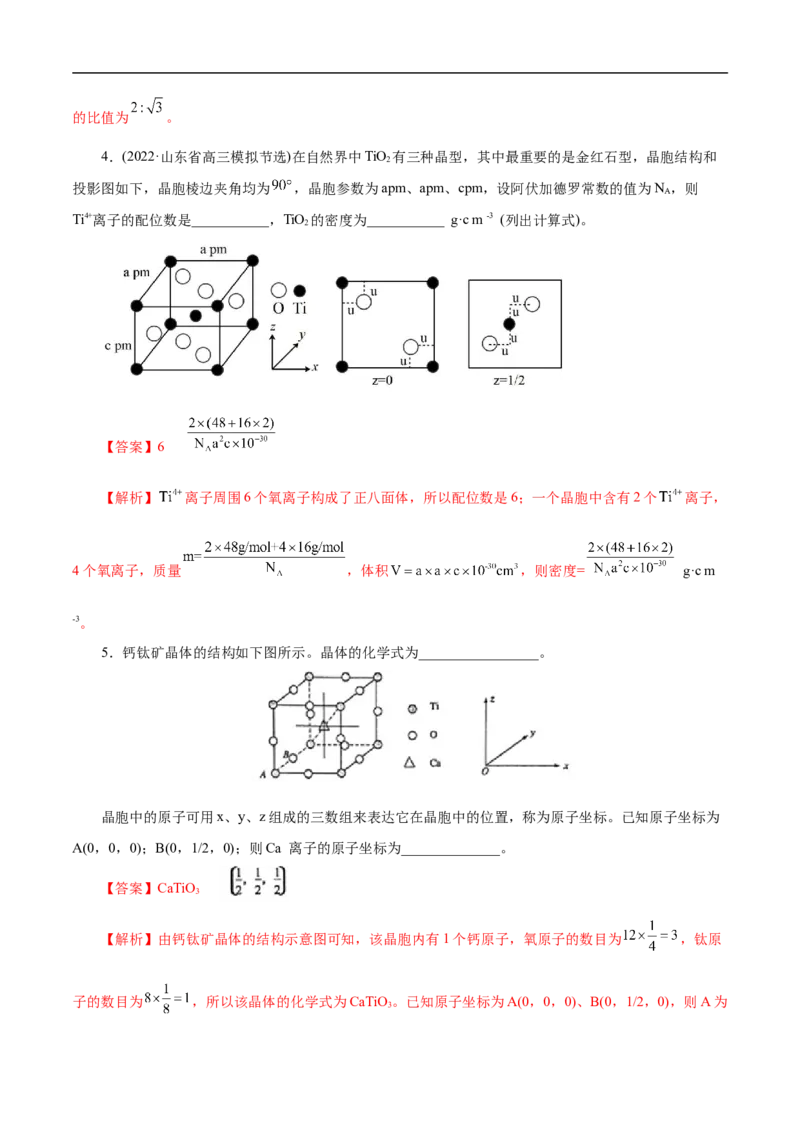
4.(2022·山东省高三模拟节选)在自然界中TiO 有三种晶型,其中最重要的是金红石型,晶胞结构和
2
投影图如下,晶胞棱边夹角均为 ,晶胞参数为apm、apm、cpm,设阿伏加德罗常数的值为N ,则
A
Ti4+离子的配位数是___________,TiO 的密度为___________ g·c m -3 (列出计算式)。
2
【答案】6
【解析】 离子周围6个氧离子构成了正八面体,所以配位数是6;一个晶胞中含有2个 离子,
4个氧离子,质量 ,体积 ,则密度= g·c m
-3。
5.钙钛矿晶体的结构如下图所示。晶体的化学式为_________________。
晶胞中的原子可用x、y、z组成的三数组来表达它在晶胞中的位置,称为原子坐标。已知原子坐标为
A(0,0,0);B(0,1/2,0);则Ca 离子的原子坐标为______________。
【答案】CaTiO
3
【解析】由钙钛矿晶体的结构示意图可知,该晶胞内有1个钙原子,氧原子的数目为 ,钛原
子的数目为 ,所以该晶体的化学式为CaTiO 。已知原子坐标为A(0,0,0)、B(0,1/2,0),则A为
3坐标原点,因为B位于晶胞y轴上且为棱的中心、钙离子在晶胞的体心,所以Ca 离子的原子坐标为
。
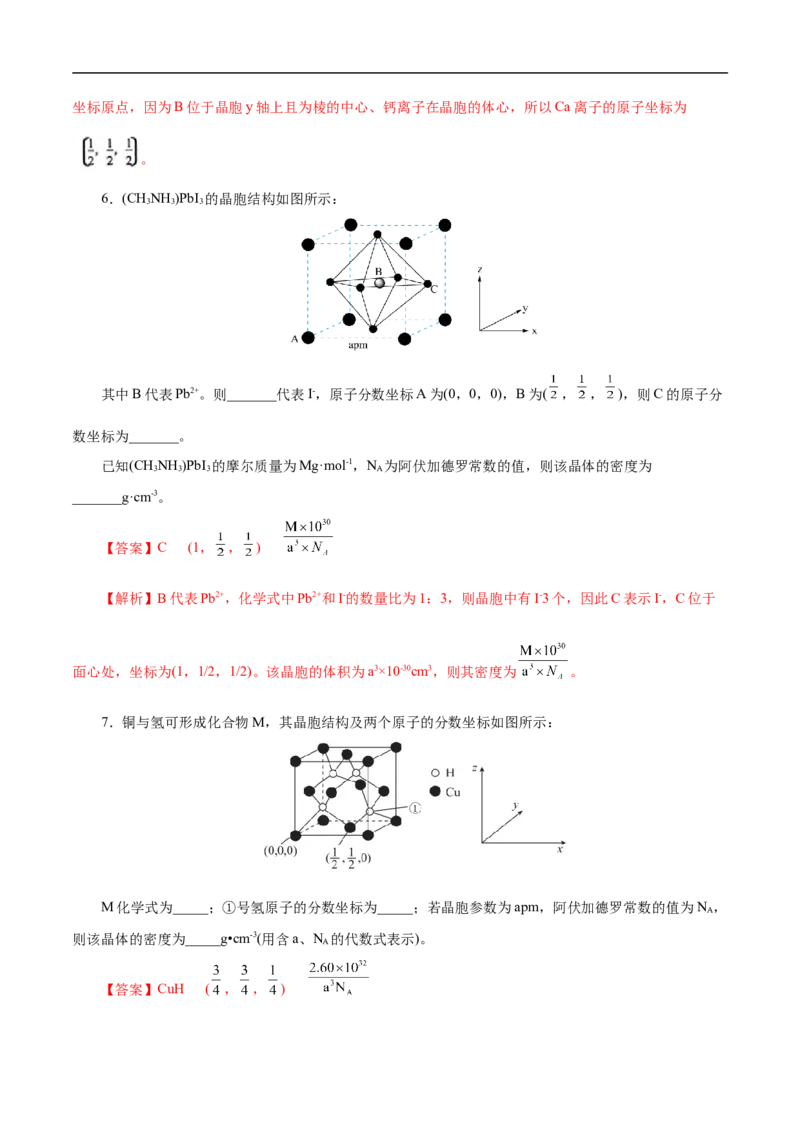
6.(CHNH )PbI 的晶胞结构如图所示:
3 3 3
其中B代表Pb2+。则_______代表I-,原子分数坐标A为(0,0,0),B为( , , ),则C的原子分
数坐标为_______。
已知(CHNH )PbI 的摩尔质量为Mg·mol-1,N 为阿伏加德罗常数的值,则该晶体的密度为
3 3 3 A
_______g·cm-3。
【答案】C (1, , )
【解析】B代表Pb2+,化学式中Pb2+和I-的数量比为1:3,则晶胞中有I-3个,因此C表示I-,C位于
面心处,坐标为(1,1/2,1/2)。该晶胞的体积为a3×10-30cm3,则其密度为 。
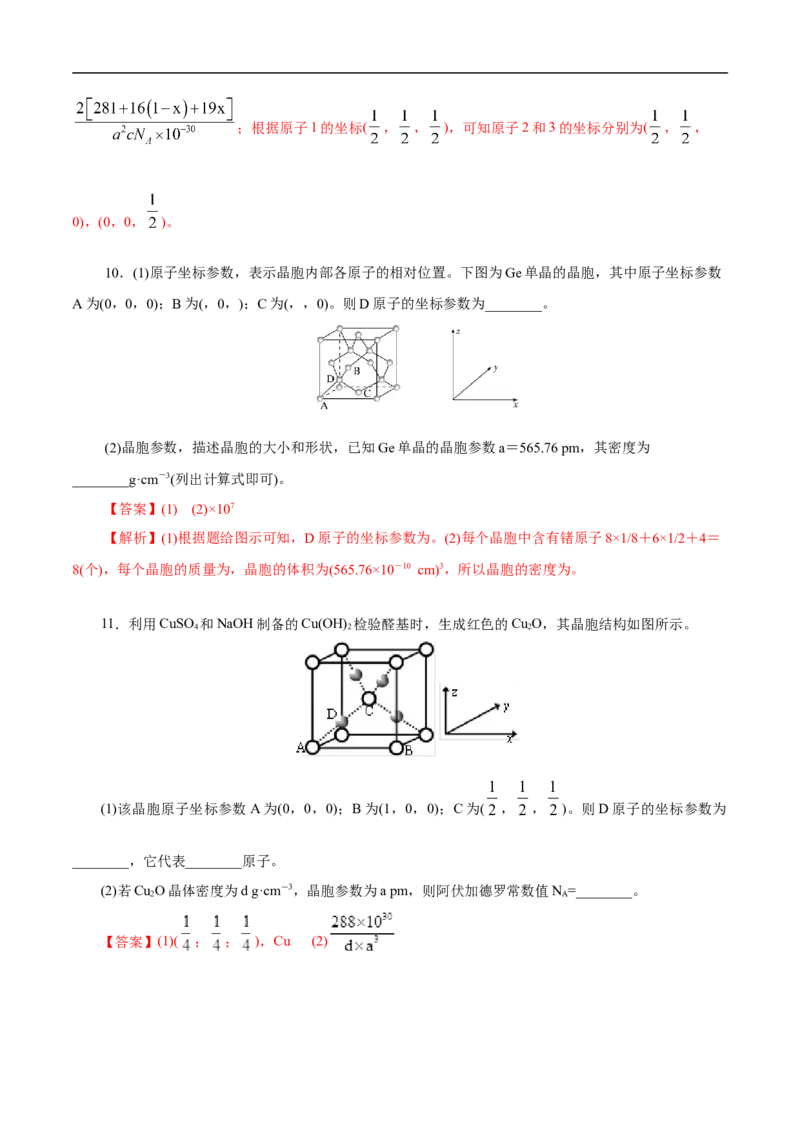
7.铜与氢可形成化合物M,其晶胞结构及两个原子的分数坐标如图所示:
M化学式为_____;①号氢原子的分数坐标为_____;若晶胞参数为apm,阿伏加德罗常数的值为N ,
A
则该晶体的密度为_____g•cm-3(用含a、N 的代数式表示)。
A
【答案】CuH ( , , )【解析】根据均摊原理易求出一个晶胞中含有 4个H、Cu的个数是 =4,M的化学式为
CuH;由已知两个原子的原子分数坐标值可知,①号氢原子的分数坐标为 ;一个晶胞的质量为
,晶胞体积为 ,晶体密度为 。
8.(2022·辽宁省营口市模拟节选)铁酸钇是一种典型的单相多铁性材料,其正交相晶胞结构如图。
铁酸钇的化学式为____。已知1号O原子分数坐标为(0,0, ),2号O原子分数坐标为( , -m,
-n),则3号Fe原子的分数坐标为____。已知铁酸钇的摩尔质量为Mg•mol-1,晶体密度为ρg•cm-3,阿伏
加德罗常数的值为N ,该晶胞的体积为____pm3(列出表达式)。
A
【答案】YFeO ( , +m, ) ×1030
3
【解析】由图可知,该晶胞中Y的个数= ,Fe的个数=2,O的个数= ,所以
铁酸钇的化学式为:YFeO ;已知1号O原子分数坐标为(0,0, ),2号O原子分数坐标为( , -m,
3
-n),则3号Fe原子的分数坐标为( , +m, );晶胞的质量 ,晶胞密度为ρg•cm-3,所以晶胞的体积 ×1030pm3。
9.一种四方结构的超导化合物的晶胞如图1所示,晶胞中Sm和As原子的投影位置如图2所示。
图1 图2
图中F−和O2−共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学
式表示为____________,通过测定密度ρ和晶胞参数,可以计算该物质的 x值,完成它们关系表达式:
ρ=________g·cm−3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图 1中
原子1的坐标为( ),则原子2和3的坐标分别为__________、__________。
【答案】SmFeAsO F ( )、( )
1−x x
【解析】由图1可知,每个晶胞中含Sm原子:4 =2,含Fe原子:4 +1=2,含As原子:4
=2,含O原子:(8 +2 )(1-x)=2(1-x),含F原子:(8 +2 )x=2x,所以该化合物的化学式为
SmFeAsO F;根据该化合物的化学式为SmFeAsO F,一个晶胞的质量为 ,一
1-x x 1-x x
个晶胞的体积为a2c 10-30cm3,则密度 = g/cm3,故答案为:SmFeAsO F;
1-x x;根据原子1的坐标( , , ),可知原子2和3的坐标分别为( , ,
0),(0,0, )。
10.(1)原子坐标参数,表示晶胞内部各原子的相对位置。下图为Ge单晶的晶胞,其中原子坐标参数
A为(0,0,0);B为(,0,);C为(,,0)。则D原子的坐标参数为________。
(2)晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为
________g·cm-3(列出计算式即可)。
【答案】(1) (2)×107
【解析】(1)根据题给图示可知,D原子的坐标参数为。(2)每个晶胞中含有锗原子8×1/8+6×1/2+4=
8(个),每个晶胞的质量为,晶胞的体积为(565.76×10-10 cm)3,所以晶胞的密度为。
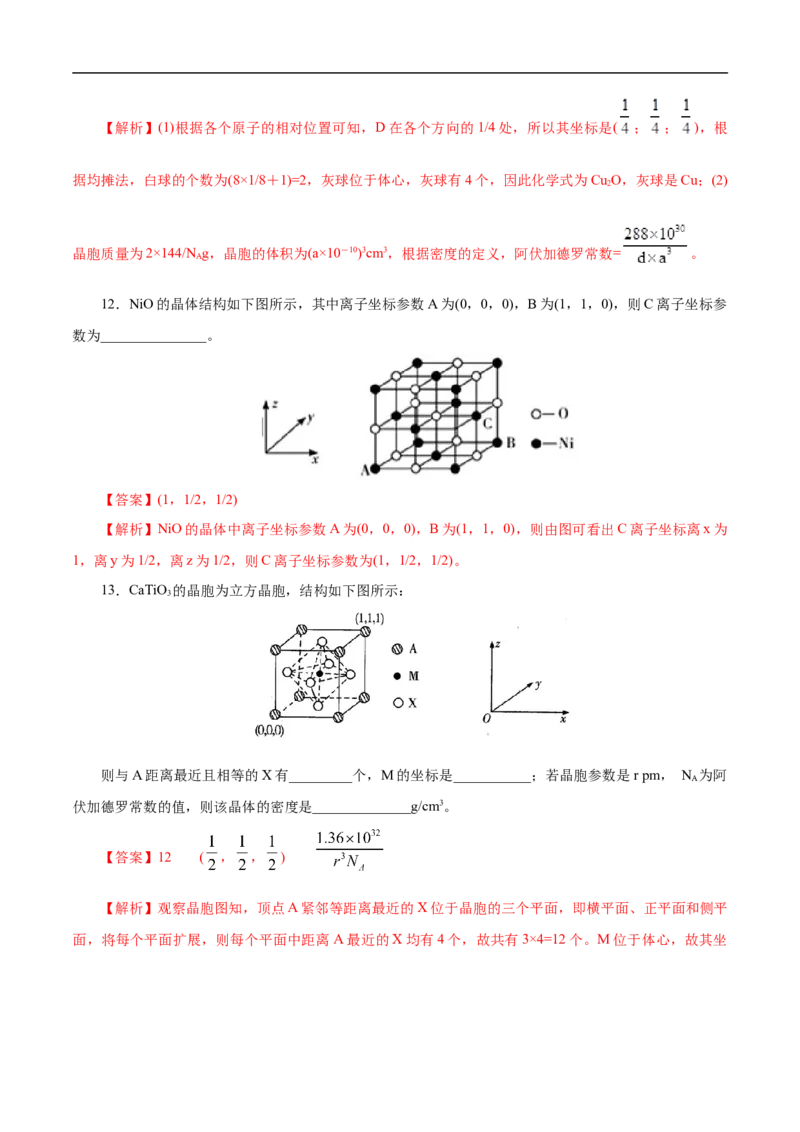
11.利用CuSO 和NaOH制备的Cu(OH) 检验醛基时,生成红色的Cu O,其晶胞结构如图所示。
4 2 2
1 1 1
(1)该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为(2 ,2 ,2 )。则D原子的坐标参数为
________,它代表________原子。
(2)若Cu O晶体密度为d g·cm-3,晶胞参数为a pm,则阿伏加德罗常数值N =________。
2 A
【答案】(1)( ; ; ),Cu (2)【解析】(1)根据各个原子的相对位置可知,D在各个方向的1/4处,所以其坐标是( ; ; ),根
据均摊法,白球的个数为(8×1/8+1)=2,灰球位于体心,灰球有4个,因此化学式为Cu O,灰球是Cu;(2)
2
晶胞质量为2×144/N g,晶胞的体积为(a×10-10)3cm3,根据密度的定义,阿伏加德罗常数= 。
A
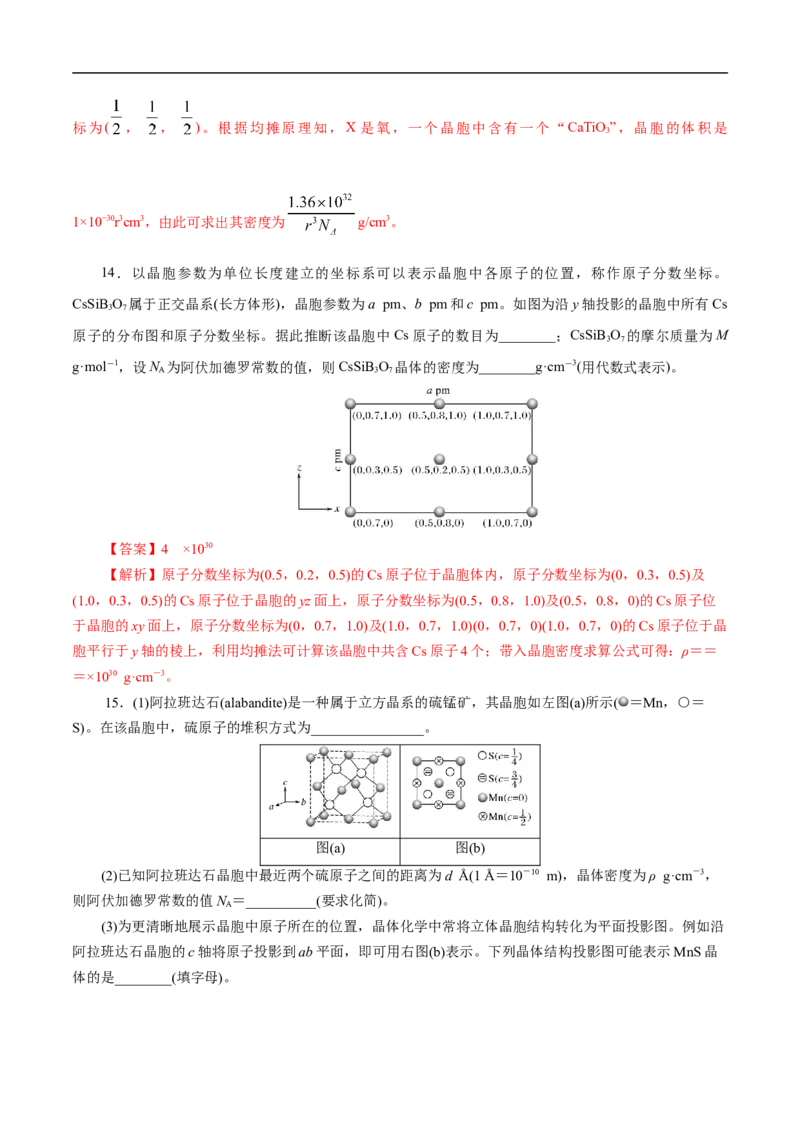
12.NiO的晶体结构如下图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参
数为_______________。
【答案】(1,1/2,1/2)
【解析】NiO的晶体中离子坐标参数A为(0,0,0),B为(1,1,0),则由图可看出C离子坐标离x为
1,离y为1/2,离z为1/2,则C离子坐标参数为(1,1/2,1/2)。
13.CaTiO 的晶胞为立方晶胞,结构如下图所示:
3
则与A距离最近且相等的X有_________个,M的坐标是___________;若晶胞参数是r pm, N 为阿
A
伏加德罗常数的值,则该晶体的密度是______________g/cm3。
【答案】12 ( , , )
【解析】观察晶胞图知,顶点A紧邻等距离最近的X位于晶胞的三个平面,即横平面、正平面和侧平
面,将每个平面扩展,则每个平面中距离A最近的X均有4个,故共有3×4=12个。M位于体心,故其坐标为( , , )。根据均摊原理知,X 是氧,一个晶胞中含有一个“CaTiO ”,晶胞的体积是
3
1×10−30r3cm3,由此可求出其密度为 g/cm3。
14.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。
CsSiB O 属于正交晶系(长方体形),晶胞参数为a pm、b pm和c pm。如图为沿y轴投影的晶胞中所有Cs
3 7
原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为________;CsSiB O 的摩尔质量为M
3 7
g·mol-1,设N 为阿伏加德罗常数的值,则CsSiB O 晶体的密度为________g·cm-3(用代数式表示)。
A 3 7
【答案】4 ×1030
【解析】原子分数坐标为(0.5,0.2,0.5)的Cs原子位于晶胞体内,原子分数坐标为(0,0.3,0.5)及
(1.0,0.3,0.5)的Cs原子位于晶胞的yz面上,原子分数坐标为(0.5,0.8,1.0)及(0.5,0.8,0)的Cs原子位
于晶胞的xy面上,原子分数坐标为(0,0.7,1.0)及(1.0,0.7,1.0)(0,0.7,0)(1.0,0.7,0)的Cs原子位于晶
胞平行于y轴的棱上,利用均摊法可计算该晶胞中共含Cs原子4个;带入晶胞密度求算公式可得:ρ==
=×1030 g·cm-3。
15.(1)阿拉班达石(alabandite)是一种属于立方晶系的硫锰矿,其晶胞如左图(a)所示( =Mn,○=
S)。在该晶胞中,硫原子的堆积方式为________________。
图(a) 图(b)
(2)已知阿拉班达石晶胞中最近两个硫原子之间的距离为d Å(1 Å=10-10 m),晶体密度为ρ g·cm-3,
则阿伏加德罗常数的值N =__________(要求化简)。
A
(3)为更清晰地展示晶胞中原子所在的位置,晶体化学中常将立体晶胞结构转化为平面投影图。例如沿
阿拉班达石晶胞的c轴将原子投影到ab平面,即可用右图(b)表示。下列晶体结构投影图可能表示MnS晶
体的是________(填字母)。A.
B.
D.
C.
【答案】(1)面心立方最密堆积 (2) (3)C
【解析】(1)据图可知S原子位于Mn原子的正四面体空隙中,整体结构与金刚石排列相似,所以S原
子的堆积方式和Mn原子的堆积方式相同,晶胞中Mn原子位于面心和顶角,为面心立方最密堆积,则硫
原子的堆积方式也为面心立方最密堆积。(2)结合图(a)和图(b)可知最近两个硫原子之间的距离为面对角线的
一半,所以晶胞的面对角线长度为2dÅ=2d×10-8 cm,所以晶胞的边长为d×10-8cm,所以晶胞的体积V=
2d3×10-24cm3,根据均摊法,晶胞中S原子的个数为4,Mn原子的个数为8×+6×=4,所以晶胞的质量m
=g,所以有ρ= g·cm-3,解得N =。(3)阿拉班达石晶胞中S原子和Mn原子的配位数均为4;A选项所示
A
投影中Mn原子的配位数为6,与晶胞结构不符,故错误;B选项所示投影中Mn原子的配位数为8,与晶
胞结构不符,故错误;C选项所示投影中Mn原子的配位数为4(以中心Mn原子为例,c=0的面上的2个S
原子和c=1的面上的2个S原子),S原子的配位数也为4(以晶胞内部的S原子为例,S原子位于4个Mn
原子的正四面体中心),与晶胞结构符合,故正确;D选项所示的Mn原子为六方最密堆积,而阿拉班达石
晶胞中Mn原子为面心立方最密堆积,与晶胞结构不符合,故错误。