文档内容
专项训练 大π键的判断和书写(解析版)
一、单选题
1.离子液体广泛应用于科研和生产中。某离子液体结构如下图,其中阳离子有类似苯
环的特殊稳定性,下列说法错误的是
A.阳离子中C有两种不同的杂化方式 B.阳离子中存在大π键
C.阳离子中所有C、N原子不可能共面 D.阴离子中含有配位键
【答案】C
【详解】A.由图可知,阳离子中的饱和碳原子的杂化方式为sp3杂化,双键碳原子的
的杂化方式为sp2杂化,共有2种,故A正确;
B.阳离子有类似苯环的特殊稳定性说明阳离子中环上的碳原子和氮原子杂化方式均为
sp2杂化,未参与杂化的p电子形成了π 大π键,故B正确;
C.阳离子有类似苯环的特殊稳定性说明环为平面结构,由三点成面可知,离子中所有
碳原子和氮原子可能共面,故C错误;
D.由化学式可知,四氯合铝离子中具有空轨道的铝离子与具有孤对电子的氯离子形
成了配位键,故D正确;
故选C。
2.锌的某种配合物结构如图所示,已知该配合物中碳原子形成的环状结构均为平面结
构。下列说法错误的是
A.该配合物中非金属元素电负性最小的是氢
B.1mol该配合物中通过螯合作用形成的配位键有4mol
C.该配合物受热时首先断裂的配位键是氮锌键
D.该配合物中存在 、 两种大π键
资料收集整理【淘宝店铺:向阳百分百】【答案】C
【详解】A.该配合物中含H、C、N、O、S五种非金属元素,同周期元素从左到右,
元素的电负性逐渐变大,同族元素从上到下,元素的电负性逐渐变小,则氢元素的电
负性最小,A正确;
B.由图可知,1mol该配合物中通过螯合作用成环形成的配位键(N→Zn)有4mol,B正
确;
C.由于电负性:O>N,因此氧锌键的成键电子对偏向于O,受热时容易断裂,同时由
于螯合作用形成的配位键氮锌键稳定性大于一般的配位键氧锌键,所以该配合物受热
时首先断裂的配位键是氧锌键,C错误;
D.该配合物中,每个N原子中的5个价层电子,2个用于形成共价键,2个用于形成
配位键,还有1个电子参与形成大π键。每个S原子中的6个价层电子,2个用于形成
共价键,2个填充在sp2杂化轨道中,还有2个电子参与形成大π键。因此在含硫五元
环中,共用6个电子,形成 大π键,在六元环中,共用6个电子,形成 大π键,
D正确;
故选C。
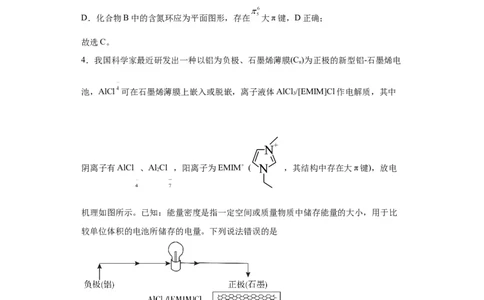
3.获得2022年度诺贝尔化学奖的科学家Sharpless教授提出点击化学,他认为分子合
成应该是模块化的,借助标准“接口”统一组装,形象地将其比喻为安全带卡扣和插
槽特异性地“click”在一起。以下是两个点击化学的标准“接口”化学反应,下列分析
不正确的是
A. 属于脂环烃 B.反应1和2均为加成反应
C. 的一氯代物有3种 D.化合物B中的含氮环中存在大π键
资料收集整理【淘宝店铺:向阳百分百】【答案】C
【详解】A. 为不含苯环的环状碳氢化合物,属于脂环烃,A正确;
B.反应1和2均含有π键断裂,并新生成σ键,均为加成反应,B正确;
C. 共有四种氢,如图 ,故一氯代物有四种,C错误;
D.化合物B中的含氮环应为平面图形,存在 大π键,D正确;
故选C。
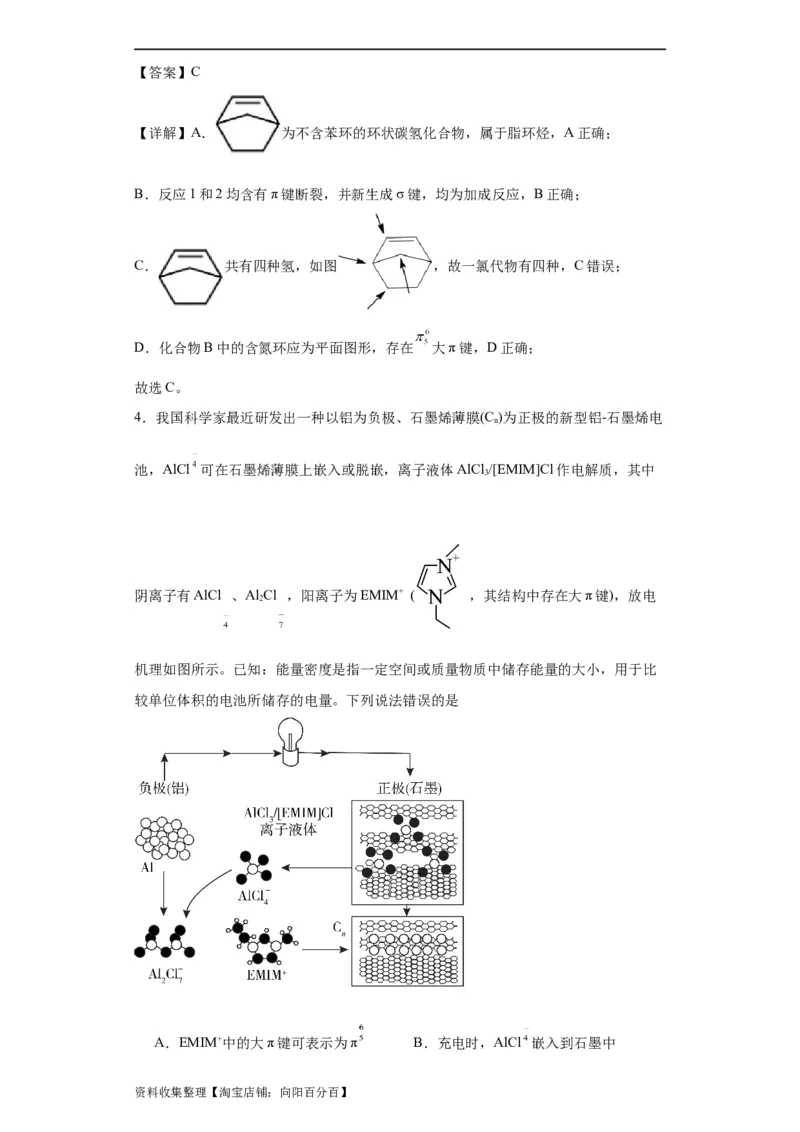
4.我国科学家最近研发出一种以铝为负极、石墨烯薄膜(C )为正极的新型铝-石墨烯电
n
池,AlCl 可在石墨烯薄膜上嵌入或脱嵌,离子液体AlCl /[EMIM]Cl作电解质,其中
3
阴离子有AlCl 、Al Cl ,阳离子为EMIM+ ( ,其结构中存在大π键),放电
2
机理如图所示。已知:能量密度是指一定空间或质量物质中储存能量的大小,用于比
较单位体积的电池所储存的电量。下列说法错误的是
A.EMIM+中的大π键可表示为π B.充电时,AlCl 嵌入到石墨中
资料收集整理【淘宝店铺:向阳百分百】C.EMIM+中I(C)小于I(N) D.该铝电极电池比锂电极的能量密度低
3 3
【答案】B
【分析】由题干知,放电时,铝为负极反应为Al+7 -3e-=4 ,石墨为正极反
应为 +3e-=3 +3C 。
n
【详解】A.EMIM+由含5个原子,与甲基相连的氮提供一个电子,与乙基相连的氮提
供2个电子,每个碳提供1个带脑子,故形成5原子6电子大Π键,可表示为 ,A
项错误;
B.从电极反应看,充电时 嵌入石墨电极,B项正确;
C.C失去第二个电子后为1s22s2,s为全满p为全空稳定难失电子,而N失去两个电
子后1s22s22p1失去一个电子后p为全空稳定,即I(C)大于I(N),C项错误;
3 3
D.27gAl产生3mol电子而7g的Li产生1mol的电子,锂的能量密度高,D项错误;
故选B。
5.胍( )是一元强碱,所有原子均在同一平面内,其盐酸盐(
)是核酸检测液的主要成分。下列说法错误的是
A.胍中N原子杂化方式不同 B.胍分子中存在大π键
C.胍中含有的化学键均为极性键 D.胍暴露在空气中易变质
【答案】B
【详解】A.胍中以单键成键的N原子为sp3杂化,以双键成键的N原子为sp2杂化,A
正确;
B.胍分子中-NH 中氮均为sp3杂化,为四面体形,不能和中心碳原子的p轨道肩并肩
2
重叠形成大π键,B错误;
C.胍中含有氮氢键、碳氮键、碳氮双键,其化学键均为极性键,C正确;
D.胍中碳氮不饱和键,故暴露在空气中易变质,D正确;
故选B。
6.临床证明磷酸氯喹对治疗“新冠肺炎”有良好的疗效,磷酸氯喹的结构如图所示。
下列有关磷酸氯喹的说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.磷酸氯喹中C、N、O元素的第一电离能:O>N>C
B.磷酸氯喹中的N-H键的键能大于C-H键的键能
C.磷酸氯喹结构中存在σ键、大π键等
D.磷酸氯喹中N的杂化方式sp2、sp3
【答案】A
【详解】A.N具有半充满电子结构,较稳定,第一电离能大于O,则第一电离能N>
O>C,A项错误;
B.原子半径越小,形成共价键的键能越大,则磷酸氯喹中的N-H键的键能大于C-
H键的键能,B项正确;
C.磷酸氯喹结构中存在单键和苯环,则存在σ键、大π键,C项正确;
D.-N=结构中N为sp2杂化,饱和N原子为sp3杂化,磷酸氯喹中存在这两种N,D项
正确。
答案选A。
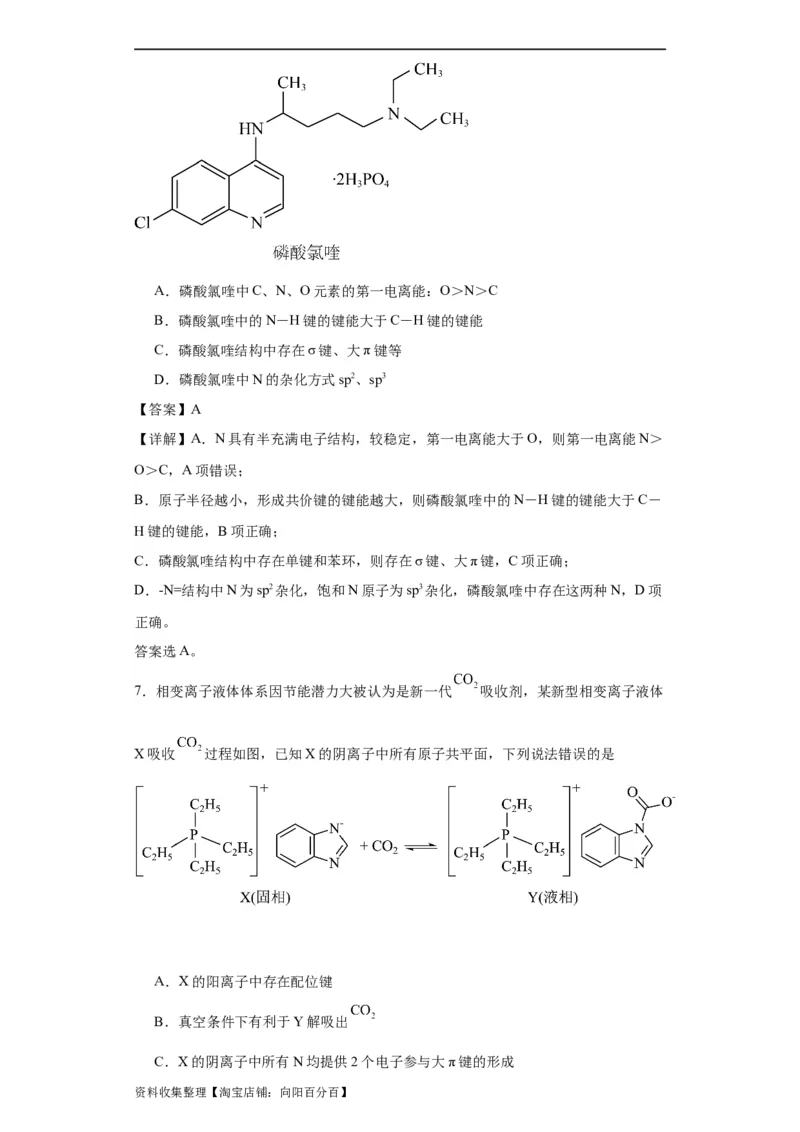
7.相变离子液体体系因节能潜力大被认为是新一代 吸收剂,某新型相变离子液体
X吸收 过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是
A.X的阳离子中存在配位键
B.真空条件下有利于Y解吸出
C.X的阴离子中所有N均提供2个电子参与大π键的形成
资料收集整理【淘宝店铺:向阳百分百】D.Y的熔点比X的低,可推知阴离子半径:Y>X
【答案】C
【详解】A.由共价键的饱和性可知,X的阳离子中磷原子形成了配位键,故A正确;
B.由方程式可知,与在空气中相比,真空条件下相当于减少二氧化碳的浓度,平衡向
逆反应方向移动,有利于Y解吸出二氧化碳,故B正确;
C.由X的阴离子中所有原子共平面可知,单键氮原子X的阴离子中有4个电子参与
大π键的形成,故C错误;
D.Y的熔点比X的低说明X中离子键强于Y,则Y的阴离子半径大于X,故D正确;
故选C。
8.南京理工大学合成某离子化合物由两种阳离子和两种阴离子构成,其中有两种10
电子离子和一种18电子离子。该离子化合物局部结构如图所示,X、Y、Z、M均为短
周期元素,且均不在同一族。下列说法错误的是
A.Y的气态氢化物的稳定性比Z的强
B.Z的气态氢化物沸点高于同族元素氢化物沸点
C.Z的最高价氧化物对应水化物的酸性比M的弱
D.五元环为一价阴离子,其中的大π键可表示为
【答案】B
【分析】该物质由两种阳离子和两种阴离子构成,其中有两种10电子离子和一种18
电子离子,且X、Y、Z、M均为短周期元素,且均不在同一族,,M的离子半径最大,
应该为18电子的离子,即M为Cl-,10电子离子应该为HO+和 ,据原子半径的关
3
系可推知X为H、Y为O、Z为N、M为Cl,含有的离子为NH 、HO+、N 、Cl−;
3
【详解】A.非金属性:O>N,则气态氢化物的稳定性:Y>Z,故A正确;
B.NH 的沸点知识比PH 、AsH 高,比SbH 、BiH 低,B错误;
3 3 3 3 3
C.非金属性N碳化硅>晶体硅
【答案】C
【详解】A.阳离子 中,五元环为平面结构,单键N原子提供
2个电子、其它原子各提供1个电子形成 大 键,故A正确;
B. 的结构式为 ,其中各原子最外层均达到8电子
结构,故B正确;
C. 中氨分子与铜离子形成配位键,N原子无孤电子对,所以
资料收集整理【淘宝店铺:向阳百分百】键的键角比 中 键的键角大,故C错误;
D.金刚石、碳化硅、晶体硅都是共价晶体,原子半径:C碳化硅>晶体硅,故D正确;
选C。
12.离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1-乙基-3-甲基咪
唑四氟硼酸盐离子液体结构如图所示,其环状结构中存在大π键。下列相关叙述错误
的是
A.阳离子中至少10原子共平面 B.阴离子呈正四面体形
C.该离子液体存在共价键、配位键、离子键 D.阳离子中 键数目是π键数目的
10倍
【答案】D
【详解】A.阳离子中五元环上C原子连接的化学键有1个双键,采用的是sp2杂化,
甲基和乙基上碳原子形成四个单键,采用的是sp3杂化,N原子接的有1个双键,采用
的是sp2杂化,另一个N原子接的都是单键判断是sp3,则五元环上2个N原子、3个
碳原子包括3个碳原子分别连接的H原子共8个原子共平面,另外甲基和乙基直接与
N原子连接的碳原子也与五元环共平面,即至少10原子共平面,故A正确;
B.阴离子为BF ,其中心原子价层电子对数为4+ ×(3+1-4×1)=4,采取sp3杂化,无
孤对电子,空间构型为正四面体形,故B正确;
C.该化合物为离子液体,是离子化合物,一定含有离子键;BF 中存在配位键,其中
B提供空轨道,F提供孤对电子,阳离子中存在共价键,故C正确;
D.根据单键是σ键,双键中1个σ键、1个π键,判断阳离子中含19个σ键、2个π
键,σ键数目是π键数目的9.5倍,故D错误;
答案选D。
13.离子液体是一类应用价值很高的绿色溶剂和催化剂,其中的EMIM+结构如图所示
(五元环为平面结构,与苯分子相似)。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.分子中碳碳键的键长相等 B.分子中∠HCN均为
C.所有C原子与N原子的杂化方式相同D.EMIM+结构中存在 大π键
【答案】D
【详解】A.分子中存在饱和的碳碳键和不饱和的碳碳键,两者键长不相等,故A错
误;
B.甲基、亚甲基C的杂化方式为sp3,但不存在正四体结构,则分子中不存在∠HCH
为109°28′,故B错误;
C.由于甲基、亚甲基C为sp3杂化,环上所有原子为sp2杂化,所以并非所有C原子
与N原子的杂化方式相同,故C错误;
D.五元环为平面结构,其中N和C均为sp2杂化,而中心五元环还要失去一个电子形
成阳离子,所以在z方向上5个原子的p 轨道耦合形成离域大π键,为
z
,即EMIM+结构中存在 大π键;故D正确;
故答案选D。
14.复印机周围的特殊腥味是 造成的。下列关于 的说法错误的是
A.分子内存在大 键 B.与 互为等电子体
C.与 互为同分异构体 D.在水中的溶解度大于
【答案】C
【详解】A. 分子内中心O原子分别与O形成 键,同时三个O原子之间形成 ,
故A正确;
B. 与 所含原子数均为3,价电子数均为18,互为等电子体,故B正确;
资料收集整理【淘宝店铺:向阳百分百】C. 与 均为O元素形成的单质,互为同素异形体,故C错误;
D. 为V形极性分子, 为非极性分子,根据相似相溶原理可知 在水中的溶解
度大于 ,故D正确;
故选:C。
15.近日科学家合成了一种新型芳香化合物 ,其结构中含有
(平面正六边形,与苯的结构类似)、 (平面正五边形)以及 。下列说法不正确的是
A.氮的原子结构示意图: B. 的电子式:
C. 和 中N原子杂化方式为 D. 和 中含有大 键
【答案】C
【详解】A.N是7号元素,N原子结构示意图: ,故A正确;
B. 的电子式: ,故B正确;
C. 时平面正六边形,与苯的结构类似, 是平面正五边形,而N原子杂化方式
为 ,应该是三角锥结构,则 和 中N原子杂化方式不是 ,故C错误;
D. 和 都是平面的环状结构,类似苯环,则 和 中含有大 键,故D正确;
故选C。
二、填空题
16. C H 表示环戊二烯负离子,已知分子中的大π键可用符号π 表示,其中m代表
5
参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表
示为π ),则C H 中的大π键应表示为 。
5
【答案】
资料收集整理【淘宝店铺:向阳百分百】【详解】
C H 形成大π键的原子是5个碳原子,每个碳原子P轨道上各拿一个电子加上负离子
5
得到的一个电子共六个电子形成大π键,因此是 。
17.分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表
参与形成大键的电子数(如苯分子中的大π键可表示为 )。一种观点认为,苯酚羟基
中的O原子是sp2杂化则苯酚中的大π键可表示为 ,
【答案】
【详解】
若苯酚羟基中的氧原子的杂化方式为sp2杂化,未参与杂化的2个p电子与苯环上6个
碳原子中未参与杂化的6个p电子形成 大π键,故答案为:
18.分子中的大 键可用符号 表示,其中m代表参与形成大键的原子数,n代表参
与形成大 键的电子数(如苯分子中的大 键可表示为 ),则 中的大 键应表示为
。
【答案】
【详解】 中中心原子S为sp2杂化,存在1对孤电子对,分子为V形,硫原子的1
对电子与每个氧原子中的1个未成对的p电子形成3中心4电子大 键,故应表示为
。
19. 在 催化作用下,呋喃 可与氨反应转化为吡咯 。二者均存在
资料收集整理【淘宝店铺:向阳百分百】与苯类似的大π键,表示方法为 ,n为成环原子个数,m为形成大π键电子个数,则
的大π键可以表示为 ,二者的熔、沸点关系为呋喃 吡
咯(填“高于”或“低于”)。
【答案】
【详解】
由题干中 的结构简式可知,分子内含有一个大π键,该大π键由4个碳原子
和一个O原子,每个碳原子给出1的电子参与形成大π键,每个O原子给出2个电子
参与形成大π键,则该大Π键的表示形式为 ;
20.点击化学(clickchemistry)是一种能够让分子的构建模块快速、高效地结合在一起的
化学反应。科学工作者可以利用基础模块搭建出变化无穷的造型,就如同玩乐高玩具
一般。叠氮化物和炔烃合成抗真菌药物三唑是点击化学的重要应用,反应示例如图:
分子乙中存在5中心6电子的大π键,其中提供两个电子形成大π键(π )的原子是
(填对应原子的序号)。
【答案】
1
【详解】
1号氮原子形成3个共价键,还有2个p电子参与形成大 键,故为答案为1;
21.回答下列问题:
中医典籍中,记载了炉甘石(ZnCO)入药,可用于治疗皮肤炎症或表面创伤。ZnCO 中
3 3
资料收集整理【淘宝店铺:向阳百分百】阴离子中的大Π键可表示为 。
【答案】
Π
【详解】
ZnCO 中的阴离子为CO ,CO 中心原子价层电子对数为3+ =3,且没
3
有孤电子对,空间构型为平面三角形,CO 中的大Π键是中心碳原子提供一个空轨道,
3个氧原子各自提供一对电子形成的4中心6电子的大Π键,可表示为:Π 。
22. 能与吡咯( )的阴离子( )形成双吡咯铜。已知吡咯
分子中所有原子在同一平面,其中存在的大π键可用符号 表示,其中m代表参与形
成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),
则吡咯分子中的大π键应表示为 。
【答案】
【详解】
存在大π键,为平面分子,C、N原子均采取sp2杂化,未杂化的p轨
道垂直于分子平面,肩并肩重叠形成大π键,且C、N未杂化的p轨道上各有1个电子
和1对电子,则该大π键含有6个电子,故吡咯分子中的大π键应表示为 ;
23.大 键可用符号表示 ,其中m代表参与形成大 键的原子数,n代表参与形成
大 键的电子数,如苯分子中的大 键可表示为 。已知 中存在大 键,该大
键可表示为 。
【答案】
资料收集整理【淘宝店铺:向阳百分百】【详解】
中键总数为4个,有6个电子可以形成大π键,可用符号表示 ;
24. 分子中 键长远比B和F的半径之和小,原因是分子中含有与苯类似的大
大 键。该分子中的大 键表示为 。
【答案】
【详解】
BF 分子中每个F提供一对孤电子对,与B原子形成大π键,即 。
3
25. 乙基 甲基咪唑四氟硼酸盐离子液体稳定性强,可溶于水,可广泛用于有
机反应,结构如图。
咪唑具有类似苯的平面结构(如图所示),其大 键应表示为
【答案】
【详解】
根据咪唑的平面结构,有5个原子和6个电子形成 键,表示为 ;
26.苯分子中6个C原子,每个C原子有一个2p轨道参与形成大 键,可记为( 右
下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为
,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大 键,可表示为
,
【答案】
资料收集整理【淘宝店铺:向阳百分百】【详解】
某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,由此推知,该分子中
存在大 键,由5个原子、6个电子构成,可表示为 。答案为:
27.苯分子中6个C原子,每个C原子有一个2p轨道参与形成大π键,可记为 (右
下角“6”表示6个原子,右上角“6”表示6个共用电子)。平面分子 中
的大π键应表示为
【答案】
【详解】
为平面分子,说明该分子中含大π键, 中每个C
原子提供1个电子,两个N原子,一个提供1个电子,一个提供1对电子,形成的为5
中心6电子的大π键,故表示为: ;故 中的大π键应表示为 ;
资料收集整理【淘宝店铺:向阳百分百】