文档内容
专题验收评价
专题 02 化学常用计量
内容概览
A·常考题不丢分
【考点一 物质的组成、分类及转化】
【考点二 化学与STSE】
【考点三 化学与传统文化】
【微专题 化学用语】
B·综合素养拿高分/拓展培优拿高分
C·挑战真题争满分
【考点一 一定物质的量浓度溶液的配制】
1.(2023·上海徐汇·统考模拟预测)实验室用98%的浓硫酸配制 的稀硫酸。下列说法错
误的是
A.应选用200mL容量瓶 B.可选用量筒量取浓硫酸
C.在烧杯中稀释浓硫酸 D.定容时应选用胶头滴管
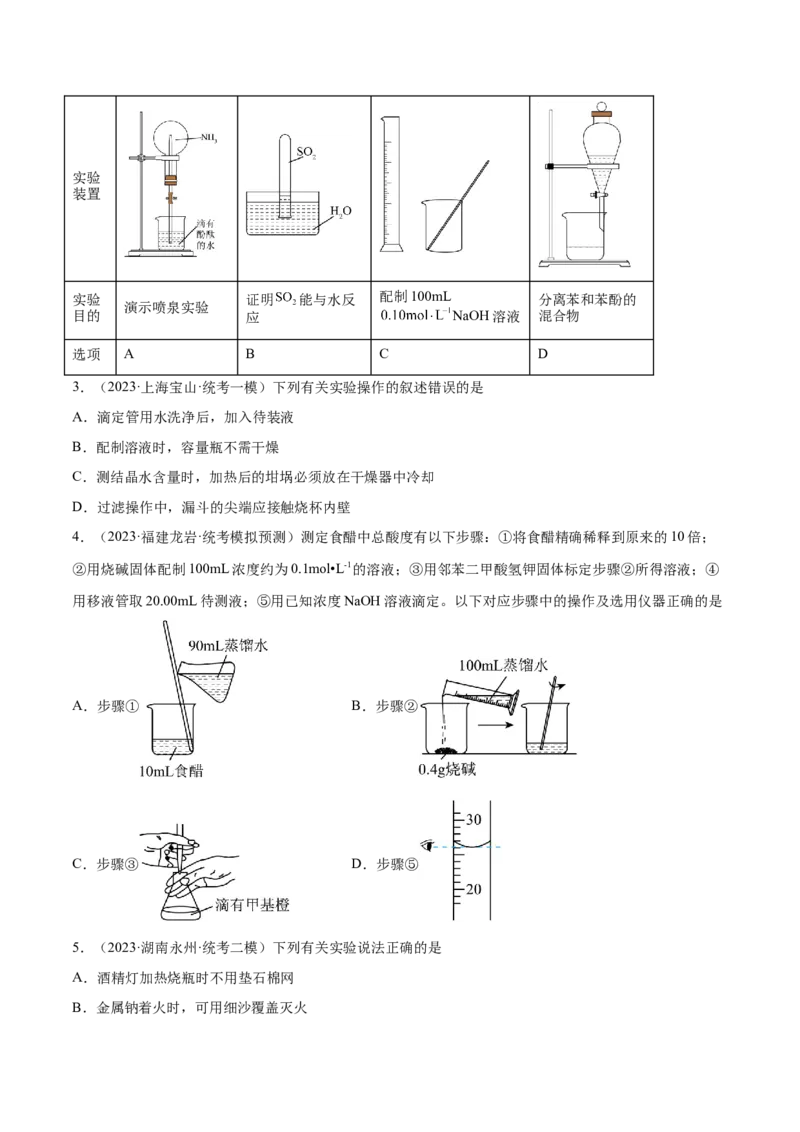
2.(2023·河北石家庄·校联考一模)下列实验装置能达到相应实验目的的是实验
装置
实验 证明 能与水反 配制100mL 分离苯和苯酚的
演示喷泉实验
目的 应 NaOH溶液 混合物
选项 A B C D
3.(2023·上海宝山·统考一模)下列有关实验操作的叙述错误的是
A.滴定管用水洗净后,加入待装液
B.配制溶液时,容量瓶不需干燥
C.测结晶水含量时,加热后的坩埚必须放在干燥器中冷却
D.过滤操作中,漏斗的尖端应接触烧杯内壁
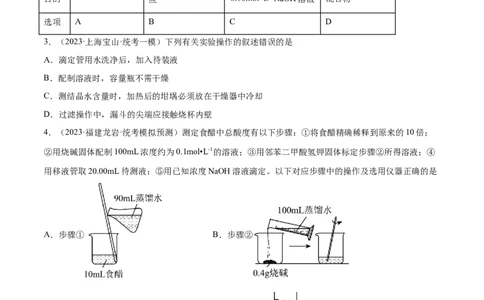
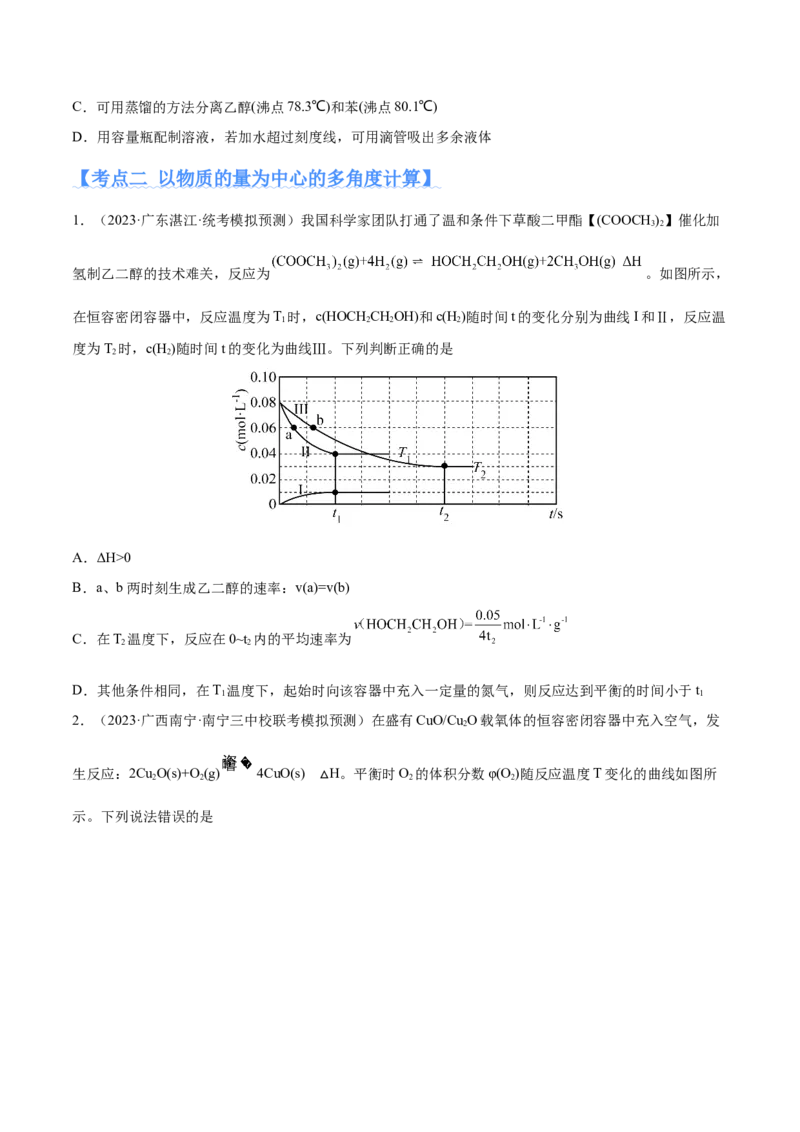
4.(2023·福建龙岩·统考模拟预测)测定食醋中总酸度有以下步骤:①将食醋精确稀释到原来的10倍;
②用烧碱固体配制100mL浓度约为0.1mol•L-1的溶液;③用邻苯二甲酸氢钾固体标定步骤②所得溶液;④
用移液管取20.00mL待测液;⑤用已知浓度NaOH溶液滴定。以下对应步骤中的操作及选用仪器正确的是
A.步骤① B.步骤②
C.步骤③ D.步骤⑤
5.(2023·湖南永州·统考二模)下列有关实验说法正确的是
A.酒精灯加热烧瓶时不用垫石棉网
B.金属钠着火时,可用细沙覆盖灭火C.可用蒸馏的方法分离乙醇(沸点78.3℃)和苯(沸点80.1℃)
D.用容量瓶配制溶液,若加水超过刻度线,可用滴管吸出多余液体
【考点二 以物质的量为中心的多角度计算】
1.(2023·广东湛江·统考模拟预测)我国科学家团队打通了温和条件下草酸二甲酯【(COOCH )】催化加
3 2
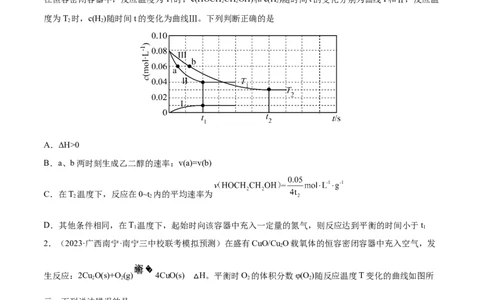
氢制乙二醇的技术难关,反应为 。如图所示,
在恒容密闭容器中,反应温度为T 时,c(HOCH CHOH)和c(H)随时间t的变化分别为曲线I和Ⅱ,反应温
1 2 2 2
度为T 时,c(H)随时间t的变化为曲线Ⅲ。下列判断正确的是
2 2
A.ΔH>0
B.a、b两时刻生成乙二醇的速率:v(a)=v(b)
C.在T 温度下,反应在0~t 内的平均速率为
2 2
D.其他条件相同,在T 温度下,起始时向该容器中充入一定量的氮气,则反应达到平衡的时间小于t
1 1
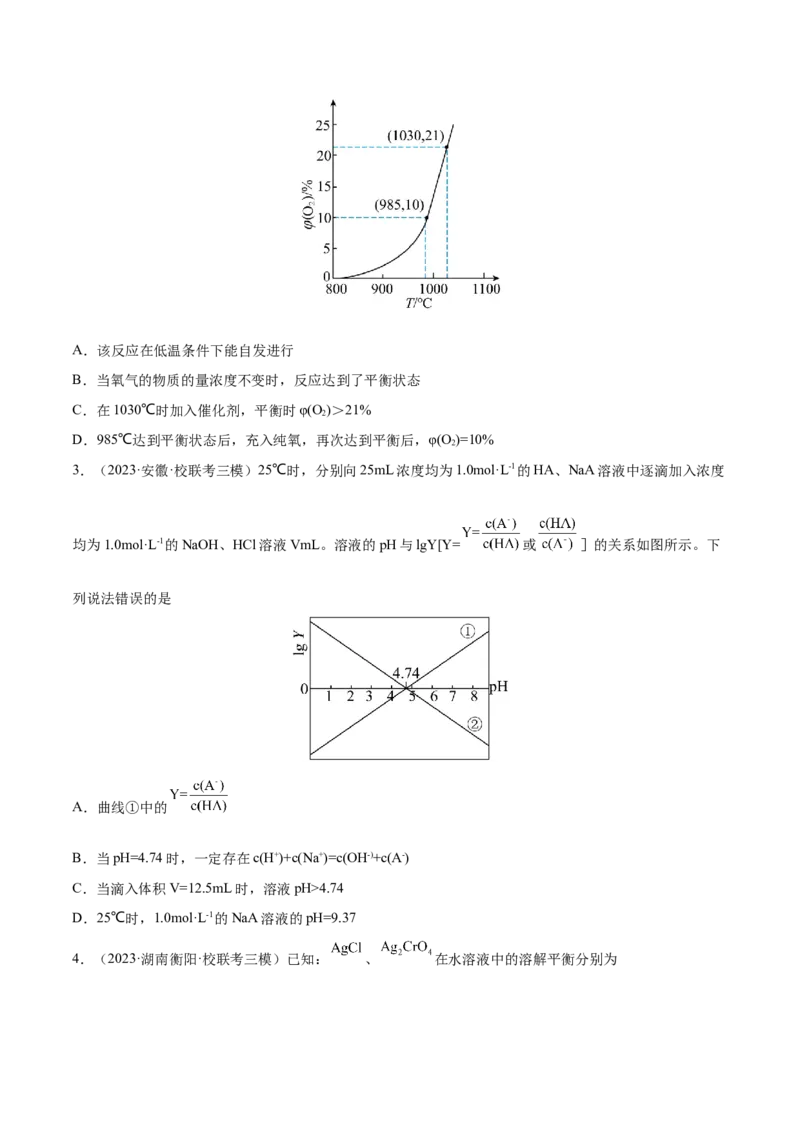
2.(2023·广西南宁·南宁三中校联考模拟预测)在盛有CuO/Cu O载氧体的恒容密闭容器中充入空气,发
2
生反应:2Cu O(s)+O (g) 4CuO(s) H。平衡时O 的体积分数φ(O)随反应温度T变化的曲线如图所
2 2 2 2
△
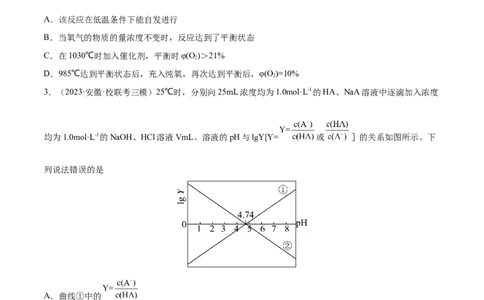
示。下列说法错误的是A.该反应在低温条件下能自发进行
B.当氧气的物质的量浓度不变时,反应达到了平衡状态
C.在1030℃时加入催化剂,平衡时φ(O)>21%
2
D.985℃达到平衡状态后,充入纯氧,再次达到平衡后,φ(O)=10%
2
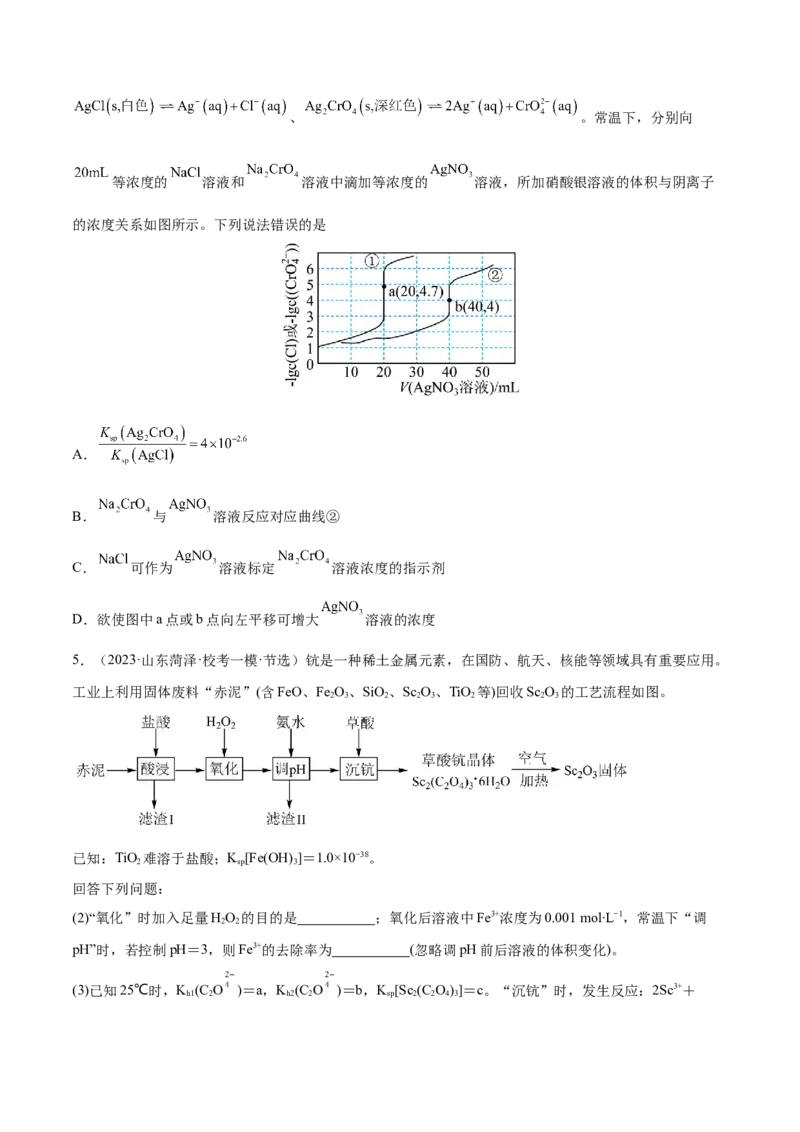
3.(2023·安徽·校联考三模)25℃时,分别向25mL浓度均为1.0mol·L-1的HA、NaA溶液中逐滴加入浓度
均为1.0mol·L-1的NaOH、HCl溶液VmL。溶液的pH与lgY[Y= 或 ]的关系如图所示。下
列说法错误的是
A.曲线①中的
B.当pH=4.74时,一定存在c(H+)+c(Na+)=c(OH-)+c(A-)
C.当滴入体积V=12.5mL时,溶液pH>4.74
D.25℃时,1.0mol·L-1的NaA溶液的pH=9.37
4.(2023·湖南衡阳·校联考三模)已知: 、 在水溶液中的溶解平衡分别为、 。常温下,分别向
等浓度的 溶液和 溶液中滴加等浓度的 溶液,所加硝酸银溶液的体积与阴离子
的浓度关系如图所示。下列说法错误的是
A.
B. 与 溶液反应对应曲线②
C. 可作为 溶液标定 溶液浓度的指示剂
D.欲使图中a点或b点向左平移可增大 溶液的浓度
5.(2023·山东菏泽·校考一模·节选)钪是一种稀土金属元素,在国防、航天、核能等领域具有重要应用。
工业上利用固体废料“赤泥”(含FeO、Fe O、SiO、Sc O、TiO 等)回收Sc O 的工艺流程如图。
2 3 2 2 3 2 2 3
已知:TiO 难溶于盐酸;K [Fe(OH) ]=1.0×10−38。
2 sp 3
回答下列问题:
(2)“氧化”时加入足量HO 的目的是 ;氧化后溶液中Fe3+浓度为0.001 mol∙L−1,常温下“调
2 2
pH”时,若控制pH=3,则Fe3+的去除率为 (忽略调pH前后溶液的体积变化)。
(3)已知25℃时,K (C O )=a,K (C O )=b,K [Sc (C O)]=c。“沉钪”时,发生反应:2Sc3++
h1 2 h2 2 sp 2 2 4 33HC O Sc (C O)↓+6H+,该反应的平衡常数K= (用含a、b、c的代数式表示)。
2 2 4 2 2 4 3
【微专题 阿伏加德罗常数的六大陷阱】
1.(2023·辽宁阜新·阜新实验中学校考模拟预测)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.常温常压下,40gSiC中所含C-Si数目为2N
A
B.标准状况下,11.2LCHCl 中含有0.5N 个C原子
3 A
C.常温常压下,20gNO 和26gNO 的混合气体中氧原子总数为2N
2 2 4 A
D.25℃时,1.0LpH=13的Ba(OH) 溶液中含有OH-的数目为0.2N
2 A
2.(2023·陕西西安·陕西师大附中校考模拟预测)N 为阿伏加德罗常数的值,下列有关说法错误的是
A
A.1molN 和3molH 充分反应后原子总数为8N
2 2 A
B.1L1mol/LNa CO 溶液中,阴离子总数大于N
2 3 A
C.14g分子式为C H 的烃中含有的C-C键数为
n 2n
D.浓硝酸受热分解生成NO 、NO 共23g,转移电子数为0.5N
2 2 4 A
3.(2023·广西南宁·南宁三中校考二模)N 为阿伏加德罗常数的值。下列说法不正确的是
A
A.0℃,101kPa下,11.2L氢气中质子的数目为N
A
B.1molK Cr O 被还原为Cr3+转移电子数目为6N
2 2 7 A
C.常温下,pH=5的NH Cl溶液中,由水电离出的H+数目为10-5N
4 A
D.0.2mol苯乙烯完全燃烧,生成CO 的数目为1.6N
2 A
4.(2023·河北邢台·邢台市第二中学校联考三模)设 为阿伏加德罗常数的值。下列说法正确的是
A.100g3.4% 溶液中含氧原子数为
B.10.4g苯乙烯( )分子中含碳碳双键数为
C.向1L 氨水中滴入 溶液至中性时溶液中 数为
D.2.24L(标准状况) 与足量NaOH溶液反应转移的电子数为
5.(2023·广东深圳·红岭中学校考模拟预测)设 为阿伏伽德罗常数的值,下列说法正确的是
A. 熔融状态下的 中含有 的数目为B.标准状况下, 中含有 原子的数目为
C. 溶液中, 的数目为
D.常温常压下, 中含有共价键的数目为
1.(2023·重庆沙坪坝·重庆南开中学校考模拟预测)金粉溶于过氧化氢-浓盐酸可以安全环保的制备氯金
酸( ),其化学方程式为: 。设 为阿伏加德罗常
数的值,下列说法正确的是
A.消耗1molAu,反应转移的电子数为
B.消耗2molHCl生成的 分子数为
C.消耗85g ,产物中形成的配位键数目为
D.2mol液态水中含有的氢键数目为
2.(2023·湖北·校联考模拟预测)甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反应制
得。N 为阿伏加德罗常数的值。下列有关说法正确的是
A
A.pH=3的甲酸溶液中氢离子数目为1×10-3N
A
B.0.5 mol甲酸甲酯中含有sp3杂化的原子数目为N
A
C.50g质量分数为64%的甲醇水溶液中含有σ键数目为5N
A
D.甲醇燃料电池中,每消耗22.4L(标准状况)甲醇,转移电子数目为6N
A
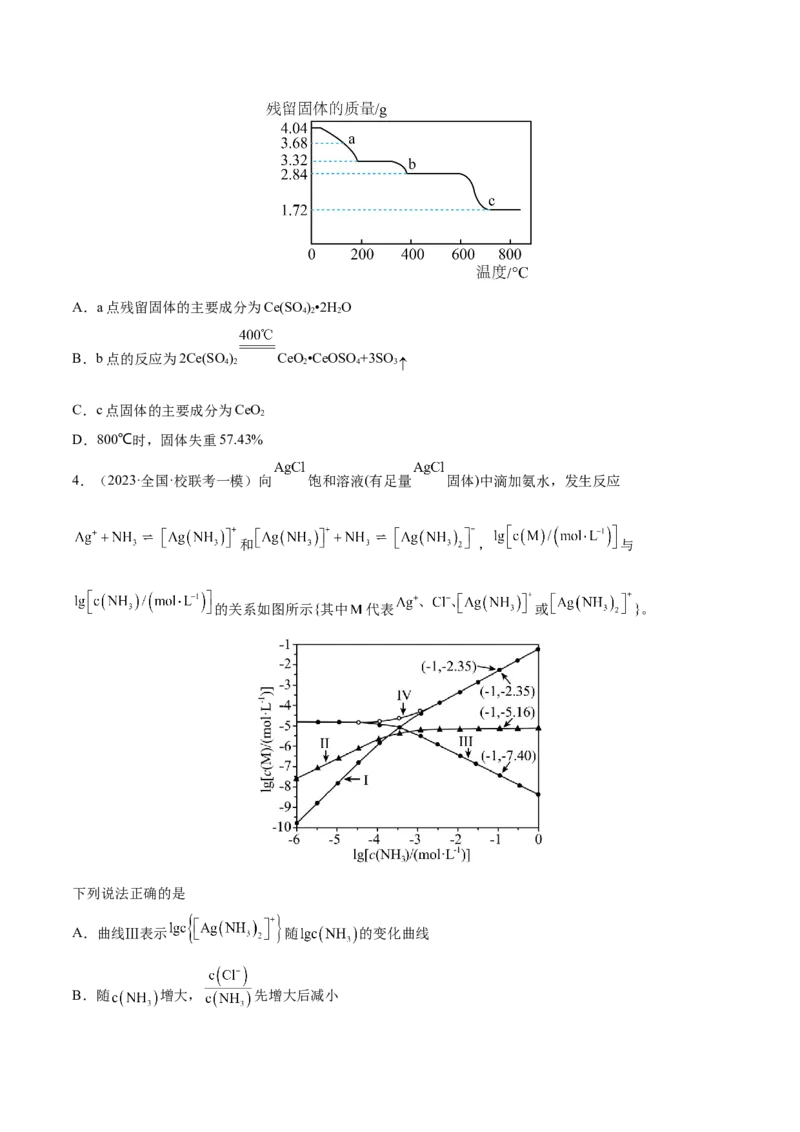
3.(2023·广东广州·统考三模)为研究Ce(SO)•4H O (相对分子质量:404)的热分解性质,进行如下实验:
4 2 2
准确称取4.04g样品,在空气中进行加热,残留固体的质量随温度的变化如图所示。下列说法不正确的是A.a点残留固体的主要成分为Ce(SO)•2H O
4 2 2
B.b点的反应为2Ce(SO) CeO•CeOSO+3SO
4 2 2 4 3
C.c点固体的主要成分为CeO
2
D.800℃时,固体失重57.43%
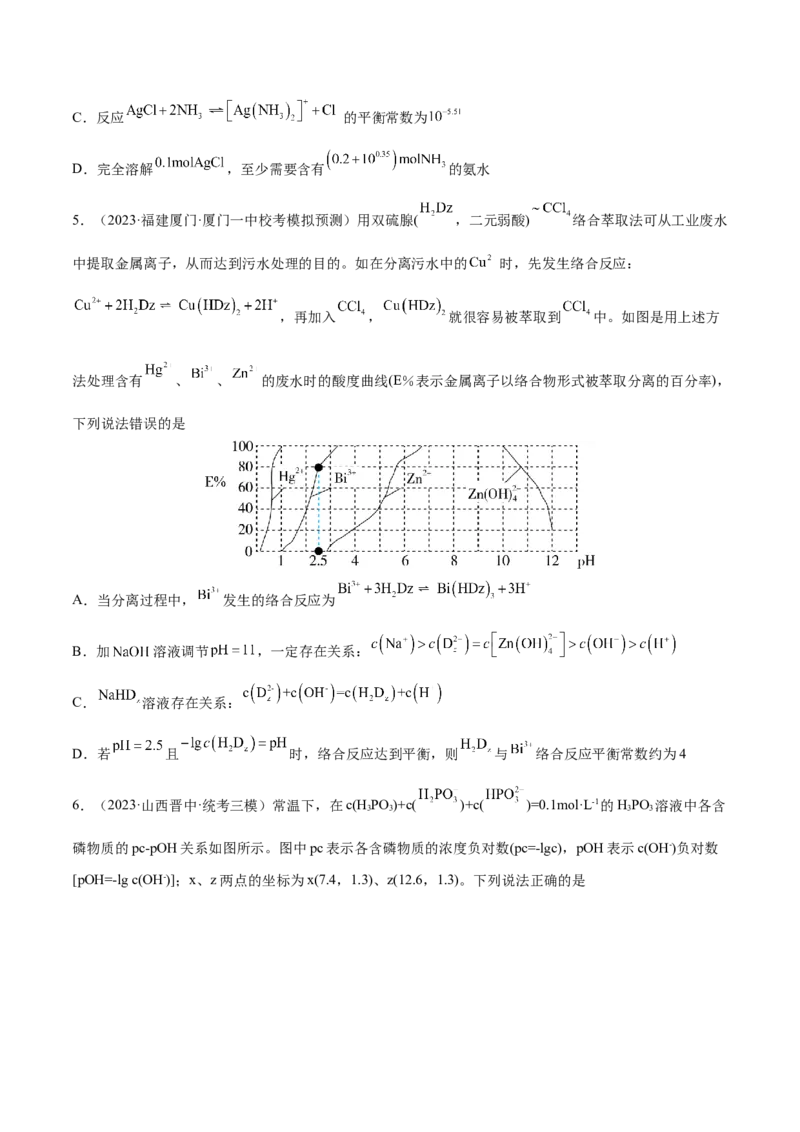
4.(2023·全国·校联考一模)向 饱和溶液(有足量 固体)中滴加氨水,发生反应
和 , 与
的关系如图所示{其中 代表 或 }。
下列说法正确的是
A.曲线Ⅲ表示 随 的变化曲线
B.随 增大, 先增大后减小C.反应 的平衡常数为
D.完全溶解 ,至少需要含有 的氨水
5.(2023·福建厦门·厦门一中校考模拟预测)用双硫腺( ,二元弱酸) 络合萃取法可从工业废水
中提取金属离子,从而达到污水处理的目的。如在分离污水中的 时,先发生络合反应:
,再加入 , 就很容易被萃取到 中。如图是用上述方
法处理含有 、 、 的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率),
下列说法错误的是
A.当分离过程中, 发生的络合反应为
B.加 溶液调节 ,一定存在关系:
C. 溶液存在关系:
D.若 且 时,络合反应达到平衡,则 与 络合反应平衡常数约为4
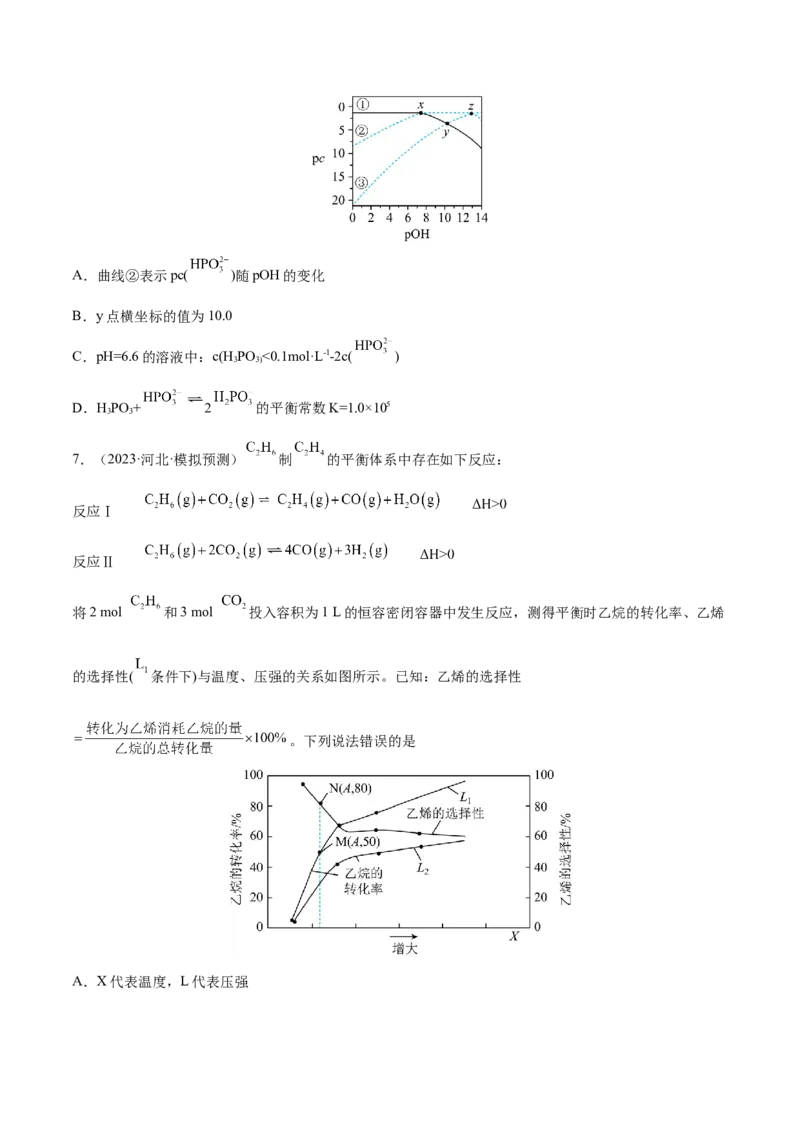
6.(2023·山西晋中·统考三模)常温下,在c(HPO )+c( )+c( )=0.1mol·L-1的HPO 溶液中各含
3 3 3 3
磷物质的pc-pOH关系如图所示。图中pc表示各含磷物质的浓度负对数(pc=-lgc),pOH表示c(OH-)负对数
[pOH=-lg c(OH-)];x、z两点的坐标为x(7.4,1.3)、z(12.6,1.3)。下列说法正确的是A.曲线②表示pc( )随pOH的变化
B.y点横坐标的值为10.0
C.pH=6.6的溶液中:c(HPO <0.1mol·L-1-2c( )
3 3)
D.HPO + 2 的平衡常数K=1.0×105
3 3
7.(2023·河北·模拟预测) 制 的平衡体系中存在如下反应:
反应Ⅰ
反应Ⅱ
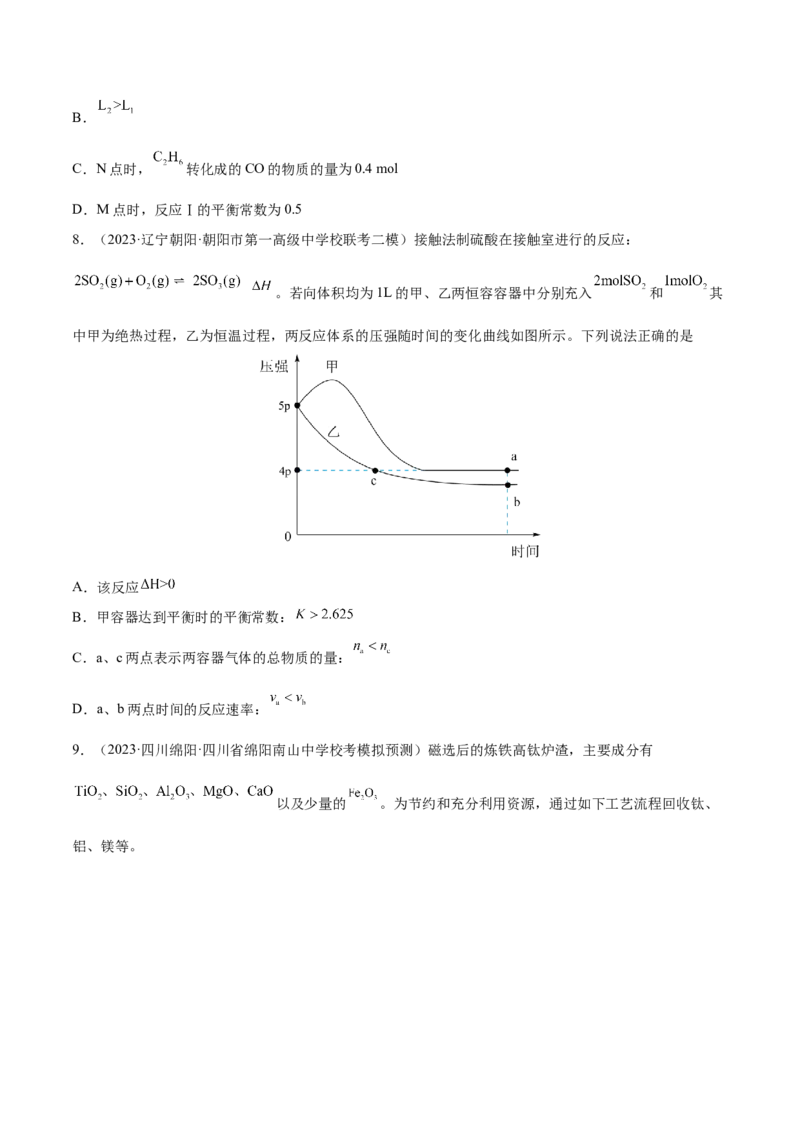
将2 mol 和3 mol 投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯
的选择性( 条件下)与温度、压强的关系如图所示。已知:乙烯的选择性
。下列说法错误的是
A.X代表温度,L代表压强B.
C.N点时, 转化成的CO的物质的量为0.4 mol
D.M点时,反应Ⅰ的平衡常数为0.5
8.(2023·辽宁朝阳·朝阳市第一高级中学校联考二模)接触法制硫酸在接触室进行的反应:
。若向体积均为1L的甲、乙两恒容容器中分别充入 和 其
中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
A.该反应
B.甲容器达到平衡时的平衡常数:
C.a、c两点表示两容器气体的总物质的量:
D.a、b两点时间的反应速率:
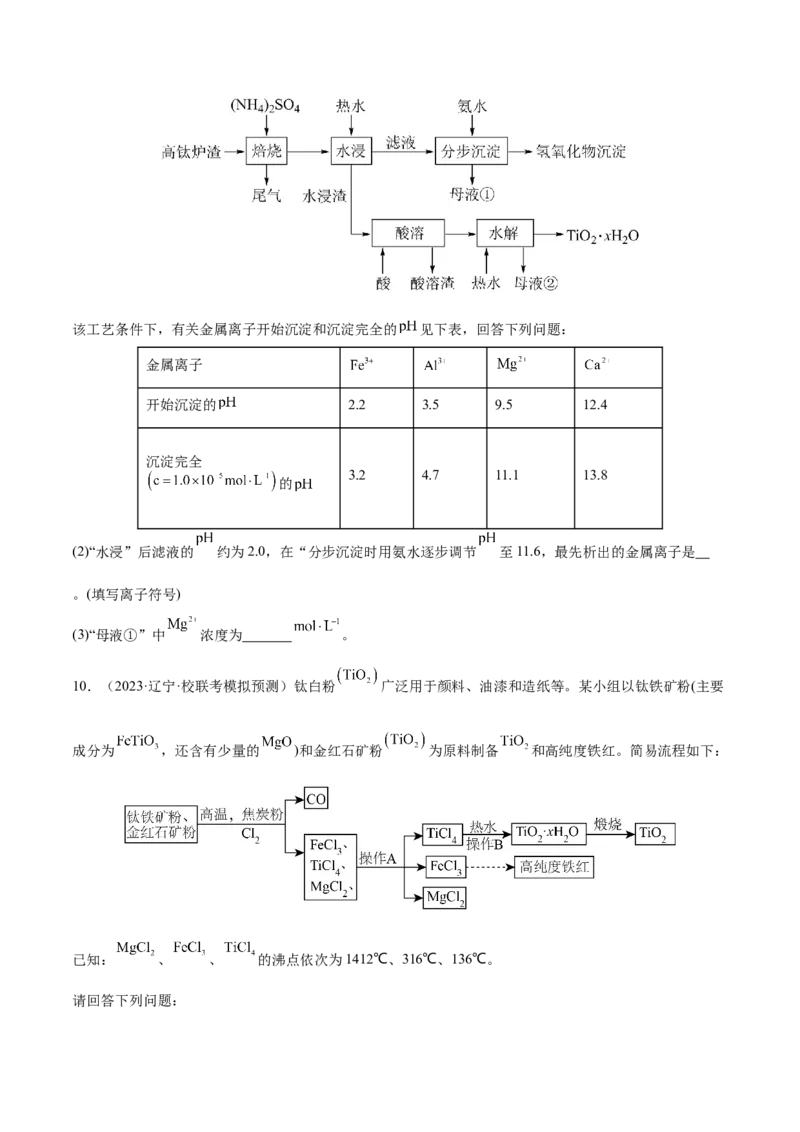
9.(2023·四川绵阳·四川省绵阳南山中学校考模拟预测)磁选后的炼铁高钛炉渣,主要成分有
以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、
铝、镁等。该工艺条件下,有关金属离子开始沉淀和沉淀完全的 见下表,回答下列问题:
金属离子
开始沉淀的 2.2 3.5 9.5 12.4
沉淀完全
3.2 4.7 11.1 13.8
的
(2)“水浸”后滤液的 约为2.0,在“分步沉淀时用氨水逐步调节 至11.6,最先析出的金属离子是
。(填写离子符号)
(3)“母液①”中 浓度为 。
10.(2023·辽宁·校联考模拟预测)钛白粉 广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉(主要
成分为 ,还含有少量的 )和金红石矿粉 为原料制备 和高纯度铁红。简易流程如下:
已知: 、 、 的沸点依次为1412℃、316℃、136℃。
请回答下列问题:(6)测定样品中 纯度。取2.000g样品,在酸性条件下充分溶解,加入适量铝粉将 还原为 。过
滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液。取25.00mL所配溶液于锥形瓶中,滴加几滴
KSCN溶液,用 标准溶液滴定,将 转化成 ,重复操作3次,平均消耗
标准溶液。
①计算该样品中 的质量分数: 。
②若其他操作都正确,盛装 标准溶液的滴定管没有润洗,则测得结果将 (填“偏高”、
“偏低”或“无影响”)。
1.(2021·海南·统考高考真题) 代表阿伏加德罗常数的值。下列说法正确的是
A. 中含有的电子数为1.3
B. 中含有的共价键的数目为0.1
C. 肼 含有的孤电子对数为0.2
D. ,生成 乙烷时断裂的共价键总数为
2.(2021·浙江·高考真题)设 为阿伏加德罗常数的值,下列说法不正确的是
A.标准状况下, 中含有中子数为
B. (分子结构: )中的共价键数目为
C. 的 水溶液中含有氧原子数为D. 三肽 (相对分子质量:189)中的肽键数目为
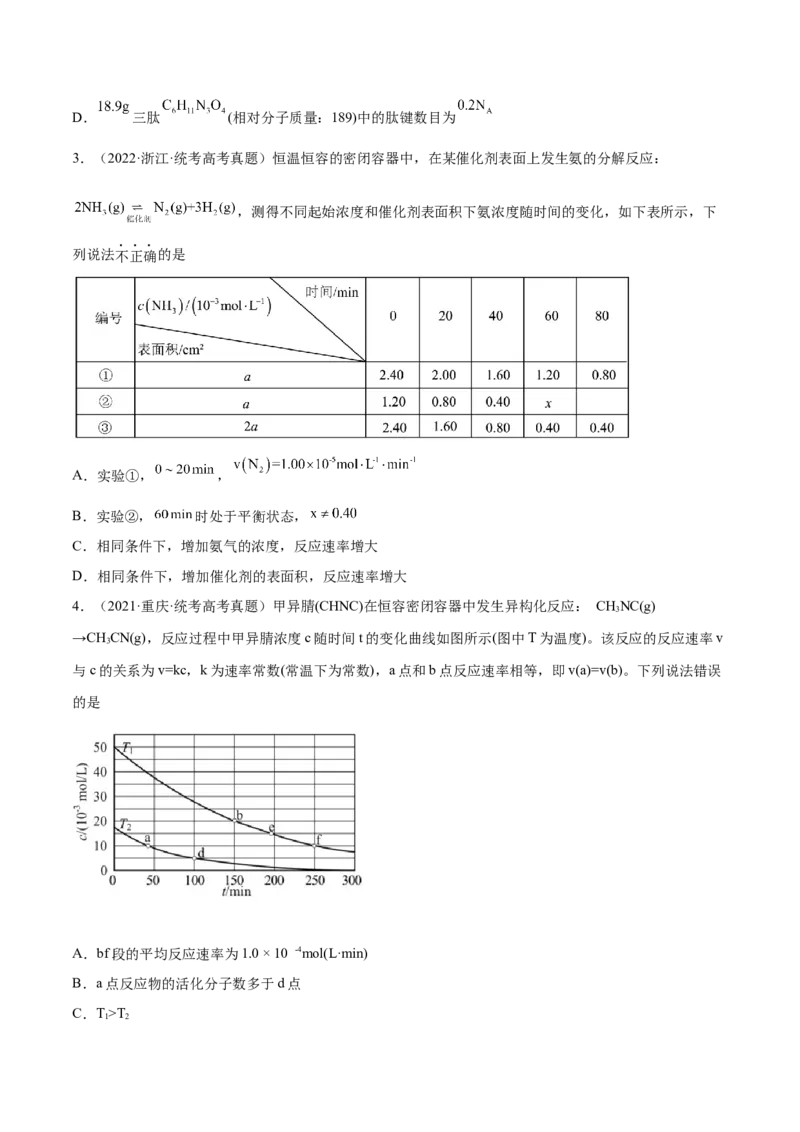
3.(2022·浙江·统考高考真题)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
4.(2021·重庆·统考高考真题)甲异腈(CHNC)在恒容密闭容器中发生异构化反应: CHNC(g)
3
→CHCN(g),反应过程中甲异腈浓度c随时间t的变化曲线如图所示(图中T为温度)。该反应的反应速率v
3
与c的关系为v=kc,k为速率常数(常温下为常数),a点和b点反应速率相等,即v(a)=v(b)。下列说法错误
的是
A.bf段的平均反应速率为1.0 × 10 -4mol(L·min)
B.a点反应物的活化分子数多于d点
C.T>T
1 2D.3v(d)=2v(e)
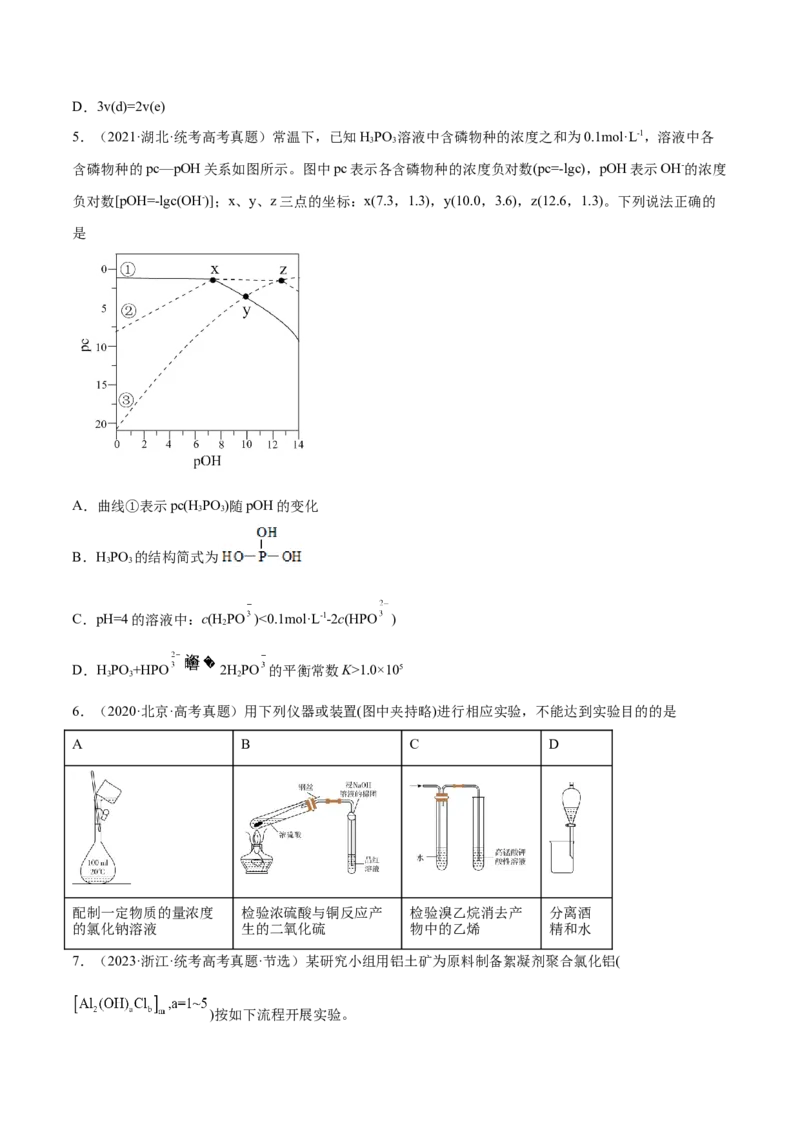
5.(2021·湖北·统考高考真题)常温下,已知HPO 溶液中含磷物种的浓度之和为0.1mol·L-1,溶液中各
3 3
含磷物种的pc—pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(pc=-lgc),pOH表示OH-的浓度
负对数[pOH=-lgc(OH-)];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的
是
A.曲线①表示pc(HPO )随pOH的变化
3 3
B.HPO 的结构简式为
3 3
C.pH=4的溶液中:c(H PO )<0.1mol·L-1-2c(HPO )
2
D.HPO +HPO 2HPO 的平衡常数K>1.0×105
3 3 2
6.(2020·北京·高考真题)用下列仪器或装置(图中夹持略)进行相应实验,不能达到实验目的的是
A B C D
配制一定物质的量浓度 检验浓硫酸与铜反应产 检验溴乙烷消去产 分离酒
的氯化钠溶液 生的二氧化硫 物中的乙烯 精和水
7.(2023·浙江·统考高考真题·节选)某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝(
)按如下流程开展实验。已知:①铝土矿主要成分为 ,含少量 和 。用 溶液溶解铝土矿过程中 转变为难
溶性的铝硅酸盐。
② 的絮凝效果可用盐基度衡量,盐基度
当盐基度为0.60~0.85时,絮凝效果较好。
请回答:
(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取 溶液于锥形瓶中,调 ,滴加指示
剂 溶液。在不断摇动下,用 标准溶液滴定至浅红色(有 沉淀),30秒
内不褪色。平行测试3次,平均消耗 标准溶液 。另测得上述样品溶液中
。
①产品的盐基度为 。
②测定 过程中溶液 过低或过高均会影响测定结果,原因是 。
8.(2021·河北·统考高考真题·节选)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设
计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原
料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:(7)工序④溶液中的铝元素恰好完全转化为沉淀的pH为 。(通常认为溶液中离子浓度小于10-5mol•L-1为沉
淀完全;A1(OH) +OH- Al(OH) :K=100.63,K =10-14,K [A1(OH) ]=10-33)
3 w sp 3
⇌