文档内容
专题02 阿伏加德罗常数及其化学计算
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.100g46%的乙醇水溶液中含有的氢原子数为6N
A
B.将22.4L(标准状况)Cl 通入足量水中,转移的电子数为N
2 A
C.12gNaHSO 固体中含阳离子数目为0.1N
4 A
D.64gSO 和32gO 混合,反应一段时间后总原子数为4N
2 2 A
2.设 为阿伏加德罗常数的值,下列说法正确的是
A.16.9g过氧化钡( )固体中阴、阳离子总数为0.2
B. 溶液中,氢原子数目为2
C.标准状况下,22.4L氯气与56g铁充分反应,转移的电子数为3
D.密闭容器中 和 充分反应后,容器中分子数为2
3. 是阿伏加德罗常数的值。下列说法正确的是
A. 固体中含阴、阳离子的总数为
B. 时, 的醋酸溶液中含有的 数目为
C. 和足量 反应,生成的 分子数目为
D. 与等物质的量的硫粉完全反应时转移的电子数为
4.N 是阿伏加德罗常数的值。下列说法错误的是
A
A.标准状况下,4.48LCl 溶于水所得氯水中含氯微粒总数为0.4N
2 A
B.常温常压下,56g乙烯和丙烯的混合物所含共用电子对数目为12N
AC.16gCH 和33.6L(标准状况)Cl 在光照条件下充分反应后的分子数为2.5N
4 2 A
D.1L0.05mol•L-1的NH Cl溶液中通入适量氨气后呈中性,此时溶液中NH 数目为0.05N
4 A
5.阿伏加德罗常数的值为N ,下列说法正确的是
A
A.物质的量浓度为0.5mol/L的 溶液中,含有 的数目为N
A
B.100gCaS与 的混合物中含有32g硫,则含有的氧原子数目为1.75N
A
C.将100ml 1mol/L 溶液水解制成胶体,所得胶体粒子数目为0.1N
A
D. 与 溶液混合产生22.4L气体时,转移电子数目为2N
A
6.N 表示阿伏加德罗常数,下列说法正确的是
A
A. 中含有的中子数为6N
A
B.标准状况下, 与 的混合气中电子数为N
A
C. 溶液中阴离子数少于0.1N
A
D. 和 充分反应后,分子总数为0.2N
A
7.设N 为阿伏加德罗常数的值,下列说法错误的是
A
A. 的NaCl溶液中含有 的个数为0.5N
A
B. 晶体中含有的离子数为0.2N
A
C. 中配位键个数为4N
A
D. 与 的混合气体中H原子个数为0.4N
A
8.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.0.1molH 与0.1mol 在密闭容器中充分反应后,其分子总数小于0.2N
2 A
B.足量的铁粉与1mol 充分反应,转移的电子数目为3N
A
C.0.1mol/L 溶液中含 数目一定小于0.3N
AD.标准状况下,2.24L 与足量的 反应,转移电子数为0.1N
A
9.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.12g金刚石中含有的C-C键数目为4N
A
B.标准状况下,11.2LNO与11.2LO 混合后的分子数目为0.75N
2 A
C.23gNa与78gNaO 分别与足量水反应生成的气体体积相同
2 2
D.100g质量分数为46%的乙醇溶液中含有氢原子数为12N
A
10.设 为阿伏加德罗常数的值,下列说法正确的是
A. 和 混合物中所含的阴离子总数为
B. 溶液中 离子数为
C.常温常压下,124g P 中所含 键的数目为
4
D.向密闭容器中充入 与 充分反应后容器内的分子数小于
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.N 是阿伏加德罗常数的值。下列说法正确的是
A
A.22.4L(标准状况)氮气中含有7N 个中子
A
B.1mol重水比1mol水多N 个质子
A
C.30g甲醛和30g乙酸分子中含有共用电子对数目均为4N
A
D.1molCl 溶于足量水中,转移电子的数目为N
2 A
12.将磷灰石混以石英砂在1773K左右用炭还原制备白磷,反应原理如下:
,下列说法正确的是
A.石墨晶体中碳原子个数与碳碳键数之比为4∶3
B. 晶体中Si—O键的数目为
C.标准状况下,1个CO分子的体积为D.31g白磷中含有的孤电子对数为
13.下列说法错误的是
A.将14%的KOH溶液蒸发掉100g水后,变为28%的KOH溶液80mL,该80mL溶液的物质的量浓度为
6.25mol/L
B.将质量分数为98%的 与水等体积混合,混合后 的质量分数大于49%
C.某 溶液的密度为1.2 , 的质量分数为5%,1L该溶液中 的物质的量为5mol
D.1mol氧气在放电条件下,有30%转化为 ,则放电后混合气体对氢气的相对密度是35.6
14. 为阿伏加德罗常数的值,下列说法正确的是
A. 石墨中含有 键的数目为1.5
B.标准状况下 , 中含有 键的数目为0.4
C.常温常压下, 气体中含有的分子数小于
D. 发生吸氧腐蚀,最终生成 ,电极之间转移的电子数为0.2
15.设 为阿伏加德罗常数的值。下列有关叙述正确的是。
A.标准状况下, 与 中所含的分子数均为
B.由 与 组成的混合物中阴离子总数为
C.10g 49%的硫酸溶液与10g 49%的 溶液中所含的氧原子数相同
D.0.1mol Fe分别与足量的盐酸和氧气反应,转移的电子数均为
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(8分) 取30.8g甲酸铜[(HCOO) Cu]在隔绝空气的条件下加热分解,会生成含两种红色固体(Cu和
2)的混合物A和混合气体B;若相同质量的甲酸铜在空气中充分加热,则生成黑色固体D和 、
,固体A和D质量相差2.4g。请计算:
(1)红色固体A中Cu单质的物质的量为_______mol,同时写出简要的计算过程。
(2)将混合气体B置于 中充分燃烧,消耗 的体积是_______L(换算为标准状况)。
17.(12分)(1)某同学进行CO 与NaO 反应的探究实验,将100 mL纯净的CO 通过一定量的NaO
2 2 2 2 2 2
粉末,反应后气体体积为65 mL,则反应消耗CO 的体积是__________mL。
2
(2)已知铜和浓硫酸可以在加热条件下发生反应:Cu + H SO (浓) →CuSO + SO ↑ +H O(方程式未
2 4 4 2 2
配平),如果一定量的铜片与100mL 18mol/L的浓HSO 充分反应,在反应过程中转移了0.2mol电子,将反应
2 4
后所得到的溶液(不考虑SO 的溶解)经一定稀释后与足量Ba(OH) 溶液充分反应。计算反应后所得沉淀的
2 2
质量为__________g(保留到0.1g)。
(3)现有 NaOH 和 Ba(OH) 混合溶液 100mL,已知该溶液中 c(OH-)=1mol/L,向溶液中缓缓通
2
入CO 气体(溶液体积变化忽略不计)),当至少通入CO 气体体积为 0.56L(标准状况)时生成的沉淀最
2 2
多,那么当通入CO 气体体积为1.792 L(标况)时,溶液中HCO 的物质的量浓度是______mol/L。
2
18.(15分)请回答下列问题:
(1)标准状况下,V L氯化氢(HCl)溶解在1 L水中(水的密度近似为1 g/mL)所得溶液的密度为ρ g/mL,则所
得盐酸物质的量浓度为_______。
(2)将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1,该溶液中溶质质量分数为
_______。
(3)在200 mL氯化镁和氯化铝的混合溶液中,c(Mg2+)为0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转
化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为_______。
(4)某铁的氧化物(Fe O)1.52 g溶于足量盐酸中,向所得溶液中通入112 mL Cl (标准状况下),恰好将Fe2+完
x 2
全氧化。x值为_______。
(5)向一定量的FeO、Fe、Fe O 的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出
3 4
224 mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质
量的此混合物,能得到铁的质量是_______。
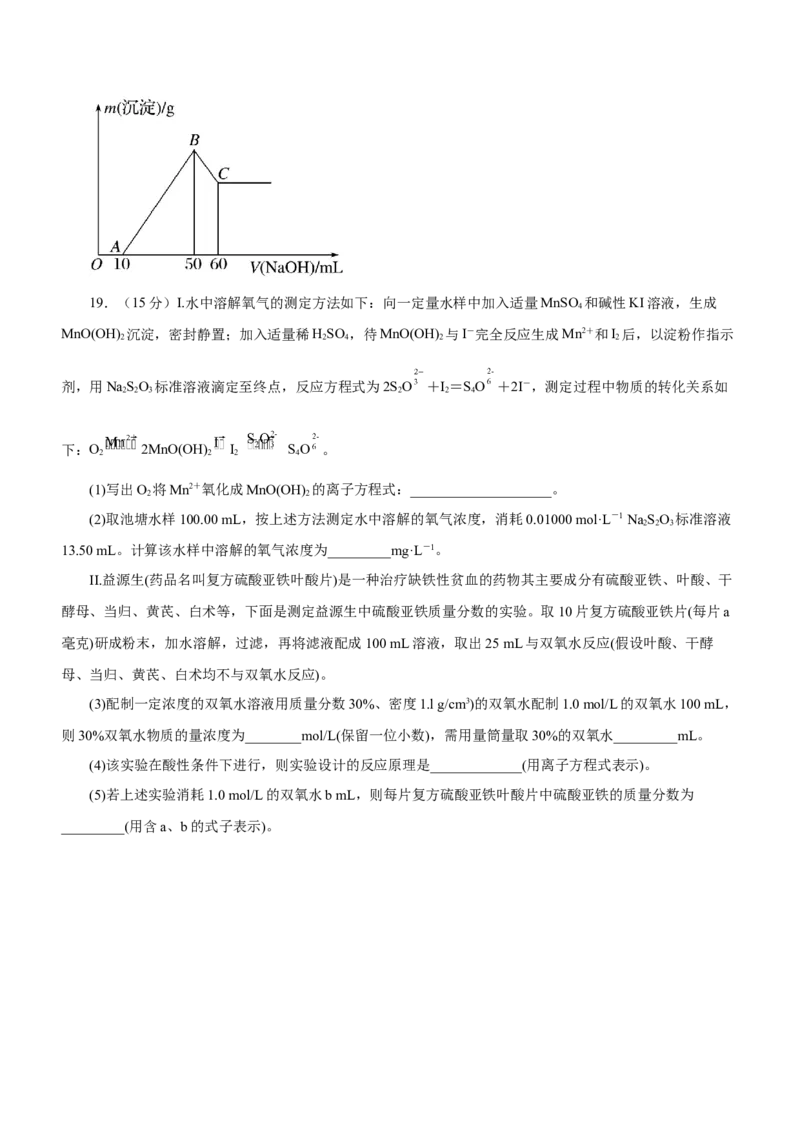
(6)某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1 mol·L-1 NaOH溶液,消耗NaOH溶液体积
和生成沉淀之间的关系如下图所示。则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为_______。19.(15分)I.水中溶解氧气的测定方法如下:向一定量水样中加入适量MnSO 和碱性KI溶液,生成
4
MnO(OH) 沉淀,密封静置;加入适量稀HSO ,待MnO(OH) 与I-完全反应生成Mn2+和I 后,以淀粉作指示
2 2 4 2 2
剂,用NaSO 标准溶液滴定至终点,反应方程式为2SO +I=SO +2I-,测定过程中物质的转化关系如
2 2 3 2 2 4
下:O 2MnO(OH) I SO 。
2 2 2 4
(1)写出O 将Mn2+氧化成MnO(OH) 的离子方程式:____________________。
2 2
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 NaSO 标准溶液
2 2 3
13.50 mL。计算该水样中溶解的氧气浓度为_________mg·L-1。
II.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干
酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每片a
毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、干酵
母、当归、黄芪、白术均不与双氧水反应)。
(3)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,
则30%双氧水物质的量浓度为________mol/L(保留一位小数),需用量筒量取30%的双氧水_________mL。
(4)该实验在酸性条件下进行,则实验设计的反应原理是_____________(用离子方程式表示)。
(5)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为
_________(用含a、b的式子表示)。