文档内容
专题 04 氧化还原反应
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列过程属于化学反应,且与氧化还原反应无关的是( )
A.石灰纯碱法除水 B.补铁口服液中添加维生 D.生活中用“暖宝宝”
C.工业上原油的分馏
垢 素 取暖
【答案】A
【解析】A项,石灰―纯碱法是向已澄清的生水中加入适量的生石灰(CaO)和纯碱(Na CO),可除去水
2 3
中的永久硬度,软化水垢,生成碳酸钙和氢氧化镁沉淀,属于非氧化还原反应,A正确;B项,补铁口服
液中添加维生素,属于物理变化,B错误;C项,原油的分馏是利用沸点不同进行分离,属于物理变化,C
错误;D项,Fe粉、活性炭、食盐水构成原电池,发生氧化还原反应,D错误;故选A。
2.(2024·北京丰台高三期中)下列物质混合后,因发生氧化还原反应使溶液pH增大的是( )
A.向酸性KMnO 溶液中加入FeSO 溶液,紫色褪去
4 4
B.向NaHSO 溶液中加入Ba(OH) 溶液,产生白色沉淀
3 2
C.向BaCl 溶液中先通入SO ,后通入O,产生白色沉淀
2 2 2
D.向饱和NaCl溶液中先通入NH ,后通入CO,产生白色沉淀
3 2
【答案】A
【解析】A项,向酸性KMnO 溶液中加入FeSO 溶液,紫色褪去,说明发生氧化还原反应,离子方程
4 4
式:MnO -+5Fe2++8H+=Mn2++5Fe3++4H O,pH增大,故A正确;B项,向NaHSO 溶液中加入Ba(OH) 溶
4 2 3 2
液,产生白色沉淀,发生复分解反应,不属于氧化还原反应,故B错误;C项,向BaCl 溶液中先通入
2
SO ,后通入O,产生白色沉淀,反应过程中未消耗H+,pH不变,故C错误;D项,向饱和NaCl溶液中
2 2
先通入NH ,后通入CO,产生白色沉淀,无元素化合价变化,不属于氧化还原反应,故D错误;故选
3 2
A。
3.(2023·浙江省义乌市高三高考适应性考试)关于反应
2MnSO +5Na SO+8H O=2NaMnO +4Na SO +8H SO ,下列说法正确的是( )
4 2 2 8 2 4 2 4 2 4
A.NaSO 中S元素化合价为+7价 B.MnSO 是氧化剂
2 2 8 4
C.生成1molNaMnO 时转移5mol电子 D.MnO -的氧化性弱于Mn2+
4 4【答案】C
【解析】A项,NaSO 中存在一个过氧键,即有2个氧显-1价,其余的氧显-2价,根据化合物的化合
2 2 8
价为0,可得硫元素为+ 6价,A错误;B项,在该反应中锰元素由+2价升高为+7价,则硫酸锰为还原
剂,B错误;C项,在该反应中锰元素由+2价升高为+7价,则生成1molNaMnO 时转移5mol电子,C正
4
确;D项,在该反应中高锰酸根是氧化产物,其中锰元素的化合价为+7价,锰离子是还原剂,其中锰元素
的化合价为+2价,一般同种元素中元素的化合价越高氧化性越强(氯的含氧酸除外),D错误;故选C。
4.(2024·安徽六安高三联考)19世纪科学家提出HO 与Cl 作用的反应过程如下:下列说法正确的是(
2 2 2
)
反应I:Cl+H O=HCl+HOOCl
2 2 2
反应II:HOOCl=HCl+O
2
A.氧化性: O>Cl
2 2
B.反应I中HO 作还原剂
2 2
C.反应I中每消耗0.1mol Cl ,转移0.2N e-
2 A
D.每产生32gO,则消耗Cl 为1
2 2
【答案】D
【解析】A项,由反应Ⅰ知,氧化性Cl>HOOCl,由反应Ⅱ知,氧化性HOOCl>O ,故氧化性Cl>
2 2 2
O,A错误;B项,反应Ⅰ中,氯气的化合价从0价既升高到+1价,又降低到-1价,即是氧化剂又是还原
2
剂,HO 的化合价没有变化,不是还原剂,B错误;C项,反应Ⅰ中,氯气的化合价从0价既升高到+1
2 2
价,又降低到-1价,每消耗0.1 mol Cl ,转移0.1N e-,C错误;D项,反应I消耗 1mol氯气和反应II生
2 A
成1mol氧气都是转移1mol电子,电子转移关系为:32g O ~e-~1mol Cl ,D正确; 故选D。
2 2
5.(2024·宁夏石嘴山高三期中)工业上用S (分子结构: )与CH 为原料制备
8 4
CS,发生反应:S+2CH =2CS +4H S,N 为阿伏加德罗常数的值,下列说法不正确的是( )
2 8 4 2 2 A
A.S 既是氧化剂,又是还原剂
8
B.生成17gHS,转移电子2 mol
2
C.消耗1 molS,断裂的S-S键数目为8N
8 A
D.CS 既是氧化产物,又是还原产物
2
【答案】A
【解析】A项,反应中C元素化合价由CH 中-4价升至CS 中+4价,CH 做还原剂,S元素化合价由0
4 2 4
价降至-2价,S 做氧化剂,A错误;B项,每生成4molH S,反应转移16mol电子,17gHS是0.5mol,转
8 2 2
移电子2mol, B正确;C项,1 molS 中含有8molS-S键,消耗1 molS,断裂8molS-S键,C正确; D
8 8
项,反应中C元素化合价由CH 中-4价升至CS 中+4价,S元素化合价由0价降至-2价,CS 既是氧化产
4 2 2
物又是还原产物,D正确;故选A。6.(2024·河南太康县联考)下面两个反应都可以生成氯气,有关说法正确的是( )
①
②
A.两个反应中盐酸均部分被氧化
B.物质氧化性由强到弱的顺序为KClO>MnO >Cl
3 2 2
C.反应②中,氧化剂与还原剂的质量之比为1∶6
D.反应①的电子转移情况分析如图:
【答案】A
【解析】A项,在两个反应的产物中都存在-1价氯离子,也存在由盐酸中-1价氯生成的氯气,故两个
反应中盐酸均部分被氧化,A正确;B项,根据氧化剂的氧化性大于氧化产物的氧化性的原理,只能得出
KClO、MnO 的氧化性均强于Cl,但两者氧化性强弱无法比较,B错误;C项,反应②中,只有5个氯化
3 2 2
氢分子被氧化,故氧化剂与还原剂的质量之比为1∶5,C错误;D项,根据得失电子守恒可知,反应①的
电子转移情况分析如图 ,D错误;故选A。
7.关于反应:10NaN +2KNO =K O+5Na O+16N↑,下列说法正确的是( )
3 3 2 2 2
A.反应物KNO 中N被氧化
3
B.NaN 中氮元素为-3价
3
C.标准状况下,若有6.5g NaN 参加反应,则生成3.584L N
3 2
D.若1mol KNO 参加反应,转移电子的物质的量为10mol
3
【答案】C
【解析】A项,该反应中KNO 中N元素由+5价变为0价,被还原,A错误;B项,NaN 中Na为+1
3 3
价,N元素平均化合价为- 价,B错误;C项,6.5g NaN 的物质的量为 =0.1mol,根据方程式可
3
知生成0.16mol氮气,标况下体积为0.16mol×22.4L/mol=3.584L,C正确;D项,KNO 为该反应中唯一得
3
电子的物质,根据其N元素的化合价变化可知,若1mol KNO 参加反应,转移电子的物质的量为5mol,D
3
错误;故选C。
8.单质硫有多种存在形式,如S、S、S、S 等,其中S 通常采用下列两种方式获得:
2 4 6 8 8
①24NaHSO S+8Na SO +8NaHSO +8H O;
3 8 2 4 3 2
②HS+H SO (浓)=S ↓+SO↑+2H O。下列说法正确的是( )
2 8 2 4 8 2 2A.S、S、S、S 互为同位素
2 4 6 8
B.反应①中每生成1 mol S ,有16 mol电子发生转移
8
C.反应②S 为还原产物
8
D.还原性:HS>SO
2 8 2
【答案】D
【解析】A项,S、S、S、S 都是由硫元素形成的单质,互为同素异形体,故A错误;B项,反应①
2 4 6 8
中NaHSO 中的硫元素部分化合价由+4价升高到+6价,部分化合价由+4价降低到0价,每生成1 mol S ,
3 8
转移电子为1mol 4 8=32mol,故B错误;C项,反应②中HS 中硫元素化合价升高,是还原剂,则S 为
2 8 8
氧化产物,故C错误;D项,反应②中HS 是还原剂,SO 是还原产物,还原剂的还原性强于还原产物的
2 8 2
还原性,说明还原性:HS>SO ,故D正确;故选D。
2 8 2
9.神舟十二号飞船的控制计算机、数据管理计算机完全使用国产CPU芯片,制作芯片刻蚀液为硝酸
与氢氟酸的混合溶液,其工艺涉及的反应为:Si+HNO +6HF=HSiF+HNO +H +H O,下列说法正确的是(
3 2 6 2 2 2
)
A.HSiF 中Si元素的化合价为+6价
2 6
B.该反应中,HNO 仅作氧化剂
3
C.该反应中,生成标准状况下2.24LH 时,转移电子的物质的量为0.2mol
2
D.芯片刻蚀液可用硫酸代替
【答案】B
【解析】A项,HSiF 中,H为+1价,F为-1价,则Si元素的化合价为+4价,故A错误;
2 6
B项,N元素的化合价由+5价降低为+3价,所以该反应中,HNO 仅作氧化剂,故B正确;
3
C项,标准状况下2.24LH 物质的量为 ,每生成1mol H 时转移4mol电子,则实
2 2
际转移电子0.4mol,故C错误;D项,芯片的主要成分是硅,硅单质与硫酸不反应,所以芯片刻蚀液不可
用稀硫酸代替,故D错误;故选B。
10.向CuSO 溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后
4
的混合物中不断通入SO 气体,溶液逐渐变成无色。下列分析正确的是( )
2
A.上述实验条件下,物质的氧化性:Cu2+>I >SO
2 2
B.通入SO 时,SO 与I 反应,I 作还原剂
2 2 2 2
C.通入SO 后溶液逐渐变成无色,体现了SO 的漂白性
2 2
D.滴加KI溶液时,转移2 mol e-时生成1 mol白色沉淀
【答案】A
【解析】由题干信息可知,向 CuSO 溶液中加入 KI溶液时发生反应:2CuSO +4KI===2K SO +
4 4 2 4
2CuI↓+I ①,当转移2 mol e-时生成2 mol CuI沉淀,D错误;向反应后的混合物中再通入SO 气体,又发
2 2生反应:I +SO +2HO===H SO +2HI②,该反应中I 作氧化剂,SO 作还原剂,体现了SO 的还原性,
2 2 2 2 4 2 2 2
故B、C均不正确;根据氧化剂的氧化性强于氧化产物的氧化性可知,反应①中氧化性Cu2+>I ,反应②
2
中I 将SO 氧化,说明氧化性I>SO,故A正确。
2 2 2 2
11.铁氰酸钾为深红色晶体,俗称“赤血盐”,常用来检验 ,碱性条件下可发生反应:
4K[Fe(CN) ]+4KOH=4 K [Fe(CN) ]+O ↑+2H O,下列说法不正确的是( )
3 6 4 6 2 2
A.该反应中K[Fe(CN) ]表现氧化性,被还原
3 6
B.K[Fe(CN) ]溶液加入到含有 的溶液中,生成的蓝色沉淀中铁元素存在两种价态
3 6
C. 作还原剂,0.4 mol KOH被氧化时,转移 电子
D. 铁氰酸钾参与反应时,生成标准状况下O560mL
2
【答案】C
【解析】A项,4K[Fe(CN) ]+4KOH=4 K [Fe(CN) ]+O ↑+2H O,K[Fe(CN) ]铁的化合价从+3价变成产
3 6 4 6 2 2 3 6
物中+4价,铁化合价降低,作氧化剂,被还原,故A正确; B项,生成的蓝色沉淀Fe [Fe(CN) ] 中铁元
3 6 2
素存在+2、+3两种价态,故B正确;C项,KOH作还原剂,0.4 mol KOH被氧化时,转移0.8 mol电子,
故C错误;D项,0.1mol铁氰酸钾参与反应时,生成标准状况下O560mL,故D正确。
2
12.已知:① 5MnSO +2 NaClO+4H O=5MnO ↓+Na SO +4H SO +Cl↑;
4 3 2 2 2 4 2 4 2
②FeSO +MnO+H SO →Fe (SO )+ MnSO +H O(末配平)。
4 2 2 4 2 4 3 4 2
下列有关说法正确的是( )
A.MnSO 在反应①中作还原剂,在反应②中作氧化产物
4
B.还原性:FeSO >Cl>MnSO
4 2 4
C.根据上述反应判断:NaClO 不能氧化FeSO
3 4
D.转移电子数相同时,反应①中生成的HSO 与反应②中消耗的HSO 的物质的量之比为2:5
2 4 2 4
【答案】D
【解析】A项,MnSO 在反应①中是还原剂,在反应②中是还原产物,故A错误;B项,根据还原
4
性:还原剂>还原产物,判断还原性:FeSO >MnSO >Cl,故B错误;C项,根据上述反应判断出氧化
4 4 2
性:NaClO>MnO >Fe (SO ),所以NaClO 能把FeSO 氧化Fe (SO ),故C错误;D项,反应①中每转
3 2 2 4 3 3 4 2 4 3
移10 mol电子,生成4 mol H SO ,反应②可配平为2FeSO +MnO+2H SO =Fe (SO )+ MnSO +2H O,每转
2 4 4 2 2 4 2 4 3 4 2
移2 mol电子,消耗2 mol H SO ,所以转移电子数相同时,反应①中生成的HSO 与反应②中消耗的
2 4 2 4
HSO 的物质的量之比为2:5,故D正确;故选D。
2 4
13.钒元素在酸性溶液中有多种存在形式,其中VO2+为蓝色,VO2+为淡黄色,VO +具有较强的氧化
2
性,Fe2+、SO 2-等能把VO +还原为VO2+。向VOSO 溶液中滴加酸性KMnO 溶液,溶液颜色由蓝色变为淡
3 2 4 4
黄色。下列说法不正确的是( )
A.在酸性溶液中氧化性:MnO ->VO+
4 2
B.FeI 溶液与酸性(VO )SO 溶液发生反应:Fe2++VO+=Fe3++VO2+
2 2 2 4 2
C.向VOSO 溶液中滴加酸性KMnO 溶液反应化学方程式为:
4 410VOSO+2H O+2KMnO =5(VO)SO +2MnSO +2H SO +K SO
4 2 4 2 2 4 4 2 4 2 4
D.向含1molVO +的酸性溶液中滴加1.5molFeSO 的溶液完全反应,转移电子为1mol
2 4
【答案】B
【解析】A项,VOSO 溶液中滴加酸性KMnO 溶液,溶液颜色由蓝色变为淡黄色,说明高锰酸根将
4 4
VO2+氧化为VO +,氧化性:氧化剂大于氧化产物,MnO ->VO+,故A正确;B项,碘离子的还原性大于
2 4 2
二价铁离子,碘离子应参与氧化还原反应反应,故B错误;C项,酸性环境下高锰酸根将VO2+氧化为
VO +,无沉淀生成说明高锰酸根被还原成Mn2+,结合电子守恒和元素守恒可知方程式为:
2
10VOSO+2H O+2KMnO =5(VO)SO +2MnSO +2H SO +K SO ,故C正确;D项,向含1molVO +的酸性溶
4 2 4 2 2 4 4 2 4 2 4 2
液中滴加含1.5molFe2+的溶液发生反应Fe2++VO++2H+=Fe3++VO2++H O,则VO +的量不足,所以转移电子
2 2 2
为1mol,故D正确;故选B。
14.(2024·江苏镇江丹阳市高三期中联考)叠氮酸钠( )是重要的化工原料。以甲醇、亚硝酸钠等为
原料制备 流程如下:
已知水合肼(N H•H O)不稳定,具有强还原性。下列描述正确的是( )
2 4 2
A.NO -的空间结构为平面三角形
2
B.反应①和反应③中浓硫酸所起的作用完全相同
C.反应②中,消耗3mol NH•H O时,NH•H O失去 电子
2 4 2 2 4 2
D.反应④中氧化剂与还原剂的物质的量之比为3:2
【答案】C
【解析】以甲醇、亚硝酸钠等为原料制备NaN ,由流程可知,①中发生
3
2CHOH+2NaNO+H SO (浓)=2CH ONO+Na SO +2H O,生成亚硝酸甲酯(CHONO),④中NaClO氧化
3 2 2 4 3 2 4 2 3
NH •H O为NH•H O,而自身被还原为Cl-,②中发生NH•H O+CHONO+NaOH=NaN +CH OH+3H O,
3 2 2 4 2 2 4 2 3 3 3 2
③中发生2NaN +H SO (浓) 2HN ↑+Na SO ,蒸馏出CHOH,最后HN 与NaOH反应可制备产品。A项,
3 2 4 3 2 4 3 3
NO -中心原子N的价电子对数为2+ =2+1=3,则N原子的VSEPR模型为平面三角形,空间构型为
2
V形,A错误;B项,反应①浓硫酸作催化剂,反应③中利用浓硫酸的高沸点、难挥发性,则浓硫酸作用
不同,B错误;C项,反应②中,NH•H O+CHONO+NaOH=NaN +CH OH+3H O,NH•H O中N化合价
2 4 2 3 3 3 2 2 4 2
由-2价升至- 价,故消耗3molN H•H O时,NH•H O失去 电子,C正确;D项,反应
2 4 2 2 4 2④中氧化剂与还原剂分别为NaClO和NH •H O,由于NaClO~Cl-~2e-,2NH •H O~NH•H O~2e-,故二者物
3 2 3 2 2 4 2
质的量之比为1:2,D错误; 故选C。
15.(2024·辽宁部分高中高三联考)中国科研团队首次提出声催化产氢的概念并将其定义为US提供外
部能量输入以激活声催化剂通过裂解双氧水在肿瘤部位原位产氢,工作原理如图所示。下列叙述正确的是(
)
已知:US提供能量使Pt -Bi S 产生电子和“空穴”( ),电子驱动阴极反应,“空穴”驱动阳极反
2 3
应。
A.反应(1)中每生成1molB i S,转移6mol e-
2 3
B.反应(2)中NaBH 作还原剂
4
C.反应(3)的反应式为2H+-2e-=H↑
2
D.反应(4)中每生成11.2L(标准状况)O ,转移4mol电子
2
【答案】B
【解析】A项,由题图知,反应(1)的反应式为2Bi(NO)·5H O +3Na S·9H O =Bi S+6NaNO +37H O,
3 3 2 2 2 2 3 3 2
该反应为非氧化还原反应,没有电子转移,A错误;B项,反应(2)的反应中,BiS 转化Pt -Bi S 被还原,
2 3 2 3
作氧化剂,故NaBH 作还原剂,B正确;C项,由题图知,反应(3)的反应式为2H++2e-=H↑,C错误;
4 2
D项,由题图知,反应(3)的反应式为2HO-2e-= 2H++O ↑,生成11.2L(标准状况)O ,转移1mol电子,D
2 2 2 2
错误;故选B。
二、非选择题(本题包括5小题,共55分)
16.(8分)(2023·山西省吕梁市二模)以萃铜余液为原料制备工业活性氧化锌,其生产工艺流程如图所
示:
(1)铜萃余液含硫酸30~60g/L,设计采用过硫酸钠(Na SO)氧化法除锰,写出Mn2+被氧化成MnO 的离
2 2 8 2
子方程式___________。
(3)用锌粉除镉(Cd2+ )的离子方程式为___________;沉锌生成碱式碳酸锌[2Zn(OH )·ZnCO·H O]的化学
2 3 2
方程式为___________。
(5)煅烧炉中发生反应的化学方程式为___________。【答案】(1) Mn2+ +S O2- +2H O= MnO +2SO2-+4H+
2 8 2 2 4
(3) Zn+Cd2+=Zn2++Cd 3ZnSO + 3Na CO+3H O= 2Zn(OH) ·ZnCO·H O↓+3Na SO + 2CO↑
4 2 3 2 2 3 2 2 4 2
(5) 2Zn(OH) ·ZnCO·H O 3ZnO+CO ↑+3H O
2 3 2 2 2
【解析】(1)铜萃余液含硫酸30~60g/L,设计采用过硫酸钠(Na SO)氧化法除锰,Mn2+被氧化成
2 2 8
MnO ,过硫酸根离子被还原为硫酸根离子,离子方程式为:Mn2+ + S O2- +2H O= MnO +2SO2-+4H+;
2 2 8 2 2 4
(3)锌与镉离子发生取代反应生成锌离子和单质镉,离子方程式为:Zn+Cd2+=Zn2++Cd;向硫酸锌溶液中加
入碳酸钠溶液生成碱式碳酸锌,相应的方程式为:3ZnSO+ 3Na CO+3H O=
4 2 3 2
2Zn(OH) ·ZnCO·H O↓+3Na SO + 2CO↑;(5)由流程可知,工业碱式碳酸锌在煅烧炉中煅烧生成活性氧化
2 3 2 2 4 2
锌,则相应的方程式为:2Zn(OH) ·ZnCO·H O 3ZnO+CO ↑+3H O。
2 3 2 2 2
17.(6分)(2023·湖北省武汉市5调)高锰酸钾在化工生产和环境保护等领域应用十分广泛。以软锰矿(主
要成分是MnO ,含有Fe O 和SiO 等杂质)为原料制备高锰酸钾的工艺流程如图:
2 2 3 2
回答下列问题:
(2)“焙烧”中有KMnO 生成,该步骤主要反应的化学方程式为_______。
2 4
(5) “歧化”过程中主要反应的离子方程式为_____。
【答案】(2)3MnO +6KOH+KClO 3KMnO +KCl+3H O
2 3 2 4 2
(5) 3MnO2-+4CO +2H O=2MnO -+ MnO ↓+4HCO-
4 2 2 4 2 3
【解析】(2)软锰矿(主要成分是MnO ,含有Fe O 和SiO 等杂质),加入KClO 和KOH,焙烧,将
2 2 3 2 3
MnO 氧化为KMnO ,化学方程式为3MnO +6KOH+KClO 3KMnO +KCl+3H O;(5)向滤液中通入足
2 2 4 2 3 2 4 2
量的CO,KMnO 发生歧化反应:3KMnO +4CO +2H O=2KMnO + MnO ↓+4KHCO ,离子方程式为:
2 2 4 2 4 2 2 4 2 3
3MnO 2-+4CO +2H O=2MnO -+ MnO ↓+4HCO-。
4 2 2 4 2 3
18.(13分)用零价铁( )去除含氮废水中的硝酸盐(NO -)是环境修复的重要方法。一种去除NO -的过程
3 3
如下。
(1)Ⅱ中充分反应后,分离混合物的方法是_______。
(2)Ⅱ中反应的离子方程式是_______。
(3)实验发现,在Ⅱ中补充一定量的 可以明显提高NO -的去除率。向两份含氮废水[n(NO -)=8.1×10-
3 35mol]中均加入足量 粉,做对比研究。
实验序号 ⅰ ⅱ
所加试剂 Fe粉 Fe粉、FeCl (3.6×10-5mol)
2
NO -的去除率 ≈50% ≈100%
3
分析ⅱ中NO -的去除率提高的原因:
3
A. 直接还原NO -了。
3
通过计算说明电子得、失数量关系:_______,证明该原因不合理。
B.研究发现:Fe O (导电)覆盖在铁粉表面;随着反应的进行,产生 (不导电),它覆盖在
3 4
Fe O 表面,形成钝化层,阻碍电子传输。
3 4
C. Fe2+能与FeO(OH)反应生成Fe O。
3 4
用57FeCl 做同位素示踪实验,证明该原因合理。
2
D. Cl-破坏钝化层。
将ⅱ中的FeCl 替换为_______,NO -的去除率约为50%,证明该原因不合理。
2 3
(4)ⅰ、ⅱ中均能发生Fe+2H+=Fe2++H ↑。该反应明显有助于ⅰ中NO -的去除,结合方程式解释原因:
2 3
_______。
(5)测定NO -含量
3
步骤1.取vmL含氮(NO -)水样,加入催化剂、v mLcmol·L-1FeSO 标准溶液(过量),再加入稀HSO 。
3 1 1 4 2 4
步骤2.用cmol·L-1KCrO 标准溶液滴定剩余的Fe2+ ( CrO2-被还原为Cr3+),终点时消耗v mL。
2 2 2 7 2 7 2
已知:3Fe2++NO-+4H+=3Fe2++NO↑+2HO
3 2
①水样中NO -的含量为_______ 。
3
②溶液中O 影响测定。向步骤1中加入适量NaHCO ,产生CO 驱赶O,否则会使测定结果
2 3 2 2
_______(填“偏大”或“偏小”)。
【答案】(1)过滤
(2) 3Fe+NO -+2H++2H O=Fe O+NH+
3 2 3 4 4
(3) 还原NO -所需电子:3.24×10-4mol,Fe2+最多提供的电子:3.6×10-5mol。Fe2+失去的电子数明显小于
3
NO -所需电子数; 7.2×10-5mol NaCl;
3
(4) Fe2++2FeO(OH)=Fe O+2H+,Fe2+破坏了钝化层;
3 4
(5) 偏大
【解析】(1)由步骤II得四氧化三铁和废水,因为四氧化三铁难溶于水,可得步骤II的分离操作为过
滤;(2)由步骤II反应产物为四氧化三铁和NH +,且铁粉和NO -在酸性条件下发生该反应,所以该氧化还
4 3
原反应为3Fe+NO-+2H++2H O=Fe O+NH+;(3)根据物质得失电子的计量关系,可知Fe2+~ Fe3+~ 1e-,
3 2 3 4 4
Fe2+最多提供的电子:3.6×10-5mol,NO -~NH+~8 e-,NO -所需电子:3.24×10-4mol,Fe2+失去的电子数明显
3 4 3小于NO -所需电子数;为说明是否是Cl-破坏钝化层,根据控制变量法的思想将3.6×10-5mol FeCl (即
3 2
n(Cl-)=7.2×10-5mol)替换为氯离子物质的量相同的氯化钠,即7.2×10-5mol NaCl看是否能达到同样的去除
率,若不能达到同样的去除率说明Cl-不能破坏钝化层,反知为Fe2+破坏了钝化层;(4)根据上述分析可知生
成的Fe O (导电)覆盖在铁粉表面;随着反应的进行,产生FeO(OH) (不导电),它覆盖在Fe O 表面,形成
3 4 3 4
钝化层,阻碍电子传输。而Fe2++2FeO(OH)=Fe O+2H+,破坏了钝化层有利于内层的铁能继续与硝酸根反
3 4
应;(5)步骤1.取vmL含氮(NO -)水样,加入催化剂、v mLcmol·L-1FeSO 标准溶液(过量),再加入稀
3 1 1 4
HSO 。发生3Fe2++NO-+4H+=3Fe2++NO↑+2HO,步骤2.用cmol·L-1KCrO 标准溶液滴定剩余的Fe2+
2 4 3 2 2 2 2 7
( CrO2-被还原为Cr3+),终点时消耗v mL。发生6Fe2++CrO2-+14H+=6Fe3++2Cr3++7H O,根据KCrO 标准
2 7 2 2 7 2 2 2 7
溶液的用量求得剩余的FeSO 的物质的量=6cv×10-3mol,则参与步骤I反应的FeSO 的物质的量=
4 2 2 4
,根据该反应3Fe2++NO-+4H+=3Fe2++NO↑+2HO可得反应消耗的硝酸根物质的量
3 2
,所以原水样中NO -的含量
3
;因为溶液中O 存在,也会消耗FeSO ,所以KCrO
2 4 2 2 7
用量偏小,由于FeSO 总量一定,所以参与步骤I反应的FeSO 物质的量会偏大(计算造成的误差),自然计
4 4
算出来的水样中NO -的含量也偏大。
3
19.(13分)Ⅰ. NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
2
回答下列问题:
(1)“反应”步骤中生成ClO 的反应中氧化剂与还原剂的物质的量之比为_______。
2
Ⅱ.某实验小组模仿工业生产的方法,设计了一套实验室制备装置,生产NaClO 产品。
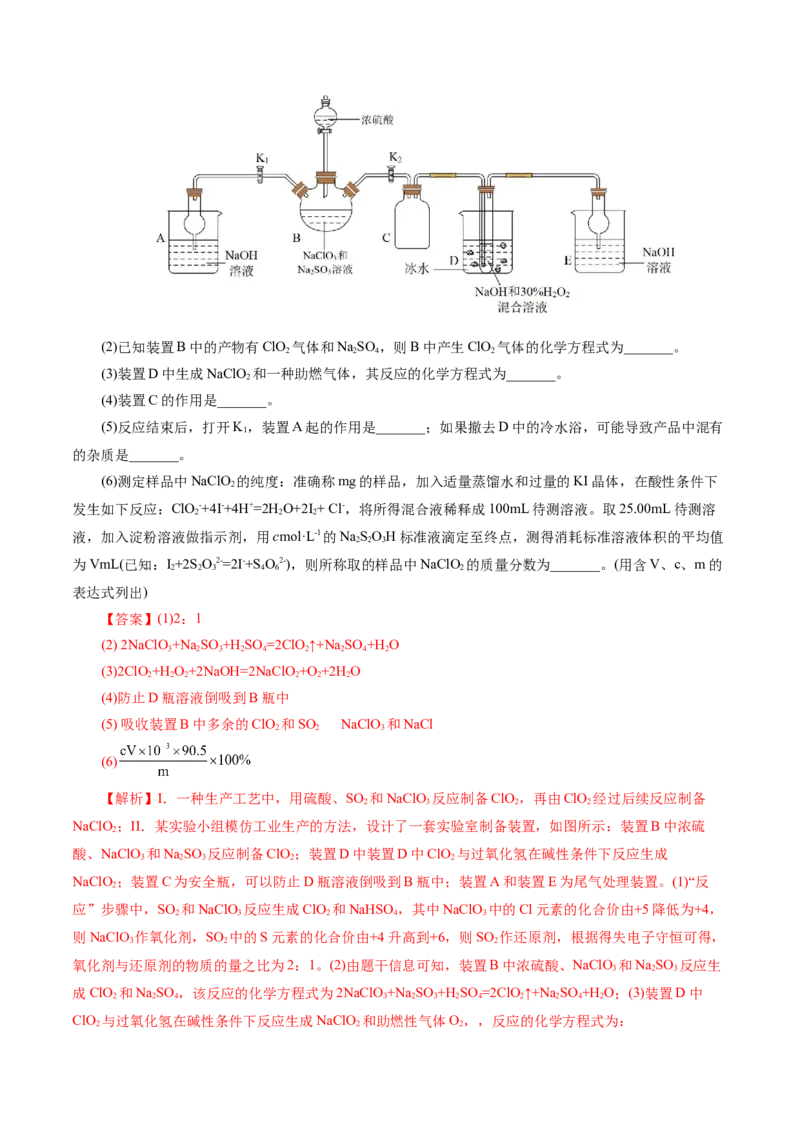
2(2)已知装置B中的产物有ClO 气体和NaSO ,则B中产生ClO 气体的化学方程式为_______。
2 2 4 2
(3)装置D中生成NaClO 和一种助燃气体,其反应的化学方程式为_______。
2
(4)装置C的作用是_______。
(5)反应结束后,打开K,装置A起的作用是_______;如果撤去D中的冷水浴,可能导致产品中混有
1
的杂质是_______。
(6)测定样品中NaClO 的纯度:准确称mg的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下
2
发生如下反应:ClO -+4I-+4H+=2H O+2I + Cl-,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶
2 2 2
液,加入淀粉溶液做指示剂,用cmol·L-1的NaSOH标准液滴定至终点,测得消耗标准溶液体积的平均值
2 2 3
为VmL(已知:I+2S O2-=2I-+S O2-),则所称取的样品中NaClO 的质量分数为_______。(用含V、c、m的
2 2 3 4 6 2
表达式列出)
【答案】(1)2:1
(2) 2NaClO +Na SO +H SO =2ClO ↑+Na SO +H O
3 2 3 2 4 2 2 4 2
(3)2ClO+H O+2NaOH=2NaClO +O +2H O
2 2 2 2 2 2
(4)防止D瓶溶液倒吸到B瓶中
(5) 吸收装置B中多余的ClO 和SO NaClO 和NaCl
2 2 3
(6)
【解析】I.一种生产工艺中,用硫酸、SO 和NaClO 反应制备ClO ,再由ClO 经过后续反应制备
2 3 2 2
NaClO;II.某实验小组模仿工业生产的方法,设计了一套实验室制备装置,如图所示:装置B中浓硫
2
酸、NaClO 和NaSO 反应制备ClO ;装置D中装置D中ClO 与过氧化氢在碱性条件下反应生成
3 2 3 2 2
NaClO;装置C为安全瓶,可以防止D瓶溶液倒吸到B瓶中;装置A和装置E为尾气处理装置。(1)“反
2
应”步骤中,SO 和NaClO 反应生成ClO 和NaHSO,其中NaClO 中的Cl元素的化合价由+5降低为+4,
2 3 2 4 3
则NaClO 作氧化剂,SO 中的S元素的化合价由+4升高到+6,则SO 作还原剂,根据得失电子守恒可得,
3 2 2
氧化剂与还原剂的物质的量之比为2:1。(2)由题干信息可知,装置B中浓硫酸、NaClO 和NaSO 反应生
3 2 3
成ClO 和NaSO ,该反应的化学方程式为2NaClO+Na SO +H SO =2ClO ↑+Na SO +H O;(3)装置D中
2 2 4 3 2 3 2 4 2 2 4 2
ClO 与过氧化氢在碱性条件下反应生成NaClO 和助燃性气体O,,反应的化学方程式为:
2 2 22ClO +H O+2NaOH=2NaClO +O +2H O;(4)装置C是安全瓶,其作用是防止D瓶溶液倒吸到B瓶中;
2 2 2 2 2 2
(5)ClO 和SO 为有毒气体,需要用NaOH吸收ClO 等有害气体,防止污染环境,故装置A起的作用是吸
2 2 2
收置B中多余的ClO 和SO ;如果撤去D中的冷水浴,ClO 会和NaOH发生反应
2 2 2
6ClO +6NaOH=NaCl+5NaClO +3H O,导致产品中混有NaClO 和NaCl;(6)已知:ClO -+4I-
2 3 2 3 2
+4H+=2H O+2I + Cl-,I+2S O2-=2I-+S O2-,得关系式NaClO~4Na SO ,n(Na SO)=cV10-3mol,则样品
2 2 2 2 3 4 6 2 2 2 3 2 2 3
中,n(NaClO)= cV10-3mol =cV10-3mol,样品中NaClO 的质量分数为
2 2
= 。
20.(15分) H O、O、O 在水中可形成具有超强氧化能力的羟基自由基(·OH),能有效去除废水中的
2 2 2 3
HPO -、CN-、苯酚等物质
2 2
(1)H O、O 在一定条件可处理废水中HPO -。
2 2 3 2 2
①弱碱性条件下·OH将HPO -氧化成PO 3-,该反应的离子方程式为___________。
2 2 4
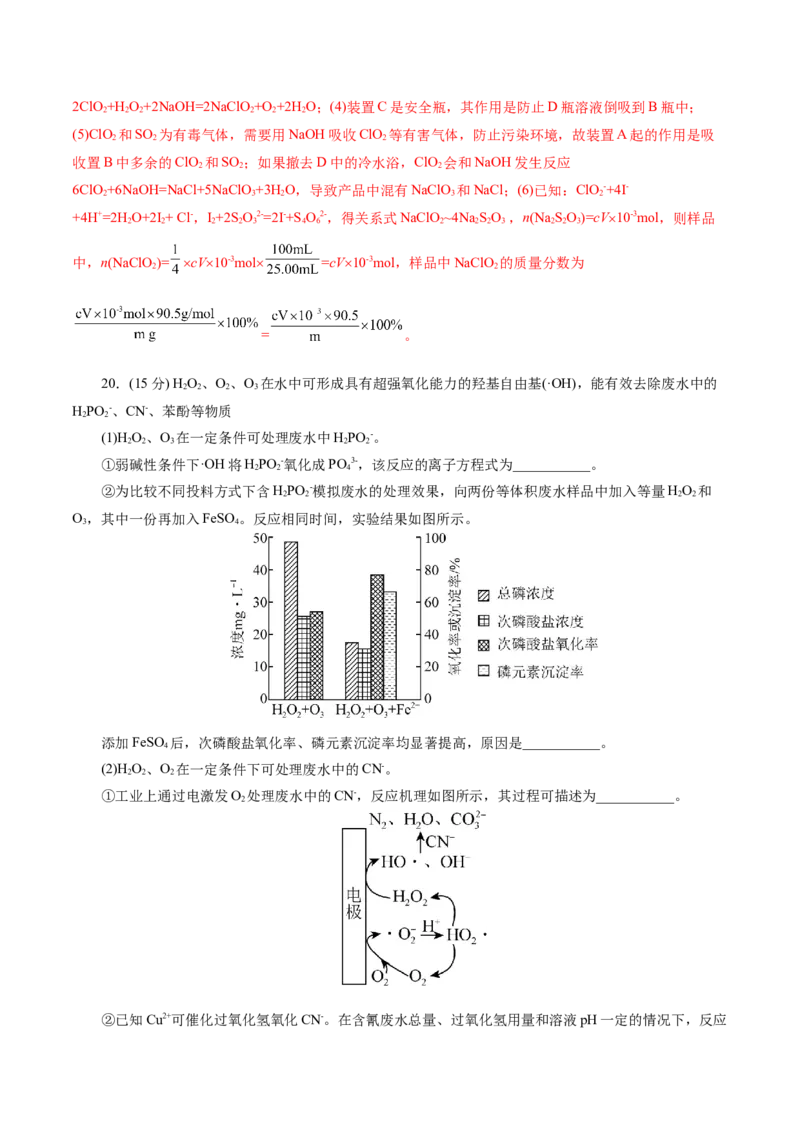
②为比较不同投料方式下含HPO -模拟废水的处理效果,向两份等体积废水样品中加入等量HO 和
2 2 2 2
O,其中一份再加入FeSO 。反应相同时间,实验结果如图所示。
3 4
添加FeSO 后,次磷酸盐氧化率、磷元素沉淀率均显著提高,原因是___________。
4
(2)H O、O 在一定条件下可处理废水中的CN-。
2 2 2
①工业上通过电激发O 处理废水中的CN-,反应机理如图所示,其过程可描述为___________。
2
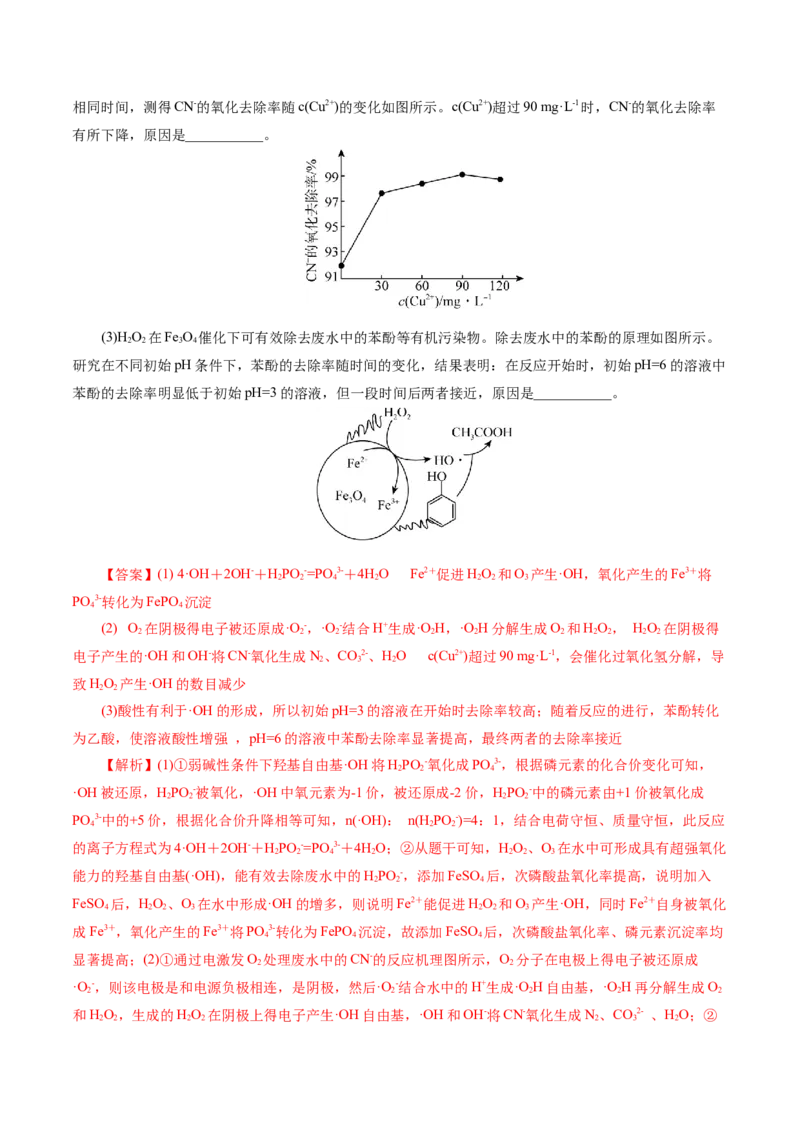
②已知Cu2+可催化过氧化氢氧化CN-。在含氰废水总量、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化如图所示。c(Cu2+)超过90 mg·L-1时,CN-的氧化去除率
有所下降,原因是___________。
(3)H O 在Fe O 催化下可有效除去废水中的苯酚等有机污染物。除去废水中的苯酚的原理如图所示。
2 2 3 4
研究在不同初始pH条件下,苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中
苯酚的去除率明显低于初始pH=3的溶液,但一段时间后两者接近,原因是___________。
【答案】(1) 4·OH+2OH-+HPO -=PO3-+4HO Fe2+促进HO 和O 产生·OH,氧化产生的Fe3+将
2 2 4 2 2 2 3
PO 3-转化为FePO 沉淀
4 4
(2) O 在阴极得电子被还原成·O -,·O -结合H+生成·O H,·O H分解生成O 和HO, HO 在阴极得
2 2 2 2 2 2 2 2 2 2
电子产生的·OH和OH-将CN-氧化生成N、CO2-、HO c(Cu2+)超过90 mg·L-1,会催化过氧化氢分解,导
2 3 2
致HO 产生·OH的数目减少
2 2
(3)酸性有利于·OH的形成,所以初始pH=3的溶液在开始时去除率较高;随着反应的进行,苯酚转化
为乙酸,使溶液酸性增强 ,pH=6的溶液中苯酚去除率显著提高,最终两者的去除率接近
【解析】(1)①弱碱性条件下羟基自由基·OH将HPO -氧化成PO 3-,根据磷元素的化合价变化可知,
2 2 4
·OH被还原,HPO -被氧化,·OH中氧元素为-1价,被还原成-2价,HPO -中的磷元素由+1价被氧化成
2 2 2 2
PO 3-中的+5价,根据化合价升降相等可知,n(·OH): n(H PO -)=4:1,结合电荷守恒、质量守恒,此反应
4 2 2
的离子方程式为4·OH+2OH-+HPO -=PO3-+4HO;②从题干可知,HO、O 在水中可形成具有超强氧化
2 2 4 2 2 2 3
能力的羟基自由基(·OH),能有效去除废水中的HPO -,添加FeSO 后,次磷酸盐氧化率提高,说明加入
2 2 4
FeSO 后,HO、O 在水中形成·OH的增多,则说明Fe2+能促进HO 和O 产生·OH,同时Fe2+自身被氧化
4 2 2 3 2 2 3
成Fe3+,氧化产生的Fe3+将PO 3-转化为FePO 沉淀,故添加FeSO 后,次磷酸盐氧化率、磷元素沉淀率均
4 4 4
显著提高;(2)①通过电激发O 处理废水中的CN-的反应机理图所示,O 分子在电极上得电子被还原成
2 2
·O -,则该电极是和电源负极相连,是阴极,然后·O -结合水中的H+生成·O H自由基,·O H再分解生成O
2 2 2 2 2
和HO,生成的HO 在阴极上得电子产生·OH自由基,·OH和OH-将CN-氧化生成N、CO2- 、HO;②
2 2 2 2 2 3 2在催化剂种类不变情况下,c(Cu2+)超过90 mg·L-1时,CN-的氧化去除率有所下降,说明HO 产生·OH的数
2 2
目减少,说明部分双氧水分解成氧气和水了,故当c(Cu2+)超过90 mg·L-1时,会催化过氧化氢分解,导致
HO 产生·OH的数目减少;(3)研究在不同初始pH条件下,苯酚的去除率随时间的变化,结果表明:在反
2 2
应开始时,初始pH=6的溶液中苯酚的去除率明显低于初始pH=3的溶液,说明酸性影响苯酚的去除率,则
酸性条件下更有利于·OH的形成,所以初始pH=3的溶液在开始时去除率较高。通过图也可知苯酚最终转
化成乙酸了,则随着反应进行,溶液酸性也会越来越强,故初始pH=6的溶液中苯酚的去除率一段时间后
也会提高,最终两者比较接近。