文档内容
专题 05 化学反应中的能量变化
1.(2022·山东省青岛高三模拟)如图(E 表示活化能)是CH 与Cl 生成CHCl的部分反应过程中各物质物
a 4 2 3
质的能量变化关系图,下列说法正确的是( )
A.Cl·可由Cl 在高温条件下生成,是CH 与Cl 反应的催化剂
2 4 2
B.升高温度,E 、E 均减小,反应速率加快
a1 a2
C.增大Cl 的浓度,可提高反应速率,但不影响△H的大小
2
D.第一步反应的速率大于第二步反应
【答案】C
【解析】Cl·由Cl 在光照条件下生成,是CH 与Cl 反应的“中间体”,而不是反应的催化剂,A错误;
2 4 2
E 、E 分别为第一步反应、第二步反应所需活化能,升高温度,反应所需活化能不变,即E 、E 不变,
a1 a2 a1 a2
B错误; Cl 是该反应的反应物,增大反应物的浓度,反应速率增大,而反应的△H和反应的途径无关,
2
只与反应的始态和终态有关,即增大氯气的浓度不影响△H的大小,C正确;第一步反应所需活化能E 大
a1
于第二步反应所需活化能E ,第一步反应单位体积内活化分子百分数低于第二步反应,故第二步反应速率
a2
更大,D错误。答案选C。
2.(2022·浙江省杭州第二中学高三模拟)卤化铵(NH X)的能量关系如图所示,下列说法正确的是(
4
)
A.ΔH>0,ΔH<0
1 2
B.B.相同条件下,NH Cl的ΔH 比NH I的小
4 2 4
C.相同条件下,NH Cl的ΔH 比NH I的小
4 3 4
D.ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5
【答案】C
【解析】卤化铵的分解为吸热反应,ΔH 对应的为HX化学键断裂过程,断裂化学键吸收热量,焓变也为
2
正值,则ΔH>0、ΔH>0,A错误;氯原子半径小于碘原子,所以H-Cl的键能大于H-I的键能,断键吸收
1 2热量焓变大于0,所以相同条件下,NH Cl的ΔH 比NH I的大,B错误;ΔH 为原子变为离子的过程,
4 2 4 3
Cl(g)Cl-(aq)比I(g)I-(aq)放出的热量多,所以相同条件下,NH Cl的ΔH 比NH I的小,C正确;途径5
4 3 4
与途径1、2、3、4之和的起点和终点相同,结合盖斯定律可知ΔH+ΔH+ΔH+ΔH=ΔH,故D错误;故选
1 2 3 4 5
C。
3.(2022·四川省广汉中学高三一模)1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二
烯生成碳正离子(CH,CHCH,);第二步Br-进攻碳正离子完成1,2-加成或1,4加成。反应进程中的能量
变化如下图所示。下列说法不正确的是
A.1,4-加成产物比1,2-加成产物更稳定
B.1,3-丁二烯与HBr发生加成反应是放热反应
C.适当升高反应温度,可能有利于1,4-加成的进行
D.选择合适的催化剂加入,可使1,2-加成的焓变小于1,4-加成
【答案】D
【解析】由图象可知,1,4-加成产物比1,2-加成产物能量低,则1,4-加成产物比1,2-加成产物更稳
定,故A正确;由图象可知,1,3-丁二烯与HBr的能量总和高于加成后生成物的能量总和,则1,3-丁二
烯与HBr发生加成反应是放热反应,故B正确;由图象可知,1,3-丁二烯与HBr发生加成反应是放热反
应,适当升高反应温度,可以加快反应速率,可能有利于1,4-加成的进行,但不利于提高反应物的转化
率,故C正确;
选择合适的催化剂加入,可以改变化学反应速率,但不能使化学平衡发生移动,所以不会改变反应物的转
化率,更不会改变焓变,故D错误;故选D。
4.(2022·江苏省南京高三零模)在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO(g)+4H(g)=CH (g)+2HO(g) ΔH= -164.7 kJ/mol
2 2 4 2
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ΔH= 41.2 kJ/mol
2 2 2
反应Ⅲ:2CO(g)+2H(g)=CO (g)+CH (g) ΔH= -247.1 kJ/mol
2 2 4
向恒压、密闭容器中通入1 mol CO 和4 mol H ,平衡时CH、CO、CO 的物质的量随温度的变化如图所
2 2 4 2
示。下列说法正确的是( )A.反应Ⅰ的平衡常数可表示为K=
B.图中曲线B表示CO的物质的量随温度的变化
C.提高 CO 转化为CH 的转化率,需要研发在低温区高效的催化剂
2 4
D.CH(g)+HO(g) =CO(g)+3H (g)的ΔH= -205.9 kJ/mol
4 2 2
【答案】C
【解析】化学平衡常数是生成物浓度幂之积与反应物浓度幂之积的比值,反应Ⅰ的平衡常数为K=
,故A错误;反应物CO 的量逐渐减小,故图中曲线A表示CO 的物质的量变化曲线,
2 2
由反应Ⅱ和Ⅲ可知,温度升高反应Ⅱ正向移动,反应Ⅲ逆向移动,CO的物质的量增大,故曲线C为CO的
物质的量变化曲线,则曲线B为CH 的物质的量变化曲线,故B错误;反应Ⅰ为放热反应,反应Ⅱ为吸热
4
反应,降低温度有利于反应Ⅰ正向移动,反应Ⅱ逆向移动,即可提高 CO 转化为CH 的转化率,所以需要
2 4
研发在低温区高效的催化剂,故C正确;得到目标反应,则CH(g)+HO(g) ===CO(g)+3H (g)的ΔH=-[41.2
4 2 2
kJ/mol +(-247.1 kJ/mol)] =205.9 kJ/mol,故D错误;故选C。
5.(2022·浙江杭州市高三一模)下列关于如图所示转化关系( 代表卤素)的说法中正确的是( )
A. 越小, 就越稳定
B.
C.按照 、 、 的顺序, 依次增大
D.过程Ⅲ能量变化形式与高温煅烧石灰石的能量变化形式相同
【答案】A
【解析】 越小,放热越多,HX能量越低, 就越稳定,故A正确;根据盖斯定律,
,故B错误;原子半径越小,键能越大,按照 、 、 的顺序, 依次减小,故
C错误;过程Ⅲ形成化学键放热,高温煅烧石灰石吸热,能量变化形式不相同,故D错误;故选A。
6.(2022·山东德州市高三二模)稀土铈(Ce)元素主要存在于独居石中,金属铈化学性质十分活泼。近年
来发现用铈(Ce)的氧化物可高效制取H,制备原理如图所示,已知0< <2,下列说法不正确的是
2A.CeO 是水分解的催化剂
2
B.T<1050℃时,CeO 比CeO 稳定
2 2—δ
C.工业上可用电解CeCl 溶液制备Ce
4
D.过程②的方程式为CeO +δH O CeO+δH
2—δ 2 2 2
【答案】C
【解析】CeO 在反应前后质量和性质不变,所以CeO 是水分解的催化剂,A正确;T<1050℃时,CeO
2 2 2﹣δ
转化成CeO,所以CeO 比CeO 稳定,B正确;Ce是活泼金属,应电解熔融的CeCl 制备Ce,C错误;
2 2 2﹣δ 4
由上图可知,过程②是CeO 和HO反应生成CeO 和H,所以方程式为CeO +δH O CeO+δH ,D
2—δ 2 2 2 2-δ 2 2 2
正确;故选C。
1.(2022.·安徽合肥市高三模拟)煤和甲烷既是重要的常用燃料,又是重要的化工原料。根据题意,回答下
列问题:
I.煤制天然气过程中,存在多种化学反应,其中在煤气化装置中发生反应①:C(s) + H O(g)=CO(g) + H (g)
2 2
∆H = +135 kJ • mol-1,而在水气变换装置中发生反应②:CO(g)+HO(g)=CO(g)+ H (g) ∆H =-41 kJ • mol-1
2 2 2
(1)煤气化前,需要通入一定量的氧气与碳发生燃烧反应,请利用平衡移动原理说明通入氧气的作用:
______________________________。
(2)写出碳和二氧化碳反应生成一氧化碳的热化学方程式___________________________________。
(3)如图表示发生反应①后进入反应②装置的n( H O)/n(CO)与反应②中CO平衡转化率、温度的变化关系。
2
若n(H O)/n(CO)为0.8,一定量的煤和水蒸气经反应①和反应②后,得到CO与H 的物质的量之比为1:3,
2 2
则反应②所对应的温度是______________(填“T”、“T”或“T”)。
1 2 3
Ⅱ.甲烷重整技术主要是利用甲烷和其他原料来制备合成气(CO和h 混合气体)。现在常(见的重整技术有甲
2
烷——二氧化碳重整、甲烷——水蒸气重整,其反应分别为CH
4
(g)+3CO
2
(g)⇌2H
2
O(g)+4CO(g);CH
4
(g)+H
2
O(g)⇌CO(g)+3H
2
(g)
(4)甲烷——二氧化碳重整的催化转化原理如图所示:
①过程(二)实现了含氢物种与含碳物种的分离,写出生成HO(g)的化学方程式:
2
________________________。
②假设过程(一)和过程(二)中各步反应均转化完全,则下列说法正确的是_____(填序号)。
a.过程(一)和过程(二)中均含有氧化还原反应
b.过程(二)中使用的催化剂为Fe O 和CaCO
3 4 3
C.若过程(一)投料比 ,可导致过程(二)中催化剂失效
(5)通过计算机模拟甲烷——水蒸气重整实验测得,在操作压强为0.1Mpa、水碳比n(H O)/n(CH )为1.0,温
2 4
度为900℃,反应达到平衡时,H 的物质的量分数为0.6。已知该反应的速率方程v=kP(CH)·P-1(H ),式中
2 4 2
k为速率常数,P为气体分压,气体分压=总压×气体物质的量分数,则此时该反应速率v=_____(用含k的
式子表示);900℃时,该反应的压强平衡常数Kp=_____(用平衡分压代替平衡浓度计算)。
【答案】(1)氧气与碳发生燃烧反应放热,放出的热被可逆反应吸收利用,促进反应正向移动 (2)C(s)
+CO (g)=2CO(g) ∆H=+176kJ/mol (3) T (4) 4H +Fe O 3Fe+4H O ac (5) 4.32×10-2(MPa)2
2 3 2 3 4 2
【解析】
(1)C(s)+H
2
O(g)⇌CO(g)+H
2
(g)△H=+135kJ⋅mol−1,是吸热反应,而碳与氧气反应放出热量,使反应C(s)
+H
2
O(g)⇌CO(g)+H
2
(g),向正反应方向移动,提高碳的利用率;答案为氧气与碳发生燃烧反应放热,放出
的热被可逆反应C(s)+H
2
O(g)⇌CO(g)+H
2
(g)吸收利用,促进反应正向移动。
(2)由①:C(s) + H O(g)=CO(g) + H (g) ∆H= +135 kJ • mol-1,②:CO(g)+HO(g)=CO(g)+ H (g) ∆H=-41 kJ
2 2 2 2 2
• mol-1,根据盖斯定律,用①-②可得出:C(s)+CO(g)=2CO(g) ∆H=+135 kJ • mol-1-(-41 kJ • mol-1)=+176 kJ •
2
mol-1;答案为C(s)+CO(g)=2CO(g) ∆H=+176 kJ • mol-1;
2
(3)如图:若n(H O)/n(CO)为0.8,设水蒸气的物质的量是4mol、则①生成的CO物质的量为5mol,同时
2
生成5mol氢气,经煤气化反应①和水气变换反应②后,设反应②中CO变化了xmol,则生成xmol氢气,则
(5−x):(5+x)=1:3,x=2.5mol,CO的转化率= ×100%=50%,根据图知,反应温度为T;答案为T。
3 3
(4)①由上述图可知,过程(一)的产物CO、H、和过量的CO 进入过程(二)中,与过程(二)中的
2 2
Fe O、CaO混合发生反应,实现了含氢物种与含碳物种的分离,生成HO(g)的反应显然是H 与Fe O 反
3 4 2 2 3 4应,则化学方程式为:Fe O+4H 3Fe+4H O;答案为Fe O+4H 3Fe+4H O。
3 4 2 2 3 4 2 2
②a.过程(一):CH+CO (g) 2H(g)+2CO,碳、氢元素化合价发生变化,属于氧化还原反应,过程
4 2 2
(二):4H+Fe O 3Fe+4H O,氢、铁元素化合价发生变化,属于氧化还原反应,过程(一)和过程
2 3 4 2
(二)中均含有氧化还原反应,故a正确;
b.过程(二)中CaCO 是CaO与CO 发生化学反应生成的,不符合催化剂的概念,CaO才是催化剂,故b错
3 2
误;
c.若过程(一)投料比 ,CH 与CO 刚好反应,CO 无剩余,则催化剂CaO在过程(二)中
4 2 2
没有二氧化碳与之反应生成CaCO ,催化剂失效,故c正确;答案为ac。
3
(5)已知n(H O)/n(CH)为1.0,可假设n(H O)=n(CH)=1mol,操作压强为0.1Mpa,温度为900℃,反应达
2 4 2 4
到平衡时,H 的物质的量分数为0.6,设达平衡时CH 变化了xmol,
2 4
根据H 的物质的量分数= =0.6,求出x= mol,则CH 的物质的
2 4
量分数= =0.1,由反应的速率方程v=kP(CH )•P-1(H )=k· =k· = ,同理可求出HO的
4 2 2
物质的量分数为0.1,CO的物质的量分数为0.2;根据气体分压=总压×气体物质的量分数,总压为
0.1Mpa,则P(CO)=0.1×0.2MPa,P(H )=0.1×0.6MPa,P(CH )=0.1×0.1MPa,P(H O)=0.1×0.1MPa,在900℃
2 4 2
时,该反应的压强平衡常数K = = =4.32×10-2(MPa)2。
p
2.(2022·四川成都市高三一模)生产生活中氨及铵盐有重要用途,而汽车尾气中含NO、NO 则应降低其
2
排放。
(1)在20℃时,已知:①N(g) +O (g)=2NO(g) ,正、逆反应活化能分别为a kJ/mol、b kJ/mol;②4NH (g)
2 2 3
+5O (g) =4NO(g)+6H O(l),正、逆反应活化能分别为c kJ/mol、d kJ/mol;则4NH (g)+6NO(g)=5N (g)
2 2 3 2
+6H O(l)的ΔH为___________。
2
(2)10.0L的密闭容器中,按物质的量比1:3投入氮气和氢气,发生反应N
2
(g)+3H
2
(g)⇌2NH
3
(g) ΔH<0用传
感器测得温度为T、T 时容器中n(N )随时间变化如表:
1 2 2
时间
0 5 min 10 min 15 min 20 min
物质的量n(N )
2温度
T 0.1 mol 0.08mol 0.062mol 0.05mol 0.05mol
1
T 0.1 mol 0.07 mol — x mol 0.06 mol
2
①T 时,0~5 min内NH 平均速率为v(NH )=___________
2 3 3
②T 时,该反应平衡常数为___________ (列出计算式);
1
③x___________0.06(填“>”“<”或“=”),原因是___________。
(3)汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除CO、NO等污染物。反应机理
如下[Pt(s)表示催化剂,右上角带“*”表示吸附状态]:
I.NO+ Pt(s) =NO* II. CO+ Pt(s)=CO* III.NO*=N*+ O* IV. CO*+ O*= CO + Pt(s) V. N*+ N*=N + Pt(s) VI.NO*+
2 2
N* = NO+ Pt(s) 经测定汽车尾气中反应物及生成物浓度随温度变化关系如图一和图二所示:
2
①图一,温度为330 ℃时发生的主要反应为___________ (填“IV”、“V”或“VI”);反应VI为
___________反应(填“放热”或“吸热”)。
②图二,温度从T 升至T 的过程中,反应物浓度急剧减小的主要原因是___________。
a b③气体在固体催化剂表面反应中,吸附和解吸同时影响总反应速率。温度一定时,反应2NO+2CO
N+2CO 的反应速率随压强的变化如图所示。结合(3)中反应机理,试从吸附和解吸角度解释bc段化学反应
2 2
速率下降的原因___________。
【答案】(1)(5b+c-5a-d)kJ/mol (2) 1.2×10-3mol/(L∙min) L2∙mol-2 = 5min时
0.08>0.07,说明T 温度高,反应速率快,T 先达到平衡所以15min时T 已达到平衡 (3) IV 放热
2 2 2
温度升高,催化剂活性增强,反应速率加快,所以反应物浓度快速减小 压强增大,吸附速率虽然增
大,但不利于解吸,解吸速率减小更多,所以反应速率减小
【解析】
(1)反应①N(g) +O (g)=2NO(g)的正、逆反应活化能分别为a kJ/mol、b kJ/mol,则①的∆H=(a-b)kJ/mol,反
2 2 1
应②4NH (g)+5O(g)=4NO(g)+6H O(l)的正、逆反应活化能分别为c kJ/mol、dkJ/mol,则②的
3 2 2
∆H=(c-d)kJ/mol,方程式4NH (g)+6NO(g)=5N (g)+6HO(l)可由②-5×①得到,根据盖斯定律,∆H=(c-
2 3 2 2
d)kJ/mol-5×(a-b)kJ/mol=(5b+c-5a-d)kJ/mol;
(2)①由表格数据可知,N 的浓度变化∆c= =0.003mol/L,v(N )= =6×10-
2 2
4(L∙min),根据反应速率之比等于化学计量数之比,v(NH )=2v(N)= 1.2×10-3mol/(L∙min);
3 2
②10.0L的密闭容器中,按物质的量比1:3投入氮气和氢气,由表格数据可列出三段式
平衡常数K= = L2∙mol-2;
③5min时T 温度时N 剩余0.08mol,而T 温度时N 剩余0.07mol,0.08>0.07,说明T 反应速率快,温度
1 2 2 2 2
越高,反应速率越快,故T>T,T 先达到平衡,15min时T 已经达到平衡,所以15min时T 也已达到平
2 1 2 1 2
衡,故x=0.06;
(3) ①由图一可知,生成CO 的量最大,反应机理中,只有反应IV生成CO,故主要进行的是反应IV;
2 2
反应VI生成NO,由图一可以看出,330℃以后,NO的浓度随温度升高而下降,故该反应为放热反应;
2 2②该反应需要催化剂,随着温度升高,催化剂活性增强,逐渐达到催化剂的最适温度,催化剂可以降低反
应的活化能,加快反应速率,随着反应速率的加快,反应物浓度快速减小
③压强增大,吸附速率增大,但是对于气体物质,压强越大,越不利于解吸,而吸附和解吸同时影响总反
应速率,解吸速率由于压强的增大减小的更多,所以反应速率减小。
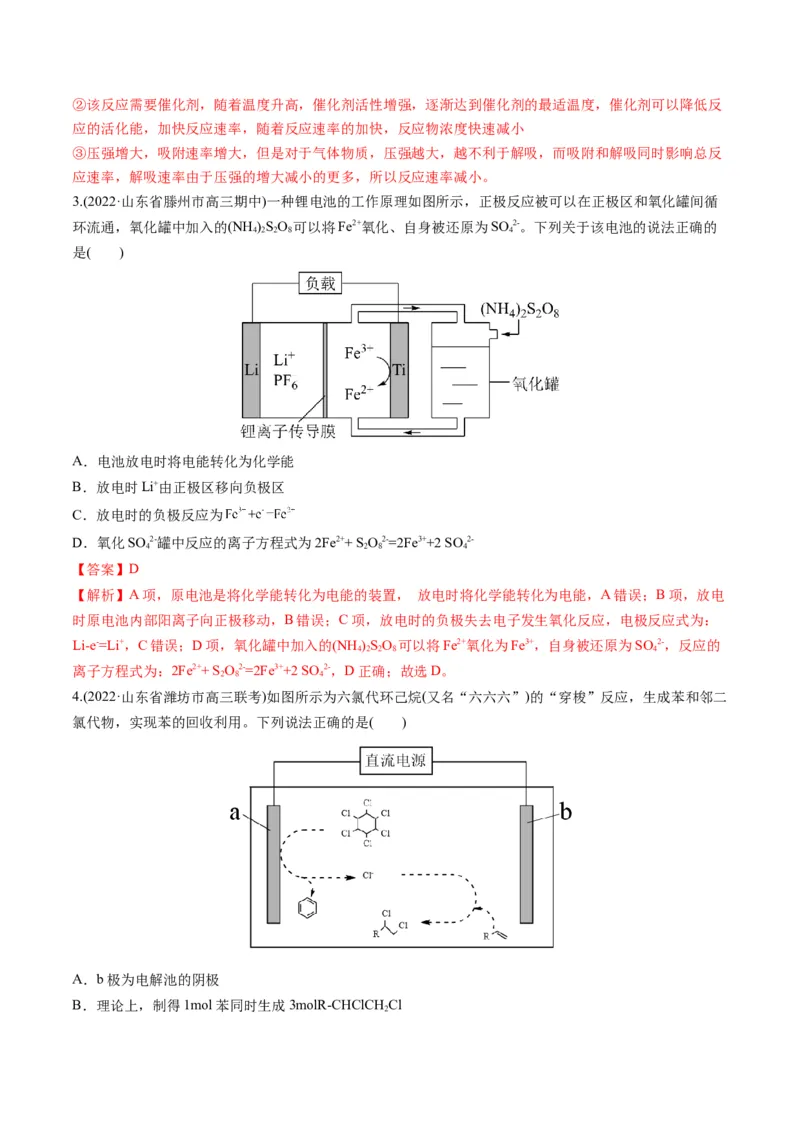
3.(2022·山东省滕州市高三期中)一种锂电池的工作原理如图所示,正极反应被可以在正极区和氧化罐间循
环流通,氧化罐中加入的(NH )SO 可以将Fe2+氧化、自身被还原为SO 2-。下列关于该电池的说法正确的
4 2 2 8 4
是( )
A.电池放电时将电能转化为化学能
B.放电时Li+由正极区移向负极区
C.放电时的负极反应为
D.氧化SO 2-罐中反应的离子方程式为2Fe2++ S O2-=2Fe3++2 SO 2-
4 2 8 4
【答案】D
【解析】A项,原电池是将化学能转化为电能的装置, 放电时将化学能转化为电能,A错误;B项,放电
时原电池内部阳离子向正极移动,B错误;C项,放电时的负极失去电子发生氧化反应,电极反应式为:
Li-e-=Li+,C错误;D项,氧化罐中加入的(NH )SO 可以将Fe2+氧化为Fe3+,自身被还原为SO 2-,反应的
4 2 2 8 4
离子方程式为:2Fe2++ S O2-=2Fe3++2 SO 2-,D正确;故选D。
2 8 4
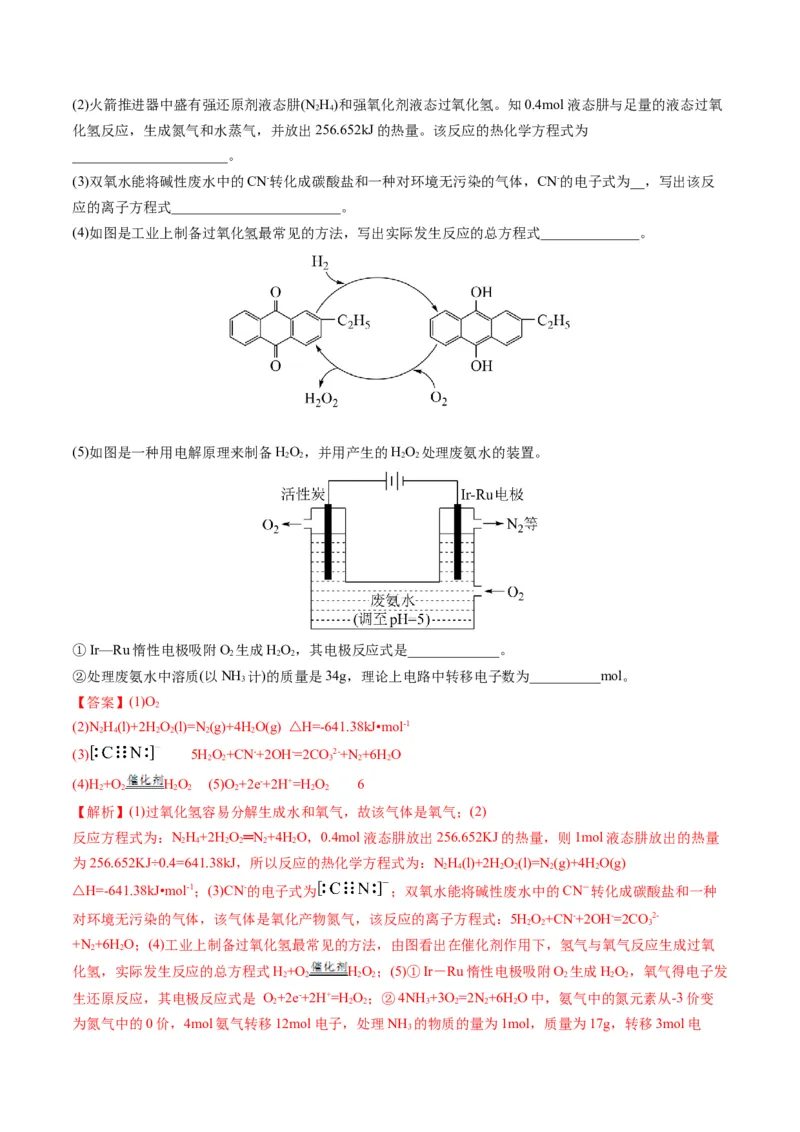
4.(2022·山东省潍坊市高三联考)如图所示为六氯代环己烷(又名“六六六”)的“穿梭”反应,生成苯和邻二
氯代物,实现苯的回收利用。下列说法正确的是( )
A.b极为电解池的阴极
B.理论上,制得1mol苯同时生成3molR-CHClCH Cl
2C.CHClCH Cl经“穿梭”反应后生成乙炔
2 2
D.利用“穿梭”反应转化等质量的“六六六”和CHClCH Cl时转移电子数相等
2 2
【答案】B
【解析】A项,b极上R-CH=CH 与Cl-作用生成RCHClCH Cl,失电子,为电解池的阳极,A错误;B
2 2
项,理论上,由六氯代环己烷(又名“六六六”)制得1mol苯时产生6molCl-,同时生成3molR-
CHClCH Cl,B正确;C项,根据上述反应情况可知,CHClCH Cl经“穿梭”反应后生成乙烯,C错误;
2 2 2
D项,利用“穿梭”反应转化等质量的“六六六”(分子式为C HCl)和CHClCH Cl(分子式为C HCl)
6 6 6 2 2 2 4 2
时,因C的价态变化不一样,故转移电子数不相等,D错误;故选B。
5.(2022·河北邢台市“五校联盟”部分重点中学高三联考)科学家采用电渗析法提纯乳清(富含NaCl的蛋白
质),有价值的蛋白质的回收率达到98%,工作原理如图所示。
下列说法错误的是( )
A.溶液R中溶质的主要成分为HCl
B.膜1为阳离子交换膜,膜2为阴离子交换膜
C.a极的电极反应式为2HO-2e-= 2OH-+H ↑
2 2
D.每转移1mol电子,理论上乳清质量减少58.5g
【答案】C
【解析】光伏电池电渗析法提纯乳清(富含NaCl的蛋白质),左侧a极附近稀NaOH溶液最终变成浓NaOH
溶液,说明溶液中水得电子生成氢气和OH-,Na+通过膜1迁移到a极区,所以a为阴极,膜1为阳离子交
换膜,同理,乳清中的氯离子通过膜2迁移到b极区,发生失电子的氧化反应。A项,氯离子发生失电子
的氧化反应,同时乳清经过膜2迁移到b极氯离子,最终输出的溶液R仍为稀盐酸,溶质的主要成分为
HCl,A正确;B项,膜1为阳离子交换膜,膜2为阴离子交换膜,B正确;C项,a极为阴极,发生得电
子的还原反应,其电极反应式为2HO+2e-= 2OH-+H ↑,C错误;D项,每转移1mol电子,理论上迁移
2 2
1molNa+和1molCl-,因此乳清质量减少23g+35.5g=58.5g,D正确;故选C。
6.(2022·辽宁省沈阳市重点高中联合体高三联考)双氧水(过氧化氢的水溶液)在工业生产和日常生活中应用广
泛。
(1)双氧水的强氧化性使其对大多数病菌和病毒具有消杀功能。用3%医用双氧水对不传染病房喷洒消毒
时,地板上有气泡冒出,该气体是___________。(2)火箭推进器中盛有强还原剂液态肼(N H)和强氧化剂液态过氧化氢。知0.4mol液态肼与足量的液态过氧
2 4
化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为
______________________。
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为__,写出该反
应的离子方程式________________________。
(4)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式______________。
(5)如图是一种用电解原理来制备HO,并用产生的HO 处理废氨水的装置。
2 2 2 2
①Ir—Ru惰性电极吸附O 生成HO,其电极反应式是_____________。
2 2 2
②处理废氨水中溶质(以NH 计)的质量是34g,理论上电路中转移电子数为__________mol。
3
【答案】(1)O
2
(2)N H(l)+2H O(l)=N (g)+4HO(g) △H=-641.38kJ•mol-1
2 4 2 2 2 2
(3) 5H O+CN-+2OH-=2CO 2-+N +6H O
2 2 3 2 2
(4)H +O HO (5)O +2e-+2H+=H O 6
2 2 2 2 2 2 2
【解析】(1)过氧化氢容易分解生成水和氧气,故该气体是氧气;(2)
反应方程式为:NH+2H O═N +4H O,0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量
2 4 2 2 2 2
为256.652KJ÷0.4=641.38kJ,所以反应的热化学方程式为:NH(l)+2H O(l)=N (g)+4HO(g)
2 4 2 2 2 2
△H=-641.38kJ•mol-1;(3)CN-的电子式为 ;双氧水能将碱性废水中的CN-转化成碳酸盐和一种
对环境无污染的气体,该气体是氧化产物氮气,该反应的离子方程式:5HO+CN-+2OH-=2CO 2-
2 2 3
+N +6H O;(4)工业上制备过氧化氢最常见的方法,由图看出在催化剂作用下,氢气与氧气反应生成过氧
2 2
化氢,实际发生反应的总方程式H+O HO;(5)①Ir-Ru惰性电极吸附O 生成HO,氧气得电子发
2 2 2 2 2 2 2
生还原反应,其电极反应式是 O+2e-+2H+=H O;②4NH +3O =2N +6H O中,氨气中的氮元素从-3价变
2 2 2 3 2 2 2
为氮气中的0价,4mol氨气转移12mol电子,处理NH 的物质的量为1mol,质量为17g,转移3mol电
3子,现处理废氨水中溶质(以NH 计)的质量是34g,理论上电路中转移电子数为6mol。
3
7.(2022·辽宁省葫芦岛市协作体高三第二次联考)某化学兴趣小组用50mL0.50mol•L-1盐酸与
50mL0.55mol•L-1NaOH溶液进行中和反应的反应热测定实验,实验装置如图。试回答下列问题:
(1)实验时玻璃搅拌器的使用方法是___;不能用铜丝搅拌器代替玻璃搅拌器的理由是__。
(2)某学生记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为1g•cm-3,中和反应后
溶液的比热容c=4.18J•g-1•℃-1)
起始温度T/℃ 终止温度T/℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.2 23.3
2 20.2 20.4 23.4
3 20.4 20.6 23.8
依据该学生的实验数据计算,该实验测得反应放出的热量为__J。
(3)下列操作会导致实验结果出现偏差的是___(填标号)。
a.用量筒量取盐酸的体积时仰视读数
b.把量筒中的氢氧化钠溶液分多次倒入盐酸中
c.将50mL0.55mol•L-1氢氧化钠溶液取成了50mL0.55mol•L-1氢氧化钾溶液
d.做本实验的当天室温较高
e.大烧杯的杯盖中间小孔太大
(4)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和喊的温度,你是否同意该
同学的观点,为什么?___。
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得中和反应的反应热(△H)___(填“偏大”、
“偏小”或“不变”)。
(6)如果用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行实验,与上述实验相比,二者所放出的热量___(填“相等”或“不相等”,下同),所求的中和反应H+(aq)+OH-(aq)=H O(1) △H的反应热
2
(△H)___。
【答案】(1)上下搅动 Cu是热的良导体,传热快,热量损失大
(2)1337.6 (3)abe
(4)不同意,因为不同的温度计误差不同
(5)偏小 (6) 不相等 相等
【解析】(1)实验时为防止打断温度计,玻璃搅拌器的使用方法是上下搅动;Cu是热的良导体,传热快,
热量损失大,所以不能用铜丝搅拌器代替玻璃搅拌器;(2)三次温度差分别为:3.2℃、3.1℃、3.3℃,温度
的平均值为3.2℃,溶液的总质量为100g,该实验测得反应放出的热量为Q=
;(3)a项,用量筒量取盐酸的体积时仰视读数,使盐酸的体积不准确,
会导致实验结果出现偏差,故a选;b项,把量筒中的氢氧化钠溶液分多次倒入盐酸中,会使热量散失,
会导致实验结果出现偏差,故b选;c项,将50mL0.55mol•L-1氢氧化钠溶液取成了50mL0.55mol•L-1氢氧化
钾溶液,氢氧根的量不变,对实验结果没有影响,故c不选;d项,做本实验的当天室温较高,但测量的
是温度差,与室温无关,对实验结果没有影响,故d不选;e项,大烧杯的杯盖中间小孔太大,会使热量
散失,会导致实验结果出现偏差,故e选;故选abe;(4)因为不同的温度计误差不同,所以不能使用两支
温度计分别测量酸和喊的温度;(5)如果将NaOH溶液换成等量的NaOH固体,由于氢氧化钠固体溶解会放
出热量,导致放热增多,使实验测得中和反应的反应热(△H)偏小;(6)如果用60mL0.50mol•L-1盐酸与
50mL0.55mol•L-1NaOH溶液进行实验,由于试剂的量不同,所放出的热量与上述实验不相等,但中和热是
换算成生成1mol水时放出的热量,所求的中和反应的反应热(△H)与上述反应相等。
8.(2022·山东市潍坊市学科核心素养高三测试)Na SO 用途广泛,可用作还原剂、防腐剂等。回答下列问
2 3
题:
(1)向3mL 0.5mol·L-1NaSO 溶液中逐滴滴入3滴0.5mol·L-1FeCl 溶液,混合液立即变为红褐色,继续滴加
2 3 3
3mLFeCl 溶液,混合液颜色变深;静置1h溶液呈浅绿色。分析反应过程中,氧化还原反应和水解反应活
3
化能较大的是___________,溶液最后呈浅绿色的原因为___________。
(2)常温下,测得NaSO 溶液中相关离子浓度随pH变化的关系如图所示:
2 3
①HSO 的电离平衡常数K =___________mol·L-1。
2 3 a1
②NaHSO 溶液显___________性(填“酸”或“碱”),通过计算说明理由___________(写出计算过程)。
3(3)常温下,用NaSO 溶液作吸收液处理SO ,当pH降低为5左右时,可用如图所示电解槽进行再生,
2 3 2
A、B为离子交换膜,电极为惰性电极。
SO 2-放电的电极反应式为___________,再生后的吸收液中 的最小值为___________;M室中将
3
pH=4.9的吸收液再生至pH=8.9,若有1mol Na+通过离子交换膜,则再生后溶液中的SO 2-的物质的量为
3
___________ (保留两位小数)
【答案】(1)氧化还原反应 水解反应的反应速率较快,开始时Fe(OH) 胶体颜色占主导,一段时间后,
3
随着氧化还原反应持续进行,水解平衡向左移动,溶液呈现Fe2+颜色
(2)10-1.9 酸 HSO - H++SO2- K ,A点pH=5.9,lg =-1,c(H+)=10-5.9mol/L,
3 3 a2
= ,代入 =10-6.9mol/L,又HSO -+H O OH-+SO2- K= =
3 2 4 h
= = =10-12.1,K >K,即HSO -的电离能力大于水解能力,NaHSO 溶液显酸
a2 h 3 3
性
(3)SO 2- -2e-+H O=SO 2- +2H+ 100 0.66mol
3 2 4
【解析】(1)氧化还原反应HO+SO 2- +2Fe3+=SO2- +2Fe2++2H+,水解反应Fe3++3H O Fe(OH) +3H+,
2 3 4 2 3
开始滴加FeCl 溶液立马变为红褐色,说明的Fe3+水解速率大于Fe3+与SO 2-的氧化还原反应速率,而活化能
3 3
越大,速率越小,因此活化能较大的是氧化还原反应;溶液最后呈浅绿色是因为水解反应的反应速率较
快,开始时Fe(OH) 胶体颜色占主导,一段时间后,随着氧化还原反应持续进行,水解平衡向左移动,溶
3
液呈现Fe2+颜色;(2)H SO H++HSO - K ,HSO - H++SO2- K ,第一步电离出的抑制了第
2 3 3 a1 3 3 a2
二步的电离,则K >K ,故曲线Ⅰ对应lg ,Ⅱ曲线对应lg ,B
a1 a2
点pH=1.9,lg =0,则 =1, =10-1.9mol/L,代入得K =10-1.9mol/L;HSO - H+
a1 3+SO2- K ,A点pH=5.9,lg =-1,c(H+)=10-5.9mol/L, = ,代入
3 a2
=10-6.9mol/L,又HSO -+H O OH-+SO2- K= = = = =10-
3 2 4 h
12.1,K >K,即HSO -的电离能力大于水解能力,NaHSO 溶液显酸性;(3)SO 2-放电失去电子得到SO 2-,
a2 h 3 3 3 4
电极反应式为SO 2- -2e-+H O=SO 2- +2H+,由图可知,再生后的吸收液pH≥8.9,时,即c(H+)≤10-8.9mol/L,
3 2 4
=10-6.9mol/L,当c(H+)最大时, 值最小,则代入c(H+)=10-8.9mol/L,得
=102=100;M室中:2HO+2e-=H ↑+2OH-,Na+经A膜(阳离子交换膜)进入M室生成NaOH,
2 2
NaOH再结合SO 生成NaSO 和NaHSO,根据物料守恒有:2c(Na+)=3[c(SO2-)+c(H SO -)+c(H SO )],当溶
2 2 3 3 3 3 2 3
液pH=8.9, =102=100, ,因此3×1.01c(SO 2-)≈2c(Na+),若有1mol Na+通
3
过离子交换膜,则 。