文档内容
专题验收评价
专题 05 金属及其重要化合物
内容概览
A·常考题不丢分
【考点一 金属及其重要化合物性质、用途】
【考点二 金属及其重要化合物与理论、实验的结合】
【微专题 无机化工流程题的解题策略】
B·综合素养拿高分/拓展培优拿高分
C·挑战真题争满分
【考点一 金属及其重要化合物性质、用途】
1.(2023·山东济宁·统考三模)下列有关物质性质的应用错误的是
A.苯甲酸钠可用作增味剂 B.碘酸钾可用作营养强化剂
C.NaH可用作野外生氢剂 D.NaOH和铝粉的混合物可用作管道疏通剂
2.(2023·浙江·校联考三模)物质的性质决定用途,下列说法不正确的是
A.碳化硅硬度大,可用作砂纸和砂轮的磨料
B.胆矾与水结合生成蓝色晶体,可用于定性检测酒精中是否含少量水
C.铝合金密度小、强度高,可用于制造飞机和宇宙飞船
D.锂盐焰色为紫红色,可用作烟花的成分
3.(2023·山东济南·山东师范大学附中校考模拟预测)下列性质或用途错误的是
A.钠钾合金—原子反应堆的导热剂 B.氯乙烷—可做冷胨麻醉剂C.冠醚—有机反应的催化剂 D.氧化亚铁—激光打印机的墨粉
4.(2023·河北秦皇岛·统考三模)如图为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系。
下列说法正确的是
A.a与水蒸气反应可转化为c
B.b是一种黑色粉末,不稳定,在空气中受热,迅速反应转化为c
C.e可以通过化合反应制得d
D.向g中加强碱溶液可制得胶体
5.(2023·上海松江·统考二模)下列各组物质的转化关系不能全部通过一步反应完成的是
A.Na→NaOH→Na CO→NaCl B.Fe→FeCl →Fe(OH) →Fe O
2 3 3 3 2 3
C.Al→Al O→Al(OH) →AlCl D.Mg→MgCl →Mg(OH) →MgSO
2 3 3 3 2 2 4
【考点二 金属及其重要化合物与理论、实验的结合】
1.(2023·吉林长春·统考一模)我国科学家研发出一种新型的锌碘单液流电池,其原理如图所示。设
为阿伏加德罗常数的值,下列说法错误的是
A.放电时,B电极反应式:
B.放电时,电解质储罐中离子总浓度增大
C.M为阳离子交换膜,N为阴离子交换膜D.充电时,A极增重32.5g时,C区增加的离子数为
2.(2023·四川南充·统考模拟预测)研究小组将混合均匀的铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图
1)。从胶头滴管中滴入一定浓度醋酸溶液,进行铁的电化学腐蚀实验,容器中的压强随时间的变化曲线如
图2。下列说法正确的是
A.0-t 时压强增大的原因可能是铁腐蚀放出热量
1
B.铁被氧化的电极反应式为:
C.碳粉上发生了氧化反应
D.铁腐蚀过程中化学能全部转化为电能
3.(2023·江西·校联考模拟预测)利用下列装置和试剂进行实验,能达到实验目的的是
A.用装置①进行钠的燃烧反应 B.用装置②制备溴苯并验证有HBr产生
C.用装置③制备无水MgCl D.用装置④在铁片上镀铜
2
4.(2023·江苏扬州·统考三模)用表面有油污的铁屑等原料可以制备 ,实验中的部分装置和
操作如下图所示,其中不能达到实验目的的是A.用装置甲去除铁屑表面的油污
B.用装置乙溶解铁屑制备
C.用装置丙吸收铁屑溶解过程中产生的
D.用装置丁蒸干溶液,获得
5.(2023·河南·校联考模拟预测)氯化铁是实验室中经常使用的物质,根据下列实验目的设计的实验方案
正确的是
选项 实验目的 实验方案
称量一定质量的氯化铁固体先溶于较浓的盐酸中,
A 实验室配制FeCl 溶液
3 再加入蒸馏水稀释至所需浓度
检验配制的FeCl 溶液中是 向酸性高锰酸钾溶液中滴入少量氯化铁溶液,观察
B 3
否含有Fe2+ 溶液颜色的变化
制备氢氧化铁胶体并鉴别氯 煮沸少许饱和氯化铁溶液一段时间后,采用丁达尔
C
化铁溶液与氢氧化铁胶体 现象鉴别所得物质和氯化铁溶液
向FeCl 溶液中先滴加一定量的NaF溶液,再滴加几
D 验证铁离子的氧化性 3
滴KSCN溶液,未出现红色
【微专题 无机化工流程题的解题策略】
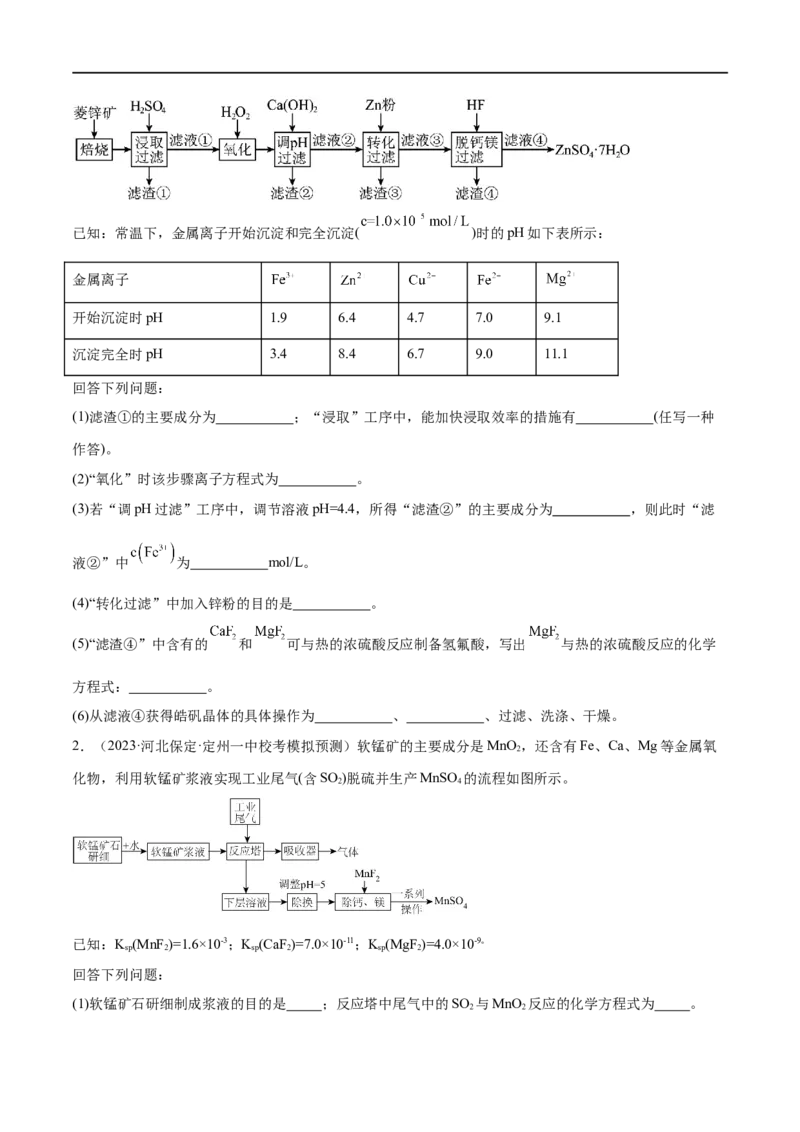
1.(2023·云南大理·统考模拟预测)皓矾( )主要用作制取颜料和其他含锌材料,在防腐、电
镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为 ,还含有少量 以及
Ca、Mg、Fe、Cu等的化合物)制备,制备流程图如图所示:已知:常温下,金属离子开始沉淀和完全沉淀( )时的pH如下表所示:
金属离子
开始沉淀时pH 1.9 6.4 4.7 7.0 9.1
沉淀完全时pH 3.4 8.4 6.7 9.0 11.1
回答下列问题:
(1)滤渣①的主要成分为 ;“浸取”工序中,能加快浸取效率的措施有 (任写一种
作答)。
(2)“氧化”时该步骤离子方程式为 。
(3)若“调pH过滤”工序中,调节溶液pH=4.4,所得“滤渣②”的主要成分为 ,则此时“滤
液②”中 为 mol/L。
(4)“转化过滤”中加入锌粉的目的是 。
(5)“滤渣④”中含有的 和 可与热的浓硫酸反应制备氢氟酸,写出 与热的浓硫酸反应的化学
方程式: 。
(6)从滤液④获得皓矾晶体的具体操作为 、 、过滤、洗涤、干燥。
2.(2023·河北保定·定州一中校考模拟预测)软锰矿的主要成分是MnO ,还含有Fe、Ca、Mg等金属氧
2
化物,利用软锰矿浆液实现工业尾气(含SO )脱硫并生产MnSO 的流程如图所示。
2 4
已知:K (MnF )=1.6×10-3;K (CaF )=7.0×10-11;K (MgF )=4.0×10-9。
sp 2 sp 2 sp 2
回答下列问题:
(1)软锰矿石研细制成浆液的目的是 ;反应塔中尾气中的SO 与MnO 反应的化学方程式为 。
2 2(2)①反应塔下层溶液中阳离子除了Mn2+外还含有Fe3+、Ca2+、Mg2+等杂质离子,也可能含有Fe2+,它们的
存在直接影响产品的质量,检验溶液中是否含有Fe2+的操作是 。
②调整溶液的pH=5除去Fe3+,调整溶液的pH可以选用下列试剂中的 (填标号)。
A.Mn(OH) B.氨水 C.烧碱 D.MnCO
2 3
③定量计算说明用MnF 可以除去Ca2+、Mg2+的原因: 。(当平衡常数大于105时,可认为反应完全)。
2
(3)如图实验测定pH和温度对Ca2+、Mg2+沉淀率的影响结果,根据图像实际生产时选择的最佳条件是 。
(4)生产中要用过硫酸钠(Na SO)溶液检测反应塔下层除杂后溶液中的MnSO 的浓度,检测过程中溶液变成
2 2 8 4
紫色,写出检测过程反应的离子方程式 ;检测时取10mL反应塔下层除杂后的溶液,用0.100mol·L-1
过硫酸钠溶液滴定三次,平均消耗过硫酸钠溶液18.60mL,则反应塔下层除杂后的溶液中MnSO 的浓度为
4
。
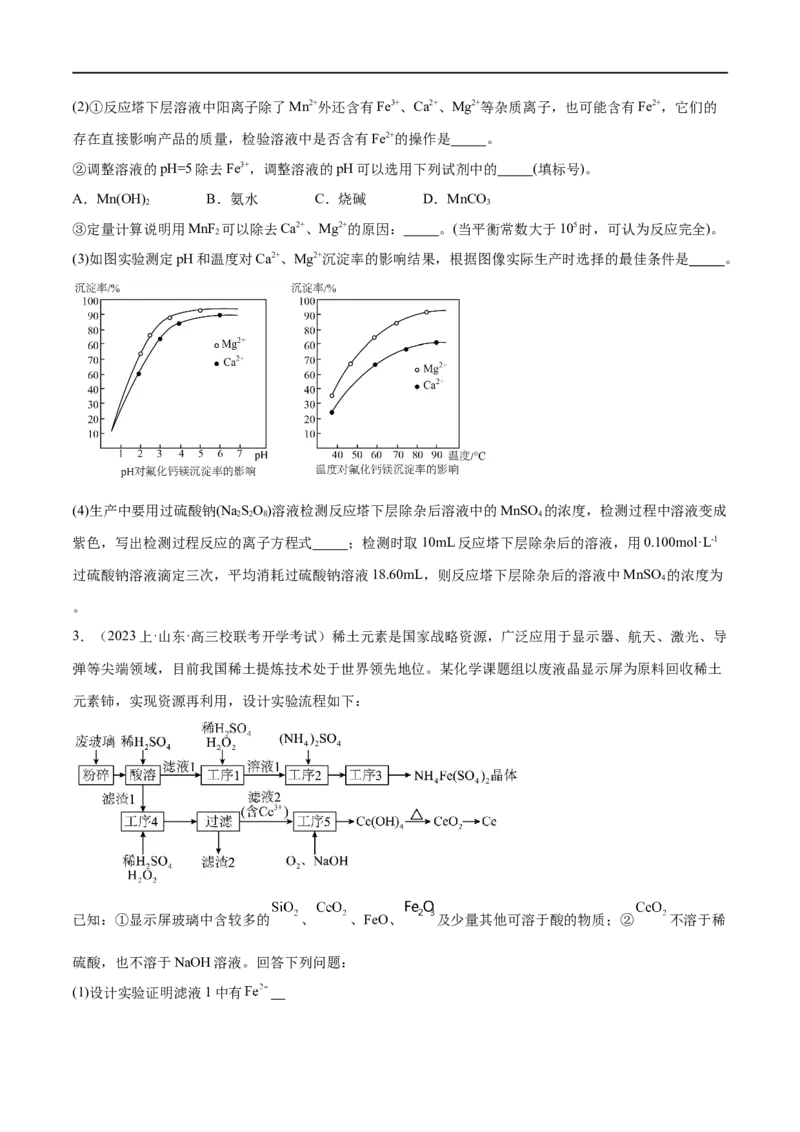
3.(2023上·山东·高三校联考开学考试)稀土元素是国家战略资源,广泛应用于显示器、航天、激光、导
弹等尖端领域,目前我国稀土提炼技术处于世界领先地位。某化学课题组以废液晶显示屏为原料回收稀土
元素铈,实现资源再利用,设计实验流程如下:
已知:①显示屏玻璃中含较多的 、 、FeO、 及少量其他可溶于酸的物质;② 不溶于稀
硫酸,也不溶于NaOH溶液。回答下列问题:
(1)设计实验证明滤液1中有(2)已知 溶液可以和难溶于水的FeO(OH)反应生成 ,书写该反应的离子反应方程式 。
(3)工序1中加入 的作用是 ;工序4中加入稀硫酸和 的作用是 ;滤渣2的主要成
分是 。
(4)工序3是蒸发浓缩、 、过滤、洗涤、常温晾干。
(5)工序5中发生反应的离子方程式 。
(6)硫酸铁铵可用作净水剂,但在除酸性废水中悬浮物时效果较差,原因是 。
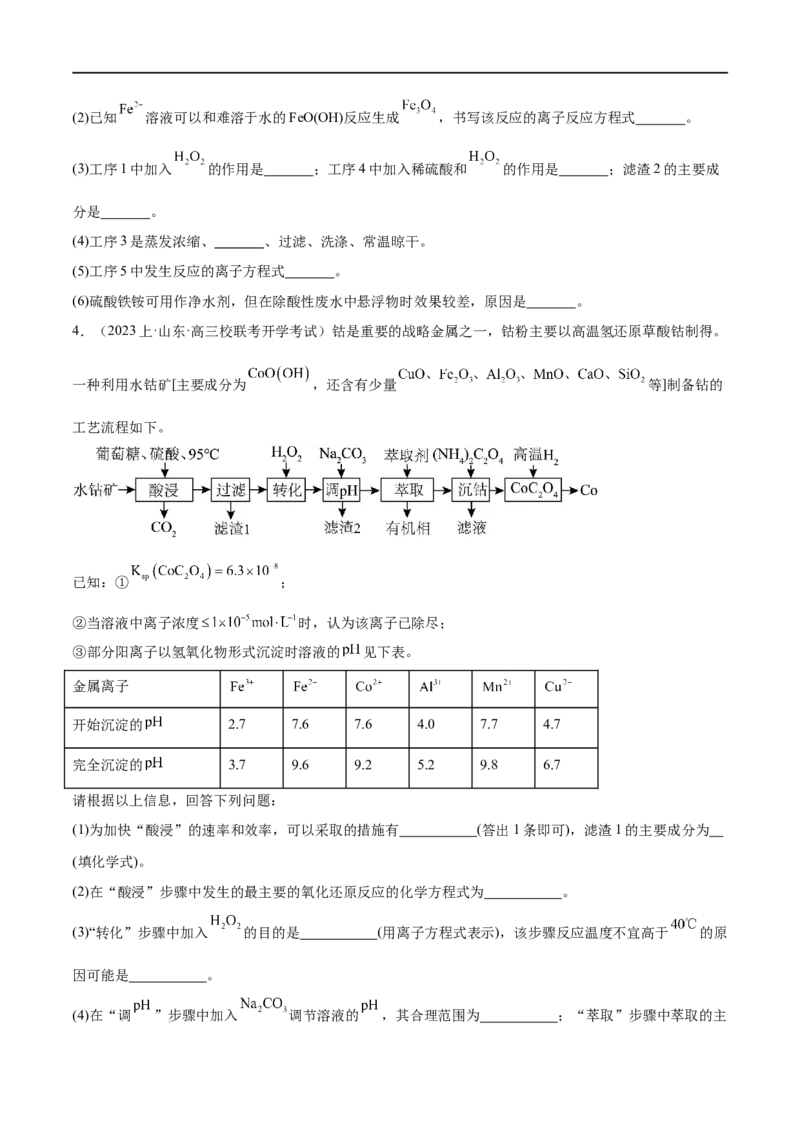
4.(2023上·山东·高三校联考开学考试)钴是重要的战略金属之一,钴粉主要以高温氢还原草酸钴制得。
一种利用水钴矿[主要成分为 ,还含有少量 等]制备钻的
工艺流程如下。
已知:① ;
②当溶液中离子浓度 时,认为该离子已除尽;
③部分阳离子以氢氧化物形式沉淀时溶液的 见下表。
金属离子
开始沉淀的 2.7 7.6 7.6 4.0 7.7 4.7
完全沉淀的 3.7 9.6 9.2 5.2 9.8 6.7
请根据以上信息,回答下列问题:
(1)为加快“酸浸”的速率和效率,可以采取的措施有 (答出1条即可),滤渣1的主要成分为
(填化学式)。
(2)在“酸浸”步骤中发生的最主要的氧化还原反应的化学方程式为 。
(3)“转化”步骤中加入 的目的是 (用离子方程式表示),该步骤反应温度不宜高于 的原
因可能是 。
(4)在“调 ”步骤中加入 调节溶液的 ,其合理范围为 ;“萃取”步骤中萃取的主要离子是 (填离子符号)。
(5)在“沉钴”步骤中为使溶液中的钻沉淀完全,混合溶液中 的最小浓度为
。
1.(2023·浙江宁波·镇海中学校考模拟预测)物质的性质决定用途,下列两者对应关系不正确的是
A. 具有强氧化性,可用作消毒剂
B. 固体具有氧化性,可作为黑火药的原料之一
C.SiC中存在共价键,硬度大,可做砂纸和砂轮等磨料
D. 溶液呈蓝色,胆矾可以与石灰乳混合制备波尔多液
2.(2023·浙江·校联考三模)下列关于物质性质与用途的说法不正确的是
A.镁在空气中可燃烧,生成氧化镁和氮化镁
B.铝与浓硝酸不反应,可用铝槽运输浓硝酸
C.铁粉具有还原性,可作食品盒中的除氧剂
D.二氧化硅导光能力强,可用来制备光导纤维
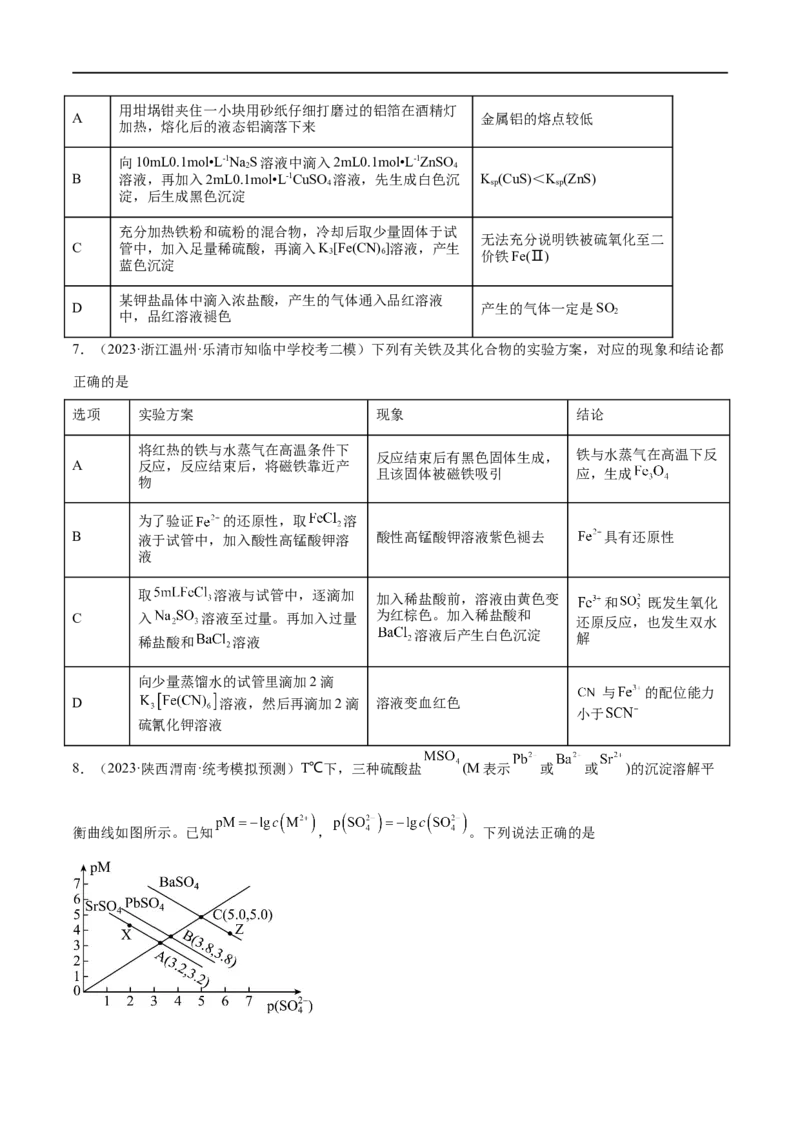
3.(2023·上海金山·统考二模)明代《徐光启手迹》中记载了硝酸的制备方法,其主要物质转化流程如图
所示。下列说法正确的是
A.X为SO
2
B.现代工业用稀硫酸吸收SO
3
C.上述转化流程涉及分解、化合和置换反应
D.制取HNO 是利用了强酸制弱酸的反应原理
3
4.(2023·江苏镇江·江苏省镇江第一中学校考一模)氯及其化合物应用广泛。氯的单质Cl 可由MnO 与浓
2 2
盐酸共热得到,Cl 能氧化Br-,可从海水中提取Br ;氯的氧化物ClO 可用于自来水消毒,ClO 是一种黄
2 2 2 2绿色气体,易溶于水,与碱反应会生成ClO 与ClO ,在稀硫酸和NaClO 的混合溶液中通入SO 气体可制
3 2
得ClO ;漂白液和漂白粉的有效成分是次氯酸盐,可作棉、麻的漂白剂。下列含氯物质的转化正确的是
2
A.漂白粉 HClO(aq) Cl(g)
2
B.MgCl (aq) 无水MgCl Mg
2 2
C.NaCl(aq) Cl(g) FeC1
2 3
D.NaCl(aq) NaHCO (aq) NaCO(s)
3 2 3
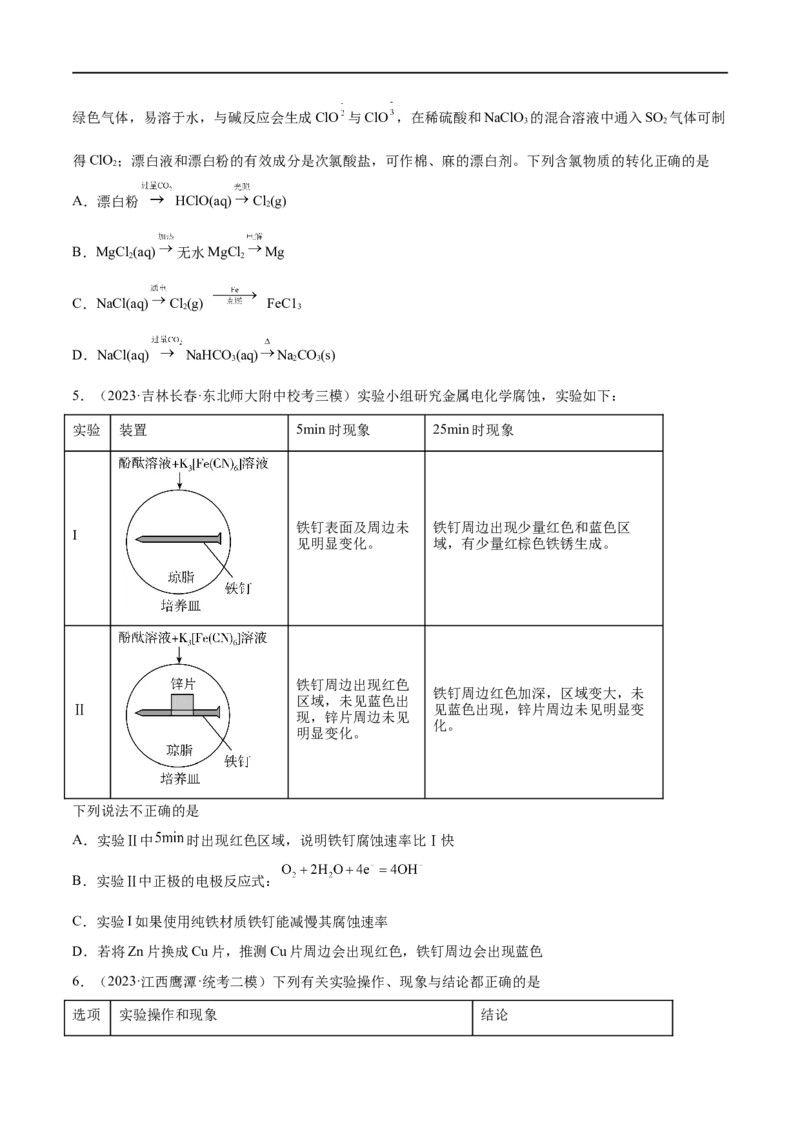
5.(2023·吉林长春·东北师大附中校考三模)实验小组研究金属电化学腐蚀,实验如下:
实验 装置 5min时现象 25min时现象
铁钉表面及周边未 铁钉周边出现少量红色和蓝色区
I
见明显变化。 域,有少量红棕色铁锈生成。
铁钉周边出现红色
铁钉周边红色加深,区域变大,未
区域,未见蓝色出
Ⅱ 见蓝色出现,锌片周边未见明显变
现,锌片周边未见
化。
明显变化。
下列说法不正确的是
A.实验Ⅱ中 时出现红色区域,说明铁钉腐蚀速率比Ⅰ快
B.实验Ⅱ中正极的电极反应式:
C.实验I如果使用纯铁材质铁钉能减慢其腐蚀速率
D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色
6.(2023·江西鹰潭·统考二模)下列有关实验操作、现象与结论都正确的是
选项 实验操作和现象 结论用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯
A 金属铝的熔点较低
加热,熔化后的液态铝滴落下来
向10mL0.1mol•L-1NaS溶液中滴入2mL0.1mol•L-1ZnSO
2 4
B 溶液,再加入2mL0.1mol•L-1CuSO 溶液,先生成白色沉 K (CuS)<K (ZnS)
4 sp sp
淀,后生成黑色沉淀
充分加热铁粉和硫粉的混合物,冷却后取少量固体于试
无法充分说明铁被硫氧化至二
C 管中,加入足量稀硫酸,再滴入K[Fe(CN) ]溶液,产生
3 6 价铁Fe(Ⅱ)
蓝色沉淀
某钾盐晶体中滴入浓盐酸,产生的气体通入品红溶液
D 产生的气体一定是SO
中,品红溶液褪色 2
7.(2023·浙江温州·乐清市知临中学校考二模)下列有关铁及其化合物的实验方案,对应的现象和结论都
正确的是
选项 实验方案 现象 结论
将红热的铁与水蒸气在高温条件下
反应结束后有黑色固体生成, 铁与水蒸气在高温下反
A 反应,反应结束后,将磁铁靠近产
且该固体被磁铁吸引 应,生成
物
为了验证 的还原性,取 溶
B 液于试管中,加入酸性高锰酸钾溶 酸性高锰酸钾溶液紫色褪去 具有还原性
液
取 溶液与试管中,逐滴加 加入稀盐酸前,溶液由黄色变 和 既发生氧化
C 入 溶液至过量。再加入过量 为红棕色。加入稀盐酸和 还原反应,也发生双水
稀盐酸和 溶液 溶液后产生白色沉淀 解
向少量蒸馏水的试管里滴加2滴
与 的配位能力
D 溶液,然后再滴加2滴 溶液变血红色
小于
硫氰化钾溶液
8.(2023·陕西渭南·统考模拟预测)T℃下,三种硫酸盐 (M表示 或 或 )的沉淀溶解平
衡曲线如图所示。已知 , 。下列说法正确的是A. 在任何条件下都不可能转化为
B.X点和Z点分别是 和 的饱和溶液,对应的溶液中
C.T℃下,反应 的平衡常数为
D.T℃时,用 溶液滴定 浓度均为 和 的混合溶液,
先沉淀
9.(2023·河北·张家口市宣化第一中学校联考二模)电池正极片由镍钴锰酸锂 正极材
料和铝片组成,以其为原料回收各金属工艺流程如下:
回答下列问题:
(1)滤液1中含铝微粒为 。
(2)“碱浸”后需进行过滤、洗涤,简述洗涤的操作过程: 。
(3)“还原”时,参加反应的 。
(4)“分离”过程包含萃取和反萃取,萃取时必须使用的仪器是 ;萃取时利用有机物HT将Co2+
从水溶液中萃取出来,该过程可表示为Co2+(水层)+2HT(有机层) CoT (有机层)+2H+(水层)。向CoT (有
2 2
机层)中加入稀硫酸能获得较纯的含Co2+的水溶液,从平衡角度解释其原因: 。
(5)“氧化”过程中MnSO 发生反应生成MnO 、(NH )SO 和HSO 的化学方程式为 。
4 2 4 2 4 2 4
(6)“沉钴”后获得CoC O·2H O,取mgCoC O·2H O进行“高温分解”,测得固体的失重率(
2 4 2 2 4 2
)与温度的关系曲线如图所示。写出加热到160℃时反应的化学方程式:
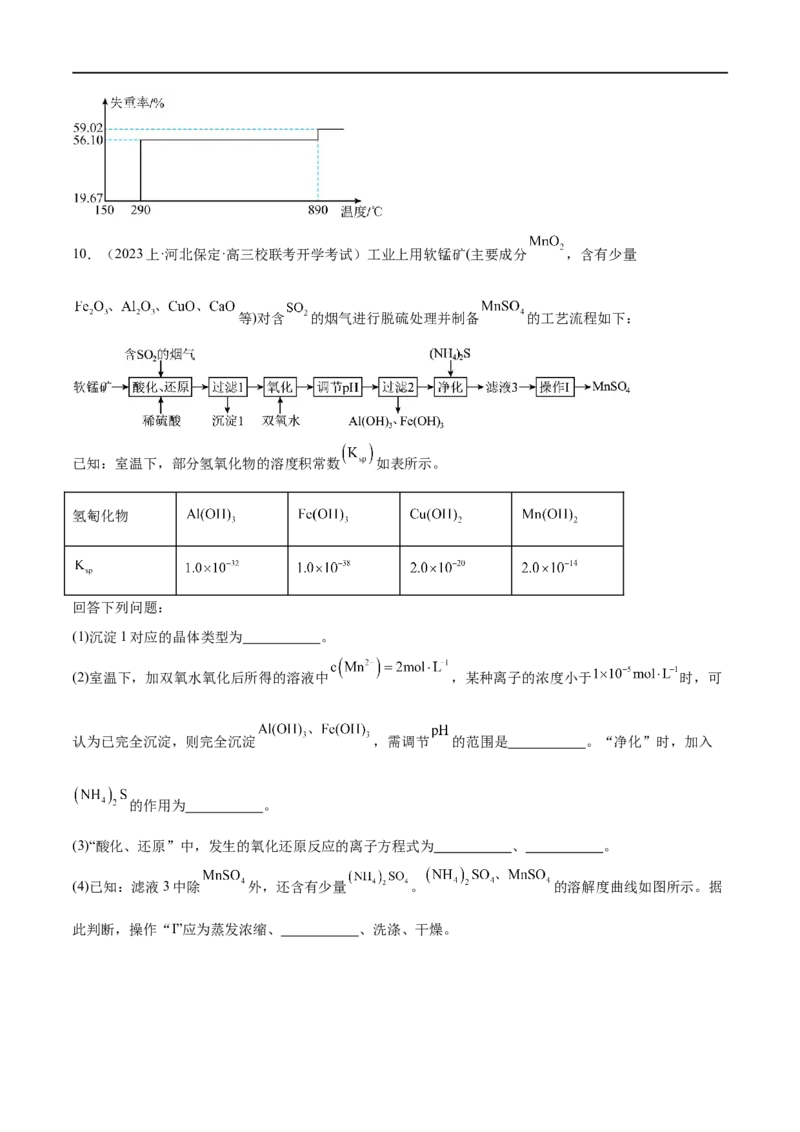
;“高温分解”需控制的最低温度为 。10.(2023上·河北保定·高三校联考开学考试)工业上用软锰矿(主要成分 ,含有少量
等)对含 的烟气进行脱硫处理并制备 的工艺流程如下:
已知:室温下,部分氢氧化物的溶度积常数 如表所示。
氢匎化物
回答下列问题:
(1)沉淀1对应的晶体类型为 。
(2)室温下,加双氧水氧化后所得的溶液中 ,某种离子的浓度小于 时,可
认为已完全沉淀,则完全沉淀 ,需调节 的范围是 。“净化”时,加入
的作用为 。
(3)“酸化、还原”中,发生的氧化还原反应的离子方程式为 、 。
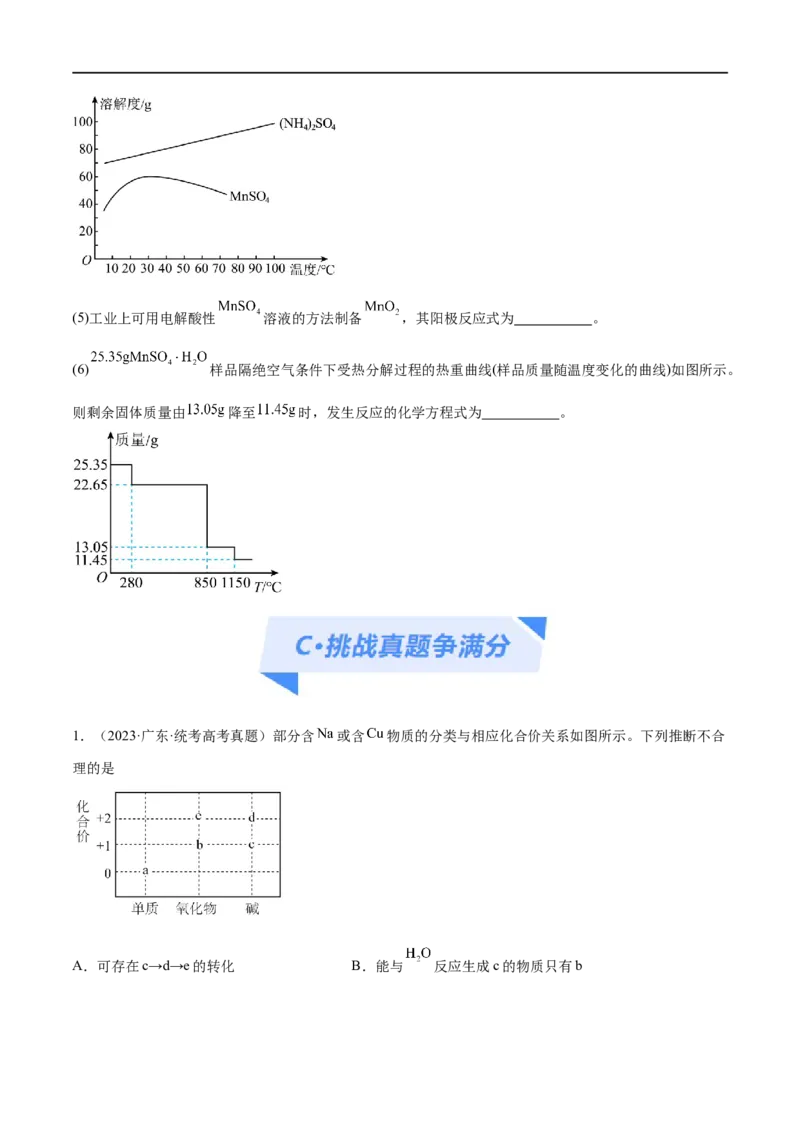
(4)已知:滤液3中除 外,还含有少量 。 的溶解度曲线如图所示。据
此判断,操作“I”应为蒸发浓缩、 、洗涤、干燥。(5)工业上可用电解酸性 溶液的方法制备 ,其阳极反应式为 。
(6) 样品隔绝空气条件下受热分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。
则剩余固体质量由 降至 时,发生反应的化学方程式为 。
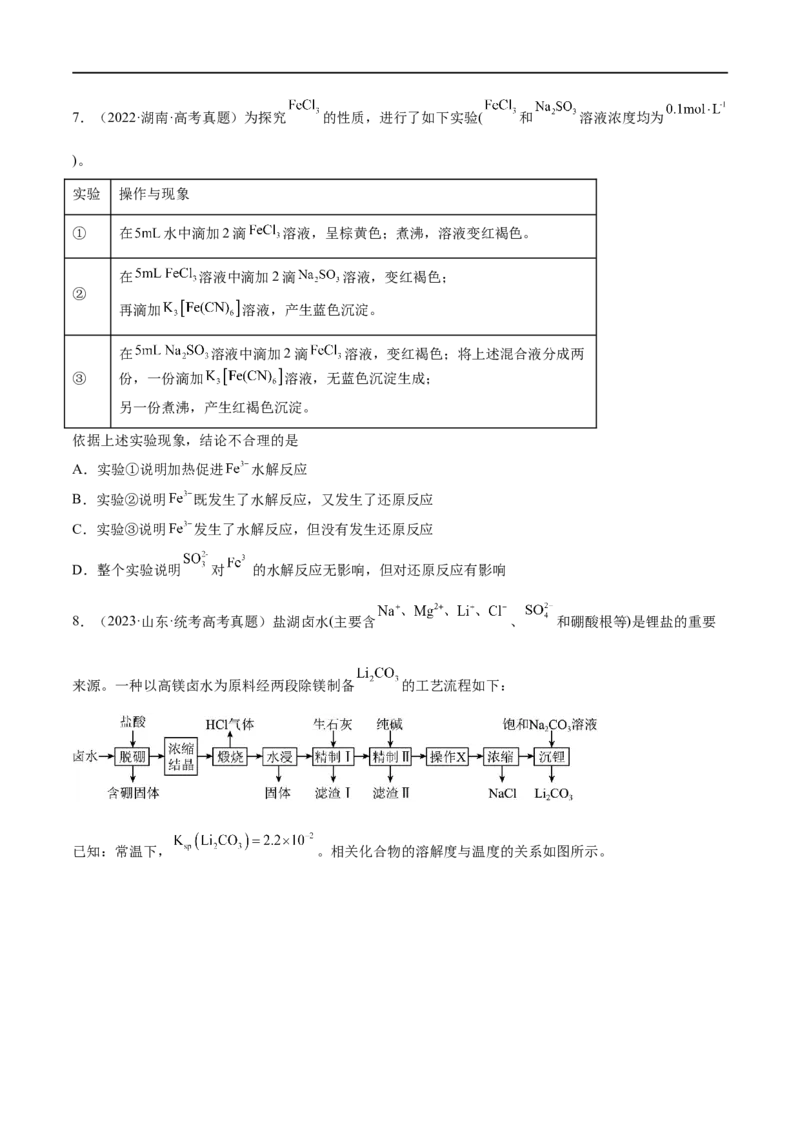
1.(2023·广东·统考高考真题)部分含 或含 物质的分类与相应化合价关系如图所示。下列推断不合
理的是
A.可存在c→d→e的转化 B.能与 反应生成c的物质只有bC.新制的d可用于检验葡萄糖中的醛基 D.若b能与 反应生成 ,则b中含共价键
2.(2023·浙江·高考真题)物质的性质决定用途,下列两者对应关系不正确的是
A. 能使某些色素褪色,可用作漂白剂 B.金属钠导热性好,可用作传热介质
C. 溶液呈碱性,可用作消毒剂 D. 呈红色,可用作颜料
3.(2022·浙江·统考高考真题)下列说法不正确的是
A.镁合金密度较小、强度较大,可用于制造飞机部件
B.还原铁粉可用作食品干燥剂
C.氯气、臭氧、二氧化氯都可用于饮用水的消毒
D.油脂是热值最高的营养物质
4.(2021·河北·统考高考真题)“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在其
《本草经集注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混
合加热,生铁熔化灌入熟铁,再锻打成钢。下列说法错误的是
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe O
2 3
5.(2021·浙江·高考真题)下列说法不正确的是
A.硅酸钠是一种难溶于水的硅酸盐 B.镁在空气中燃烧可生成氧化镁和氮化镁
C.钠与水反应生成氢氧化钠和氢气 D.常温下,铝遇浓硝酸或浓硫酸时会发生钝化
6.(2023·重庆·统考高考真题)下列实验操作和现象,得出的相应结论正确的是
选项 实验操作 现象 结论
向盛有 和 的试 盛 的试管中产生 氧化性:
A
管中分别滴加浓盐酸 黄绿色气体
B 向 溶液中通入 气体 出现黑色沉淀(CuS) 酸性:
乙醇和浓硫酸共热至 ,将产
C 溴水褪色 乙烯发生了加成反应
生的气体通入溴水中
向 溶液中滴加 溶
D 出现黄色沉淀 发生了水解反应
液7.(2022·湖南·高考真题)为探究 的性质,进行了如下实验( 和 溶液浓度均为
)。
实验 操作与现象
① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;
②
再滴加 溶液,产生蓝色沉淀。
在 溶液中滴加2滴 溶液,变红褐色;将上述混合液分成两
③ 份,一份滴加 溶液,无蓝色沉淀生成;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是
A.实验①说明加热促进 水解反应
B.实验②说明 既发生了水解反应,又发生了还原反应
C.实验③说明 发生了水解反应,但没有发生还原反应
D.整个实验说明 对 的水解反应无影响,但对还原反应有影响
8.(2023·山东·统考高考真题)盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要
来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如下:
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下, );
与 溶液反应可制备硼砂 。常温下,在 硼砂溶液中,
水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为 ,该溶
液 。
(2)滤渣Ⅰ的主要成分是 (填化学式);精制Ⅰ后溶液中 的浓度为 ,则常温下精制Ⅱ过程中
浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加 的
用量(填化学式)。
(3)精制Ⅱ的目的是 ;进行操作 时应选择的试剂是 ,若不进行该操作而直接浓缩,将导致
。
9.(2023·浙江·高考真题)某研究小组制备纳米 ,再与金属有机框架 )材料复合制备荧光材料
,流程如下:
已知:①含
锌组分间的转化关系:
② 是 的一种晶型, 以下稳定。
请回答:
(1)步骤Ⅰ,初始滴入 溶液时,体系中主要含锌组分的化学式是 。(2)下列有关说法不正确的是___________。
A.步骤Ⅰ,搅拌的作用是避免反应物浓度局部过高,使反应充分
B.步骤Ⅰ,若将过量 溶液滴入 溶液制备 ,可提高 的利用率
C.步骤Ⅱ,为了更好地除去杂质,可用 的热水洗涤
D.步骤Ⅲ,控温煅烧的目的是为了控制 的颗粒大小
(3)步骤Ⅲ,盛放样品的容器名称是 。
(4)用 和过量 反应,得到的沉淀可直接控温煅烧得纳米 ,沉淀无需洗涤的原
因是 。
(5)为测定纳米 产品的纯度,可用已知浓度的 标准溶液滴定 。从下列选项中选择合理的仪
器和操作,补全如下步骤[“___________”上填写一件最关键仪器,“(___________)”内填写一种操作,均用
字母表示]。
用___________(称量 样品 )→用烧杯(___________)→用___________(___________)→用移液管
(___________)→用滴定管(盛装 标准溶液,滴定 )
仪器:a、烧杯;b、托盘天平;c、容量瓶;d、分析天平;e、试剂瓶
操作:f、配制一定体积的Zn2+溶液;g、酸溶样品;h、量取一定体积的 溶液;i、装瓶贴标签
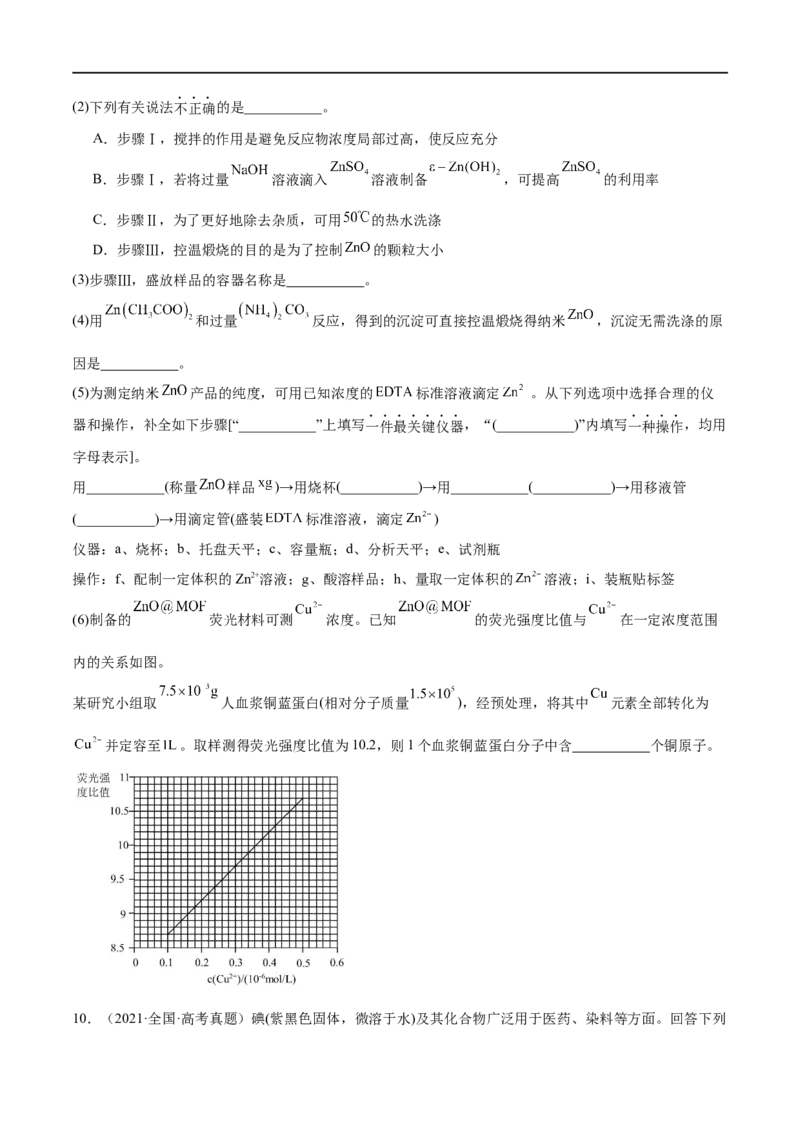
(6)制备的 荧光材料可测 浓度。已知 的荧光强度比值与 在一定浓度范围
内的关系如图。
某研究小组取 人血浆铜蓝蛋白(相对分子质量 ),经预处理,将其中 元素全部转化为
并定容至 。取样测得荧光强度比值为10.2,则1个血浆铜蓝蛋白分子中含 个铜原子。
10.(2021·全国·高考真题)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为 ,生成的沉淀与硝酸反应,生成 后可循环使用。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为 ;若反应物用量比
时,氧化产物为 ;当 ,单质碘的收率会降低,原因是
。
(2)以 为原料制备 的方法是:先向 溶液中加入过量的 ,生成碘化物;再向混合溶液
中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为 。
(3) 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少为 。 在
溶液中可发生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水蒸气蒸馏
可制得高纯碘。反应中加入过量 的原因是 。
11.(2022·全国·统考高考真题)废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。还有少量
Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
(1)在“脱硫”中 转化反应的离子方程式为 ,用沉淀溶解平衡原理解释选择 的原因
。
(2)在“脱硫”中,加入 不能使铅膏中 完全转化,原因是 。
(3)在“酸浸”中,除加入醋酸( ),还要加入 。
(ⅰ)能被 氧化的离子是 ;
(ⅱ) 促进了金属Pb在醋酸中转化为 ,其化学方程式为 ;
(ⅲ) 也能使 转化为 , 的作用是 。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是 。
(5)“沉铅”的滤液中,金属离子有 。
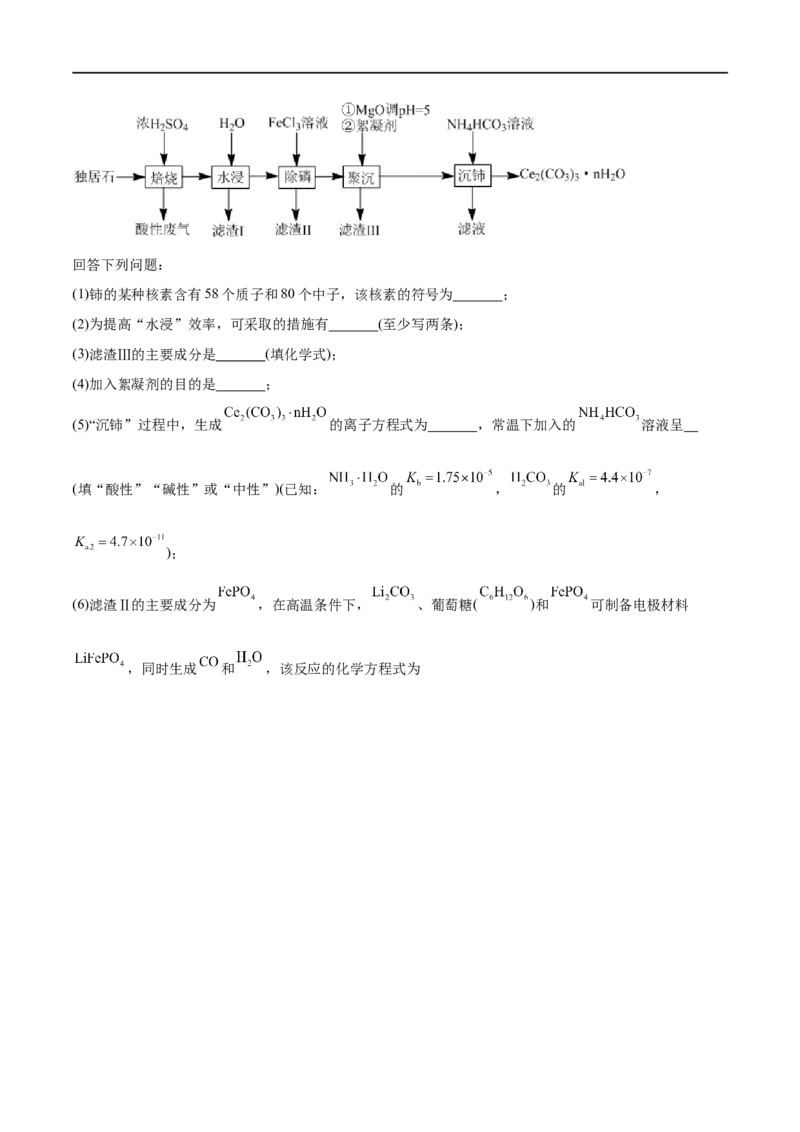
12.(2021·湖南·统考高考真题) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)
主要以 形式存在,还含有 、 、 、 等物质。以独居石为原料制备
的工艺流程如下:回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为 ;
(2)为提高“水浸”效率,可采取的措施有 (至少写两条);
(3)滤渣Ⅲ的主要成分是 (填化学式);
(4)加入絮凝剂的目的是 ;
(5)“沉铈”过程中,生成 的离子方程式为 ,常温下加入的 溶液呈
(填“酸性”“碱性”或“中性”)(已知: 的 , 的 ,
);
(6)滤渣Ⅱ的主要成分为 ,在高温条件下, 、葡萄糖( )和 可制备电极材料
,同时生成 和 ,该反应的化学方程式为