文档内容
专题 05 化学反应与能量
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.某化学反应A(g)+B (g)=2AB(g)的能量变化如图所示,则下列说法中正确的是( )
2 2
A.该反应为放热反应,无需加热就可以发生
B.断裂1molA-A键和1molB-B键要吸收xkJ的能量
C.根据图示可知生成1molAB (g)放出 的能量
D.三种物质A(g)、B (g)、AB(g)中,最稳定的物质一定是AB(g)
2 2
【答案】B
【解析】A项,由图可知反应物总能量高于生成物能量为放热反应,但A-A键和B-B键断裂需要吸收
能量,可能需要加热破坏反应物化学键以发生反应,反应放热与反应是否需要加热无关,选项A错误;B
项,断裂1moLA-A键和1molB-B键要吸收xkJ的能量,选项B正确;C项,根据图示可知生成1mol AB
(g)放出 的能量,选项C错误;D项,物质能量越低越稳定,由图知A(g)和B (g)的总能量高
2 2
于2 AB (g)的能量,但不知单独物质的能量大小,所以无法确定谁最稳定,选项D错误;故选B。
2.(2024·江苏无锡高三教学质量调研测试)1mol液态肼完全燃烧生成N 气体和液态水放出577kJ的热
2
量。工业上利用NH 和CO 制取尿素[CO(NH)],尿素在高温条件下可将汽车尾气中的NO 转化为无毒气
3 2 2 2 x
体N。下列化学反应表示正确的是( )
2
A.NH 燃烧的热化学方程式:NH(l)+O (g)=N(g)+2HO(g) ΔH=-577 kJ·mol-1
2 4 2 4 2 2 2
B.碱性NH 燃料电池负极发生的电极反应式:NH+4e- +4OH-=N ↑+4H O
2 4 2 4 2 2
C.NaClO氧化氨气制取NH 的离子方程式:2NH +ClO-=N H+Cl-+H O
2 4 3 2 4 2
D.NH 与NO 高温下反应的化学方程式:NH+NO N↑+2HO
2 4 2 2 4 2 2 2
【答案】C
【解析】A项,1mol液态肼完全燃烧生成N 气体和液态水放出577kJ的热量,则NH 燃烧的热化学
2 2 4
方程式为:NH(l)+O (g)=N(g)+2HO(l) ΔH=-577 kJ·mol-1,故A错误;B项,负极失电子,负极反应
2 4 2 2 2为:NH-4e- +4OH-=N ↑+4H O,故B错误;C项,NaClO氧化氨气制取NH,1molNaClO得2mol电子,
2 4 2 2 2 4
1mol氨气失1mol电子,根据得失电子守恒得离子方程式:2NH +ClO-=N H+Cl-+H O,故C正确;D项,
3 2 4 2
1mol NH 失去4mol电子生成氮气,1mol二氧化氮得4mol电子生成氮气,根据得失电子守恒得反应方程
2 4
式:2NH+2NO 3N↑+4HO,故D错误;故选C。
2 4 2 2 2
3.(2024·河北迁安市高三期中)下列装置能达到实验目的是( )
A.用图Ⅰ所示装置测定55mL1mol/L盐酸与50mL11mol/LNaOH溶液发生中和反应的反应热
B.为探究铁制品生锈,用图Ⅱ所示装置,正极材料是铁
C.图Ⅲ所示装置实现Ag+2HCl=2AgC1↓+H ↑
2
D.图Ⅳ装置可实现粗铜的精炼
【答案】C
【解析】A项,该实验装置没有玻璃搅拌器,碎纸条没有充满这个大烧杯,散热较多,不能用来测定
55mL1mol/L盐酸与50mL11mol/LNaOH溶液发生中和反应的反应热,故A错误;B项,为探究铁制品生
锈,用图Ⅱ所示装置,正极材料是C,负极材料是Fe,故B错误;C项,图Ⅲ中阳极为Ag电极,电极方
程式为:Ag-e-+Cl-=AgCl↓,阴极为C电极,电极方程式为:2H++2e-=H ↑,总反应为:
2
Ag+2HCl=2AgC1↓+H ↑,故C正确;D项,铜的电解精炼装置中粗铜应该为阳极,连接电源的正极,故D
2
错误;故选C。
4.(2023·辽宁省名校联盟高考模拟调研卷)“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷
的温室效应率是CO 的84倍。已知管道接口处有钢铁材料等,海水的pH约为8.0。设N 为阿伏伽德罗常
2 A
数的值。下列有关叙述不正确的是( )
A.损坏的钢铁材料在海水中主要发生吸氧腐蚀
B.制造管道时表面涂层能起到抗腐蚀作用
C.w g铁在海水中完全发生电化学腐蚀时转移电子数一定为D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法
【答案】C
【解析】A项,钢铁在弱碱性环境中主要发生吸氧腐蚀,A项正确;B项,表面涂层能防止钢铁管道
和水、O 等物质接触,从而起到抗腐蚀作用,B项正确;C项,钢铁腐蚀时负极电极反应式为Fe-2e-
2
=Fe2+,w g铁在海水中完全发生电化学腐蚀时转移电子数为 ,后续发生
,不属于电化学腐蚀,C项错误;D项,锌比铁活泼,在海水中构成原
电池,锌为负极,铁为正极,这种保护钢铁的方法叫牺牲阳极法,D项正确。故选C。
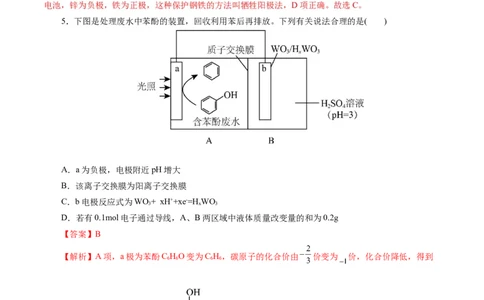
5.下图是处理废水中苯酚的装置,回收利用苯后再排放。下列有关说法合理的是( )
A.a为负极,电极附近pH增大
B.该离子交换膜为阳离子交换膜
C.b电极反应式为WO+ xH++xe-=H WO
3 x 3
D.若有0.1mol电子通过导线,A、B两区域中液体质量改变量的和为0.2g
【答案】B
【解析】A项,a极为苯酚C HO变为C H,碳原子的化合价由 价变为 价,化合价降低,得到
6 6 6 6
电子,a极为正极,电极反应式为: ,电极附近pH增大,A错
误;B项,自由移动的离子为H+,阳离子向正极移动,则离子交换膜为阳离子交换膜,从右向左移动,B
项正确;C项,b电极为负极,失电子发生氧化反应,电极反应式为:HWO-xe-= WO + xH+,C项错误;
x 3 3
D项,若有0.1mol电子通过导线,就有0.1molH+从B迁移到A,A区溶液质量增加0.1g,B区溶液的质量
不变,A、B两区域中液体质量改变量的和为0.1g,D项错误;故选B。
6.(2023·浙江省温州市高三第三次模拟适应性考试)标准状态下,气态反应物、生成物及活化分子[A(B)表示“A+B→产物”的活化分子]的相对能量如表所示:
物质 NO(g) NO (g) SO (g) SO (g) O(g) O(g) NO(O) SO (O )
2 2 3 2 3 3 2 3
相对能量/ 91.3 33.2 -296.8 -395.7 0 142.7 237.2 -96.1
下列说法不正确的是( )
A.NO (g)+SO (g) NO (g)+ SO (g) ΔH=-40.8 kJ·mol-1
2 2 3
B.3O(g) 2O(g)反应不能自发进行
2 3
C.相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率快
2 3 2 3 3 2 2
D.1mol NO (g)的总键能大于1mol NO(g)总键能
2
【答案】C
【解析】A项,NO (g)+SO(g) NO (g)+ SO (g) ΔH=生成物总能量-反应物总能量=91.3kJ/mol+
2 2 3
(-395.7kJ/mol)-[33.2kJ/mol+(-296.8kJ/mol)]=-40.8kJ/mol,故A正确;B项,3O(g) 2O(g) H=生成物
2 3
总能量-反应物总能量=+285.4kJ/mol>0,且 S<0,则任何温度下 H-T S>0,即反应3O(g)
2
2O(g)不能自发进行,故B正确;C项,反应SO (g)+O(g) O (g)+ SO (g)的活化能=活化分子能量-
3 2 3 2 3
反应物总能量=-96.1kJ/mol-(-296.8kJ/mol+142.7kJ/mol)=58kJ/mol,反应NO (g)+O(g) O (g)+ NO (g)
3 2 2
的活化能为237.2kJ/mol-(91.3kJ/mol+142.7kJ/mol)=3.2kJ/mol<58kJ/mol,反应的活化能越高,反应速率越
慢,则相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率慢,故C
2 3 2 3 3 2 2
错误;D项,反应2NO (g)+O(g) 2NO (g)ΔH=生成物总能量-反应物总能
2 2
量=2×33.2kJ/mol-2×91.3kJ/mol-0kJ/mol=-116.2kJ/mol,为放热反应,焓变△H=反应物总键能-生成物总键
能,则该反应反应物总键能<生成物总键能,即1molNO(g)和0.5molO 总键能<1molNO (g)的总键能,所
2 2
以1molNO (g)的总键能大于1molNO(g)总键能,故D正确;故选C。
2
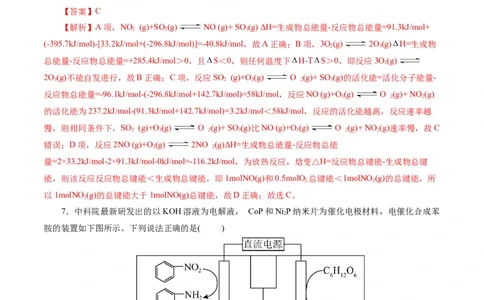
7.中科院最新研发出的以KOH溶液为电解液, CoP和Ni P纳米片为催化电极材料,电催化合成苯
2
胺的装置如下图所示。下列说法正确的是( )
A.阳极区溶液的pH不断增大
B.若用铅蓄电池作为电源,Ni P 极应连接铅蓄电池的Pb极
2
C.CoP极的电极反应式为C HNO + 6e- + 4H O = C HNH + 6OH-
6 5 2 2 6 5 2
D.电解液可换成稀硫酸溶液【答案】C
【解析】Ni P电极C H O 变为CO2-发生了氧化反应,在电解池的阳极,该极与电源的正极相连。而
2 6 12 6 3
CoP这一极为阴极,与电源的负极相连。阴极的反应为C HNO + 6e- + 4H O = C HNH + 6OH-,阳极反应
6 5 2 2 6 5 2
为C H O- 24e- + 36OH-=6CO 2-+24H O。A项,根据电极反应阳极区消耗OH-导致pH降低,A项错误;B
6 12 6 3 2
项,铅蓄电池的Pb为负极应该与CoP相连,B项错误;C项,已知分析,电极反应为C HNO + 6e- + 4H O
6 5 2 2
= C HNH + 6OH-,C项正确;D项,电解质换成稀硫酸两电极的反应发生变化,阴极无法产生 OH-而阳极
6 5 2
也无法产生CO2-,D项错误;故选C。
3
8.过硫酸铵[(NH )SO]可用作氧化剂、漂白剂。利用电解法在两极分别生产过硫酸铵和过氧化氢的
4 2 2 8
装置如图所示。下列说法错误的是( )
A.a为外接电源的负极
B.电解总反应:O+2H++2SO2- HO+S O2-
2 4 2 2 2 8
C.阴离子交换膜可用阳离子交换膜替代
D.电解池工作时,I室溶液质量理论上逐渐减小
【答案】C
【解析】S元素化合价由+6价升高为+7价,化合价升高被氧化,故右侧Pt电极为阳极,b为外接电
源正极,a为外接电源负极,左侧Pt电极为阴极。A项,a为外接电源的负极,A正确;B项,阴极氧气被
还原,阳极硫酸根被氧化,电解总反应正确,B正确;C项,根据阳极产物可知,反应需要消耗硫酸根,
阴离子交换膜不可用阳离子交换膜替代,C错误;D项,电解池工作时,I室溶液中氢离子移向阴极,硫酸
根移向阳极,消耗硫酸,I室溶液质量理论上逐渐减小,D正确;故选C。
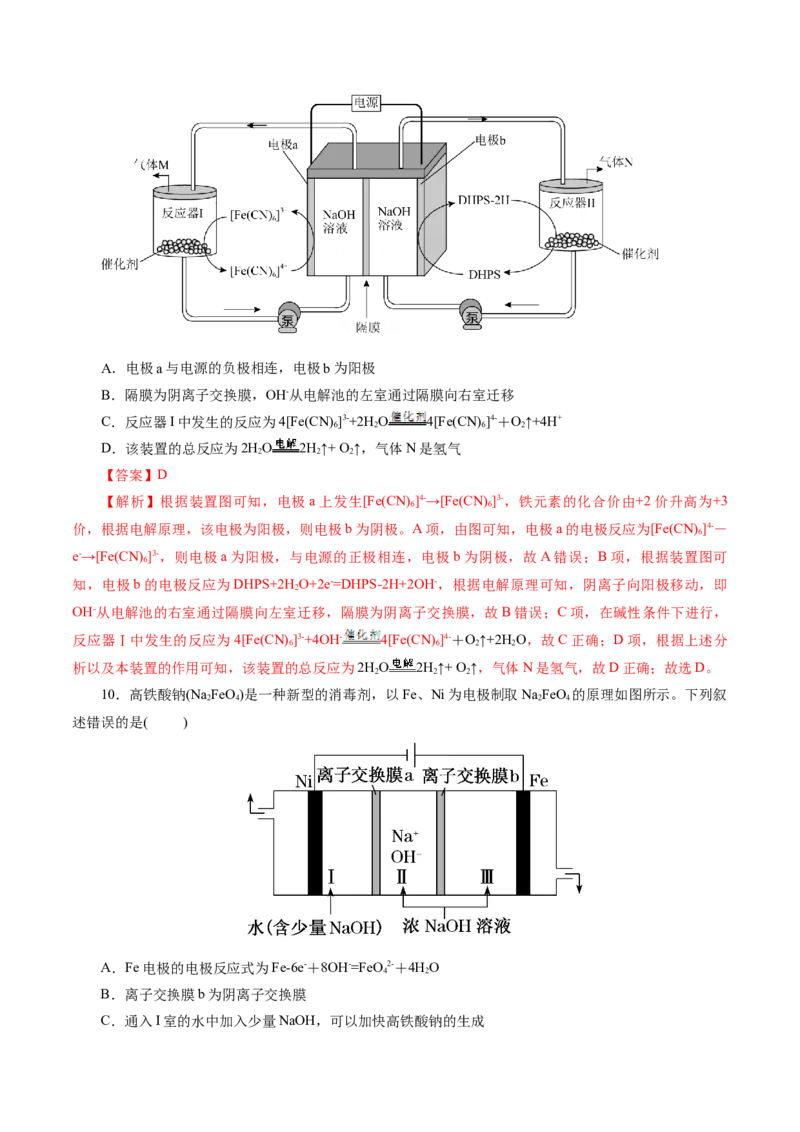
9.一种能在较低电压下获得氢气和氧气的电化学装置如图所示。下列说法正确的是( )A.电极a与电源的负极相连,电极b为阳极
B.隔膜为阴离子交换膜,OH-从电解池的左室通过隔膜向右室迁移
C.反应器I中发生的反应为4[Fe(CN) ]3-+2H O 4[Fe(CN) ]4-+O↑+4H+
6 2 6 2
D.该装置的总反应为2HO 2H↑+ O ↑,气体N是氢气
2 2 2
【答案】D
【解析】根据装置图可知,电极a上发生[Fe(CN) ]4-→[Fe(CN) ]3-,铁元素的化合价由+2价升高为+3
6 6
价,根据电解原理,该电极为阳极,则电极b为阴极。A项,由图可知,电极a的电极反应为[Fe(CN) ]4--
6
e-→[Fe(CN) ]3-,则电极a为阳极,与电源的正极相连,电极b为阴极,故A错误;B项,根据装置图可
6
知,电极b的电极反应为DHPS+2H O+2e-=DHPS-2H+2OH-,根据电解原理可知,阴离子向阳极移动,即
2
OH-从电解池的右室通过隔膜向左室迁移,隔膜为阴离子交换膜,故B错误;C项,在碱性条件下进行,
反应器Ⅰ中发生的反应为4[Fe(CN) ]3-+4OH- 4[Fe(CN) ]4-+O↑+2H O,故C正确;D项,根据上述分
6 6 2 2
析以及本装置的作用可知,该装置的总反应为2HO 2H↑+ O ↑,气体N是氢气,故D正确;故选D。
2 2 2
10.高铁酸钠(Na FeO)是一种新型的消毒剂,以Fe、Ni为电极制取NaFeO 的原理如图所示。下列叙
2 4 2 4
述错误的是( )
A.Fe电极的电极反应式为Fe-6e-+8OH-=FeO 2-+4HO
4 2
B.离子交换膜b为阴离子交换膜
C.通入I室的水中加入少量NaOH,可以加快高铁酸钠的生成D.每生成0.1 mol Na FeO,II室中溶液减少的质量为32.0 g
2 4
【答案】D
【解析】该装置以Fe、Ni为电极制取NaFeO ,为电解池装置,Fe电极为阳极,Ni电极为阴极,阳
2 4
极电极反应式为Fe-6e-+8OH-=FeO 2-+4HO,OH-移动向Ⅱ室,阴极电极反应式为2HO+2e-=H ↑+2OH-,
4 2 2 2
Na+应移动向I室。A项,Fe电极为阳极,Fe失电子生成FeO2-,电极反应式为Fe-6e-+8OH-=FeO 2-+
4 4
4HO,故A正确;B项,Fe电极为阳极,Ni电极为阴极,II室中的Na+移动向I室,OH-移动向Ⅱ室,故
2
离子交换膜 a、b分别为阳离子交换膜、阴离子交换膜,故 B正确;C项,通入 I室的水中加入少量
NaOH,可以增强溶液的导电性,可以加快高铁酸钠的生成,故 C正确;D项,每生成0.1 mol Na FeO ,
2 4
外电路中通过0.6mol电子,则II室溶液中减少的NaOH的物质的量为0.6mol,质量为24.0g,故D错误;
故选D。
11.铜基配合物电催化还原CO 的装置原理如图所示,下列说法不正确的是( )
2
A.石墨烯为阳极,发生电极反应为CO+2e-+2H+=HCOOH
2
B.Pt电极附近溶液的pH值减小
C.每转移2mol电子,阳极室、阴极室溶液质量变化量的差值为28g
D.该装置可减少CO 在大气中累积和实现可再生能源有效利用
2
【答案】A
【解析】A项,石墨烯为阴极,A错误;B项,Pt电极上HO失电子转化为O ,电极反应为2HO-4e-
2 2 2
=4H++O ↑,所以电极附近溶液的pH减小,B正确;C项,每转移2mol电子,由阴极电极反应式可知生成
2
1molHCOOH,所以阴极室溶液| |=46g/mol×1mol=46g;根据阳极室反应可知每转移2mol电子时阳极消
m阴
耗1mol水,生成0.5mol氧气,同时有2molH+转移至阴极室,所以| |=18g/mol×1mol=18g,所以| ||
m阳 m阴
|=46g-18g=28g,C正确;D项,该装置可减少CO 在大气中累计和实现可再生能源有效利用,D正
m阳 2
确;故选A。
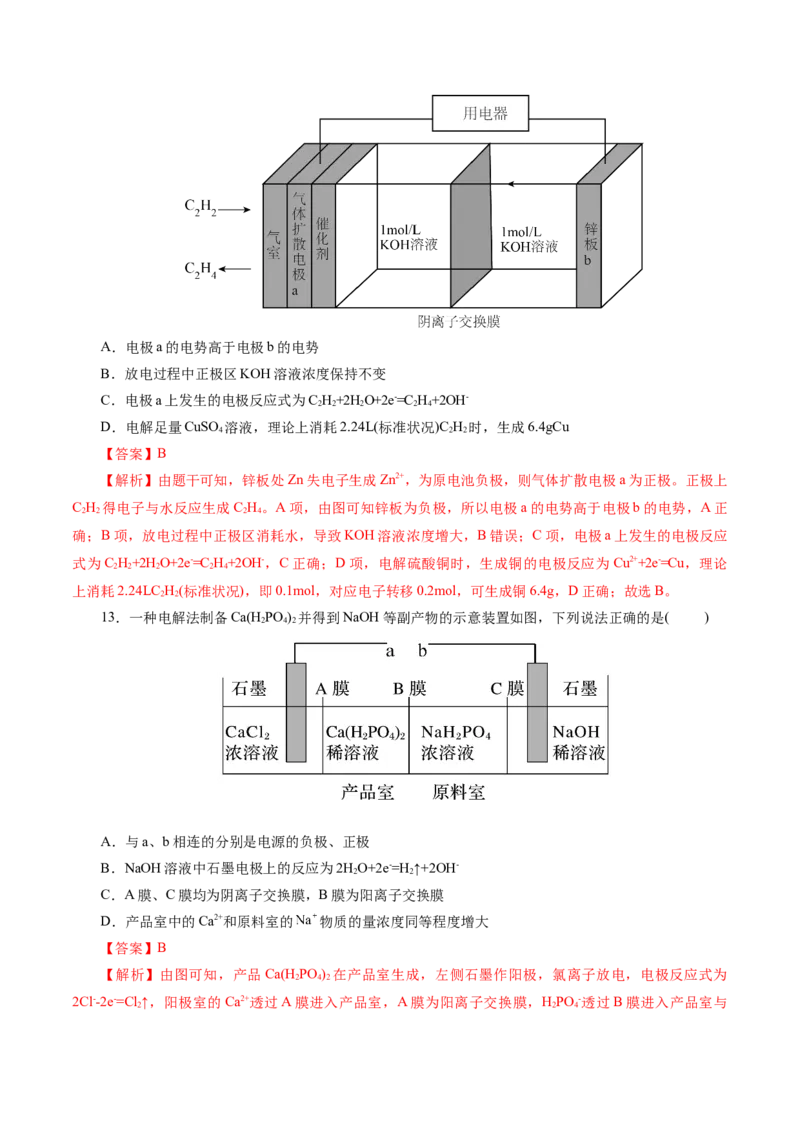
12.某科研小组利用下图装置完成乙炔转化为乙烯的同时为用电器供电。其中锌板处发生的反应有:
① Zn-2e-=Zn2+;② Zn2++4OH-=[Zn((OH) ]2-;③ Zn [Zn((OH) ]2-=ZnO+2OH-+H O。下列说法不正确的是
4 4 2
( )A.电极a的电势高于电极b的电势
B.放电过程中正极区KOH溶液浓度保持不变
C.电极a上发生的电极反应式为C H+2H O+2e-=C H+2OH-
2 2 2 2 4
D.电解足量CuSO 溶液,理论上消耗2.24L(标准状况)C H 时,生成6.4gCu
4 2 2
【答案】B
【解析】由题干可知,锌板处Zn失电子生成Zn2+,为原电池负极,则气体扩散电极a为正极。正极上
C H 得电子与水反应生成C H 。A项,由图可知锌板为负极,所以电极a的电势高于电极b的电势,A正
2 2 2 4
确;B项,放电过程中正极区消耗水,导致KOH溶液浓度增大,B错误;C项,电极a上发生的电极反应
式为C H+2H O+2e-=C H+2OH-,C正确;D项,电解硫酸铜时,生成铜的电极反应为 Cu2++2e-=Cu,理论
2 2 2 2 4
上消耗2.24LCH(标准状况),即0.1mol,对应电子转移0.2mol,可生成铜6.4g,D正确;故选B。
2 2
13.一种电解法制备Ca(HPO ) 并得到NaOH等副产物的示意装置如图,下列说法正确的是( )
2 4 2
A.与a、b相连的分别是电源的负极、正极
B.NaOH溶液中石墨电极上的反应为2HO+2e-=H ↑+2OH-
2 2
C.A膜、C膜均为阴离子交换膜,B膜为阳离子交换膜
D.产品室中的Ca2+和原料室的 物质的量浓度同等程度增大
【答案】B
【解析】由图可知,产品Ca(HPO ) 在产品室生成,左侧石墨作阳极,氯离子放电,电极反应式为
2 4 2
2Cl--2e-=Cl↑,阳极室的Ca2+透过A膜进入产品室,A膜为阳离子交换膜,HPO -透过B膜进入产品室与
2 2 4Ca2+结合生成Ca(HPO ) ,B膜为阴离子交换膜,右侧石墨极为阴极,水放电,电极反应式为 2HO+2e-
2 4 2 2
=H ↑+2OH-,Na +透过C膜进入阴极室,C膜为阳离子交换膜。A项,左侧电极为阳极,应连接电源正极,
2
即a、b相连的分别是电源的正极、负极,故A错误;B项,右侧石墨极为阴极,水放电,电极反应式为
2HO+2e-=H ↑+2OH-,故B正确;C项,A膜、C膜为阳离子交换膜,B膜为阴离子交换膜,故C错误;D
2 2
项,阳极室的Ca2+透过A膜进入产品室,产品室中的Ca2+离子浓度增大,Na+透过C膜进入阴极室,原料
室的Na+浓度减小,故D错误;故选B。
14.中科院福建物构所YaobingWang团队首次构建了一种可逆水性Zn—CO 电池,实现了CO 和
2 2
HCOOH之间的高效可逆转换,其反应原理如图所示:
已知双极膜可将水解离为H+和OH-,并实现其定向通过。下列说法中错误的是( )
A.放电时,负极电极反应式为Zn+4OH--2e-=Zn(OH) 2-
4
B.CO 转化为HCOOH过程中,Zn电极的电势低于多孔Pd电极的
2
C.充电过程中,甲酸在多孔Pd电极表面转化为CO
2
D.当外电路通过2mol电子时,双极膜中离解水的物质的量为1mol
【答案】D
【解析】由图中可知,Zn发生失去电子的反应,为电池的负极;CO 得电子生成HCOOH,多孔Pd为
2
电池的正极。A项,根据图中知,Zn发生失去电子的反应,电极反应式为Zn+4OH--2e-=Zn(OH) 2-,A项正
4
确;B项,CO 转化为HCOOH时为放电过程,Zn电极为负极,多孔Pd电极为正极,负极电势较低,B项
2
正确;C项,充电过程中,HCOOH转化为CO ,C项正确;D项,根据溶液呈电中性,可知外电路通过
2
2mol电子时,双极膜中离解的水的物质的量为2mol,D项错误。故选D。
15.(2023·浙江省Z20名校联盟)为了探究NaCO、NaHCO 与盐酸反应过程中的热效应,某化学活动
2 3 3
小组获得如下实验数据(假设实验中试剂均充分反应,生成的HCO 完全分解为CO 逸出):
2 3 2
序号 试剂1 试剂2 混合前温度 混合后温度
含0.03 mol NaHCO 的溶液32.5
Ⅰ 35mL2mol·L-1盐酸 3 20.0℃ 19.0℃
mL
含0.03 mol Na CO 的溶液32.5
Ⅱ 35mL2mol·L-1盐酸 2 3 20.0℃ 24.2℃
mL下列说法不正确的是( )
①CO2−(aq)+H+(aq) HCO -(aq) ΔH
3 3 1
②HCO −(aq)+H+(aq) HCO(aq) ΔH
3 2 3 2
③HCO(aq) CO(g)+ HO(l) ΔH
2 3 2 2 3
④CO2−(aq)+CO(g)+ HO(l)= 2HCO −(aq) ΔH
3 2 2 3 4
⑤H+(aq)+OH−(aq)=H O(l) ΔH
2 5
A.ΔH+ΔH+ΔH<0 B.ΔH<0 C.ΔH>ΔH D.ΔH>0
1 2 3 1 2 5 4
【答案】D
【解析】A项,由盖斯定律可知①+②+③得CO2−(aq)+2H+(aq)= CO(g)+ H O(l),结合表数据可知,反
3 2 2
应为放热反应,焓变小于零,则ΔH+ΔH+ΔH<0,A正确;B项,①中只存在化学键的形成,成键释放
1 2 3
能量,焓变小于0,B正确;C项,⑤为氢离子和氢氧根离子直接生成水,属于中和反应;②为氢离子和弱
酸根离子碳酸氢根离子生成碳酸;等量氢离子在中和反应中放热更多,则ΔH>ΔH,C正确; D项,由
2 5
表可知,⑥HCO −(aq)+H+(aq)= CO(g)+ H O(l)反应后温度降低,则ΔH>0;⑦CO2−(aq)+2H+(aq)=CO (g)
3 2 2 6 3 2
+ H O(l)反应后温度升高,则ΔH<0;由盖斯定律可知,⑦-2×⑥得④CO2−(aq)+CO (g)+ H O(l)= 2HCO −
2 7 3 2 2 3
(aq) ΔH=ΔH-2ΔH<0,D错误;故选D。
4 7 6
二、非选择题(本题包括5小题,共55分)
16.(10分)Ⅰ.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过 ,在
此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通过。
(1)分析比较图示中 与 的大小: ___________ (填“>”“<”或“=”)。
(2)写出燃料电池B中的正极的电极反应:___________。
(3)图中Y是___________(填化学式),若电解产生 (标准状况)该物质,则至少转移电子
___________ ;X元素的基态原子的电子排布式为___________。Ⅱ.某实验小组同学利用如图装置对电化学原理进行了一系列探究活动。
(4)甲池装置为___________(填“原电池”或“电解池”)。
(5)甲池反应前两电极质量相等,一段时间后,两电极质量相差14 g,导线中通过___________ mol电
子。
(6)实验过程中,甲池左侧烧杯中NO -的浓度___________(填“增大”、“减小”或“不变”)。
3
(7)若乙池中溶液为足量的硝酸银溶液,工作一段时间后,若要使乙池中溶液恢复原浓度,可向溶液中
加入___________。(填化学式)
【答案】(1)<(1分) (2)O +4e-+2HO=4OH-(1分)
2 2
(3)H (1分) 1(1分) 1s22s22p63s23p5(1分)
2
(4)原电池(1分) (5)0.1(2分) (6)增大(1分) (7)Ag O或Ag CO(1分)
2 2 3
【解析】(1)燃料电池中,通入Y气体的电极为负极,电解饱和食盐水生成的Y为氢气,X为Cl,由
2
于燃料电池正极发生O+4e-+2H O=4OH-,燃料电池中的离子膜只允许阳离子通过,而燃料电池中正极氧
2 2
气得到电子产生OH-,所以反应后氢氧化钠的浓度升高,即a%<b%;(2)燃料电池B中的正极是氧气得到
电子,电极反应为O+4e-+2H O=4OH-。(3)根据以上分析可知图中Y是H,若电解产生11.2L(标准状况)
2 2 2
该物质,氢气的物质的量是0.5mol,则至少转移电子1.0mol;X是氯气,其中氯元素的基态原子的电子排
布式为。(4)甲池装置是铜和银构成的原电池,即装置为原电池。(5)甲池反应前两电极质量相等,一段时间
后,两电极质量相差14 g,设消耗铜的物质的量是xmol,则同时生成银的物质的量是2xmol,则有
64x+108×2x=14,解得x=0.05,所以导线中通过0.05mol×2=0.1mol电子。(6)原电池中阴离子向负极移
动,则实验过程中硝酸根离子移向左池,甲池左侧烧杯中NO -的浓度增大。(7)若乙池中溶液为足量的硝酸
3
银溶液,惰性电极电解硝酸银溶液生成硝酸、氧气和银,因此工作一段时间后,若要使乙池中溶液恢复原
浓度,可向溶液中加入Ag O或Ag CO。
2 2 3
17.(13分)(2023·黑龙江省齐齐哈尔市八校联合体高三联考)回答下列问题:
(1)在微生物作用的条件下, NH +经过两步反应被氧化成NO -。两步反应的能量变化示意图如图:
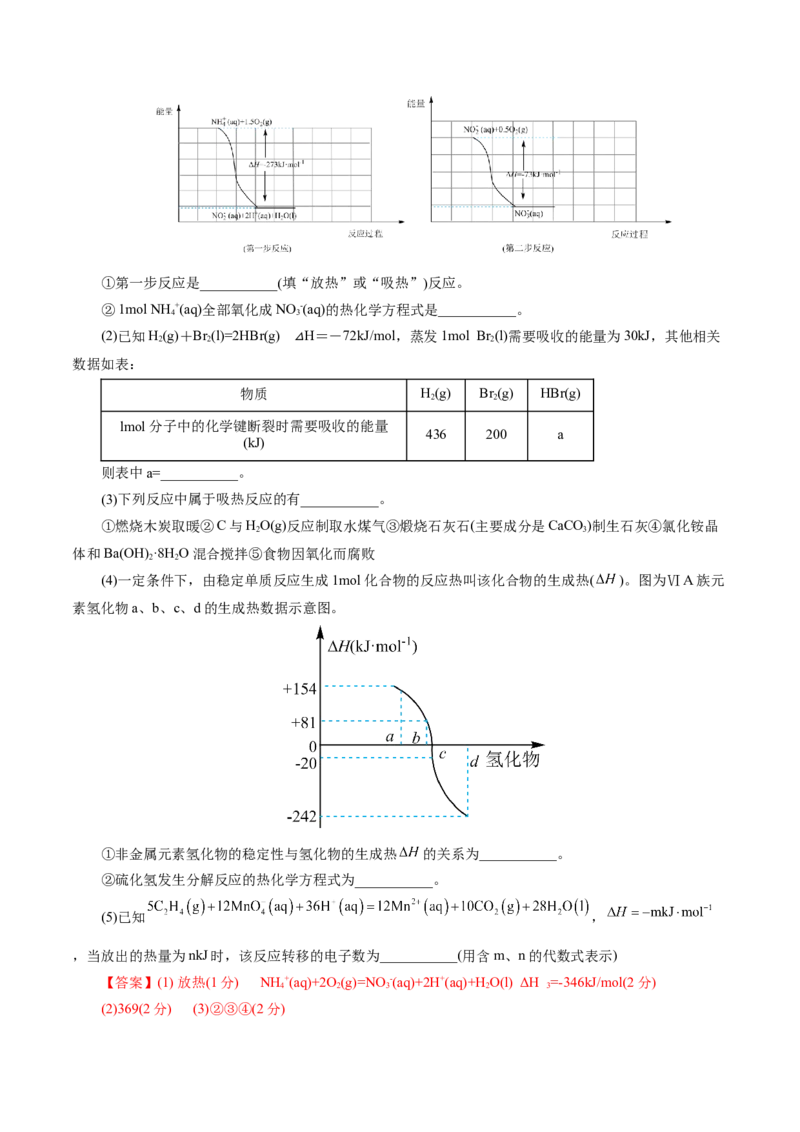
4 3①第一步反应是___________(填“放热”或“吸热”)反应。
②1mol NH +(aq)全部氧化成NO -(aq)的热化学方程式是___________。
4 3
(2)已知H(g)+Br(l)=2HBr(g) H=-72kJ/mol,蒸发1mol Br(l)需要吸收的能量为30kJ,其他相关
2 2 2
数据如表: △
物质 H(g) Br(g) HBr(g)
2 2
lmol分子中的化学键断裂时需要吸收的能量
436 200 a
(kJ)
则表中a=___________。
(3)下列反应中属于吸热反应的有___________。
①燃烧木炭取暖②C与HO(g)反应制取水煤气③煅烧石灰石(主要成分是CaCO)制生石灰④氯化铵晶
2 3
体和Ba(OH) ·8H O混合搅拌⑤食物因氧化而腐败
2 2
(4)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热( )。图为ⅥA族元
素氢化物a、b、c、d的生成热数据示意图。
①非金属元素氢化物的稳定性与氢化物的生成热 的关系为___________。
②硫化氢发生分解反应的热化学方程式为___________。
(5)已知 ,
,当放出的热量为nkJ时,该反应转移的电子数为___________(用含m、n的代数式表示)
【答案】(1) 放热(1分) NH +(aq)+2O (g)=NO -(aq)+2H+(aq)+H O(l) ΔH =-346kJ/mol(2分)
4 2 3 2 3
(2)369(2分) (3)②③④(2分)(4) 非金属元素形成的气态氢化物稳定性越强,其ΔH越小(2分)
HS(g)=S(s)+H(g) ΔH=+20kJ·mol-1(2分)
2 2
(5) (2分)
【解析】(1)①由图可知,焓变小于0,即反应物的总能量大于生成物的总能量,所以反应为放热反
应;②第一步的热化学方程式为 △H=-273kJ/mol,第二步的热
1
化学方程式为 △H=-73kJ/mol,根据盖斯定律,则
2
△H=-346kJ/mol;(2)蒸发1mol Br(l)需要吸收的能量为30kJ,结
2
合反应及表格中数据可知,436+(200+30)-2a=-72,解得a=369;(3)①大多数燃烧反应为放热反应,则①为
放热反应;②C与HO (g)高温下反应制取水煤气的反应为吸热反应,则②为吸热反应;③大多数分解反应
2
为吸热反应,煅烧石灰石(主要成分是CaCO )制生石灰的反应为分解反应,则③为吸热反应;④氯化铵晶
3
体和Ba(OH) ·8H O的反应为吸热反应,则④为吸热反应;食物因氧化而腐败是⑤食物中的有机物质被空
2 2
气中的氧气氧化生成一些小分 子产物,同时放出热量的过程,则⑤为放热反应;故答案为②③④;(4)①
根据元素周期律,同一主族元素非金属性越强,生成气态氢化物越容易,气态氢化物越稳定,而根据热力
学,能量越低越稳定,则非金属元素形成的气态氢化物稳定性越强,其△H越小;②结合①的分析,a、
b、c、d依次为HTe、HSe、HS、HO,则c为HS,再结合上图,生成HS的△H为-20kJ/mol,则硫化
2 2 2 2 2 2
氢发生分解反应的△H为+ 20kJ/mol,热化学方程式为:H S(g)=S(s)+H(g) ΔH=+20kJ·mol-1;(5)反应中Mn
2 2
元素的化合价由+7价降低至+2价,12 molMnO 被还原时转移60 mol电子,放出m kJ热量,当放出的热量
2
为nkJ时,该反应转移的电子的物质的量为 mol,转移的电子数为 。
18.(10分)(2023·宁夏石嘴山市模拟)回答下列问题
(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类化合物
[Mn(L) ]( ClO ) 是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知
3 4 2
△H= -299kJ/mol,则△H (kJ/mol )为_____________
2 1
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO 利用的研究热点
4 2 2
之一、该重整反应体系主要涉及以下反应:(a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
(b)CO (g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
(c)CH(g) C(s)+2H(g) ∆H
4 2 3
(d)2CO(g) CO(g)+C(s) ∆H
2 4
(e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(3)用H 还原SiCl 蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,则该反应
2 4
的热化学方程式为___________________________________。
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的HSO 稀溶液反应放出11.46kJ的热量。请写出KOH
2 4
的稀溶液与的HSO 稀溶液发生中和反应,表示中和热的热化学方程式为___________________。
2 4
(5)1mol CH (g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催化剂作用
4
下,CH 可以还原SO 生成单质S(g)、HO(g)和CO,写出该反应的热化学方程式:________________。
4 2 2 2
【答案】(1)-1703kJ/mol(2分) (2)∆H+∆H-∆H 或∆H-∆H(2分)
2 3 5 3 4
(3)SiCl (g)+2H(g)=Si(s)+4HCl(g) H=+236kJ/mol(2分)
4 2
△
(4)KOH(aq)+ HSO (aq)= KSO (aq)+H O(l) H=-57.3kJ/mol(2分)
2 4 2 4 2
(5)CH (g)+2SO(g) 2S(g)+CO(g)+2HO(g) △ H=+352kJ/mol(2分)
4 2 2 2
【解析】(1)由盖斯定律可知,△H =2 H2+ H-
1 3△
H
4
=2×(-299kJ/mol)+(-1018kJ/mol)-(+87kJ/m△ol)=-1△703kJ/mol;(2)根据盖斯定律,反应(b)+ (c)- (e)或(c)- (d)
△ 得反应(a),故反应a的∆H 1 =∆H 2 +∆H 3 -∆H 5 或∆H 3 -∆H 4 ;(3)SiCl 4 (g)+2H 2 (g)=Si(s)+4HCl(g),反应中氢化合价
由0变为+1,反应中转移电子为4个,则4mol电子转移时吸收4×59kJ热量,故该反应的热化学方程式为
SiCl (g)+2H(g)=Si(s)+4HCl(g) H=+236kJ/mol;(4)中和热是在稀溶液中,强酸跟强碱发生中和反应生成1
4 2
mol液态水时所释放的热量;已 △ 知含11.2gKOH的稀溶液(含0.2mol氢氧根离子)与1L0.1mol•L-1的H 2 SO 4 稀
溶液(含有氢离子0.2mol)反应放出11.46kJ的热量,则生成1 mol液态水时所释放的热量为5×11.46kJ,故表
示中和热的热化学方程式为KOH(aq)+ HSO (aq)= KSO (aq)+H O(l) H=-57.3kJ/mol。(5)由图可知,
2 4 2 4 2
△
①CH(g) +2O (g)=CO (g) +2H O(g) H=(126-928)kJ/mol=-802kJ/mol,②S(g)+O(g)= SO (g) H
4 2 2 2 2 2
=-577kJ/mol,根据盖斯定律可知,① △-2②得:CH
4
(g)+2SO
2
(g) 2S(g)+CO
2
(g)+2H
2
O(g)△H=+352kJ/
mol。
△
19.(10分)某实验小组通过以下实验,探究镀件表面镀铜的最佳条件。【查阅资料】①Cu2++2P O4- [Cu(P O)]6- K=1×109
2 7 2 7 2
②Cu+在溶液中不稳定,容易发生歧化。
【实验设计】用CuSO ·5H O、NaPO·10H O(焦磷酸钠)、添加剂配制一定浓度的电镀液,分别用纯
4 2 4 2 7 2
铜和镀件作为两极材料,探究电镀液的pH、电流密度、电极板间距对层的影响。
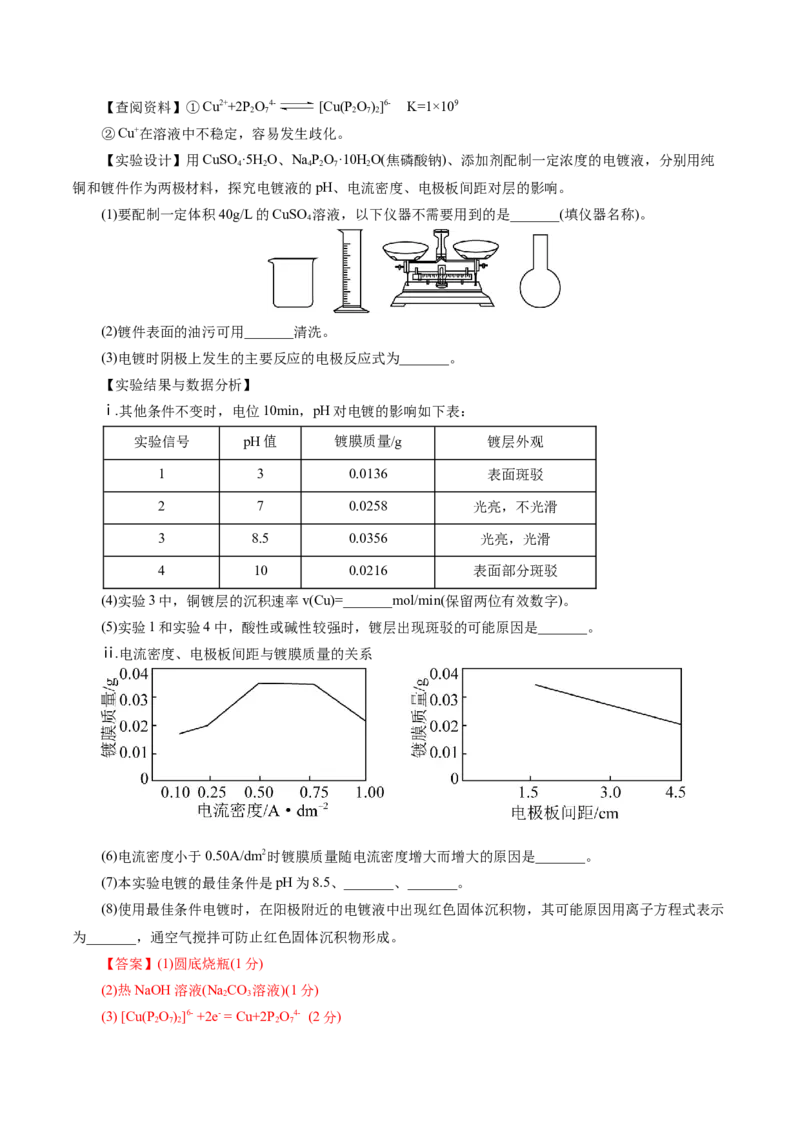
(1)要配制一定体积40g/L的CuSO 溶液,以下仪器不需要用到的是_______(填仪器名称)。
4
(2)镀件表面的油污可用_______清洗。
(3)电镀时阴极上发生的主要反应的电极反应式为_______。
【实验结果与数据分析】
ⅰ.其他条件不变时,电位10min,pH对电镀的影响如下表:
实验信号 pH值 镀膜质量/g 镀层外观
1 3 0.0136 表面斑驳
2 7 0.0258 光亮,不光滑
3 8.5 0.0356 光亮,光滑
4 10 0.0216 表面部分斑驳
(4)实验3中,铜镀层的沉积速率v(Cu)=_______mol/min(保留两位有效数字)。
(5)实验1和实验4中,酸性或碱性较强时,镀层出现斑驳的可能原因是_______。
ⅱ.电流密度、电极板间距与镀膜质量的关系
(6)电流密度小于0.50A/dm2时镀膜质量随电流密度增大而增大的原因是_______。
(7)本实验电镀的最佳条件是pH为8.5、_______、_______。
(8)使用最佳条件电镀时,在阳极附近的电镀液中出现红色固体沉积物,其可能原因用离子方程式表示
为_______,通空气搅拌可防止红色固体沉积物形成。
【答案】(1)圆底烧瓶(1分)
(2)热NaOH溶液(Na CO 溶液)(1分)
2 3
(3) [Cu(P O)]6- +2e- =Cu+2P O4- (2分)
2 7 2 2 7(4)5.6×10-5(1分)
(5) pH=3酸性强H+放电产生氢气,pH=10碱性强易生成Cu(OH) 沉淀均影响镀件上铜的沉积(1分)
2
(6)电流密度越大,单位时间内转移电子数目越多,电镀铜沉积速率越快,故镀膜质量越大(1分)
(7) 电流密度为0.5A·dm-2 (或0.5~0.75A·dm-2之间)(1分) 电极板间距为1.5cm(1分)
(8)2Cu++2H O=Cu O+2H+或2Cu++2OH-=Cu O+HO或2Cu+=Cu+Cu2+(1分)
2 2 2 2
【解析】(1)配制一定体积40g/L的CuSO 溶液,需要用托盘天平称取一定质量的硫酸铜固体,需要量
4
筒量取一定体积的蒸馏水,需要在烧杯中配制,故不需要的仪器为:圆底烧瓶;(2)油污在碱性条件下容易
水解生成易溶于水的物质,故镀件表面的油污可用热NaOH溶液(Na CO 溶液)清洗;(3)电镀时阴极上析出
2 3
单质铜,主要的电极反应式为:[Cu(P O)]6- +2e- =Cu+2P O4- ;(4)实验3中,铜镀层的沉积速率v(Cu)=
2 7 2 2 7
;(5)pH较低时氢离子也可以在阴极得到电子生成氢气,从而影响铜离子得到电子,pH
较高时,容易生成氢氧化铜沉淀,也会影响铜离子得到电子,从而出现斑驳,故镀层出现斑驳的可能原因
是:pH=3酸性强H+放电产生氢气,pH=10碱性强易生成Cu(OH) 沉淀均影响镀件上铜的沉积;(6)铜离子
2
得到电子形成单质铜,吸附到镀件上,形成镀膜,电流密度越大单位时间内转移电子数目越多,形成的单
质铜越多,镀膜越厚,故镀膜质量随电流密度增大而增大的原因是:电流密度越大,单位时间内转移电子
数目越多,电镀铜沉积速率越快,故镀膜质量越大;(7)电镀时镀膜质量越大效果越好,由表格中的数据和
图中信息可知本实验电镀的最佳条件是pH为8.5、电流密度为电流密度为0.5A·dm-2 (或0.5~0.75A·dm-2之
间)、电极板间距为1.5cm时镀膜质量较大;(8)铜为阳极材料,在阳极可能出现铜失去电子形成+1价铜和
水失去电子形成的氢氧根结合形成了红色的氧化亚铜,或者单质铜;也可能是+1价铜发生的歧化反应生成
的单质铜,相关的方程式为:2Cu++2H O=Cu O+2H+或2Cu++2OH-=Cu O+HO或2Cu+=Cu+Cu2+。
2 2 2 2
20.(12分)(2023·江苏省盐城市高三模拟)电催化还原CO 是当今资源化利用二氧化碳的重点课题,常
2
用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
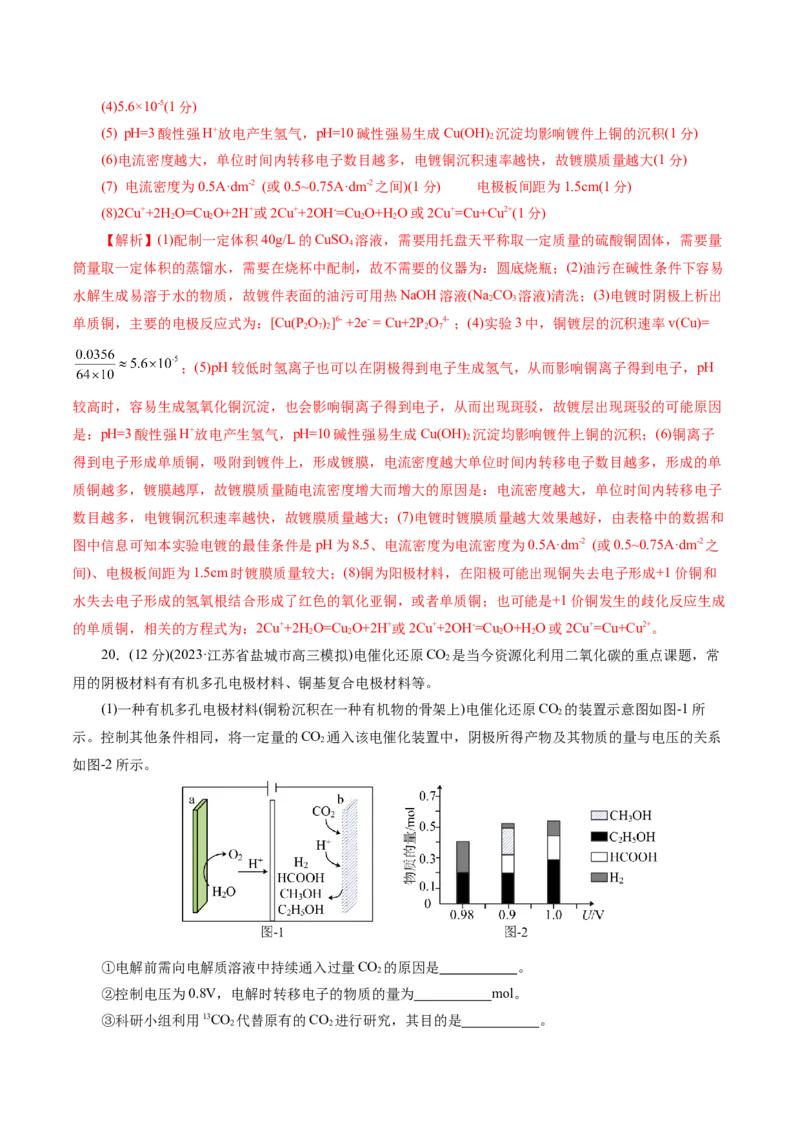
(1)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO 的装置示意图如图-1所
2
示。控制其他条件相同,将一定量的CO 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系
2
如图-2所示。
①电解前需向电解质溶液中持续通入过量CO 的原因是 。
2
②控制电压为0.8V,电解时转移电子的物质的量为 mol。
③科研小组利用13CO 代替原有的CO 进行研究,其目的是 。
2 2(2)一种铜基复合电极材料Au/Cu O的制备方法:将一定量Cu O分散至水与乙醇的混合溶液中,向溶
2 2
液中逐滴滴加HAuCl (一种强酸)溶液,搅拌一段时间后离心分离,得Au/Cu O,溶液呈蓝色。写出Cu O
4 2 2
还原HAuCl 的离子方程式: 。
4
(3)金属Cu/La复合电极材料电催化还原CO₂制备甲醛和乙醇的可能机理如图-3所示。研究表明,在不
同电极材料上形成中间体的部分反应活化能如图-4所示。
①X为 。在答题卡上相应位置补充完整虚线框内Y的结构 。
②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原CO 的优点是 。
2
【答案】(1)使阴极表面尽可能被CO 附着,减少析氢反应的发生(减少氢离子在阴极上放电的几率),
2
提高含碳化合物的产率(2分) 2.8(2分) 为确定阴极上生成的含碳化合物源自CO 而非有机多
2
孔电极材料(2分)
(2)3Cu O+6H++2AuCl -=2Au+6Cu2++8Cl-+3H O(2分)
2 4 2
(3)H++ e-(1分) (1分) 加快了生成乙醇与甲醛的速率,提高了乙醇的选择性(2分)
【解析】(1)①电解前需向电解质溶液中持续通入过量CO 的原因是使阴极表面尽可能被CO 附着,减
2 2
少析氢反应的发生(减少氢离子在阴极上放电的几率),提高含碳化合物的产率。②控制电压为0.8V,产生
0.2mol氢气和0.2mol乙醇,根据电极反应2H++2e-=H ↑,2CO+12e-+12H+=C HOH+3H O,故电解时转移
2 2 2 5 2
电子的物质的量为0.4+2.4=2.8mol。③科研小组利用13CO 代替原有的CO 进行研究,其目的是为确定阴极
2 2
上生成的含碳化合物源自CO 而非有机多孔电极材料。(2)将一定量Cu O分散至水与乙醇的混合溶液中,
2 2
向溶液中逐滴滴加HAuCl (一种强酸)溶液,搅拌一段时间后离心分离,溶液呈蓝色,说明生成铜离子。
4
故Cu O还原HAuCl 的离子方程式:3Cu O+6H++2AuCl -=2Au+6Cu2++8Cl-+3H O;(3)从过程分析,两步都
2 4 2 4 2
与X反应,上两个氢原子,故X为氢离子和一个电子,则Y处的图为 。从图-4分析,与单纯
的Cu电极相比,利用Cu/La复合电极材料电催化还原CO 的优点是加快了生成乙醇与甲醛的速率,提高
2
了乙醇的选择性。