文档内容
专题 07 化学反应速率与化学平衡
目录
01 模拟基础练
【题型一】化学反应速率及其影响因素
【题型二】化学平衡及其影响因素
【题型三】化学反应速率和化学平衡的综合计算
02 重难创新练
03 真题实战练
题型一 化学反应速率及其影响因素
1.在容积为2L的密闭容器中进行如下反应:A(s)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为
6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.1 mol/(L·min)。下列说法
错误的是( )
A.前5min内用A表示的化学反应速率v(A)为0.1mol/(L·min)
B.化学方程式中n值为1
C.反应达到平衡时3v (B)=2v (C)
正 逆
D.此反应在两种不同情况下的速率分别表示为:①v(B)=6 mol/(L·min),②v(D)=4.5 mol/(L·min),其
中反应速率快的是②
2.以反应 5HC O+2MnO -+6H+ = 10CO↑+ 2Mn2+ + 8H O 为例探究“外界条件对化学反应速率的
2 2 4 4 2 2
影响”。实验时,分别量取 HC O 溶液和酸性 KMnO 溶液,迅速混合并开始计时,通过测定溶液褪色所
2 2 4 4
需时间来判断反应的快慢。
下列说法不正确的是( )
A.实验①、 ②、 ③所加的HC O 溶液均要过量
2 2 4B.若实验①测得 KMnO 溶液的褪色时间为 40 s,则这段时间内平均反应速率 v(KMnO)= 2. 5×10-
4 4
4 mol/L/s
C.实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影
响
D.实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的 Mn2+对反应起催化作用
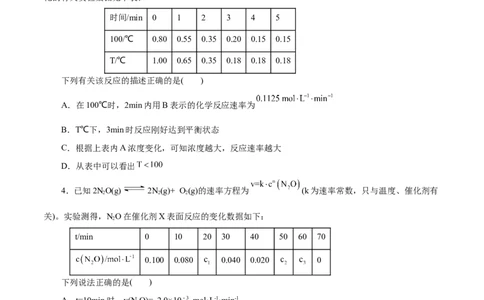
3.反应A(g) 4B (g)+ C (g),在100℃和T℃时,A的物质的量浓度(单位: )随时间变
化的有关实验数据见下表:
时间/min 0 1 2 3 4 5
100/℃ 0.80 0.55 0.35 0.20 0.15 0.15
T/℃ 1.00 0.65 0.35 0.18 0.18 0.18
下列有关该反应的描述正确的是( )
A.在100℃时,2min内用B表示的化学反应速率为
B.T℃下,3min时反应刚好达到平衡状态
C.根据上表内A浓度变化,可知浓度越大,反应速率越大
D.从表中可以看出
4.已知2NO(g) 2N(g)+ O(g)的速率方程为 (k为速率常数,只与温度、催化剂有
2 2 2
关)。实验测得,NO在催化剂X表面反应的变化数据如下:
2
t/min 0 10 20 30 40 50 60 70
0.100 0.080 0.040 0.020 0
下列说法正确的是( )
A.t=10min时,v(N O)= 2.0×10-3 mol·L-1·min-1
2
B.速率方程中n=1,表格中c>c=c
1 2 3
C.相同条件下,增加NO的浓度或催化剂X的表面积,都能加快反应速率
2
D.保持其他条件不变,若起始浓度为 ,当减至一半时共耗时70min
5.[新考法] (2025·浙江省七彩阳光新高考研究联盟高三联考,节选)能源与化工生产、生活等密切相
关,氢能的有效利用是实现“碳达峰、碳中和”的重要途径。
(3) NHBH 是近年来发现的氢含量最高、常温下呈稳定固态的新型储氢化合物,在Co催化剂的作用下
3 3可水解释放H:NH BH+2H O NH BO+3H↑。
2 3 3 2 4 2 2
①Co催化剂可用NaBH 还原CoCl·6H O制得(已知:NaBH +2H O=NaBO+3H↑,NaBH 用量对Co催
4 2 2 4 2 2 2 4
化剂的微晶尺寸没有影响)。不同NaBH 用量制备的Co催化剂催化NH BH 水解产氢体积随时间的变化如
4 3 3
下图所示:
当 时,NH BH 水解产氢速率反而降低的可能原因是 。
3 3
②NH BH 水解脱氢后的再生可采用电解法,第一步是电解BO-转化为BH-,请写出该转化的电极反应
3 3 2 4
。
题型二 化学平衡及其影响因素
6.下列反应在任何温度下均能自发进行的是( )
A.2N(g)+O(g)===2N O(g) ΔH=163 kJ·mol-1
2 2 2
B.Ag(s)+Cl(g)===AgCl(s) ΔH=-127 kJ·mol-1
2
C.HgO(s)===Hg(l)+O(g) ΔH=91 kJ·mol-1
2
D.HO(l)===O (g)+HO(l) ΔH=-98 kJ·mol-1
2 2 2 2
7.某温度下,反应2CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列说法正确
2 2 2 3 2
的是( )
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2
C.恒压下,充入一定量的N,平衡向逆反应方向移动
2
D.恒容下,充入一定量的CH=CH (g),CH=CH (g)的平衡转化率增大
2 2 2 2
8.在PdCl -CuCl 做催化剂和适宜的温度条件下,用O 将HCl氧化为Cl:4HCl(g)+O (g)=2HO(g)
2 2 2 2 2 2
+2Cl(g) ΔH<0,下列有关说法不正确的是( )
2
A.降低温度,可提高Cl 产率
2B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式
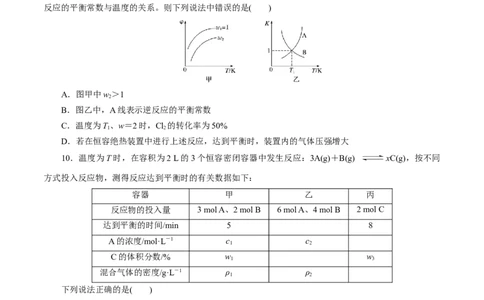
9.已知反应:CH==CHCH (g)+Cl(g) CH==CHCH Cl(g)+HCl(g)。在一定压强下,按w=向
2 3 2 2 2
密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(φ)与温度(T)、w的关系,图乙表示正、逆
反应的平衡常数与温度的关系。则下列说法中错误的是( )
A.图甲中w >1
2
B.图乙中,A线表示逆反应的平衡常数
C.温度为T、w=2时,Cl 的转化率为50%
1 2
D.若在恒容绝热装置中进行上述反应,达到平衡时,装置内的气体压强增大
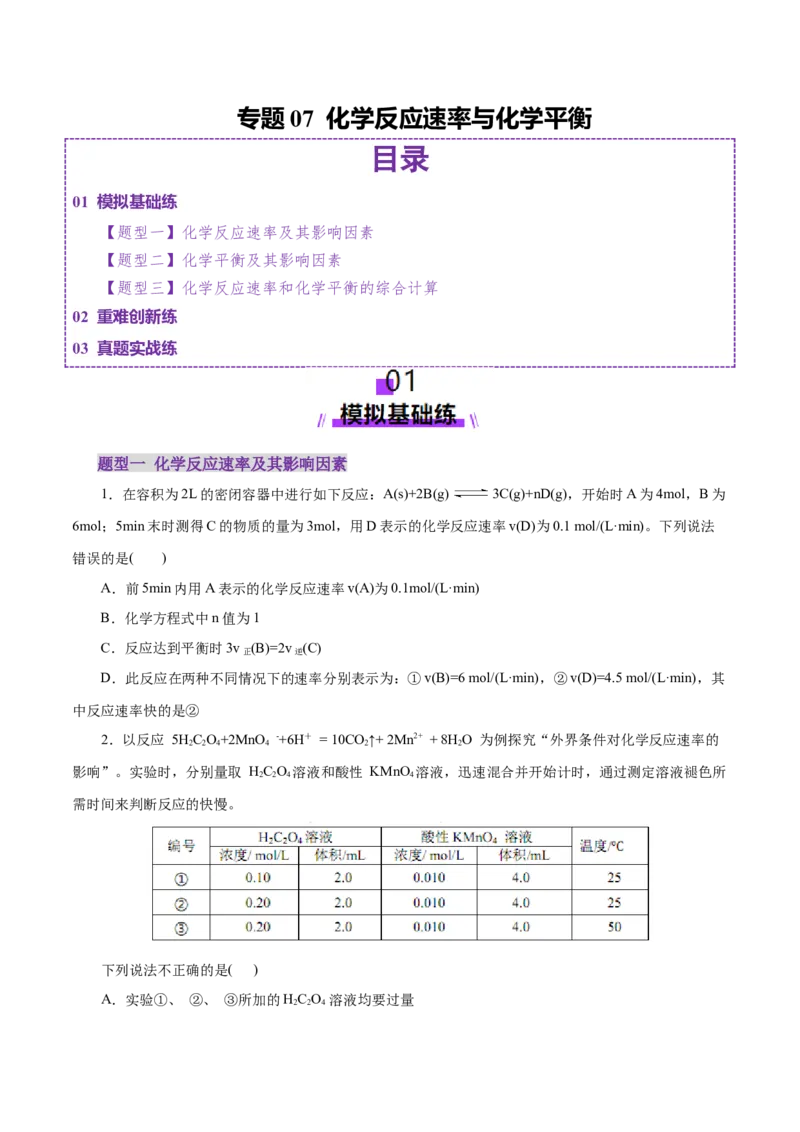
10.温度为T时,在容积为2 L的3个恒容密闭容器中发生反应:3A(g)+B(g) xC(g),按不同
方式投入反应物,测得反应达到平衡时的有关数据如下:
容器 甲 乙 丙
反应物的投入量 3 mol A、2 mol B 6 mol A、4 mol B 2 mol C
达到平衡的时间/min 5 8
A的浓度/mol·L-1 c c
1 2
C的体积分数/% w w
1 3
混合气体的密度/g·L-1 ρ ρ
1 2
下列说法正确的是( )
A.若x<4,则2c<c
1 2
B.若x=4,则w =w
1 3
C.无论x的值是多少,均有2ρ=ρ
1 2
D.甲容器达到平衡所需的时间比乙容器达到平衡所需的时间短
题型三 化学反应速率和化学平衡的综合计算
11.将xmolH S气体平均分成两份,分别通入容器A、容器B(容积均为1L),其中一容器为绝热环境,
2
另一容器为25℃恒温环境,在容器内均发生:2HS(g) 2H(g) +S (g) ΔH>0 (25℃),相关数据
2 2 2如下表:
时间/min 0 10 20 30 40 50 60
容器A 0 0.8 1.5 2 2.3 2.4 2.4
容器B 0 1 1.8 2.5 3 3 3
下列说法正确的是( )
A.根据上表信息,可推算出x=3
B.容器A为25℃恒温环境,容器B为绝热环境
C.1~60min内,25℃恒温环境反应速率可表示为v(H S生成)=0.1mol·L-1·min-1
2
D.可通过降低容器的温度,从而加快逆反应的速率,达到抑制HS气体分解的目的
2
12.甲酸乙酯在OH-存在下发生水解:HCOOC H+OH- HCOO-+C HOH,两种反应物的初始浓
2 5 2 5
度均为0.500 mol·L-1,不同温度下测得HCOOC H 的浓度(mol·L-1)随时间变化的数据如表所示。下列有关说
2 5
法不正确的是( )
t/s 0 120 180 240 330 530 600 700 800
15
0.500 0.335 0.291 0.256 0.210 0.156 0.148 0.145 0.145
℃
35
0.500 0.325 0.2775 0.238 0.190 … 0.130 0.130 0.130
℃
A.该反应在15 ℃,120 s~180 s区间的v(HCOOC H)为7.33×10-5 mol·L-1·s-1
2 5
C.530 s时,表格中35 ℃对应的数据一定是0.130
D.由表中数据可知,温度升高,反应速率加快
D.其他条件不变,提高c(OH-),可使该反应的化学平衡常数增大
13.某反应A(g)+B(g)→C(g)+D(g)的速率方程为v=k•cm(A)•cn(B),其半衰期(当剩余反应物恰好是起始
的一半时所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示:
c(A)/(mol•L-1) 0.25 0.50 1.00 0.50 1.00 c
1
c(B)/(mol•L-1) 0.050 0.050 0.100 0.100 0.200 c
2
v/(10-3mol•L-1•min-1) 1.6 3.2 v 3.2 v 4.8
1 2
下列说法不正确的是( )
A.上述表格中的c=0.75、v=6.4
1 2
B.该反应的速率常数k=6.4×10-3min-1C.在过量的B存在时,反应掉93.75%的A所需的时间是500min
D.升温、加入催化剂、缩小容积(加压),使k增大导致反应的瞬时速率加快
14.化学反应进行的方向和限度是化学反应原理所要研究的两个重要问题,下列有关化学反应进行的
方向和限度的说法中不正确的是( )
A.恒温恒容的密闭容器中发生反应mA(g)+nB(g) pC(g),若B是有色物质,A,C均为无色物
质,达到平衡后,加入一定量C,体系的颜色会变深
B.一定温度下两个体积相同密闭容器中,分别放有二氧化氮、气态溴,起始时两个容器中气体颜色
相同,若将容器体积压缩至原来的一半,则C >C
NO2 Br2
C.综合考虑反应速率和限度,以及催化剂活性,合成氨一般选择400℃~500℃
D.恒温时,对于反应A(g)+3B(g) 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积
分数为n%,此时若给体系加压为原来的两倍,则A体积分数仍为n%
15.将0.8 mol 放入一个装满O 的恒压密闭容器中,在 、 的条件下使之充分反应至t
2 1
时刻,此时容器中无S剩余,剩余0.2 mol O。再向该体系中迅速投入 无水FeSO 固体,此过程容器
2 4
与外界未发生气体交换,充分反应至t 时刻。已知此条件下可以发生如下反应:
2
S(s)+O(g) SO (g)
2 2
2FeSO (s) Fe O(s)+SO (g)+SO(g) K =8.1×107Pa2
4 2 3 2 3 P2
2SO (g) 2SO (g)+O(g) K =7.2×103Pa
3 2 2 P2
下列说法不正确的是( )
A.t 时刻,容器中气体总物质的量为1.0mol
1
B.t 时刻,容器中S(s)+O(g) SO (g)的分压为
1 2 2
C.起始时,容器中n(O )=1.25mol
2
D.t 时刻,容器中的固体为FeSO 与Fe O 的混合物
2 4 2 3
16.在3个容积均为2.0L的恒容密闭容器中,反应HO(g)+C(s) CO(g)+H(g) ΔH>0 ,分别在
2 2
一定温度下达到平衡,下列说法正确的是( )
起始时物质的量/mol 平衡时物质的量/mol
温度
容器
(T >T)
1 2 n(H O) n(C) n(CO) n(H ) n(CO)
2 2
I T 0.6 1.2 0 0 0.2
1
II T 1.2 1.2 0 0 x
1
III T 0 0 0.6 0.6 y
2A.当温度为T 时,该反应的化学平衡常数值为0.1
1
B.达到平衡时,容器II中HO的转化率比容器I中的小
2
C.若5min后容器I中达到平衡,则HO的平衡浓度为1.0 mol/L
2
D.达到平衡时,容器III中 CO的转化率小于66.6%
17.对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的。汽车
尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g) N(g)+2CO (g)+Q (Q>0)。
2 2
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
时间/s 0 1 2 3 4 5
4.50 × 2.50 × 1.50 × 1.00 ×
c(NO)/mol·L-1 1.00 ×10-3 1.00 ×10-4
10-4 10-4 10-4 10-4
3.60 × 2.85 × 2.70 ×
c(CO)/mol·L-1 3.05 ×10-3 2.75 ×10-3 2.70 ×10-3
10-3 10-3 10-3
(1)根据表格中数据计算该反应的平衡常数K=___________。
(2)前2s内的平均反应速率 (N ) =___________ ; 达到平衡时, CO的转化率为___________。
2
1.某温度下,将2mol H 和2molI 充入密闭的刚性容器中发生反应H(g)+I(g) 2HI(g),该反应
2 2 2 2
的v-t图象如图所示,t 时刻测定容器内HI的物质的量为1mol,t 时刻保持等温等容,抽走0.5mol HI。下
1 2
列有关叙述正确的是( )
A.该温度下H(g)+I(g) 2HI(g)的平衡常数
2 2
B.反应过程中,可以利用气体的总压强保持不变来判断是否达到平衡
C.t 时刻,抽取HI的瞬间,v′(逆)在图象上的变化应该是c点
2
D.t 时刻,抽取HI后达到平衡后H 的百分含量减少
2 22.(2025·河南省部分重点高中高三青桐呜大联考)已知反应SiHCl (g)+H(g) Si(s)+3HCl(g)
3 2
ΔH=+210kJ·mol−1,在三个不同容积的恒容密闭容器中分别充入1mol SiHCl (g)与2molH (g),恒温条件下,
3 2
测得平衡时SiHCl (g)的转化率与体系压强如表。
3
序号 温度℃ 容器容积/L 平衡转化率 体系平衡压强kPa
① 200 V 50% p
1 1
② 200 V 70% p
2 2
③ 350 V 50% p
3 3
下列说法错误的是( )
A.初始反应速率:①>② B.p:p=35:37
1 2
C.容器容积:V>V D.若从实验②的容器中取走部分 ,SiHCl 的转化率不变
1 3 3
3.高炉炼铁中的一个反应为FeO(s)+CO(g) Fe(s)+CO (g) ΔH>0,在1100℃下,若CO起始浓
2
度为1.2mol/L,10min后达到平衡时 的体积分数为 ,下列说法错误的是( )
A.1100℃下,此反应的平衡常数
B.达到平衡过程中,反应的平均速率为v(CO)=0.02 mol·L-1·min-1
C.达到平衡后,若增大c(CO),则达到新平衡时, 增大
2
D.测得某时刻c(CO)=0.8mol/L,则此时
4.向体积均为1L的两恒容容器中分别充入2molX和1molY发生反应:2X(g)+Y(g) Z(g)
ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法不正确
的是( )
A.a点平衡常数: B.气体的总物质的量:n<n
a c
C.ΔH<0 D.平衡转化率:甲<乙5.一定温度下,在3个体积均为1.0L的恒容密闭容器中反应:CO(g)+2H(g) CHOH(g),达到
2 3
平衡,下列说法不正确的是( )
物质的起始浓度 物质的平衡浓度
容
温度/K
器
Ⅰ 400 0.20 0.10 0 0.080
Ⅱ 400 0.40 0.20 0
Ⅲ 500 0 0 0.10 0.025
A.该反应的正反应为放热反应
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小
C.达到平衡时,容器Ⅱ中c (H )大于容器Ⅲ中c (H )的两倍
2 2
D.达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的大
6.(2025·山西省部分学校联考)在甲、乙均为 的恒容密闭容器中均充入1molCO (g)和3molH (g),
2 2
在恒温和绝热两种条件下仅发生反应:CO(g)+3H(g) CHOH(g)+HO(g) ΔH=-49kJ·mol−1,测得
2 2 3 2
压强变化如图所示。下列说法正确的是( )
A.放出的热量:Q>Q
a b
B.乙容器中0~5min内v(H O)=0.4 mol·L-1·min-1
2
C.CO 的转化率:c>b
2
D.平衡常数:K>K
b c
7.(2025·江西省南昌市高三联考)恒温20L密闭容器内发生2NO(g)+2CO(g) 2CO(g)+N(g)
2 2
ΔH=-746.8kJ·mol−1,一开始投入一定量的CO和NO,测得NO、CO的物质的量浓度随时间变化的关系如
图所示。下列说法错误的是( )A.该反应是熵减小的反应,低温有利于自发进行
B.a点理论上化学反应释放的能量约为4.1kJ
C.0~4s,氮气的反应速率v(N )=2.25 mol·L-1·s-1
2
D.b点氮气的体积分数约为8.9%
8.(2025·湖南省炎德英才名校联考联合体高三第四次联考)某温度下,向1L刚性密闭容器中充入
1molN 和适量H 合成氨,化学反应为N(g)+3H(g) 2NH (g) ΔH<0,,测得平衡体系中,各物质浓度
2 2 2 2 3
关系如图所示。
下列叙述错误的是( )
A.L 代表c(NH )变化趋势 B.平衡常数K=0.2L2·mol-2
1 3
C.b点中x=12 D.b点沿L 移向d点时,平衡正移
1
1.(2024·江苏卷,5,3分)下列说法正确的是( )
A.豆科植物固氮过程中,固氮酶能提高该反应的活化能B.C H 与O 反应中,Ag催化能提高生成CHCHO的选择性
2 4 2 3
C.HO 制O 反应中,MnO 能加快化学反应速率
2 2 2 2
D.SO 与O 反应中,VO 能减小该反应的焓变
2 2 2 5
2.(2023•北京卷,4)下列事实能用平衡移动原理解释的是( )
A.HO 溶液中加入少量MnO 固体,促进HO 分解
2 2 2 2 2
B.密闭烧瓶内的NO 和NO 的混合气体,受热后颜色加深
2 2 4
C.铁钉放入浓HNO 中,待不再变化后,加热能产生大量红棕色气体
3
D.锌片与稀HSO 反应过程中,加入少量CuSO 固体,促进H 的产生
2 4 4 2
3.(2023•海南卷,13)工业上苯乙烯的生产主要采用乙苯脱氢工艺:C HCHCH(g)
6 5 2 3
C HCH=CH(g)+H(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图
6 5 2 2
所示。下列说法正确的是( )
A.曲线①表示的是逆反应的v-t关系 B.t 时刻体系处于平衡状态
2
C.反应进行到t 时,Q>K (Q为浓度商) D.催化剂存在时,v、v 都增大
1 1 2
4.(2023•湖南卷,13)向一恒容密闭容器中加入1molCH 和一定量的HO,发生反应:CH(g)+ H O(g)
4 2 4 2
CO (g)+ 3H (g)。CH 的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列
2 4
说法错误的是( )A.x<x
1 2
B.反应速率:v <vc
正b 正
C.点a、b、c对应的平衡常数:K<K =K
a b c
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
5.(2021•浙江6月选考)一定温度下:在NO 的四氯化碳溶液(100mL)中发生分解反应:2NO
2 5 2 5
4NO +O 。在不同时刻测量放出的O 体积,换算成NO 浓度如下表:
2 2 2 2 5
171 282
0 600 1200 2220 x
0 0
1.40 0.96 0.66 0.48 0.35 0.24 0.12
下列说法正确的是( )
A.600~1200 s,生成NO 的平均速率为5.0×10-4mol·L-1·s-1
2
B.反应2220 s时,放出的O 体积为11.8L(标准状况)
2
C.反应达到平衡时,v (N O)=2v (NO )
正 2 5 逆 2
D.推测上表中的x为3930
6.(2022·河北,16节选](2)工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.CH (g)+HO(g) CO(g)+3H(g)
4 2 2
Ⅱ.CO(g)+HO(g) CO(g)+H(g)
2 2 2
恒温恒压条件下,1 mol CH (g)和1 mol H O(g)反应达平衡时,CH(g)的转化率为a,CO(g)的物质的量
4 2 4 2
为b mol,则反应Ⅰ的平衡常数K=__________(写出含有a、b的计算式;对于反应mA(g)+nB(g)
x
pC(g)+qD(g), ,x为物质的量分数)。其他条件不变,HO(g)起始量增加到5 mol,达平衡
2
时,a=0.90,b=0.65,平衡体系中H(g)的物质的量分数为__________(结果保留两位有效数字)。
2
7.(2022•福建卷,13节选)异丙醇(C HO)可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯
3 8
(C H)的工业化技术已引起人们的关注,其主要反应如下:
3 6
Ⅰ. C HO(g) C H(g)+HO(g) ΔH =+52kJ·mol−1
3 8 3 6 2 1
Ⅱ. 2C H(g) C H (g) ΔH =-97kJ·mol−1
3 6 6 12 2
(2)在 下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
反应时间 0 4 8 12 t 20
HO浓度/ppm 0 2440 3200 3600 4000 4100
2① 内,v(C HO)= _______ ;
3 8
②t_______16(填“>”“<”或“=”)。
(4)在一定条件下,若反应Ⅰ、Ⅱ的转化率分别为98%和40%,则丙烯的产率为_______。
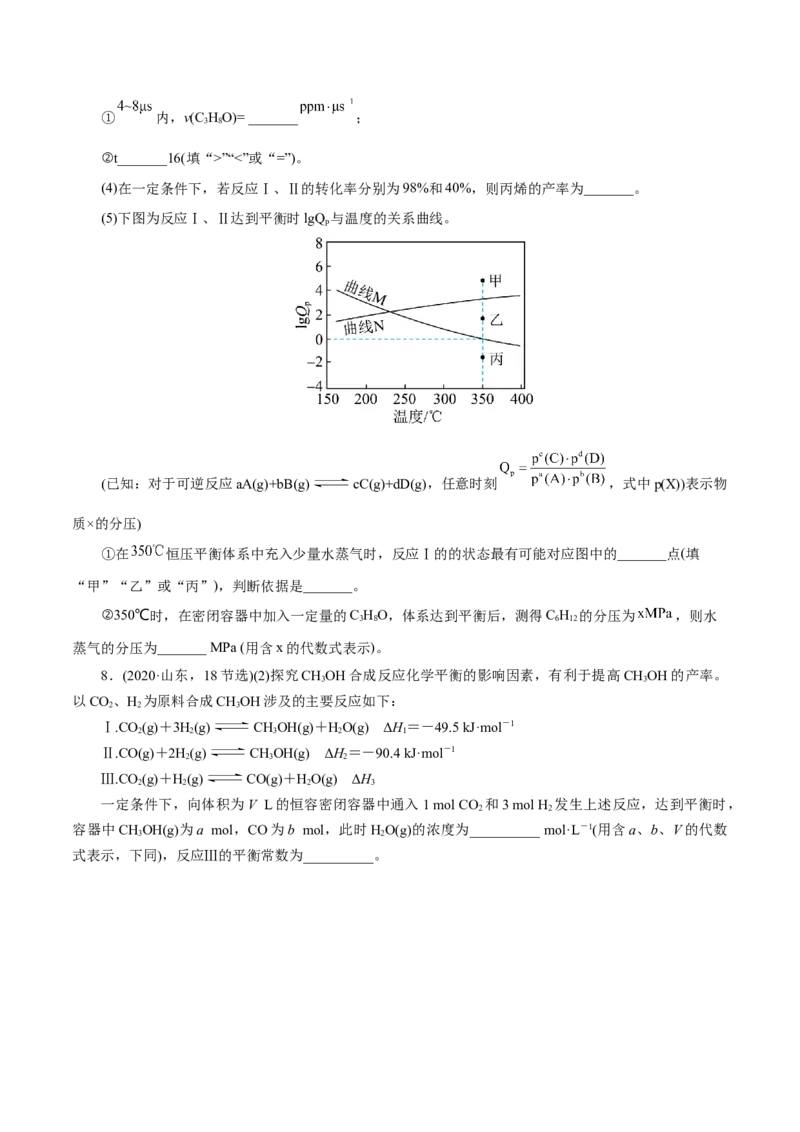
(5)下图为反应Ⅰ、Ⅱ达到平衡时lgQ 与温度的关系曲线。
p
(已知:对于可逆反应aA(g)+bB(g) cC(g)+dD(g),任意时刻 ,式中p(X))表示物
质×的分压)
①在 恒压平衡体系中充入少量水蒸气时,反应Ⅰ的的状态最有可能对应图中的_______点(填
“甲”“乙”或“丙”),判断依据是_______。
②350℃时,在密闭容器中加入一定量的C HO,体系达到平衡后,测得C H 的分压为 ,则水
3 8 6 12
蒸气的分压为_______ MPa (用含x的代数式表示)。
8.(2020·山东,18节选)(2)探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。
3 3
以CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.CO (g)+3H(g) CHOH(g)+HO(g) ΔH=-49.5 kJ·mol-1
2 2 3 2 1
Ⅱ.CO(g)+2H(g) CHOH(g) ΔH=-90.4 kJ·mol-1
2 3 2
Ⅲ.CO (g)+H(g) CO(g)+HO(g) ΔH
2 2 2 3
一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO 和3 mol H 发生上述反应,达到平衡时,
2 2
容器中CHOH(g)为a mol,CO为b mol,此时HO(g)的浓度为__________ mol·L-1(用含a、b、V的代数
3 2
式表示,下同),反应Ⅲ的平衡常数为__________。