文档内容
专题 08 化学反应与能量变化
一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)
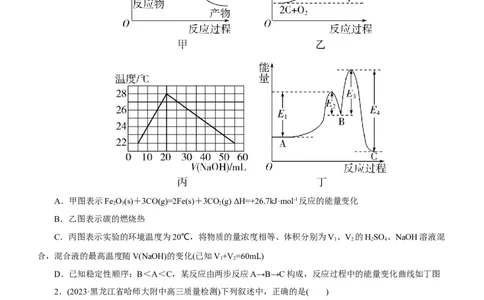
1.(2023·河南省濮阳市南乐一高高三月考)下列示意图表示正确的是( )
A.甲图表示Fe O(s)+3CO(g)=2Fe(s)+3CO(g) ΔH=+26.7kJ·mol-1反应的能量变化
2 3 2
B.乙图表示碳的燃烧热
C.丙图表示实验的环境温度为20℃,将物质的量浓度相等、体积分别为V、V 的HSO 、NaOH溶液混
1 2 2 4
合,混合液的最高温度随V(NaOH)的变化(已知V+V =60mL)
1 2
D.已知稳定性顺序:B<A<C,某反应由两步反应A→B→C构成,反应过程中的能量变化曲线如丁图
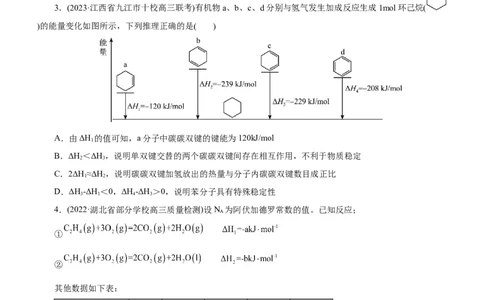
2.(2023·黑龙江省哈师大附中高三质量检测)下列叙述中,正确的是( )A.由图1可知H 的燃烧热为
2
B.由图2可知ΔH=ΔH+ΔH
1 2 3
C.若将0.5molN 和1.5mol H 置于某密闭容器中充分反应生成NH (g)放热 ,则其热化学方程式为:
2 2 3
N(g)+ 3H (g) 2NH (g) ΔH=-38.6 kJ·mol-1
2 2 3
D.已知25℃、101KPa条件下:4Al(s)+3O(g)=2Al O(s) ΔH= -2834.9kJ·mol-1,4Al(s)+3O(g)=2Al O(s)
2 2 3 3 2 3
ΔH= -3119.1kJ·mol-1,则O 比O 稳定
3 2
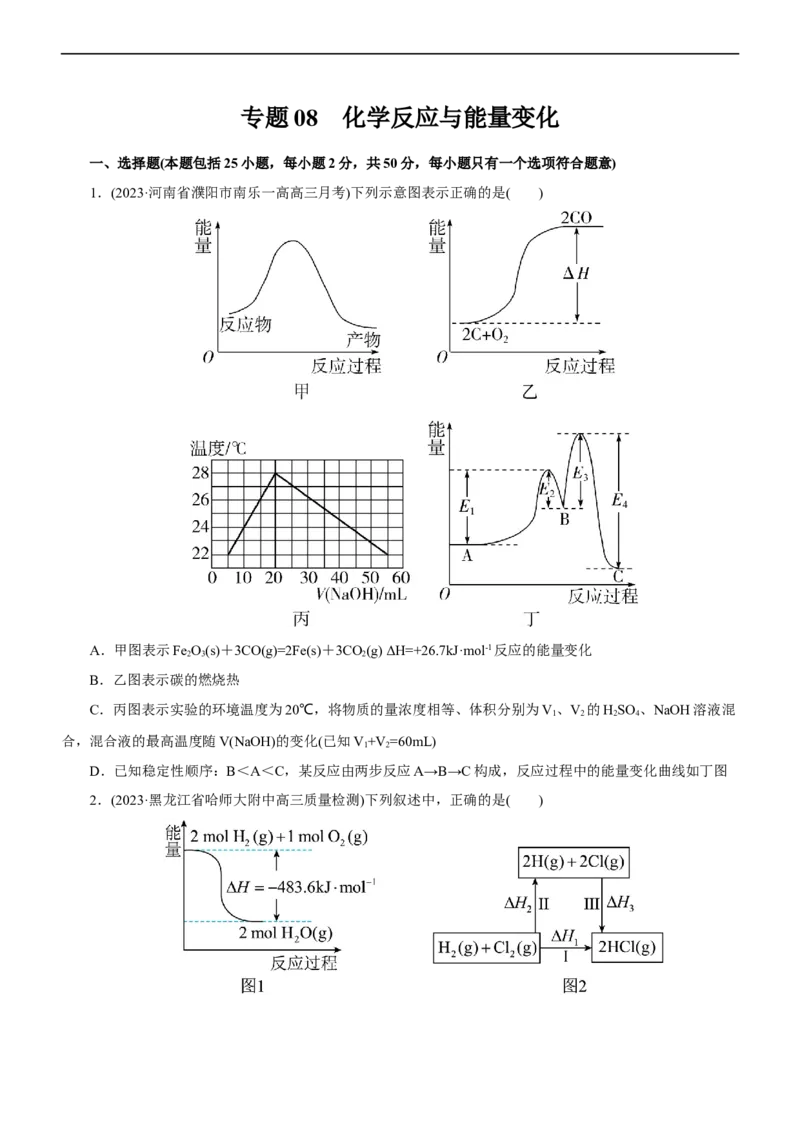
3.(2023·江西省九江市十校高三联考)有机物a、b、c、d分别与氢气发生加成反应生成1mol环己烷(
)的能量变化如图所示,下列推理正确的是( )
A.由ΔH 的值可知,a分子中碳碳双键的键能为120kJ/mol
1
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,不利于物质稳定
2 3
C.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
4.(2022·湖北省部分学校高三质量检测)设N 为阿伏加德罗常数的值。已知反应;
A
①
②
其他数据如下表:
化学键 C=O O=O C-H O-H C=C
键能/( ) 798 x 413 463 610
下列说法正确的是( )
A.aΔH
2 2 2 2 1 2 2 2 2 1 2
C.4Al(s)+3O (g)=2Al O(s) ΔH ,4Fe(s)+3O (g)=2Fe O(s) ΔH ,则有ΔH<ΔH
2 2 3 1 2 2 3 2 1 2
D.C(s)+O(g)=CO (g) ΔH ,C(s)+O(g)=CO(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 1 2
7.(2022·黑龙江省龙东地区四校高三联考)煤的液化可以合成甲醇。下列有关说法正确的是( )
①“气化”: C(s)+2HO(g)=CO(g)+2H(g) ΔH=+90.1kJ·mol-1;
2 2 2 1
②催化液化Ⅰ:CO(g)+3H(g)= CH OH(g)+H O(g) ΔH = -49.0kJ•mol-1;
2 2 3 2 2
③催化液化Ⅱ:CO(g)+2H(g)=CH OH(g)+ O(g) ΔH = akJ•mol-1;
2 2 3 2 3
A.催化液化Ⅰ中使用催化剂,反应的活化能E、ΔH 都减小
a 2
B.反应C(s)+HO(g) +H (g)=CH OH(g) ΔH= 41.1 kJ•mol-1
2 2 3
C.ΔH>ΔH
2 3
D.KOH为电解质溶液的甲醇燃料电池中负极的电极反应为:CHOH-6e-+6OH-= CO+5H O
3 2 2
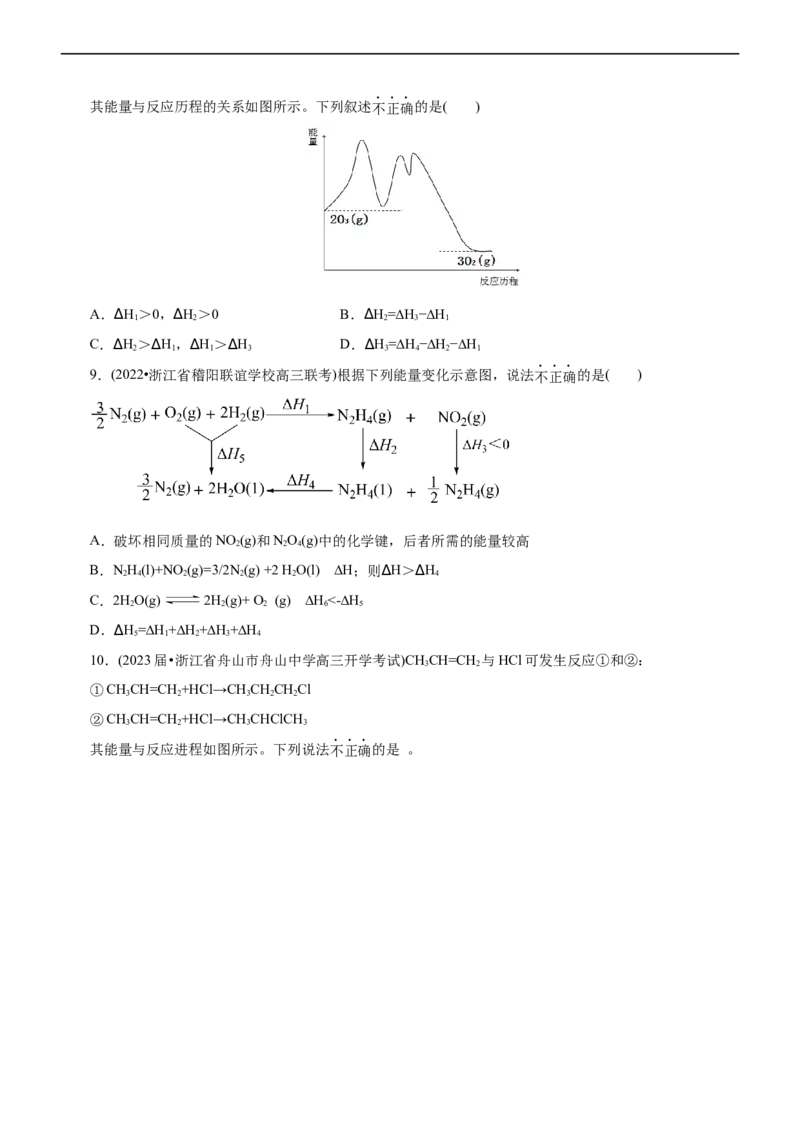
8.(2022•浙江省湖州、衢州、丽水三地市高三教学质量检测)NO催化O 分解的反应机理与总反应为:
3
第一步:O(g)+NO(g)→O (g)+NO g) ∆H
3 2 2( 1
第二步:NO (g)→NO(g)+O(g) ∆H
2 2
第三步:O(g)+O (g)→2O (g) ∆H
3 2 3
总反应:2O(g) →3Q (g) ∆H
3 2 4其能量与反应历程的关系如图所示。下列叙述不正确的是( )
A.∆H>0,∆H>0 B.∆H=∆H−∆H
1 2 2 3 1
C.∆H>∆H,∆H>∆H D.∆H=∆H−∆H−∆H
2 1 1 3 3 4 2 1
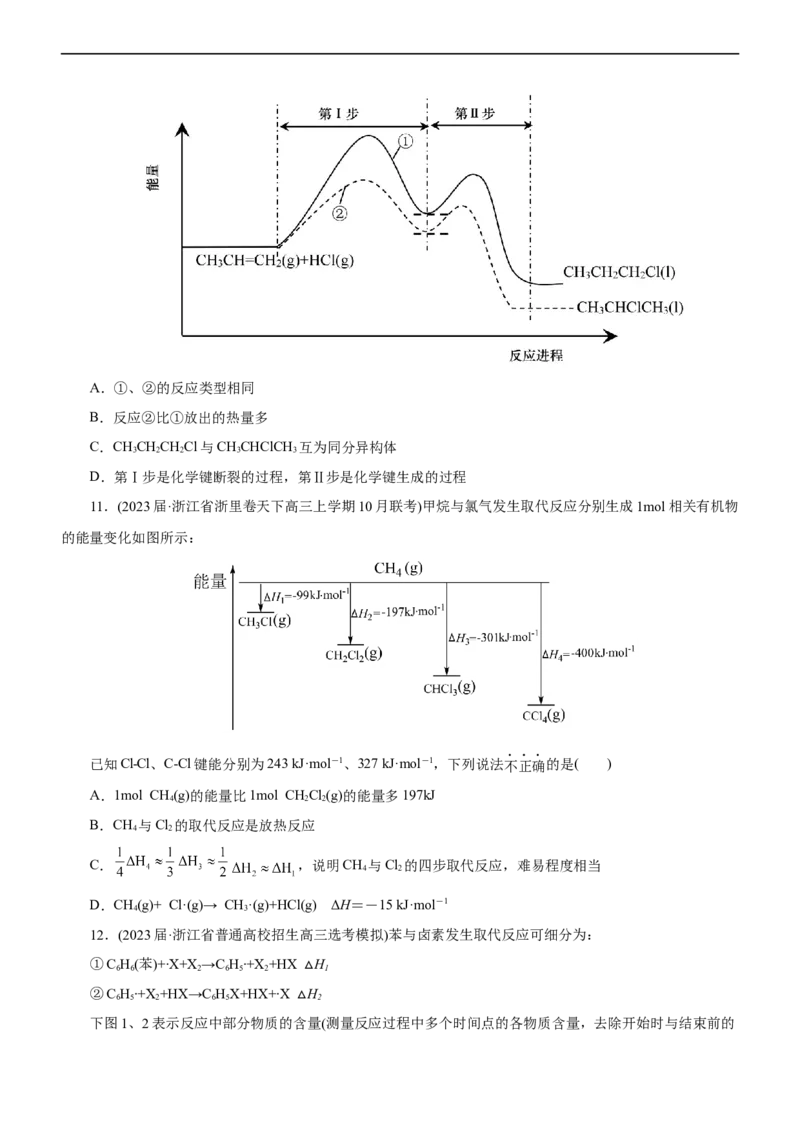
9.(2022•浙江省稽阳联谊学校高三联考)根据下列能量变化示意图,说法不正确的是( )
A.破坏相同质量的NO (g)和NO(g)中的化学键,后者所需的能量较高
2 2 4
B.NH(l)+NO(g)=3/2N (g) +2 HO(l) ∆H;则∆H>∆H
2 4 2 2 2 4
C.2HO(g) 2H(g)+ O (g) ∆H<-∆H
2 2 2 6 5
D.∆H=∆H+∆H+∆H+∆H
5 1 2 3 4
10.(2023届•浙江省舟山市舟山中学高三开学考试)CHCH=CH 与HCl可发生反应①和②:
3 2
①CHCH=CH+HCl→CH CHCHCl
3 2 3 2 2
②CHCH=CH+HCl→CH CHClCH
3 2 3 3
其能量与反应进程如图所示。下列说法不正确的是 。A.①、②的反应类型相同
B.反应②比①放出的热量多
C.CHCHCHCl与CHCHClCH 互为同分异构体
3 2 2 3 3
D.第Ⅰ步是化学键断裂的过程,第Ⅱ步是化学键生成的过程
11.(2023届·浙江省浙里卷天下高三上学期10月联考)甲烷与氯气发生取代反应分别生成1mol相关有机物
的能量变化如图所示:
已知Cl-Cl、C-Cl键能分别为243 kJ·mol-1、327 kJ·mol-1,下列说法不正确的是( )
A.1mol CH(g)的能量比1mol CHCl(g)的能量多197kJ
4 2 2
B.CH 与Cl 的取代反应是放热反应
4 2
C. ,说明CH 与Cl 的四步取代反应,难易程度相当
4 2
D.CH(g)+ Cl·(g)→ CH·(g)+HCl(g) ΔH=-15 kJ·mol-1
4 3
12.(2023届·浙江省普通高校招生高三选考模拟)苯与卤素发生取代反应可细分为:
①C H(苯)+∙X+X→C H∙+X +HX H
6 6 2 6 5 2 1
②C
6
H
5
∙+X
2
+HX→C
6
H
5
X+HX+∙X △H
2
下图1、2表示反应中部分物质的含△量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。
X Cl Br
H(kJ∙mol-1) 10 20
1
△H(kJ∙mol-1) -111 -100
2
下列说法正确△的是( )
A.可推知H-Cl键的键能比H-Br键的键能大10 kJ∙mol-1
B.1mol苯与1mol氯气反应将会向环境释放101kJ热量
C.使用催化剂后会改变△H,但不会改变△H+ H
1 1 2
D.反应②为总反应的决速步,催化剂的机理为降△低反应②的活化能
13.(2023届·浙江省温州市高三第一次适应性考试)标准状态下,1mol纯物质的相对能量及解离为气态原
子时所消耗的能量如下表所示:
物质 O(g) N(g) NO g) C(s,石墨) CH(g) CO(g)
2 2 2 4 2
相对能量/ kJ·mol−1 0 0 x 0 -75 -393.5
解离总耗能/kJ 498 946 632 717 1656 y
下列说法正确的是( )
A.x =180
B.逐级断开CH(g)中的每摩尔C—H所消耗的能量均为414kJ
4
C.解离每摩尔C(s,石墨)中的碳碳键平均耗能为239kJ
D.根据NO(g)+CH(g) CO(g)+N(g)+2H O(g)的ΔH可计算出H—O键能
4 2 2
14.(2023届·浙江省部分校高三开学摸底考试)物质 、 与 的相对能量关如下,下列有
关说法错误的是( )A.三种物质中 最稳定
B.过程③的ΔH=+211kJ·mol−1
C.由图可推知,发生消去反应①或②时,环戊烷断键吸收的能量高于环戊烯断键吸收的能量
D.物质变化过程中所放出或吸收的热量的多少与路径无关
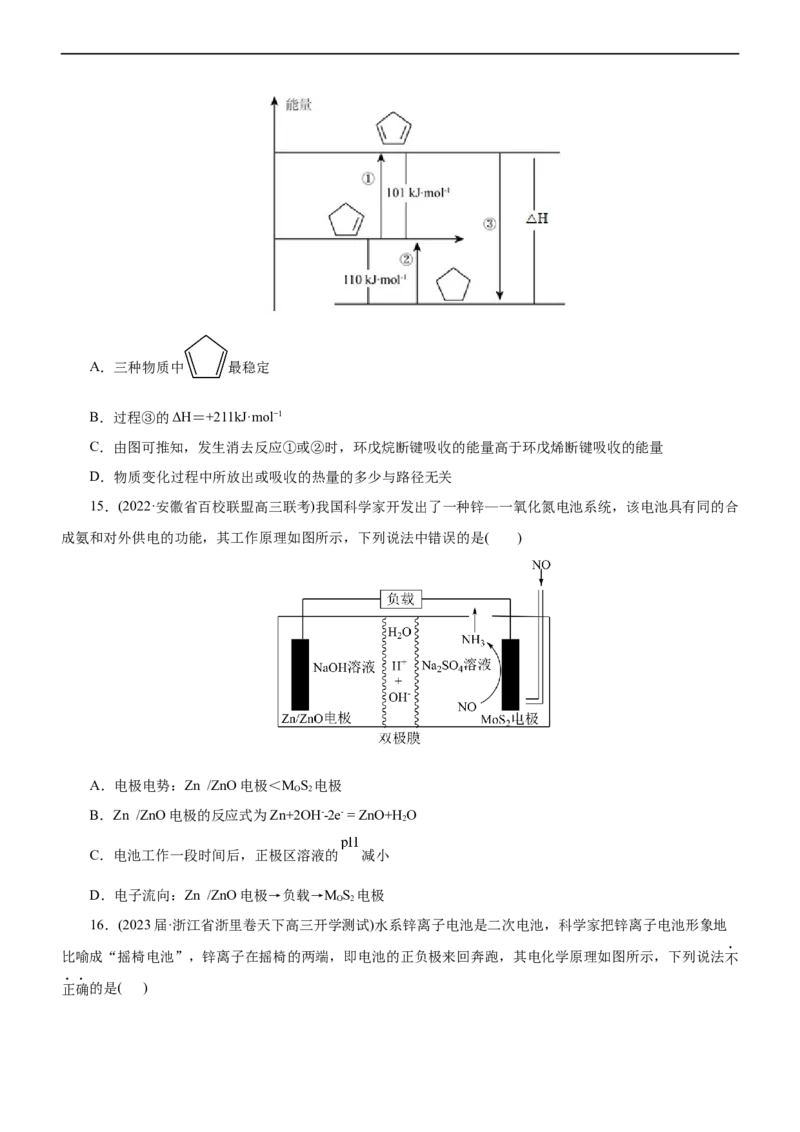
15.(2022·安徽省百校联盟高三联考)我国科学家开发出了一种锌—一氧化氮电池系统,该电池具有同的合
成氨和对外供电的功能,其工作原理如图所示,下列说法中错误的是( )
A.电极电势:Zn /ZnO电极<M S 电极
O 2
B.Zn /ZnO电极的反应式为Zn+2OH--2e- =ZnO+HO
2
C.电池工作一段时间后,正极区溶液的 减小
D.电子流向:Zn /ZnO电极→负载→M S 电极
O 2
16.(2023届·浙江省浙里卷天下高三开学测试)水系锌离子电池是二次电池,科学家把锌离子电池形象地
比喻成“摇椅电池”,锌离子在摇椅的两端,即电池的正负极来回奔跑,其电化学原理如图所示,下列说法不
正确的是( )A.锌离子从MnO 隧道结构中脱出,此时ZnMn O 为阳极
2 2 4
B.锌失去电子变为锌离子,嵌入MnO 的隧道中,能量转化形式:电能→化学能
2
C.Zn发生氧化反应过程中,溶液中 浓度不变
D.水系锌离子二次电池的总反应式:Zn+2MnO ZnMn O
2 2 4
17.(2023届•浙江省舟山市普陀中学高三返校考试)苯甲醛(C HCHO)是生产除草剂野燕枯、植物生长调
6 5
节剂抗倒胺的中间体。某研究团队以 为电极材料,由苯甲醇(C HCHOH)电催化氧化合成苯甲醛(C HCHO)
6 5 2 6 5
的装置如图所示。下列说法错误的是( )
A.M极的电势高于N极的电势
B.隔膜适宜选用阴离子交换膜
C.阳极区的总反应为C HCHOH-2e-=C HCHO+2H+
6 5 2 6 5
D.MnO 是苯甲醇电催化氧化合成苯甲醛的中间产物
2
18.(2023届•浙江省舟山市舟山中学高三开学考试)电解合成1 ,2-二氯乙烷的实验装置如图所示。下列
说法中不正确的是( )A.a为电源正极
B.该装置总反应为CH =CH +2NaCl+2H O ClCH CHCl+2NaOH+H
2 2 2 2 2 2
C.X、Y依次为阳离子交换膜、阴离子交换膜
D.液相反应为CH =CH +2CuCl = ClCH CHCl+ 2CuCl(s)
2 2 2 2 2
19.(2023·河北省邯郸市部分学校高三联考)香港城市大学化学工作者首次提出了Al-N 电池(如图),该电
2
池使用N 为原料,以离子液体(Al Cl--AlCl-)为电解质,既实现了能量的存储,又实现了AlN的生产, 和
2 2 7 4
碱反应能产生NH ,可进一步生产氮肥。下列说法错误的是( )
3
A.Al极为负极,发生氧化反应
B.电池总反应为2Al+N =2
2
C.石墨烯电极反应式为8Al Cl-+N +6e- =2AlN+14AlCl-
2 7 2 4
D.生成标准状况下33.6LNH ,电池中转移3mol电子
3
20.(2023·浙江省9+1联盟高三选考模拟)高电压水系锌-有机混合液流电池的装置如图所示。下列说法不
正确的是( )A.放电时,正极反应式为2FQ+2e-+2H+═FQH
2
B.充电时,1molFQH 转化为 转移 电子
2
C.放电时,中性电解质中 向左侧迁移
D.充电时,正极区溶液的 减小
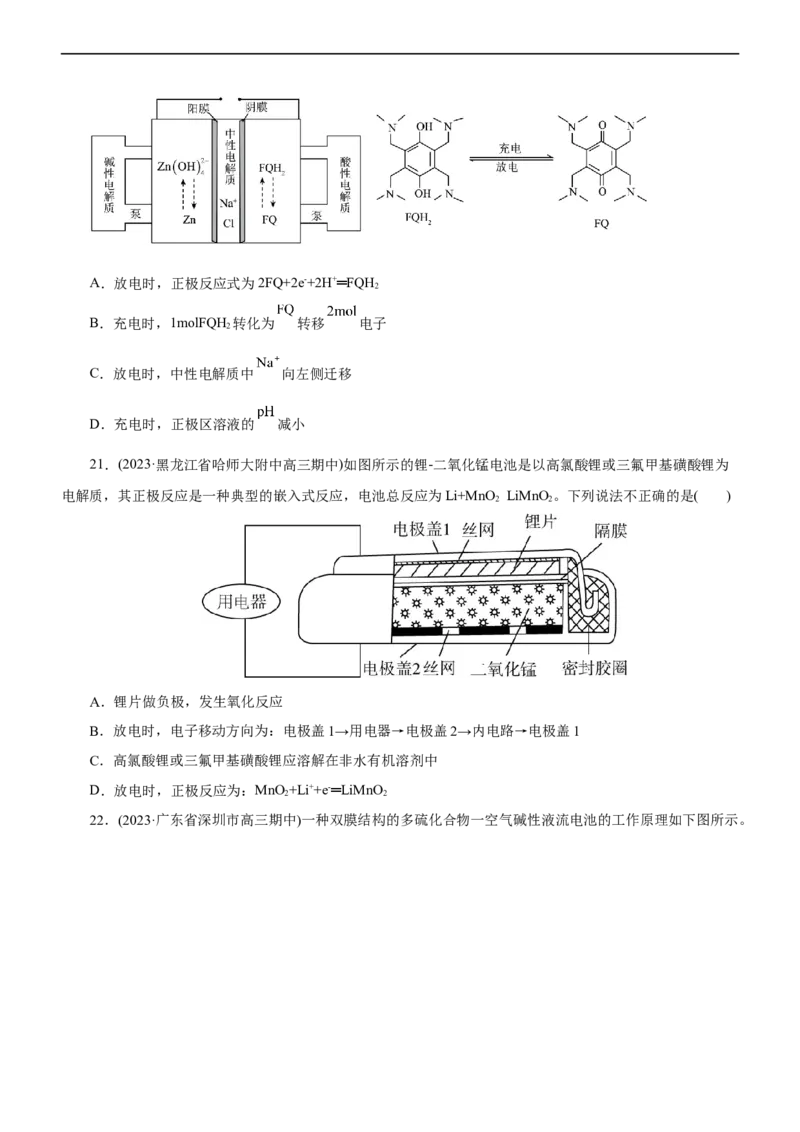
21.(2023·黑龙江省哈师大附中高三期中)如图所示的锂-二氧化锰电池是以高氯酸锂或三氟甲基磺酸锂为
电解质,其正极反应是一种典型的嵌入式反应,电池总反应为Li+MnO LiMnO 。下列说法不正确的是( )
2 2
A.锂片做负极,发生氧化反应
B.放电时,电子移动方向为:电极盖1→用电器→电极盖2→内电路→电极盖1
C.高氯酸锂或三氟甲基磺酸锂应溶解在非水有机溶剂中
D.放电时,正极反应为:MnO +Li++e-═LiMnO
2 2
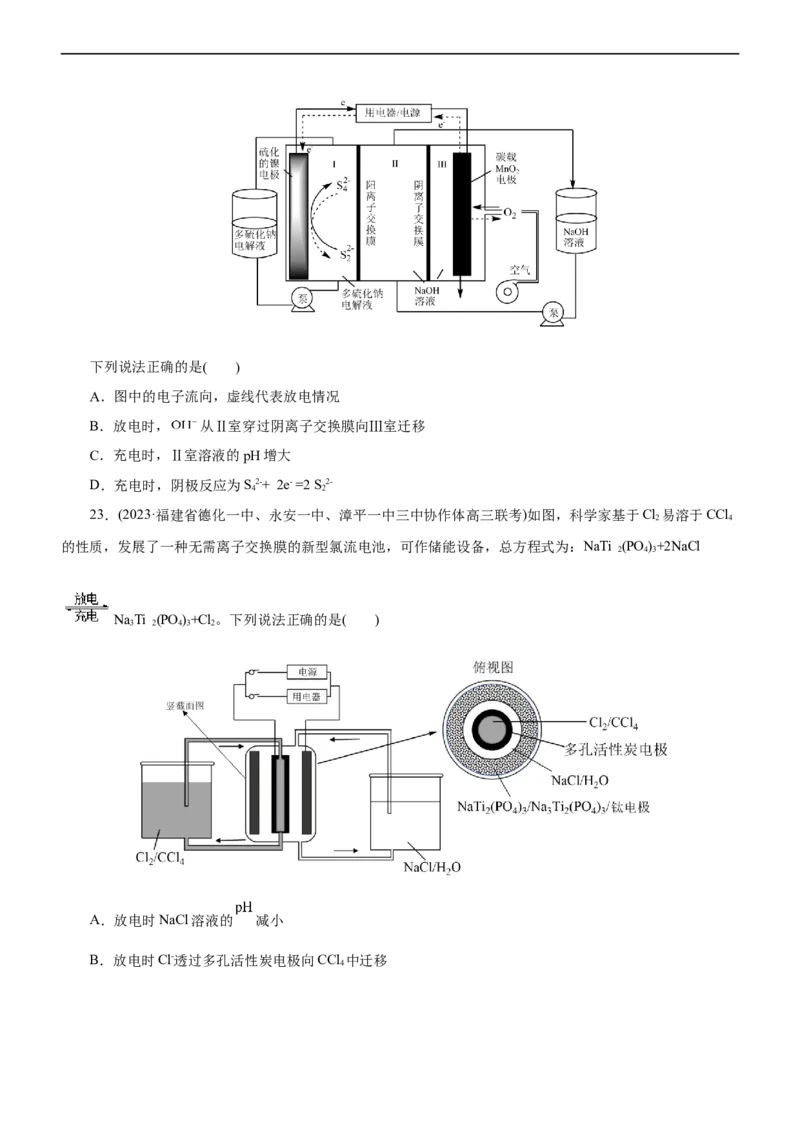
22.(2023·广东省深圳市高三期中)一种双膜结构的多硫化合物一空气碱性液流电池的工作原理如下图所示。下列说法正确的是( )
A.图中的电子流向,虚线代表放电情况
B.放电时, 从Ⅱ室穿过阴离子交换膜向Ⅲ室迁移
C.充电时,Ⅱ室溶液的pH增大
D.充电时,阴极反应为S2-+ 2e- =2 S2-
4 2
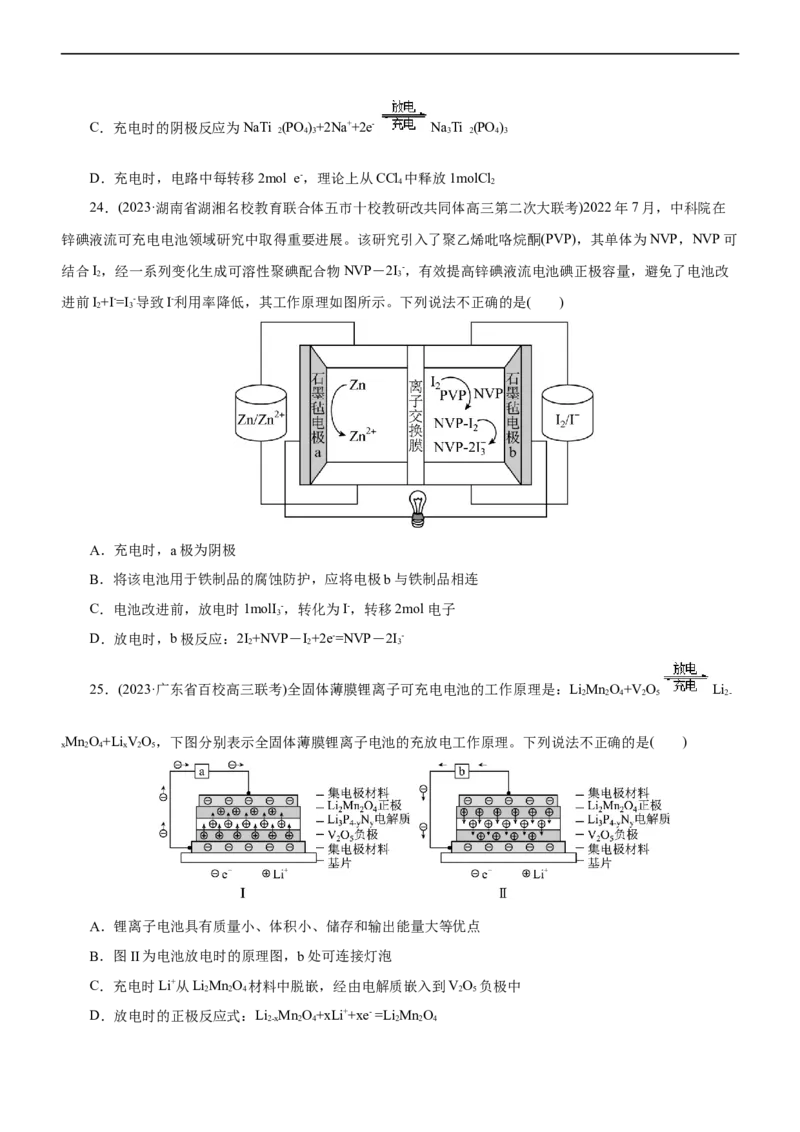
23.(2023·福建省德化一中、永安一中、漳平一中三中协作体高三联考)如图,科学家基于Cl 易溶于CCl
2 4
的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备,总方程式为:NaTi (PO )+2NaCl
2 4 3
NaTi (PO )+Cl。下列说法正确的是( )
3 2 4 3 2
A.放电时NaCl溶液的 减小
B.放电时Cl-透过多孔活性炭电极向CCl 中迁移
4C.充电时的阴极反应为NaTi (PO )+2Na++2e- NaTi (PO )
2 4 3 3 2 4 3
D.充电时,电路中每转移2mol e-,理论上从CCl 中释放1molCl
4 2
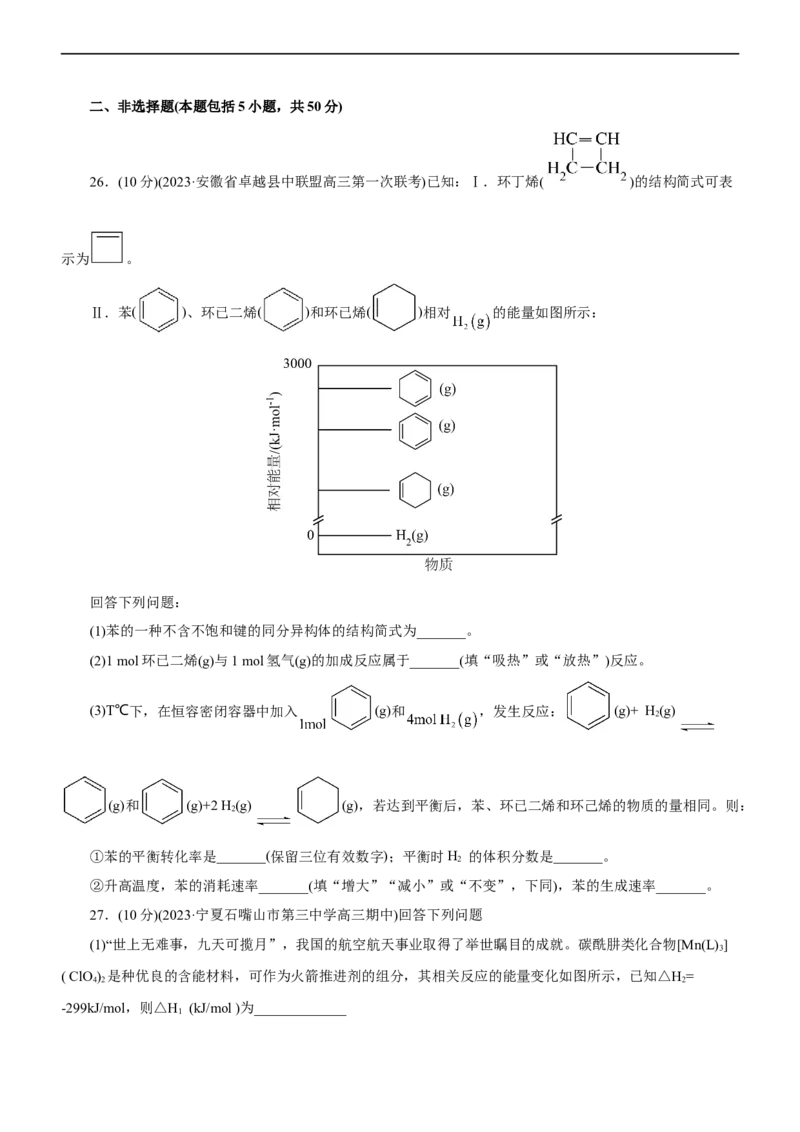
24.(2023·湖南省湖湘名校教育联合体五市十校教研改共同体高三第二次大联考)2022年7月,中科院在
锌碘液流可充电电池领域研究中取得重要进展。该研究引入了聚乙烯吡咯烷酮(PVP),其单体为NVP,NVP可
结合I,经一系列变化生成可溶性聚碘配合物NVP-2I-,有效提高锌碘液流电池碘正极容量,避免了电池改
2 3
进前I+I-=I -导致I-利用率降低,其工作原理如图所示。下列说法不正确的是( )
2 3
A.充电时,a极为阴极
B.将该电池用于铁制品的腐蚀防护,应将电极b与铁制品相连
C.电池改进前,放电时1molI -,转化为I-,转移2mol电子
3
D.放电时,b极反应:2I+NVP-I+2e-=NVP-2I-
2 2 3
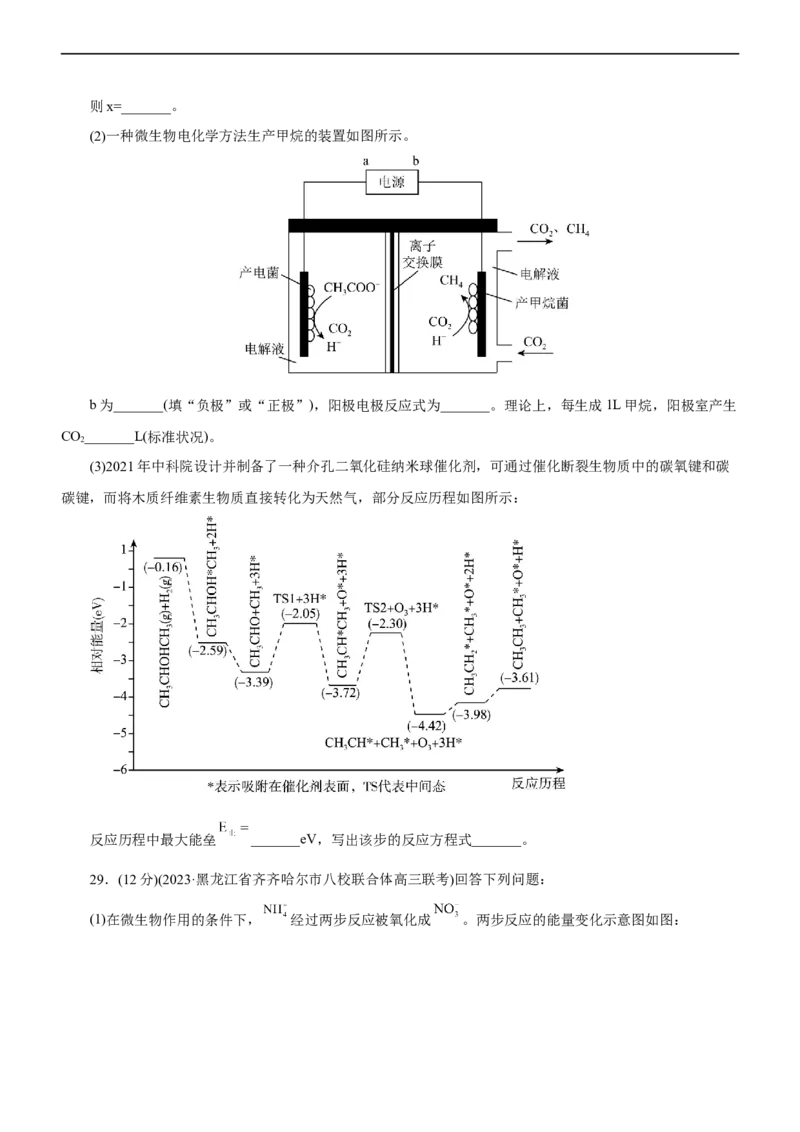
25.(2023·广东省百校高三联考)全固体薄膜锂离子可充电电池的工作原理是:LiMnO+VO Li
2 2 4 2 5 2-
MnO+Li VO,下图分别表示全固体薄膜锂离子电池的充放电工作原理。下列说法不正确的是( )
x 2 4 x 2 5
A.锂离子电池具有质量小、体积小、储存和输出能量大等优点
B.图II为电池放电时的原理图,b处可连接灯泡
C.充电时Li+从LiMnO 材料中脱嵌,经由电解质嵌入到VO 负极中
2 2 4 2 5
D.放电时的正极反应式:Li MnO+xLi++xe- =LiMnO
2-x 2 4 2 2 4二、非选择题(本题包括5小题,共50分)
26.(10分)(2023·安徽省卓越县中联盟高三第一次联考)已知:Ⅰ.环丁烯( )的结构简式可表
示为 。
Ⅱ.苯( )、环已二烯( )和环已烯( )相对 的能量如图所示:
回答下列问题:
(1)苯的一种不含不饱和键的同分异构体的结构简式为_______。
(2)1 mol环已二烯(g)与1 mol氢气(g)的加成反应属于_______(填“吸热”或“放热”)反应。
(3)T℃下,在恒容密闭容器中加入 (g)和 ,发生反应: (g)+ H(g)
2
(g)和 (g)+2 H (g) (g),若达到平衡后,苯、环已二烯和环己烯的物质的量相同。则:
2
①苯的平衡转化率是_______(保留三位有效数字);平衡时H 的体积分数是_______。
2
②升高温度,苯的消耗速率_______(填“增大”“减小”或“不变”,下同),苯的生成速率_______。
27.(10分)(2023·宁夏石嘴山市第三中学高三期中)回答下列问题
(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类化合物[Mn(L) ]
3
( ClO ) 是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知△H=
4 2 2
-299kJ/mol,则△H (kJ/mol )为_____________
1(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO 利用的研究热点之一、
4 2 2
该重整反应体系主要涉及以下反应:
(a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
(b)CO (g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
(c)CH(g) C(s)+2H(g) ∆H
4 2 3
(d)2CO(g) CO(g)+C(s) ∆H
2 4
(e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(3)用H 还原SiCl 蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,则该反应的热
2 4
化学方程式为___________________________________。
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的HSO 稀溶液反应放出11.46kJ的热量。请写出KOH的稀
2 4
溶液与的HSO 稀溶液发生中和反应,表示中和热的热化学方程式为___________________。
2 4
(5)1mol CH (g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催化剂作用下,
4
CH 可以还原SO 生成单质S(g)、HO(g)和CO,写出该反应的热化学方程式:________________。
4 2 2 2
28.(10分)(2023·山东省曹县一中高三第二次月考)甲烷是常见的燃料,可作为化工原料生产一系列化工有
机产品,可用多种方法进行人工合成。回答下列问题:
(1) CO 加氢制备甲烷:CO(g)+4H(g) CH (g)+2HO(g) ΔH=-164.7kJ/mol。已知:
2 2 2 4 2
,298K时,几种气态物质的标准摩尔生成焓如下表:
物质 CO CO CH (g) H(g)
2 2 4 2
-393.5 -241.8 x 0则x=_______。
(2)一种微生物电化学方法生产甲烷的装置如图所示。
b为_______(填“负极”或“正极”),阳极电极反应式为_______。理论上,每生成1L甲烷,阳极室产生
CO_______L(标准状况)。
2
(3)2021年中科院设计并制备了一种介孔二氧化硅纳米球催化剂,可通过催化断裂生物质中的碳氧键和碳
碳键,而将木质纤维素生物质直接转化为天然气,部分反应历程如图所示:
反应历程中最大能垒 _______eV,写出该步的反应方程式_______。
29.(12分)(2023·黑龙江省齐齐哈尔市八校联合体高三联考)回答下列问题:
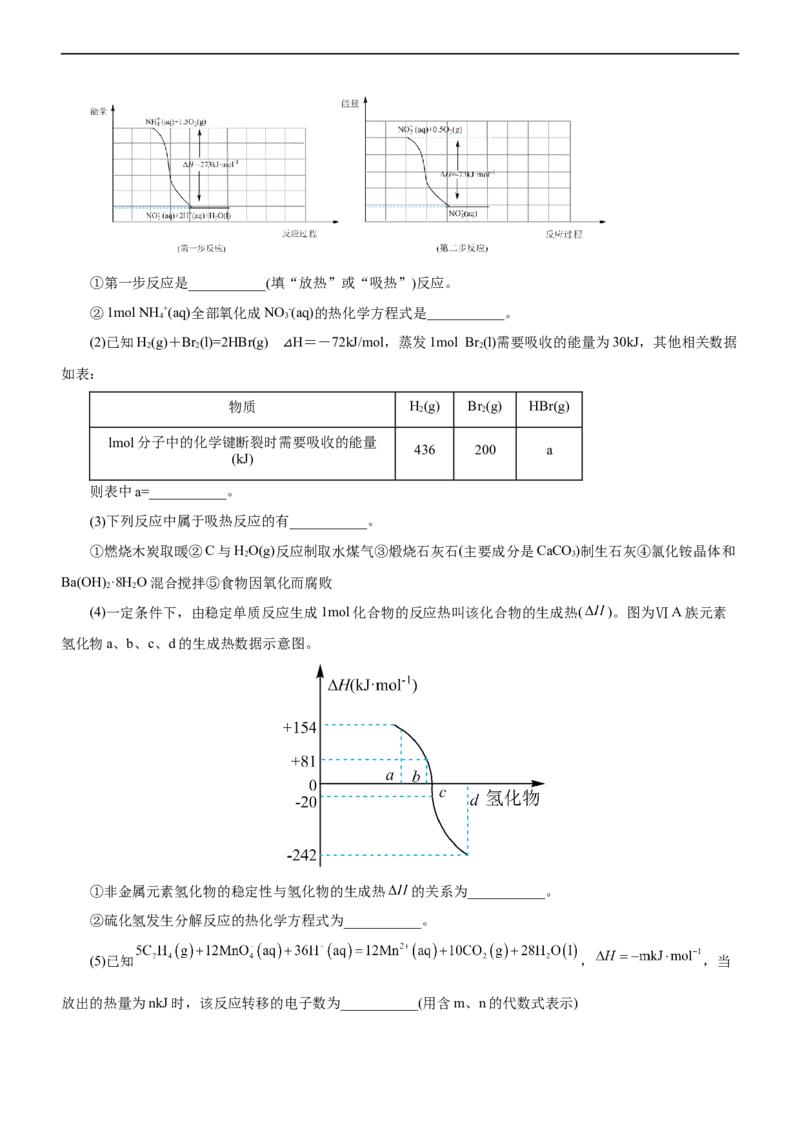
(1)在微生物作用的条件下, 经过两步反应被氧化成 。两步反应的能量变化示意图如图:①第一步反应是___________(填“放热”或“吸热”)反应。
②1mol NH +(aq)全部氧化成NO -(aq)的热化学方程式是___________。
4 3
(2)已知H(g)+Br(l)=2HBr(g) H=-72kJ/mol,蒸发1mol Br(l)需要吸收的能量为30kJ,其他相关数据
2 2 2
如表: △
物质 H(g) Br(g) HBr(g)
2 2
lmol分子中的化学键断裂时需要吸收的能量
436 200 a
(kJ)
则表中a=___________。
(3)下列反应中属于吸热反应的有___________。
①燃烧木炭取暖②C与HO(g)反应制取水煤气③煅烧石灰石(主要成分是CaCO)制生石灰④氯化铵晶体和
2 3
Ba(OH) ·8H O混合搅拌⑤食物因氧化而腐败
2 2
(4)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热( )。图为ⅥA族元素
氢化物a、b、c、d的生成热数据示意图。
①非金属元素氢化物的稳定性与氢化物的生成热 的关系为___________。
②硫化氢发生分解反应的热化学方程式为___________。
(5)已知 , ,当
放出的热量为nkJ时,该反应转移的电子数为___________(用含m、n的代数式表示)30.(10分)(2023·辽宁省沈阳二中高三期中)甲醇是重要的含碳燃料。
(1)以CO和H为原料合成甲醇是工业上的成熟方法,直接以CO 为原料生产甲醇是目前的研究热点。我
2
国科学家用CO 人工合成淀粉时,第一步就需要将CO 转化为甲醇。已知:
2 2
①CO(g)+2H(g)=CH OH(g) ΔH =-90.5kJ/mol
2 3 1
②CO(g)+HO(g)=CO(g)+H(g) ΔH =-41.1kJ/mol
2 2 2 2
CO 与H 合成甲醇的热化学方程式为___________。
2 2
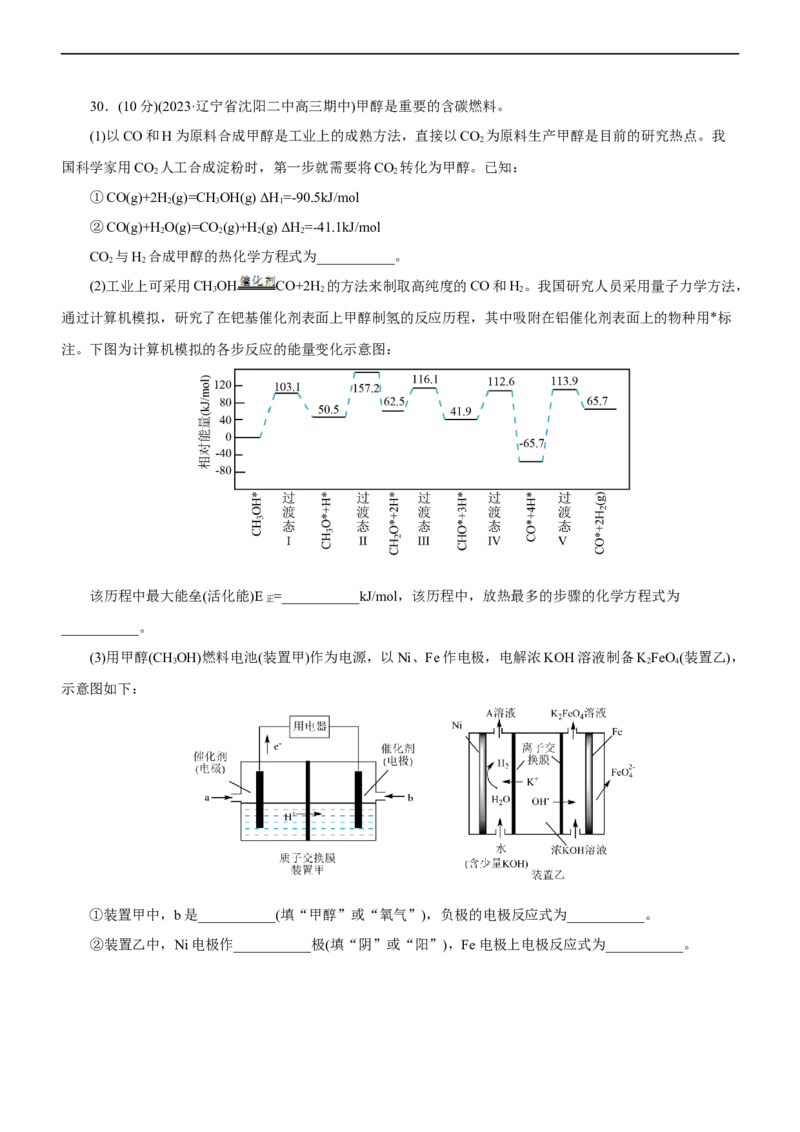
(2)工业上可采用CHOH CO+2H 的方法来制取高纯度的CO和H。我国研究人员采用量子力学方法,
3 2 2
通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在铝催化剂表面上的物种用*标
注。下图为计算机模拟的各步反应的能量变化示意图:
该历程中最大能垒(活化能)E =___________kJ/mol,该历程中,放热最多的步骤的化学方程式为
正
___________。
(3)用甲醇(CHOH)燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备KFeO(装置乙),
3 2 4
示意图如下:
①装置甲中,b是___________(填“甲醇”或“氧气”),负极的电极反应式为___________。
②装置乙中,Ni电极作___________极(填“阴”或“阳”),Fe电极上电极反应式为___________。