文档内容
专题 09 化学反应速率与化学平衡
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共70分)
一、选择题:本题共10个小题,每小题4分,共40分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.下列事实不能用勒夏特列原理解释的是
A.工业上SO 和O 在常压下生成SO
2 2 3
B.加热蒸干AlCl 溶液不能得到无水AlCl
3 3
C.用浓氨水和氢氧化钠制取氨气
D.水中的c(H+)比0.1mol·L-1 NaOH溶液中的大
【答案】A
【解析】工业上SO 和O 在常压下生成SO ,正反应 是气体体积缩小的反应,
2 2 3
所以常压不利于三氧化硫的转化,不能用勒夏特列原理解释,故A符合;AlCl 溶液在加热时水解生成
3
Al(OH) ,生成的HCl易挥发,最终生成Al(OH) ,在加强热时,Al(OH) 不稳定,分解生成Al O,能用平衡移
3 3 3 2 3
动的原理解释,故B不符合;浓氨水中加入氢氧化钠固体,会放出大量的热,促使氨水的电离平衡正向移
动,能用勒夏特列原理解释,故C不符合;氢氧化钠对水的电离起抑制作用,所以水中的c(H+)比0.1mol/
LNaOH溶液中c(H+)大,能用勒夏特列原理解释,故D不符合;故选A。
2.下列有关NO与O 生成NO 的反应的说法正确的是
2 2
A.该反应在任意温度下都可自发进行
B.该反应达到平衡时,2v(O ) =v(NO)
2 正 逆
C.及时移出部分生成的NO 可加快NO的反应速率
2
D.当反应中消耗22.4 LNO时,转移的电子数约为
【答案】B
【解析】要使反应自发进行,△G=△H-T△S<0,而2NO(g)+O (g) 2NO (g)的正反应是气体体积减小的
2 2
放热反应,△H<0,△S<0,所以△G<0,反应进行的温度应该是低温条件,若高温条件下,△G>0,反应
不能自发进行,A错误;在任何条件下v(NO) :v(O ) =2:1,若2v(O ) =v(NO) ,则v(NO) =v(NO) ,反应
正 2 正 2 正 逆 正 逆
处于平衡状态,B正确;若及时移出部分生成的NO ,瞬间NO的速率不变,后来NO的反应速率减慢,C错
2
误;未指明22.4 LNO是否处于标准状况,因此不能确定其物质的量,也就不能计算反应过程中电子转移数目,D错误;故合理选项是B。
3.一定温度下,向2.0L恒容密闭容器中充入 ,发生反应 ,
反应过程中测得的有关数据见下表:
0 2 4 6 8
0 0.30 0.39 0.40 0.40
下列说法正确的是A.0~2s,用CO表示的平均反应速率为
B.若达平衡后缩小容器体积,重新达到平衡前,
C.其他条件不变,若改用更高效的催化剂,2~6s时测得的数据均会增大
D.其他条件不变,改为在恒容绝热密闭容器中进行该反应,化学平衡常数不变
【答案】B
【解析】0~2s,用CO表示的平均反应速率为 ,故A错误;该反应是
体积增大的反应,若达平衡后缩小容器体积,平衡逆向移动,因此重新达到平衡前, ,故B
正确;其他条件不变,若改用更高效的催化剂,反应速率加快,但由于6s时已经达到平衡,因此6s时测得的
数据不会增大,故C错误。平衡常数与温度有关,其他条件不变,改为在恒容绝热密闭容器中进行该反应,
温度发生改变,因此化学平衡常数改变,故D错误。综上所述,答案为B。
4.在一定条件下的1L密闭容器中,X、Y、C三种气体的物质的量随时间的变化如图所示。下列说法不
正确的是A.0~15min,消耗C的平均速率约为
B.X、Y、C三种气体发生反应的化学方程式为:
C.反应开始到25min,X的转化率为25%
D.25min时改变的一个条件可能是缩小容器体积
【答案】A
【解析】据图可知C为生成物,0~15min内生成C而不是消耗C,A错误;据图可知X、Y的物质的量减
少为反应物,C的物质的量增加为生成物,达到平衡时X、Y、C的物质的量变化之比为0.75mol:0.25mol:
0.5mol=3:1:2,化学方程式为Y(g)+3X(g) 2C(g),B正确;25min时反应已达到平衡,该时段内
Δn(X)=0.75mol,转化率为 ×100%=25%,C正确;25min时的瞬间各物质的物质的量不变,所以不是改
变投料,而之后C的物质的量增加,X、Y的物质的量减小,说明平衡正向移动,该反应为气体系数之和减小
的反应,缩小容器体积增大压强,平衡正向移动,D正确;故选A。
5.已知 。一定温度下,在体积恒定的密闭容器中,加入1mol
与1mol ,下列说法正确的是
A.充分反应后,放出热量为akJ
B.若增大Y的浓度,正反应速率增大,逆反应速率减小
C.当X的物质的量分数不再改变,表明该反应已达平衡
D.当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
【答案】C
【解析】该反应为可逆反应,不能完全转化,充分反应后,放出热量小于akJ,A错误;若增大Y的浓
度,压强增大,正反应速率增大,逆反应速率也增大,B错误;当X的物质的量分数不再改变时,说明X的
物质的量不再变化,表明该反应已达平衡,C正确;当反应达到平衡状态时,X与W的物质的量浓度之不一
定为1:2,与各物质的初始浓度和转化率有关,D错误;故答案为C。
6.氮及其化合物在生产生活中具有广泛应用。氮气经过一系列的变化可以合成氨、氮的氧化物、硝酸等
重要的化工原料; 能被 溶液吸收生成配合物 ,减少环境污染。对于反应
,下列有关说法不正确的是A.上述反应的平衡常数表达式
B.适当提高 的浓度,可以加快反应速率,提高 的转化率
C. 断裂同时有 断裂,说明达该条件下的平衡状态
D.其它条件不变,加入高效的催化剂能提高单位体积内的活化分子百分数
【答案】B
【解析】根据平衡常数表达式, ,A正确;适当提高 的浓度,可以加快反应速
率,但因为提高了 的浓度,所以 的转化率降低,B错误; 断裂,说明有 发生反
应,反应正向进行, 断裂,有 发生反应,反应逆向进行,且符合两种物质的比值为,
2∶3,C正确;加入高效的催化剂,能够降低活化能,提高单位体积内的活化分子百分数,D正确;故答案为
B。
7.在 下,向 的恒容密闭容器里按 充入气体A,B,发生反应:
。 时达到平衡,测得部分数据如表所示:
物质及状态
平衡时的物质的量分数 40% 20%
平衡时的物质的量/ 4
下列说法正确的是A.
B.起始时,充入 的物质的量为
C. 时,该反应的化学平衡常数
D.平衡时, 的物质的量浓度为
【答案】B【解析】根据三段式: , , ,
。 ,A错误;根据上述计算, ,充入的 为2a,为6mol,B正确;根据以上三段式计
算: ,C错误;平衡时, 的物质的量为 ,浓度为 ,D错误;故选
B。
8.在一定温度下,在2个容积均为2L的恒容密闭容器中,加入一定量的反应物,发生反应:
∆H<0,相关数据见表。
起始物质的量/mol 平衡物质的量/mol
容器编号 温度/℃
NO(g) CO(g)
(g)
Ⅰ 0.4 0.4 0.2
Ⅱ 0.4 0.4 0.24
下列说法不正确的是A.
B.Ⅰ中反应达到平衡时,CO的转化率为50%
C.达到平衡所需要的时间:Ⅱ<Ⅰ
D.对于Ⅰ,平衡后向容器中再充入0.4mol CO和0.2mol ,平衡正向移动
【答案】C
【解析】∆H<0,升高温度平衡逆向移动,平衡时CO 的物质的量变小,由表中数据可知T>T,故A正
2 1 2
确;由表中数据可知,I达到平衡时转化的CO为0.4mol-0.2mol=0.2mol,则平衡时,CO的转化率为
,故B正确;温度越高、反应速率越快,T>T,可知平衡所需要的时间:II>I,故C错
1 2误;I中: ,平衡常数 ,平衡后向容
器中再充入0.4mol CO和0.2mol ,此时 ,QT
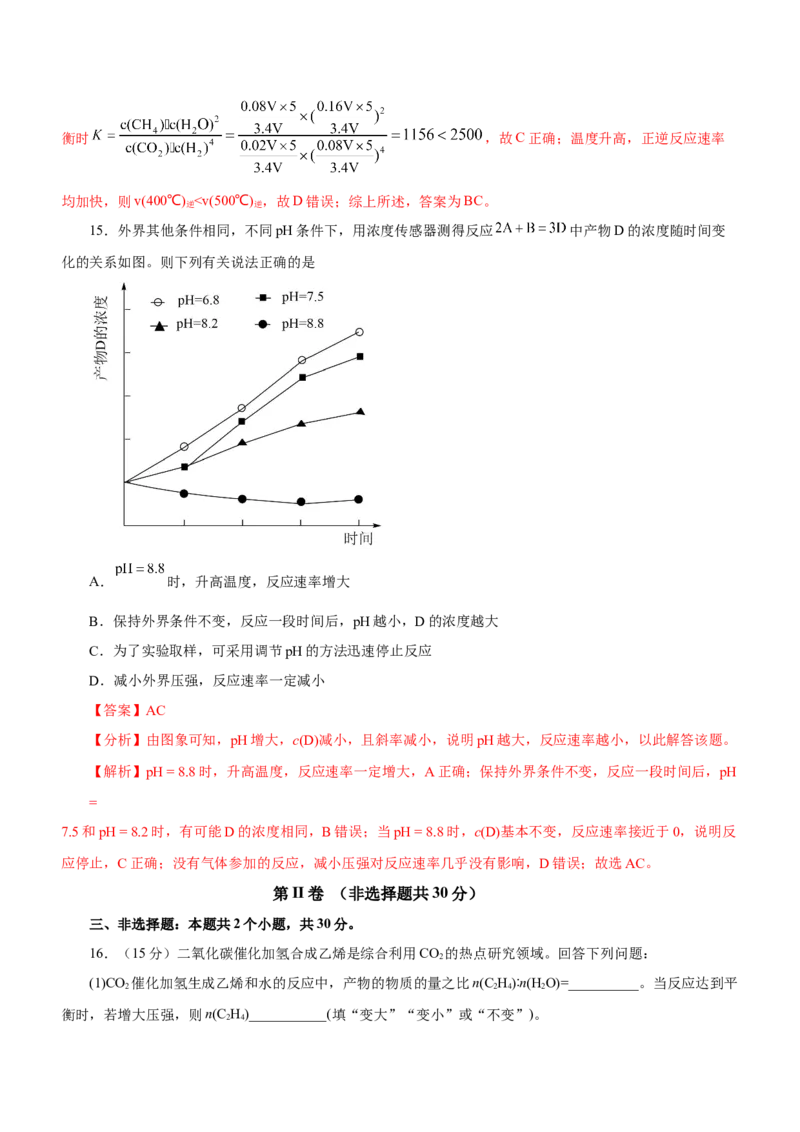
1
,在其他条件不变的情况下,将处于E点的体系的
体积压缩到原来的 ,平衡正向移动,氢气浓度增大
D.图4所示,用水稀释pH相同的盐酸和醋酸,Ⅰ表示盐酸,Ⅱ表示醋酸,且溶液导电性:c>b>a
【答案】C
【解析】图1所示反应:X(g)+2Y(g) 3Z(g),反应前后气体体积不变,b曲线表示的可以是使用催化剂或
增大压强,使用催化剂时压强关系为a=b,故A错误;CO生成CO 的反应过程和能量关系是反应物先要吸收
2
能量达到活化能,成为活化分子然后再变成生成物放出热量,而图中只能表示反应物总能量和生成物总能量,
不能表示过程中的能量变化情况,故B错误;由图可知,T 时的反应速率大于T 时的,反应CO+2H═CH OH
1 2 2 3
达到平衡后体系的体积压缩到原来的,平衡正向移动,所有物质的浓度都会增大,故C正确;用水稀释pH相
同的盐酸和醋酸,因醋酸为弱酸,稀释时能促进弱电解质的电离,所以醋酸比盐酸中氢离子浓度减小的慢,所
以Ⅰ表示盐酸,Ⅱ表示醋酸,但氢离子浓度变小,溶液导电性减弱,所以溶液导电性b>c,故D错误;故答案
选C。
12.已知:CH(g)+2HS(g) CS(g)+4H(g)。向恒容密闭容器中充入0.lmolCH 和0.2molHS,下图所
4 2 2 2 4 2
示:
下列说法正确的是
A.该反应的△H<O
B.X 点CH 的转化率为30%
4
C.X点与Y点容器内压强比为55:51
D.维持Z点温度,向容器中再充入CH、HS、CS、H 各0.1mol 时v(正)<v(逆)
4 2 2 2【答案】D
【解析】由图象可知,随温度的升高,反应物在减小,生成物在增大,所以该反应为吸热反应,即
△H>O,(或者由图象不能确定反应的热效应),A错误;设X点时CS 为xmol,则CH 为(0.1-x)mol,HS为
2 4 2
(0.2-2x)mol,H 为4xmol,即得(0.1-x)= 4x,x=0.02 mol,则CH 的转化率为20%,B错误;在同温同容时,压
2 4
强之比等于物质的量之比,X点容器内的总物质的量为n =(0.1-x)mol+(0.2-2x)mol+ xmol+4xmol=0.34 mol,同
(X)
理可得Y点CS 为1/30mol,则n =(0.1-1/30)mol+(0.2-2×1/30)mol+1/30mol+4×1/30mol=11/30 mol,则X点与Y
2 (Y)
点容器内压强比= n :n = 51:55,C错误;同理可求得Z点CS 为0.05mol,则CH 为0.05mol,HS为
(X) (Y) 2 4 2
0.1mol,H 为0.2mol,设容器的体积为1L,此时的浓度商Q=0.16,当向容器中再充入CH、HS、CS、H 各
2 1 4 2 2 2
0.1mol 时,各物质的量分别为CH0.15mol,HS 0.2mol,CS 0.15mol,H 0.3mol,此时的Q=0.2025 > Q =
4 2 2 2 1
0.16,所以反应向左进行,即V(正)0
2 2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O 的浓度不能提高NO转化率
2
D.380℃下,c (O )=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
起始 2
【答案】BD
【解析】随温度升高NO的转化率先升高后降低,说明温度较低时反应较慢,一段时间内并未达到平衡,
分析温度较高时,已达到平衡时的NO转化率可知,温度越高NO转化率越低,说明温度升高平衡向逆方向移
动,根据勒夏特列原理分析该反应为放热反应,∆H<0,故A错误;根据上述分析,X点时,反应还未到达平
衡状态,反应正向进行,所以延长反应时间能提高NO的转化率,故B正确;Y点,反应已经达到平衡状态,
此时增加O 的浓度,使得正反应速率大于逆反应速率,平衡向正反应方向移动,可以提高NO的转化率,故C
2
错误;设NO起始浓度为amol/L,NO的转化率为50%,则平衡时NO、O 和NO 的浓度分别为0.5amol/L、
2 2(5×10-4-0.25a)mol/L、0.5amol/L,根据平衡常数表达式K= >
=2000,故D正确;故选BD。
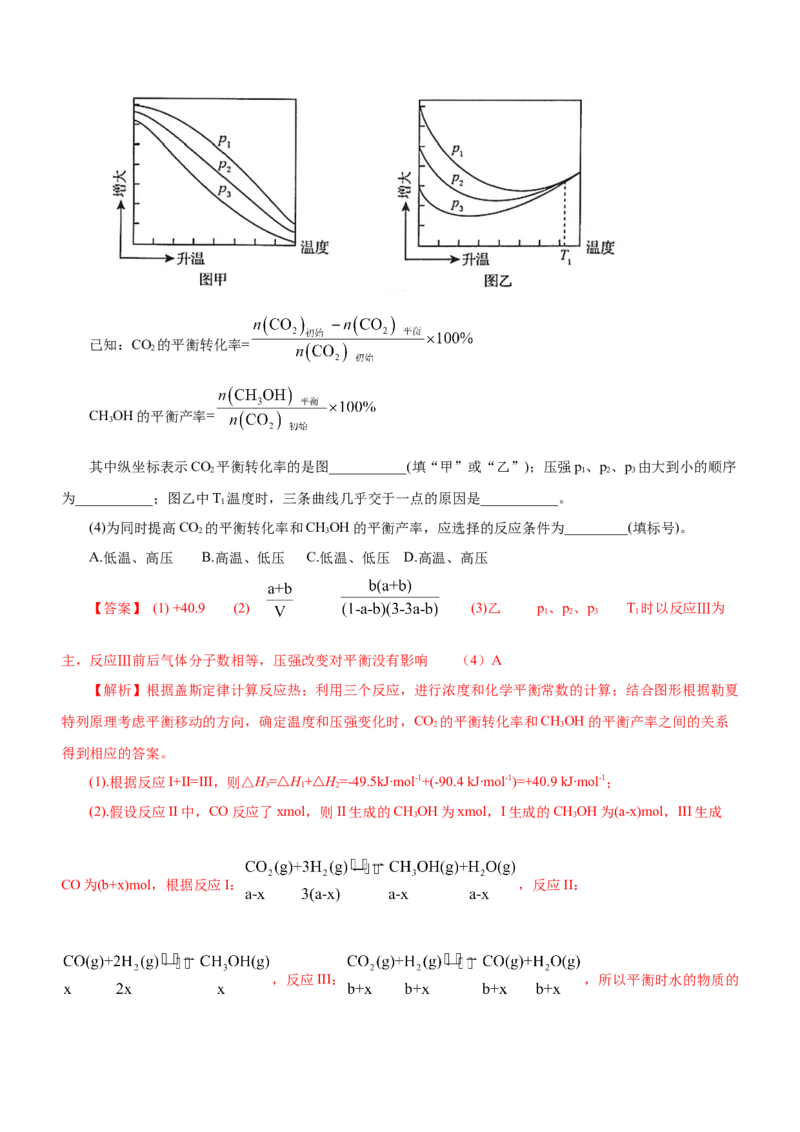
14.恒压下,将CO 和H 以体积比1∶4混合进行反应CO(g)+4H(g) CH(g)+2HO(g)(假定过程中无
2 2 2 2 4 2
其他反应发生),用Ru/TiO 催化反应相同时间,测得CO 转化率随温度变化情况如图所示。下列说法正确的是
2 2
( )
A.反应CO(g)+4H(g)=CH (g)+2HO(g)的ΔH>0
2 2 4 2
B.图中450 ℃时,延长反应时间无法提高CO 的转化率
2
C.350 ℃时,c(H) =0.4 mol·L-1,CO 平衡转化率为80%,则平衡常数K<2 500
2 起始 2
D.当温度从400 ℃升高至500 ℃,反应处于平衡状态时,v(400℃) >v(500℃)
逆 逆
【答案】BC
【解析】如图所示为用Ru/TiO 催化反应相同时间,测得CO 转化率随温度变化情况,约350℃之前,反
2 2
应还未达到平衡态,CO 转化率随温度升高而增大,约350℃之后,反应达到化学平衡态,CO 转化率随温度
2 2
升高而减小,由此可知该反应为放热反应。由分析可知该反应为放热反应,则ΔH<0,故A错误;图中450 ℃
时,反应已达平衡态,则延长反应时间无法提高CO 的转化率,故B正确; 350 ℃时,设起始时容器的容积
2
为V,c(H) =0.4 mol·L-1,则n(H ) =0.4 Vmol,CO 平衡转化率为80%,可列三段式为:
2 起始 2 起始 2
根据阿伏加德罗定律有 ,平衡时的体积为V(平衡)= ,则平衡时 ,故C正确;温度升高,正逆反应速率
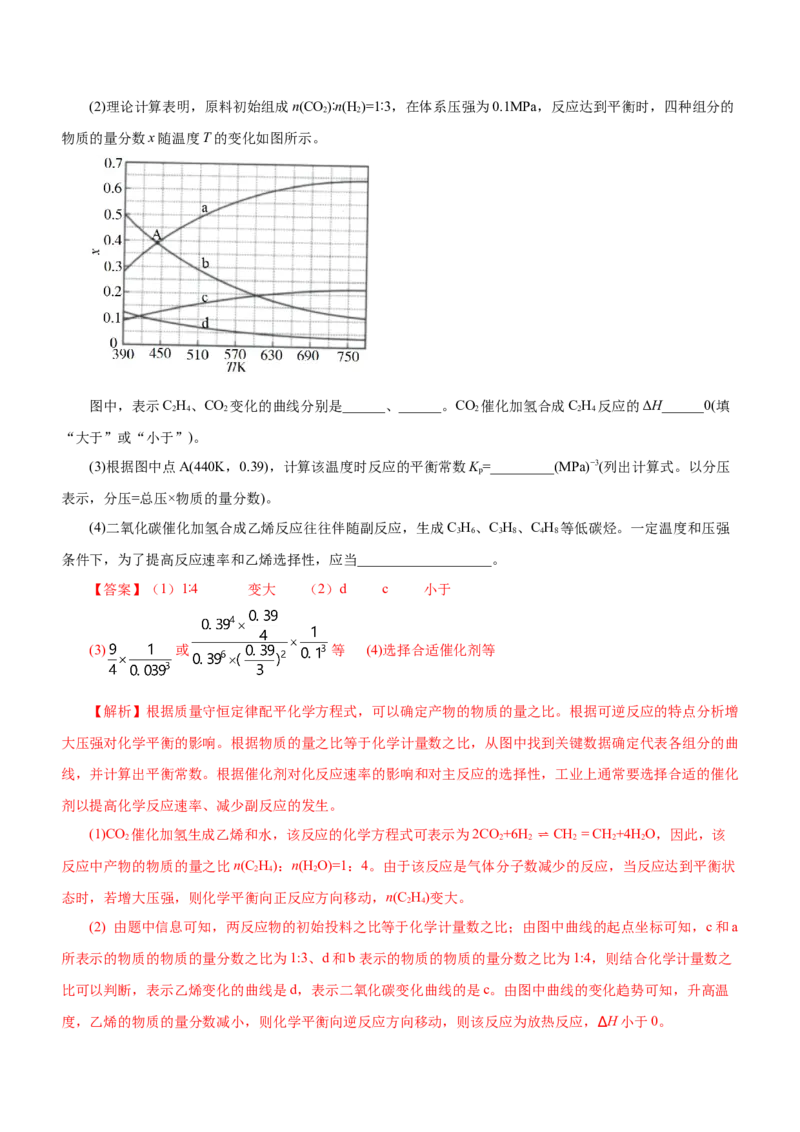
均加快,则v(400℃) p>p;温度升高,反应I和II平衡逆向移动,反应III向正反应方向移动,所以T 温度时,三
1 2 3 1
条曲线交与一点的原因为:T 时以反应III为主,反应III前后分子数相等,压强改变对平衡没有影响;
1
(4).根据图示可知,温度越低,CO 的平衡转化率越大,CHOH的平衡产率越大,压强越大,CO 的平衡
2 3 2
转化率越大,CHOH的平衡产率越大,所以选择低温和高压,答案选A。
3