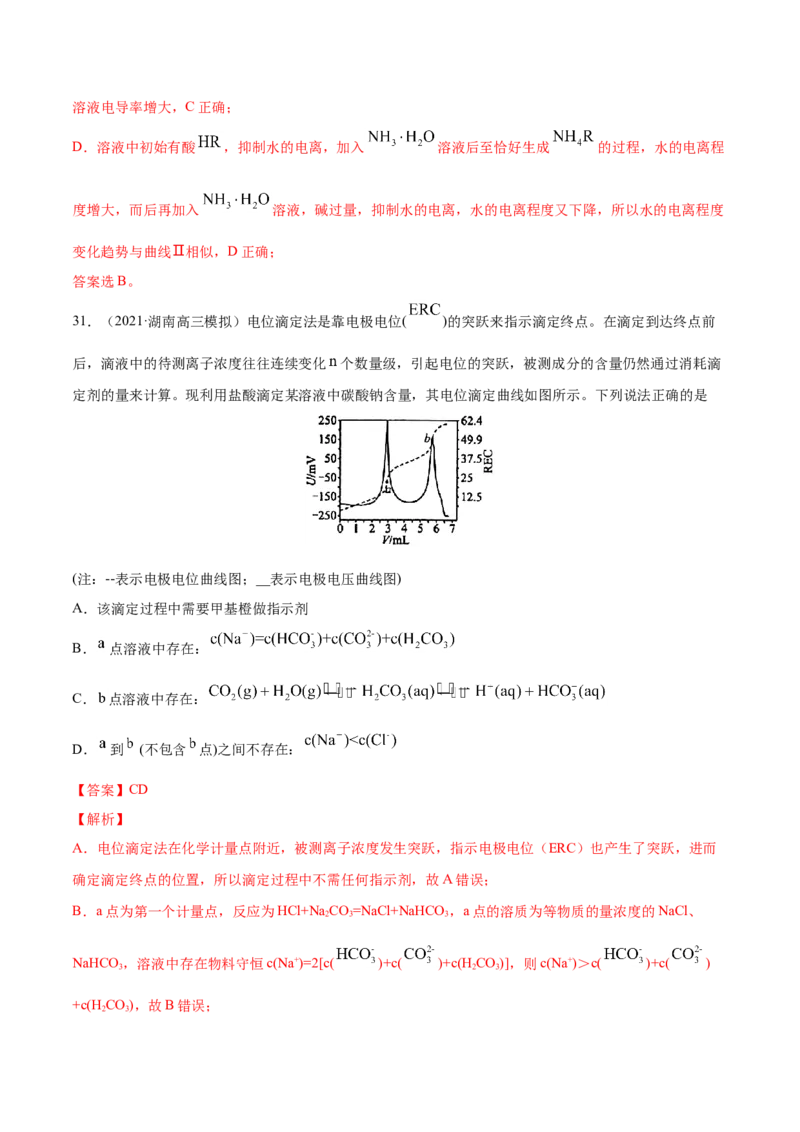
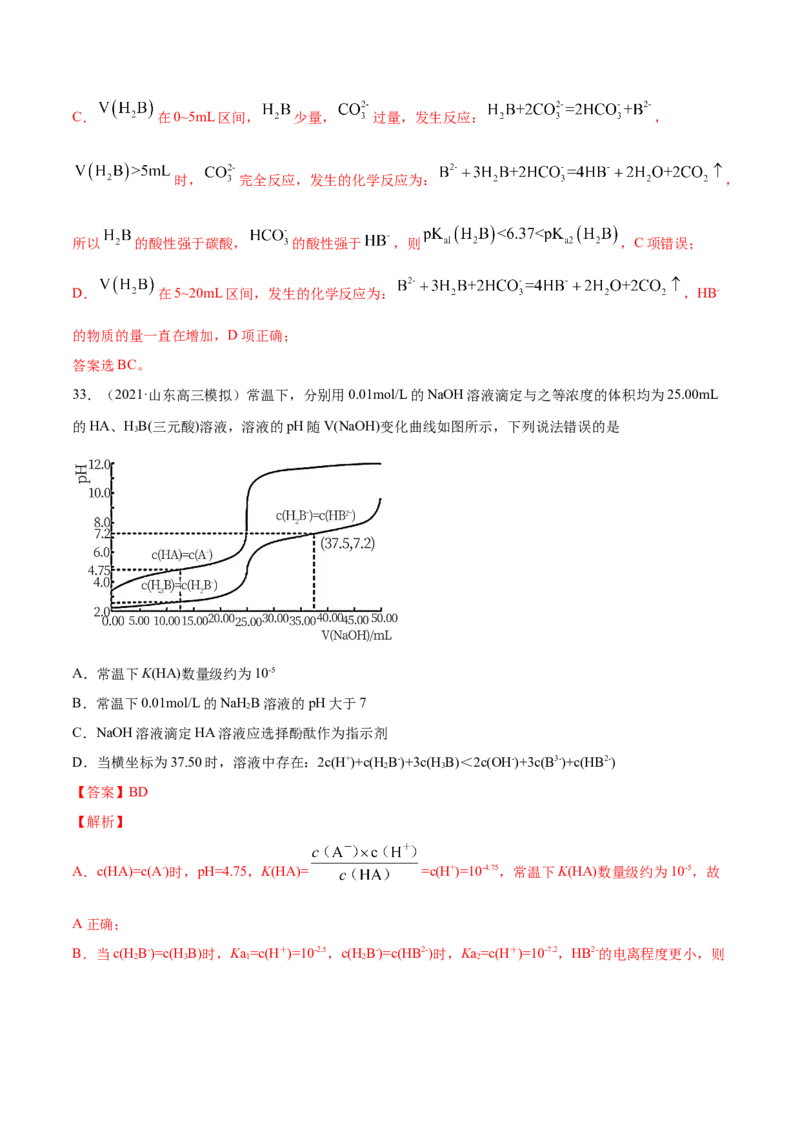
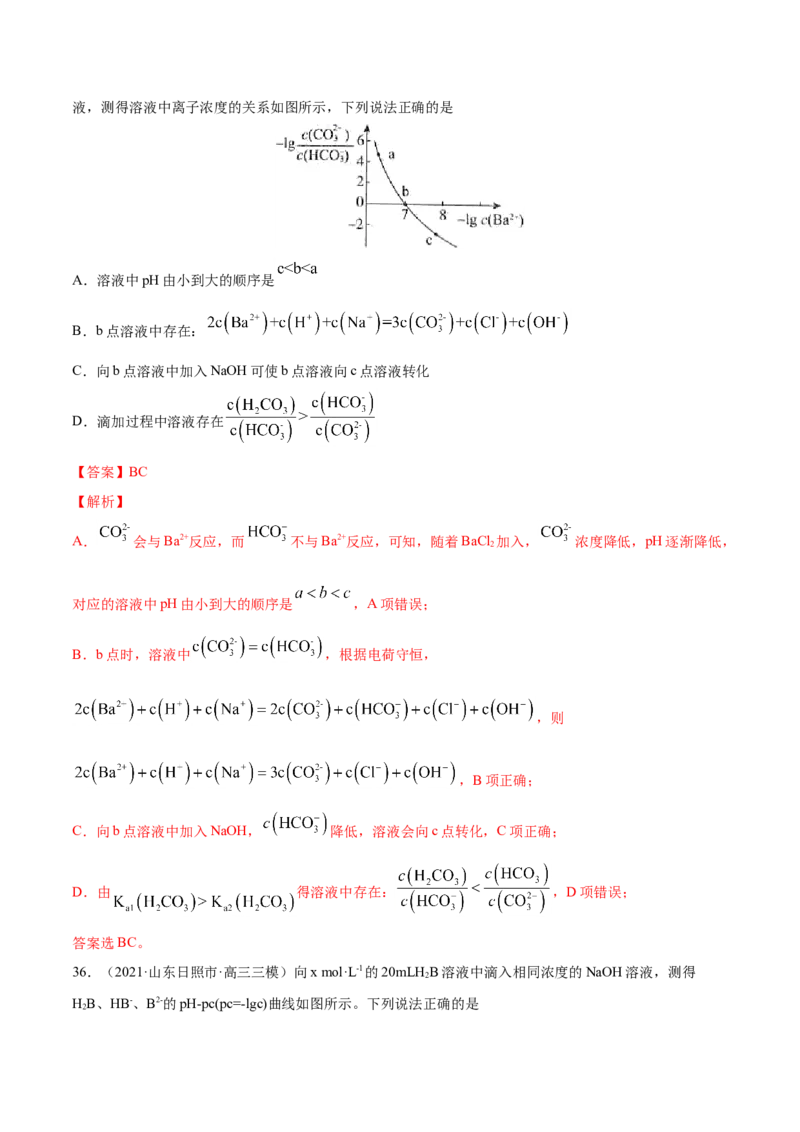
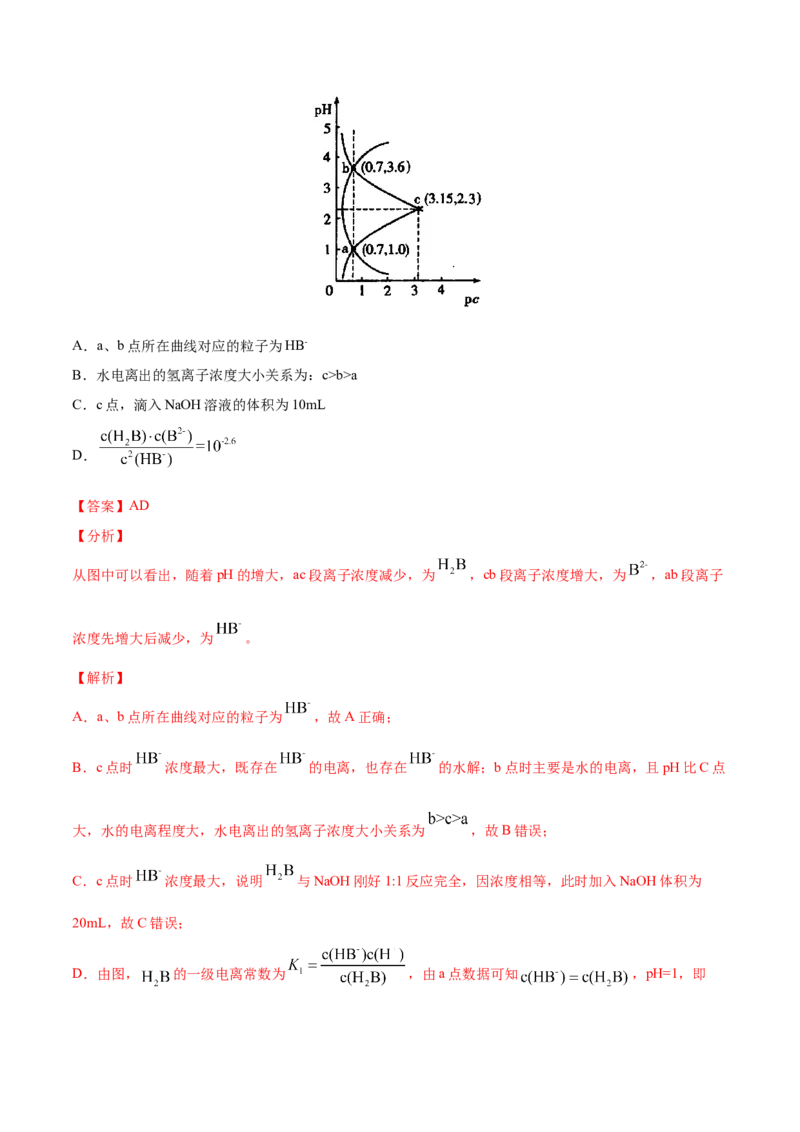
文档内容
专题 10 水溶液中的离子平衡
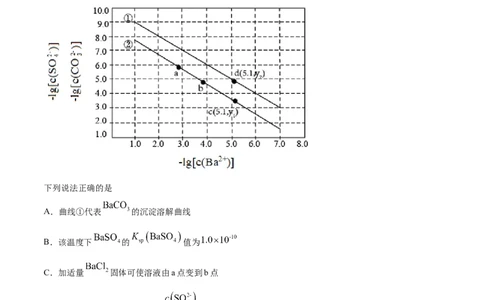
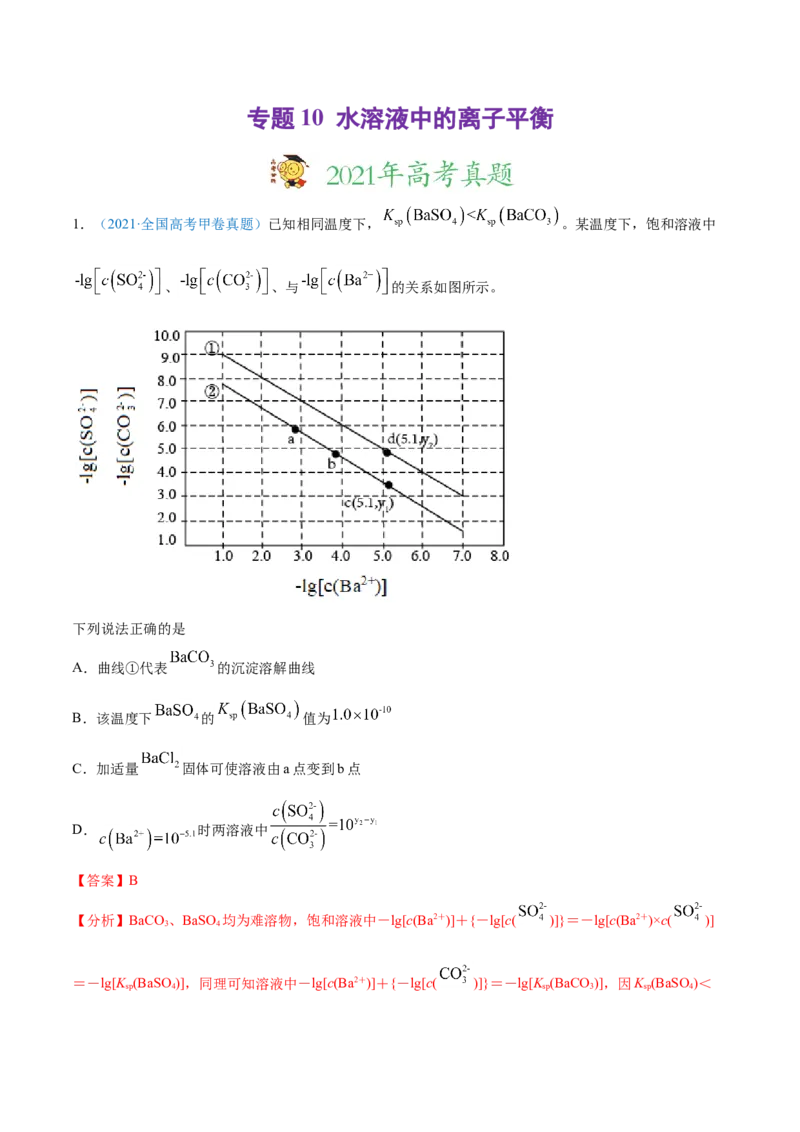
1.(2021·全国高考甲卷真题)已知相同温度下, 。某温度下,饱和溶液中
、 、与 的关系如图所示。
下列说法正确的是
A.曲线①代表 的沉淀溶解曲线
B.该温度下 的 值为
C.加适量 固体可使溶液由a点变到b点
D. 时两溶液中
【答案】B
【分析】BaCO 、BaSO 均为难溶物,饱和溶液中-lg[c(Ba2+)]+{-lg[c( )]}=-lg[c(Ba2+)×c( )]
3 4
=-lg[K (BaSO)],同理可知溶液中-lg[c(Ba2+)]+{-lg[c( )]}=-lg[K (BaCO)],因K (BaSO)<
sp 4 sp 3 sp 4K (BaCO),则-lg[K (BaCO)]<-lg[K (BaSO)],由此可知曲线①为-lg[c(Ba2+)]与-lg[c( )]的关系,
sp 3 sp 3 sp 4
曲线②为-lg[c(Ba2+)]与-lg[c( )]的关系。
【解析】A.由题可知,曲线上的点均为饱和溶液中微粒浓度关系,由上述分析可知,曲线①为BaSO 的
4
沉淀溶解曲线,选项A错误;
B.曲线①为BaSO 溶液中-lg[c(Ba2+)]与-lg[c( )]的关系,由图可知,当溶液中-lg[c(Ba2+)]=3时,
4
-lg[c( )=7,则-lg[K (BaSO)]=7+3=10,因此K (BaSO)=1.0×10-10,选项B正确;
sp 4 sp 4
C.向饱和BaSO 溶液中加入适量BaCl 固体后,溶液中c(Ba2+)增大,根据温度不变则K (BaSO)不变可知,
4 2 sp 4
溶液中c( )将减小,因此a点将沿曲线①向左上方移动,选项C错误;
D.由图可知,当溶液中c(Ba2+)=10-5.1时,两溶液中 = = ,选项D错误;
答案选B。
2.(2021·全国高考乙卷真题)HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化, 不
发生水解。实验发现, 时 为线性关系,如下图中实线所示。
下列叙述错误的是A.溶液 时,
B.MA的溶度积度积
C.溶液 时,
D.HA的电离常数
【答案】C
【分析】本题考查水溶液中离子浓度的关系,在解题过程中要注意电荷守恒和物料守恒的应用,具体见详
解。
【解析】A.由图可知pH=4,即c(H+)=10×10-5mol/L时,c2(M+)=7.5×10-8mol2/L2,c(M+)=
mol/L<3.0×10-4mol/L,A正确;
B.由图可知,c(H+)=0时,可看作溶液中有较大浓度的OH-,此时A-的水解极大地被抑制,溶液中
c(M+)=c(A-),则 ,B正确;
C.设调pH所用的酸为HX,则结合电荷守恒可知
n
,题给等式右边缺阴离子部分nc(Xn-),C错误;
D. 当 时,由物料守恒知 ,则
, ,则 ,对应图得此时溶
液中 , ,D正确;
故选C。
3.(2021·广东高考真题)鸟嘌呤( )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知水溶液呈酸性,下列叙述正确的是
A. 水溶液的
B. 水溶液加水稀释, 升高
C. 在水中的电离方程式为:
D. 水溶液中:
【答案】B
【解析】A.GHCl为强酸弱碱盐,电离出的GH+会发生水解,弱离子的水解较为微弱,因此0.001mol/L
GHCl水溶液的pH>3,故A错误;
B.稀释GHCl溶液时,GH+水解程度将增大,根据勒夏特列原理可知溶液中c(H+)将减小,溶液pH将升高,
故B正确;
C.GHCl为强酸弱碱盐,在水中电离方程式为GHCl=GH++Cl-,故C错误;
D.根据电荷守恒可知,GHCl溶液中c(OH-)+c(Cl-)=c(H+)+c(GH+),故D错误;
综上所述,叙述正确的是B项,故答案为B。
4.(2021·湖南高考真题)常温下,用 的盐酸分别滴定20.00mL浓度均为
三种一元弱酸的钠盐 溶液,滴定曲线如图所示。下列判断错误的是
A.该 溶液中:
B.三种一元弱酸的电离常数:C.当 时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
【答案】C
【分析】由图可知,没有加入盐酸时,NaX、NaY、NaZ溶液的pH依次增大,则HX、HY、HZ三种一元
弱酸的酸性依次减弱。
【解析】A.NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为c(Na+)>
c(X-)>c(OH-)>c(H+),故A正确;
B.弱酸的酸性越弱,电离常数越小,由分析可知,HX、HY、HZ三种一元弱酸的酸性依次减弱,则三种
一元弱酸的电离常数的大小顺序为K(HX)>K (HY)>K(HZ),故B正确;
a a a
C.当溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,则三种盐溶液中
酸根的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;
D.向三种盐溶液中分别滴加20.00mL盐酸,三种盐都完全反应,溶液中钠离子浓度等于氯离子浓度,将
三种溶液混合后溶液中存在电荷守恒关系c(Na+)+ c(H+)= c(X-)+c(Y-)+c(Z-)+ c(Cl-)+ c(OH-),由c(Na+)= c(Cl-)
可得:c(X-)+c(Y-)+c(Z-)= c(H+)—c(OH-),故D正确;
故选C。
5.(2021·浙江高考真题)某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列说法正确
的是
A.25℃时,若测得 溶液 ,则HR是弱酸
B.25℃时,若测得 溶液 且 ,则HR是弱酸
C.25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,
则HR是弱酸
D.25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱
酸
【答案】B
【解析】A.25℃时,若测得 溶液 ,可知 为强酸强碱盐,则 为强酸,A错误;
B.25℃时,若测得 溶液 且 ,可知溶液中 ,所以
未完全电离, 为弱酸,B正确;
C.假设 为强酸,取 的该溶液 ,加蒸馏水稀释至 测得此时溶液 ,C错
误;
D.假设 为强酸,则 为强酸强碱盐,溶液呈中性,升温至50℃,促进水的电离,水的离子积常
数增大, 减小,D错误;
答案为:B。
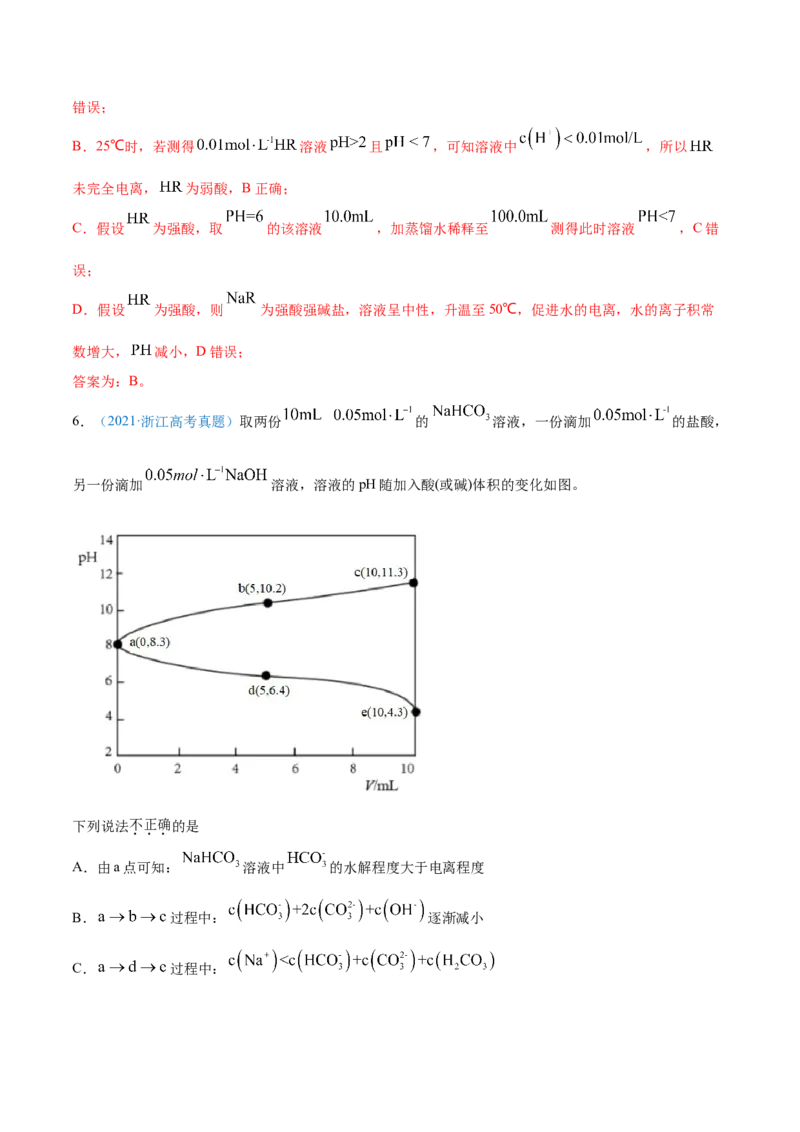
6.(2021·浙江高考真题)取两份 的 溶液,一份滴加 的盐酸,
另一份滴加 溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法不正确的是
A.由a点可知: 溶液中 的水解程度大于电离程度
B. 过程中: 逐渐减小
C. 过程中:D.令c点的 ,e点的 ,则
【答案】C
【分析】向 溶液中滴加盐酸,溶液酸性增强,溶液pH将逐渐减小,向 溶液中滴加
NaOH溶液,溶液碱性增强,溶液pH将逐渐增大,因此abc曲线为向 溶液中滴加NaOH溶液,
ade曲线为向 溶液中滴加盐酸。
【解析】A.a点溶质为 ,此时溶液呈碱性, 在溶液中电离使溶液呈酸性, 在溶液
中水解使溶液呈碱性,由此可知, 溶液中 的水解程度大于电离程度,故A正确;
B.由电荷守恒可知, 过程溶液中 ,滴加
NaOH溶液的过程中 保持不变, 逐渐减小,因此 逐渐减
小,故B正确;
C.由物料守恒可知,a点溶液中 ,向 溶液中滴加
盐酸过程中有CO 逸出,因此 过程中 ,故C错
2
误;
D.c点溶液中 =(0.05+10-11.3)mol/L,e点溶液体积增大1倍,此时溶液中
=(0.025+10-4)mol/L,因此x>y,故D正确;
综上所述,说法不正确的是C项,故答案为C。
7.(2021·浙江高考真题)25℃时,下列说法正确的是
A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2D.100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5mol
2 3
【答案】D
【解析】A.NaHA溶液呈酸性,可能是HA-的电离程度大于其水解程度,不能据此得出HA为强酸的结
2
论,A错误;
B.可溶性正盐BA溶液呈中性,不能推测BA为强酸强碱盐,因为也可能是B+和A-的水解程度相同,即
也可能是弱酸弱碱盐,B错误;
C.弱酸的浓度越小,其电离程度越大,因此0.010 mol·L-1、0.10 mol·L-1的醋酸溶液的电离度分别为α 、
1
α ,则α >α ,C错误;
2 1 2
D.100 mL pH=10.00的NaCO 溶液中氢氧根离子的浓度是1×10-4mol/L,碳酸根水解促进水的电离,则水
2 3
电离出H+的浓度是1×10-4mol/L,其物质的量为0.1L×1×10-4mol/L=1×10-5mol,D正确;
答案选D。
8.(2021·浙江高考真题)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的
4 3
pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为1.8×10-
3 3 2
5.下列说法不正确的是
A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B.将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4C.随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH )
4 3 3
【答案】C
【分析】由题中信息可知,图中两条曲线为10 mL 0. 50 mol·L-1 NHCl溶液、10 mL 0.50mol·L-1CHCOONa
4 3
溶液的pH分别随温度与稀释加水量的变化曲线,由于两种盐均能水解,水解反应为吸热过程,且温度越
高、浓度越小其水解程度越大。氯化铵水解能使溶液呈酸性,浓度越小,虽然水程度越大,但其溶液的酸
性越弱,故其pH越大;醋酸钠水解能使溶液呈碱性,浓度越小,其水溶液的碱性越弱,故其pH越小。温
度越高,水的电离度越大。因此,图中的实线为pH随加水量的变化,虚线表示pH随温度的变化。
【解析】A.由分析可知,图中实线表示pH随加水量的变化,虚线表示pH随温度的变化,A说法正确;
B.将NH Cl溶液加水稀释至浓度 mol·L-1时,若氯化铵的水解平衡不发生移动,则其中的c(H+)变为
4
原来的 ,则溶液的pH将增大lgx,但是,加水稀释时,氯化铵的水解平衡向正反应方向移动,c(H+)大于
原来的 ,因此,溶液pH的变化值小于lgx,B说法正确;
C.随温度升高,水的电离程度变大,因此水的离子积变大,即K 增大;随温度升高,CHCOONa的水解
w 3
程度变大,溶液中c(OH-)增大,因此,C说法不正确;
D. 25℃时稀释相同倍数的NH C1溶液与CHCOONa溶液中均分别存在电荷守恒,c(Na+ ) +c(H+) =c(OH-)
4 3
+c(CHCOO- ) ,c(NH +)+c(H+ ) =c(Cl-)+c(OH- )。因此,氯化铵溶液中,c(Cl-)-c(NH +) =c(H+ )-c(OH- ),醋酸
3 4 4
钠溶液中,c(Na+ )-c(CHCOO- )= c(OH-) -c(H+) 。由于25 ℃时CHCOOH和NH ·H O的电离常数均为1.8
3 3 3 2
×10-5,因此,由于原溶液的物质的量浓度相同,稀释相同倍数后的NH C1溶液与CHCOONa溶液,溶质
4 3
的物质的量浓度仍相等,由于电离常数相同,其中盐的水解程度是相同的,因此,两溶液中c(OH-) -c(H+)
(两者差的绝对值)相等,故c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH +),D说法正确。
3 4
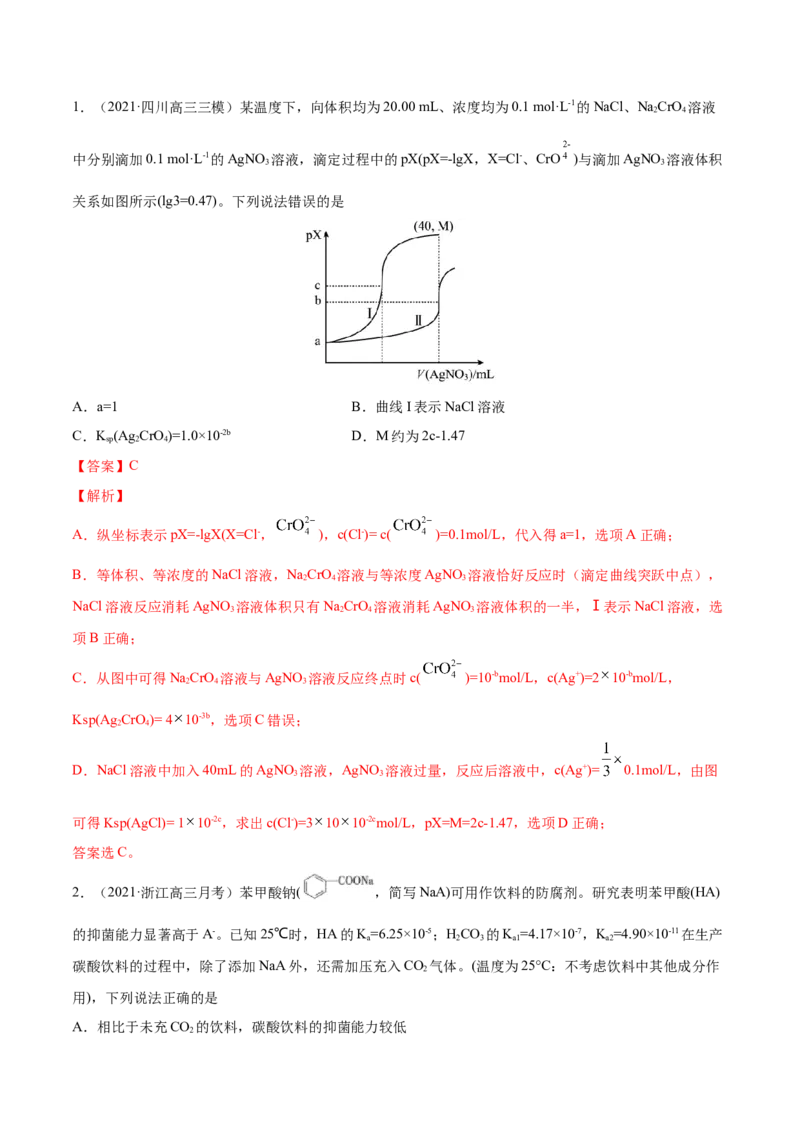
综上所述,本题选C。1.(2021·四川高三三模)某温度下,向体积均为20.00 mL、浓度均为0.1 mol·L-1的NaCl、NaCrO 溶液
2 4
中分别滴加0.1 mol·L-1的AgNO 溶液,滴定过程中的pX(pX=-lgX,X=Cl-、CrO )与滴加AgNO 溶液体积
3 3
关系如图所示(lg3=0.47)。下列说法错误的是
A.a=1 B.曲线I表示NaCl溶液
C.K (Ag CrO)=1.0×10-2b D.M约为2c-1.47
sp 2 4
【答案】C
【解析】
A.纵坐标表示pX=-lgX(X=Cl-, ),c(Cl-)= c( )=0.1mol/L,代入得a=1,选项A正确;
B.等体积、等浓度的NaCl溶液,NaCrO 溶液与等浓度AgNO 溶液恰好反应时(滴定曲线突跃中点),
2 4 3
NaCl溶液反应消耗AgNO 溶液体积只有NaCrO 溶液消耗AgNO 溶液体积的一半,Ⅰ表示NaCl溶液,选
3 2 4 3
项B正确;
C.从图中可得NaCrO 溶液与AgNO 溶液反应终点时c( )=10-bmol/L,c(Ag+)=2 10-bmol/L,
2 4 3
Ksp(Ag CrO)= 4 10-3b,选项C错误;
2 4
D.NaCl溶液中加入40mL的AgNO 溶液,AgNO 溶液过量,反应后溶液中,c(Ag+)= 0.1mol/L,由图
3 3
可得Ksp(AgCl)= 1 10-2c,求出c(Cl-)=3 10 10-2cmol/L,pX=M=2c-1.47,选项D正确;
答案选C。
2.(2021·浙江高三月考)苯甲酸钠( ,简写NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)
的抑菌能力显著高于A-。已知25℃时,HA的K=6.25×10-5;HCO 的K =4.17×10-7,K =4.90×10-11在生产
a 2 3 a1 a2
碳酸饮料的过程中,除了添加NaA外,还需加压充入CO 气体。(温度为25°C:不考虑饮料中其他成分作
2
用),下列说法正确的是
A.相比于未充CO 的饮料,碳酸饮料的抑菌能力较低
2B.提高CO 充气压力,饮料中c(A-)不变
2
C.当pH为5.0时,饮料中c(HA)/(A-)=0.16
D.碳酸饮料中各种粒子的浓度关系为:c(H+)=c( )+c( )+c(OH-)-(HA)
【答案】C
【解析】
A.由题中的信息可知,碳酸的酸性强于苯甲酸,所以充入二氧化碳后,苯甲酸(HA)的浓度增大,抑菌能
力较高,A错误;
B.提高二氧化碳充气压力,溶液的酸性增强,溶液中的c(A-)减小,B错误;
C.HA的电离平衡常数K= ,所以 = =0.16,C正确;
a
D.根据电荷守恒得c(H+)+c(Na+)=c(HCO )+2c(CO )+c(OH-)+c(A-),根据物料守恒得c(Na+)=c(A-)
+c(HA),两式联立,消去c(Na+)得c(H+)=c(OH-)+c(HCO )+2c(CO )-c(HA),D错误;
综上所述答案选C。
3.(2021·江西新余市·高三二模)常温下,向10mL一定浓度的硝酸银溶液中,逐滴加入 的氨
水,反应过程中 或 与加入氨水体积的关系如图所示。下列说法正确的是
A.原硝酸银溶液的浓度是
B.反应生成氢氧化银的 的数量级为
C.溶液b点 的浓度小于溶液m点的 浓度D.溶液m点
【答案】D
【分析】
向硝酸银溶液中,逐滴加入氨水,先生成氢氧化银沉淀,银离子浓度减小,加入过量的氨水,氢氧化银和
氨水反应生成 。
【解析】
A.由图像可知加入10mL 的氨水,恰好生成氢氧化银沉淀,发生反应
,所以原硝酸银溶液的浓度是 ,故A错误;
B.硝酸银完全生成氢氧化银沉淀时,银离子浓度是 mol/L,氢氧化银的 的数量级为 ,
故B错误;
C.b→m发生反应 ,氢氧根离子结合铵根离子生成
一水合氨,所以溶液b点 的浓度大于溶液m点的 浓度,故C错误;
D.根据电荷守恒,溶液m点 ,m
点 的浓度是0.01mol/L,溶液呈碱性,所以 ,故D正确;
选D。
4.(2021·吉林东北师大附中高三月考)酒石酸是葡萄酒中主要的有机酸之一,它的结构式为
HOOCCH(OH)CH(OH)COOH(简写为HR)。已知:25℃时,HR和HCO 的电离平衡常数如下,下列说法
2 2 2 3
正确的是
化学式 HR HCO
2 2 3
K =9.1×10-4 K =4.2×10-7
1 1
电离平衡常数
K =4.3×10-5 K =5.6×10-11
2 2
A.NaHR溶液呈酸性,且溶液中c(Na+)>c(HR-)>c(H R)>c(R2-)
2
B.在NaR溶液中通入足量CO 生成的盐是NaHR和NaHCO
2 2 3C.1molH R分别与足量的NaOH、NaCO、Na反应消耗三者的物质的量之比为1:1:1
2 2 3
D.25℃时,将等物质的量浓度的NaR和NaHCO 溶液等体积混合,反应的离子方程式为:R2-+
2 3
=HR-+
【答案】C
【分析】
对于HR来说,K (H R)=9.1×10-4,则K (H R)= = 1.1×10-11 。
2 1 2 h2 2
【解析】
A.由于K (H R)=4.3×10-5>K (H R),则NaHR在溶液中以电离为主,溶液呈酸性,所以溶液中c(Na+)>
2 2 h2 2
c(HR-)>c(R2-)>c(H R),A不正确;
2
B.由于K (H R)=4.3×10-5>K (H CO),所以在NaR溶液中通入足量CO 气体,不能发生反应,B不正确;
2 2 1 2 3 2 2
C.1molH R分别与足量的NaOH、NaCO、Na反应,都生成NaR,且NaCO 转化为NaHCO ,所以消耗
2 2 3 2 2 3 3
NaOH、NaCO、Na都为2mol,则消耗三者的物质的量之比为1:1:1,C正确;
2 3
D.25℃时,将等物质的量浓度的NaR和NaHCO 溶液等体积混合,由于K (H R)=4.3×10-5>K (H CO),
2 3 2 2 2 2 3
所以不能发生反应,D不正确;
故选C。
5.(2021·江西南昌市·高三二模)用 溶液滴定 溶液,溶液
和温度随 的变化曲线如图所示.下列说法正确的
A.从W至Z点,水的电离程度逐渐增大, 不变B.当 =1时,2
C. 的电离常数
D.Y点为第二反应终点
【答案】C
【解析】
A.从W至Z点,溶液温度逐渐升高,因此 逐渐增大,故A错误;
B.当 =1时,溶液中溶质为NaHA,根据物料守恒得到
,故B错误;
C.当c(HA-)=c(A2−)时,溶液温度为 pH=9.7,则 的电离常数 ,
故C正确;
D.X为第一反应终点,即 =1时,当 =2时为第二反应终点即Z点,故D
错误。
答案为C。
6.(2021·重庆高三三模)常温下,已知K (H CO)=4.3×10-7,K (H CO)=5.6×10-11。某二元酸HR及其钠
a1 2 3 a2 2 3 2
盐的溶液中,HR、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确的是
2A.反应HR+R2- 2HR-的平衡常数K=1000
2
B.向NaCO 溶液中加入少量HR溶液,发生的反应是:CO +H R=CO ↑+H O+R2-
2 3 2 2 2 2
C.等体积、等浓度的NaOH溶液与HR溶液混合后,溶液中:(R2-)c(H R),故C错误;
2 2
D.如图在pH=4.3时溶液中c(R2-)=c(HR-),溶液中电荷守恒为c(Na+)+c(H+)=2c(R2-)+c(HR-)+c(OH-),故
3c(R2-)=c(Na+)+c(H+)-c(OH-),则pH=4时3c(R2-)c(M+)>c(H+)=c(OH-)
D.室温下M+的水解常数K =10×10-5
h
【答案】B
【分析】
a点主要是MOH和少量MSO ,b点MOH和MSO 比为2:1,c点为酸碱恰好反应的点,生成了强酸弱碱
2 4 2 4
盐,促进了水解,从c点以后,硫酸过量,酸抑制水的电离,硫酸属于强酸,对水的电离平衡抑制程度较
大;根据电荷守恒和物料守恒分析溶液中浓度关系;利用起点MOH溶液中,AG=lg =-8,计算
MOH的电离常数,再利用M+的水解常数K = 计算。
h
【解析】
A. c点为酸碱恰好反应的点,生成了强酸弱碱盐,促进了水解,从c点以后,硫酸过量,酸抑制水的电
离,硫酸属于强酸,对水的电离平衡抑制程度较大,因此水的电离程度:c>b>d,故A错误;
B.b点,MOH和MSO 比为2:1,电荷守恒:2c(SO )+c(OH-)=c(M+)+c(H+),物料守恒:c(M+)
2 4
+c(MOH)=4c(SO ), 消去c(SO )得b点对应的溶液中:c(M+)-c(MOH)=2c(OH-)-2c(H+),故B正确;C.当AG=lg =0时,则 =1,即c(H+)=c(OH-),根据电荷守恒:2c(SO )+c(OH-)=c(M+)
+c(H+),则有2c(SO )=c(M+),所以溶液中有:c(M+)>c(SO )>c(H+)=c(OH-),故C错误;
D.由图可知,MOH溶液中,AG=lg =-8,则 =10-8,根据Kw=c(H+)×c(OH-)=1×10-14可知:
c(OH-)=1×10-3mol/L,K = ≈ =10-5, 室温下M+的水解常数K =
b h
=1.0×10-9,故D错误;故选B。
8.(2021·江西九江市·高三一模)已知: ,25℃时, 的 , 。
用 溶液滴定 溶液的滴定曲线如图所示(曲线上的数字为pH)。下
列说法正确的是
A.a点所得溶液中:
B.c点所得溶液中:
C.当溶液的pH为7时,此时加入NaOH溶液体积为30mL
D.随着NaOH溶液滴入,水的电离程度一直增大
【答案】B
【解析】
A.a点所得溶液中,pH=1.85,即c(H+)=10-1.85,又 ,故c(H A)=c(HA-),又a
2点溶液体积大于20mL,导致含有A元素微粒浓度之和减小,所以c(H A) +c(A2-)+c(HA-) < 0.1mol∙L-1,故
2
a点溶液中, ,故A错误;
B. c点所得溶液中,pH=7.19,即c(H+)=10-7.19,又 ,则c(A2-)=c(HA-),溶液中
存在电荷守恒2c(A2-)+c(HA-) + c(OH-)=c(H+) + c(Na+),3c(HA-) + c(OH-)=c(H+) + c(Na+),此时溶液显碱性,
c(OH-)>c(H+) ,则c点所得溶液中: ,故B正确;
C. 当加入NaOH溶液体积为30mL时,溶液恰好为等物质的量浓度的NaHA、NaA的混合溶液,A2-的水
2
解常数为 ,即A2-的水解程度大于HA-的电离程度,则此时溶液显碱性,故
C错误;
D. 随着NaOH溶液滴入,依次发生反应HA+ OH-= HA-+H O、HA-+ OH-= A2-+H O,水的电离程度逐渐增
2 2 2
大,当恰好反应生成NaA时,水的电离程度最大,继续滴入NaOH,水的电离程度逐渐减小,故D错误;
2
故选B。
9.(2021·浙江高三三模)一定温度下,难溶电解质在水中存在沉淀溶解和生成的平衡,常用溶度积
来表示溶解程度的大小,如 。常温下用 的 标准溶液(
)分别滴定 的 溶液和 溶液,混合溶液的 [定义为
]与 溶液体积的变化关系如图所示。下列说法不正确的是A.
B.当 时, 溶液中:
C.当 时, 溶液中:
D.相同实验条件下,若改用 溶液,则滴定曲线(滴定终点前)可能变为
【答案】C
【解析】
A.由图可知,当未加入AgNO 溶液时,溶液中Ag+的浓度即为AgCl、AgBr分别在0.1mol/L的NaCl、
3
NaBr溶液中的Ag+浓度,故有 ,
,故有 ,A正确;
B.当 时,即AgNO 与NaBr恰好完全反应,根据溶液中电荷守恒可知, 溶
3
液中: ,B正确;
C.当 时,溶液为NaNO 、AgNO 和AgCl的溶解平衡,由图可知,此时c(Ag+)≈10-
3 3
1.5,故c(Cl-)= = <c(H+),故 溶液中:,C错误;
D.相同实验条件下,若改用 溶液,由于起始时c(Cl-)增大,故开始时
c(Ag+)更小, 更大,则滴定曲线(滴定终点前)可能变为 ,D正确;
故答案为:C。
10.(2021·河南高三三模)常温下,铁的氢氧化物 ( 或3)的沉淀溶解平衡与溶液pH的关系
如图所示,其中 。下列叙述错误的是
A.Ⅰ表示 的曲线
B. 的
C.在Y点通入足量的 将达到R点(忽略溶液体积变化)
D.在Q点加水稀释可能移到M点
【答案】C
【分析】
铁的氢氧化物的溶度积为K =c(Fen+)cn(OH—)可得,饱和溶液中pFe=pK +3pH—14n,则氢氧化铁饱和溶液
sp sp
中pFe=pK +3pH—42,氢氧化亚铁饱和溶液中pFe=pK +2pH—28,则曲线Ⅰ表示氢氧化铁的沉淀溶解平
sp sp
衡与溶液pH的关系,曲线Ⅱ表示氢氧化亚铁的沉淀溶解平衡与溶液pH的关系。
【解析】
A.由分析可知,曲线Ⅰ表示氢氧化铁的沉淀溶解平衡与溶液pH的关系,故A正确;
B.由图可知,X点pFe为1、pH为7,则pK =pFe—2pH+28=15,K =1×10—15,故B正确;
sp spC.由分析可知,氢氧化铁饱和溶液中的铁离子浓度小于氢氧化亚铁饱和溶液中亚铁离子浓度,由图可知,
Y点溶液中亚铁离子浓度与R点溶液中铁离子浓度相等,则在Y点通入足量的氧气不可能将达到R点,故
C错误;
D.在Q点加水稀释时,氢氧化铁饱和溶液中的铁离子浓度和氢氧根离子的浓度都会减小,可能移到M点,
故D正确;
故选C。
11.(2021·山东潍坊市·高三模拟) 时,向 邻苯二甲酸 溶液中加入 固
体,混合溶液的pH随 以及 的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发).
下列有关叙述错误的是
A.邻苯二甲酸的 约为
B.b点有关微粒浓度大小关系为
C.从a点到c点,水电离的 先增大后减小
D. 时,
【答案】C
【解析】
A.pH=0时,c(H+)=1mol/L,-lgc(HA-)=4,则c(HA-)=10-4mol/L,HA电离程度较小,则溶液中
2
c(HA)≈0.1mol/L,邻苯二甲酸的K = ≈≈ =1.0×10-3,A正确;
2 a1
B.b点溶液中纵坐标最小,则该溶液中c(HA-)最大,溶液中溶质为KHA,溶液pH<7,溶液呈酸性,说明HA-电离程度大于水解程度但电离和水解程度都较小,水电离也生成H+,所以溶液中存在c(K+)>c(HA-)
>c(H+)>c(A2-)>c(OH-),B正确;
C.a点的溶质为HA,b点溶质为KHA,c点溶质为KA和KHA,此时溶液都呈酸性,说明HA-电离程度
2 2
大于水解程度,抑制水电离,但由于溶液的pH值一直增大,说明HA、HA-电离出的H+的抑制作用减弱,
2
故水电离出的c(H+)一直增大,C错误;
D.由图像可知,c点时,c(HA-)=c(A2-),故HA的Ka= =10-5.8,故当pH=10时,溶液中的
2 2
溶质为KA,故Kh = = = ,故 ,D
2 1
正确;
故答案为:C。
12.(2021·重庆高三三模)向一定体积的稀 溶液中逐滴滴加某浓度的稀盐酸溶液,混合溶液的
、温度变化如图所示,下列有关说法错误的是
A.c点溶液,有
B. ,温度升高说明 与 反应放热
C. ,滴入 消耗 ,导致 迅速降低
D. ,发生的主要离子反应为
【答案】A
【解析】A. c点为碳酸钠与盐酸按1:1滴定形成的NaHCO 溶液,根据物料守恒有
3
,选项A错误;
B. ,是发生反应 ,温度升高说明 与 反应放热,选项B正确;
C. ,滴入 消耗 ,反应 ,溶液碱性减弱,导致 迅速降低,选项C正
确;
D. ,碳酸氢钠与盐酸反应产生二氧化碳,发生的主要离子反应为 ,选项
D正确;
答案选A。
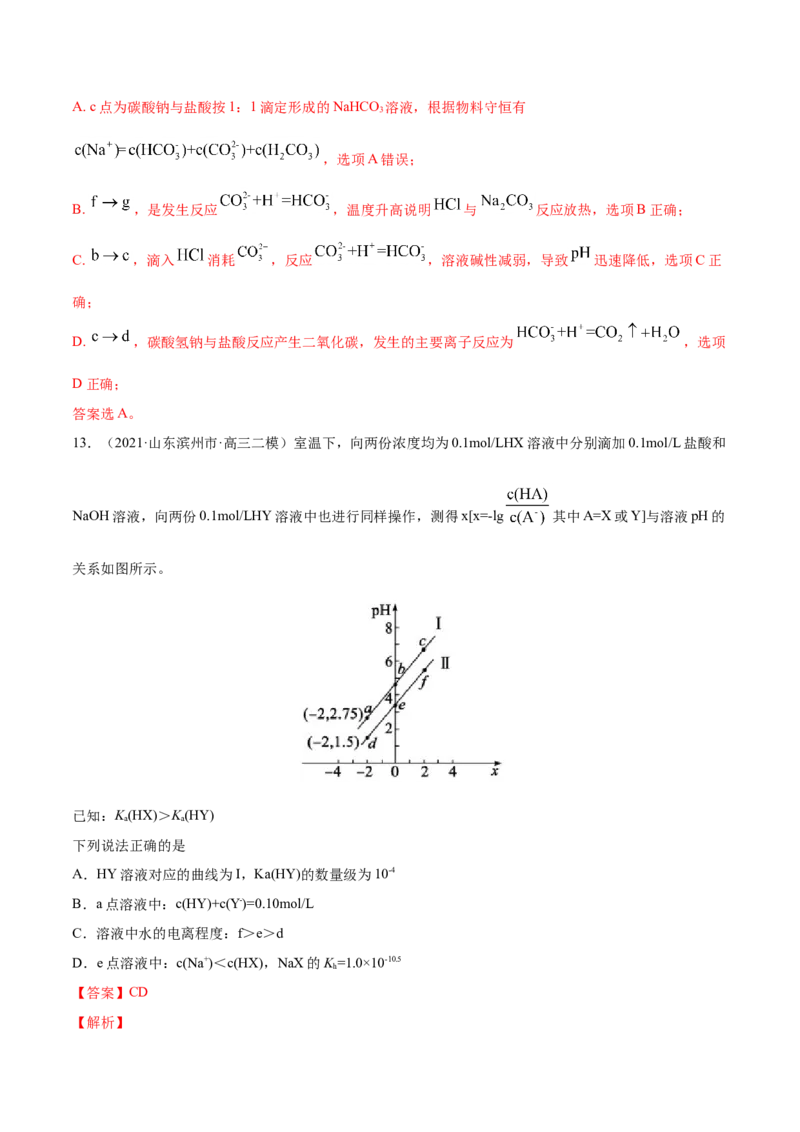
13.(2021·山东滨州市·高三二模)室温下,向两份浓度均为0.1mol/LHX溶液中分别滴加0.1mol/L盐酸和
NaOH溶液,向两份0.1mol/LHY溶液中也进行同样操作,测得x[x=-lg 其中A=X或Y]与溶液pH的
关系如图所示。
已知:K(HX)>K(HY)
a a
下列说法正确的是
A.HY溶液对应的曲线为I,Ka(HY)的数量级为10-4
B.a点溶液中:c(HY)+c(Y-)=0.10mol/L
C.溶液中水的电离程度:f>e>d
D.e点溶液中:c(Na+)<c(HX),NaX的K =1.0×10-10.5
h
【答案】CD
【解析】A.由HA H++A-可知:K(HA)= ,-lg K(HA)=- lg =- lg c(H+)+lg
a a
,整理得:pH=- lg K(HA)+[- lg ]=- lg K(HA)+ x,又因为K(HX)>K(HY),所以pH:HX
a a a a
II,所以HY溶液对应的曲线为I,Ka(HY)的数量级为10-5,故A错
误;
B.曲线I为对应的HY溶液,设0.10mol/LHY溶液中c(H+ )=m mol · L-l,K (HY) = =10-4.75, c(H+ )
10-2.9 mol · L-l,pH=2.9,a点时溶液pH=2.75,说明加了盐酸,溶液体积增大,根据物料守恒c(HY)
+c(Y-)<0.10mol/L,故B错误;
C.HX为弱酸,设0.10mol/LHX溶液中c(H+ )=m mol · L-l,K (HX) = =10-3.5, c(H+ ) 10-2.25
mol · L-l,pH=2.25,d点的pH=1.5,说明d点滴加了酸,抑制了水的电离,e点和f点滴加了NaOH溶液,
趙向于滴定終点,但滴定终点为碱性溶液,所以f点还没有达到滴定終点,所以溶液中水的电离程度:f>
e>d,故C正确;
D.根据上述分析可知:e点x=0、 pH=3.5说明c(HX)=c(X- ),溶液中电荷守恒关系为c(H+ )+c(Na+ )=c(X-)
+c(OH-),所以c(H+)+c(Na+ )=c(HX)+c(OH- ),由于溶液中 c(H+)>c(OH- ),所以c(Na+ )c(HCOO-)>c(OH-)>c(H+)
C.滴加NaOH溶液的过程中,混合溶液的导电性逐渐增强
D.常温下,K(HCOOH)的数量级为10-5
a
【答案】D
【解析】
A.a点为HCOOH和HCOONa的混合溶液,pH=7,酸电离对水电离的抑制作用于盐水解对水电离的促进
作用相抵消,水的电离程度与纯水相同。最高点为HCOONa溶液,水的电离程度最大,b点为NaOH和
HCOONa的混合溶液,水的电离程度与纯水相同,但pH>7,A说法正确;
B.b点为NaOH和HCOONa的混合溶液,虽然水的电离程度与纯水相同,但pH>7,离子浓度大小为
c(Na+)>c(HCOO-)>c(OH-)>c(H+),B说法正确;
C.NaOH溶液加入的过程中,溶液由1mol·L-1的HCOOH(弱电解质)溶液到0.5mol·L-1的HCOONa(强电解
质)溶液,最后无限接近1mol·L-1的NaOH(强电解质)溶液,整个过程导电性一直增强,C描述正确;
D.该过程中,起始点为1mol·L-1的HCOOH溶液,c (H+)=1×10-12mol/L,则HCOOH电离产生的
水
c(H+)=1×10-2mol/L,故K 约等于(1×10-2)2/1,数量应为10-4,D说法错误;
a
答案为D。
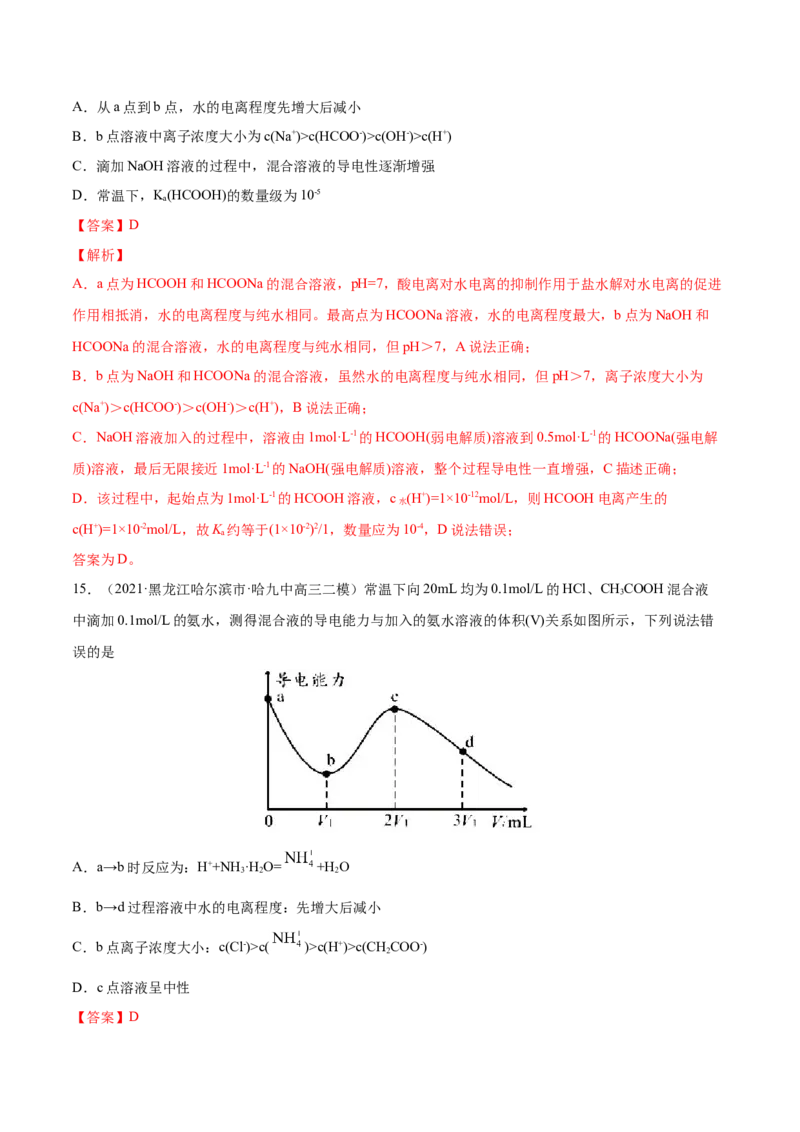
15.(2021·黑龙江哈尔滨市·哈九中高三二模)常温下向20mL均为0.1mol/L的HCl、CHCOOH混合液
3
中滴加0.1mol/L的氨水,测得混合液的导电能力与加入的氨水溶液的体积(V)关系如图所示,下列说法错
误的是
A.a→b时反应为:H++NH·H O= +H O
3 2 2
B.b→d过程溶液中水的电离程度:先增大后减小
C.b点离子浓度大小:c(Cl-)>c( )>c(H+)>c(CH COO-)
2
D.c点溶液呈中性
【答案】D【解析】
A.a→b时溶液导电能力减弱到最低,为氨水与盐酸反应,离子数量不变但溶液体积增大,故发生反应为:
H++NH·H O= +H O,选项A正确;
3 2 2
B.b→d过程溶液导电能力先增大后减小,为氨水与醋酸反应至氨水过量,先对水的电离抑制程度变小后
增大,故水的电离程度:先增大后减小,选项B正确;
C.b点氨水与盐酸完全反应,为氯化氨和醋酸按1:1形成的溶液,离子浓度大小:c(Cl-)>c(
)>c(H+)>c(CH COO-),选项C正确;
2
D.c点为氯化铵和醋酸铵按1:1形成的溶液,氯化铵为强酸弱碱盐水解呈酸性,醋酸铵为弱酸弱碱盐水
解呈中性,故溶液呈酸性,选项D错误;
答案选D。
16.(2021·浙江高三模拟)25℃时,分别用浓度为 、 和 的NaOH溶液
滴定浓度不同、体积均为20mL的3种HCl溶液,测得3个溶液的pH随 变化的曲线如图,在
恰好中和。下列说法不正确的是
A.以a作指示剂时,滴定终点颜色变化为无色恰好变为浅红色
B.曲线X、Y、Z对应的
C.滴定溶液浓度不宜过高,因为在中和点附近多加l滴溶液引入的误差较大
D.由图可知溶液浓度越小,突跃范围越大,可供选择的指示剂越多【答案】D
【解析】
A.a指示剂的变色范围为8-10,则a为酚酞,滴定终点颜色变化为无色恰好变为浅红色,故A正确;
B.根据滴定后pH 值 ,可知曲线X、Y、Z对应的 ,故B正确;
C.滴定溶液浓度不宜过高,因为盐酸浓度不确定,两者弱浓度差较大,中和点附近多加l滴溶液引入的误
差较大,故C正确;
D.由图可知溶液浓度越小,突跃范围越大,可供选择的指示剂越少,故D错误;
故选D。
17.(2021·福建龙岩市·高三三模)室温下,向20.00mL 0.10mol·L﹣1 HX溶液中逐滴滴加0.10mol·L﹣1
NaOH溶液,溶液pH随 变化关系如图所示,已知 。下列说法错误的是
A.HX的电离常数
B.当 时,加入NaOH溶液的体积小于10.00mL
C.当加入10.00mL NaOH溶液时:
D.如图所示各点对应溶液中水的电离程度:a>c
【答案】D
【解析】
A.K= ,pK= =-lg =-lgc(H+)-lg =pH-(- lg )= pH-p
a a,即pK= pH-p 。温度不变pK 为常数,将(-1,3.75)带入可得3.75= pK-1,pK=4.75,则
a a a a
, 故A正确;
B. K=10-4.75,则X-的K = =10-9.25,即X-的水解程度小于HX的电离程度。当NaOH溶液的体积为
a h
10.00mL时,溶液中的溶质为等浓度的HX和NaX,则等浓度的HX和NaX的混合溶液中c(X-)> c(HX) ,
当p =0时,c(X-)= c(HX),则加入NaOH溶液的体积应小于10.00 mL,故B正确;
C.当NaOH溶液的体积为10.00mL时,溶液中的溶质为等浓度的HX和NaX,存在电荷守恒c(H+)+c(Na
+)=c(X-)+c(OH-),存在物料守恒2c(Na+)=c(X-)+c(HX),二式联立可得
,故C正确;
D.由图可知,c点的pH大于a点的pH,溶液的酸性越强,水的电离被抑制越大,故a点水的电离程度小
于c点水的电离程度,即ac(H PO )>c(HPO )>c(H PO )
2 4 2 3 4
B.当pH=7.1时,溶液中c(Na+)>3c(H PO )+3c(PO )
2
C.甲基橙的变色范围为3.1~4.4,若以甲基橙为指示剂,当溶液由红色变为橙色时,主要反应的离子方程式为HPO +OH-=HPO +H O
2 2
D.25℃,pH=3时溶液中 =0.1
【答案】C
【解析】
A.由图可知pH=2时c(HPO )=c(H PO ),此时K =c(H+)=10-2mol·L-1,同理可得K =10-7.1,K =10-12.2,
2 3 4 a1 a2 a3
NaH PO 的水解常数K= = c(H PO ),溶液中:c(Na+)>c(H PO )>c(HPO )>c(H PO ),故A正确;
3 4 2 3 4
B.当pH=7.1时,由电荷守恒可知:c(Na+)+c(H+)=c(OH-)+c(H PO )+3c(PO )+2c(HPO ),由图可知此时:
2
c(HPO )=c(HPO ),则c(Na+)+c(H+)=c(OH-)+3c(H PO )+3c(PO ),同时c(H+)3c(H PO )+3c(PO ),故B正确;
2
C.甲基橙由红色变橙色时的pH值为3.1,根据Ka=10-7.1可以计算0.1mol/LpH约为4,可知此时主要的转
2
化为HPO +OH-=H PO +H O,故C错误;
3 2 2
D.K = , ,当pH值为3时,c(H+)=10-3mol·L-1, =
a1
=0.1,故D正确;
故选:C。
19.(2021·广东茂名市·高三三模)常温下,用如图1所示装置,分别向 溶液
和 溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积
的变化曲线如图2所示。下列说法正确的是A.X曲线为 溶液的滴定曲线
B.b点溶液的pH大于c点溶液的pH
C.c点的溶液中:
D.a、d两点水的电离程度:a>d
【答案】D
【解析】
A.碳酸钠溶液中滴加盐酸时先发生反应 ,然后发生
,碳酸氢钠溶液中滴加盐酸时发生 ,所以滴加
25mL盐酸时,碳酸钠溶液中几乎不产生二氧化碳,压强几乎不变,而碳酸氢钠恰好完全反应,压强达到
最大,所以X代表 溶液,Y代表 溶液,A错误;
B.b点溶液溶质为NaCl,c点溶液溶质为 ,所以c点代表溶液的pH更大,B错误;
C.c点溶液溶质主要为 ,溶液显碱性,碳酸氢根的水解程度大于电离程度,而水解和弱电解质
的电离都是微弱的,所以 ,C错误;
D.d点盐酸和碳酸钠恰好完全反应,溶质为NaCl,还有少量溶解的二氧化碳,而a点溶质为碳酸钠和碳
酸氢钠, 、 的水解都会促进水的电离,所以a点水的电离程度更大,D正确;
综上所述答案为D。
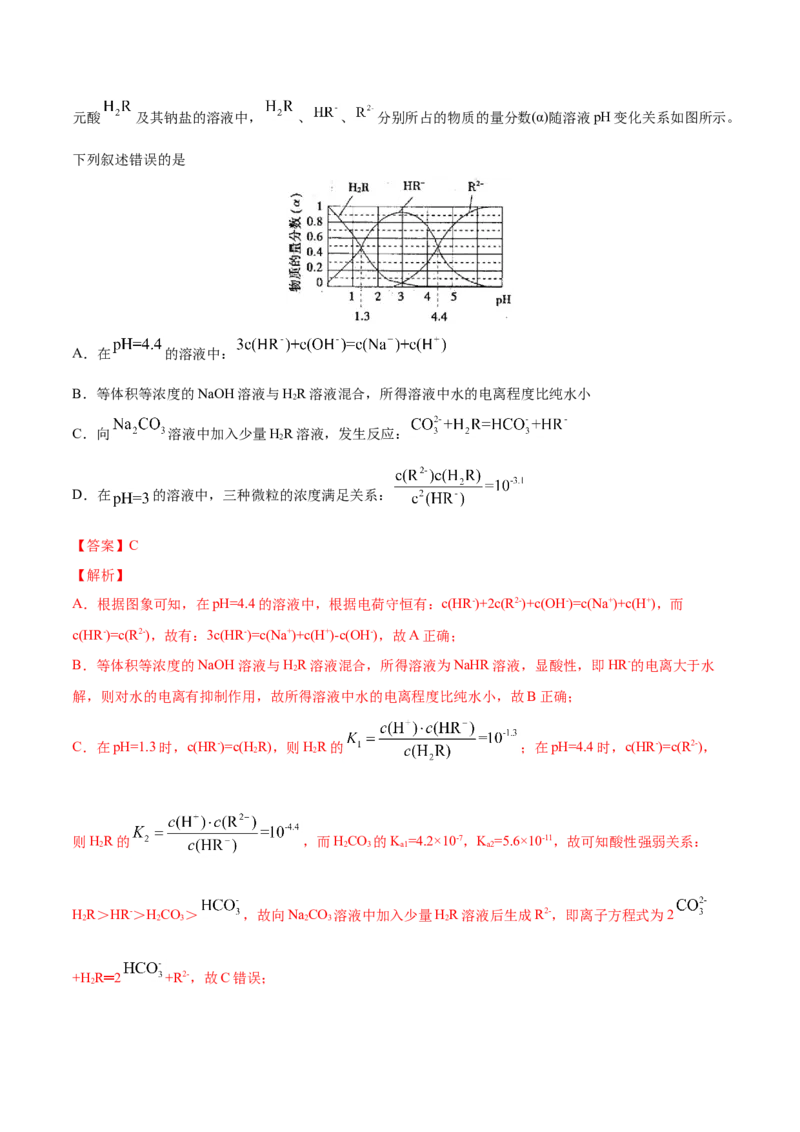
20.(2021·广东梅州市·高三二模)已知:常温下, 的 , ;某二元酸 及其钠盐的溶液中, 、 、 分别所占的物质的量分数(α)随溶液pH变化关系如图所示。
下列叙述错误的是
A.在 的溶液中:
B.等体积等浓度的NaOH溶液与HR溶液混合,所得溶液中水的电离程度比纯水小
2
C.向 溶液中加入少量HR溶液,发生反应:
2
D.在 的溶液中,三种微粒的浓度满足关系:
【答案】C
【解析】
A.根据图象可知,在pH=4.4的溶液中,根据电荷守恒有:c(HR-)+2c(R2-)+c(OH-)=c(Na+)+c(H+),而
c(HR-)=c(R2-),故有:3c(HR-)=c(Na+)+c(H+)-c(OH-),故A正确;
B.等体积等浓度的NaOH 溶液与HR溶液混合,所得溶液为NaHR溶液,显酸性,即HR-的电离大于水
2
解,则对水的电离有抑制作用,故所得溶液中水的电离程度比纯水小,故B正确;
C.在pH=1.3时,c(HR-)=c(H R),则HR的 ;在pH=4.4时,c(HR-)=c(R2-),
2 2
则HR的 ,而HCO 的 K =4.2×10-7,K =5.6×10-11,故可知酸性强弱关系:
2 2 3 a1 a2
HR>HR->HCO> ,故向NaCO 溶液中加入少量HR溶液后生成R2-,即离子方程式为2
2 2 3 2 3 2
+H R═2 +R2-,故C错误;
2D.在pH=3 的溶液中,HR的 ,而NaR的
2 2
,则
,则
,故D正确;
故选:C。
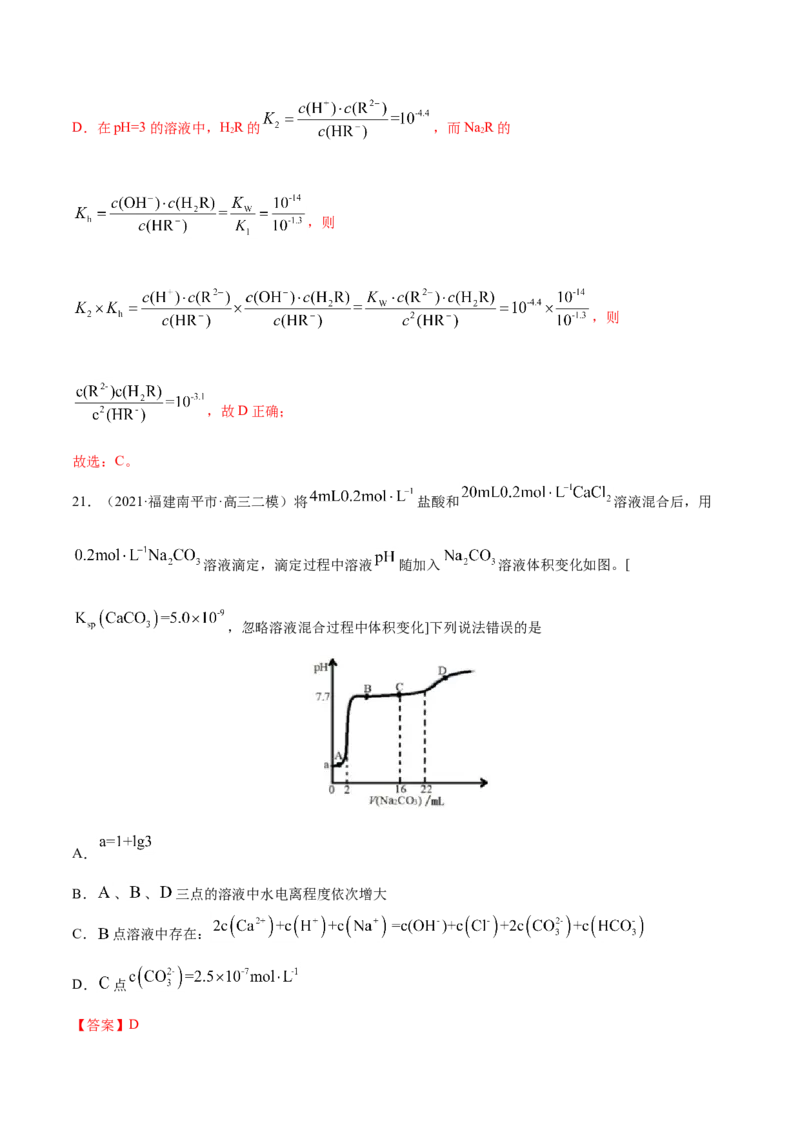
21.(2021·福建南平市·高三二模)将 盐酸和 溶液混合后,用
溶液滴定,滴定过程中溶液 随加入 溶液体积变化如图。[
,忽略溶液混合过程中体积变化]下列说法错误的是
A.
B. 、 、 三点的溶液中水电离程度依次增大
C. 点溶液中存在:
D. 点
【答案】D【解析】
A. 盐酸和 溶液混合后,c(HCl)=
,故pH=-lgc(H+),故 ,A正确;
B.将 盐酸和 溶液混合后,用 溶液滴定,
反应的顺序为:NaCO+2HCl=NaCl+H O+CO↑,CaCl +Na CO=CaCO ↓+2NaCl,故 点对应的溶质为
2 3 2 2 2 2 3 3
HCl和NaCl、CaCl , 对应的溶质为NaCl、CaCl , 对应的溶质为:NaCl、CaCl 和NaCO,故A点
2 2 2 2 3
HCl电离出的H+抑制水的电离,B点则无水解也无电离,对水的电离无影响,D由于NaCO 的水解而促进
2 3
水的电离,故A、B、D三点的溶液中水电离程度依次增大,C正确;
C.根据溶液中电荷守恒可知, 点溶液中存在:
,C正确;
D. 点对应的溶液中,c(Ca2+)= ,故
,D错误;
故答案为:D。
22.(2021·广东汕头市·高三二模)柠檬酸(用HA表示)是一种高效除垢剂,现用一定浓度的柠檬酸溶液去
3
除水垢,溶液中HA、HA-、HA2-、A3-的百分含量随pH的变化曲线如图所示。下列说法中不正确的是
3 2
A.曲线b表示HA-的变化曲线
2
B.HA的第二步电离常数K (H A)约为10-4.8
3 a2 3C.NaHA溶液中HA2-的水解程度小于电离程度
2
D.pH=4时,
【答案】D
【分析】
根据酸碱中和原理,随着pH逐渐增大,HA逐步被中和,故曲线a代表HA,曲线b代表HA-,曲线c代
3 3 2
表HA2-,曲线d代表A3-。
【解析】
A.由分析知,曲线b代表HA-,A正确;
2
B.曲线b、c的交点对应pH=4.8,此时c(H A-)=c(HA2-),HA的第二步电离方程式为:HA- HA2-+H+,
2 3 2
则K (H A)= =c(H+)=10-4.8,B正确;
a2 3
C.在NaHA溶液中,c(HA2-)浓度达到最大,对应图中c点,此时溶液pH<7,说明HA2-水解程度小于电
2
离程度,C正确;
D.柠檬酸除水垢后,溶液中含有H+、Ca2+、Mg2+、HA-、HA2-、A3-、OH-等离子,对应电荷守恒为:
2
c(H+)+2c(Ca2+)+2c(Mg2+)=c(H A-)+2c(HA2-)+3c(A3-)+c(OH-),由图知,此时溶液中c(A3-)浓度非常小,而由于
2
柠檬酸pH由起始约为1增大到4,说明柠檬酸已经反应了一定量水垢,故溶液中有一定量的Ca2+、Mg2+,
即2c(Ca2+)+2c(Mg2+)>3c(A3-),则c(H+)<c(H A-)+2c(HA2-)+c(OH-),D错误;
2
故答案选D。
23.(2021·辽宁大连市·高三二模)化学中常用AG表示溶液的酸度[ ]。室温下,向
20.00mL0.1000mol•L-1的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积
的变化如图所示。下列说法错误的是A.稀硫酸的物质的量浓度为0.0500mol•L-1
B.a、b、c三点对应的溶液中,水的电离程度大小关系:c>b>a
C.当AG=0时,溶液中存在c( )>c( )>c(H+)=c(OH-)
D.室温下 的电离常数K=1.0×10-6
b
【答案】D
【解析】
A.酸碱中和恰好完全时放出的热量最大,温度最高,由图像可知,c点为恰好中和的点,2
+H SO =(NH)SO +2H O,c处消耗硫酸20ml,所以n(H SO )= 0.5×n( )=0.5×20.00×10-
2 4 4 2 4 2 2 4
3L×0.1000mol•L-1=10-3mol,故c(HSO )= = =0.0500mol•L-1,A正确;
2 4
B.c点为恰好中和的点,生成的硫酸铵最多,水解程度最大,对水的电离促进程度最大,a点生成的硫酸
铵比b点还少,故水的电离程度大小关系:c>b>a,B正确;
C.根据电荷守恒c( )+c(H+)=2c( )+c(OH-),当AG=0时,即 =0,c(H+)= c(OH-),
故c( )=2c( ),溶液中硫酸铵完全电离, 、 大量存在,综上所述,当AG=0时,溶液中
存在c( )>c( )>c(H+)=c(OH-),C正确;D.由图像可知,当 =-8时,溶液为氨水, =10-8,因室温下K = c(H+)c(OH-)= 10-
W
14,得c(OH-)= 10-3 mol•L-1,室温下 的电离常数K= =1.0×10-5,D
b
错误。故选D。
24.(2021·浙江高三二模)甲胺 的性质与氨相似,25℃时向 的甲胺中逐滴
滴入 稀盐酸。溶液中水电离出的氢离子浓度的负对数[用pC表示, ]与加入盐
酸体积的关系如图所示。下列叙述不正确的是
A. 的数量级为
B.甲胺的电离方程式:
C.b点溶液中甲胺的电离程度大于盐酸甲胺的水解程度
D.e点溶液:
【答案】B
【分析】
CHNH 性质与氨相似,故甲胺溶于水存在如下平衡:
2 2
,由于甲胺溶于水后电离产生OH-,所以会抑制水
的电离,随着盐酸的加入,甲胺逐渐转化为甲胺盐CHNH Cl,由CHNH ·HO电离产生的OH-减少,对水
3 3 3 2 2
电离的抑制程度逐渐减弱,同时生成的 水解会促进水的电离,当甲胺完全反应生成CHNH Cl时,
3 3水的电离程度达到最大(受 水解促进),对应图中e点,e点之后过量的盐酸又抑制水的电离,
故水的电离又逐渐减弱。
【解析】
A.可用图中a点数据计算K (CHNH ),此时c(H+,水)=10-11.8,在甲胺溶液中,H+只有HO一个来源,故
b 3 2 2
溶液中c(H+)= c(H+,水)=10-11.8,则c(OH-)= ,c( )与c(OH-)近似相等,甲胺
浓度近似等于起始浓度,故K (CHNH )= ,对应数量级为10-4,A正确;
b 3 2
B.甲胺性质类似氨,故CHNH ·HO类似NH ·HO,属于弱电解质,不完全电离,电离方程式连接符号
3 2 2 3 2
应该用可逆符号“ ”,B错误;
C.由数据知,b点加入的HCl与甲胺物质的量之比为1:2,故b点对应溶液组成为CHNH 、CHNH Cl,
3 2 3 3
两者近似1:1,由图示知,此时溶液中水电离产生的c(H+,水)小于10-7 mol/L,说明水的电离受到抑制,故
此时CHNH 的电离程度大于 的水解程度,C正确;
3 2
D.由分析知,e点甲胺恰好反应,故溶液组成为CHNH Cl,CHNH Cl完全电离,故溶液中大量存在Cl-
3 3 3 3
与 ,由于 水解损耗,故c(Cl-)>c( ),H+、OH-都是微弱过程产生,故微量存
在,由于 水解使溶液显酸性,故c(H+)>c(OH-),综上所述:c(Cl-)>c( )>c(H+)>
c(OH-),D正确;故答案选B。
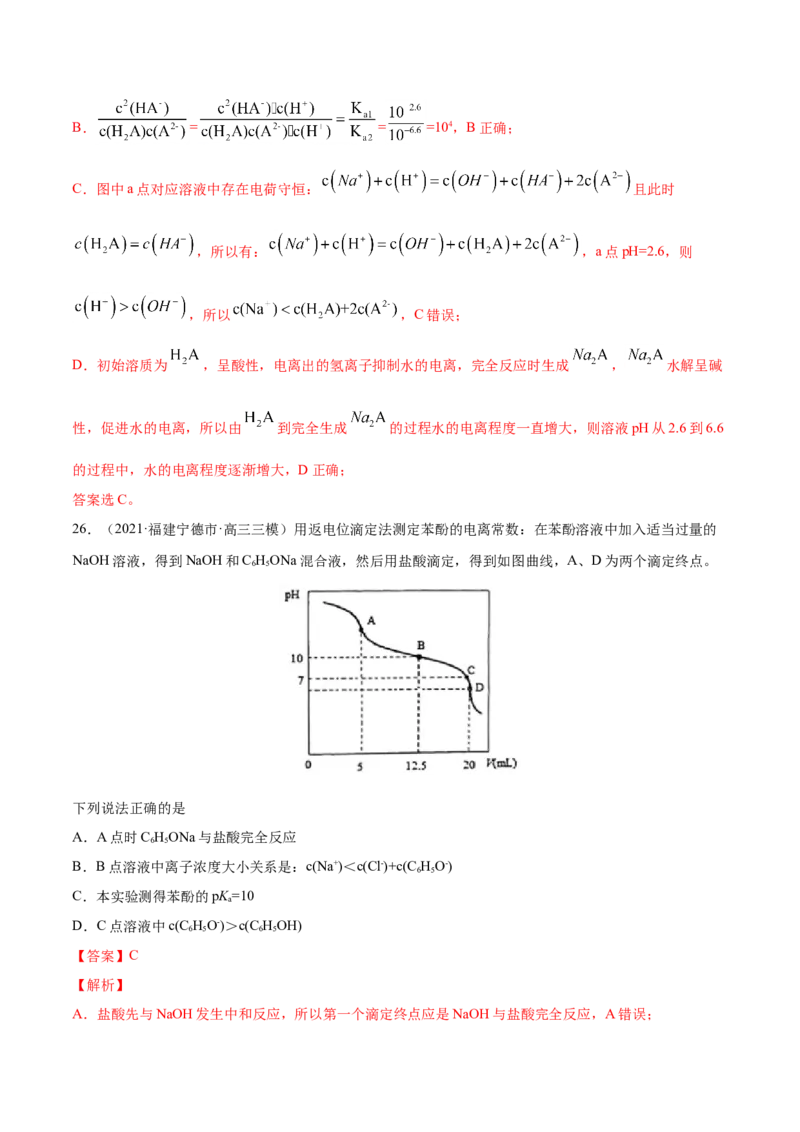
25.(2021·陕西西安市·高三二模)常温下将 溶液滴加到 溶液中,混合溶液的 与离子浓度
变化的关系如图所示(纵坐标为 )。下列叙述错误的是A.曲线M表示pH与 的关系
B. = 104
C.图中a点对应溶液中:
D.溶液pH从2.6到6.6的过程中,水的电离程度逐渐增大
【答案】C
【分析】
, ,因为纵坐标为 ,分别取a、b点,
则此时对应曲线上有 和 ,可以算出对应曲线的电离平衡常数为10-2.6
和10-6.6,因为 > ,所以 =10-2.6, =10-6.6,所以曲线M、N分别表示pH与 和pH与
的关系的关系。
【解析】
A.根据分析可知曲线M表示pH与 的关系,A正确;B. = = =104,B正确;
C.图中a点对应溶液中存在电荷守恒: 且此时
,所以有: ,a点pH=2.6,则
,所以 ,C错误;
D.初始溶质为 ,呈酸性,电离出的氢离子抑制水的电离,完全反应时生成 , 水解呈碱
性,促进水的电离,所以由 到完全生成 的过程水的电离程度一直增大,则溶液pH从2.6到6.6
的过程中,水的电离程度逐渐增大,D正确;
答案选C。
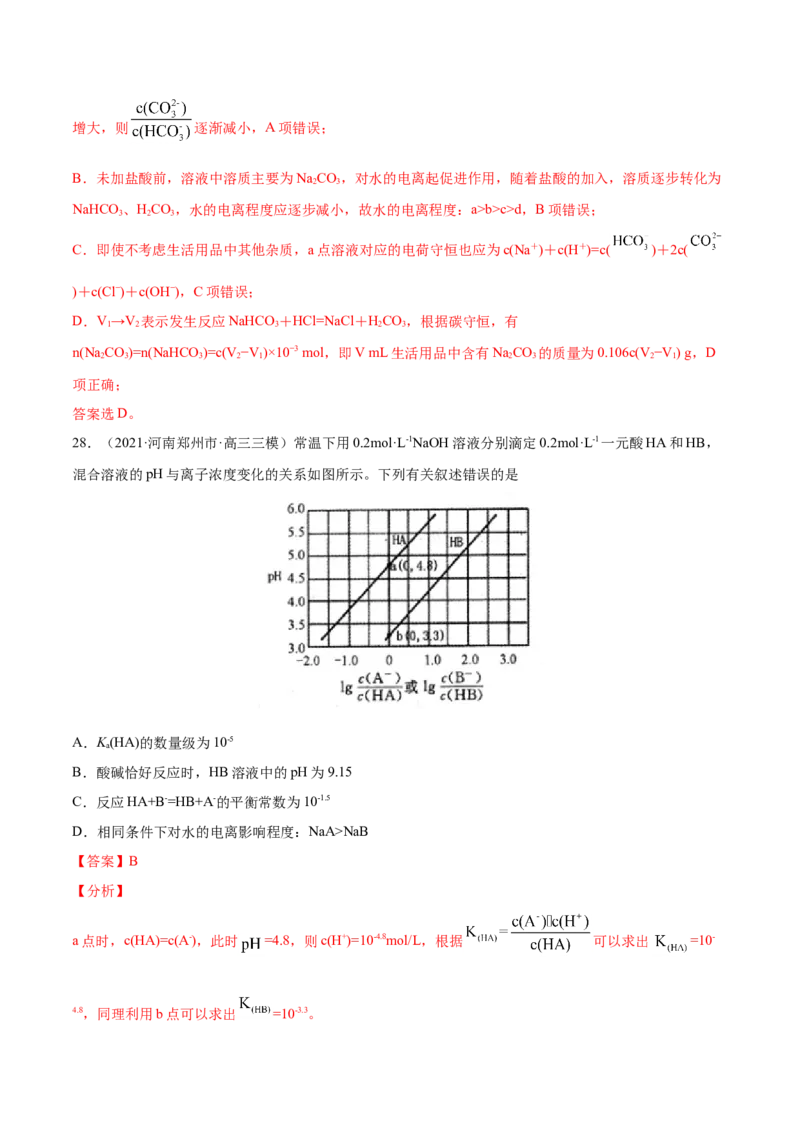
26.(2021·福建宁德市·高三三模)用返电位滴定法测定苯酚的电离常数:在苯酚溶液中加入适当过量的
NaOH溶液,得到NaOH和C HONa混合液,然后用盐酸滴定,得到如图曲线,A、D为两个滴定终点。
6 5
下列说法正确的是
A.A点时C HONa与盐酸完全反应
6 5
B.B点溶液中离子浓度大小关系是:c(Na+)<c(Cl-)+c(C HO-)
6 5
C.本实验测得苯酚的pK=10
a
D.C点溶液中c(C HO-)>c(C HOH)
6 5 6 5
【答案】C
【解析】
A.盐酸先与NaOH发生中和反应,所以第一个滴定终点应是NaOH与盐酸完全反应,A错误;B.B点溶液中存在电荷守恒c(H+)+c(Na+)=c(Cl-)+c(C HO-)+c(OH-),据图可知此时pH为10,溶液显碱性,
6 5
所以c(H+)<c(OH-),则c(Na+)>c(Cl-)+c(C HO-),B错误;
6 5
C.苯酚的K= ,从A点到D点消耗15mL盐酸,即C HONa消耗15mL盐酸,从A点
a 6 5
到B点所用盐酸为7.5mL,则恰好反应一半C HONa,可近似认为此时溶液中c(C HOH)=c(C HO-),则
6 5 6 5 6 5
K=c(H+),所以pK=pH=10,C正确;
a a
D.C点接近C HONa完全反应的点,溶液中溶质为NaCl、C HOH和极少量的C HONa,C HOH的电离
6 5 6 5 6 5 6 5
微弱,所以c(C HO-)<c(C HOH),D错误;
6 5 6 5
综上所述答案为C。
27.(2021·广东高三模拟)电位滴定是利用溶液电位突变指示终点的滴定法。常温下,用cmol·L−1HCl标
准溶液测定VmL某生活用品中NaCO 的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过
2 3
程中溶液电位与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出NaCO 的量。
2 3
下列说法正确的是
A.a至c点对应溶液中 逐渐增大
B.水的电离程度:a>b>d>c
C.a溶液中存在:c(Na+)+c(H+)=c( )+2c( )+c(OH−)
D.VmL生活用品中含有NaCO 的质量为0.106c(V −V )g
2 3 2 1
【答案】D
【解析】
A.根据 ,推出 ,温度不变,K 不变,但随着盐酸的加入,c(H+)逐渐
a2增大,则 逐渐减小,A项错误;
B.未加盐酸前,溶液中溶质主要为NaCO,对水的电离起促进作用,随着盐酸的加入,溶质逐步转化为
2 3
NaHCO 、HCO,水的电离程度应逐步减小,故水的电离程度:a>b>c>d,B项错误;
3 2 3
C.即使不考虑生活用品中其他杂质,a点溶液对应的电荷守恒也应为c(Na+)+c(H+)=c( )+2c(
)+c(Cl−)+c(OH−),C项错误;
D.V→V 表示发生反应NaHCO +HCl=NaCl+HCO,根据碳守恒,有
1 2 3 2 3
n(Na CO)=n(NaHCO )=c(V −V )×10−3 mol,即V mL生活用品中含有NaCO 的质量为0.106c(V −V ) g,D
2 3 3 2 1 2 3 2 1
项正确;
答案选D。
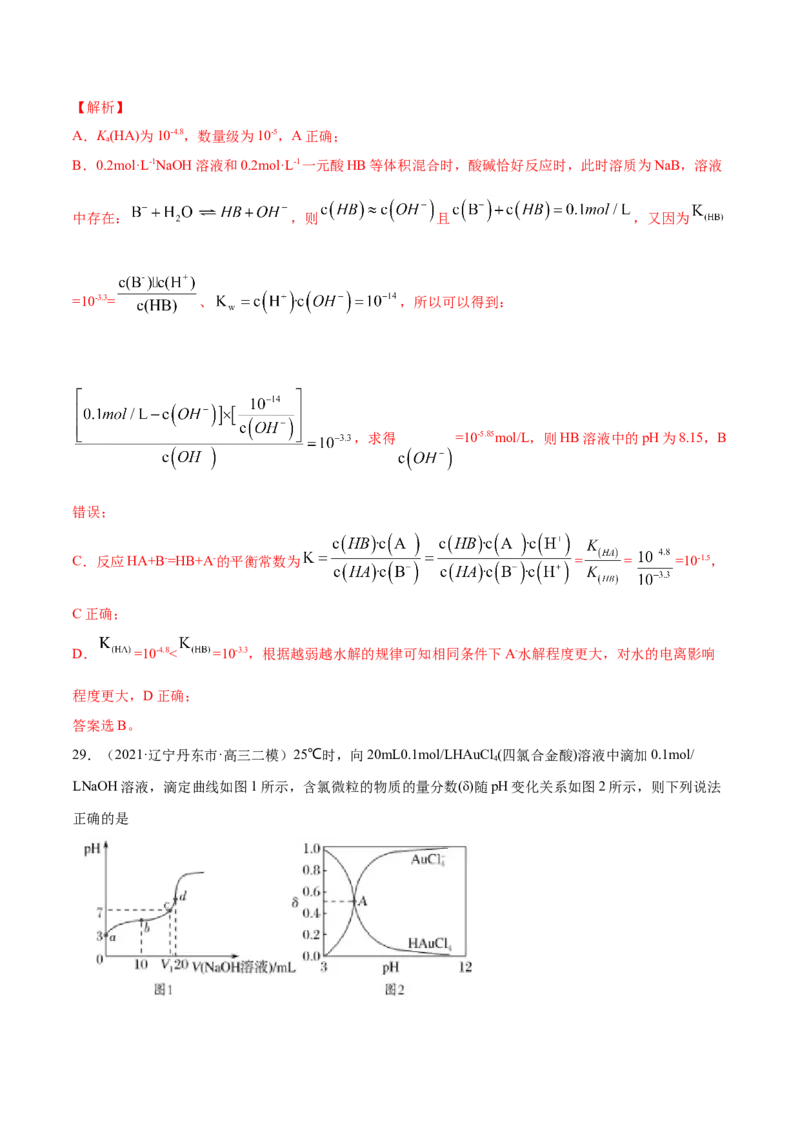
28.(2021·河南郑州市·高三三模)常温下用0.2mol·L-1NaOH溶液分别滴定0.2mol·L-1一元酸HA和HB,
混合溶液的pH与离子浓度变化的关系如图所示。下列有关叙述错误的是
A.K(HA)的数量级为10-5
a
B.酸碱恰好反应时,HB溶液中的pH为9.15
C.反应HA+B-=HB+A-的平衡常数为10-1.5
D.相同条件下对水的电离影响程度:NaA>NaB
【答案】B
【分析】
a点时,c(HA)=c(A-),此时 =4.8,则c(H+)=10-4.8mol/L,根据 可以求出 =10-
4.8,同理利用b点可以求出 =10-3.3。【解析】
A.K(HA)为10-4.8,数量级为10-5,A正确;
a
B.0.2mol·L-1NaOH溶液和0.2mol·L-1一元酸HB等体积混合时,酸碱恰好反应时,此时溶质为NaB,溶液
中存在: ,则 且 ,又因为
=10-3.3= 、 ,所以可以得到:
,求得 =10-5.85mol/L,则HB溶液中的pH为8.15,B
错误;
C.反应HA+B-=HB+A-的平衡常数为 = = =10-1.5,
C正确;
D. =10-4.8< =10-3.3,根据越弱越水解的规律可知相同条件下A-水解程度更大,对水的电离影响
程度更大,D正确;
答案选B。
29.(2021·辽宁丹东市·高三二模)25℃时,向20mL0.1mol/LHAuCl (四氯合金酸)溶液中滴加0.1mol/
4
LNaOH溶液,滴定曲线如图1所示,含氯微粒的物质的量分数(δ)随pH变化关系如图2所示,则下列说法
正确的是A.滴定过程中c( )与c(HAuCl )之和保持不变
4
B.a、b、c、d四点对应溶液中,c点溶液中水的电离程度最大
C. b点对应溶液中:c( )>c(Na+)
D.图2中A点对应溶液中2c(Na+)=c( )+c(HAuCl )
4
【答案】C
【分析】
图1中a点代表HAuCl 起始状态,点时加入NaOH量恰好中和一半HAuCl ,即此时组成为HAuCl 与
4 4 4
NaAuCl 两者浓度相等,c点呈中性,d点代表HAuCl 与NaOH恰好完全反应,组成为NaAuCl 。图2中A
4 4 4
点表示HAuCl 与NaAuCl 浓度相等。
4 4
【解析】
A. 根据元素守恒知HAuCl 与 都来源于起始的HAuCl ,即两者物质的量之和等于原HAuCl 物质
4 4 4
的量,但溶液体积增大,c( )与c(HAuCl )之和减小,选项A错误;
4
B.a、b、c、d四点对应溶液中,a、b、c 点酸还没反应完,酸碱均抑制水的电离,d点完全中和生成强碱
弱酸盐,促进水的电离,故d点溶液中水的电离程度最大,选项B错误;
C.b点组成为HAuCl 与NaAuCl ,存在电荷守恒:c( )+c(OH-)=c(Na+)+ c(H+),由图知b点显酸性,
4 4
即c(OH-)c(Na+),选项C正确;
D.图2中A点表示HAuCl 与NaAuCl 浓度相等,由分析知图1中b点与之对应,c( )>c(Na+),溶液
4 4
中存在2c(Na+)b>a
C.c点,滴入NaOH溶液的体积为10mL
D.
【答案】AD
【分析】
从图中可以看出,随着pH的增大,ac段离子浓度减少,为 ,cb段离子浓度增大,为 ,ab段离子
浓度先增大后减少,为 。
【解析】
A.a、b点所在曲线对应的粒子为 ,故A正确;
B.c点时 浓度最大,既存在 的电离,也存在 的水解;b点时主要是水的电离,且pH比C点
大,水的电离程度大,水电离出的氢离子浓度大小关系为 ,故B错误;
C.c点时 浓度最大,说明 与NaOH刚好1:1反应完全,因浓度相等,此时加入NaOH体积为
20mL,故C错误;
D.由图, 的一级电离常数为 ,由a点数据可知 ,pH=1,即,解得 ;二级电离常数为 ,同理由c点数据可得
, = = ,故D正确;
故选AD。
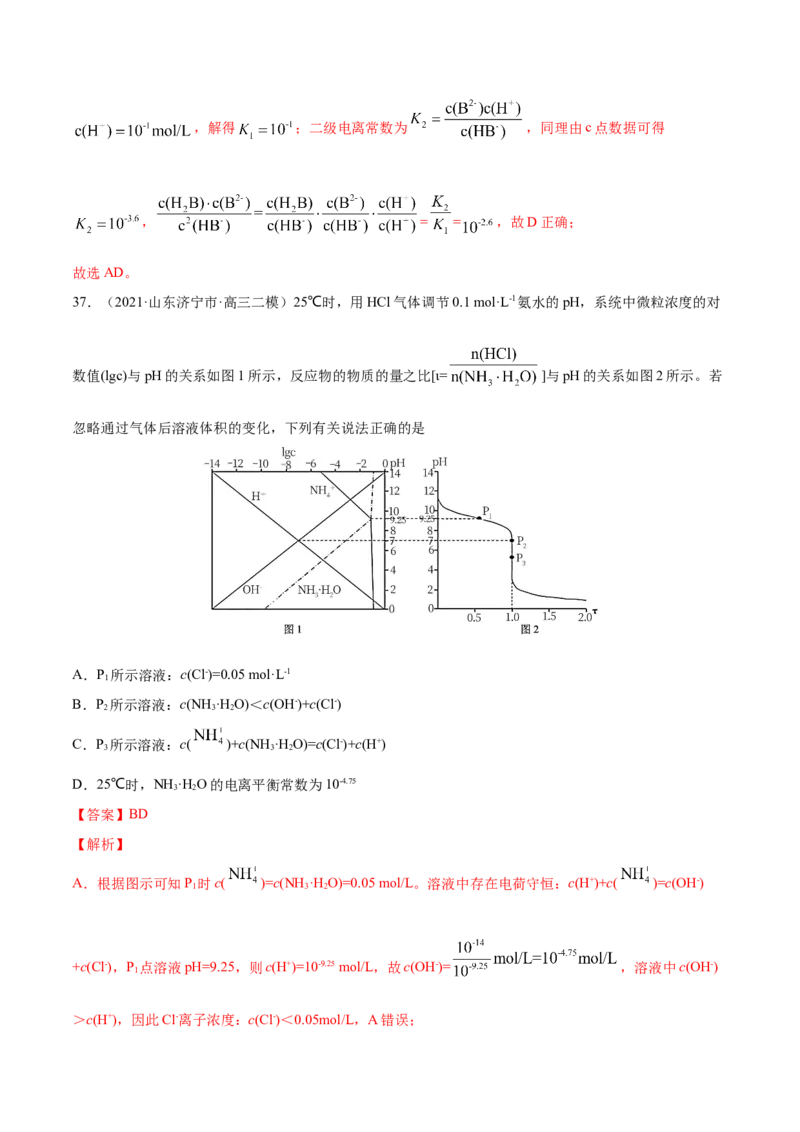
37.(2021·山东济宁市·高三二模)25℃时,用HCl气体调节0.1 mol·L-1氨水的pH,系统中微粒浓度的对
数值(lgc)与pH的关系如图1所示,反应物的物质的量之比[ι= ]与pH的关系如图2所示。若
忽略通过气体后溶液体积的变化,下列有关说法正确的是
A.P 所示溶液:c(Cl-)=0.05 mol·L-1
1
B.P 所示溶液:c(NH ·H O)<c(OH-)+c(Cl-)
2 3 2
C.P 所示溶液:c( )+c(NH ·H O)=c(Cl-)+c(H+)
3 3 2
D.25℃时,NH ·H O的电离平衡常数为10-4.75
3 2
【答案】BD
【解析】
A.根据图示可知P 时c( )=c(NH ·H O)=0.05 mol/L。溶液中存在电荷守恒:c(H+)+c( )=c(OH-)
1 3 2
+c(Cl-),P 点溶液pH=9.25,则c(H+)=10-9.25 mol/L,故c(OH-)= ,溶液中c(OH-)
1
>c(H+),因此Cl-离子浓度:c(Cl-)<0.05mol/L,A错误;B.根据电荷守恒c(H+)+c( )=c(OH-)+c(Cl-),根据图示可知P 时c( )>c(NH ·H O),c(H+)+c(
2 3 2
)>c(NH ·H O),所以c(NH ·H O)<c(OH-)+c(Cl-),B正确;
3 2 3 2
C.根据图示可知P 时t= ,溶液的溶质为NH Cl,根据物料守恒可得c(Cl-)=c( )
3 4
+c(NH ·H O)=0.1 mol/L,所以c( )+c(NH ·H O)<c(Cl-)+ c(H+),C错误;
3 2 3 2
D.25℃时,NH ·H O的电离平衡常数为K= ,当溶液中c( )=c(NH ·H O)时,
3 2 3 2
= ,D正确;
故合理选项是BD。
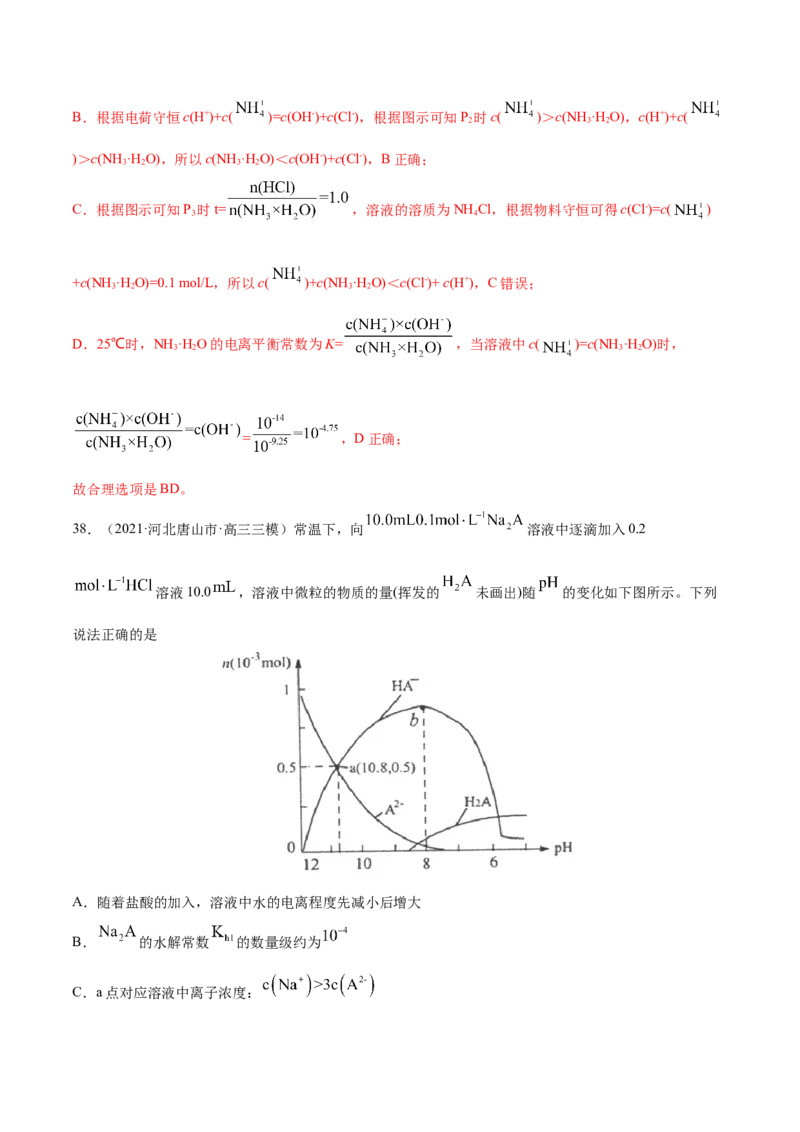
38.(2021·河北唐山市·高三三模)常温下,向 溶液中逐滴加入0.2
溶液10.0 ,溶液中微粒的物质的量(挥发的 未画出)随 的变化如下图所示。下列
说法正确的是
A.随着盐酸的加入,溶液中水的电离程度先减小后增大
B. 的水解常数 的数量级约为
C.a点对应溶液中离子浓度:D.b点对应溶液中:
【答案】BC
【解析】
A. 未加入盐酸时,溶液中只有NaA溶质,因为水解而促进水的电离,随着盐酸的加入,水解程度减小,
2
促进作用减小,故水的电离程度也减小,若盐酸过量,则由于盐酸电离出的H+而抑制水的电离,故随着盐
酸的加入,溶液中水的电离程度一直减小至不变,但不会增大,A错误;
B. 的水解反应为:A2-+H O HA-+OH-,故水解常数 = ,由图可知,当
2
c(HA-)=c(A2-)时,pH=10.8,故水解常数 = ,故 的数量级约为
,B正确;
C. 由电荷守恒可知,c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),又a点对应溶液中c(HA-)=c(A2-),pH=10.8故离
子浓度c(Na+)=3c(A2-)+c(OH-)-c(H+),故 ,C正确;
D. 由图中可知,b点对应溶液实质时NaHA溶液,由电荷守恒: c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),物
料守恒:c(Na+)=c(A2-)+c(HA-)+c(H A)可知 ,D错误;
2
故答案为:BC。
39.(2021·河北邯郸市·高三三模)室温下实验室用 的氢氧化钠溶液滴定
醋酸溶液,滴定曲线如图所示(设 )。下列有关叙述正确的是A.该条件下,醋酸的电离度(已电离的醋酸分子数与原醋酸分子数的比)约为1%
B.y点处加入的NaOH溶液体积小于
C.x→y→z的过程中,水的电离程度逐渐增大
D.y→z的曲线上任意一点,始终存在
【答案】AB
【解析】
A.由x点I为6可知,溶液中c(H+)= mol/L=1×10—4 mol/L,则醋酸的电离度约为
,故A正确:
B.当20mL0.01mol/L醋酸溶液与20mL0.01mol/L氢氧化钠溶液恰好完全反应得到醋酸钠溶液,溶液呈碱
性,由y点I为6可知,溶液中c(H+)=c(OH—),溶液呈中性,中性溶液为醋酸钠和醋酸的混合溶液,则反
应的氢氧化钠溶液体积小于20mL,故B正确;
C.由图可知,x点为醋酸溶液,溶液中氢离子抑制水的电离,完全反应点在y点后,得到的是醋酸钠溶液,
溶液中醋酸根离子水解促进水的电离,完全反应点→z点时,得到的是醋酸钠和氢氧化钠混合溶液,氢氧
化钠溶液浓度增大,水的电离程度减小,则x→y→z的过程中,水的电离程度先增大后减小,故C错误;
D.当20mL0.01mol/L醋酸溶液与20mL0.01mol/L氢氧化钠溶液恰好完全反应得到醋酸钠溶液时,溶液中
存在质子守恒关系 ,当氢氧化钠溶液不足或过量时,混合溶液中
的关系不成立,故D错误;故选AB。
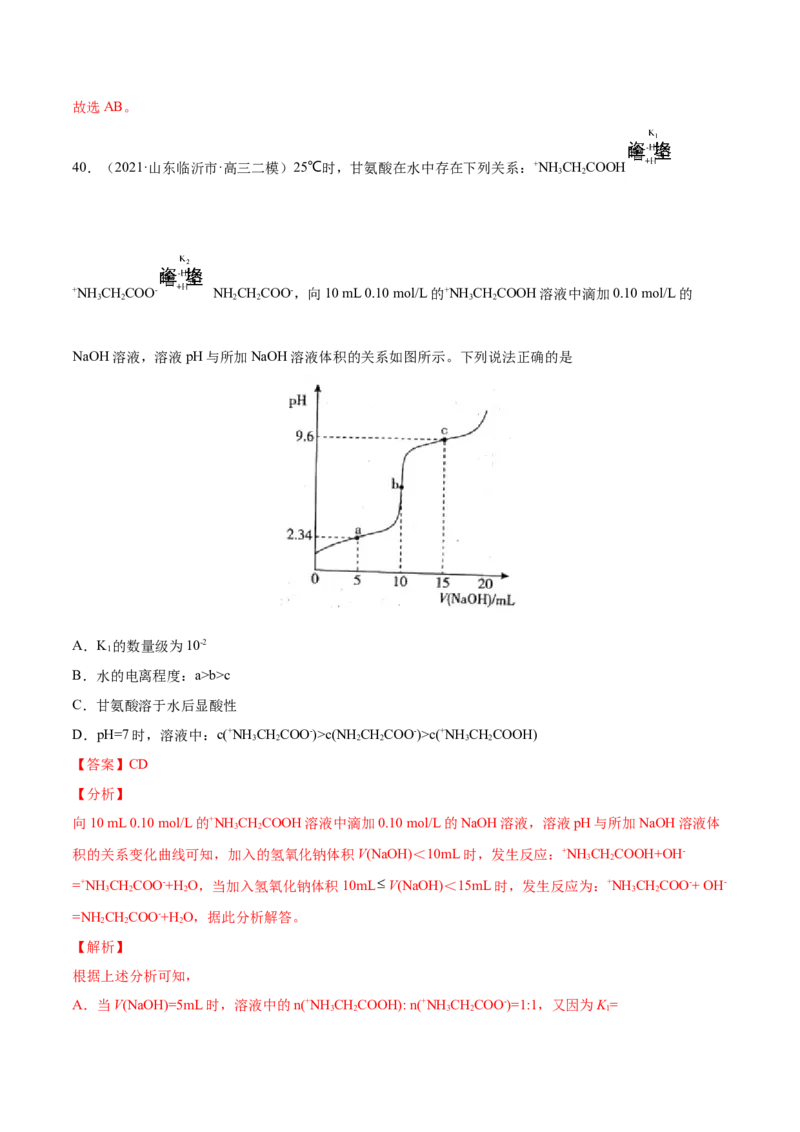
40.(2021·山东临沂市·高三二模)25℃时,甘氨酸在水中存在下列关系:+NH CHCOOH
3 2
+NH CHCOO- NH CHCOO-,向10 mL 0.10 mol/L的+NH CHCOOH溶液中滴加0.10 mol/L的
3 2 2 2 3 2
NaOH溶液,溶液pH与所加NaOH溶液体积的关系如图所示。下列说法正确的是
A.K 的数量级为10-2
1
B.水的电离程度:a>b>c
C.甘氨酸溶于水后显酸性
D.pH=7时,溶液中:c(+NH CHCOO-)>c(NHCHCOO-)>c(+NH CHCOOH)
3 2 2 2 3 2
【答案】CD
【分析】
向10 mL 0.10 mol/L的+NH CHCOOH溶液中滴加0.10 mol/L的NaOH溶液,溶液pH与所加NaOH溶液体
3 2
积的关系变化曲线可知,加入的氢氧化钠体积V(NaOH)<10mL时,发生反应:+NH CHCOOH+OH-
3 2
=+NH CHCOO-+H O,当加入氢氧化钠体积10mL V(NaOH)<15mL时,发生反应为:+NH CHCOO-+ OH-
3 2 2 3 2
=NHCHCOO-+H O,据此分析解答。
2 2 2
【解析】
根据上述分析可知,
A.当V(NaOH)=5mL时,溶液中的n(+NH CHCOOH): n(+NH CHCOO-)=1:1,又因为K =
3 2 3 2 1,所以此时K =c(H+)=10-2.34,其数量级为10-3,A错误;
1
B.根据曲线分析可知,a b的过程中,氢氧化钠中和+NH CHCOOH电离的氢离子,水的电离程度被抑
3 2
制作用减弱,所以水的电离程度增强,即b>a,b点溶质为+NH CHCOONa,c点为等物质的量的
3 2
+NH CHCOONa和NH CHCOONa,因为NH CHCOO-的水解程度大于+NH CHCOO-的,所以水的电离程
3 2 2 2 2 2 3 2
度:c>b,综上所述,水的电离程度:c>b>a,B错误;
C.当V(NaOH)=0mL时,溶液的pH<2.34,则说明甘氨酸溶于水显酸性,C正确;
D.曲线上c点时,n(+NH CHCOO-)=n(NH CHCOO-),K = = c(H+)=10-9.6,而
3 2 2 2 2
+NH CHCOO-的水解常数K = <K ,说明+NH CHCOO-的电离程度大于
3 2 h 2 3 2
+NH CHCOO-的水解程度,又+NH CHCOO-与氢氧化钠恰好反应时溶液呈酸性,所以当pH=7时,氢氧化
3 2 3 2
钠超过了10mL,已和+NH CHCOO-反应生成了NH CHCOO-,则溶液中离子浓度的大小关系为:
3 2 2 2
c(+NH CHCOO-)>c(NHCHCOO-)>c(+NH CHCOOH),D正确;
3 2 2 2 3 2
故选CD。
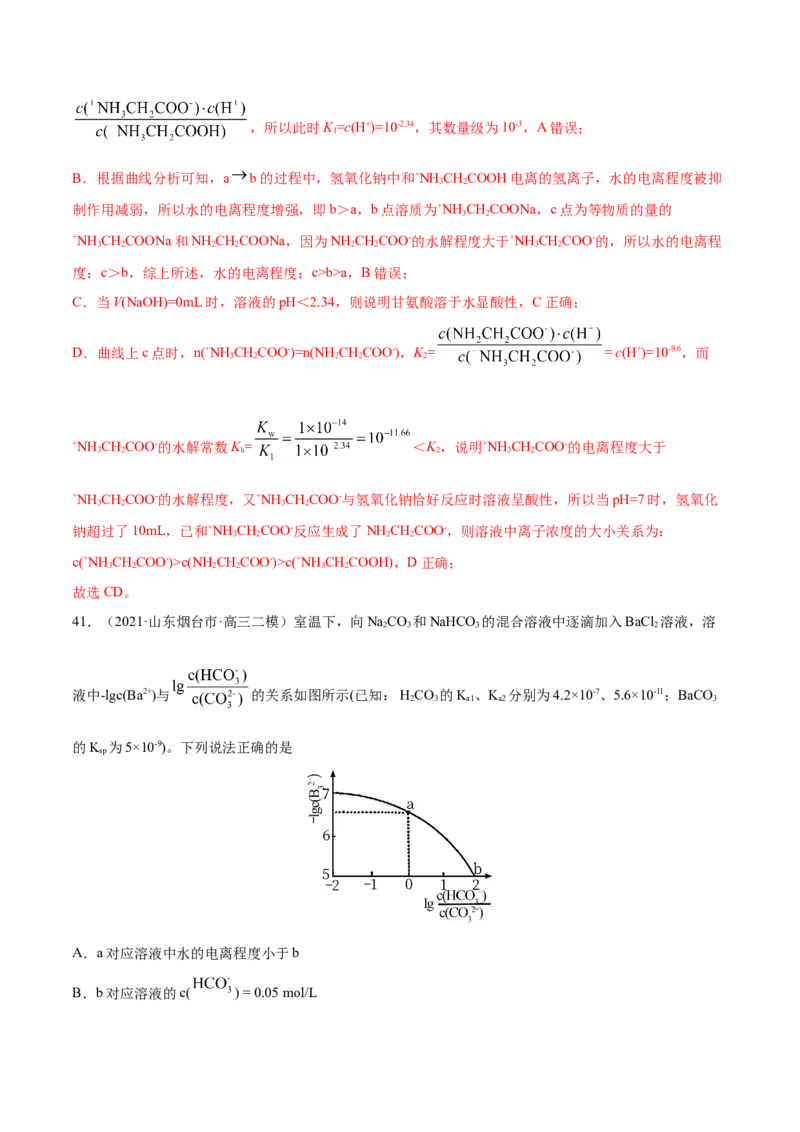
41.(2021·山东烟台市·高三二模)室温下,向NaCO 和NaHCO 的混合溶液中逐滴加入BaCl 溶液,溶
2 3 3 2
液中-lgc(Ba2+)与 的关系如图所示(已知: HCO 的K 、K 分别为4.2×10-7、5.6×10-11;BaCO
2 3 a1 a2 3
的K 为5×10-9)。下列说法正确的是
sp
A.a对应溶液中水的电离程度小于b
B.b对应溶液的c( ) = 0.05 mol/LC.a→b的过程中,溶液中 一直减小
D.a对应的溶液中一定存在:c(Na+)+2c(Ba2+) <3c( )+c(Cl-)
【答案】BC
【解析】
A.由a到b时,Ba2+持续增大,BaCO 的K 不变,所以 浓度持续减小,因为 会水解促进水
3 sp
的电离,所以该过程水的电离程度持续减小,则a对应溶液中水的电离程度大于b,A错误;
B.b点时,c( ) = 102 且c(Ba2+)=10-5mol/L,BaCO 的K 为5×10-9= c(Ba2+)× ,所以
3 sp
此时 =5×10-4mol/L,则c( ) = 102 =0.05mol/L,B正确;
C.a→b的过程中,由a到b时,Ba2+持续增大,BaCO 的K 不变,所以 浓度持续减小,碳酸根
3 sp
水解呈碱性,所以溶液碱性会变弱,导致 增大,溶液中 =
,K 、K 不改变, 增大,所以 一直减小,
a1 a2
即 一直减小,C正确;
D.a对应的溶液中c( ) = ,溶液电荷守恒为:c(Na+)+2c(Ba2+)+ =2 +c(
)+c(Cl-)+ ,所以此时有:c(Na+)+2c(Ba2+)+ =3c( )+c(Cl-)+ ,碳酸钠和碳酸氢
钠混合溶液显碱性,则 ,所以:c(Na+)+2c(Ba2+) >3c( )+c(Cl-),D错误;
答案选BC。