文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题11 化学实验(选择题)
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
实验原理、实验技能和实验仪器是实验的三要素,在高考中常将“ 三要素”进行组合,形成综合性
强、能力层次要求高的实验题。
综合性化学实验题(选择题)考查内容全面,从定性分析到定量分析、从化学原理到实际操作、从无
机物到有机物都有涉及,主要考查:
(1)气体物质的制备方法;
(2)物质的净化、除杂、检验;
(3)物质性质的验证;
(4)化学常见仪器的使用;
(5)试剂的选择与操作;
(6)实验方案的设计与评价等内容;
(7)产率的计算;
预计2025年高考综合实验选择题,将结合文字叙述、图表数据、实验装置,探究内容上主要取材于教
材实验、日常生活和社会热点问题等,考察物质的制备、检验、鉴别等。
1.(2024·江西·高考真题)“稀土之父”徐光宪先生提出了稀土串级萃取理论,其基本操作是利用有机络
合剂把稀土离子从水相富集到有机相再进行分离。分离时可用的玻璃装置是
A. B. C. D.
2.(2023·西藏四川·高考真题)实验室将粗盐提纯并配制 的 溶液。下列仪器中,本实
验必须用到的有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥ B.①④⑤⑥ C.②③⑦⑧ D.①⑤⑥⑧
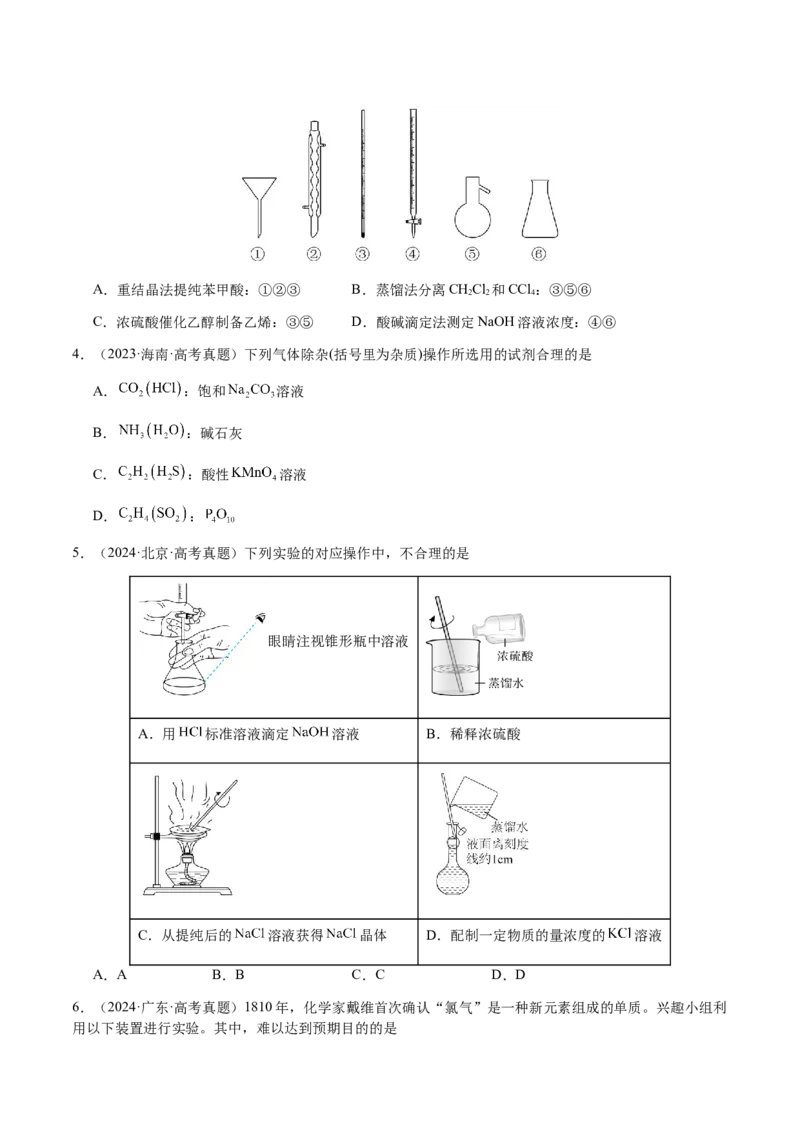
3.(2023·湖南·高考真题)下列玻璃仪器在相应实验中选用不合理的是A.重结晶法提纯苯甲酸:①②③ B.蒸馏法分离CHCl 和CCl :③⑤⑥
2 2 4
C.浓硫酸催化乙醇制备乙烯:③⑤ D.酸碱滴定法测定NaOH溶液浓度:④⑥
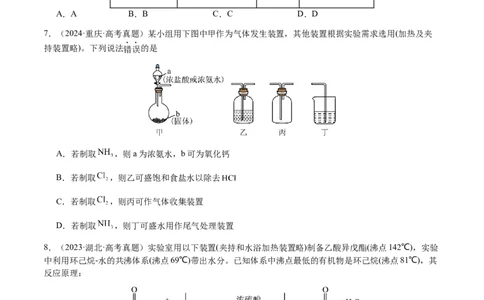
4.(2023·海南·高考真题)下列气体除杂(括号里为杂质)操作所选用的试剂合理的是
A. :饱和 溶液
B. :碱石灰
C. :酸性 溶液
D. :
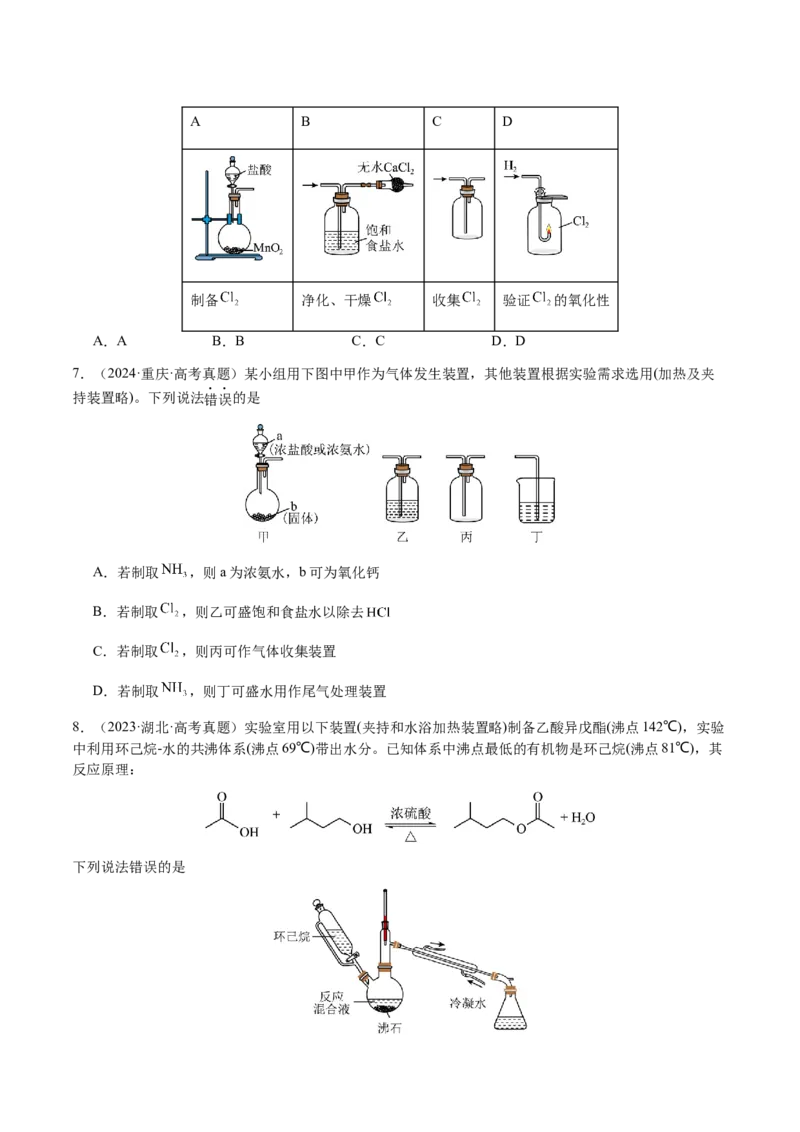
5.(2024·北京·高考真题)下列实验的对应操作中,不合理的是
眼睛注视锥形瓶中溶液
A.用 标准溶液滴定 溶液 B.稀释浓硫酸
C.从提纯后的 溶液获得 晶体 D.配制一定物质的量浓度的 溶液
A.A B.B C.C D.D
6.(2024·广东·高考真题)1810年,化学家戴维首次确认“氯气”是一种新元素组成的单质。兴趣小组利
用以下装置进行实验。其中,难以达到预期目的的是A B C D
制备 净化、干燥 收集 验证 的氧化性
A.A B.B C.C D.D
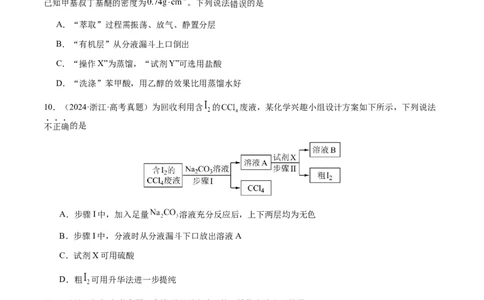
7.(2024·重庆·高考真题)某小组用下图中甲作为气体发生装置,其他装置根据实验需求选用(加热及夹
持装置略)。下列说法错误的是
A.若制取 ,则a为浓氨水,b可为氧化钙
B.若制取 ,则乙可盛饱和食盐水以除去
C.若制取 ,则丙可作气体收集装置
D.若制取 ,则丁可盛水用作尾气处理装置
8.(2023·湖北·高考真题)实验室用以下装置(夹持和水浴加热装置略)制备乙酸异戊酯(沸点142℃),实验
中利用环己烷-水的共沸体系(沸点69℃)带出水分。已知体系中沸点最低的有机物是环己烷(沸点81℃),其
反应原理:
下列说法错误的是A.以共沸体系带水促使反应正向进行 B.反应时水浴温度需严格控制在69℃
C.接收瓶中会出现分层现象 D.根据带出水的体积可估算反应进度
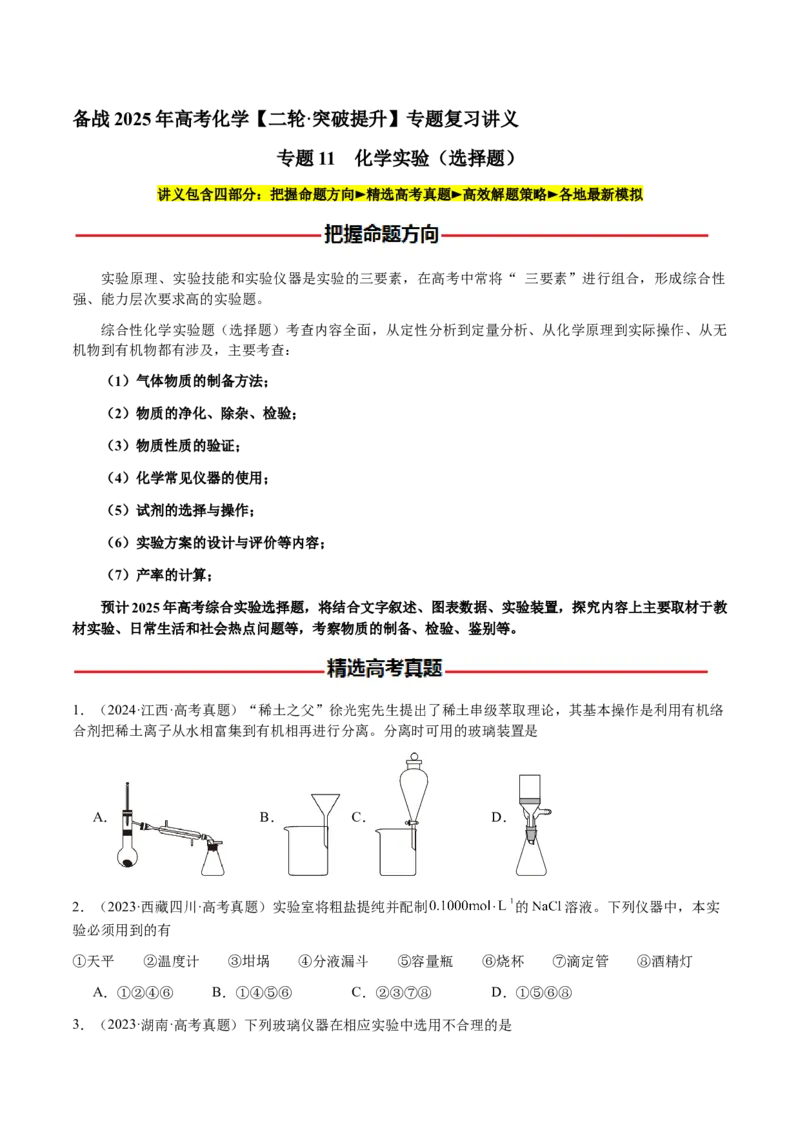
9.(2023·福建·高考真题)从苯甲醛和 溶液反应后的混合液中分离出苯甲醇和苯甲酸的过程如下:
已知甲基叔丁基醚的密度为 。下列说法错误的是
A.“萃取”过程需振荡、放气、静置分层
B.“有机层”从分液漏斗上口倒出
C.“操作X”为蒸馏,“试剂Y”可选用盐酸
D.“洗涤”苯甲酸,用乙醇的效果比用蒸馏水好
10.(2024·浙江·高考真题)为回收利用含 的 废液,某化学兴趣小组设计方案如下所示,下列说法
不正确的是
A.步骤I中,加入足量 溶液充分反应后,上下两层均为无色
B.步骤I中,分液时从分液漏斗下口放出溶液A
C.试剂X可用硫酸
D.粗 可用升华法进一步提纯
11.(2024·湖南·高考真题)为达到下列实验目的,操作方法合理的是
实验目的 操作方法
A 从含有 的NaCl固体中提取 用CCl 溶解、萃取、分液
4
B 提纯实验室制备的乙酸乙酯 依次用 溶液洗涤、水洗、分液、干燥
C 用 标准溶液滴定未知浓度的 溶液 用甲基橙作指示剂进行滴定D 从明矾过饱和溶液中快速析出晶体 用玻璃棒摩擦烧杯内壁
A.A B.B C.C D.D
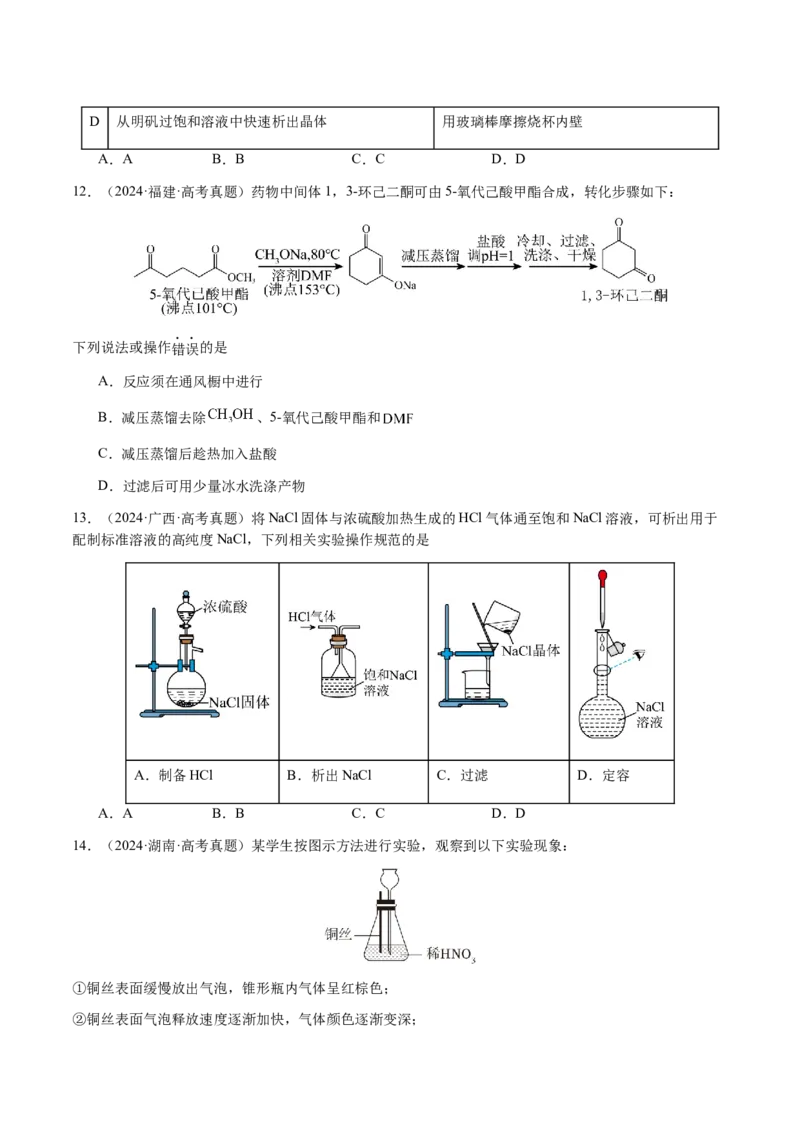
12.(2024·福建·高考真题)药物中间体1,3-环己二酮可由5-氧代己酸甲酯合成,转化步骤如下:
下列说法或操作错误的是
A.反应须在通风橱中进行
B.减压蒸馏去除 、5-氧代己酸甲酯和
C.减压蒸馏后趁热加入盐酸
D.过滤后可用少量冰水洗涤产物
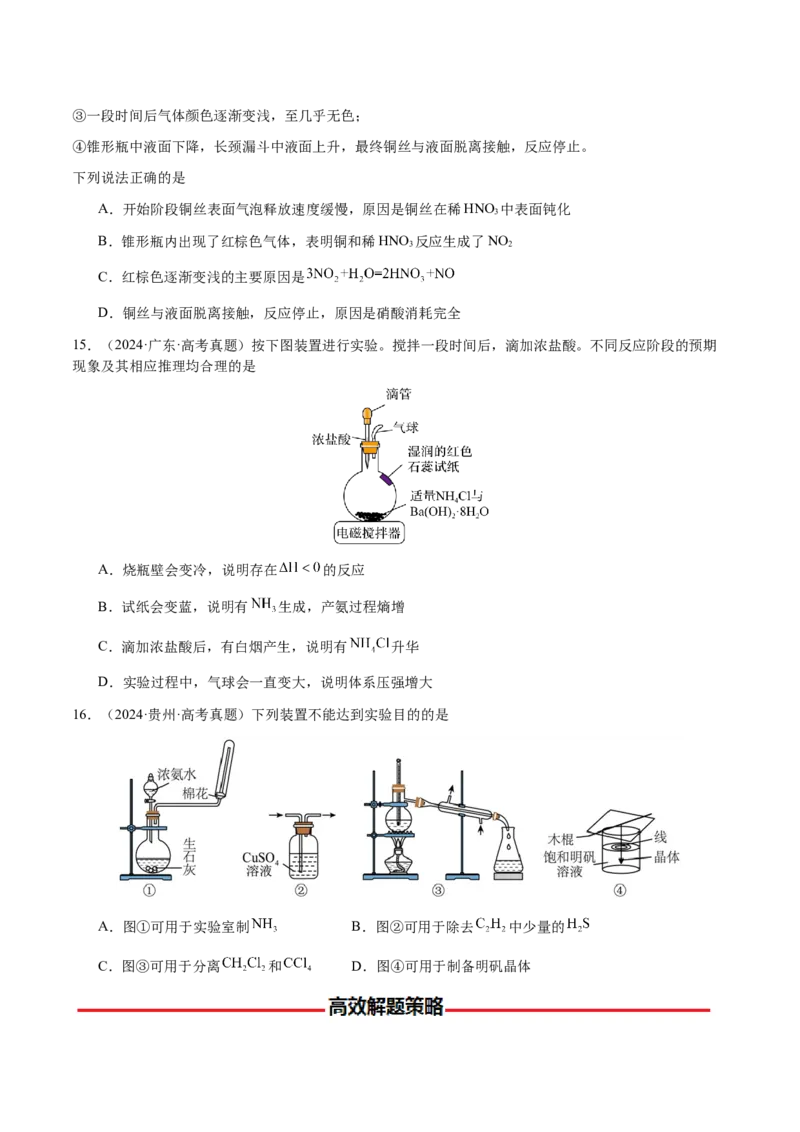
13.(2024·广西·高考真题)将NaCl固体与浓硫酸加热生成的HCl气体通至饱和NaCl溶液,可析出用于
配制标准溶液的高纯度NaCl,下列相关实验操作规范的是
A.制备HCl B.析出NaCl C.过滤 D.定容
A.A B.B C.C D.D
14.(2024·湖南·高考真题)某学生按图示方法进行实验,观察到以下实验现象:
①铜丝表面缓慢放出气泡,锥形瓶内气体呈红棕色;
②铜丝表面气泡释放速度逐渐加快,气体颜色逐渐变深;③一段时间后气体颜色逐渐变浅,至几乎无色;
④锥形瓶中液面下降,长颈漏斗中液面上升,最终铜丝与液面脱离接触,反应停止。
下列说法正确的是
A.开始阶段铜丝表面气泡释放速度缓慢,原因是铜丝在稀HNO 中表面钝化
3
B.锥形瓶内出现了红棕色气体,表明铜和稀HNO 反应生成了NO
3 2
C.红棕色逐渐变浅的主要原因是
D.铜丝与液面脱离接触,反应停止,原因是硝酸消耗完全
15.(2024·广东·高考真题)按下图装置进行实验。搅拌一段时间后,滴加浓盐酸。不同反应阶段的预期
现象及其相应推理均合理的是
A.烧瓶壁会变冷,说明存在 的反应
B.试纸会变蓝,说明有 生成,产氨过程熵增
C.滴加浓盐酸后,有白烟产生,说明有 升华
D.实验过程中,气球会一直变大,说明体系压强增大
16.(2024·贵州·高考真题)下列装置不能达到实验目的的是
A.图①可用于实验室制 B.图②可用于除去 中少量的
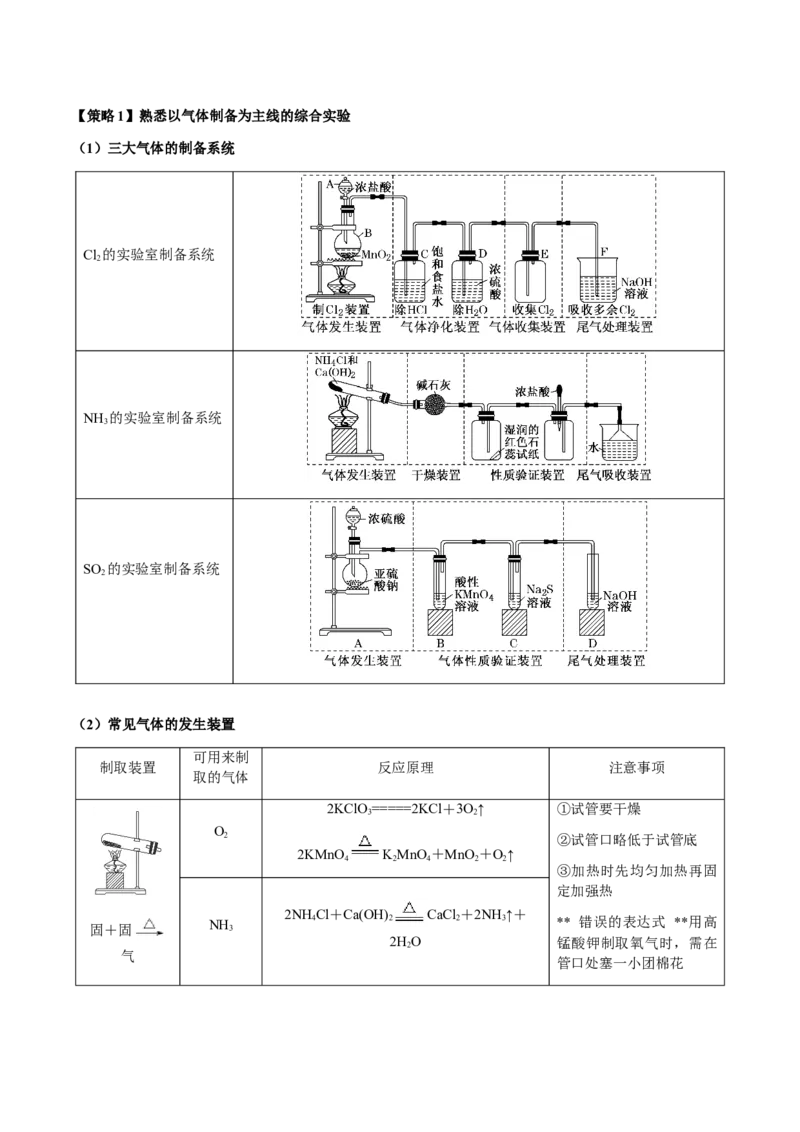
C.图③可用于分离 和 D.图④可用于制备明矾晶体【策略1】熟悉以气体制备为主线的综合实验
(1)三大气体的制备系统
Cl 的实验室制备系统
2
NH 的实验室制备系统
3
SO 的实验室制备系统
2
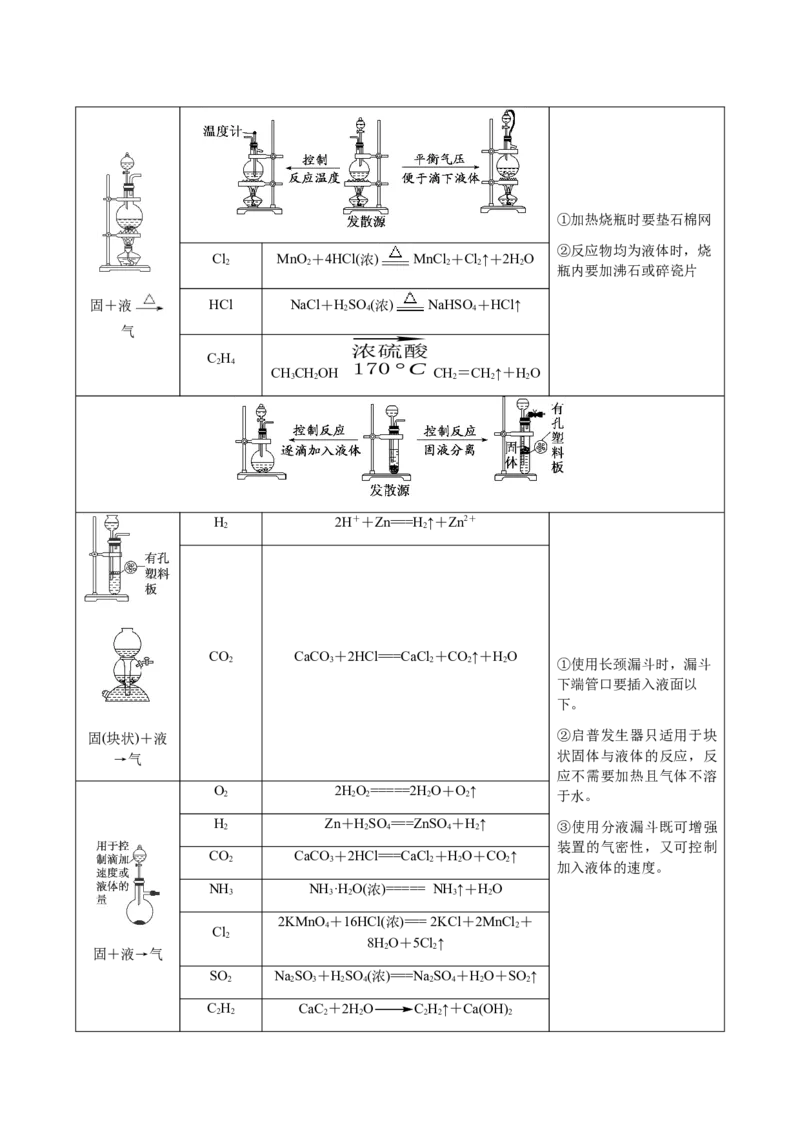
(2)常见气体的发生装置
可用来制
制取装置 反应原理 注意事项
取的气体
2KClO=====2KCl+3O↑ ①试管要干燥
3 2
O
2 ②试管口略低于试管底
2KMnO KMnO +MnO +O↑
4 2 4 2 2
③加热时先均匀加热再固
定加强热
2NH Cl+Ca(OH) CaCl +2NH ↑+
NH 4 2 2 3 ** 错误的表达式 **用高
固+固 3
2HO 锰酸钾制取氧气时,需在
2
气
管口处塞一小团棉花①加热烧瓶时要垫石棉网
②反应物均为液体时,烧
Cl MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2 2
瓶内要加沸石或碎瓷片
固+液 HCl NaCl+HSO (浓) NaHSO+HCl↑
2 4 4
气
⃗
浓硫酸
C H
2 4 170°C
CHCHOH CH=CH↑+HO
3 2 2 2 2
H 2H++Zn===H ↑+Zn2+
2 2
CO CaCO +2HCl===CaCl +CO↑+HO
2 3 2 2 2 ①使用长颈漏斗时,漏斗
下端管口要插入液面以
下。
固(块状)+液 ②启普发生器只适用于块
→气 状固体与液体的反应,反
应不需要加热且气体不溶
O 2HO=====2HO+O↑
2 2 2 2 2 于水。
H 2 Zn+H 2 SO 4 ===ZnSO 4 +H 2 ↑ ③使用分液漏斗既可增强
装置的气密性,又可控制
CO CaCO +2HCl===CaCl +HO+CO↑
2 3 2 2 2
加入液体的速度。
NH NH ·H O(浓)===== NH ↑+HO
3 3 2 3 2
2KMnO +16HCl(浓)=== 2KCl+2MnCl +
4 2
Cl
2
8HO+5Cl↑
2 2
固+液→气
SO NaSO +HSO (浓)===Na SO +HO+SO ↑
2 2 3 2 4 2 4 2 2
C H CaC +2HO C H↑+Ca(OH)
2 2 2 2 2 2 23Cu+8HNO(稀)===3Cu(NO)+2NO↑+
NO 3 3 2
4HO
2
NO Cu+4HNO(浓)===Cu(NO)+2NO ↑+2HO
2 3 3 2 2 2
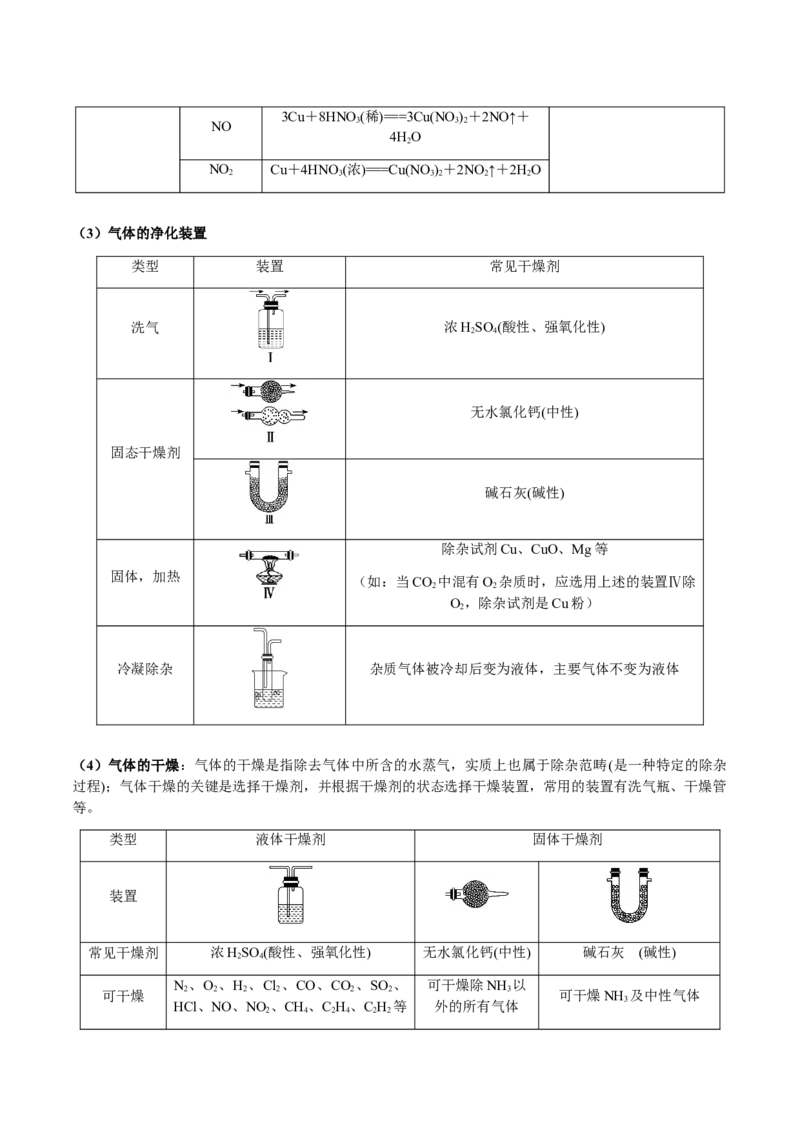
(3)气体的净化装置
类型 装置 常见干燥剂
洗气 浓HSO (酸性、强氧化性)
2 4
无水氯化钙(中性)
固态干燥剂
碱石灰(碱性)
除杂试剂Cu、CuO、Mg等
固体,加热
(如:当CO 中混有O 杂质时,应选用上述的装置Ⅳ除
2 2
O,除杂试剂是Cu粉)
2
冷凝除杂 杂质气体被冷却后变为液体,主要气体不变为液体
(4)气体的干燥:气体的干燥是指除去气体中所含的水蒸气,实质上也属于除杂范畴(是一种特定的除杂
过程);气体干燥的关键是选择干燥剂,并根据干燥剂的状态选择干燥装置,常用的装置有洗气瓶、干燥管
等。
类型 液体干燥剂 固体干燥剂
装置
常见干燥剂 浓HSO (酸性、强氧化性) 无水氯化钙(中性) 碱石灰 (碱性)
2 4
N 、O 、H 、Cl 、CO、CO 、SO 、 可干燥除NH 以
可干燥 2 2 2 2 2 2 3 可干燥NH 及中性气体
HCl、NO、NO 、CH、C H、C H 等 外的所有气体 3
2 4 2 4 2 2的气体
不可干燥
Cl、HS、HCl、SO 、CO
NH 、HS、HBr、HI等 NH 2 2 2 2
3 2 3
等
的气体
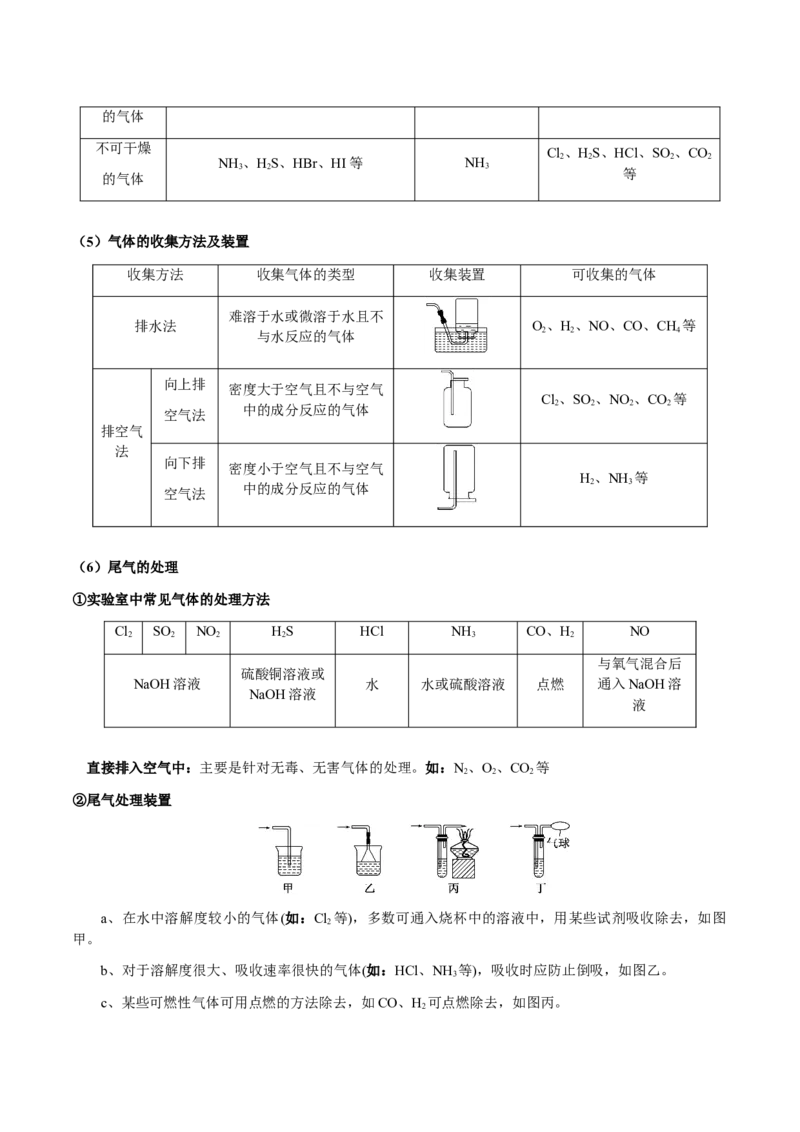
(5)气体的收集方法及装置
收集方法 收集气体的类型 收集装置 可收集的气体
难溶于水或微溶于水且不
排水法 O、H、NO、CO、CH 等
与水反应的气体 2 2 4
向上排
密度大于空气且不与空气
Cl、SO 、NO 、CO 等
中的成分反应的气体 2 2 2 2
空气法
排空气
法
向下排
密度小于空气且不与空气
H、NH 等
中的成分反应的气体 2 3
空气法
(6)尾气的处理
①实验室中常见气体的处理方法
Cl SO NO HS HCl NH CO、H NO
2 2 2 2 3 2
与氧气混合后
硫酸铜溶液或
NaOH溶液 水 水或硫酸溶液 点燃 通入NaOH溶
NaOH溶液
液
直接排入空气中:主要是针对无毒、无害气体的处理。如:N、O、CO 等
2 2 2
②尾气处理装置
a、在水中溶解度较小的气体(如:Cl 等),多数可通入烧杯中的溶液中,用某些试剂吸收除去,如图
2
甲。
b、对于溶解度很大、吸收速率很快的气体(如:HCl、NH 等),吸收时应防止倒吸,如图乙。
3
c、某些可燃性气体可用点燃的方法除去,如CO、H 可点燃除去,如图丙。
2d、尾气也可以采用收集的方法处理,如CH、C H、H、CO等,如图丁。
4 2 4 2
(7)实验条件的控制
为了防止空气中的成分氧气、CO 、水蒸气干扰实验,常用其他稳定的气体(如氮气)排尽
2
排气方法 装置中的空气;有时也可充分利用反应产物气体(如:氨气、氯气、二氧化硫)等排尽装置
中的空气。
①用分液漏斗控制液体滴加的速度和用量。
②观察气泡,控制气流速度,如图 ,可观察气泡得到N 、H 的体
2 2
控制气体的流
速及用量 积比约为1∶3的混合气。
③平衡气压如图 ,用长玻璃管平衡气压,防堵塞。
根据装置的密封性,让反应生成气体或消耗气体,产生压强差,将液体压入或倒流入另
一反应容器。
压送液体
①控制低温的目的:减少某些反应物或产品分解如HO 、NH HCO 等;减少某些反应物
2 2 4 3
或产品挥发,如盐酸、氨水等;防止某物质水解,避免副反应发生等。
②采取加热的目的:加快反应速率或使平衡移动,加速溶解等。
③常考温度控制方式:
温度控制 a.水浴加热:均匀加热,反应温度100 ℃以下。
b.油浴加热:均匀加热,反应温度100~260 ℃。
c.冰水冷却:使某物质液化、降低产物的溶解度;减少其他副反应,提高产品纯度
等。
d.保温:如中和反应反应热测定时,两烧杯之间填泡沫,真空双层玻璃容器等。
(8)有关沉淀的洗涤操作与规范解答
(1)若滤渣是所需的物质,洗涤的目的是除去其表面的可溶性杂质,得到更纯净的
沉淀物。
洗涤沉淀的目的
(2)若滤液是所需的物质,洗涤的目的是洗涤过滤所得到的滤渣,把有用的物质如
目标产物尽可能洗出来。(1)蒸馏水:主要适用于除去沉淀吸附的可溶性杂质。
(2)冷水:除去沉淀表面的可溶性杂质,降低沉淀在水中的溶解度而减少沉淀损
失。
常用洗涤剂
(3)沉淀的饱和溶液:减小沉淀的溶解。
(4)有机溶剂(酒精、乙醚等):适用于易溶于水的固体,既减少了固体溶解,又利
用有机溶剂的挥发性,除去固体表面的水分,产品易干燥。
(1)检验沉淀是否完全的答题模板:
静置,取上层清液→加沉淀剂→有无沉淀→结论
(2)沉淀洗涤的答题模板:
三套答题模板 注洗涤液(沿玻璃棒向漏斗中注入洗涤液)→标准(使洗涤液完全浸没沉淀或晶
体)→重复(待洗涤液流尽后,重复操作2~3次)
(3)检验沉淀是否洗净的答题模板:
取样(取少量最后一次洗涤液于一洁净的试管中)→加试剂[加入××试剂(必要时加
热,如检验NH)]→现象(不产生××沉淀、溶液不变××色或不产生××气体)→结论(说明
沉淀已经洗涤干净)
【策略2】掌握有机物制备的实验装置和提纯方法
(1)熟悉常用仪器
(2)熟悉常用装置
①反应装置:有机物易挥发,常采用冷凝回流装置减少有机物的挥发,提高原料的利用率和产物的产
率。
②蒸馏装置:利用有机物沸点的不同,用蒸馏的方法可以实现分离。(3)有机物制备常考问题:
若要控制反应温度,温度计的水银球应插入反应液中;
温度计水银球
若要选择收集某温度下的馏分,则温度计的水银球应放在蒸馏烧瓶支管口附
的位置
近。
有机化合物易挥发,因此在反应中通常要采用冷凝回流装置,以减少有机化合
物的挥发,提高原料的利用率和产物的产率。如图1、图3中的冷凝管,图2中
的长玻璃管B的作用都是冷凝回流。
冷凝回流
球形冷凝管只能用于冷凝回流,直形冷凝管既能用于冷凝回流,又能用于冷凝
冷凝管的选择
收集馏分。
冷凝管的进出
下口进上口出
水方向
酒精灯的火焰温度一般在400~500 ℃,所以需要温度不太高的实验都可用酒精
灯加热,例如乙酸乙酯的制取、石油的蒸馏等实验等。若温度要求更高,可选
加热方法的选
用酒精喷灯或电炉加热。
择
除上述加热方式外还可以根据加热的温度要求选择水浴、油浴、沙浴加热,水
浴加热的温度不超过100 ℃
防暴沸 加沸石或碎瓷片,防止溶液暴沸,若开始忘加沸石,需冷却后补加。
常见的用于干
燥有机物的药 无水氯化钙、无水硫酸镁、无水硫酸钙、无水碳酸钾等;
品
(4)提纯有机物的常用步骤及方法
有机制备实验有反应物转化率低、副反应多等特点,制得的产物中常混有杂质(无机物与有机物),根
据目标产物与杂质的性质差异,可用如下方法分离提纯:如苯与液溴发生取代反应后,产物为棕褐色,混合物中含有目标产物溴苯、有机杂质苯、无机杂质
Br 、FeBr 、HBr等,提纯溴苯可用如下工艺流程:
2 3
提纯有机物的常用方法:
①分液:用于分离两种互不相溶(密度也不同)的液体。
②蒸馏:用于分离沸点不同的液体。分馏的原理与此相同。
③洗气:用于除去气体混合物中的杂质,如乙烷中的乙烯可通过溴水洗气除去。
④萃取分液:如分离溴水中的溴和水,可用四氯化碳或苯进行萃取,然后分液。
(5)有机物产率计算公式
产品产率=×100%;
【策略3】明确性质探究类综合实验的角度(1)物质氧化性、还原性及其强弱的判断。
如探究SO 具有还原性的方法是将气体通入酸性 KMnO 溶液中,通过观察酸性KMnO 溶液是否褪色
2 4 4
来说明;如探究Fe3+的氧化性强于I 时,可利用FeCl 与淀粉KI溶液反应,通过溶液变蓝色来说明Fe3+的
2 3
氧化性强于I。
2
(2)验证同周期、同主族元素性质的递变规律.
一般通过设计比较元素金属性、非金属性强弱的实验来完成。如通过比较Mg、Al与同浓度盐酸反应
产生H 的快慢来说明Mg、Al的活泼性顺序。
2
(3)电解质强弱的判断。
如探究化合物HA是弱电解质的方法是常温下配制NaA溶液,测pH,若pH>7,则说明HA为弱电解
质。
(4)物质酸性强弱的判断。
如探究碳酸和硅酸的酸性强弱,可利用相对强的酸制备相对弱的酸的反应原理,将 CO 气体通入
2
NaSiO 溶液,看是否有白色沉淀生成来判断。
2 3
(5)钢铁发生电化学腐蚀的规律探究。
可以通过控制钢铁是否与空气接触、所接触的电解质溶液的酸碱度、钢铁在腐蚀过程中体系内的气压
变化等设计实验,找出规律。
(6)热分解产物的性质探究、判断。
①难溶性碳酸盐 氧化物+CO;
2
②碳酸的酸式盐 碳酸的正盐+CO+HO;
2 2
③铵盐(NH NO 除外) NH +相应的酸(或酸性氧化物+HO);
4 3 3 2
④硝酸盐 金属(或金属氧化物、亚硝酸盐)+氮氧化物(NO或NO )+O;
2 2
⑤草酸晶体 CO+CO+HO。
2 2
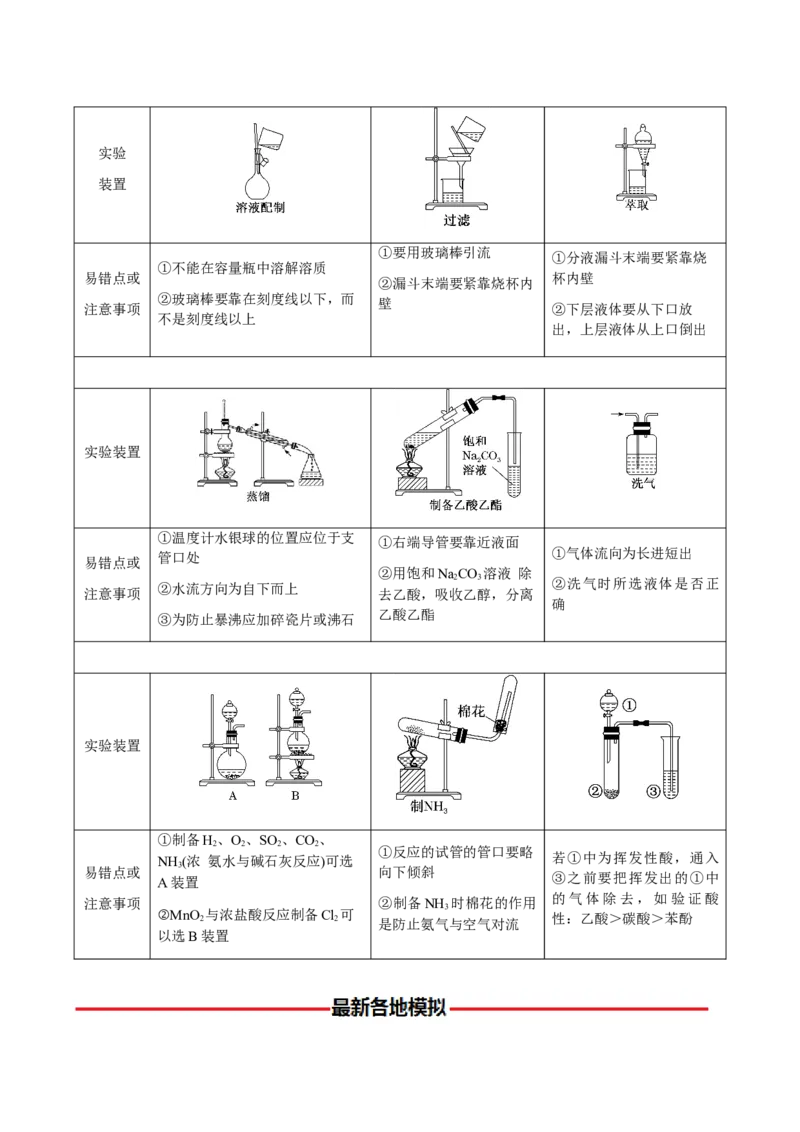
【策略4】仪器组合型实验方案的设计与评价实验
装置
①要用玻璃棒引流
①分液漏斗末端要紧靠烧
①不能在容量瓶中溶解溶质
易错点或 杯内壁
②漏斗末端要紧靠烧杯内
②玻璃棒要靠在刻度线以下,而
壁
注意事项 ②下层液体要从下口放
不是刻度线以上
出,上层液体从上口倒出
实验装置
①温度计水银球的位置应位于支
①右端导管要靠近液面
①气体流向为长进短出
管口处
易错点或
②用饱和NaCO 溶液 除
2 3 ②洗气时所选液体是否正
②水流方向为自下而上
注意事项 去乙酸,吸收乙醇,分离
确
乙酸乙酯
③为防止暴沸应加碎瓷片或沸石
实验装置
①制备H、O、SO 、CO、
2 2 2 2
①反应的试管的管口要略
NH (浓 氨水与碱石灰反应)可选 若①中为挥发性酸,通入
3
易错点或 向下倾斜
A装置 ③之前要把挥发出的①中
的气体除去,如验证酸
注意事项 ②制备NH 时棉花的作用
3
②MnO 2 与浓盐酸反应制备Cl 2 可 是防止氨气与空气对流 性:乙酸>碳酸>苯酚
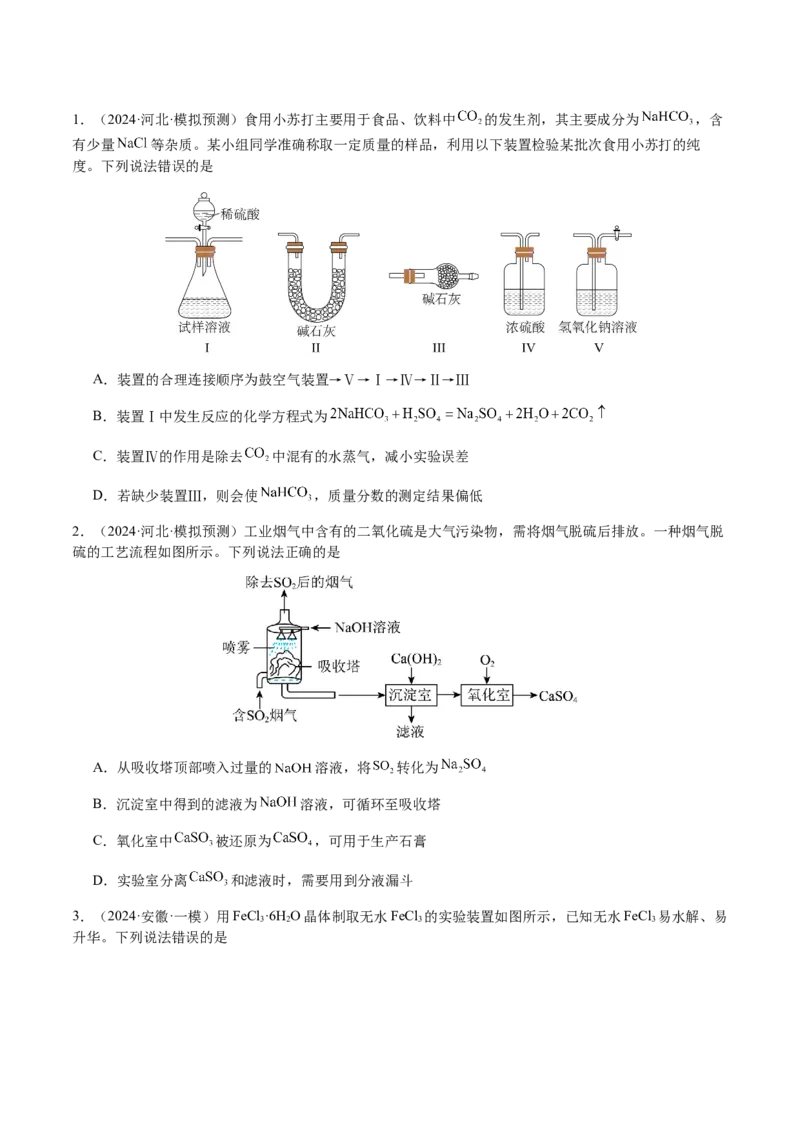
以选B装置1.(2024·河北·模拟预测)食用小苏打主要用于食品、饮料中 的发生剂,其主要成分为 ,含
有少量 等杂质。某小组同学准确称取一定质量的样品,利用以下装置检验某批次食用小苏打的纯
度。下列说法错误的是
A.装置的合理连接顺序为鼓空气装置→Ⅴ→Ⅰ→Ⅳ→Ⅱ→Ⅲ
B.装置Ⅰ中发生反应的化学方程式为
C.装置Ⅳ的作用是除去 中混有的水蒸气,减小实验误差
D.若缺少装置Ⅲ,则会使 ,质量分数的测定结果偏低
2.(2024·河北·模拟预测)工业烟气中含有的二氧化硫是大气污染物,需将烟气脱硫后排放。一种烟气脱
硫的工艺流程如图所示。下列说法正确的是
A.从吸收塔顶部喷入过量的 溶液,将 转化为
B.沉淀室中得到的滤液为 溶液,可循环至吸收塔
C.氧化室中 被还原为 ,可用于生产石膏
D.实验室分离 和滤液时,需要用到分液漏斗
3.(2024·安徽·一模)用FeCl ·6H O晶体制取无水FeCl 的实验装置如图所示,已知无水FeCl 易水解、易
3 2 3 3
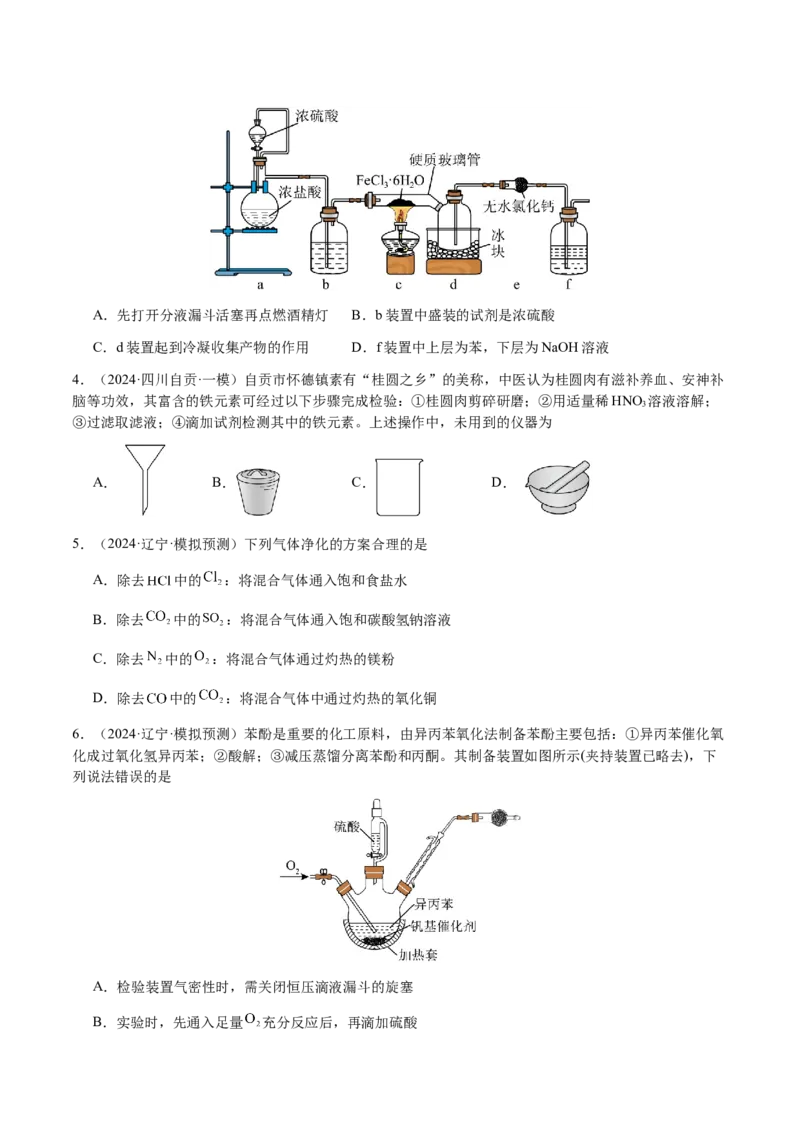
升华。下列说法错误的是A.先打开分液漏斗活塞再点燃酒精灯 B.b装置中盛装的试剂是浓硫酸
C.d装置起到冷凝收集产物的作用 D.f装置中上层为苯,下层为NaOH溶液
4.(2024·四川自贡·一模)自贡市怀德镇素有“桂圆之乡”的美称,中医认为桂圆肉有滋补养血、安神补
脑等功效,其富含的铁元素可经过以下步骤完成检验:①桂圆肉剪碎研磨;②用适量稀HNO 溶液溶解;
3
③过滤取滤液;④滴加试剂检测其中的铁元素。上述操作中,未用到的仪器为
A. B. C. D.
5.(2024·辽宁·模拟预测)下列气体净化的方案合理的是
A.除去 中的 :将混合气体通入饱和食盐水
B.除去 中的 :将混合气体通入饱和碳酸氢钠溶液
C.除去 中的 :将混合气体通过灼热的镁粉
D.除去 中的 :将混合气体中通过灼热的氧化铜
6.(2024·辽宁·模拟预测)苯酚是重要的化工原料,由异丙苯氧化法制备苯酚主要包括:①异丙苯催化氧
化成过氧化氢异丙苯;②酸解;③减压蒸馏分离苯酚和丙酮。其制备装置如图所示(夹持装置已略去),下
列说法错误的是
A.检验装置气密性时,需关闭恒压滴液漏斗的旋塞
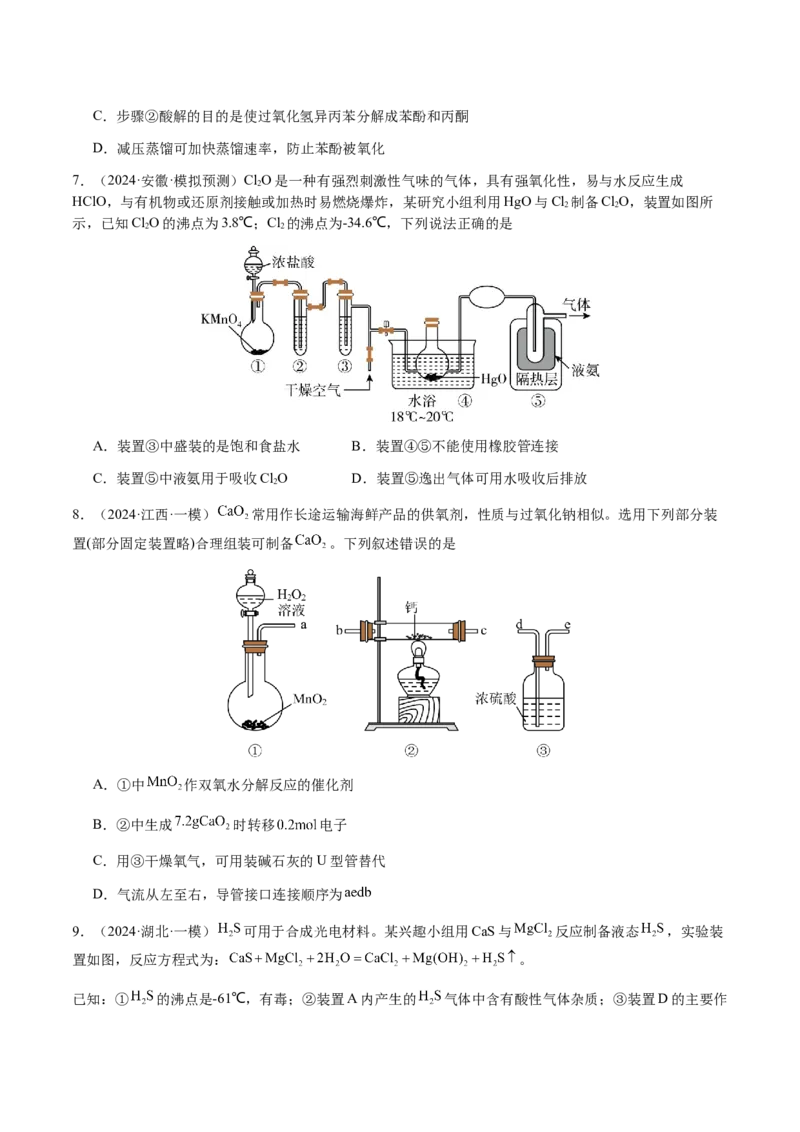
B.实验时,先通入足量 充分反应后,再滴加硫酸C.步骤②酸解的目的是使过氧化氢异丙苯分解成苯酚和丙酮
D.减压蒸馏可加快蒸馏速率,防止苯酚被氧化
7.(2024·安徽·模拟预测)ClO是一种有强烈刺激性气味的气体,具有强氧化性,易与水反应生成
2
HClO,与有机物或还原剂接触或加热时易燃烧爆炸,某研究小组利用HgO与Cl 制备ClO,装置如图所
2 2
示,已知ClO的沸点为3.8℃;Cl 的沸点为-34.6℃,下列说法正确的是
2 2
A.装置③中盛装的是饱和食盐水 B.装置④⑤不能使用橡胶管连接
C.装置⑤中液氨用于吸收ClO D.装置⑤逸出气体可用水吸收后排放
2
8.(2024·江西·一模) 常用作长途运输海鲜产品的供氧剂,性质与过氧化钠相似。选用下列部分装
置(部分固定装置略)合理组装可制备 。下列叙述错误的是
A.①中 作双氧水分解反应的催化剂
B.②中生成 时转移 电子
C.用③干燥氧气,可用装碱石灰的U型管替代
D.气流从左至右,导管接口连接顺序为
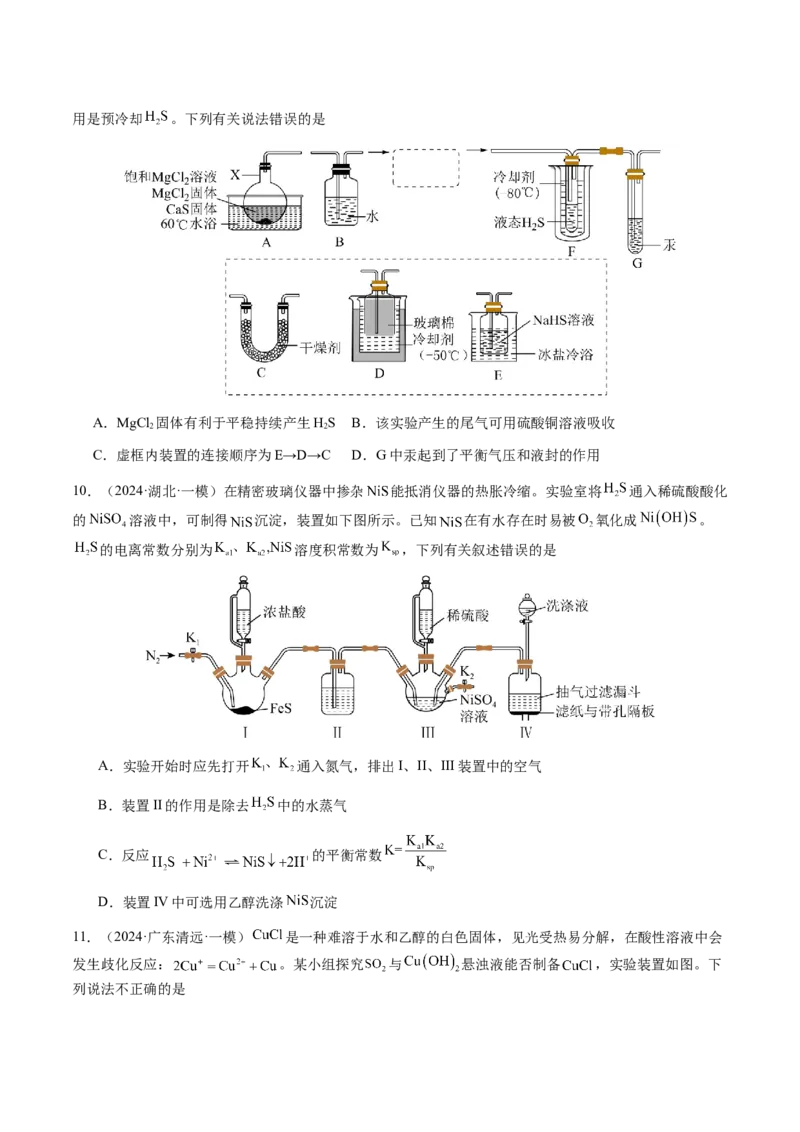
9.(2024·湖北·一模) 可用于合成光电材料。某兴趣小组用CaS与 反应制备液态 ,实验装
置如图,反应方程式为: 。
已知:① 的沸点是-61℃,有毒;②装置A内产生的 气体中含有酸性气体杂质;③装置D的主要作用是预冷却 。下列有关说法错误的是
A.MgCl 固体有利于平稳持续产生HS B.该实验产生的尾气可用硫酸铜溶液吸收
2 2
C.虚框内装置的连接顺序为E→D→C D.G中汞起到了平衡气压和液封的作用
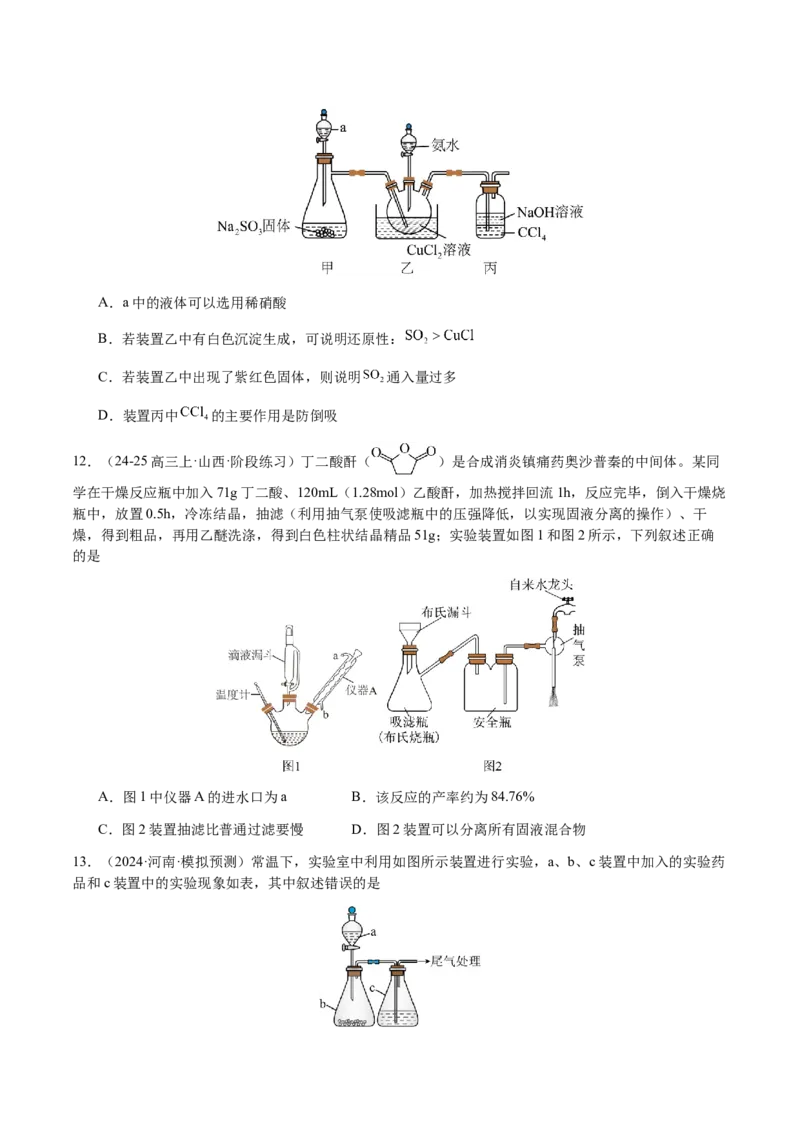
10.(2024·湖北·一模)在精密玻璃仪器中掺杂 能抵消仪器的热胀冷缩。实验室将 通入稀硫酸酸化
的 溶液中,可制得 沉淀,装置如下图所示。已知 在有水存在时易被 氧化成 。
的电离常数分别为 溶度积常数为 ,下列有关叙述错误的是
A.实验开始时应先打开 通入氮气,排出I、II、III装置中的空气
B.装置II的作用是除去 中的水蒸气
C.反应 的平衡常数
D.装置IV中可选用乙醇洗涤 沉淀
11.(2024·广东清远·一模) 是一种难溶于水和乙醇的白色固体,见光受热易分解,在酸性溶液中会
发生歧化反应: 。某小组探究 与 悬浊液能否制备 ,实验装置如图。下
列说法不正确的是A.a中的液体可以选用稀硝酸
B.若装置乙中有白色沉淀生成,可说明还原性:
C.若装置乙中出现了紫红色固体,则说明 通入量过多
D.装置丙中 的主要作用是防倒吸
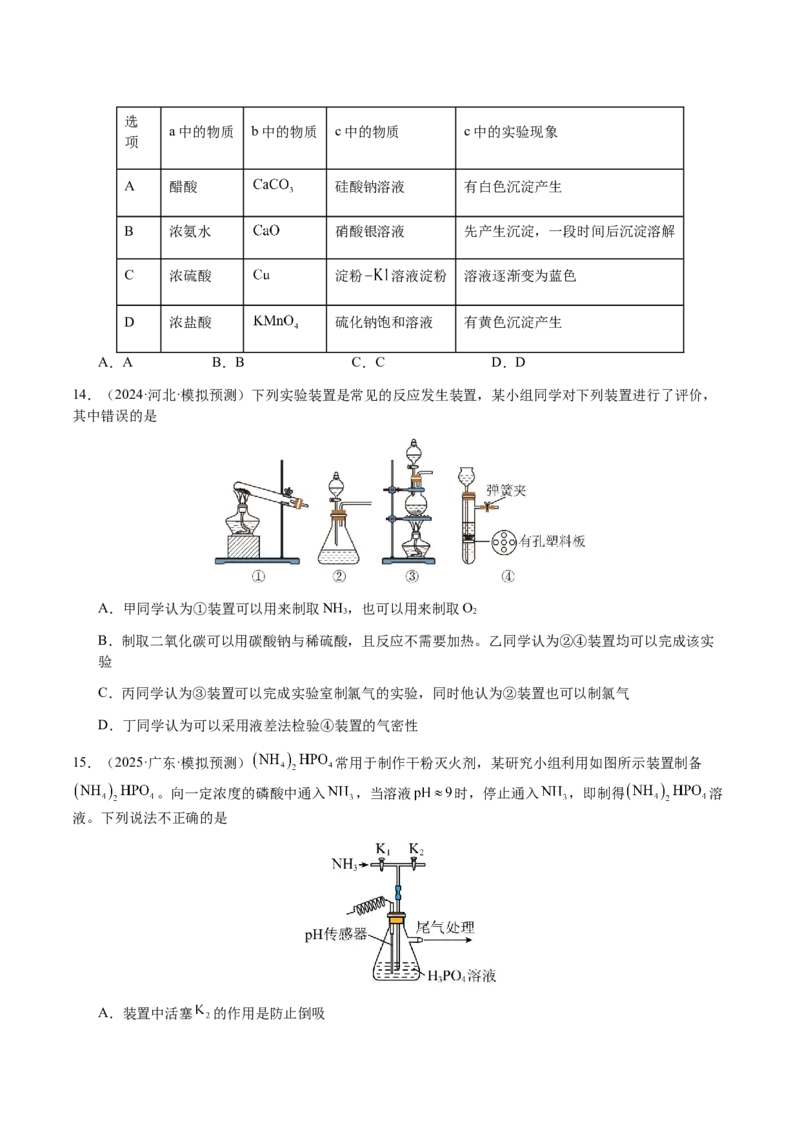
12.(24-25高三上·山西·阶段练习)丁二酸酐( )是合成消炎镇痛药奥沙普秦的中间体。某同
学在干燥反应瓶中加入71g丁二酸、120mL(1.28mol)乙酸酐,加热搅拌回流1h,反应完毕,倒入干燥烧
瓶中,放置0.5h,冷冻结晶,抽滤(利用抽气泵使吸滤瓶中的压强降低,以实现固液分离的操作)、干
燥,得到粗品,再用乙醚洗涤,得到白色柱状结晶精品51g;实验装置如图1和图2所示,下列叙述正确
的是
A.图1中仪器A的进水口为a B.该反应的产率约为84.76%
C.图2装置抽滤比普通过滤要慢 D.图2装置可以分离所有固液混合物
13.(2024·河南·模拟预测)常温下,实验室中利用如图所示装置进行实验,a、b、c装置中加入的实验药
品和c装置中的实验现象如表,其中叙述错误的是选
a中的物质 b中的物质 c中的物质 c中的实验现象
项
A 醋酸 硅酸钠溶液 有白色沉淀产生
B 浓氨水 硝酸银溶液 先产生沉淀,一段时间后沉淀溶解
C 浓硫酸 淀粉 溶液淀粉 溶液逐渐变为蓝色
D 浓盐酸 硫化钠饱和溶液 有黄色沉淀产生
A.A B.B C.C D.D
14.(2024·河北·模拟预测)下列实验装置是常见的反应发生装置,某小组同学对下列装置进行了评价,
其中错误的是
A.甲同学认为①装置可以用来制取NH ,也可以用来制取O
3 2
B.制取二氧化碳可以用碳酸钠与稀硫酸,且反应不需要加热。乙同学认为②④装置均可以完成该实
验
C.丙同学认为③装置可以完成实验室制氯气的实验,同时他认为②装置也可以制氯气
D.丁同学认为可以采用液差法检验④装置的气密性
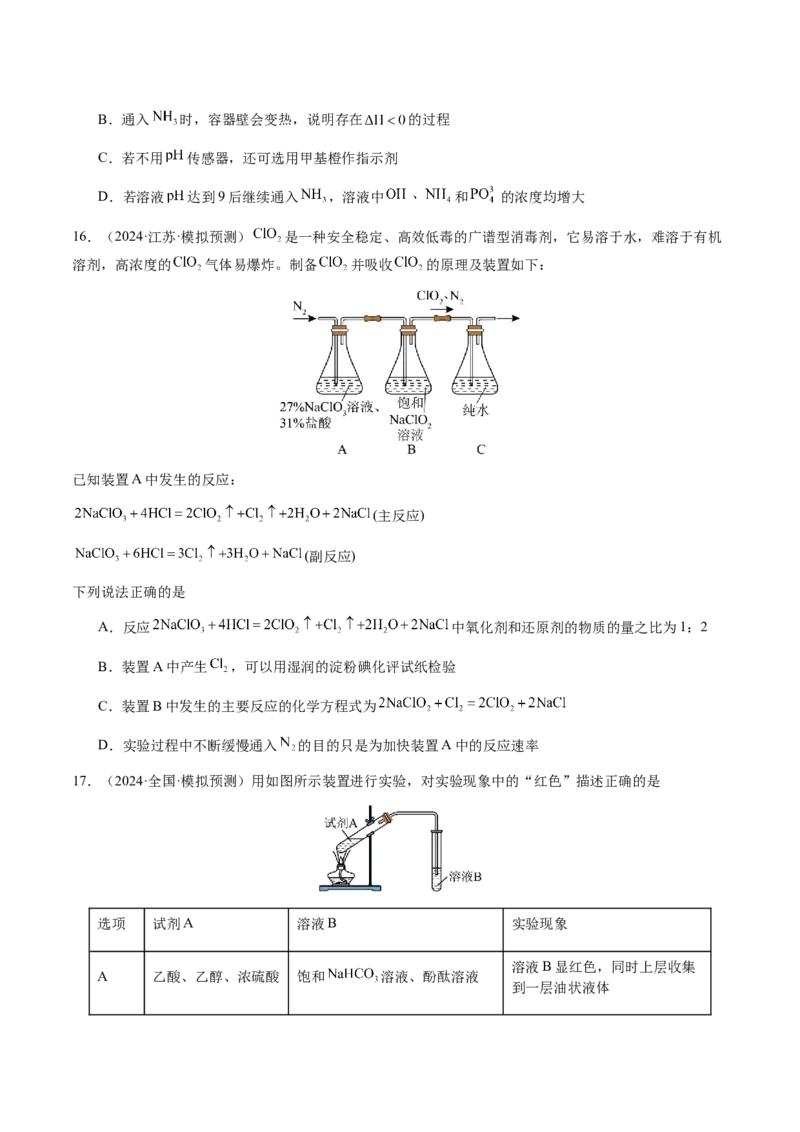
15.(2025·广东·模拟预测) 常用于制作干粉灭火剂,某研究小组利用如图所示装置制备
。向一定浓度的磷酸中通入 ,当溶液 时,停止通入 ,即制得 溶
液。下列说法不正确的是
A.装置中活塞 的作用是防止倒吸B.通入 时,容器壁会变热,说明存在 的过程
C.若不用 传感器,还可选用甲基橙作指示剂
D.若溶液 达到9后继续通入 ,溶液中 和 的浓度均增大
16.(2024·江苏·模拟预测) 是一种安全稳定、高效低毒的广谱型消毒剂,它易溶于水,难溶于有机
溶剂,高浓度的 气体易爆炸。制备 并吸收 的原理及装置如下:
已知装置A中发生的反应:
(主反应)
(副反应)
下列说法正确的是
A.反应 中氧化剂和还原剂的物质的量之比为1:2
B.装置A中产生 ,可以用湿润的淀粉碘化评试纸检验
C.装置B中发生的主要反应的化学方程式为
D.实验过程中不断缓慢通入 的目的只是为加快装置A中的反应速率
17.(2024·全国·模拟预测)用如图所示装置进行实验,对实验现象中的“红色”描述正确的是
选项 试剂A 溶液B 实验现象
溶液B显红色,同时上层收集
A 乙酸、乙醇、浓硫酸 饱和 溶液、酚酞溶液
到一层油状液体B 浓 溶液 滴有酚酞的 溶液 溶液B红色逐渐变浅至无色
C 混有铜粉的浓硫酸 品红溶液 品红溶液红色加深
D 浓氨水 紫色石蕊溶液 石蕊溶液变红色
A.A B.B C.C D.D
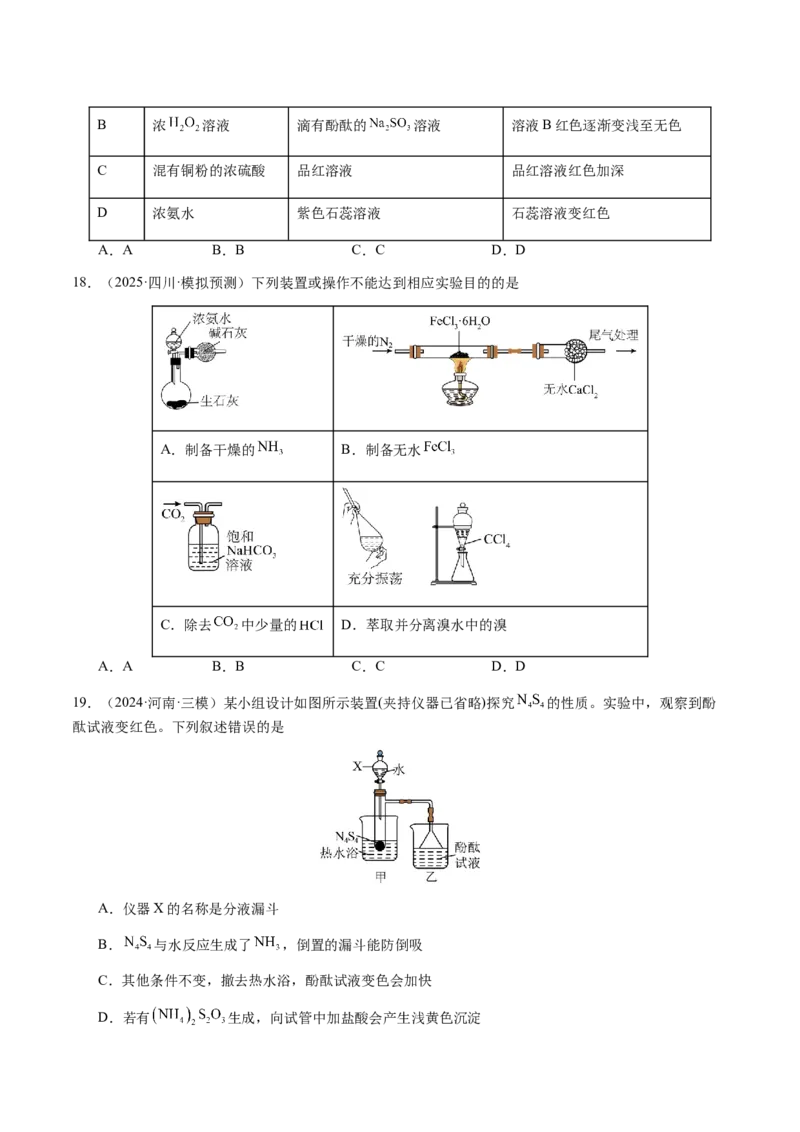
18.(2025·四川·模拟预测)下列装置或操作不能达到相应实验目的的是
A.制备干燥的 B.制备无水
C.除去 中少量的 D.萃取并分离溴水中的溴
A.A B.B C.C D.D
19.(2024·河南·三模)某小组设计如图所示装置(夹持仪器已省略)探究 的性质。实验中,观察到酚
酞试液变红色。下列叙述错误的是
A.仪器X的名称是分液漏斗
B. 与水反应生成了 ,倒置的漏斗能防倒吸
C.其他条件不变,撤去热水浴,酚酞试液变色会加快
D.若有 生成,向试管中加盐酸会产生浅黄色沉淀20.(2024·新疆·一模)三氯三(四氢呋喃)合铬(Ⅲ)[ ]易溶于四氢呋喃,极易水解,是重要的有
机反应固相催化剂。实验室常用如下装置合成 ,步骤如下:
①取适量无水 和锌粉放入滤纸套筒内,将滤纸套筒置于提取管中,并向双颈烧瓶中加入 无水
四氢呋喃;
②打开活塞,通入 , 后关闭活塞;
③保持四氢呋喃沸腾,冷凝回流反应 ;
④停止加热,通入 冷却至室温;
⑤处理掉多余的 ,冷却、抽滤、干燥得产品。
下列相关说法正确的是
A.步骤②和④中通入 的作用相同
B.步骤③中,先加热,再打开水龙头,将冷凝水从 处接入
C. 蒸汽从3管进入,反应液从2管回流至双颈烧瓶
D.无水 和锌粉放在滤纸套筒中是为了使产物及时脱离反应体系,提高转化率