文档内容
专题 11 物质结构与元素周期律
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 原子结构 核素...................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.原子结构..............................................................................
2.元素、核素、同位素.........................................................................................................................................
【命题预测】...........................................................................................................................................................
题型二 元素周期表 元素周期律...................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.强化记忆元素周期表的结构.............................................................................................................................
2.利用区间定位推断元素.....................................................................................................................................
3.粒子半径大小比较规律.....................................................................................................................................
4.金属性、非金属性强弱的判断.........................................................................................................................
【命题预测】...........................................................................................................................................................
考向1元素周期律...................................................................................................................................................
考向2通过元素推断判断递变规律.......................................................................................................................
题型三 微粒间的相互作用力.........................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.共价键、离子键、金属键的比较.....................................................................................................................
2.几种典型物质的电子式、结构式和模型.........................................................................................................
3.共价键类型.........................................................................................................................................................
4.范德华力、共价键、氢键的比较.....................................................................................................................【命题预测】...........................................................................................................................................................
题型四 杂化轨道理论与分子空间构型.........................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.键的极性与分子极性的关系.............................................................................................................................
2.中心原子杂化类型和分子空间构型的相互判断............................................................................................
3.常见等电子体.....................................................................................................................................................
【命题预测】...........................................................................................................................................................
题型五 简单晶体结构分析及晶胞计算.........................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.晶体类型及性质的比较.....................................................................................................................................
2.物质熔、沸点高低的比较.................................................................................................................................
3.晶体结构的相关计算.........................................................................................................................................
【命题预测】...........................................................................................................................................................
考向1晶体类型及性质的比较...............................................................
考向2晶体结构的相关计算.................................................................
考点要求 考题统计 考情分析
2024·江苏卷,1,3分;2024·北京卷,1,3分; 物质结构和元素
2024·上海卷;2022•山东卷,3,3分;2022·浙江 周期律,是历年高考
原子结构 核素
省1月卷,7,2分;2022·浙江省6月卷,7,2 的必考内容。试题以
选择题为主,重点考
分;
查元素性质的递变规
律,应用元素周期律
2024·江西卷,2,3分;2024· 重庆卷,5,3分; 和元素周期表进行元
元素周期表 元 2024·甘肃卷,13,3分;2024·江苏卷,4,3分; 素推断。预测 2025
素周期律 2023•湖北卷,6,3分;2023•广东卷,14,3分; 年该知识将是一个必
2022•辽宁卷,5,3分; 考点,题型依然会以
选择题为主,难度不
会有大的变化。重点
2024· 重庆卷,3,3分;2024·广西卷,1,3分;
掌握通过结构理论来
微粒间的相互作 2024· 海南卷,4,2分;2024· 海南卷,11,4
解释现象、性质比
用力 分;2024·甘肃卷,14,3分;2024·山东卷,9,2
较、定性推断、归纳
分;2024·湖北卷,12,3分;2024·浙江6月卷,14,3分;2022•江苏卷,5,3分;
杂化轨道理论与 2024·湖北卷,5,3分;2024·河北卷,9,3分;
分子空间构型 2024·福建卷,6,4分;2024·湖南卷,9,3分;
2024·广西卷,1,3分;2024· 重庆卷,10,3分;
2024· 贵州卷,8,3分;2024·江西卷,12,3分; 总结等。
简单晶体结构分 2024·甘肃卷,12,3分;2024·安徽卷,14,3
析及晶胞计算 分;2024·湖北卷,11,3分;2024·湖南卷,12,3
分;2024·河北卷,12,3分;2024·辽吉黑卷,
14,3分;
题型一 原子结构 核素
1.(2024·江苏卷,1,3分)我国探月工程取得重大进展。月壤中含有Ca、Fe等元素的磷酸盐,下列元
素位于元素周期表第二周期的是( )
A.O B.P C.Ca D.Fe
2.(2024·上海卷)下列关于18F与19F说法正确的是( )
A.是同种核素 B.是同素异形体 C.19F比18F多一个电子 D.19F比18F多一个中子
3.(2024·北京卷,1,3分)我国科研人员利用激光操控方法,从Ca原子束流中直接俘获41Ca原子,实
41Ca
现了对同位素41Ca的灵敏检测。 的半衰期(放射性元素的原子核有半数发生衰变所需的时间)长达10万年,是14C的17倍,可应用于地球科学与考古学。下列说法正确的是( )
20 Ca
钙
4s2
40.08
A.41Ca的原子核内有21个中子
B.41Ca的半衰期长,说明41Ca难以失去电子
C.41Ca衰变一半所需的时间小于14C衰变一半所需的时间
D.从Ca原子束流中直接俘获41Ca原子的过程属于化学变化
1 . 原子结构
(1)微粒间“三个”数量关系
中性原子:核电荷数=核内质子数=核外电子数=原子序数
阴离子:核外电子数=质子数+所带的电荷数
阳离子:核外电子数=质子数-所带的电荷数
(2)核素(原子)的表示及其数量关系
①表示: 表示质子数为 Z 、质量数为 A 、中子数为 A - Z 的核素原 子。
+c
③符号b Xd+中各数字的含义
a e
(3)10e-、18e-微粒
10电子体和18电子体是元素推断题的重要突破口。
以Ne为中心记忆10电子体:
Ne
以Ar为中心记忆18电子体:Ar
此外,由10电子体中的CH 、NH 、HO、HF失去一个H原子后的剩余部分如—CH 、—NH 、—
4 3 2 3 2
OH、—F等为9电子体,两两组合得到的物质如CHCH、CHOH、HO、NH、F 等为18电子体。
3 3 3 2 2 2 4 2
【易错提醒】
(1)同种元素,可以有若干种不同的核素,即核素种类远大于元素种类。
(2)同位素的研究对象是核素,因此分子之间、离子之间不可能互称为同位素。
(3)一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子。
(4)质子数相同而中子数不同的同一种元素的不同核素互为同位素,不指具体原子。
(5)不同的核素可能具有相同的质子数,如H与H;也可能具有相同的中子数,如6C与O;也可能具
有相同的质量数,如C与N;也可能质子数、中子数、质量数均不相同,如H与C。
(6)同位素原子之间化学性质几乎完全相同,物理性质不同。
(7)不同核素之间的转化属于核反应,不属于化学反应。
2 .元素、核素、同位素
(1)“三素”关系
同位素的“六同三不同”
【名师提醒】
“四同”的判断方法——关键是抓住描述的对象
①同位素——原子,如1 H、2 H、3 H。
1 1 1②同素异形体——单质,如O 与O,金刚石与石墨,红磷与白磷。
2 3
③同系物——有机化合物,如CH CH 、CH CH CH 。
3 3 3 2 3
④同分异构体——化合物,如正戊烷与新戊烷。
(2)相对原子质量
1.下列有关元素及其化合物的判断正确的是( )
A.
134Cs和 137Cs等发生变化变成其他元素发生了化学变化
55 55
B.8个中子的碳原子的核素符号为
8C
6
C.
45Fe衰变放出两个质子后变成 43Fe
26 26
D.
131I是碘元素的一种放射性核素,加碘食盐中的“碘”不是碘 131I
53 53
203 205
2.天然铊有两种稳定同位素 Tl和 Tl。下列有关铊的同位素说法中,不正确的是( )
81 81
203 205 203 205
A. Tl和 Tl质子数相同 B. Tl和 Tl互为同素异形体
81 81 81 81
203 205 205
C. Tl和 Tl中子数之差为2 D. Tl原子核内中子数与核外电子数之差为43
81 81 81
3.钋-210属于极毒性放射性元素,以相同重量来比较,钋-210的毒性是氰化物的2.5亿倍,只需
一颗尘埃大小就足以取人性命,而且没有解毒剂。下列有关210 P 说法正确的是( )
84 O
A.
210Po
与
209Po
互为同素异形体 B.
210Po
与
210At互为同位素
84 84 84 85
C.
210Po的质子数为84,中子数为126
D.Po元素的相对原子质量为210
84
4 W W
4.1934年约里奥—居里夫妇在核反应中用a粒子(即氦2He)轰击金属原子Z X,得到核素Z X,开创了
W 4 30 1
人造放射性核素的先河:Z X+2He→Z2Y+0n,其中元素X、Y的最外层电子数之和为8。下列叙述正确的
是( )A.X的相对原子质量为26 B.X、Y均可形成三氯化物
C.X的原子半径小于Y的 D.Y仅有一种含氧酸
5.日本将福岛核废水排海,引起全世界强烈谴责。核废水中含有放射性的氚、碘-131、铯-134、
铯-137、碳-14、钴-60和锶-90等。下列叙述正确的是( )
A. 原子所含中子数与质子数之差为25 B.铯-134和铯-137是两种不同元素
C.氕、氘、氚三种核素都含有中子 D. 和 的核外电子数之差为1
6.地表水和地下水都来源于大气降水,但重水和轻水中同位素含量是不同的,有时差别还相当大,
氢包括两种稳定核素:H和D,氧常见的核素16O、17O和18O,下列有关说法正确的是( )
A.H 和D 互为同分异构体,其化学性质完全相同
2 2
B.HO、HO、HO互为同位素,都能与金属钠发生反应
C.18O 和18O 互为同素异形体,其密度之比为2∶3
2 3
D.电解一定量的DO时,阴、阳两极所得气体的质量之比约为2∶9
题型二 元素周期表 元素周期律
1.(2024·江西卷,2,3分)科学家发现宇宙中存在100多种星际分子。下列关于星际分子说法正确的
是( )
A.分子的极性:SiH>NH B.键的极性:H—Cl>H—H
4 3
C.键角:HO>CH D.分子中三键的键长:HC≡N>HC≡CH
2 4
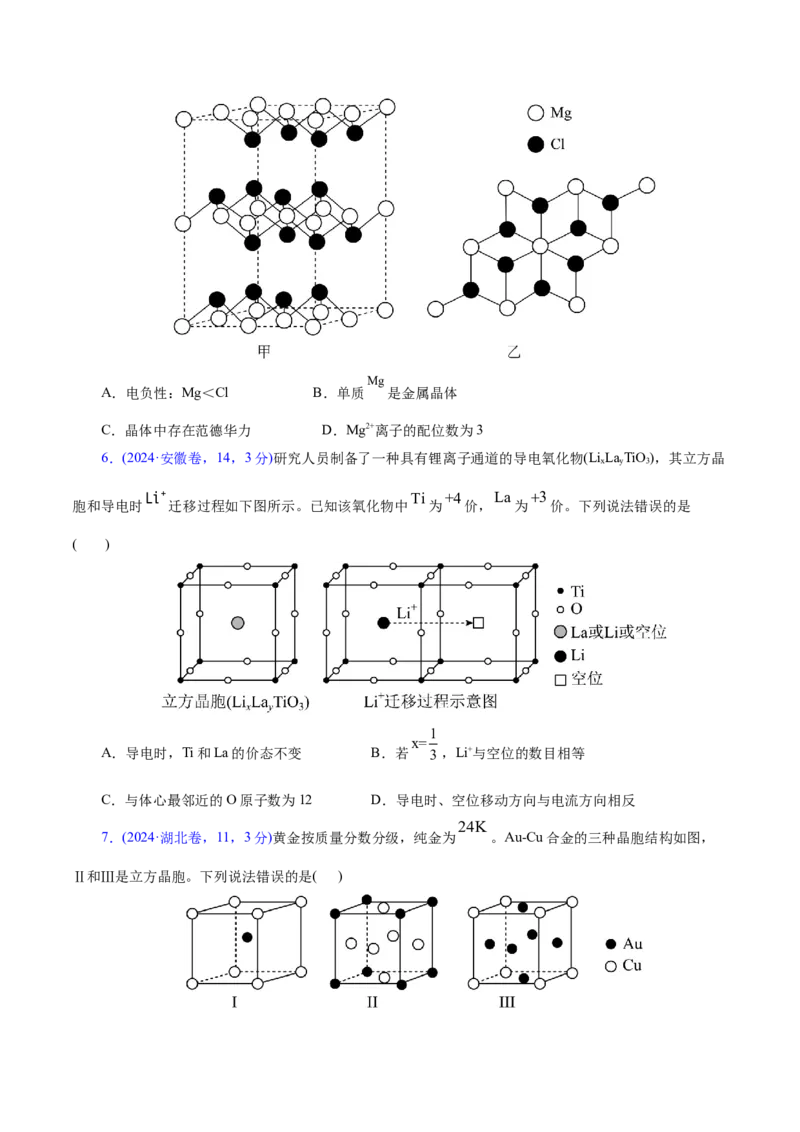
2.(2024· 重庆卷,5,3分)某合金含Mg、Al、Si、Mn和Cu等元素。下列说法正确的是( )
A.Si的电负性大于Al B.Mn和Cu均为d区元素
C.Mg的第一电离能小于Al D.基态时,Mg原子和Mn原子的单电子数相等
3.(2024·甘肃卷,13,3分)温室气体NO在催化剂作用下可分解为O 和N,也可作为氧化剂氧化苯
2 2 2
制苯酚。下列说法错误的是( )
A.原子半径:Or(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl);r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)。
“三看”核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。例:r(Cl-)>r(Cl);r(Fe2+)>r(Fe3+)。
4 .金属性、非金属性强弱的判断
本质 原子越易失电子,金属性越强(与原子失电子数目无关)
①在金属活动性顺序表中越靠前,金属性越强
②单质与水或非氧化性酸反应越剧烈,金属性越强
金属性比
③单质还原性越强或阳离子氧化性越弱,金属性越强
较
判断方法
④最高价氧化物对应水化物的碱性越强,金属性越强
⑤若Xn++Y→X+Ym+,则Y比X的金属性强
⑥元素在周期表中的位置:左边或下方元素的金属性强
本质 原子越易得电子,非金属性越强(与原子得电子数目无关)
①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
非金属性
②单质氧化性越强或阴离子还原性越弱,非金属性越强
比较
判断方法
③最高价氧化物对应水化物的酸性越强,非金属性越强
④元素在周期表中的位置:右边或上方元素的非金属性强
【易错提醒】
(1)对于主族元素而言,元素的最高正化合价和主族序数相同,但是氧无最高正价,氟无正价,一般为
零价或负价。
(2)判断元素非金属性或金属性的强弱,依据是元素原子在化学反应中得失电子的难易而不是得失电子
数目的多少。
(3)根据元素氧化物对应水化物的酸碱性的强弱判断元素非金属性或金属性的强弱时,必须是其最高价
氧化物的水化物。
(4) 不 能 根 据 热 稳 定 性 HF>HCl>HBr>HI , 来 判 断 酸 性 : HF>HCl>HBr>HI , 实 际 是 酸 性
HF As>P B.热稳定性NH > PH > AsH
3 3 3
C.酸性:HAsO >H SO >H PO D.Ga(OH) 的化学性质可能与Al (OH) 相似
3 4 2 4 3 4 3 3
2.下列性质的比较,不能用元素周期律解释的是( )A.非金属性: O>S>P B.热稳定性:NH >PH >SiH
3 3 4
C.碱性: KOH>NaOH>Mg(OH) D.酸性:HCl>HF>HS
2 2
3.(2025·浙江省部分学校高三选考模拟)下列说法正确的是( )
A.键能:H-O>H-S,因此HO的沸点高于HS的沸点
2 2
B.原子轨道具有一定的伸展方向,所形成的共价键都具有方向性
C.杂化轨道可用于形成σ键和容纳未参与成键的孤电子对,不能用于形成π键
D.电负性越大,非金属性越强,第一电离能也越大
4.(2025·浙江省强基联高三联考)对金属材料中C、O、N、S的含量进行定性和定量分析,可以确定
金属材料的等级。下列说法正确的是( )
A.半径:r(S2-)>r(O2-)>r(N3-)
B.沸点:HO> H S>NH >CH
2 2 3 4
C.键角:CH>NH>HO> H S
4 3 2 2
D.四种元素形成的单质的晶体类型一定相同
考向 2 通过 元素推断判断递变规律
5.(2025·浙江省七彩阳光新高考研究联盟高三返校联考)核电荷数依次增大的X、Y、Z、R和T五种
主族元素,X原子的原子核只含质子,短周期中T元素的最高价氧化物的水化物的酸性最强,Y原子的最
外层电子数是内层电子数的2倍,Z与Y相邻,基态R原子的s能级电子数与p能级电子数比为6:7,下
列说法不正确的是( )
A.原子半径:Z<Y<R B.键的极性:ZX<RT
3 3
C.热稳定性:YX <YX D.熔、沸点:YT>YX
4 4 10 4 4
6.(2025· 浙江省杭州市浙南联盟高三10月联考)W、X、Y、Z、M为短周期主族元素,原子序数依次
增大,分别位于三个不同短周期,最外层电子数之和为20。Z的最外层电子数与其K层电子数相等,XY
2
是形成酸雨的物质之一。下列说法不正确的是( )
A.熔点:ZY>ZM B.键角: XW>XW+
3 4
C.热稳定性:XW<WY D.分子的极性:XY <XY
3 2 3 2
7.[真题改编](2022•辽宁省选择性考试,5改编)短周期元素X、Y、Z、W、Q原子序数依次增大。基
态X、Z、Q原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误
的是( )
A.X能与多种元素形成共价键 B.简单氢化物沸点:ZZ D.电负性:WQ B.单质的熔点:X>Y
C.简单氢化物的沸点:Z>Q D.最高价含氧酸的酸性:Z>Y
题型三 微粒间的相互作用力
1.(2024· 重庆卷,3,3分)下列各分子既含有sp2杂化的原子又能与HO形成氢键的是( )
2
A.CHCH B.CH=CHBr C.CHCOOH D.CHCHNH
3 3 2 3 3 2 2
2.(2024·甘肃卷,14,3分)温室气体NO在催化剂作用下可分解为O 和N,也可作为氧化剂氧化苯
2 2 2
制苯酚。下列说法错误的是( )
A.相同条件下N 比O 稳定 B.NO与NO +的空间构型相同
2 2 2 2
N-O N-N σ π
C.NO中 键比 键更易断裂 D.NO中 键和大 键的数目不相等
2 2
3.(2024·广西卷,1,3分)白磷(P )是不溶于水的固体,在空气中易自燃。下列有关白磷的说法错误的
4
是( )
P
A.分子中每个 原子的孤电子对数均为1
B.常保存于水中,说明白磷密度大于1g· cm-3
C.难溶于水,是因为水是极性分子,P 是非极性分子
4
D.熔点低,是因为P 分子内的P-P键弱
4
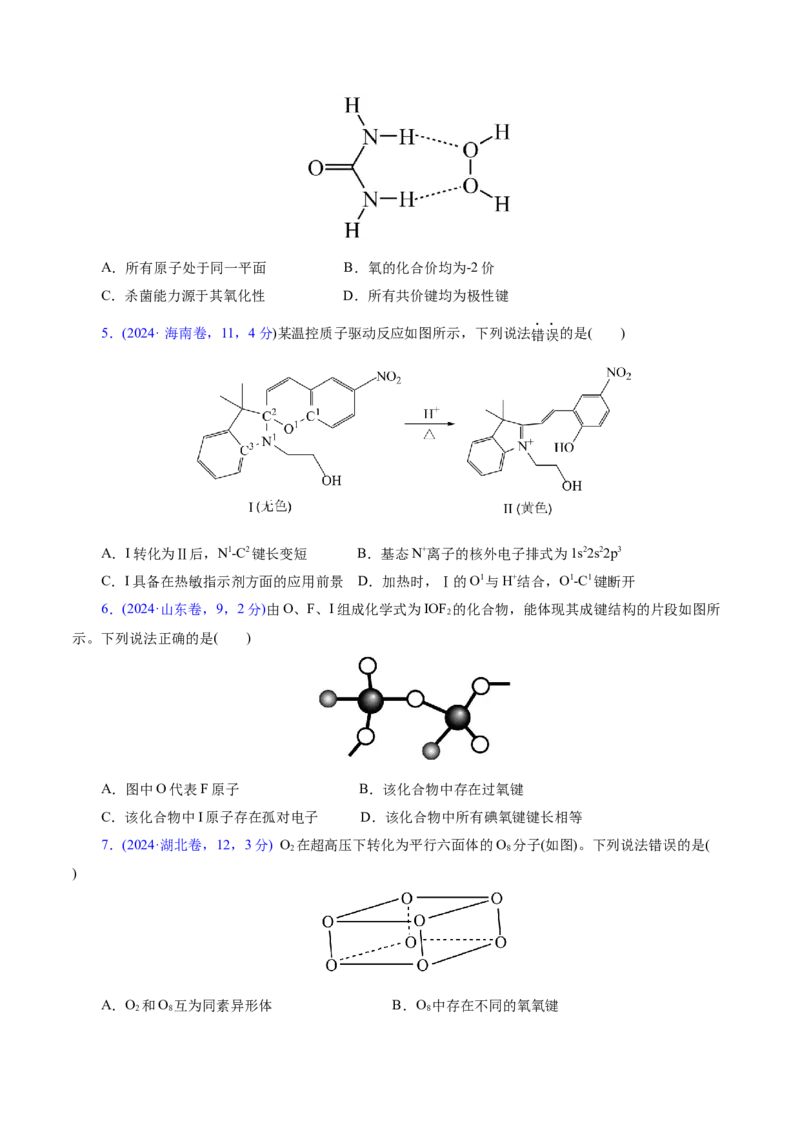
4.(2024· 海南卷,4,2分)过氧化脲[CO(NH)·2H O]是一种常用的消毒剂,可由过氧化氢(HO)和脲
2 2 2 2 2 2
[CO(NH)]加合而成,代表性结构如图所示。下列关于过氧化脲的说法正确的是( )
2 2A.所有原子处于同一平面 B.氧的化合价均为-2价
C.杀菌能力源于其氧化性 D.所有共价键均为极性键
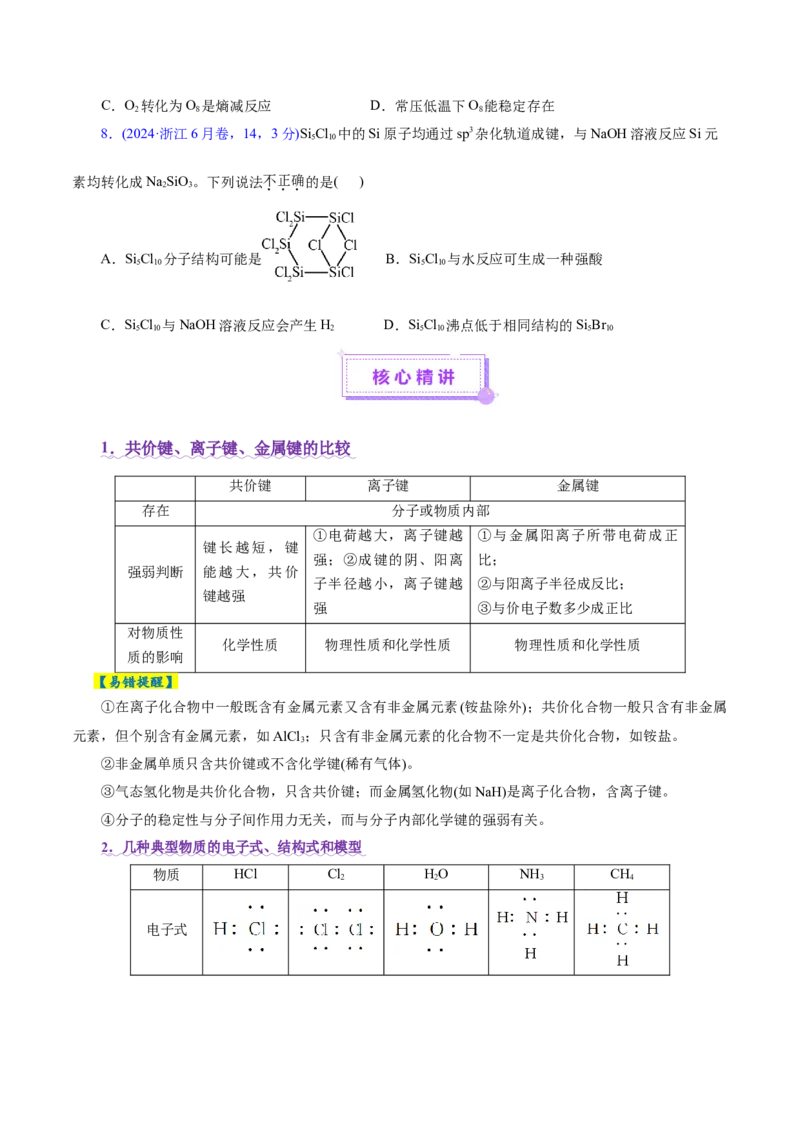
5.(2024· 海南卷,11,4分)某温控质子驱动反应如图所示,下列说法错误的是( )
A.I转化为Ⅱ后,N1-C2键长变短 B.基态N+离子的核外电子排式为1s22s22p3
C.I具备在热敏指示剂方面的应用前景 D.加热时,Ⅰ的O1与H+结合,O1-C1键断开
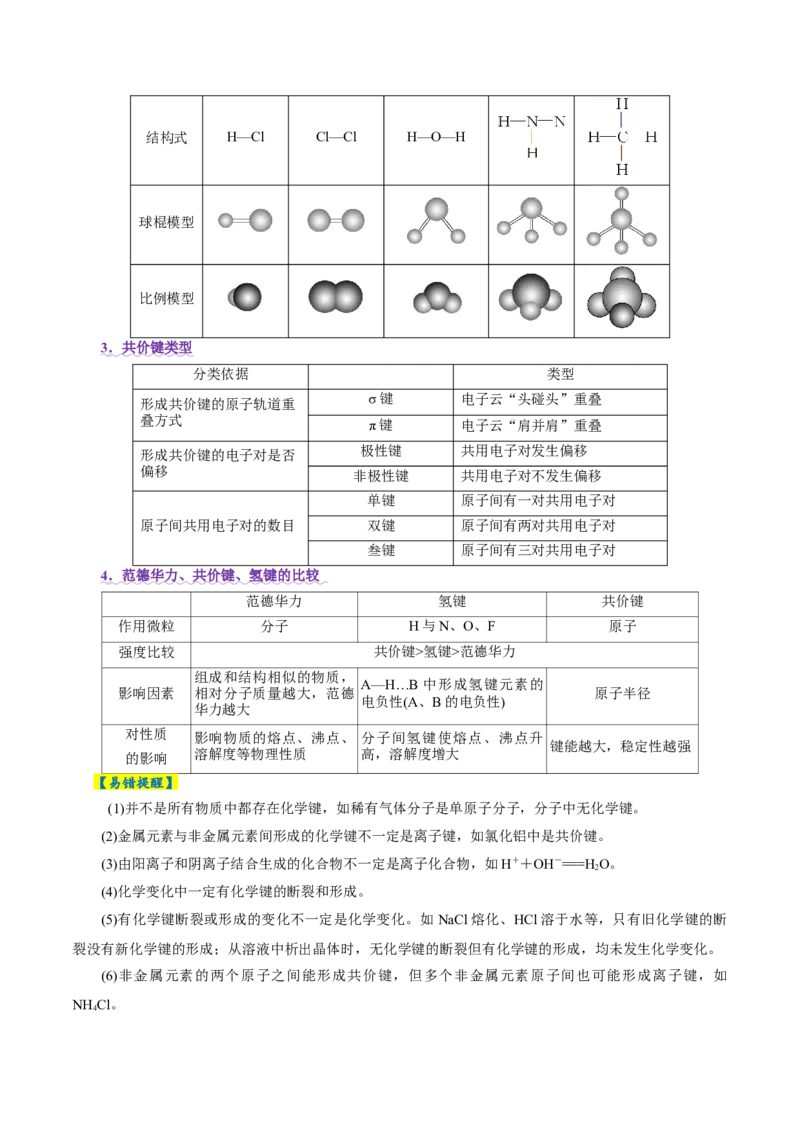
6.(2024·山东卷,9,2分)由O、F、I组成化学式为IOF 的化合物,能体现其成键结构的片段如图所
2
示。下列说法正确的是( )
A.图中O代表F原子 B.该化合物中存在过氧键
C.该化合物中I原子存在孤对电子 D.该化合物中所有碘氧键键长相等
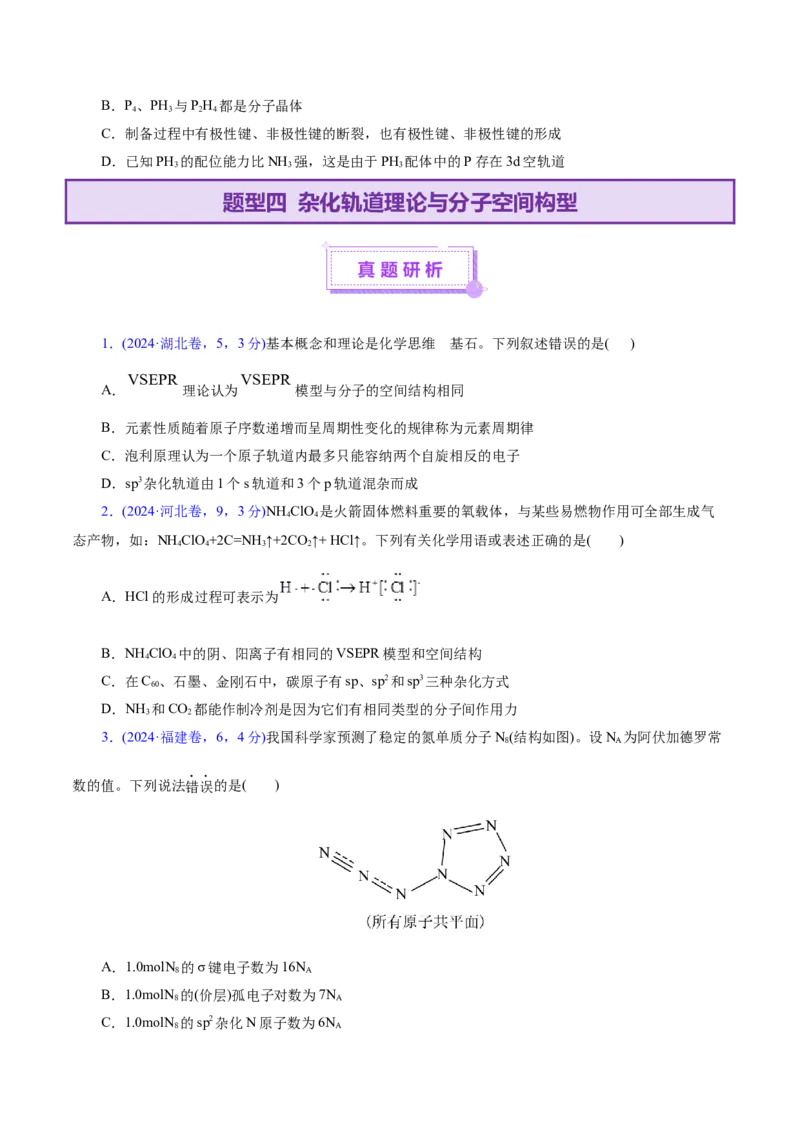
7.(2024·湖北卷,12,3分) O 在超高压下转化为平行六面体的O 分子(如图)。下列说法错误的是(
2 8
)
A.O 和O 互为同素异形体 B.O 中存在不同的氧氧键
2 8 8C.O 转化为O 是熵减反应 D.常压低温下O 能稳定存在
2 8 8
8.(2024·浙江6月卷,14,3分)Si Cl 中的Si原子均通过sp3杂化轨道成键,与NaOH溶液反应Si元
5 10
素均转化成NaSiO。下列说法不正确的是( )
2 3
A.Si Cl 分子结构可能是 B.Si Cl 与水反应可生成一种强酸
5 10 5 10
C.Si Cl 与NaOH溶液反应会产生H D.Si Cl 沸点低于相同结构的Si Br
5 10 2 5 10 5 10
1 .共价键、离子键、金属键的比较
共价键 离子键 金属键
存在 分子或物质内部
①电荷越大,离子键越 ①与金属阳离子所带电荷成正
键长越短,键
强;②成键的阴、阳离 比;
强弱判断 能越大,共价
子半径越小,离子键越 ②与阳离子半径成反比;
键越强
强 ③与价电子数多少成正比
对物质性
化学性质 物理性质和化学性质 物理性质和化学性质
质的影响
【易错提醒】
①在离子化合物中一般既含有金属元素又含有非金属元素(铵盐除外);共价化合物一般只含有非金属
元素,但个别含有金属元素,如AlCl ;只含有非金属元素的化合物不一定是共价化合物,如铵盐。
3
②非金属单质只含共价键或不含化学键(稀有气体)。
③气态氢化物是共价化合物,只含共价键;而金属氢化物(如NaH)是离子化合物,含离子键。
④分子的稳定性与分子间作用力无关,而与分子内部化学键的强弱有关。
2 .几种典型物质的电子式、结构式和模型
物质 HCl Cl HO NH CH
2 2 3 4
电子式结构式 H—Cl Cl—Cl H—O—H
球棍模型
比例模型
3 .共价键类型
分类依据 类型
σ键 电子云“头碰头”重叠
形成共价键的原子轨道重
叠方式
π键 电子云“肩并肩”重叠
极性键 共用电子对发生偏移
形成共价键的电子对是否
偏移
非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对的数目 双键 原子间有两对共用电子对
叁键 原子间有三对共用电子对
4 .范德华力、共价键、氢键的比较
范德华力 氢键 共价键
作用微粒 分子 H与N、O、F 原子
强度比较 共价键>氢键>范德华力
组成和结构相似的物质,
A—H…B中形成氢键元素的
影响因素 相对分子质量越大,范德 原子半径
电负性(A、B的电负性)
华力越大
对性质 影响物质的熔点、沸点、 分子间氢键使熔点、沸点升
键能越大,稳定性越强
的影响 溶解度等物理性质 高,溶解度增大
【易错提醒】
(1)并不是所有物质中都存在化学键,如稀有气体分子是单原子分子,分子中无化学键。
(2)金属元素与非金属元素间形成的化学键不一定是离子键,如氯化铝中是共价键。
(3)由阳离子和阴离子结合生成的化合物不一定是离子化合物,如H++OH-===H O。
2
(4)化学变化中一定有化学键的断裂和形成。
(5)有化学键断裂或形成的变化不一定是化学变化。如NaCl熔化、HCl溶于水等,只有旧化学键的断
裂没有新化学键的形成;从溶液中析出晶体时,无化学键的断裂但有化学键的形成,均未发生化学变化。
(6)非金属元素的两个原子之间能形成共价键,但多个非金属元素原子间也可能形成离子键,如
NH Cl。
4(7)离子键存在于强碱、绝大多数盐(包括铵盐)、活泼金属氧化物、过氧化物等离子化合物中。
(8)分子之间一定存在分子间作用力,分子间作用力只存在于分子之间。
(9)离子晶体熔化时破坏离子键,共价晶体熔化时破坏共价键,而分子晶体熔化时破坏分子间作用力。
(10)分子的稳定性与分子间的作用力无关,而与分子内部的化学键的强弱有关。
1.下列物质中含有相同的化学键类型的是( )
A.NaCl、HCl、HO、NaOH B.Cl、NaS、HCl、SO
2 2 2 2
C.HBr、CO、HO、CS D.NaO、HO、HO、O
2 2 2 2 2 2 2 2 3
2.在下列化学反应中,既有离子键、共价键断裂,又有离子键、共价键形成的是( )
A.2Na +2H O = 2NaOH + H ↑ B.SO +2H S = 3S↓+2H O
2 2 2 2 2
C.MgN+6H O=3Mg(OH)↓+2NH↑ D.AgNO+NaCl=AgCl↓+NaNO
3 2 2 2 3 3 3
3.下列说法正确的是( )
A.二氧化硅,碳化硅和金刚石中只存在共价键,都是共价化合物
B.CCl 和NaCl两种分子中,每个原子的最外层都具有8电子稳定结构
4
C.NH 溶于水,既有共价键的断裂,也有共价键和离子键的形成
3
D.醋酸钠溶于水,破坏了离子键和共价键
4.下列说法正确的是( )
A.NaOH固体熔化的过程中,离于键和共价键均被破坏
B.NaHSO 在水溶液中或熔融状态下,都能电高出H+
4
C.CO 和PCl 分子中,每个原子最外层都具有8电子稳定结构
2 3
D.HBr比HCl的热稳定性差,说明HBr的分子间作用力比HC1弱
5.(2025·浙江部分高中高三开学考试)2023年诺贝尔化学奖颁发给量子点的发现与研究。其中巯基乙
酸(HSCH COOH)是量子点合成过程中的一种保护剂。下列说法不正确的是( )
2
A.亲水性:羧基(-COOH)>巯基(-SH)
B.酸性:巯基乙酸(HSCH COOH)>乙酸(CHCOOH)
2 3
C.与量子点上的过渡金属离子配位的原子是S,结合后水溶性降低
D.与水分子形成的氢键强度:HSCH CO-OH>HSCH CS-OH>HSCH CSe-OH
2 2 2
6.(2025·浙江省Z20名校联盟高三开学考试)加热煮沸的浓NaOH溶液和白磷反应可制PH ,该过程同
3
时可获得PH。其中一个反应为:P+3NaOH+3HO=3NaHPO + PH ↑。下列说法不正确的是( )
2 4 4 2 2 3
A.热稳定性:NH >PH ,沸点:NH<PH
3 3 2 4 2 4B.P、PH 与PH 都是分子晶体
4 3 2 4
C.制备过程中有极性键、非极性键的断裂,也有极性键、非极性键的形成
D.已知PH 的配位能力比NH 强,这是由于PH 配体中的P存在3d空轨道
3 3 3
题型四 杂化轨道理论与分子空间构型
的
1.(2024·湖北卷,5,3分)基本概念和理论是化学思维 基石。下列叙述错误的是( )
VSEPR VSEPR
A. 理论认为 模型与分子的空间结构相同
B.元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律
C.泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子
D.sp3杂化轨道由1个s轨道和3个p轨道混杂而成
2.(2024·河北卷,9,3分)NH ClO 是火箭固体燃料重要的氧载体,与某些易燃物作用可全部生成气
4 4
态产物,如:NH ClO +2C=NH ↑+2CO ↑+ HCl↑。下列有关化学用语或表述正确的是( )
4 4 3 2
A.HCl的形成过程可表示为
B.NH ClO 中的阴、阳离子有相同的VSEPR模型和空间结构
4 4
C.在C 、石墨、金刚石中,碳原子有sp、sp2和sp3三种杂化方式
60
D.NH 和CO 都能作制冷剂是因为它们有相同类型的分子间作用力
3 2
3.(2024·福建卷,6,4分)我国科学家预测了稳定的氮单质分子N(结构如图)。设N 为阿伏加德罗常
8 A
数的值。下列说法错误的是( )
A.1.0molN 的σ键电子数为16N
8 A
B.1.0molN 的(价层)孤电子对数为7N
8 A
C.1.0molN 的sp2杂化N原子数为6N
8 AD.112.0gN 完全分解,产生的N 分子数为4mol
8 2
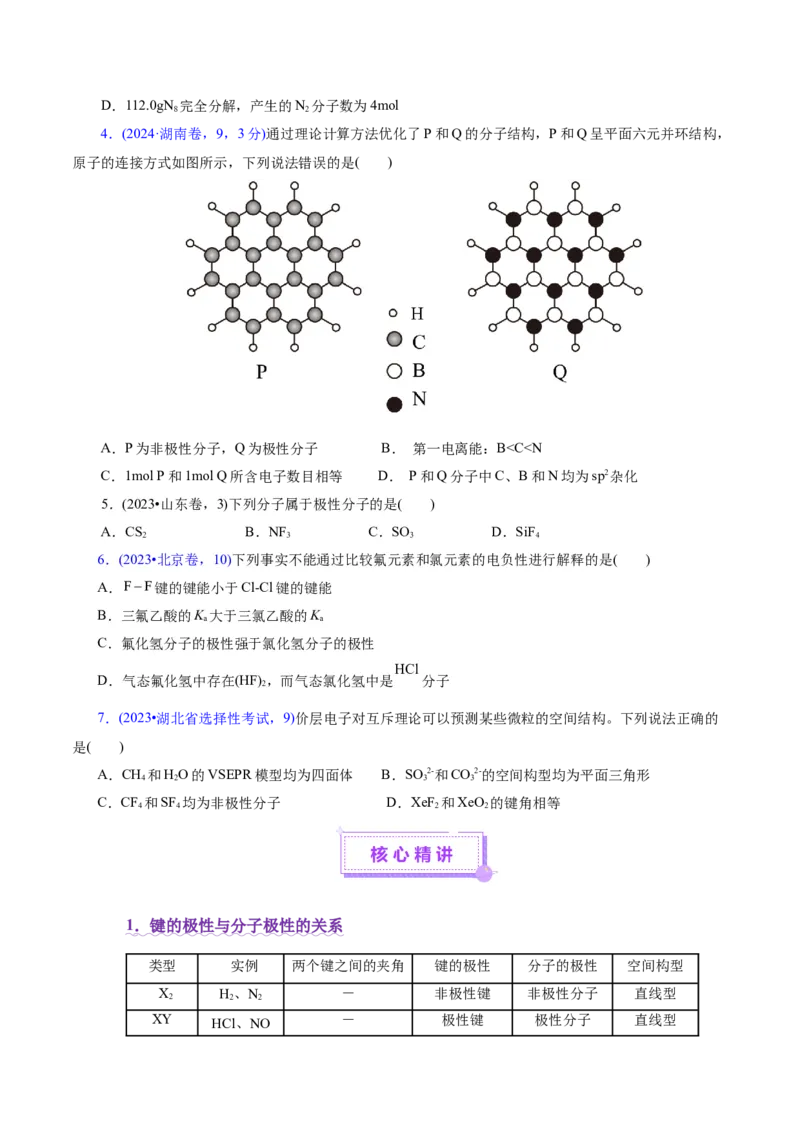
4.(2024·湖南卷,9,3分)通过理论计算方法优化了P和Q的分子结构,P和Q呈平面六元并环结构,
原子的连接方式如图所示,下列说法错误的是( )
A.P为非极性分子,Q为极性分子 B. 第一电离能:B离子晶体>分子晶体,如:金刚石>NaCl>Cl ;金属晶体>分子晶
2
体,如:Na>Cl 。(金属晶体熔、沸点有的很高,如钨、铂等,有的则很低,如汞等)
2
共价晶体 →→,如:金刚石>石英>晶体硅
一般地说,阴阳离子的电荷数越多,离子半径越小,离子键越强,晶格能
离子晶体
越大,熔、沸点就越高。如:MgO>MgCl ,NaCl>CsCl
2
金属离子半径越小,离子所带电荷数越多,其形成的金属键越强,金属单
金属晶体
质的熔、沸点就越高,如Al>Mg>Na
①分子间作用力越大,物质的熔、沸点越高;具有分子间氢键的分子晶体
熔、沸点反常的高。如HO>HTe>HSe>HS
2 2 2 2
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如
SnH >GeH >SiH>CH
4 4 4 4
分子晶体
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔沸
点越高,如CO>N
2
在同分异构体中,一般支链越多,熔、沸点越低,如正戊烷>异戊烷>新
戊烷
3 . 晶体结构的相关计算
(1)晶胞中粒子数目的计算——均摊法
立方体中粒子周围粒子的个数判断(2)晶体微粒与M、ρ之间的关系
若1个晶胞(立方晶胞)中含有x个微粒,则1 mol该晶胞中含有x mol 微粒,其质量为xM g(M为微粒
的相对分子质量);又1个晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3N g,因此有
A
xM=ρa3N 。
A
(3)金属晶体中体心立方堆积、面心立方堆积中的几组公式(设棱长为a)
①面对角线长=a。
②体对角线长=a。
③体心立方堆积4r=a(r为原子半径)。
④面心立方堆积4r=a(r为原子半径)。
(4)空间利用率=。
考向 1 晶体类型及性质的比较
1.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A.SO 和SiO B.CO 和HO C.NaCl和HCl D.CCl 和KCl
3 2 2 2 4
2.下列每组物质发生状态变化所克服的微粒间的相互作用属同种类型是
A.食盐和蔗糖的熔化 B.白磷和硫的熔化
C.氯化铵固体和干冰受热后的气化 D.氧化镁和金属镁的熔化
3.下表所列物质的晶体类型全部正确的一组是( )
共价晶体 离子晶体 分子晶体
A 氯化硅 磷酸 单质硫
B 单晶硅 碳酸氢铵 白磷
C 金刚石 尿素 冰
D 铁 烧碱 冰醋酸
4.(2025·浙江省天域全国名校协作体高三联考)科学家合成了由氮原子组成的N+、N-等高能量微粒,
5 5
它们的结构如图:已知:N+的5个N原子在同一平面上,属于V形结构;N-属五元环结构,结构类似于苯;N 是立方
5 5 8
结构;N 为两个五元环互相垂直连接。下列判断合理的是( )
10
A.NAsF 与NaAsO 中As化合价不同 B.N-中N原子轨道杂化形式有sp2、sp3
5 6 3 4 5
C.N+N-属于离子化合物 D.N-比N+稳定
5 5 5 5
5.(2025·浙江省新阵地教育联盟高三第一次联考)实验室将KF溶入18-冠-6 (结构如图1)的乙腈
(CHCN)溶液中可轻松实现氯的取代,反应过程如图2所示:
3
下列说法不正确的是( )
A.18-冠-6可循环使用
B.KF与18-冠-6形成的化合物熔点比KF低
C.KF与18-冠-6形成化合物的过程体现超分子自组装的特征
D.相同条件下, 比 更快被取代生成相应的氟化物
6.[新考法](2025·四川省绵阳市高三适应性考试) 下,PO 在CHCl 中与臭氧反应生成PO (结
2 3 2 2 4 18
构如图所示),下列说法正确的是( )
A.PO 属于超分子
4 18
B.CHCl 分子空间构型为正四面体形
2 2
C.PO 中含有极性键和非极性键
4 18
D.O 是极性分子,在水中的溶解度大于在CCl 中的溶解度
3 4
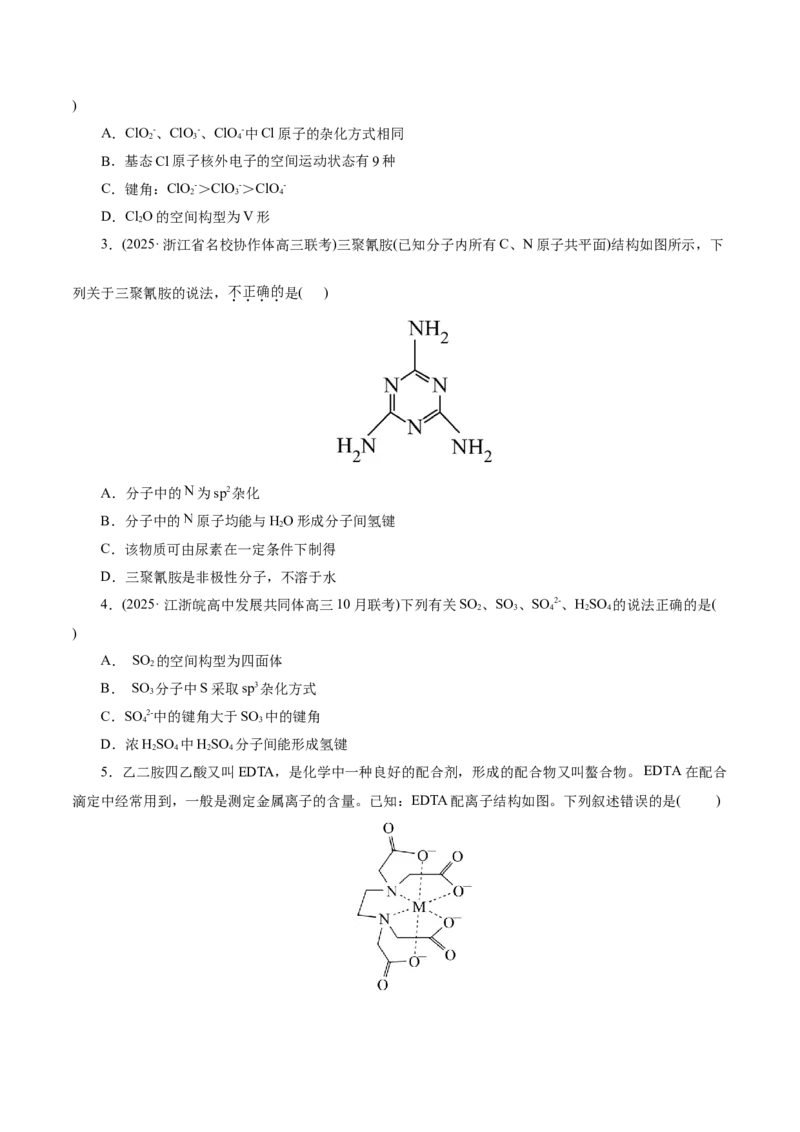
7.[新题型](2025·上海市进才中学高三期中)配合物顺铂[Pt(NH )Cl] (结构如图所示)是临床使用的第
3 2 2
一代铂类抗癌药物。其抗癌机理为在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的
[Pt(NH )(OH)Cl]与DNA结合,破坏DNA的结构,阻止癌细胞增殖。其同分异构体反铂不具有抗癌作用。
3 2下列说法错误的是( )
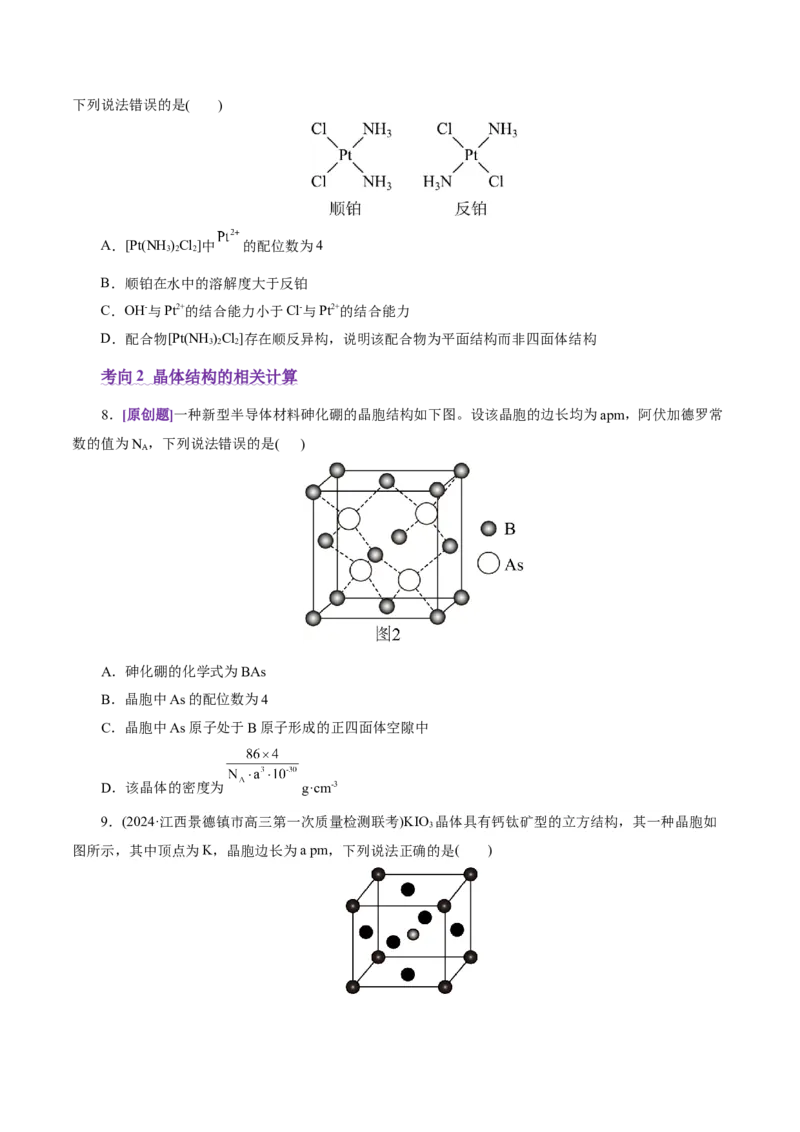
A.[Pt(NH )Cl]中 的配位数为4
3 2 2
B.顺铂在水中的溶解度大于反铂
C.OH-与Pt2+的结合能力小于Cl-与Pt2+的结合能力
D.配合物[Pt(NH )Cl]存在顺反异构,说明该配合物为平面结构而非四面体结构
3 2 2
考向 2 晶体结构的相关计算
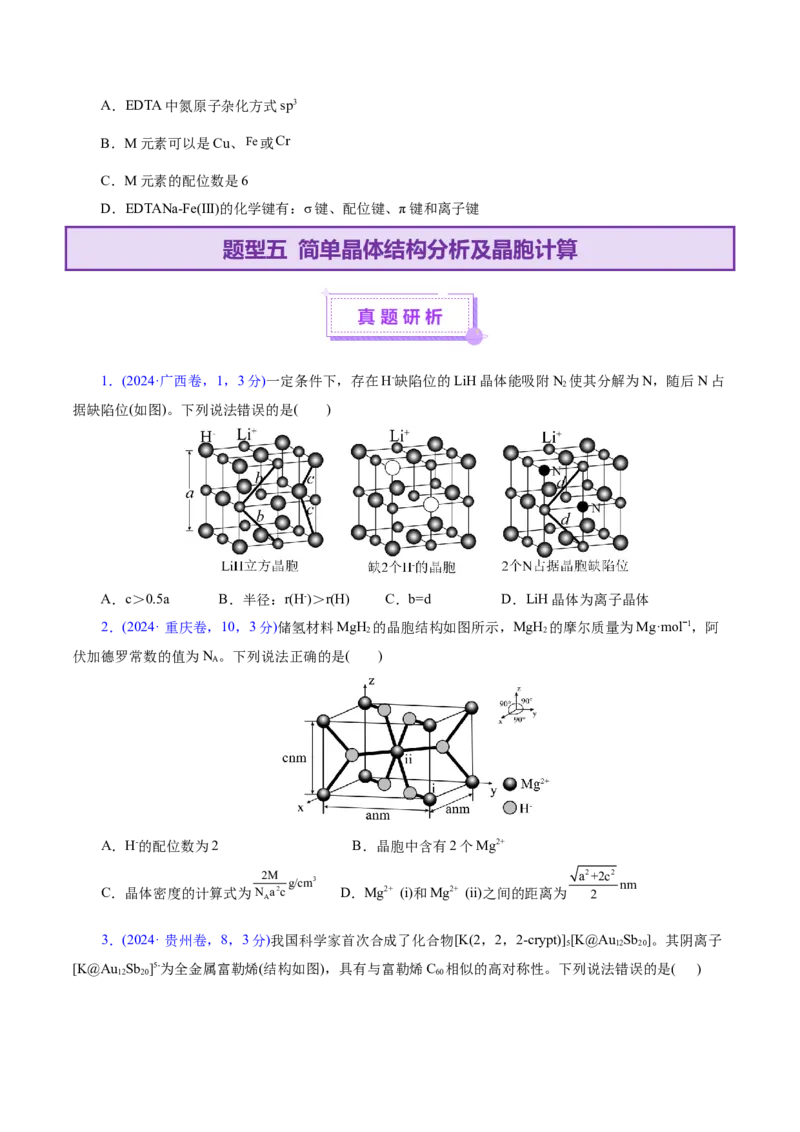
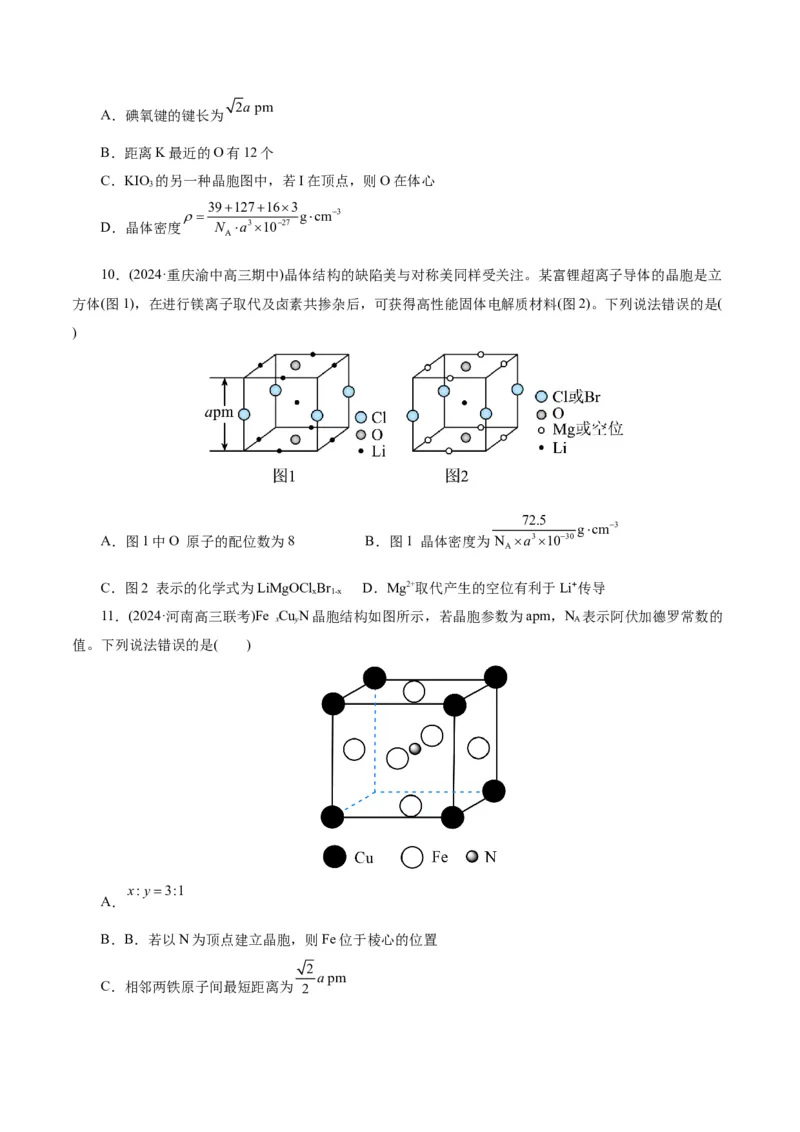
8.[原创题]一种新型半导体材料砷化硼的晶胞结构如下图。设该晶胞的边长均为apm,阿伏加德罗常
数的值为N ,下列说法错误的是( )
A
A.砷化硼的化学式为BAs
B.晶胞中As的配位数为4
C.晶胞中As原子处于B原子形成的正四面体空隙中
D.该晶体的密度为 g·cm-3
9.(2024·江西景德镇市高三第一次质量检测联考)KIO 晶体具有钙钛矿型的立方结构,其一种晶胞如
3
图所示,其中顶点为K,晶胞边长为a pm,下列说法正确的是( )2a pm
A.碘氧键的键长为
B.距离K最近的O有12个
C.KIO 的另一种晶胞图中,若I在顶点,则O在体心
3
39127163
gcm3
D.晶体密度 N a31027
A
10.(2024·重庆渝中高三期中)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立
方体(图1),在进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是(
)
72.5
gcm3
A.图1中O 原子的配位数为8 B.图1 晶体密度为N a31030
A
C.图2 表示的化学式为LiMgOCl Br D.Mg2+取代产生的空位有利于Li 传导
x 1-x
11.(2024·河南高三联考)Fe
x
Cu
y
N晶胞结构如图所示,若晶胞参数为apm,N⁺A 表示阿伏加德罗常数的
值。下列说法错误的是( )
x:y3:1
A.
B.B.若以N为顶点建立晶胞,则Fe位于棱心的位置
2
apm
C.相邻两铁原子间最短距离为 26435614
gcm3
D.晶体密度为 a3N
A
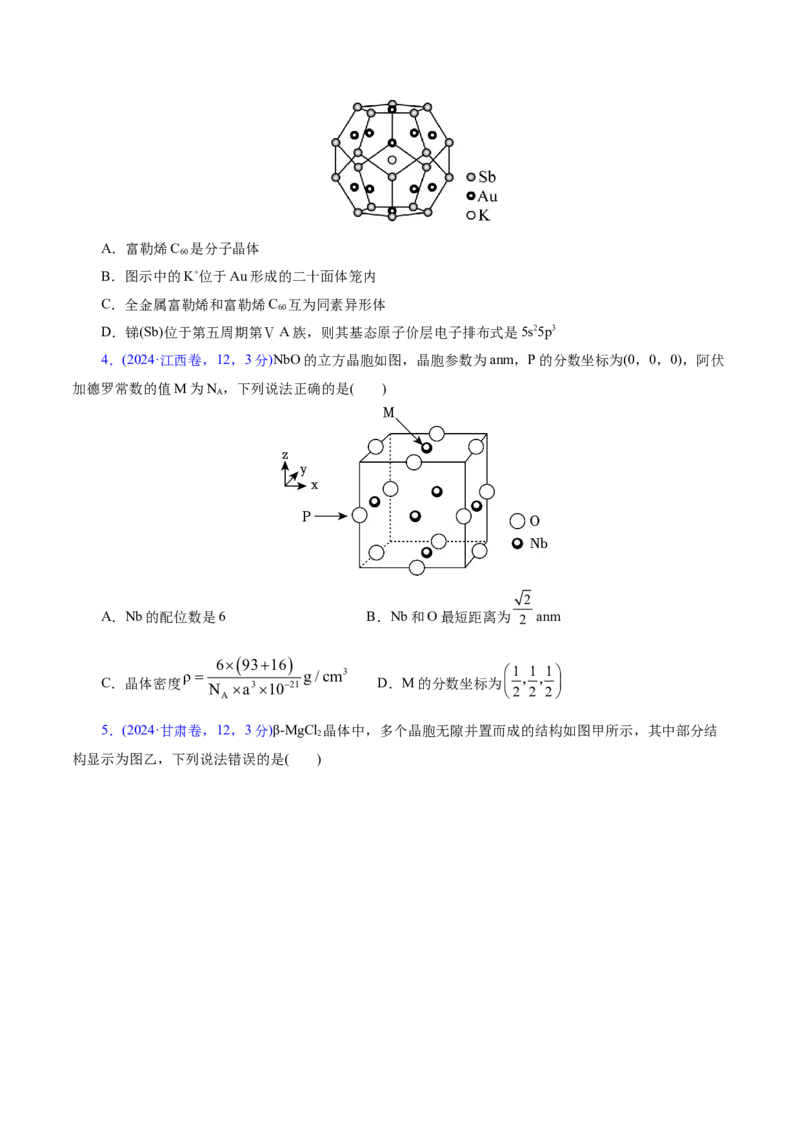
12.砷化镓(GaAs)作为第二代半导体材料的代表,是目前研究最成熟、生产量最大的半导体材料。
GaAs晶胞结构如图所示,晶胞边长为apm,下列说法正确的是( )
A.GaAs属于离子晶体
B.基态砷原子价电子排布图为
C.As的配位数为4
5.81036
D.该晶体密度为
g/cm3
N a3
A