文档内容
专题 13 物质的反应和转化
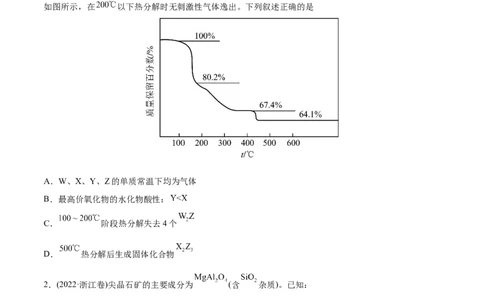
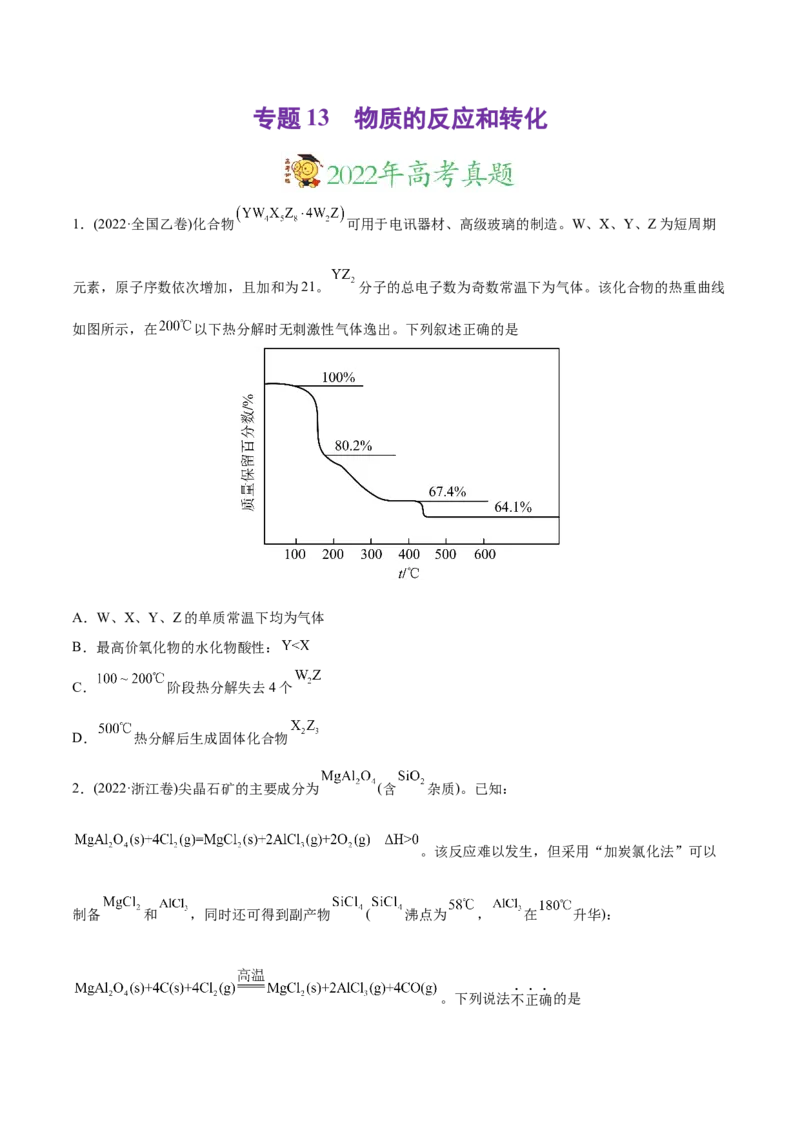
1.(2022·全国乙卷)化合物 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期
元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数常温下为气体。该化合物的热重曲线
如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:
C. 阶段热分解失去4个
D. 热分解后生成固体化合物
2.(2022·浙江卷)尖晶石矿的主要成分为 (含 杂质)。已知:
。该反应难以发生,但采用“加炭氯化法”可以
制备 和 ,同时还可得到副产物 ( 沸点为 , 在 升华):
。下列说法不正确的是A.制备时要保持无水环境
B.输送气态产物的管道温度要保持在 以上
C.氯化时加炭,既增大了反应的趋势,又为氯化提供了能量
D.为避免产生大量 ,反应过程中需保持炭过量
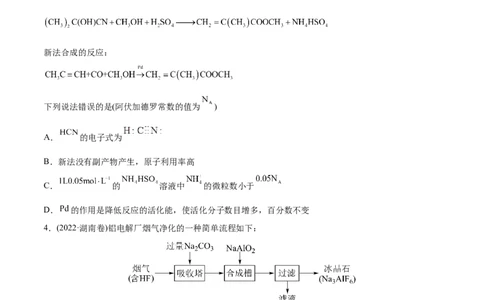
3.(2022·湖南卷)甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为 )
A. 的电子式为
B.新法没有副产物产生,原子利用率高
C. 的 溶液中 的微粒数小于
D. 的作用是降低反应的活化能,使活化分子数目增多,百分数不变
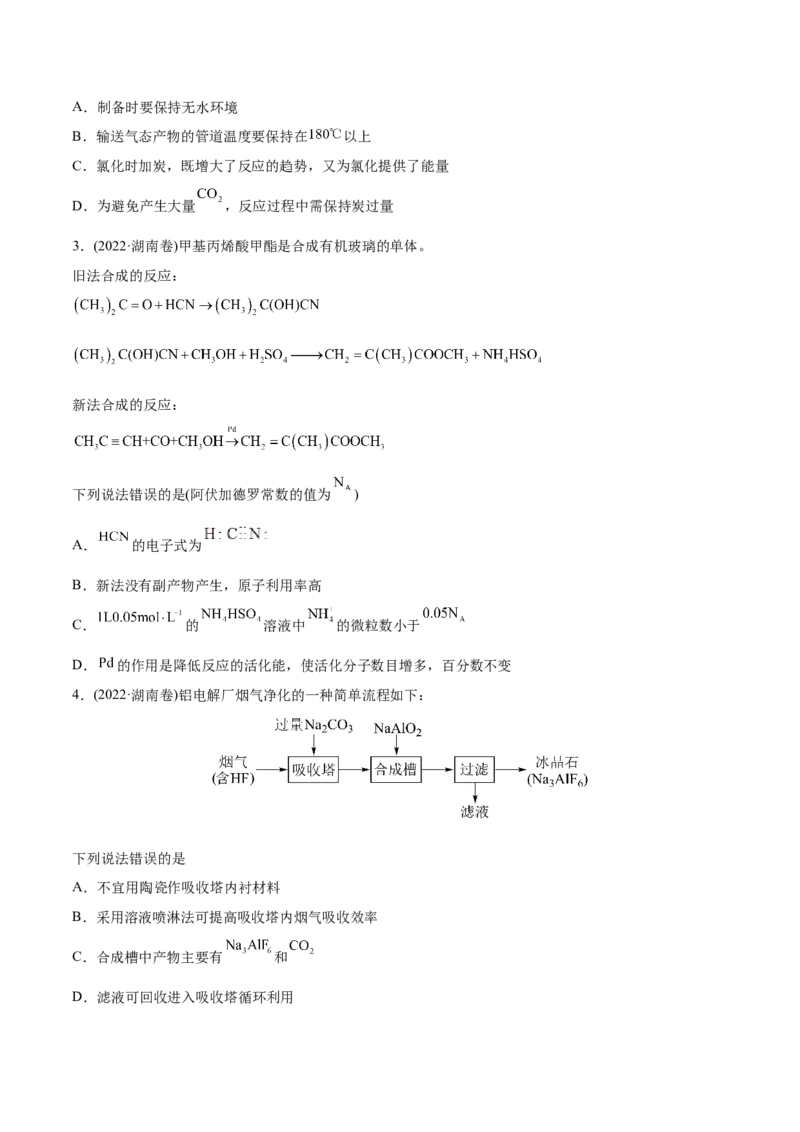
4.(2022·湖南卷)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有 和
D.滤液可回收进入吸收塔循环利用FeCl FeCl Na SO 0.1molL-1
5.(2022·湖南卷)为探究 3的性质,进行了如下实验( 3和 2 3溶液浓度均为 )。
实
操作与现象
验
① 在5mL水中滴加2滴 FeCl 3溶液,呈棕黄色;煮沸,溶液变红褐色。
在 5mL FeCl 3溶液中滴加2滴Na 2 SO 3溶液,变红褐色;
②
K Fe(CN)
再滴加 3 6 溶液,产生蓝色沉淀。
5mL Na SO FeCl
在 2 3溶液中滴加2滴 3溶液,变红褐色;
③ K Fe(CN)
将上述混合液分成两份,一份滴加 3 6 溶液,无蓝色沉淀生;
另一份煮沸,产生红褐色沉淀。
Fe3+
依据上述实验现象,结论不合理的是A.实验①说明加热促进 水解反应
Fe3+
B.实验②说明 既发生了水解反应,又发生了还原反应
Fe3+
C.实验③说明 发生了水解反应,但没有发生还原反应
SO2- Fe3+
D.整个实验说明 3 对 的水解反应无影响,但对还原反应有影响
1.(2022·内蒙古·包钢一中一模)硫元素的几种化合物存在下列转化关系。下列说法正确的是
浓HSO SO NaSO 溶液 NaSO 溶液 S
2 4 2 2 3 2 2 3
A.反应①中生成的SO 具有漂白性,可使溴水褪色
2
B.反应②中若SO 过量,就会生成NaHSO
2 3
C.反应④中生成 S 既是氧化产物,也是还原产物
D.反应④中当消耗 1mol 稀硫酸时,电子转移为4mol
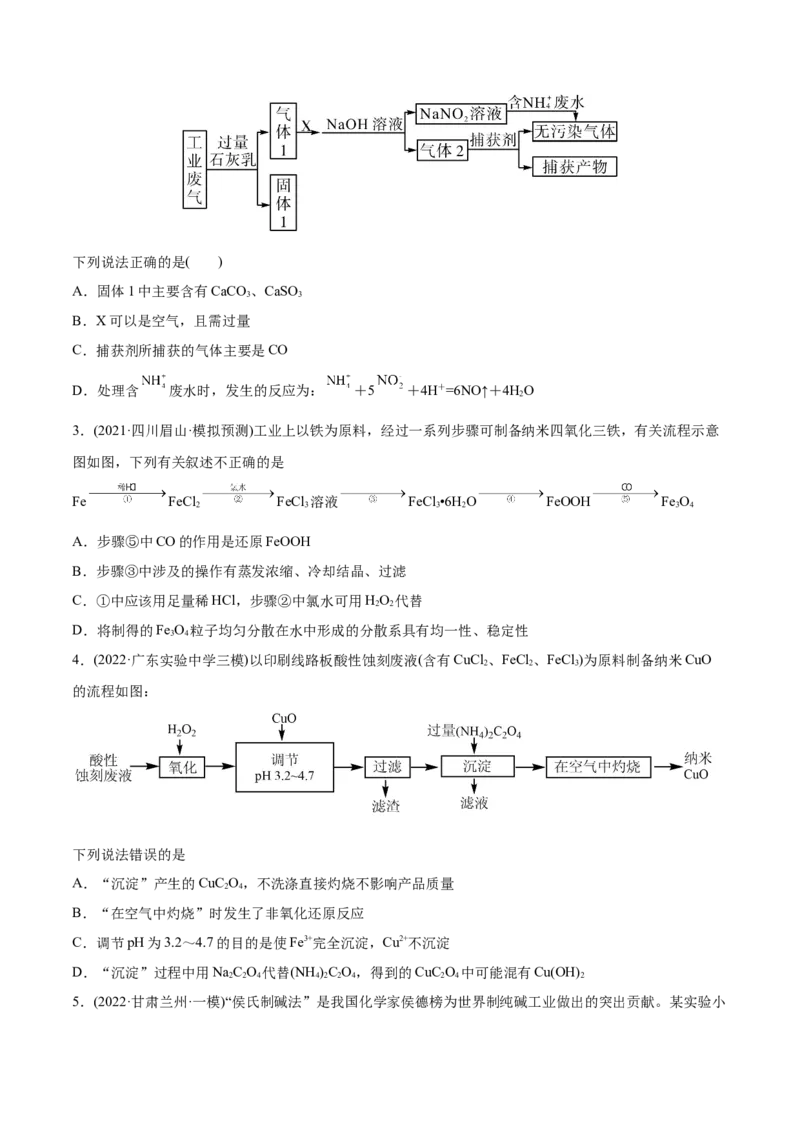
2.(2022·新疆·二模)绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含 废水和
工业废气(主要含N、CO、SO 、NO、CO,不考虑其他成分),设计了如下流程:
2 2 2下列说法正确的是( )
A.固体1中主要含有CaCO 、CaSO
3 3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
D.处理含 废水时,发生的反应为: +5 +4H+=6NO↑+4HO
2
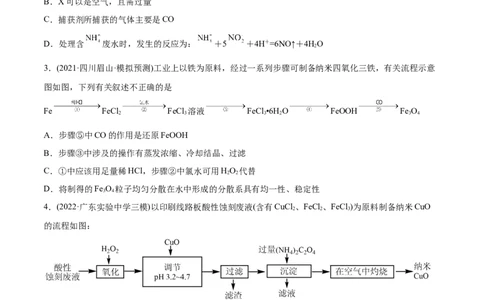
3.(2021·四川眉山·模拟预测)工业上以铁为原料,经过一系列步骤可制备纳米四氧化三铁,有关流程示意
图如图,下列有关叙述不正确的是
Fe FeCl FeCl 溶液 FeCl •6H O FeOOH Fe O
2 3 3 2 3 4
A.步骤⑤中CO的作用是还原FeOOH
B.步骤③中涉及的操作有蒸发浓缩、冷却结晶、过滤
C.①中应该用足量稀HCl,步骤②中氯水可用HO 代替
2 2
D.将制得的Fe O 粒子均匀分散在水中形成的分散系具有均一性、稳定性
3 4
4.(2022·广东实验中学三模)以印刷线路板酸性蚀刻废液(含有CuCl 、FeCl 、FeCl )为原料制备纳米CuO
2 2 3
的流程如图:
下列说法错误的是
A.“沉淀”产生的CuC O,不洗涤直接灼烧不影响产品质量
2 4
B.“在空气中灼烧”时发生了非氧化还原反应
C.调节pH为3.2~4.7的目的是使Fe3+完全沉淀,Cu2+不沉淀
D.“沉淀”过程中用NaC O 代替(NH )C O,得到的CuC O 中可能混有Cu(OH)
2 2 4 4 2 2 4 2 4 2
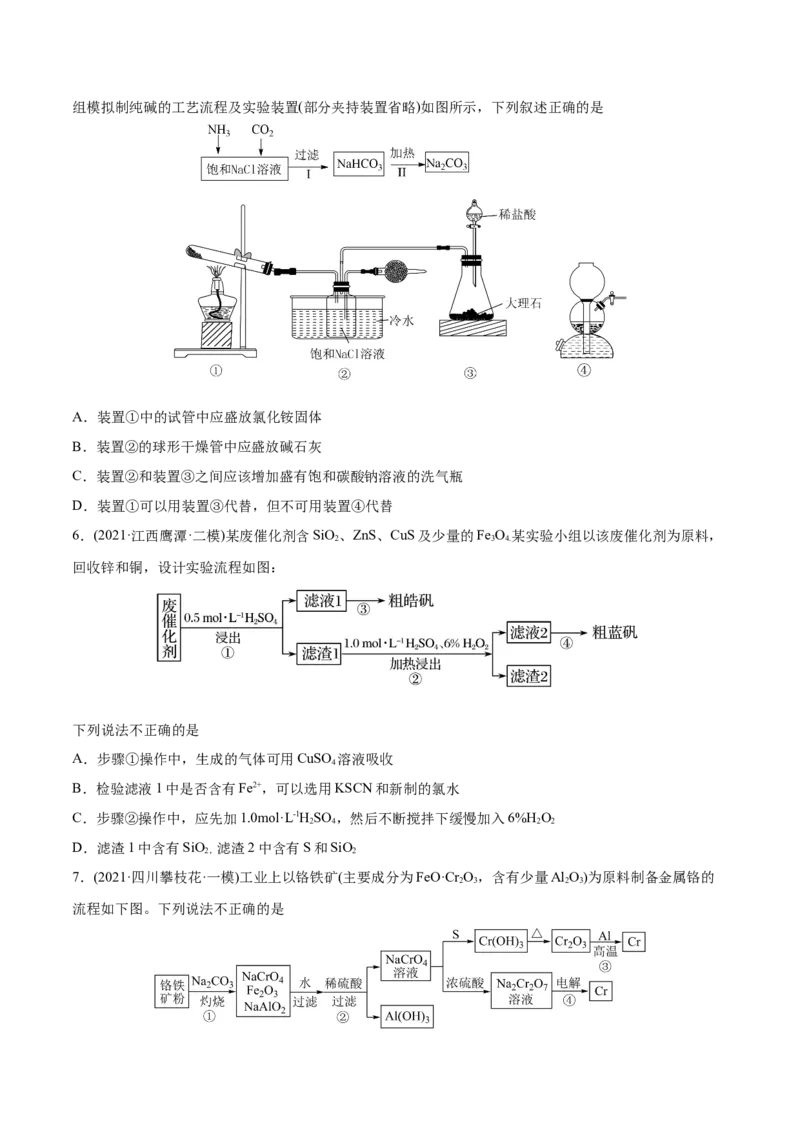
5.(2022·甘肃兰州·一模)“侯氏制碱法”是我国化学家侯德榜为世界制纯碱工业做出的突出贡献。某实验小组模拟制纯碱的工艺流程及实验装置(部分夹持装置省略)如图所示,下列叙述正确的是
A.装置①中的试管中应盛放氯化铵固体
B.装置②的球形干燥管中应盛放碱石灰
C.装置②和装置③之间应该增加盛有饱和碳酸钠溶液的洗气瓶
D.装置①可以用装置③代替,但不可用装置④代替
6.(2021·江西鹰潭·二模)某废催化剂含SiO、ZnS、CuS及少量的Fe O 某实验小组以该废催化剂为原料,
2 3 4.
回收锌和铜,设计实验流程如图:
下列说法不正确的是
A.步骤①操作中,生成的气体可用CuSO 溶液吸收
4
B.检验滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水
C.步骤②操作中,应先加1.0mol·L-1HSO ,然后不断搅拌下缓慢加入6%H O
2 4 2 2
D.滤渣1中含有SiO 滤渣2中含有S和SiO
2, 2
7.(2021·四川攀枝花·一模)工业上以铬铁矿(主要成分为FeO·Cr O,含有少量Al O)为原料制备金属铬的
2 3 2 3
流程如下图。下列说法不正确的是A.①中需持续吹入空气作氧化剂
B.②中需加入过量稀硫酸
C.③中发生了铝热反应
D.④中阴极反应生成1molCr时,消耗7molH+
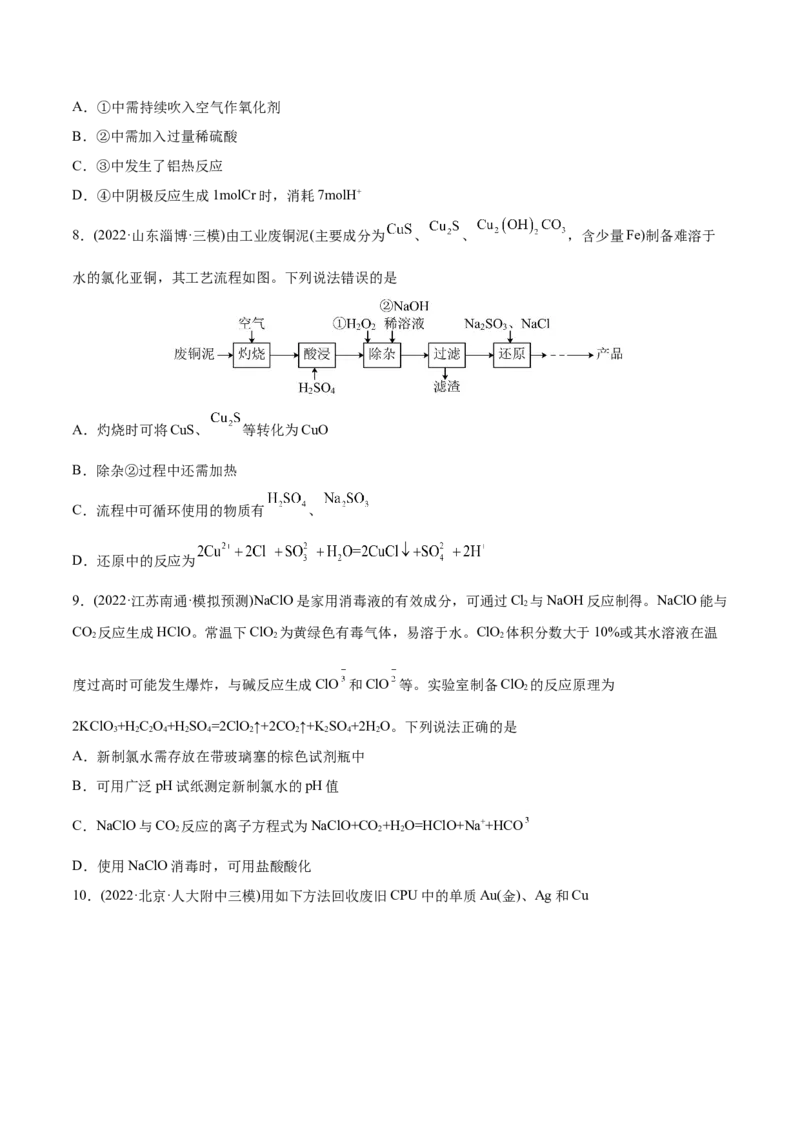
8.(2022·山东淄博·三模)由工业废铜泥(主要成分为 、 、 ,含少量Fe)制备难溶于
水的氯化亚铜,其工艺流程如图。下列说法错误的是
A.灼烧时可将CuS、 等转化为CuO
B.除杂②过程中还需加热
C.流程中可循环使用的物质有 、
D.还原中的反应为
9.(2022·江苏南通·模拟预测)NaClO是家用消毒液的有效成分,可通过Cl 与NaOH反应制得。NaClO能与
2
CO 反应生成HClO。常温下ClO 为黄绿色有毒气体,易溶于水。ClO 体积分数大于10%或其水溶液在温
2 2 2
度过高时可能发生爆炸,与碱反应生成ClO 和ClO 等。实验室制备ClO 的反应原理为
2
2KClO+H C O+H SO =2ClO ↑+2CO ↑+K SO +2H O。下列说法正确的是
3 2 2 4 2 4 2 2 2 4 2
A.新制氯水需存放在带玻璃塞的棕色试剂瓶中
B.可用广泛pH试纸测定新制氯水的pH值
C.NaClO与CO 反应的离子方程式为NaClO+CO +H O=HClO+Na++HCO
2 2 2
D.使用NaClO消毒时,可用盐酸酸化
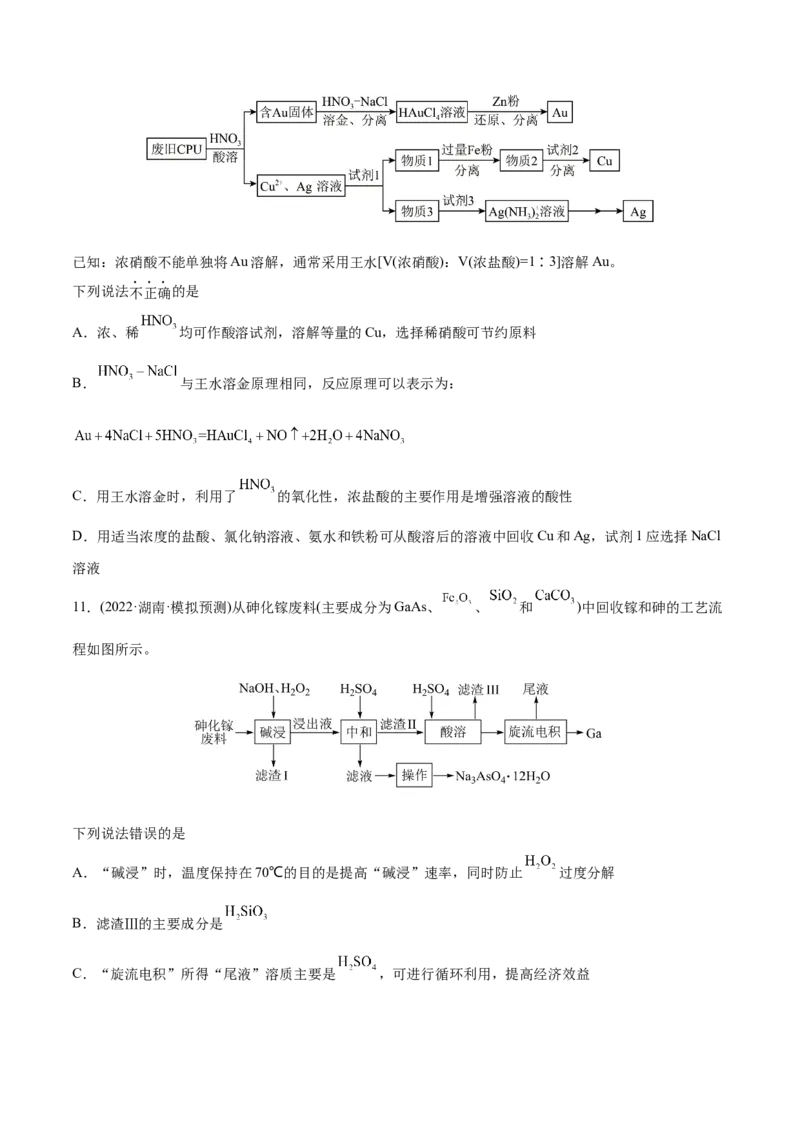
10.(2022·北京·人大附中三模)用如下方法回收废旧CPU中的单质Au(金)、Ag和Cu已知:浓硝酸不能单独将Au溶解,通常采用王水[V(浓硝酸):V(浓盐酸)=1∶3]溶解Au。
下列说法不正确的是
A.浓、稀 均可作酸溶试剂,溶解等量的Cu,选择稀硝酸可节约原料
B. 与王水溶金原理相同,反应原理可以表示为:
C.用王水溶金时,利用了 的氧化性,浓盐酸的主要作用是增强溶液的酸性
D.用适当浓度的盐酸、氯化钠溶液、氨水和铁粉可从酸溶后的溶液中回收Cu和Ag,试剂1应选择NaCl
溶液
11.(2022·湖南·模拟预测)从砷化镓废料(主要成分为GaAs、 、 和 )中回收镓和砷的工艺流
程如图所示。
下列说法错误的是
A.“碱浸”时,温度保持在70℃的目的是提高“碱浸”速率,同时防止 过度分解
B.滤渣Ⅲ的主要成分是
C.“旋流电积”所得“尾液”溶质主要是 ,可进行循环利用,提高经济效益D.得到 的操作为直接蒸干