文档内容
专题 14 元素及其化合物知识的综合应用
1.(2022·浙江·高考真题)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到 ,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
(4)设计实验,检验尾气中相对活泼的2种气体_______。
【答案】(1) Ba、Cu、O BaCu O
3 4
(2)HCl、HSO
2 4
(3) 2NH +BaCu O Ba(OH) +3Cu+N +2H O BaCu O+12NH HO=3Cu(NH ) +Ba2++8OH-
3 3 4 2 2 2 3 4 3 2 3
+8H O
2
(4)将湿润的红色石蕊试纸置尾气出口,若变蓝,说明尾气中有NH 。将尾气通入冷的集气瓶中,若有液珠,
3
说明有HO
2
【解析】化合物X由三种元素组成,在加热条件下和足量氨气反应生成固体混合物A,A和盐酸反应生成
0.960g紫红色固体应该是Cu,无色溶液B中加入0.015mol稀硫酸生成白色沉淀1.165g应该是BaSO,无
4
色溶液C中加入足量BaCl 溶液生成白色沉淀2.330g是BaSO,据此解答。
2 4
(1)根据以上分析可知Cu的物质的量是0.96g÷64g/mol=0.015mol,第一次生成硫酸钡的物质的量是
1.165g÷233g/mol=0.005mol,第二次生成硫酸钡的物质的量是2.33g÷233g/mol=0.01mol,因此1.965gX中
一定含有0.96gCu,Ba的质量是0.005mol×137g/mol=0.685g,二者质量之和是1.645g<1.965g,相差
0.32g,根据原子守恒可知应该是氧元素,物质的量是0.32g÷16g/mol=0.02mol,则Ba、Cu、O三种原子的
个数之比是1:3:4,所以组成X的三种元素为Ba、Cu、O,X的化学式为BaCu O。
3 4(2)根据氯原子原子守恒以及溶液C仍然能与氯化钡反应生成硫酸钡可知溶液C的溶质组成为HCl、
HSO 。
2 4
(3)①反应中Cu元素化合价降低,得到电子,则氨气中氮元素化合价升高,被氧化生成氮气,根据原子守
恒可知由X到A的化学方程式为2NH +BaCu O Ba(OH) +3Cu+N +2H O。
3 3 4 2 2 2
②X难溶于水,但可溶于氨水中,说明有Cu(NH ) 生成,所以该反应的离子方程式为BaCu O+12NH
3 3 4 3
HO=3Cu(NH ) +Ba2++8OH-+8H O。
2 3 2
(4)反应中氨气可能过量,高温下水是气态,氮气性质稳定,所以需要检验的是氨气和水蒸气,实验方案为:
将湿润的红色石蕊试纸置尾气出口,若变蓝,说明尾气中有NH 。将尾气通入冷的集气瓶中,若有液珠,
3
说明有HO。
2
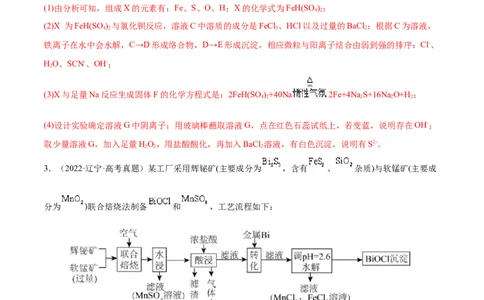
2.(2022·浙江·高考真题)化合物X由4种元素组成。某兴趣小组按如图流程进行实验:
请回答:
(1)组成X的元素有______,X的化学式为______。
(2)溶液C中溶质的成分是______(用化学式表示);根据C→D→E的现象,给出相应微粒与阳离子结合由弱
到强的排序______。
(3)X与足量Na反应生成固体F的化学方程式是______。
(4)设计实验确定溶液G中阴离子______。
【答案】(1) Fe、S、O、H FeH(SO )
4 2
(2) FeCl 、HCl、BaCl Cl-、HO、SCN-、OH-
3 2 2(3)2FeH(SO )+40Na 2Fe+4Na S+16Na O+H
4 2 2 2 2
(4)用玻璃棒蘸取溶液G,点在红色石蕊试纸上,若变蓝,说明存在OH-;取少量溶液G,加入足量HO,
2 2
用盐酸酸化,再加入BaCl 溶液,有白色沉淀,说明有S2-
2
【解析】X形成水溶液,与氯化钡反应生产白色沉淀,且沉淀不与盐酸反应说明生产硫酸钡,说明X含有
硫酸根,溶液加入KSCN变红说明含有Fe3+,B为4.66g则为0.02mol硫酸钡,说明X含有0.02mol的硫酸
根,H中为Fe单质,即为0.01mol,X中含有0.01molFe,由此可知X中应含有0.01的H,据此分析解题。
(1)由分析可知,组成X的元素有:Fe、S、O、H;X的化学式为FeH(SO );
4 2
(2)X 为FeH(SO ) 与氯化钡反应,溶液C中溶质的成分是FeCl 、HCl以及过量的BaCl ;根据C为溶液,
4 2 3 2
铁离子在水中会水解,C→D形成络合物,D→E形成沉淀,相应微粒与阳离子结合由弱到强的排序:Cl-、
HO、SCN-、OH-;
2
(3)X与足量Na反应生成固体F的化学方程式是:2FeH(SO )+40Na 2Fe+4Na S+16Na O+H;
4 2 2 2 2
(4)设计实验确定溶液G中阴离子:用玻璃棒蘸取溶液G,点在红色石蕊试纸上,若变蓝,说明存在OH-;
取少量溶液G,加入足量HO,用盐酸酸化,再加入BaCl 溶液,有白色沉淀,说明有S2-。
2 2 2
3.(2022·辽宁·高考真题)某工厂采用辉铋矿(主要成分为 ,含有 、 杂质)与软锰矿(主要成
分为 )联合焙烧法制备 和 ,工艺流程如下:
已知:①焙烧时过量的 分解为 , 转变为 ;
②金属活动性: ;
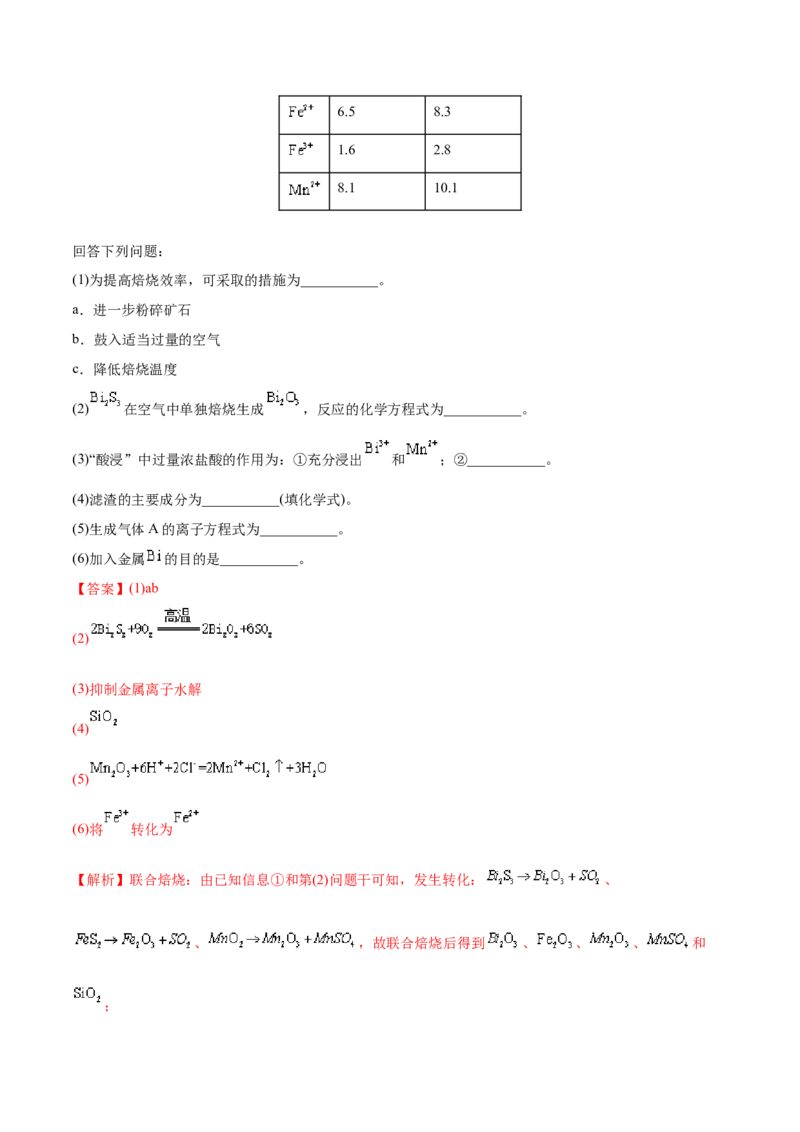
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀 完全沉淀6.5 8.3
1.6 2.8
8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为___________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2) 在空气中单独焙烧生成 ,反应的化学方程式为___________。
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出 和 ;②___________。
(4)滤渣的主要成分为___________(填化学式)。
(5)生成气体A的离子方程式为___________。
(6)加入金属 的目的是___________。
【答案】(1)ab
(2)
(3)抑制金属离子水解
(4)
(5)
(6)将 转化为
【解析】联合焙烧:由已知信息①和第(2)问题干可知,发生转化: 、
、 ,故联合焙烧后得到 、 、 、 和
;水浸: 进入滤液,滤渣为 、 、 和 ;
酸浸:加入过量浓盐酸后, 和 发生转化: 、 ,因 有氧化性,
会与浓盐酸发生氧化还原反应: ,气体A为 ,滤渣主要为不
溶于浓盐酸的 ,滤液中金属离子为 ;
第(4)(5)问转化:由已知信息②知, 的金属活动性强于 ,且调pH=2.6时 和 进入滤液,可知
加入金属 的目的是将 还原为 。
(1)a.联合焙烧时,进一步粉碎矿石,可以增大矿石与空气的接触面积,能够提高焙烧效率,选项a符合题
意;
b.鼓入适当过量的空气有利于矿石充分反应,选项b符合题意;
c.降低焙烧温度,反应速率减慢,不利于提高焙烧效率,选项c不符合题意;
答案选ab;
(2) 在空气中单独焙烧生成 ,根据原子守恒可知还应生成 ,结合得失电子守恒,反应的化学
方程式为 ;
(3)加入浓盐酸后,溶液中含有的离子主要为 、 、 、 、 ,而酸浸后取滤液进行转化,故
要防止金属离子水解生成沉淀,进入滤渣,造成制得的 产率偏低;
(4)滤渣主要为不溶于浓盐酸的 ,答案为 ;
(5)因 有氧化性,会与浓盐酸发生氧化还原反应: ;
(6)由已知信息③知,调pH=2.6时, 会水解生成 沉淀,但 还没开始沉淀,故要将 转
化为 ,在调 后获得含 的滤液,为了不引入新的杂质,加入 作还原剂。4.(2022·河北·高考真题)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
颜料。工艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程式
为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和_______(填化学式,不
引入杂质)。
【答案】(1) Fe O SiO
2 3 2
(2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
(3)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(4)蒸发浓缩、冷却结晶、过滤洗涤
(5) +2; Fe(NH )Fe(CN) +ClO-+2H+=Fe(NH)Fe(CN) +H O+Cl-+
4 2 6 4 6 2
(6) H O NH ·H O
2 2 3 2
【解析】已知黄铁矿高温煅烧生成Fe O,反应原理为:4FeS+11O 2Fe O+8SO,故产生的红渣主要
2 3 2 2 2 3 2
成分为Fe O 和SiO,将红渣粉碎后加入足量的50%的HSO 溶液加热充酸浸,反应原理为:
2 3 2 2 4
Fe O+3H SO =Fe (SO )+3H O,过滤出滤渣①,主要成分为SiO,向滤液中加入黄铁矿进行还原,将
2 3 2 4 2 4 3 2 2Fe3+还原为Fe2+,由(3)小问可知不生成S沉淀,则硫元素被氧化为 ,反应原理为:14Fe3+
+FeS +8H O=15Fe2++2 +16H+,然后进行工序①为蒸发浓缩、冷却结晶,得到FeSO 晶体和母液主要含
2 2 4
有FeSO 溶液和HSO ,加水溶解FeSO 晶体,向所得溶液中加入(NH )SO 、K[Fe(CN) ]并用HSO 调节
4 2 4 4 4 2 4 4 6 2 4
溶液的pH为3,进行沉铁过程,反应原理为:Fe2++2 +[Fe(CN)]3-=Fe(NH)Fe(CN) ↓,然后过滤出沉淀,
6 4 2 6
洗涤后加入HSO 和NaClO 进行氧化步骤,反应原理为:6Fe(NH )Fe(CN) +
2 4 3 4 2 6
+6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ,过滤、洗涤干燥即制得Fe(NH )Fe(CN) ,据此分析解题。
4 6 2 4 6
(1)由分析可知,红渣的主要成分为:Fe O,滤渣①的主要成分为:SiO,故答案为:Fe O;SiO;
2 3 2 2 3 2
(2)黄铁矿研细的主要目的是增大固液接触面积,加快反应速率,提高黄铁矿的利用率,故答案为:增大固
液接触面积,加快反应速率,提高黄铁矿的利用率;
(3)由分析可知,还原工序中,不产生S单质沉淀,则硫元素被氧化为 ,反应原理为:14Fe3+
+FeS +8H O=15Fe2++2 +16H+,故化学方程式为:7Fe (SO )+FeS +8H O=15FeSO +8H SO ,故答案为:
2 2 2 4 3 2 2 4 2 4
7Fe (SO )+FeS +8H O=15FeSO +8H SO ;
2 4 3 2 2 4 2 4
(4)由分析可知,工序①的名称为蒸发浓缩、冷却结晶、过滤洗涤,所得母液主要含有FeSO 溶液和HSO
4 2 4
可以循环利用,故答案为:蒸发浓缩、冷却结晶、过滤洗涤;
(5)沉铁工序中产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,由分析可知,
4 2 6 6
氧化工序所发生的离子方程式为:6Fe(NH )Fe(CN) + +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ,故答
4 2 6 4 6 2
案为:+2;6Fe(NH )Fe(CN) + +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ;
4 2 6 4 6 2
(6)由分析可知,还原工序所得的滤液中主要含有FeSO 溶液和HSO ,向滤液中先加入一定量的HO 溶液
4 2 4 2 2
将Fe2+完全氧化为Fe3+,在向氧化后的溶液中加入氨水至不再产生沉淀为止,过滤洗涤,对沉淀进行灼烧,
即可制得Fe O·x H O和(NH )SO ,故所需要加入的试剂为HO 和NH ·H O,故答案为:HO;
2 3 2 4 2 4 2 2 3 2 2 2
NH ·H O。
3 2
5.(2022·广东·高考真题)稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,稀土
离子保持 价不变; 的 , 开始溶解时的pH为8.8;有关金属离子
沉淀的相关pH见下表。
离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,可提
高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两位有效数
字)。
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 。
①还原 和 熔融盐制备 时,生成1mol 转移_______ 电子。
② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为_______。【答案】(1)Fe2+
(2) 4.7 pH<6.2
(3)4.0 10-4
(4) 加热搅拌可加快反应速率 冷却结晶
(5)MgSO
4
(6) 15 O +4e-+2H O=4OH-
2 2
【解析】由流程可知,该类矿(含铁、铝等元素)加入酸化MgSO 溶液浸取,得到浸取液中含有 、
4
、 、 、 、 等离子,经氧化调pH使 、 形成沉淀,经过滤除去,滤液1中含
有 、 、 等离子,加入月桂酸钠,使 形成 沉淀,滤液2主要含有
MgSO 溶液,可循环利用,滤饼加盐酸,经加热搅拌溶解后,再冷却结晶,析出月桂酸,再固液分离得到
4
RECl 溶液。
3
(1)由分析可知,“氧化调pH”目的是除去含铁、铝等元素的离子,需要将Fe2+氧化为Fe3+,以便后续除杂,
所以化合价有变化的金属离子是Fe2+,故答案为:Fe2+;
(2)由表中数据可知, 沉淀完全的pH为4.7,而 开始沉淀的pH为6.2~7.4,所以为保证 、
沉淀完全,且 不沉淀,要用 溶液调pH至4.7 pH<6.2的范围内,该过程中 发生反应的离
子方程式为 ,故答案为:4.7 pH<6.2; ;
(3)滤液2中 浓度为 ,即0.1125mol/L,根据 ,
若要加入月桂酸钠后只生成 ,而不产生 ,则
= =4.0 10-4 ,故答案为:4.0 10-4;
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是加热搅拌可加快反应速率,故答案为:加热搅拌可加快反应速率;
② “操作X”的结果是分离出月桂酸,由信息可知,月桂酸 熔点为 ,故“操作X”的过
程为:先冷却结晶,再固液分离,故答案为:冷却结晶;
(5)由分析可知,该工艺中,可再生循环利用的物质有MgSO ,故答案为:MgSO ;
4 4
(6)① 中Y为+3价, 中Pt为+4价,而 中金属均为0价,所以还原 和 熔融盐制备
时,生成1mol 转移15 电子,故答案为:15;
②碱性溶液中,氢氧燃料电池正极发生还原反应,发生的电极反应为O+4e-+2H O=4OH,故答案为:
2 2
O+4e-+2H O=4OH-。
2 2
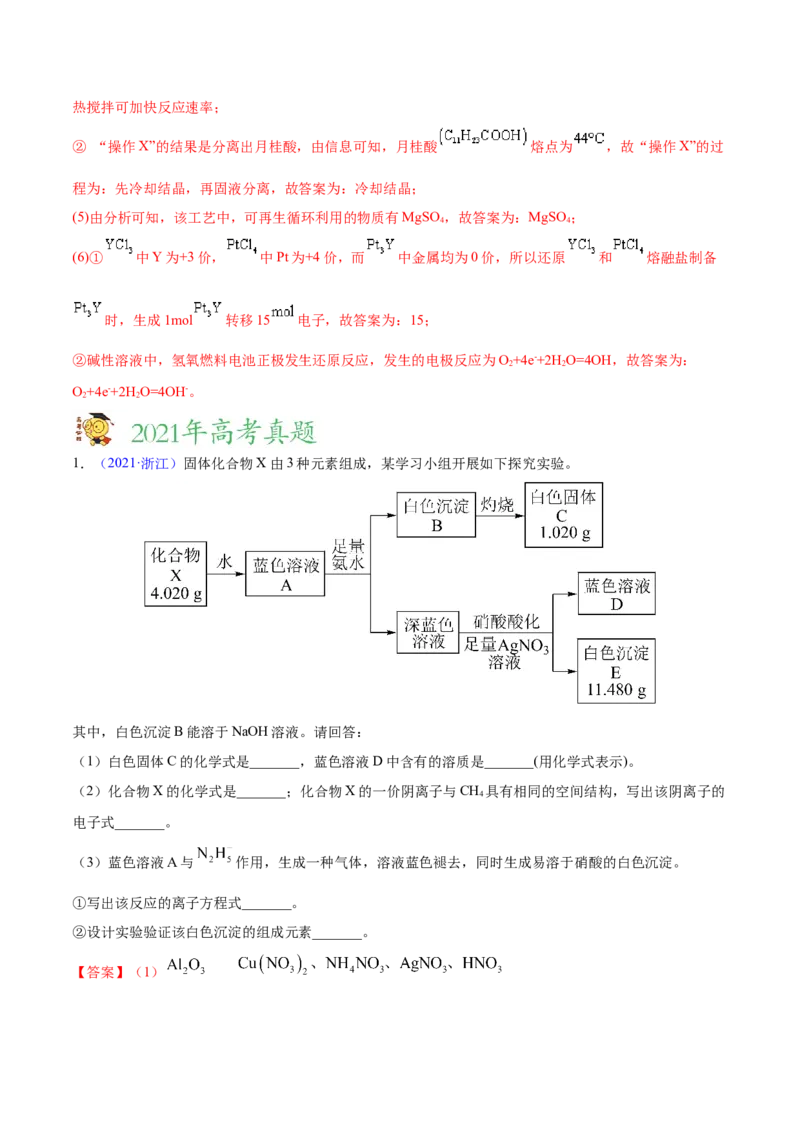
1.(2021·浙江)固体化合物X由3种元素组成,某学习小组开展如下探究实验。
其中,白色沉淀B能溶于NaOH溶液。请回答:
(1)白色固体C的化学式是_______,蓝色溶液D中含有的溶质是_______(用化学式表示)。
(2)化合物X的化学式是_______;化合物X的一价阴离子与CH 具有相同的空间结构,写出该阴离子的
4
电子式_______。
(3)蓝色溶液A与 作用,生成一种气体,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀。
①写出该反应的离子方程式_______。
②设计实验验证该白色沉淀的组成元素_______。
【答案】(1)(2)CuAl Cl
2 8
(3) 将白色沉淀溶于硝酸,得到蓝色溶液,说明有
元素;再向溶液中加入 溶液,有白色沉淀,说明有 元素
【分析】
含有Cu2+的溶液显蓝色,含有[Cu(NH )]2+的溶液显深蓝色,化合物X溶解后得到的溶液A呈现蓝色,且加
3 4
入足量氨水后得到深蓝色溶液,即可推得化合物X中含有Cu2+;向含有Al3+的溶液中加入氨水可用于制备
Al(OH) ,且Al(OH) 为可溶于NaOH溶液的白色沉淀,即可推断白色沉淀B为Al(OH) 沉淀;深蓝色溶液
3 3 3
在加入硝酸酸化的AgNO 溶液后有白色沉淀析出,可推得化合物X中含有Cl-,综上,化合物X中含有
3
Al3+、Cu2+和Cl-。
【解析】
(1)由上述分析可得,白色沉淀D为Al(OH) ,灼烧Al(OH) 得到Al O,故白色固体为Al O;溶液D中
3 3 2 3 2 3
含有的阳离子有Cu2+、 、Ag+、H+,阴离子有 ,故溶液中含有:
,故答案为: ;
。
(2)由图示数据并根据原子守恒可知,4.020g X中含有铝离子物质的量为: =0.02mol,含
有氯离子物质的量为: =0.08mol,由化合物应显电中性可得三种离子物质的量比值为n(Cu2+):
n(Al3+):n(Cl-)=1:2:8,则可得X的化学式为CuAl Cl;阴离子 中Al原子的杂化方式为sp3,空间
2 8结构为正四面体,与CH 相同,其电子式为 ,故答案为:CuAl Cl;
4 2 8
。
(3)①由上述分析可知,蓝色溶液A中含有Al3+、Cu2+和Cl-,与 反应时溶液蓝色褪去,即反应后
溶液中不存在Cu2+,可推测铜元素以沉淀形式析出,反应得到的沉淀为白色且可溶于硝酸,可推测铜元素
在其中不是蓝色且稳定的+2价,而是+1价,即反应过程中Cu元素化合价降低, 中氮元素显-2价,
具有还原性,反应过程中N元素化合价升高生成N,符合反应中有气体产生,根据化合价升降守恒、电荷
2
守恒以及原子守恒和溶液呈酸性可知反应离子方程式为 。
②Cu2+在溶液中显蓝色,CuCl中Cu元素为+1价,能被硝酸氧化为+2价,CuCl与硝酸反应过程中Cl元素
以Cl-形式存在于溶液中,Cl-与AgNO 溶液反应生成不溶于硝酸的白色沉淀,故答案为:将白色沉淀于硝
3
酸,得到蓝色溶液,说明有 元素;再向溶液中加入 溶液,有白色沉淀,说明有 元素。
2.(2021·浙江)某兴趣小组对化合物X开展探究实验。
其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。请回答:(1)组成X的3种元素是______(填元素符号),X的化学式是______。
(2)将固体X加入温热的稀HSO 中,产生气体B,该反应的离子方程式是______。
2 4
(3)步骤I,发生反应的化学方程式是______。
(4)步骤II,某同学未加HO 溶液,发现也会缓慢出现白色浑浊,原因是______。
2 2
(5)关于气体B使品红水溶液褪色的原因,一般认为:B不能使品红褪色,而是B与水反应的生成物使
品红褪色。请设计实验证明______。
【答案】(1)Cu、S、O CuS O
2 6
(2)SO SO + SO ↑
2 2
(3) + Cu(OH) → + 2H O
2 2
(4)SO 与水反应生成HSO ; HSO 能被氧气氧化为HSO ,与BaCl 反应生成BaSO
2 2 3 2 3 2 4 2 4
(5)配制品红无水乙醇溶液(其他非水溶剂亦可),通入SO ,不褪色;品红水溶液中加入亚硫酸钠(亚硫酸
2
氢钠)固体,褪色更快
【分析】
将固体隔绝空气加热,能生成一种固体和一种气体,其中将固体溶于水分成两等分,一份加入盐酸酸化的
氯化钡溶液,能生成白色沉淀,说明固体中有硫酸根的存在,另一份溶液加入适量的NaOH溶液,出现蓝
色悬浊液,加入甘油后能形成绛蓝色溶液,说明固体中存在Cu,则固体A为CuSO ;将气体B通入足量
4
的BaCl 溶液和HO 溶液中,出现白色沉淀,说明该气体可以被HO 氧化,则该气体为SO ,再根据产生
2 2 2 2 2 2
沉淀C和固体X的质量计算固体X的化学式。
【解析】
(1)根据分析,固体X中含有的元素是C、S、O;加入盐酸酸化的氯化钡溶液,生成1.165g硫酸钡沉淀,
则该份硫酸铜的质量为0.005mol,则固体CuSO 的物质的量为0.010mol,质量为1.6g,根据质量守恒的气
4
体SO 的质量为0.640g,该物质中三种元素的质量比m(Cu):m(S):m(O)=0.640g:0.640g:0.960g,则这三种原
2
子的物质的量的比 n(Cu):n(S):n(O)=1:2:6,故固体X的化学式为CuSO;
2 6
(2)根据题目,固体X与温热的稀硫酸反应可以生成SO 气体,根据原子守恒和电荷守恒配平,则该过
2
程的离子方程式为SO SO + SO ↑;
2 2(3)步骤Ⅰ为甘油和氢氧化铜发生反应,反应的化学方程式为 +Cu(OH) →
2
+2H O;
2
(4)步骤Ⅱ中未加入过氧化氢,也可以出现白色沉淀,说明SO 溶于水后可以被空气中的氧气氧化,故答
2
案为:SO 与水反应生成HSO ;HSO 能被氧气氧化为HSO ,与BaCl 反应生成BaSO;
2 2 3 2 3 2 4 2 4
(5)SO 可以使品红溶液褪色,SO 溶液中存在SO 分子和HSO ,欲知道是哪一种物质能够使品红溶液
2 2 2 2 3
褪色,可以利用如下实验验证:配制品红无水乙醇溶液(其他非水溶剂亦可),通入SO ,不褪色;品红
2
水溶液中加入亚硫酸钠(亚硫酸氢钠)固体,褪色更快。
3.(2021·浙江)玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH 2KS+KSO +3H O
2 2 3 2
(x-1)S+KS KS(x=2~6)
2 2 x
S+ K SO KSO
2 3 2 2 3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS和KSO ,则V=______。
2 2 3
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS 和KSO,则
2 x 2 2 3
x=______。(写出计算过程)
【答案】(1)30.0 (2)3
【解析】
(1)根据方程式3S+6KOH 2KS+KSO +3H O可知,3mol S可以和6mol KOH反应,0.48g S的物质的
2 2 3 2
量n=0.015mol,则需要消耗KOH的物质的量n=2n(S)=0.03mol,故需要KOH溶液的体积V= ==0.03L=30.0mL,故答案为30.0;
(2)若S与KOH溶液反应生成KS 和KSO,则反应的化学方程式为(2x+2)S+6KOH
2 x 2 2 3
2KS+K SO+3H O,根据反应方程式有
2 x 2 2 3 2
解得x=3,故答案为3。
4.(2021·海南·高考真题)无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废
铁屑(含有少量碳和 杂质)为原料制备无水 。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和___________。
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
A. 溶液 B. 水 C. 水 D. 溶液
(3)操作②是蒸发结晶,加热的同时通入 的目的是___________。
(4)取少量 晶体,溶于水并滴加 溶液,现象是___________。
(5)反应 的化学方程式为___________。
(6)由 转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂___________,并设计实验验证是该还原剂将 还原___________。
【答案】(1)漏斗
(2)BD
(3)防止水解
(4)溶液变为血红色
(5)
(6) 先加盐酸酸化,再加溶液,产生白色沉淀,则是将还原
【解析】废铁屑(含有少量碳和SiO 杂质)加入盐酸,铁粉反应生成氯化亚铁,过滤除去少量碳和SiO 杂质,
2 2
A(氯化亚铁)加入氧化剂B生成C(氯化铁),蒸发结晶生成 ,通入SOCl 生成FeCl 。
2 3
(1)过滤用到的玻璃仪器有烧杯、玻璃棒和漏斗。
(2)A(氯化亚铁)加入氧化剂B生成C(氯化铁),A、C都引入杂质离子,故选BD。
(3)加热促进氯化铁溶液的水解,会生成氢氧化铁,故加入 的目的是防止水解。
(4)KSCN溶液遇Fe3+变为红色。
(5)根据已知信息氯化亚砜( )熔点-101℃,沸点76℃,易水解,可得 与SOCl 生成
2
FeCl 的化学方程式为 。
3
(6)可能反应中生成的二氧化硫将氯化铁还原为氯化亚铁,若二氧化硫作还原剂,则氧化产物为硫酸盐,故
若加盐酸酸化,再加溶液,产生白色沉淀,则是二氧化硫作还原剂。
5.(2021·北京·高考真题)某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原
性的变化规律。
(1)浓盐酸与MnO 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO
2 2。
①反应的离子方程式是_______。
②电极反应式:
i.还原反应:MnO +2e-+4H+=Mn2++2H O
2 2ii.氧化反应:_______。
③根据电极反应式,分析A中仍存在盐酸和MnO 的原因。
2
i.随c(H+)降低或c(Mn2+)浓度升高,MnO 氧化性减弱。
2
ii.随c(Cl-)降低,_______。
④补充实验证实了③中的分析。
实验操作 试剂 产物
I 较浓HSO 有氯气
2 4
II a 有氯气
III a+b 无氯气
a是_______,b是_______。
(2)利用c(H+)浓度对MnO 氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能
2
与MnO 反应所需的最低c(H+)由大到小的顺序是_______,从原子结构角度说明理由______________。
2
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO 。经实验
2
证实了推测,该化合物是_______。
(4)Ag分别与1mol·L1的盐酸、氢溴酸和氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:_______。
(5)总结:物质氧化性和还原性变化的一般规律是_______。
【答案】(1) MnO +4H+ +2Cl- Mn2++Cl↑ + 2H O 2Cl--2e- =Cl↑ Cl-还原性减弱或Cl 的氧
2 2 2 2 2
化性增强 KCl固体(或浓/饱和溶液) MnSO 固体(或浓/饱和溶液)
4
(2) KCl>KBr>KI Cl、Br、I位于第VIIA族,从上到下电子层数逐渐增加,原子半径逐渐增大,
得电子能力逐渐减弱,阴离子的还原性逐渐增强
(3)AgNO 或Ag SO
3 2 4
(4)比较AgX的溶解度,AgI 溶解度最小,Ag++I-= AgI↓使得Ag还原性增强的最多,使得2Ag+2H+=2Ag++
H↑反应得以发生
2
(5)氧化剂(还原剂)的浓度越大,其氧化性(还原性)越强,还原产物(还原产物)的浓度越大,氧化剂(还原剂)
的氧化性(还原性)越小;还原反应中,反应物浓度越大或生成物浓度越小,氧化剂氧化性越强【解析】(1)①二氧化锰和浓盐酸制氯气的离子方程式为:MnO +4H+ +2Cl- Mn2++Cl↑ + 2H O;②氧化
2 2 2
反应是元素化合价升高,故氧化反应为:2Cl--2e- =Cl↑③反应不能发生也可能是还原剂还原性减弱,或者
2
产生了氧化性更强的氧化剂,故答案为:Cl-还原性减弱或Cl 的氧化性增强④可以从增大氯离子浓度的角
2
度再结合实验II的现象分析,试剂a可以是KCl固体(或浓/饱和溶液);结合实验III的显现是没有氯气,且
实验III也加入了试剂a,那一定是试剂b影响了实验III的现象,再结合原因i可知试剂b是MnSO 固体
4
(或浓/饱和溶液);
(2)非金属性越弱其阴离子的还原性越强,反应时所需的氢离子浓度越小,故顺序是KCl>KBr>KI;其原因
是Cl、Br、I位于第VIIA族,从上到下电子层数逐渐增加,原子半径逐渐增大,得电子能力逐渐减弱,阴
离子的还原性逐渐增强;
(3)根据(1)中的结论推测随Cl-浓度降低导致二氧化锰的氧化性减弱,那么如果进一步降低Cl-浓度降低则可
以导致可以提高溴的氧化性,将Mn2+氧化为MnO ,故答案为:AgNO 或Ag SO ;
2 3 2 4
(4)若要使反应2Ag+2H+=2Ag++ H ↑发生,根据本题的提示可以降低Ag+浓度,对比AgX的溶解度,AgI 溶
2
解度最小,故Ag只与氢碘酸发生置换反应的原因是:比较AgX的溶解度,AgI 溶解度最小,Ag++I-=
AgI↓使得Ag还原性增强的最多,使得2Ag+2H+=2Ag++ H ↑反应得以发生;
2
(5)通过本题可以发现,物质氧化性和还原性还与物质的浓度有关,浓度越大氧化性或者还原性越强,故答
案为:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越强,还原产物(还原产物)的浓度越大,氧化剂(还原
剂)的氧化性(还原性)越小;还原反应中,反应物浓度越大或生成物浓度越小,氧化剂氧化性越强。
6.(2021·北京·高考真题)铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。
资料:
i.钛白粉废渣成分:主要为FeSO ·H O,含少量TiOSO 和不溶物
4 2 4
ii.TiOSO +(x+1)H O TiO·xH O↓+HSO
4 2 2 2 2 4
iii.0.1 mol/L Fe2+生成⇌Fe(OH)
2
,开始沉淀时pH=6.3,完全沉淀时pH=8.3;
0.1 mol/L Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(1)纯化
①加入过量铁粉的目的是_______。
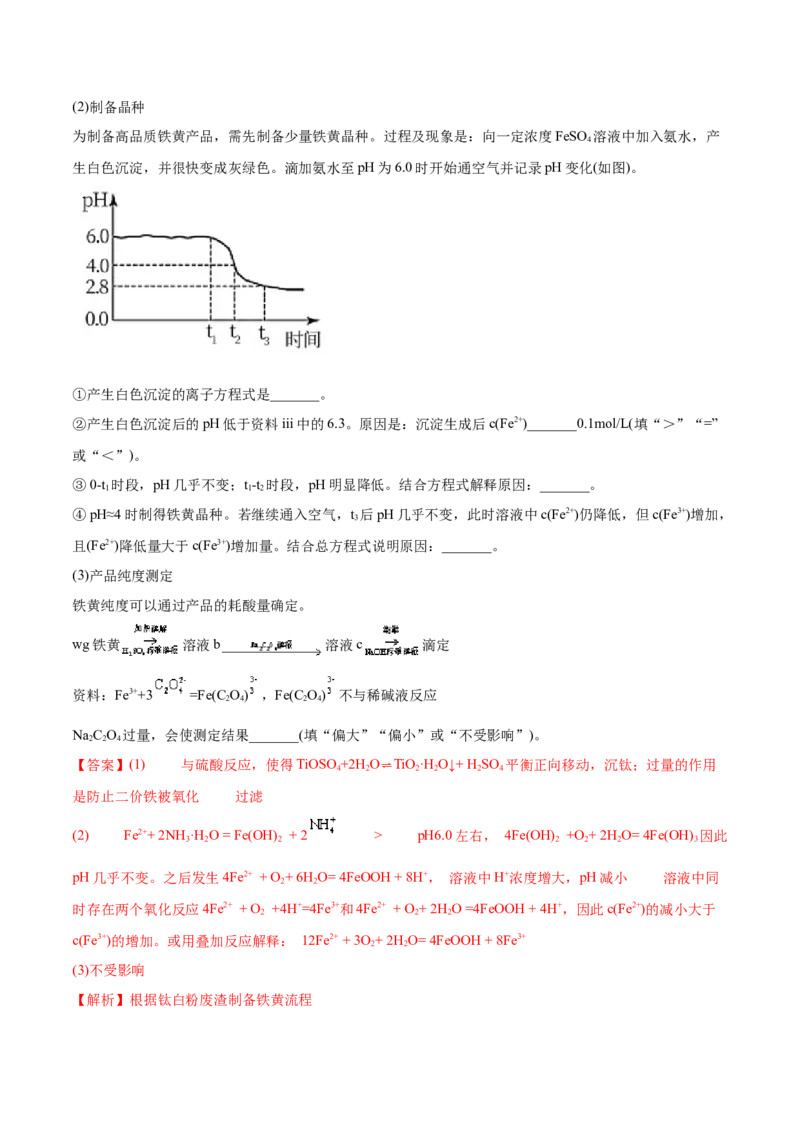
②充分反应后,分离混合物的方法是_______。(2)制备晶种
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO 溶液中加入氨水,产
4
生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如图)。
①产生白色沉淀的离子方程式是_______。
②产生白色沉淀后的pH低于资料iii中的6.3。原因是:沉淀生成后c(Fe2+)_______0.1mol/L(填“>”“=”
或“<”)。
③0-t 时段,pH几乎不变;t-t 时段,pH明显降低。结合方程式解释原因:_______。
1 1 2
④pH≈4时制得铁黄晶种。若继续通入空气,t 后pH几乎不变,此时溶液中c(Fe2+)仍降低,但c(Fe3+)增加,
3
且(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明原因:_______。
(3)产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。
wg铁黄 溶液b 溶液c 滴定
资料:Fe3++3 =Fe(C O) ,Fe(C O) 不与稀碱液反应
2 4 2 4
NaC O 过量,会使测定结果_______(填“偏大”“偏小”或“不受影响”)。
2 2 4
【答案】(1) 与硫酸反应,使得TiOSO
4
+2H
2
O⇌TiO
2
·H
2
O↓+ H
2
SO
4
平衡正向移动,沉钛;过量的作用
是防止二价铁被氧化 过滤
(2) Fe2++ 2NH ·H O = Fe(OH) + 2 > pH6.0左右, 4Fe(OH) +O + 2H O= 4Fe(OH) 因此
3 2 2 2 2 2 3
pH几乎不变。之后发生4Fe2+ + O + 6H O= 4FeOOH + 8H+, 溶液中H+浓度增大,pH减小 溶液中同
2 2
时存在两个氧化反应4Fe2+ + O +4H+=4Fe3+和4Fe2+ + O + 2H O =4FeOOH + 4H+,因此c(Fe2+)的减小大于
2 2 2
c(Fe3+)的增加。或用叠加反应解释: 12Fe2+ + 3O + 2H O= 4FeOOH + 8Fe3+
2 2
(3)不受影响
【解析】根据钛白粉废渣制备铁黄流程和钛白粉废渣成分:FeSO ·H O、TiOSO 及其它难溶物,可知:加入蒸馏水、铁粉纯化后,
4 2 4
TiOSO +2H O TiO·H O↓+HSO ,TiO·H O是沉淀,通过过滤后,得到精制FeSO 溶液,加入氨水和空气
4 2 2 2 2 4 2 2 4
后,FeSO 溶液⇌被氧化成三价铁离子,同时调整PH(0.1mol/LFe2+沉淀为Fe(OH) ,起始的pH为6.3,完全
4 2
沉淀的pH为8.3;0.1mol/LFe3+沉淀为FeOOH,起始的pH:1.5,完全沉淀的pH为2.8)和空气,生成
FeOOH,再经过系列提纯,最终制得FeOOH固体。
(1)与硫酸反应,使得TiOSO
4
+2H
2
O⇌TiO
2
·H
2
O↓+ H
2
SO
4
平衡正向移动,沉钛;过量的作用是防止二价铁被
氧化. 钛白粉废渣成分:FeSO4·H2O、TiOSO4及其它难溶物,充分反应后有沉淀出现,所以分离混合物的
方法是过滤;
(2)pH6.0左右, 4Fe(OH) +O + 2H O= 4Fe(OH) 因此pH几乎不变。之后发生4Fe2+ + O + 6H O= 4FeOOH
2 2 2 3 2 2
+ 8H+, 溶液中H+浓度增大,pH减小.溶液中同时存在两个氧化反应4Fe2+ + O +4H+=4Fe3+和4Fe2+ + O +
2 2
2HO =4FeOOH + 4H+,因此c(Fe2+)的减小大于c(Fe3+)的增加。或用叠加反应解释: 12Fe2+ + 3O + 2H O=
2 2 2
4FeOOH + 8Fe3+
(3)由于Fe3++3C O2- =Fe(C O) ,Fe(C O) 不与稀碱溶液反应, 所以加入的NaC O 过量,则测定结果不
2 4 2 4 3 2 4 3 2 2 4
受影响
1.[2020江苏卷]吸收工厂烟气中的SO ,能有效减少SO 对空气的污染。氨水、ZnO水悬浊液吸收烟气中
2 2
SO 后经O 催化氧化,可得到硫酸盐。
2 2
已知:室温下,ZnSO 微溶于水,Zn(HSO ) 易溶于水;溶液中HSO 、HSO -、SO 2-的物质的量分数随
3 3 2 2 3 3 3
pH的分布如图-1所示。
(1)氨水吸收SO 。向氨水中通入少量SO ,主要反应的离子方程式为___________;当通入SO 至溶
2 2 2液pH=6时,溶液中浓度最大的阴离子是_____________(填化学式)。
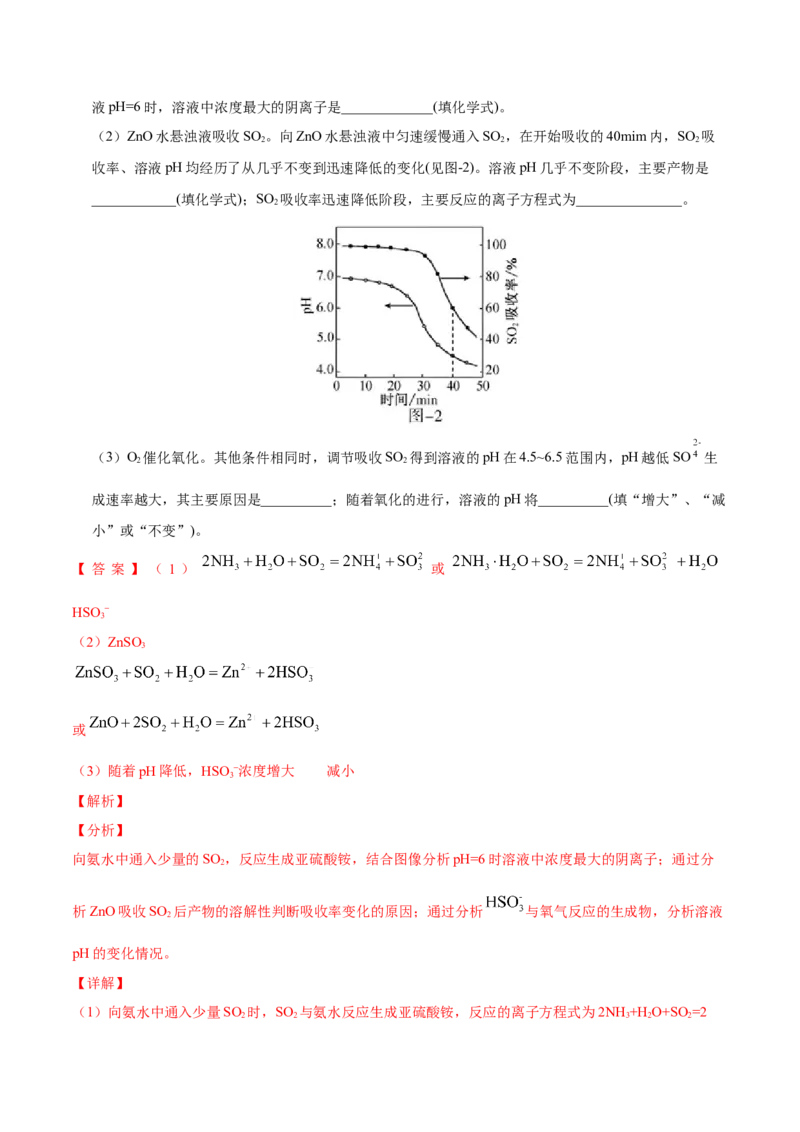
(2)ZnO水悬浊液吸收SO 。向ZnO水悬浊液中匀速缓慢通入SO ,在开始吸收的40mim内,SO 吸
2 2 2
收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是
____________(填化学式);SO 吸收率迅速降低阶段,主要反应的离子方程式为_______________。
2
(3)O 催化氧化。其他条件相同时,调节吸收SO 得到溶液的pH在4.5~6.5范围内,pH越低SO 生
2 2
成速率越大,其主要原因是__________;随着氧化的进行,溶液的pH将__________(填“增大”、“减
小”或“不变”)。
【 答 案 】 ( 1 ) 或
HSO −
3
(2)ZnSO
3
或
(3)随着pH降低,HSO −浓度增大 减小
3
【解析】
【分析】
向氨水中通入少量的SO ,反应生成亚硫酸铵,结合图像分析pH=6时溶液中浓度最大的阴离子;通过分
2
析ZnO吸收SO 后产物的溶解性判断吸收率变化的原因;通过分析 与氧气反应的生成物,分析溶液
2
pH的变化情况。
【详解】
(1)向氨水中通入少量SO 时,SO 与氨水反应生成亚硫酸铵,反应的离子方程式为2NH +H O+SO =2
2 2 3 2 2+ (或2NH ·H O +SO =2 + +H O);根据图-1所示,pH=6时,溶液中不含有亚硫酸,
3 2 2 2
仅含有 和 ,根据微粒物质的量分数曲线可以看出溶液中阴离子浓度最大的是 ;
(2)反应开始时,悬浊液中的ZnO大量吸收SO ,生成微溶于水的ZnSO,此时溶液pH几乎不变;一旦
2 3
ZnO完全反应生成ZnSO 后,ZnSO 继续吸收SO 生成易溶于水的Zn(HSO ),此时溶液pH逐渐变小,SO
3 3 2 3 2 2
的吸收率逐渐降低,这一过程的离子方程式为ZnSO+SO+H O=Zn2++2 (或ZnO+2SO+H O=Zn2++2
3 2 2 2 2
)
(3) 可以经氧气氧化生成 ,这一过程中需要调节溶液pH在4.5~6.5的范围内,pH越低,溶液
中的 的浓度越大,使得催化氧化过程中反应速率越快;随着反应的不断进行,大量的 反应生
成 ,反应的离子方程式为2 +O =2 +2H+,随着反应的不断进行,有大量的氢离子生成,导
2
致氢离子浓度增大,溶液pH减小。
2.[2020浙江7月选考] Ⅰ. 化合物Ⅹ由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝
的气体Y,Y为纯净物;取 ,用含 的盐酸完全溶解得溶液A,将溶液A分成
和 两等份,完成如下实验(白色沉淀C可溶于 溶液):
请回答:
(1)组成X的四种元素是N、H和_______(填元素符号),X的化学式是_________。
(2)溶液B通入过量 得到白色沉淀C的离子方程式是______________。(3)写出一个化合反应(用化学方程式或离子方程式表示)_____________。
要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“ ”相同。
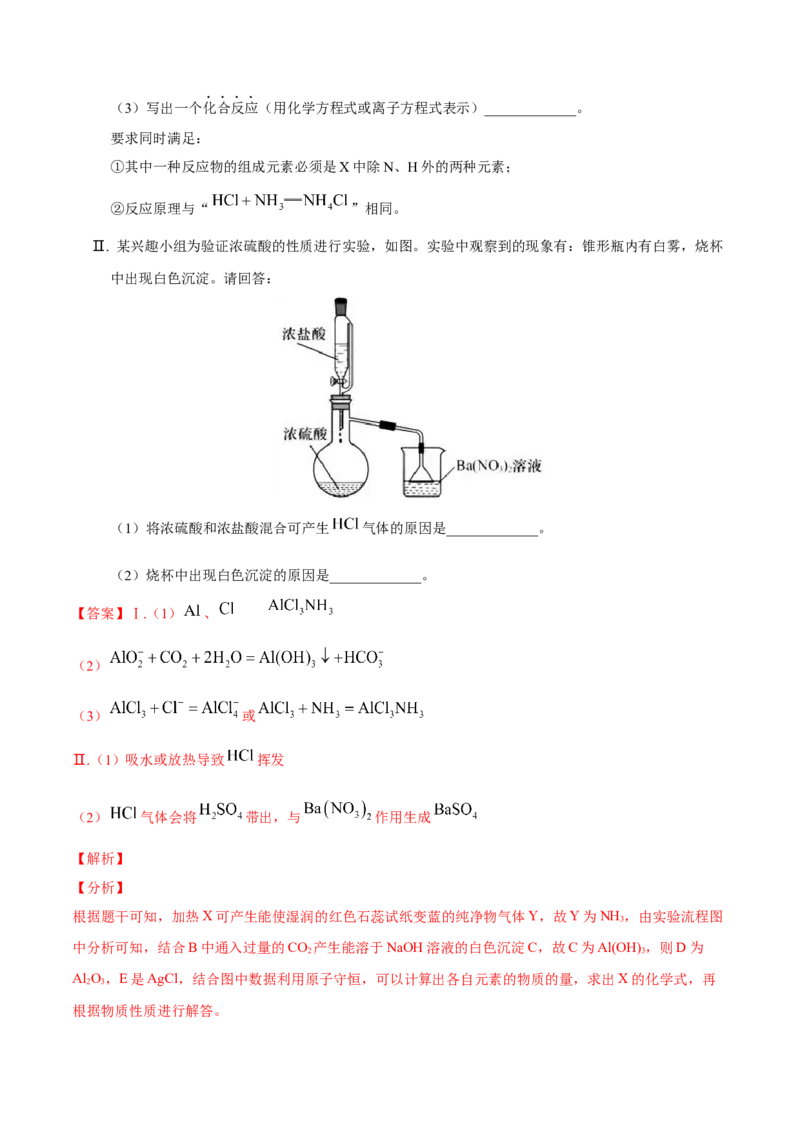
Ⅱ. 某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:锥形瓶内有白雾,烧杯
中出现白色沉淀。请回答:
(1)将浓硫酸和浓盐酸混合可产生 气体的原因是_____________。
(2)烧杯中出现白色沉淀的原因是_____________。
【答案】Ⅰ.(1) 、
(2)
(3) 或
Ⅱ.(1)吸水或放热导致 挥发
(2) 气体会将 带出,与 作用生成
【解析】
【分析】
根据题干可知,加热X可产生能使湿润的红色石蕊试纸变蓝的纯净物气体Y,故Y为NH ,由实验流程图
3
中分析可知,结合B中通入过量的CO 产生能溶于NaOH溶液的白色沉淀C,故C为Al(OH) ,则D为
2 3
Al O,E是AgCl,结合图中数据利用原子守恒,可以计算出各自元素的物质的量,求出X的化学式,再
2 3
根据物质性质进行解答。【详解】
Ⅰ.(1)由分析可知,Y为NH ,由实验流程图中分析可知,结合B中通入过量的CO 产生能溶于NaOH
3 2
溶液的白色沉淀C,故C为Al(OH) ,则D为Al O,E是AgCl,利用原子守恒可知:A 溶液中含有N原
3 2 3 1
子的物质的量为: ,Al原子的物质的量为:
,A 溶液中含有的Cl-的物质的量为:
2
;
故一半溶液中含有的H原子的物质的量为:
,故X中含有
四种元素即N、H、Al、Cl,其个数比为:
,故X的化学式为:AlCl NH ,故
3 3
答案为:Al Cl AlCl NH ;
3 3
(2)根据分析(1)可知,溶液B中通入过量的CO 所发生的离子方程式为:
2
,故答案为: ;
(3)结合题给的两个条件,再分析化合物X(AlCl NH )是NH 和AlCl 通过配位键结合成的化合物,不难
3 3 3 3
想到类似于NH 和HO反应,故可以很快得出该反应的离子方程式为AlCl +Cl-= 或者
3 2 3
AlCl +NH=AlCl NH ,故答案为:AlCl +Cl-= 或者AlCl +NH=AlCl NH ;
3 3 3 3 3 3 3 3 3
Ⅱ.(1)由于浓硫酸具有吸水性且浓硫酸稀释是个放热过程,而且HCl的挥发性随浓度增大而增大,随温度升高而增大,从而得出用浓硫酸和浓盐酸混合制备HCl的原理是浓硫酸吸收浓盐酸中的水分且放热,使
浓盐酸的挥发性增强,使HCl挥发出来,故答案为:浓硫酸吸收浓盐酸中的水分且放热,使浓盐酸的挥发
性增强,使HCl挥发出来;
(2)浓硫酸虽然难挥发,但也会随HCl气流而带出少量的HSO 分子,与Ba(NO ) 反应生成硫酸钡白色
2 4 3 2
沉淀,故答案为:HCl气体能够带出HSO 分子,与Ba(NO ) 反应生成BaSO 沉淀。
2 4 3 2 4
【点睛】
本题为实验题结合有关物质的量计算,只要认真分析题干信息,利用(元素)原子守恒就能较快求出化合
物X的化学式,进而推到出整个流程过程。
3.[2020江苏卷]次氯酸钠溶液和二氯异氰尿酸钠(C NOClNa)都是常用的杀菌消毒剂。 NaClO可用于
3 3 3 2
制备二氯异氰尿酸钠。
(1)NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为 ▲
2
;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会
导致消毒作用减弱,其原因是 ▲ 。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到
优质品标准。实验检测原理为
准确称取1.1200 g样品,用容量瓶配成250.0 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入
适量稀硫酸和过量KI溶液,密封在暗处静置5 min;用 NaSO 标准溶液滴定至
2 2 3
溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗NaSO 溶液20.00 mL。
2 2 3
①通过计算判断该样品是否为优质品。
(写出计算过程, )
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值 ▲ (填“偏高”或“偏
低”)
【答案】(1)
NaClO溶液吸收空气中的CO 后产生HClO,HClO见光分解
2(2)①
根据物质转换和电子得失守恒关系:
得
氯元素的质量:
该样品的有效氯为:
该样品的有效氯大于60%,故该样品为优质品
②偏低
【解析】
(1) 由题意可知,氯气通入氢氧化钠中产生次氯酸钠,同时产生氯化钠,反应的离子方程式为:
;次氯酸钠溶液长期暴露在空气中会吸收空气中的二氧化碳气体,因次氯酸
酸性比碳酸弱,因此次氯酸钠可以与二氧化碳在水中反应产生HClO,HClO具有不稳定性,在受热或见光
条件下会发生分解反应,产生HCl和O,从而是次氯酸钠失效,故答案为: ;
2
NaClO溶液吸收空气中的CO 后产生HClO,HClO见光分解;
2
(2) ①由题中反应可知, 在酸性条件产生HClO,HClO氧化碘离子产生碘单质,碘单质再
用硫代硫酸钠滴定,结合反应转化确定物质之间的关系为: ,
,根据物质转换和电子得失守恒关系:得
n(Cl)=0.5 = ,
氯元素的质量:m(Cl)= =0.03550g,该样品中的有效氯为:=63.39%,
该样品中的有效氯大于60%,故该样品为优质品
故答案为:n(S O )= ,根据物质转换和电子得失守恒关系:
2
,得n(Cl)=0.5 = ,
氯元素的质量:m(Cl)= =0.03550g,该样品中的有效氯为:
=63.39%,
该样品中的有效氯大于60%,故该样品为优质品
②如果硫酸的用量过少,则导致反应 不能充分进行,产生的
HClO的量偏低,最终导致实验测得的有效氯含量会偏低,
故答案为:偏低;