专题 15 化学反应原理综合题
(本卷共10小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
一、非选择题:本题共10个小题,每小题10分,共100分。
1.我国自主研发的DMTO技术是以煤或天然气代替石油作原料生产乙烯和丙烯的新技术。DMTO工业化
技术的成功研发,对开辟我国烯烃产业新途径具有重要意义。回答下列问题:
(1)煤气化包含一系列化学反应,热化学方程式如下:
①
②
③ ,则a=_______。
(2)在一定温度下,向某刚性容器中充入一定量 、 仅发生反应:
。下列情况表明反应已达到平衡状态的是_______(填标
号)。
A.混合气体的密度保持不变 B.混合气体的平均摩尔质量保持不变
C.混合气体的总压强保持不变 D.含碳粒子总浓度保持不变
(3)向一密闭容器中充入 ,发生反应: 。其
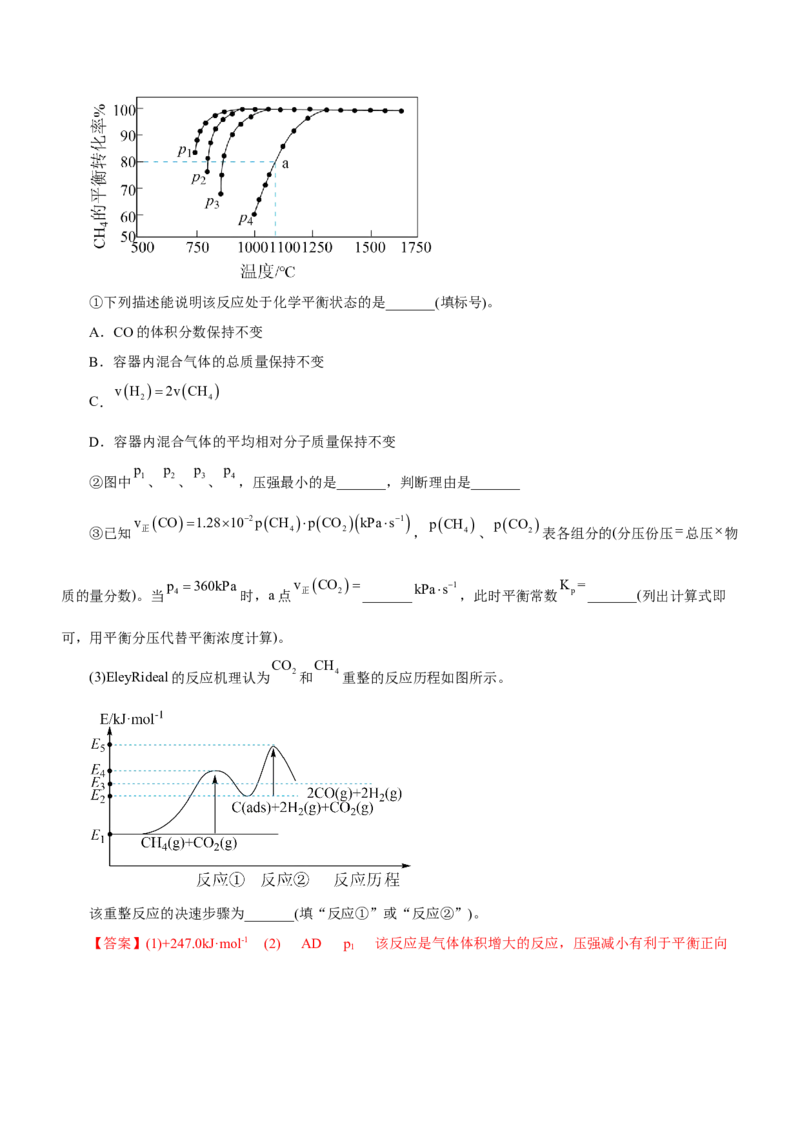
他条件不变时, 的平衡转化率随着温度(T)、压强(p)的变化如图所示:
① _______(填“>”或“<”) , 时,N点的平衡常数K=_______。已知M点、N点时容器的体积分
别为1L、0.5L。②欲提高 的平衡转化率,可采取的措施是_______(填一条,下同),欲增大反应速率,可采取的措
施是_______。
(4) 一定温度下,向一恒容密闭容器中投入1.5molCO、 发生反应:
。测得反应开始时容器内压强为 ,10min后
反应到达平衡,平衡时体系压强降低了 。 _______ ,该温度下的平衡常数
_______ ( 为分压表示的平衡常数,分压=总压X物质的量分数)。
【答案】(1)172 (2)BC (3) > 减小压强、降低温度 增大压强、升高温度(4)
1×104 1×10-10
【解析】(1)①
② 根据盖斯定律①-②得
,则a=172。
(2)A.反应前后气体总质量不变、容器体积不变,密度是恒量,混合气体的密度保持不变,反应不一
定平衡,故不选A; B.反应前后气体总质量不变,反应后气体物质的量减少,混合气体的平均摩尔质
量是变量,混合气体的平均摩尔质量保持不变,反应一定达到平衡状态,故选B;C.反应后气体物质的量减
少,压强是变量,混合气体的总压强保持不变,反应一定达到平衡状态,故选C;D.根据碳元素守恒,含碳
粒子总数不变,含碳粒子总浓度保持不变,反应不一定平衡,故不选D;选BC。
(3)①增大压强, 平衡逆向移动, 的平衡转化率减小,所
以 > ;平衡常数只与温度有关, 时,N点的平衡常数与M点相同,根据M点数据,K= 。
②根据影响平衡移动的因素,减小压强、降低温度平衡正向移动, 的转化率增大;根据影响反应速率
的因素,增大压强、升高温度,可增大反应速率。(4)一定温度下,向一恒容密闭容器中投入1.5molCO、
发生反应: 。同温同体积,压强比等于物质的
量比,反应开始时容器内压强为 ,10min后反应到达平衡,平衡时体系压强降低了 ,
3×105-2x=2×105,x=5×104MPa; ÷10min=1×104 ,该温度下的平衡常数
。
2.当前,实现碳中和已经成为全球的广泛共识,化学科学在此过程中发挥着至关重要的作用。
(1)一种将二氧化碳催化合成甲醇的技术原理为 。
①一定条件下,将 和 充入某恒温恒容密闭容器中发生上述反应,下列不能说明反应达到
平衡状态的是___________(填字母序号)。
A. 的消耗速率与 的消耗速率相等
B. 的体积分数保持不变
C.混合气体的平均密度保持不变
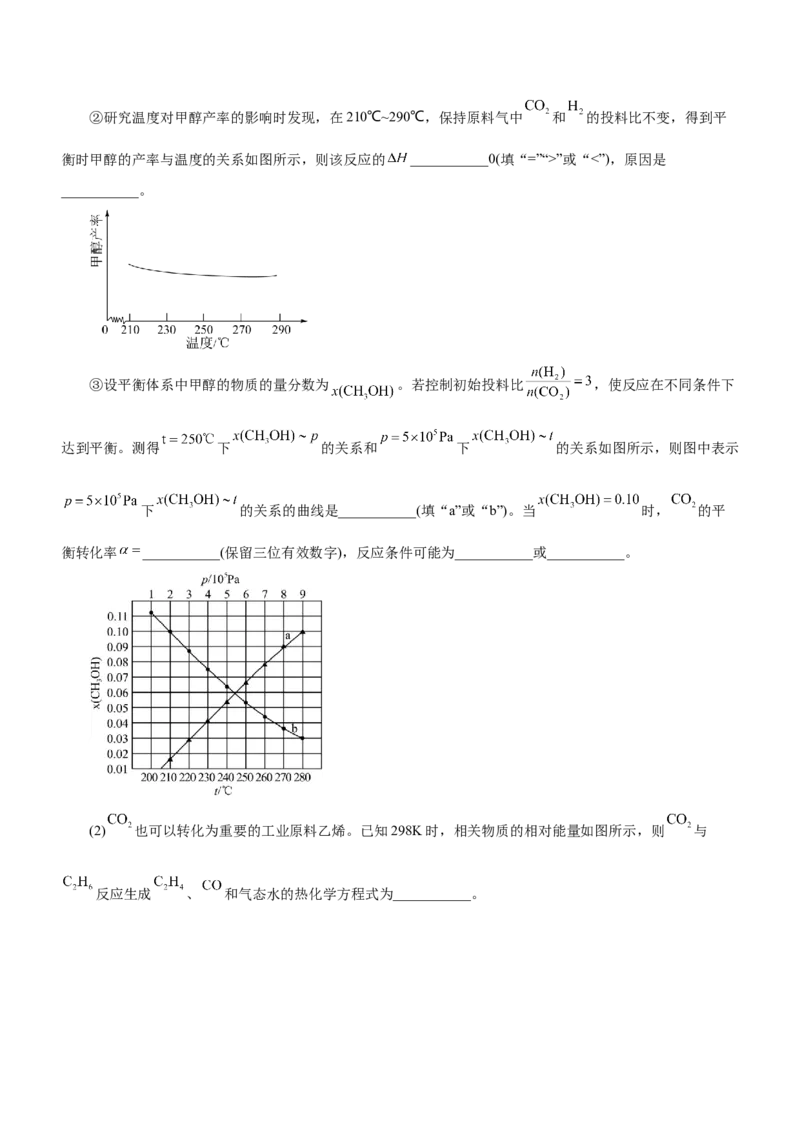
D.混合气体的平均相对分子质量保持不变②研究温度对甲醇产率的影响时发现,在210℃~290℃,保持原料气中 和 的投料比不变,得到平
衡时甲醇的产率与温度的关系如图所示,则该反应的 ___________0(填“=”“>”或“<”),原因是
___________。
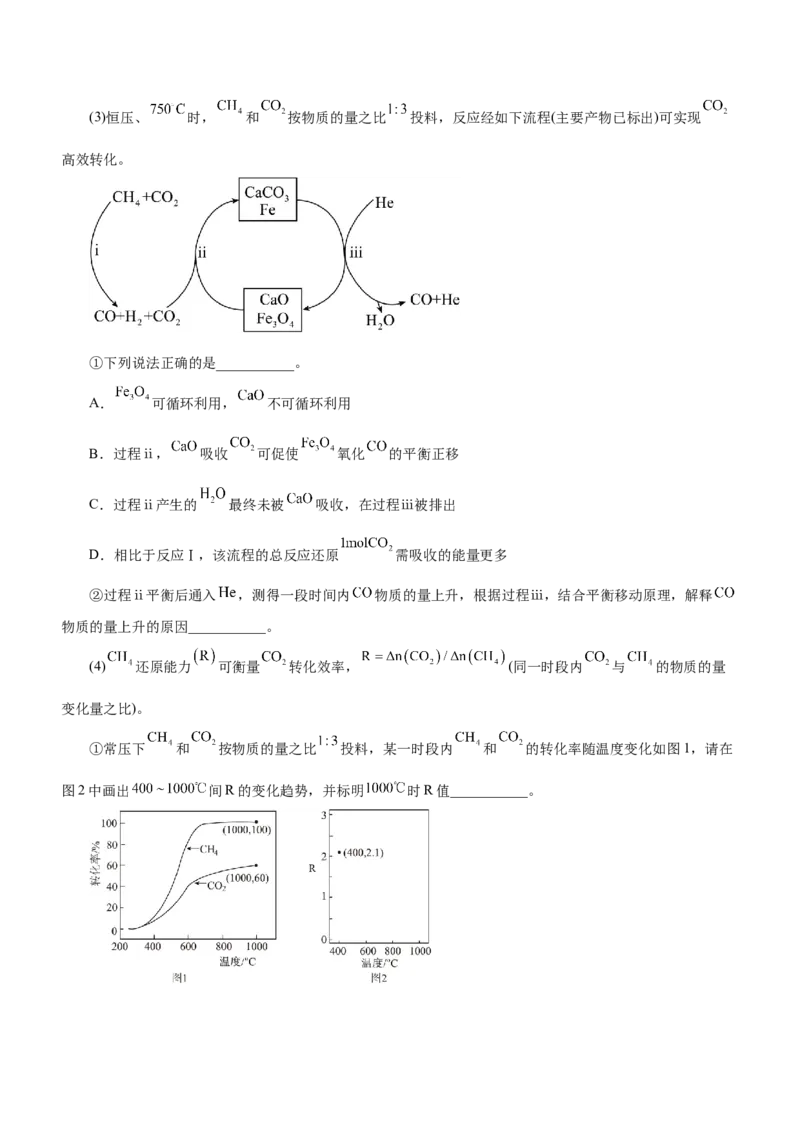
③设平衡体系中甲醇的物质的量分数为 。若控制初始投料比 ,使反应在不同条件下
达到平衡。测得 下 的关系和 下 的关系如图所示,则图中表示
下 的关系的曲线是___________(填“a”或“b”)。当 时, 的平
衡转化率 ___________(保留三位有效数字),反应条件可能为___________或___________。
(2) 也可以转化为重要的工业原料乙烯。已知298K时,相关物质的相对能量如图所示,则 与
反应生成 、 和气态水的热化学方程式为___________。(3) 辅助的 电池电容量大,能有效利用 ,其工作原理如图所示。其中,离子液体是优良的
溶剂,具有导电性;电池反应产物 重要的化工原料。此电池的正极区反应式有: ,
___________,反应过程中 的作用是___________。
【答案】(1) D < 升高温度,甲醇的产率降低,说明升高温度,化学平衡逆向移动,逆反应为吸热
反应,则该反应的正反应为放热反应 b 33.3% 2×105Pa,210℃ 9×105Pa,280℃
(2)C H(g)+CO (g)=C H(g)+CO(g)+HO(g) ∆H =+177 kJ·mol-1
2 6 2 2 4 2
(3) 6CO+6O -=3C O2-+6O 正极反应的催化剂
2 2 2 4 2
【解析】(1)①A. 的消耗速率与 的消耗速率相等,则正逆反应速率相等,反应达到平衡,
A不选;B.该反应为体积减小的反应, 的体积分数保持不变,反应达到平衡,B不选;C.反应前后
均为气体,且在恒容密闭容器中发生,混合气体的平均密度始终保持不变,则不能判断反应达到平衡,C选;
D.该反应为体积减小的反应,混合气体的平均相对分子质量保持不变,反应达到平衡,D不选;②根据图示可知:升高温度,甲醇的产率降低,说明升高温度,化学平衡逆向移动,逆反应为吸热反应,则该反应的正反
应为放热反应,所以△H<0。③该反应正向为放热反应,升高温度时平衡逆向移动,体系中x(CHOH)将减
3
小,因此图中对应等压过程的曲线是b;设起始n(CO)=1mol,n(H )=3mol,则
2 2
当平衡时 时, ,解得x= mol,平衡时CO 的转化率α=
2
;由图可知,满足平衡时 的条件有:2×105Pa,210℃或9×105Pa,
280℃; (2)结合图像,反应的热化学方程式为C H(g)+CO (g)=C H(g)+CO(g)+HO(g) ∆H =[52+(-110)+
2 6 2 2 4 2
(-242)-(-84)-(-393)]kJ· mol-1=+177 kJ· mol-1;(3)铝电极失去电子,则电池的负极为Al,电解质为氯化铝离
子液体,所以Al失电子应转化为Al3+,铝电极的电极反应为:Al-3e–=Al3+(或2Al-6e–=2Al3+)。正极发生分步
反应,对应的电极反应为:6O+6e−=6O -、6CO+6O -=3C O2-+6O ,氧气在第一步被消耗,又在第二步生成,
2 2 2 2 2 4 2
所以氧气为正极反应的催化剂,将方程式加和得到总反应为:2Al+6CO =Al(C O)。
2 2 2 4 3
3.“碳达峰·碳中和”是我国社会发展重大战略之一, 还原 是实现“双碳”经济的有效途径之
一,相关的主要反应有:
Ⅰ:
Ⅱ:
请回答:
(1)有利于提高 平衡转化率的条件是___________。
A.低温低压 B.低温高压 C.高温低压 D.高温高压
(2)反应 的 __________ , _________(用 表
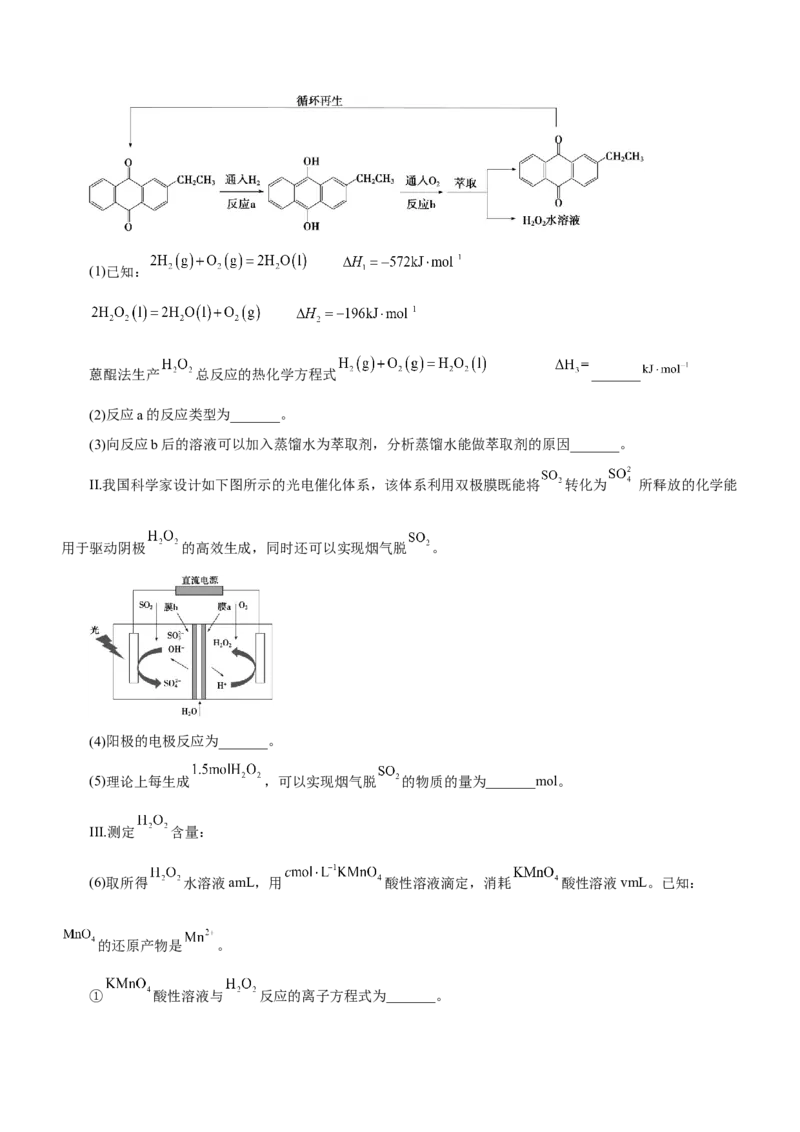
示)。(3)恒压、 时, 和 按物质的量之比 投料,反应经如下流程(主要产物已标出)可实现
高效转化。
①下列说法正确的是___________。
A. 可循环利用, 不可循环利用
B.过程ⅱ, 吸收 可促使 氧化 的平衡正移
C.过程ⅱ产生的 最终未被 吸收,在过程ⅲ被排出
D.相比于反应Ⅰ,该流程的总反应还原 需吸收的能量更多
②过程ⅱ平衡后通入 ,测得一段时间内 物质的量上升,根据过程ⅲ,结合平衡移动原理,解释
物质的量上升的原因___________。
(4) 还原能力 可衡量 转化效率, (同一时段内 与 的物质的量
变化量之比)。
①常压下 和 按物质的量之比 投料,某一时段内 和 的转化率随温度变化如图1,请在
图2中画出 间R的变化趋势,并标明 时R值___________。②催化剂X可提高R值,另一时段内 转化率、R值随温度变化如下表:
48
温度/℃ 500 520 550
0
转化率/% 7.9 11.5 20.2 34.8
R 2.6 2.4 2.1 1.8
下列说法不正确的是___________
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中 占比越高
C.温度升高, 转化率增加, 转化率降低,R值减小
D.改变催化剂提高 转化率,R值不一定增大
【答案】(1)C (2) (3) BC 通入 分解平衡正移,导致 增大,
促进 还原 平衡正移 (4) C
【解析】(1)反应Ⅰ为气体体积增大的吸热反应,反应Ⅱ为气体体积不变的吸热反应,△H>0,升高温
度,平衡右移,CH 平衡转化率增大;降低压强,平衡右移,CH 平衡转化率增大,故有利于提高 平衡转
4 4
化率的条件是高温低压;答案选C;(2)已知:Ⅰ:Ⅱ:
根据盖斯定律,由Ⅰ+Ⅱ 2得反应 ;
故 △H+2△H =+329 , ;
1 2
(3)①A.根据流程可知, 转化为Fe,Fe又转化为 , 可循环利用;CaCO 受热分解生
3
成 和CO, 又与CO 反应生成CaCO , 也可循环利用,A错误;B.过程ⅱ, 吸收 使
2 2 3
浓度降低,促进 氧化 的平衡正移,B正确;C.过程ⅱ 吸收 而产生的 最终未被
吸收,在过程ⅲ被排出,C正确;D.焓变只与起始物质的量有关,与过程无关,故相比于反应Ⅰ,该流
程的总反应还原 需吸收的能量一样多,D错误;答案选BC;②通入 分解平衡正移,导致
增大,促进 还原 平衡正移,故过程ⅱ平衡后通入 ,测得一段时间内 物质的量上升;
(4)①根据图1可知 时, 转化率为100%,即 =1mol, 转化率为60%,即
=3mol 60%=1.8mol,故 = =1.8,故 间R的变化趋势如图:
。②A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率,使单位时间内反应Ⅱ中CO 的转化率增大, 增大的倍数比 大,则R提高,A正确;B.根据表中数据可知,温度越
2
低, 转化率越小,而R越大, 增大的倍数比 大,含氢产物中 占比越高,B正确;
C.温度升高, 转化率增加, 转化率也增大,且两个反应中的 转化率均增大,增大倍数多,故R
值增大,C不正确;D.改变催化剂使反应有选择性按反应Ⅰ而提高 转化率,若 转化率减小,则R值
不一定增大,选项D正确;答案选C。
4.乙醇是重要的有机化工原料,可由乙烯气相直接水合法或电解法制取。回答下列问题:
Ⅰ、乙烯气相直接水合法制乙醇
(1)已知:
①2CHOH(g)=CH OCH (g)+HO(g) △H=-23.9kJ·mol
3 3 3 2 1
②2CH OH(g)=C H(g)+2HO(g) △H=-29.1kJ·mol
3 2 4 2 2
③C HOH(g)=CH OCH (g) △H=+50.6kJ·mol
2 5 3 3 3
则乙烯气相直接水合反应C H(g)+HO(g)=C HOH(g)的△H=___________。
2 4 2 2 5
(2)已知等物质的量的C H 和HO的混合气体在一定的条件下反应,乙烯的平衡转化率与温度、压强的关
2 4 2
系如图。
①图中压强P、P、P 由小到大的顺序为___________。
1 2 3
②乙烯水合制乙醇反应在图中A点(P =8.1MPa)的平衡常数K=___________(用平衡分压代替平衡浓度计
2 p
算,分压=总压×物质的量分数,结果保留两位有效数字)。
③若保持其他条件不变,将容器改为恒压密闭容器,则C H 的平衡转化率将___________(填“增大”、
2 4
“减小”或“不变”)。
Ⅱ、电解法制乙醇
(3)以铅蓄电池为电源可将CO 转化为乙醇,其原理如图所示,电极材料均为惰性电极。该电解池阴极上
2
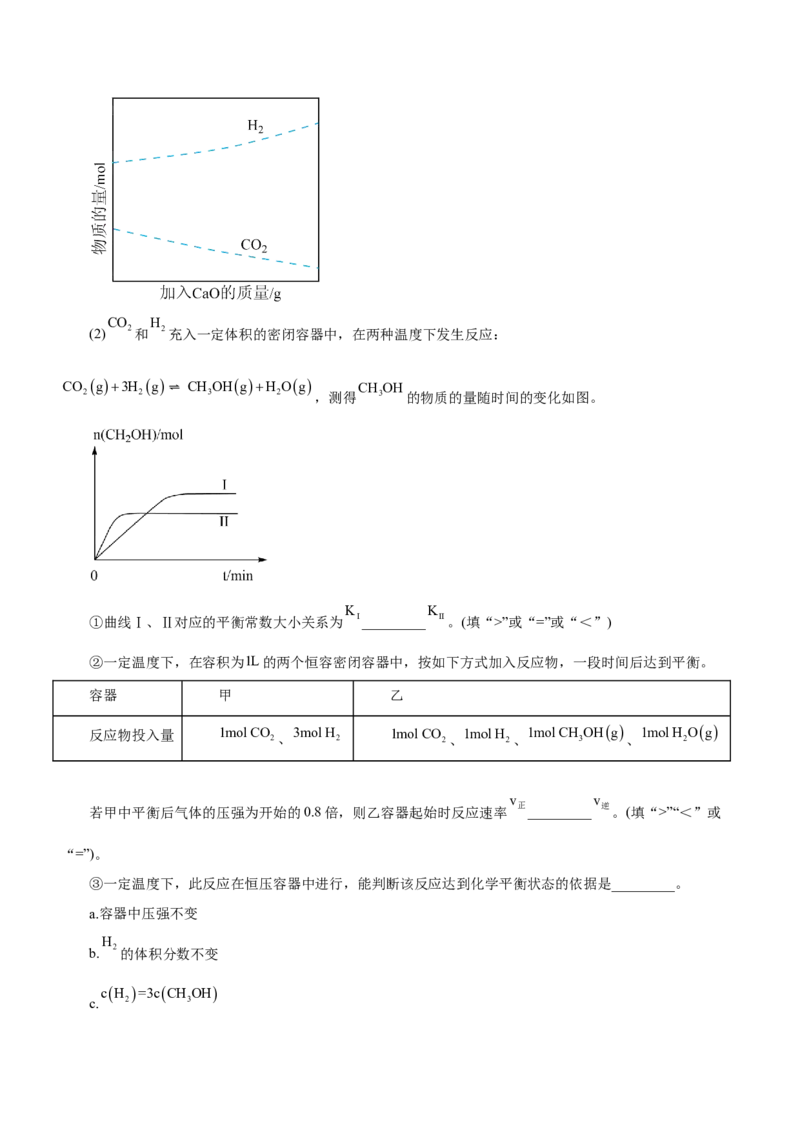
的电极反应式为___________;每生成0.2mol乙醇,理论上消耗铅蓄电池中___________mol硫酸。【答案】(1)-45.4kJ/mol (2)P
”或“=”或“<”)
②一定温度下,在容积为1L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容器 甲 乙
反应物投入量 1mol CO 2、 3mol H 2 1mol CO 2、 1mol H 2、 1mol CH 3 OHg 、 1mol H 2 Og
v v
若甲中平衡后气体的压强为开始的0.8倍,则乙容器起始时反应速率 正 _________ 逆。(填“>”“<”或
“=”)。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是_________。
a.容器中压强不变
H
b. 2的体积分数不变
cH =3cCH OH
c. 2 3d.容器中密度不变
e.2个CO断裂的同时有3个HH断裂
HCN K =4.91010 H CO K =4.3107 K =5.61011 KCN
(3)已知电离常数 : a , 2 3: a1 , a2 ,则向 溶液中通入
CO
少量 2时的离子方程式为_________。
CO H O
(4)利用人工光合作用,借助太阳能使 2和 2 转化为 HCOOH ,如图所示,在催化剂b表面发生的电
极反应为:_________。
【答案】(1) b—a CaO消耗CO,生成物CO 的浓度减小,平衡向正反应方向移动,氢气的产率增大
2 2
(2) > < bd (3)CO +CN—+H O=HCN+HCO - (4)CO +2H++2e—=HCOOH
2 2 3 2
【解析】(1)①由盖斯定律可知,反应Ⅲ—反应Ⅱ可得反应Ⅰ,则ΔH=ΔH—ΔH=(b—a)kj/mol;②二氧
1 3 2
化碳能与氧化钙反应生成碳酸钙,则加入氧化钙可以使反应Ⅰ生成的二氧化碳浓度减小,平衡向正反应方向移
动,氢气的产率增大;(2)①由图可知,曲线Ⅱ达到平衡达到平衡所需时间小于曲线Ⅰ,甲醇的物质的量小
于曲线Ⅰ说明反应温度Ⅱ大于Ⅰ,平衡向逆反应方向移动,该反应为放热反应,所以化学平衡常数K 大于
I
K ;②设甲中平衡水蒸气的浓度为amol,由题意可建立如下三段式:
II
CO g+ 3H g CH OHg+ H Og
2 2 3 2
起(mol) 1 3 0 0
变(mol) a 3a a a
平(mol) 1-a 3-3a a a
1 4
由平衡后气体的压强为开始的0.8倍可得:0.8=4-2a,解得a=0.4,则平衡时二氧化碳、氢气、甲醇、水
0.40.4
蒸气的浓度分别为0.6mol/L、1.8mol/L、0.4mol/L、0.4mol/L,反应的平衡常数K=0.61.83 ≈0.046,容器乙中
11
的浓度熵Q=113 =1>K,所以反应向正反应方向进行,正反应速率大于逆反应速率;
c③a.恒压容器中混合气体的压强始终不变,则容器中压强不变不能说明正逆反应速率相等,无法判断反
应是否达到平衡,故错误;b.氢气的体积分数不变说明正逆反应速率相等,反应已达到平衡,故正确;c.
cH =3cCH OH
2 3 不能说明正逆反应速率相等,无法判断反应是否达到平衡,故错误;d.由质量守恒定律可
知,反应前后气体的质量相等,该反应是气体体积减小的反应,反应中气体体积减小,混合气体的密度增大,
则容器中密度不变说明正逆反应速率相等,反应已达到平衡,故正确;e.2个CO断裂的同时有3个HH
断裂均代表正反应速率,不能说明正逆反应速率相等,无法判断反应是否达到平衡,故错误;故选bd;(3)
由电离常数可知,氢氰酸的电离程度大于碳酸氢根离子,小于碳酸,所以由强酸制弱酸的原理可知,氰化钾溶
液与二氧化碳反应生成氢氰酸和碳酸氢钾,反应的离子方程式为CO+CN—+H O=HCN+HCO -;(4)由图中电
2 2 3
子移动方向可知,催化剂b为原电池的正极,酸性条件下二氧化碳在正极得到电子发生还原反应生成甲酸,电
极反应式为CO+2H++2e—=HCOOH。
2
CO
10.习近平主席在第75届联合国大会提出我国要实现2030年碳达峰、2060年碳中和的目标。因此 2的
CO g CH g
捕获、利用与封存成为科学家研究的重要课题。研究表明 2 和 4 在催化剂存在下可发生反应制得
合成气:
CO
2
gCH
4
g
2COg2H
2
g
H。回答下列问题:
(1)已知 CH 4 g 、 COg 和 H 2 g 的燃烧热 H 分别为890.3kJmol1 、283.0kJmol1和
285.8kJmol1 H kJmol1
。上述反应的焓变 _________ 。
(2)将原料按
nCH
4
:nCO
2
1:1
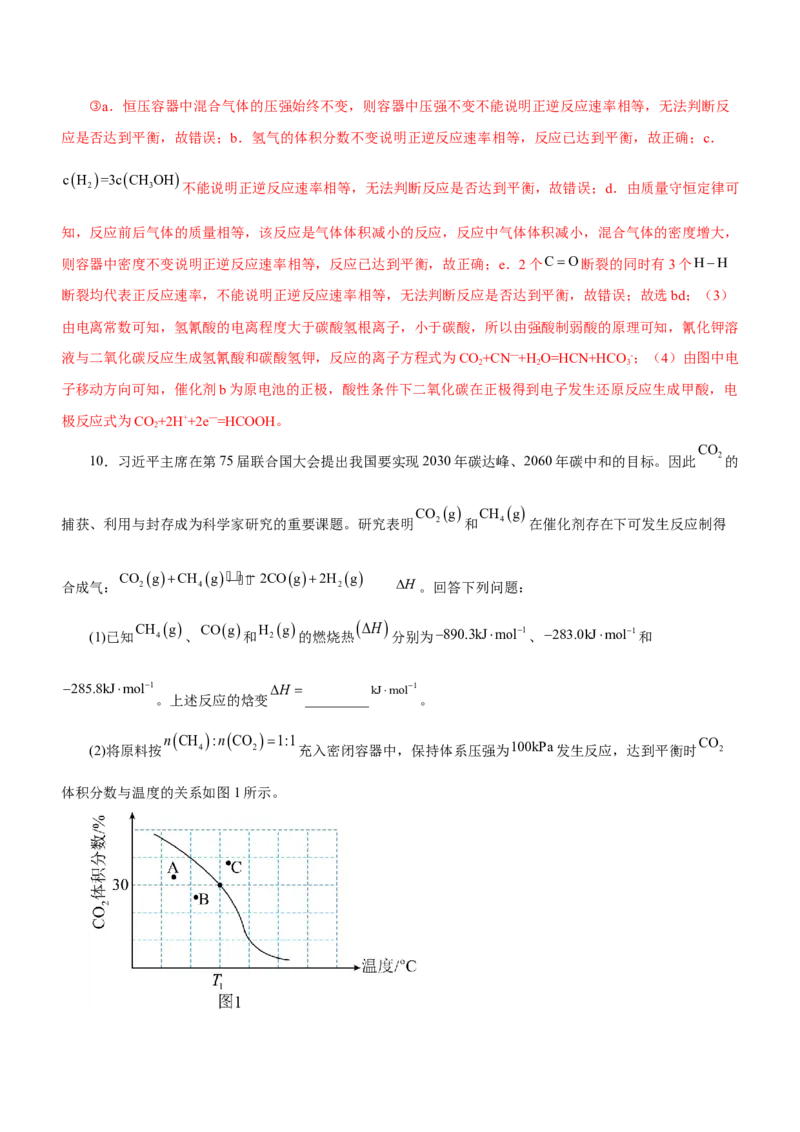
充入密闭容器中,保持体系压强为100kPa发生反应,达到平衡时 CO 2
体积分数与温度的关系如图1所示。T C、100kPa
① 1 下,平衡时容器体积与初始容器体积之比为_________;该温度下,此反应的平衡常数
K kPa2
p _________ (用平衡分压代替平衡浓度计算,分压总压物质的量分数)
CO
②若A、B、C三点表示不同温度和压强下已达平衡时 2的体积分数,_________点对应的平衡常数最
小,_________点对应的压强最大。
CO g CH g COg
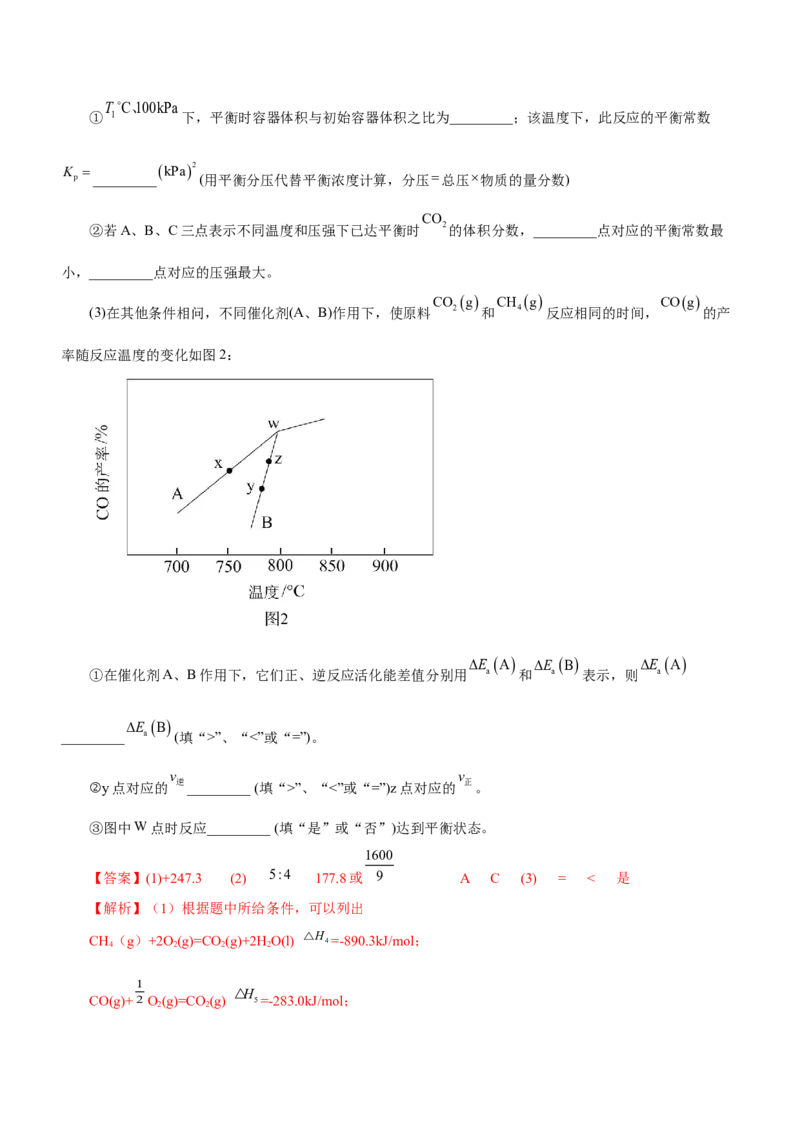
(3)在其他条件相问,不同催化剂(A、B)作用下,使原料 2 和 4 反应相同的时间, 的产
率随反应温度的变化如图2:
E A E B E A
①在催化剂A、B作用下,它们正、逆反应活化能差值分别用 a 和 a 表示,则 a
E B
_________ a (填“>”、“<”或“=”)。
v v
②y点对应的 逆_________ (填“>”、“<”或“=”)z点对应的 正。
③图中W点时反应_________ (填“是”或“否”)达到平衡状态。
1600
【答案】(1)+247.3 (2) 5:4 177.8或 9 A C (3) = < 是
【解析】(1)根据题中所给条件,可以列出
CH
4
(g)+2O
2
(g)=CO
2
(g)+2H
2
O(l) △H 4=-890.3kJ/mol;
1
△H
CO(g)+2O(g)=CO (g) 5=-283.0kJ/mol;
2 21
△H △H =△H -2(△H +△H )
H(g)+ 2O(g)=HO(l) 6=-285.8kJ/mol,根据盖斯定律可得 1 4 5 6 =+247.3kJ/mol;
2 2 2
CH g +CO g 2COg+2H g
4 2 2
起始量(mol) a a 0 0
转化量(mol) x x 2x 2x
平衡量(mol) a-x a-x 2x 2x
(2)①T℃、100kPa下,由三段式分析可知, ,根
1
a-x
×100%
据气体的体积分数即为物质的量分数,故有:2a+2x =30%,即得:x=0.25a,n(初始气体):n(平衡时气
体)=2a:(2a+2x)=2a:(2a+2×0.25a)=4:5,同温同压,体积之比等于物质的量之比,平衡时容器体积与初始容器
a-x
×p
体积之比为5:4;该温度下,CH、CO、CO、H 的平衡分压分别为:p(CH)= p(CO )=2a+2x 总 =
4 2 2 4 2
a-0.25a 2x 20.25a
×100kPa ×p ×100kPa
2a+20.25a =30kPa,,p(CO)=p(H )= 2a+2x 总 =2a+20.25a =20kPa,此反应的平衡常数Kp=
2
p2(CO)p2(H ) (20kPa)2(20kPa)2 1600
2
p(CH 4 )p(CO 2 ) = (30kPa)(30kPa) = 9 (kPa)2;②若A、B、C三点表示不同温度和压强下已达平衡时CO 2 的
体积分数,由于平衡常数仅仅是温度的函数,且该反应正反应是一个吸热反应,升高温度平衡正向移动,平衡
常数增大,A点对应的平衡常数最小;该反应增大压强平衡逆向移动,CO 的体积分数增大,故C点对应CO
2 2
的体积分数大,温度高,压强最大,故答案为:A;C;(3)①在催化剂A、B作用下,它们正、逆反应活化
能差值即该反应的反应热H,催化剂影响反应速率但不影响反应的焓变,分别用E(A)、E(B)表示,则
E(A)=E(B),故答案为:=; ②由图可知,y点对应的温度低于z点对应的温度,温度越高反应速率越快,故y
点对应的 <z点对应的 ,故答案为:<;③催化剂改变反应速率,但不影响平衡状态,W点及之后升
(逆) (正)
温,一氧化碳的产率相同,说明反应已达到平衡。