文档内容
专题 15 物质结构与性质
1.(2023·湖南省雅礼中学高三第四次月考)下列有关化学用语表示正确的是( )
A.氮原子所有价电子的电子云轮廓图均为哑铃形
B.HCN的电子式:
C.键线式为 的有机物存在顺反异构
D.基态氮原子价电子的轨道表示式:
2.(2023·江苏省苏州市高三期中调研)N、 P、 As、 Sb是周期表中ⅤA族元素。下列说法正确的是(
7 15 33 51
)
A.电负性大小: B.氢化物沸点高低:AsH >PH >NH
3 3 3
C.酸性强弱:HNO>HPO >HAsO D.ⅤA族元素单质的晶体类型相同
3 3 4 3 4
3.某种原子的电子排布式为1s22s22p63s23p1,有关该原子的下列说法中正确的是( )
A.该原子核内有13个中子 B.该原子的简化电子排布式为[He]3s23p1
C.该原子最外层有1个电子 D.该原子第二能层上有8个电子
4.已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素
原子的最外层2p轨道上有2个未成对电子。X与Y可形成化合物XY,2元素可形成负一价离子。下列说法
2 3
正确的是( )
A.X元素基态原子的电子排布式为
B.X元素是第4周期第VA族元素
C.Y元素原子的轨道表示式为
D.Z元素的单质Z 在氧气中不能燃烧
2
5.下列各组表述中,两个微粒一定不属于同种元素原子的是( )
A.3p能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2的原子C.最外层电子数是核外电子总数的的原子和价电子排布为4s24p5的原子
D.2p能级有一个未成对电子的基态原子和原子的价电子排布为2s22p5的原子
6.元素周期表共有18个纵行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列。按这
种规定,下面说法正确的是( )
A.第9列元素中不完全是金属元素
B.第15列元素的原子最外层电子的排布式为ns2np3
C.最外层电子数为ns2的元素都在第2列
D.第10、11列为ds区的元素,形成化合物种类最多的元素在第14列
7.现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5。
则下列有关比较中正确的是( )
A.第一电离能:④>③>②>① B.原子半径:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
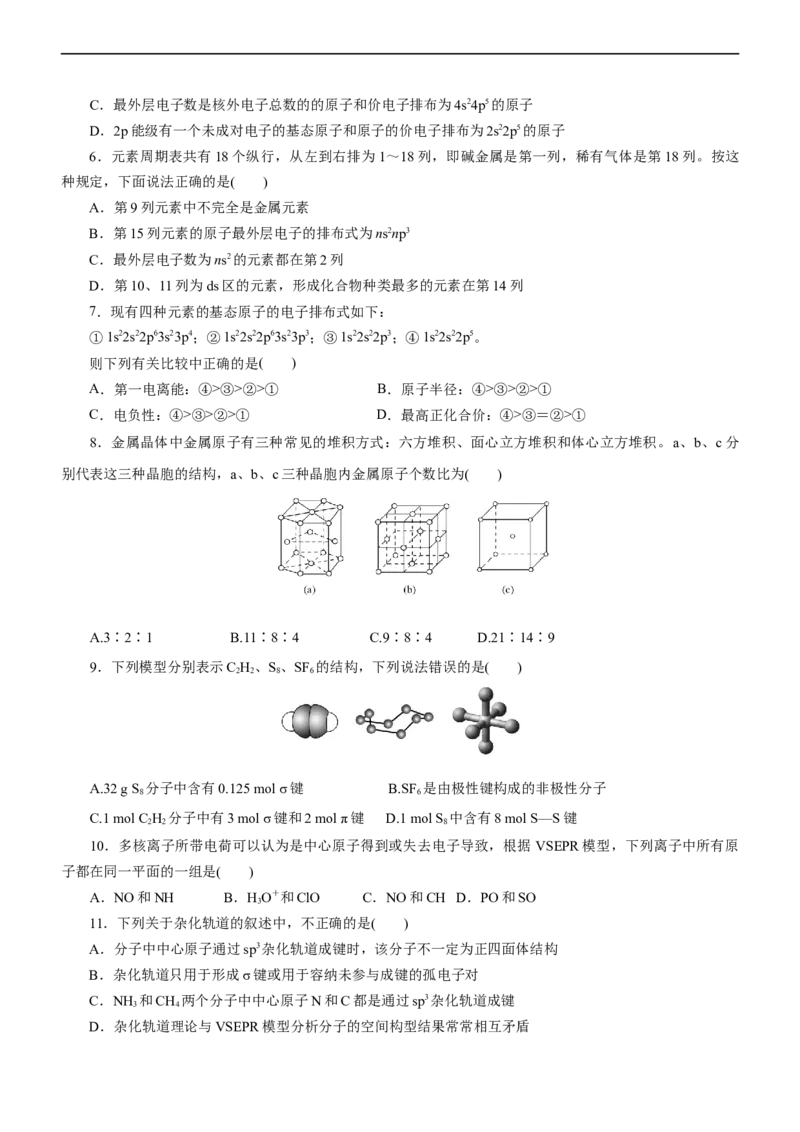
8.金属晶体中金属原子有三种常见的堆积方式:六方堆积、面心立方堆积和体心立方堆积。a、b、c分
别代表这三种晶胞的结构,a、b、c三种晶胞内金属原子个数比为( )
A.3∶2∶1 B.11∶8∶4 C.9∶8∶4 D.21∶14∶9
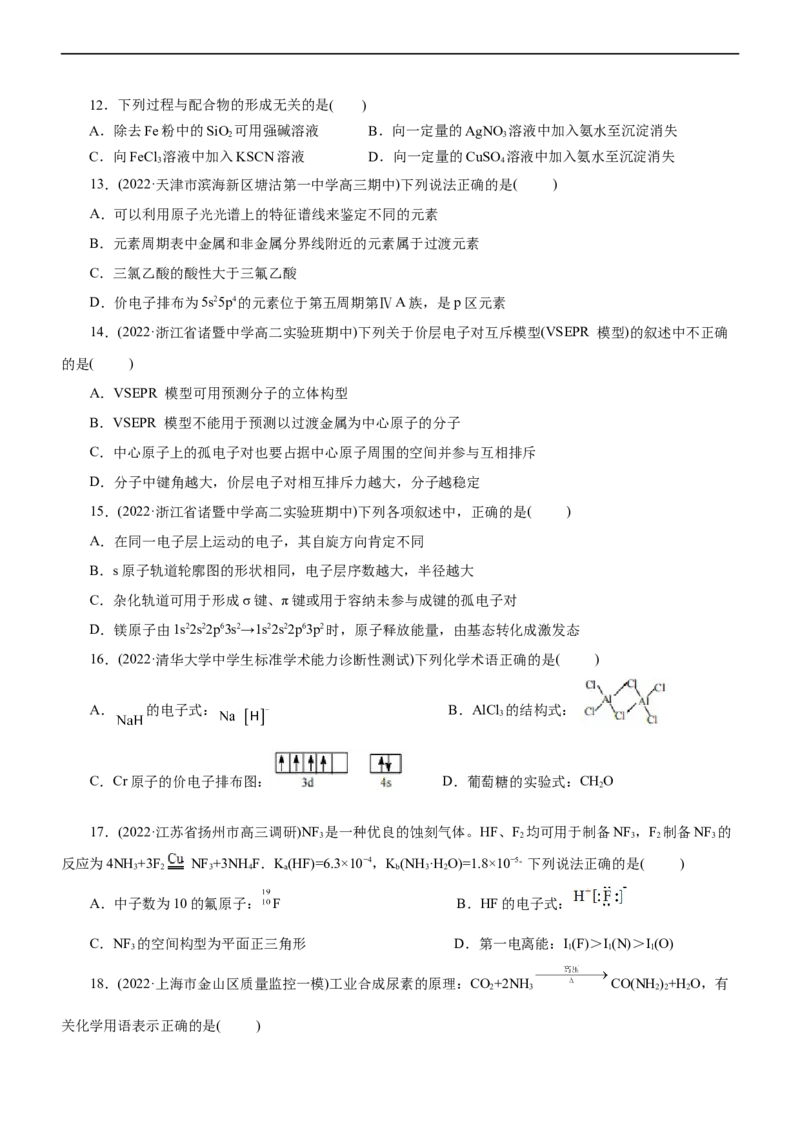
9.下列模型分别表示C H、S、SF 的结构,下列说法错误的是( )
2 2 8 6
A.32 g S 分子中含有0.125 mol σ键 B.SF 是由极性键构成的非极性分子
8 6
C.1 mol C H 分子中有3 mol σ键和2 mol π键 D.1 mol S 中含有8 mol S—S键
2 2 8
10.多核离子所带电荷可以认为是中心原子得到或失去电子导致,根据 VSEPR模型,下列离子中所有原
子都在同一平面的一组是( )
A.NO和NH B.HO+和ClO C.NO和CH D.PO和SO
3
11.下列关于杂化轨道的叙述中,不正确的是( )
A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
C.NH 和CH 两个分子中中心原子N和C都是通过sp3杂化轨道成键
3 4
D.杂化轨道理论与VSEPR模型分析分子的空间构型结果常常相互矛盾12.下列过程与配合物的形成无关的是( )
A.除去Fe粉中的SiO 可用强碱溶液 B.向一定量的AgNO 溶液中加入氨水至沉淀消失
2 3
C.向FeCl 溶液中加入KSCN溶液 D.向一定量的CuSO 溶液中加入氨水至沉淀消失
3 4
13.(2022·天津市滨海新区塘沽第一中学高三期中)下列说法正确的是( )
A.可以利用原子光光谱上的特征谱线来鉴定不同的元素
B.元素周期表中金属和非金属分界线附近的元素属于过渡元素
C.三氯乙酸的酸性大于三氟乙酸
D.价电子排布为5s25p4的元素位于第五周期第ⅣA族,是p区元素
14.(2022·浙江省诸暨中学高二实验班期中)下列关于价层电子对互斥模型(VSEPR 模型)的叙述中不正确
的是( )
A.VSEPR 模型可用预测分子的立体构型
B.VSEPR 模型不能用于预测以过渡金属为中心原子的分子
C.中心原子上的孤电子对也要占据中心原子周围的空间并参与互相排斥
D.分子中键角越大,价层电子对相互排斥力越大,分子越稳定
15.(2022·浙江省诸暨中学高二实验班期中)下列各项叙述中,正确的是( )
A.在同一电子层上运动的电子,其自旋方向肯定不同
B.s原子轨道轮廓图的形状相同,电子层序数越大,半径越大
C.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
D.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
16.(2022·清华大学中学生标准学术能力诊断性测试)下列化学术语正确的是( )
A. 的电子式: B.AlCl 的结构式:
3
C.Cr原子的价电子排布图: D.葡萄糖的实验式:CHO
2
17.(2022·江苏省扬州市高三调研)NF 是一种优良的蚀刻气体。HF、F 均可用于制备NF ,F 制备NF 的
3 2 3 2 3
反应为4NH +3F NF +3NHF.K(HF)=6.3×10−4,K(NH ·H O)=1.8×10−5。下列说法正确的是( )
3 2 3 4 a b 3 2
A.中子数为10的氟原子: F B.HF的电子式:
C.NF 的空间构型为平面正三角形 D.第一电离能:I(F)>I(N)>I(O)
3 1 1 1
18.(2022·上海市金山区质量监控一模)工业合成尿素的原理:CO+2NH CO(NH)+H O,有
2 3 2 2 2
关化学用语表示正确的是( )A.中子数为8的碳原子:8C
B.NH 的电子式:
3
C.氧原子的核外电子轨道表示式:
D.CO(NH) 的结构简式:
2 2
19.(2022·山东省潍坊市高三学科核心素养测评)光气(COCl )是一种重要的有机中间体。可用反应
2
CHCl +H O=COCl ↑+HCl+H O制备光气。下列叙述错误的是( )
3 2 2 2 2
A.CHCl 为极性分子
3
B.电负性:O>Cl>C
C.基态Cl原子的价电子轨道表示式:
D.COCl 中碳原子的杂化类型为sp3杂化
2
20.(2022·江苏省苏州八校联盟高三第二次适应性考试)CHOH、NH 和(CH)NNH 均为常见的燃料,关
3 2 4 3 2 2
于这三者的结构与性质,下列说法错误的是( )
A.CHOH的电子式为 B.NH 空间结构为平面形
3 2 4
C.CHOH、NH 和(CH)NNH 都易溶于水 D.CHOH和(CH)NNH中C、O、N杂化方式均相
3 2 4 3 2 2 3 3 2
同
21.(2022·江苏省如皋市高三期中调研)X、Y、Z、W为前四周期原子序数依次增大的四种元素,X、Y、
Z的原子半径和最外层电子数如图所示。W的基态原子最外层只有1个电子且内层电子全部充满。下列说法正
确的是( )
A.第一电离能:X<Y B.W的基态原子的电子排布式:1s22s22p63s23p64s1C.Z元素没有正化合价 D.X的简单氢化物分子间能形成氢键
22.(2022·辽宁省名校联盟高三第四次联合考试)我国的激光技术在世界上处于领先地位,科学家用激光将
置于铁室中石墨靶上的碳原子炸松,与此同时再用射频电火花喷射氮气,此时碳、氮原子结合成氮碳化合物薄
膜,氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,其中β一氮化碳的结构如图。下列有关氮化碳
的说法错误的是( )
A.氮化碳属于共价晶体 B.氮化碳的化学式为C N
3 4
C.碳、氮原子均采取sp3杂化 D.1mol氮化碳中含有4molN—C键
23.(2022·山东省东明县第一中学高三期中)联氨(NH)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,
2 4
其中一种反应机理如图所示。下列叙述正确的是( )
A.NH 分子中σ键与 键的数目之比为5:1
2 4
B.1molN H 可处理水中2mol O
2 4 2
C.[Cu(NH )]2+中存在离子键、配位键和极性共价键
3 4
D.氨水中NH 与HO间存在氢键
3 2
24.(2022·山东省学情高三质量检测)叶酸拮抗剂是一种多靶向性抗癌药物,常以苯和丁二酸酐为原料合成
过程中,某一中间体(X)结构如右图所示:下列有关说法错误的是( )
A.基态N原子的核外电子空间运动状态有5种B.沸点: 高于
C.X结构中,C、N原子杂化方式种数相同
D.X结构中含有 大 键
1.(2023·福建省诏安县桥东中学高三期中)下表是元素周期表的一部分,表中所列的字母分别代表一种化
学元素。试回答下列问题:
(1)元素y为26号元素,请写出其基态原子的电子排布式:_______。
(2)元素x的价电子排布图为_______。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_______。
(4)x、y两元素的部分电离能数据列于下表:
元素 x y
I 717 759
1
电离能/(kJ/mol) I 1 509 1 561
2
I 3 248 2 957
3
比较两元素的I、I 可知,气态x2+再失去一个电子比气态y2+再失去一个电子难。对此,你的解释是
2 3
_______。
(5)第三周期8种元素按单质熔点高低的顺序排列如图所示,其中电负性最大的是_______(填序号)。(6)表中所列的某主族元素的电离能情况如图所示,则该元素是_______(填元素符号)。
2.(2023·广东省名校联盟高三大联考)我国在商代或更早就掌握了冶炼铜的技术。以黄铜矿为原料冶炼铜
涉及多个反应,其中一个反应为8CuFeS+21O 8Cu+4FeO+2Fe O+16SO。
2 2 2 3 2
(1)基态Cu+的电子排布式为_______,从原子结构角度上解释,高温下CuO能转化为Cu O的原因是
2
_______。铜、铁两类原子核外电子运动状态相差_______种。
(2) SO、SO 、SO 2-、SO 2-四种含硫微粒中,中心原子为sp3杂化的是_______,属于极性分子的是
2 3 3 4
_______,空间构型为平面三角形的微粒是_______。
(3) FeO、Fe O 的熔点是下列两个值中的一个: , ,则两种氧化物的品体类型都是_______,
2 3
是_______的熔点。
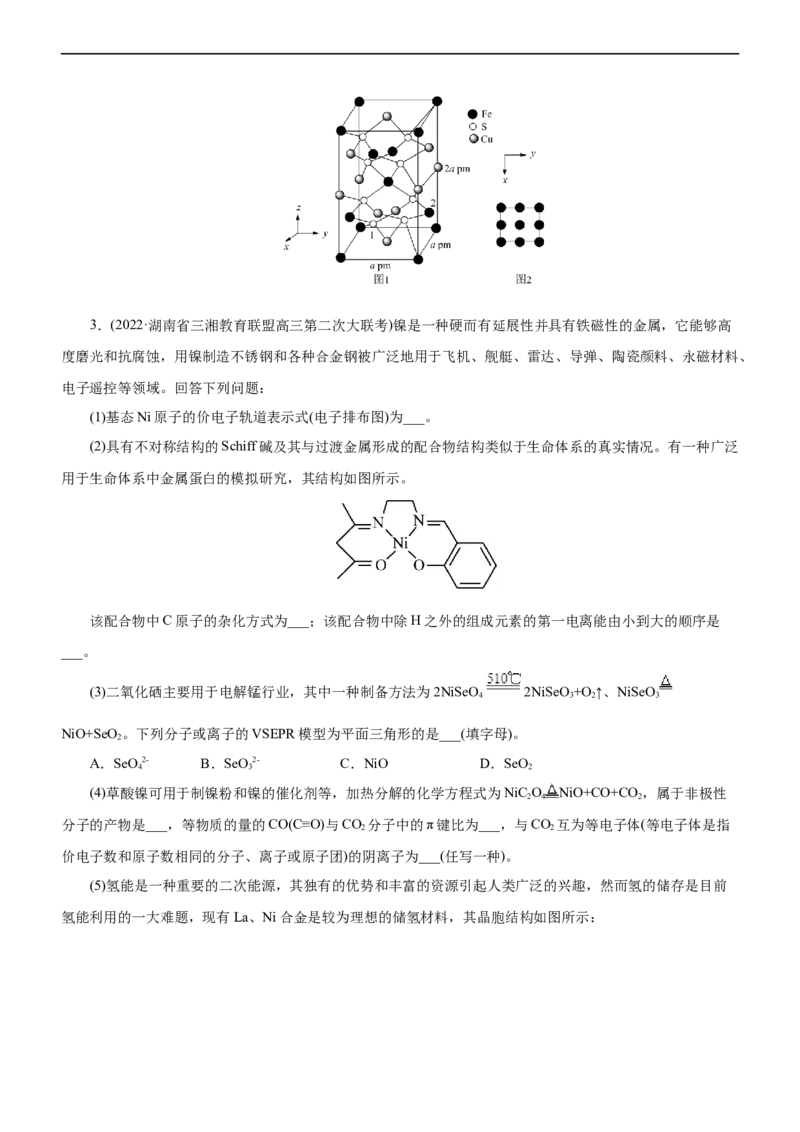
(4) CuFeS 晶胞结构如图1所示。晶胞中 的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系
2
可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图 1中原子1的坐标分数为 ,则原子2的
分数坐标为_______;该晶体的密度为ρg· cm-3,则阿伏加德罗常数N =_______ mol-1 (用含ρ、a的代数式表
A
示)。3.(2022·湖南省三湘教育联盟高三第二次大联考)镍是一种硬而有延展性并具有铁磁性的金属,它能够高
度磨光和抗腐蚀,用镍制造不锈钢和各种合金钢被广泛地用于飞机、舰艇、雷达、导弹、陶瓷颜料、永磁材料、
电子遥控等领域。回答下列问题:
(1)基态Ni原子的价电子轨道表示式(电子排布图)为___。
(2)具有不对称结构的Schiff碱及其与过渡金属形成的配合物结构类似于生命体系的真实情况。有一种广泛
用于生命体系中金属蛋白的模拟研究,其结构如图所示。
该配合物中C原子的杂化方式为___;该配合物中除H之外的组成元素的第一电离能由小到大的顺序是
___。
(3)二氧化硒主要用于电解锰行业,其中一种制备方法为2NiSeO 2NiSeO+O ↑、NiSeO
4 3 2 3
NiO+SeO。下列分子或离子的VSEPR模型为平面三角形的是___(填字母)。
2
A.SeO2- B.SeO2- C.NiO D.SeO
4 3 2
(4)草酸镍可用于制镍粉和镍的催化剂等,加热分解的化学方程式为NiC O NiO+CO+CO ,属于非极性
2 4 2
分子的产物是___,等物质的量的CO(C≡O)与CO 分子中的π键比为___,与CO 互为等电子体(等电子体是指
2 2
价电子数和原子数相同的分子、离子或原子团)的阴离子为___(任写一种)。
(5)氢能是一种重要的二次能源,其独有的优势和丰富的资源引起人类广泛的兴趣,然而氢的储存是目前
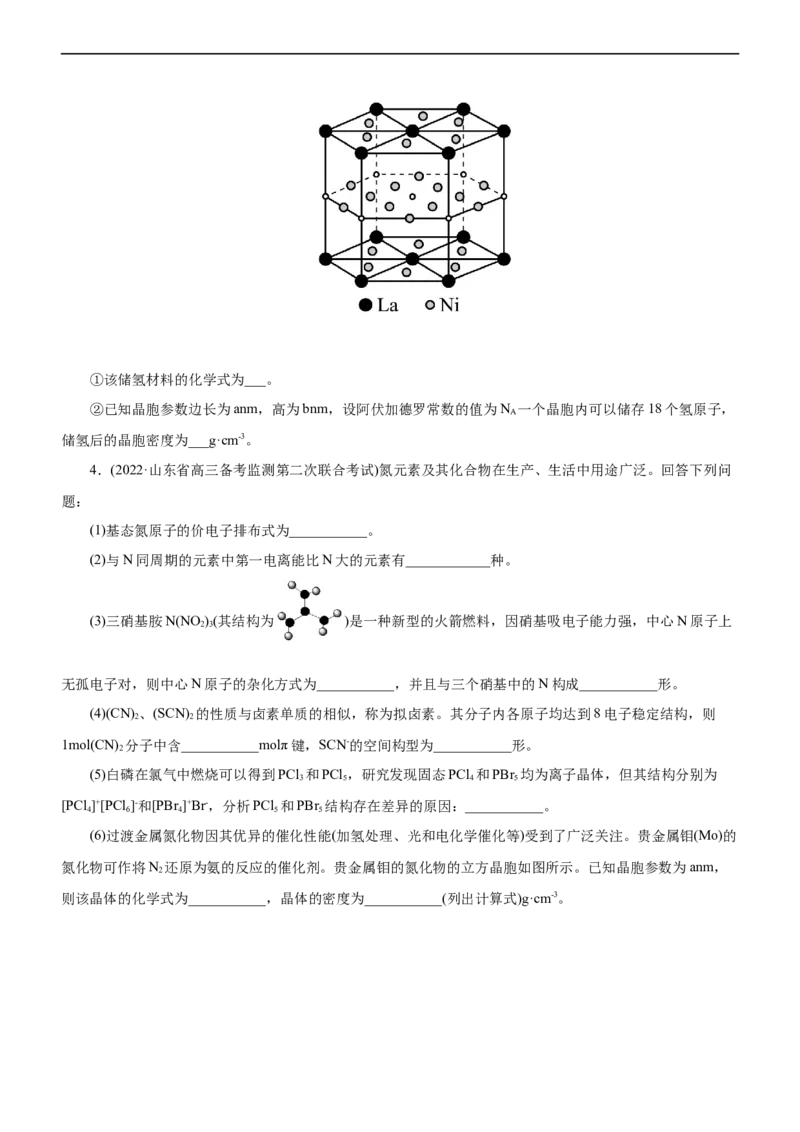
氢能利用的一大难题,现有La、Ni合金是较为理想的储氢材料,其晶胞结构如图所示:①该储氢材料的化学式为___。
②已知晶胞参数边长为anm,高为bnm,设阿伏加德罗常数的值为N 一个晶胞内可以储存18个氢原子,
A
储氢后的晶胞密度为___g·cm-3。
4.(2022·山东省高三备考监测第二次联合考试)氮元素及其化合物在生产、生活中用途广泛。回答下列问
题:
(1)基态氮原子的价电子排布式为___________。
(2)与N同周期的元素中第一电离能比N大的元素有____________种。
(3)三硝基胺N(NO)(其结构为 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上
2 3
无孤电子对,则中心N原子的杂化方式为___________,并且与三个硝基中的N构成___________形。
(4)(CN) 、(SCN) 的性质与卤素单质的相似,称为拟卤素。其分子内各原子均达到8电子稳定结构,则
2 2
1mol(CN) 分子中含___________molπ键,SCN-的空间构型为___________形。
2
(5)白磷在氯气中燃烧可以得到PCl 和PCl ,研究发现固态PCl 和PBr 均为离子晶体,但其结构分别为
3 5 4 5
[PCl ]+[PCl ]-和[PBr ]+Br-,分析PCl 和PBr 结构存在差异的原因:___________。
4 6 4 5 5
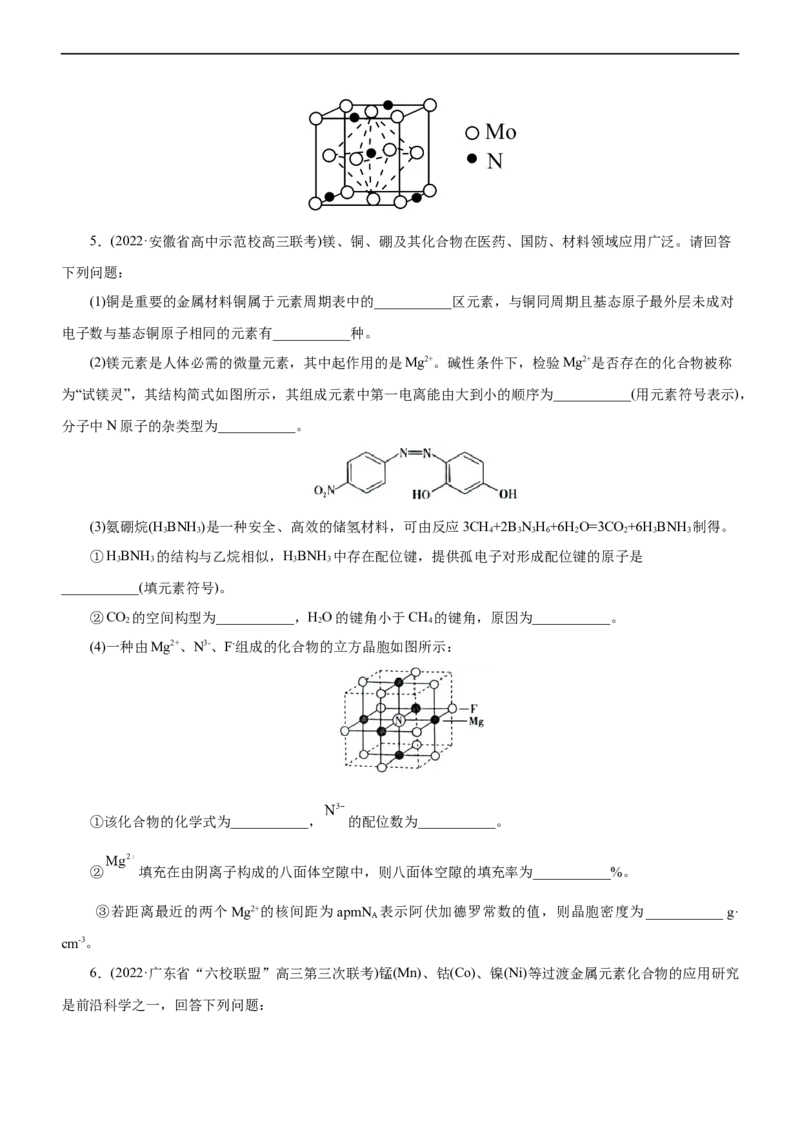
(6)过渡金属氮化物因其优异的催化性能(加氢处理、光和电化学催化等)受到了广泛关注。贵金属钼(Mo)的
氮化物可作将N 还原为氨的反应的催化剂。贵金属钼的氮化物的立方晶胞如图所示。已知晶胞参数为anm,
2
则该晶体的化学式为___________,晶体的密度为___________(列出计算式)g·cm-3。5.(2022·安徽省高中示范校高三联考)镁、铜、硼及其化合物在医药、国防、材料领域应用广泛。请回答
下列问题:
(1)铜是重要的金属材料铜属于元素周期表中的___________区元素,与铜同周期且基态原子最外层未成对
电子数与基态铜原子相同的元素有___________种。
(2)镁元素是人体必需的微量元素,其中起作用的是Mg2+。碱性条件下,检验Mg2+是否存在的化合物被称
为“试镁灵”,其结构简式如图所示,其组成元素中第一电离能由大到小的顺序为___________(用元素符号表示),
分子中N原子的杂类型为___________。
(3)氨硼烷(H BNH )是一种安全、高效的储氢材料,可由反应3CH+2B NH+6H O=3CO+6H BNH 制得。
3 3 4 3 3 6 2 2 3 3
①HBNH 的结构与乙烷相似,HBNH 中存在配位键,提供孤电子对形成配位键的原子是
3 3 3 3
___________(填元素符号)。
②CO 的空间构型为___________,HO的键角小于CH 的键角,原因为___________。
2 2 4
(4)一种由Mg2+、N3-、F-组成的化合物的立方晶胞如图所示:
①该化合物的化学式为___________, 的配位数为___________。
② 填充在由阴离子构成的八面体空隙中,则八面体空隙的填充率为___________%。
③若距离最近的两个Mg2+的核间距为apmN 表示阿伏加德罗常数的值,则晶胞密度为___________ g·
A
cm-3。
6.(2022·广东省“六校联盟”高三第三次联考)锰(Mn)、钴(Co)、镍(Ni)等过渡金属元素化合物的应用研究
是前沿科学之一,回答下列问题:(1)Mn的价电子排布式为___________。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用
“___________理论”解释。
(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列___________(填序号),每个Mn原子周
围紧邻的原子数为___________。
A. B. C. D.
(3)[Co(DMSO) ](ClO) 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为SO(CH )。DMSO中硫原
6 4 2 3 2
子的杂化轨道类型为___________,SO(CH ) 中键角∠C—S—O___________CHCOCH 中键角∠C—C—O(填
3 2 3 3
“大于”“小于”或“等于”),ClO 的空间构型是___________,元素S、Cl、O的电负性由大到小的顺序为
___________。
(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(CH=CH—CHOH),其相对分子质量等于丙醛
2 2
(CHCHCHO),但两者沸点相差较大,原因是___________。
3 2
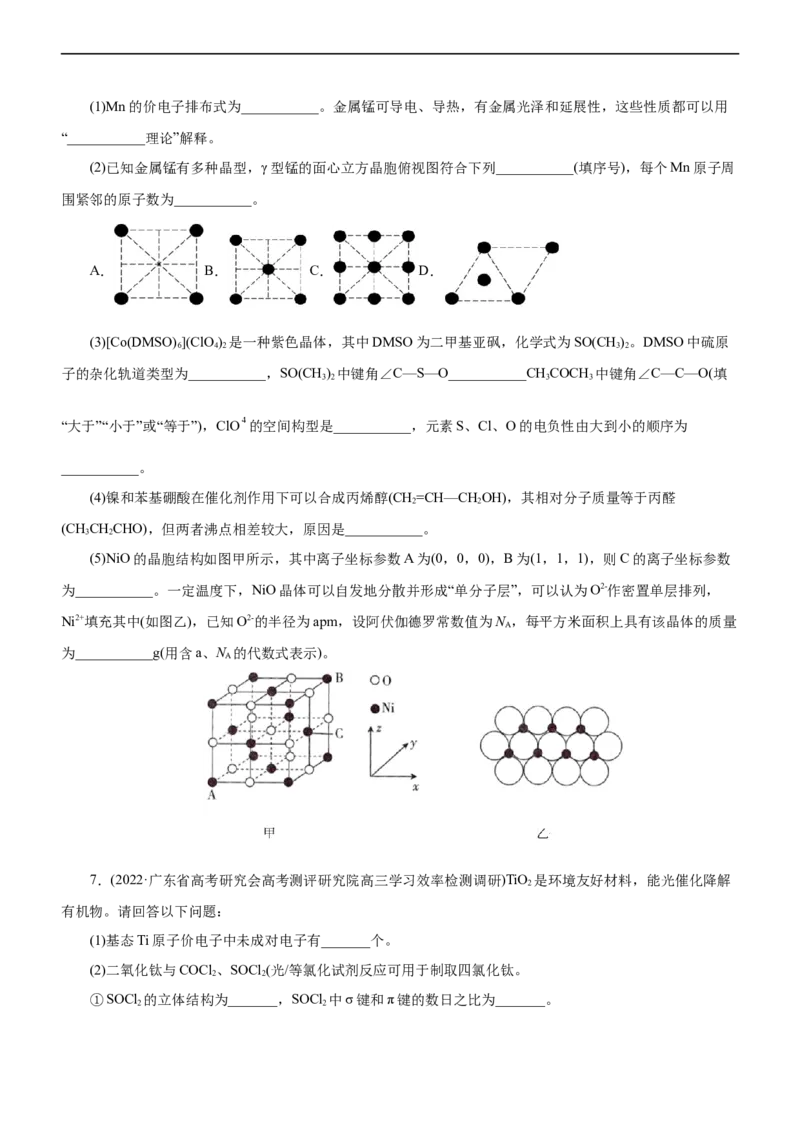
(5)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数
为___________。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,
Ni2+填充其中(如图乙),已知O2-的半径为apm,设阿伏伽德罗常数值为N ,每平方米面积上具有该晶体的质量
A
为___________g(用含a、N 的代数式表示)。
A
7.(2022·广东省高考研究会高考测评研究院高三学习效率检测调研)TiO 是环境友好材料,能光催化降解
2
有机物。请回答以下问题:
(1)基态Ti原子价电子中未成对电子有_______个。
(2)二氧化钛与COCl 、SOCl (光/等氯化试剂反应可用于制取四氯化钛。
2 2
①SOCl 的立体结构为_______,SOCl 中σ键和π键的数日之比为_______。
2 2②COCl 是_______分子。(填“极性”或“非极性”)
2
(3)香豆素 是一种天然香料,能被TiO 光降解。
2
①香豆素分子中C、О元素的第一电离能大小关系是_______,理由足_______。
②分子中C原子的杂化类型是_______。
③已知单双键交替的共轭结构可以形成大π键,大π键可用符号“π”表示,其中n代表参形成大π键的原子
数,m代表参与形成大π键的电子数(如香豆素中的大π键可表示为 ),则苯分子中的大π键应该表示为
_______。
(4)研究表明,在TiO 通过氮掺杂反应生成TiO N,能使TiO 对可见光具有活性,反应如图所示。
2 2-a b 2
TiO N 晶体中a:b=_______
2-a b
8.(2022·湖北省重点校联考高三试题)氮族元素N、P、As等元素在农药、化肥等领域有广泛应用。回答
下列问题:
(1)基态磷原子中,电子占据的最高能层符号为___________。
(2)基态As原子的核外电子排布式为___________。
(3)氮元素的简单气态氢化物为NH ,其沸点比PH 的___________(填“高”或“低”),理由是
3 3
___________。
(4)氮元素的常见含氧酸根为NO -,其空间构型为___________,其中N的杂化方式为___________。NO -
3 3
和Co2+可形成配离子[Co(NO )]2+,该配离子中各元素的第一电离能由小到大的顺序为___________(用元素符号
3 4
表示),1mol该配离子中含有的 键数目为___________ N 。
A
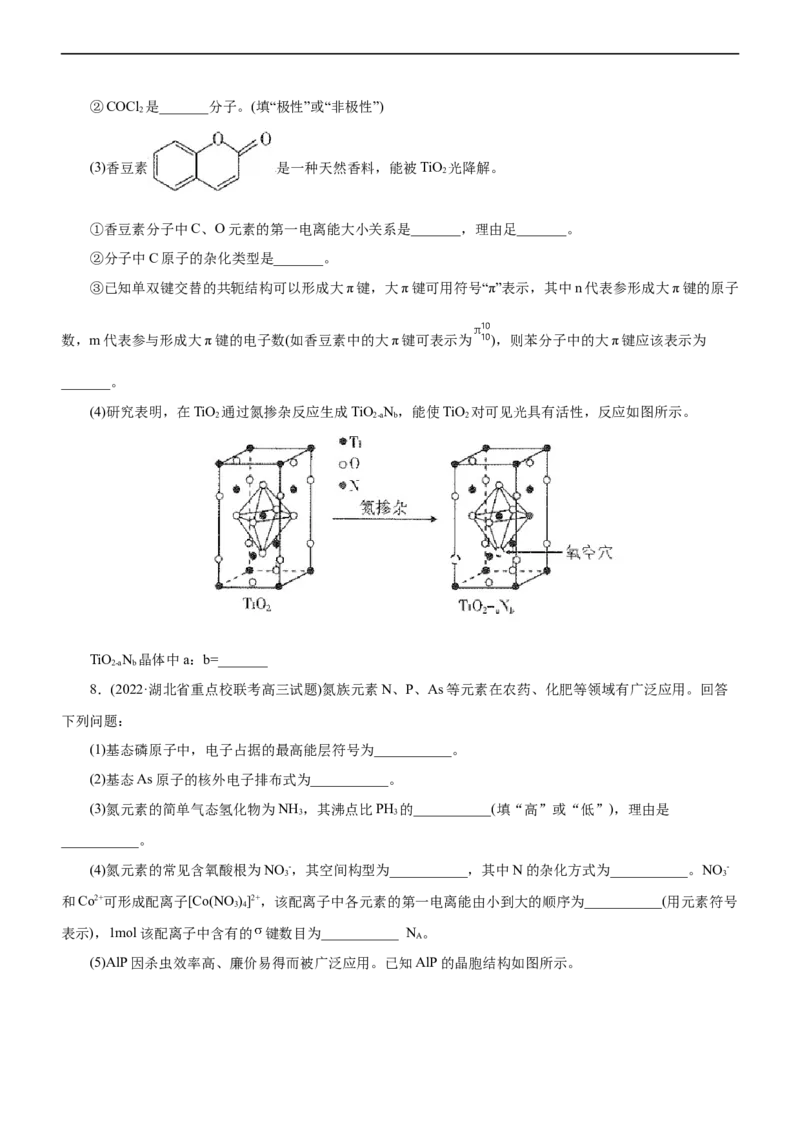
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的晶胞结构如图所示。①A、B点的原子坐标如图所示,则C点的原子坐标为___________。
②磷化铝的晶胞参数 (1pm=10-12m),其密度为___________g/cm3(列出计算式即可,N 表示阿
A
伏加德罗常数的值)。
9.(2022·山东省潍坊市高三学科核心素养测评)铜和钴掺杂的含氮碳层材料是一种新型催化材料,具有氧
还原催化性能。回答下列问题:
(1)下列状态的N原子或离子的核外电子在跃迁时,用光谱仪可捕捉到发射光谱的是_____(填序号)。
A.1s22s22p3 B.1s22s2 C.1s22s12p4 D.1s22s22p6
(2)已知氮的两种化合物NH 和NH OH都能结合H+而具有弱碱性,二者的碱性强弱:
2 4 2
NH_____NH OH(填“强于”或“弱于”),理由是___。
2 4 2
(3)叠氮酸根NN-的空间结构是______,NONO -中含有的价层电子对数目为______。
3 2
(4)Co的第四电离能比铁的第四电离能______(填“大”或“小”),理由是____。
(5)高导电紫铜常用硼化钙提高导电率,其晶胞如图所示,具有立方晶系的对称性,B原子全部组成正八面
体,各个顶点通过B—B键连接成三维骨架,则该硼化钙的化学式是___________,B原子半径为r nm,阿伏
加德罗常数的值为N ,则硼化钙的密度 为___________g·cm-3。
A
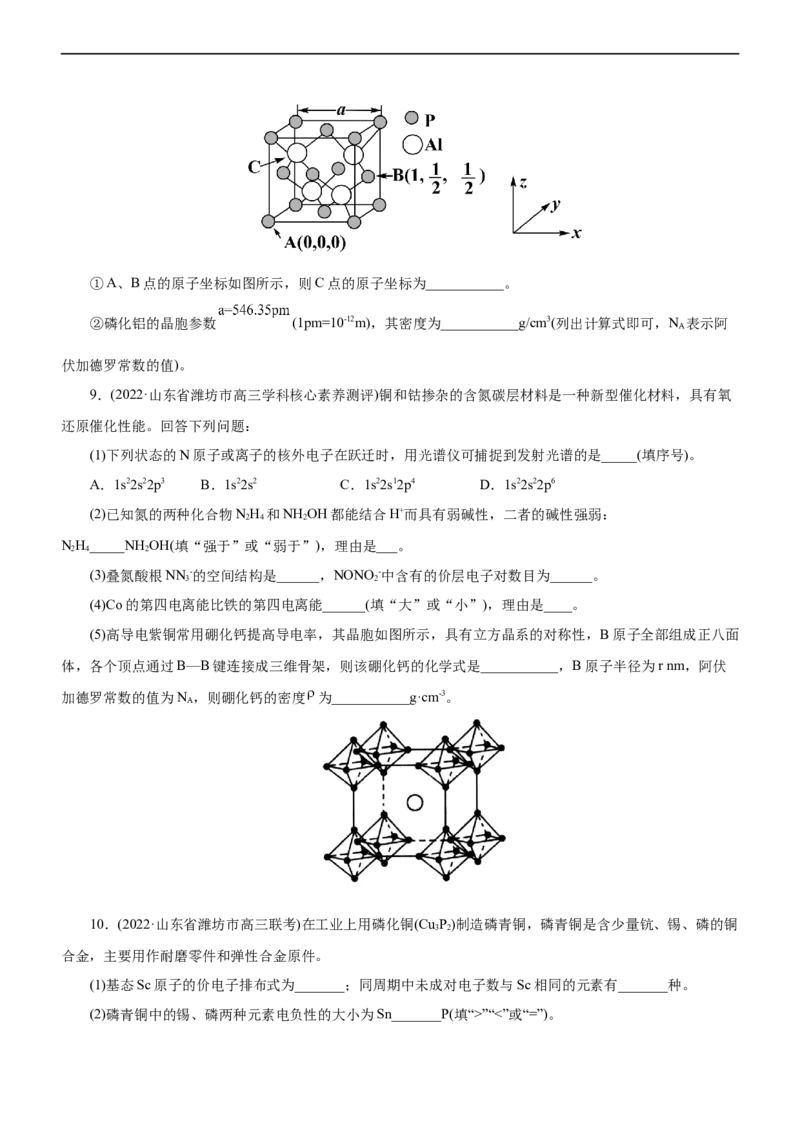
10.(2022·山东省潍坊市高三联考)在工业上用磷化铜(Cu P)制造磷青铜,磷青铜是含少量钪、锡、磷的铜
3 2
合金,主要用作耐磨零件和弹性合金原件。
(1)基态Sc原子的价电子排布式为_______;同周期中未成对电子数与Sc相同的元素有_______种。
(2)磷青铜中的锡、磷两种元素电负性的大小为Sn_______P(填“>”“<”或“=”)。(3)NH 易与Cu2+形成[Cu(NH )]2+配离子,在该配离子中H-N-H键角比NH 分子中H-N-H键角大的原因是
3 3 4 3
_______。[Cu(NH )]2+中2个NH 被2个HO取代,得到两种结构的配离子,则[Cu(NH )]2+的空间构型是
3 4 3 2 3 4
_______(填“正四面体”或“正四边形”)。
(4)某立方磷青铜晶体的晶胞结构如图所示。
①原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0),B为(1,1,
0),C为(0,1,1),则D原子的分数坐标为_______。
②若晶体密度为ρg/cm3,最近的Cu原子核间距为_______pm(用含ρ、N 的代数式表示)。
A
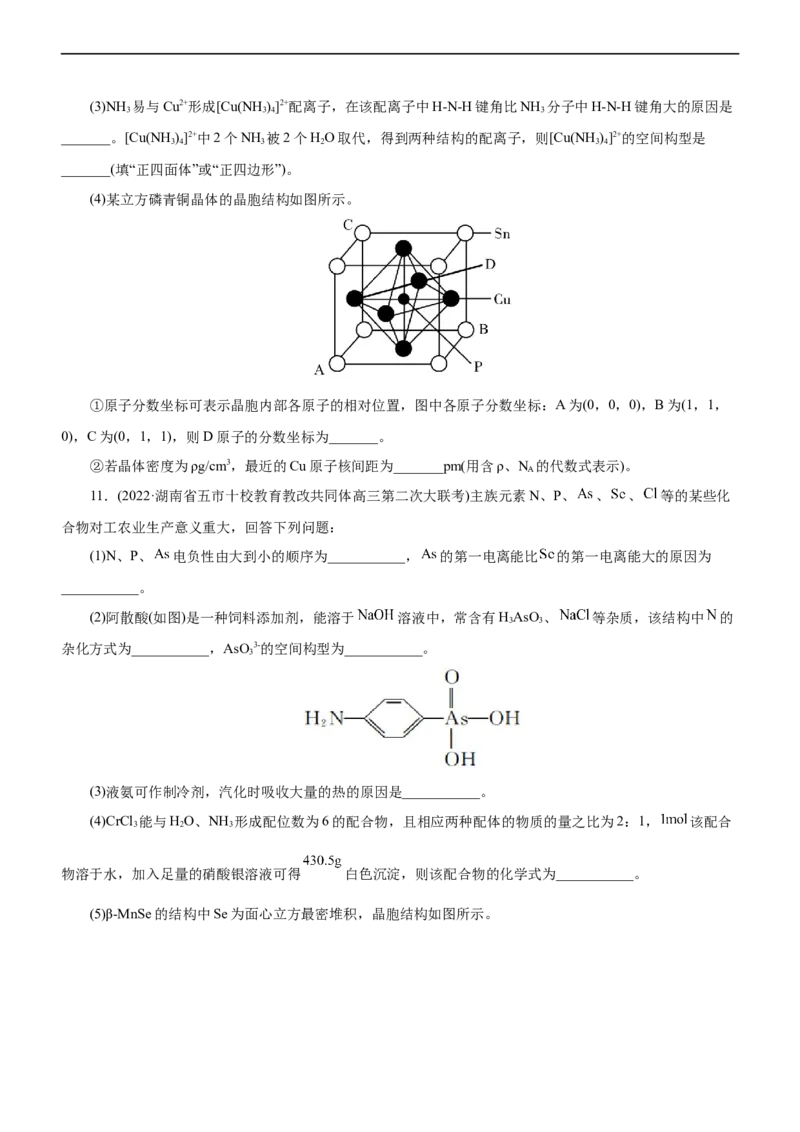
11.(2022·湖南省五市十校教育教改共同体高三第二次大联考)主族元素N、P、 、 、 等的某些化
合物对工农业生产意义重大,回答下列问题:
(1)N、P、 电负性由大到小的顺序为___________, 的第一电离能比 的第一电离能大的原因为
___________。
(2)阿散酸(如图)是一种饲料添加剂,能溶于 溶液中,常含有HAsO、 等杂质,该结构中 的
3 3
杂化方式为___________,AsO3-的空间构型为___________。
3
(3)液氨可作制冷剂,汽化时吸收大量的热的原因是___________。
(4)CrCl 能与HO、NH 形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1, 该配合
3 2 3
物溶于水,加入足量的硝酸银溶液可得 白色沉淀,则该配合物的化学式为___________。
(5)β-MnSe的结构中Se为面心立方最密堆积,晶胞结构如图所示。① 中 的配位数为___________。
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为N ,则β-MnSe的密度 ___________(列出表达
A
式) g· cm-3。
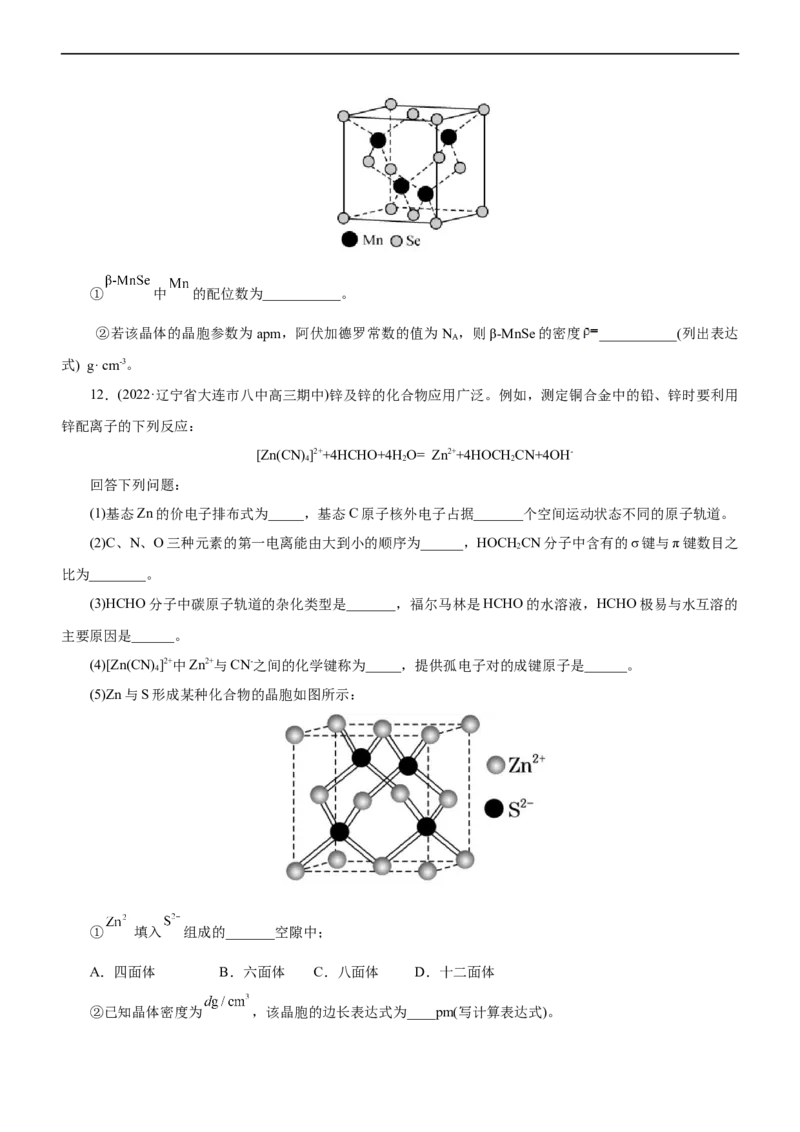
12.(2022·辽宁省大连市八中高三期中)锌及锌的化合物应用广泛。例如,测定铜合金中的铅、锌时要利用
锌配离子的下列反应:
[Zn(CN)]2++4HCHO+4H O= Zn2++4HOCH CN+4OH-
4 2 2
回答下列问题:
(1)基态Zn的价电子排布式为_____,基态C原子核外电子占据_______个空间运动状态不同的原子轨道。
(2)C、N、O三种元素的第一电离能由大到小的顺序为______,HOCH CN分子中含有的σ键与π键数目之
2
比为________。
(3)HCHO分子中碳原子轨道的杂化类型是_______,福尔马林是HCHO的水溶液,HCHO极易与水互溶的
主要原因是______。
(4)[Zn(CN)]2+中Zn2+与CN-之间的化学键称为_____,提供孤电子对的成键原子是______。
4
(5)Zn与S形成某种化合物的晶胞如图所示:
① 填入 组成的_______空隙中;
A.四面体 B.六面体 C.八面体 D.十二面体
②已知晶体密度为 ,该晶胞的边长表达式为____pm(写计算表达式)。13.(2022·山东省日照市高三校际联考)“掺杂”和“包覆”是改善电极性能的重要手段。工业上以LiCO 为原
2 3
料制备锂离子电池的正极材料NCM811(LiNi Co Mn O)。
0.8 0.1 0.1 2
回答下列问题:
(1)基态氧原子价电子轨道表示式为___;Mn属于__区元素;基态Co原子核外电子有__种运动状态。
(2)与LiCO 的阴离子互为等电子体的分子有__(填化学式);LiCO 阴离子的中心原子采取了__杂化方式,
2 3 2 3
LiCO 热稳定性__(填“>”或“<”)其同族其他元素的碳酸盐。
2 3
(3)“掺杂”能够提高电极的电导率和结构稳定性。MgF 是常用的掺杂剂,其熔点高于MgCl 熔点的原因为
2 2
___。
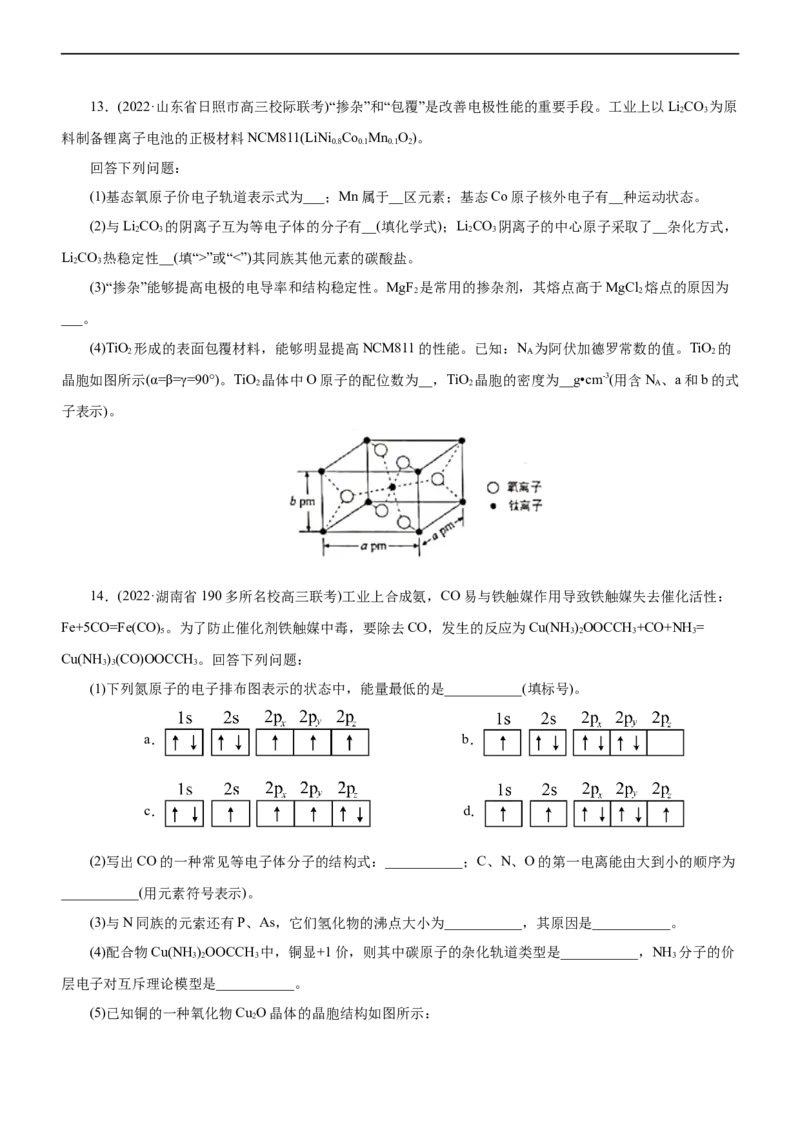
(4)TiO 形成的表面包覆材料,能够明显提高NCM811的性能。已知:N 为阿伏加德罗常数的值。TiO 的
2 A 2
晶胞如图所示(α=β=γ=90°)。TiO 晶体中O原子的配位数为__,TiO 晶胞的密度为__g•cm-3(用含N 、a和b的式
2 2 A
子表示)。
14.(2022·湖南省190多所名校高三联考)工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:
Fe+5CO=Fe(CO) 。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH )OOCCH +CO+NH=
5 3 2 3 3
Cu(NH )(CO)OOCCH 。回答下列问题:
3 3 3
(1)下列氮原子的电子排布图表示的状态中,能量最低的是___________(填标号)。
a. b.
c. d.
(2)写出CO的一种常见等电子体分子的结构式:___________;C、N、O的第一电离能由大到小的顺序为
___________(用元素符号表示)。
(3)与N同族的元索还有P、As,它们氢化物的沸点大小为___________,其原因是___________。
(4)配合物Cu(NH )OOCCH 中,铜显+1价,则其中碳原子的杂化轨道类型是___________,NH 分子的价
3 2 3 3
层电子对互斥理论模型是___________。
(5)已知铜的一种氧化物Cu O晶体的晶胞结构如图所示:
2①若坐标参数A为(0,0,0),C为( , , ),则B的坐标参数为___________。
②若阿伏加德罗常数的值为N ,该晶胞的边长为a pm,则晶体的密度为___________g/cm3。
A
15.(2022·河北省邢台市“五岳联盟”部分重点学校高三联考)我国科学家发现AgCrS (AMX 家族成员之
2 2
一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。基态硫原子核外最多有___________个
电子顺时针旋转。基态铬原子有___________个未成对电子。
(2)氧族元素有氧、硫、硒(Se)、碲(Te)等元素。
①这四种元素中,电负性最大的是___________(填元素符号)。
②科学家用亚硒酸盐和硫酸盐跟踪固氮酶,研究反应机理。SeO2-的空间构型为___________,TeO2-中碲
3 4
的杂化类型是___________。
③HO、HS、HSe、HTe的键角依次减小,其主要原因可能是___________。
2 2 2 2
(3)配合物[Cr(OH) (H O)en] (en为HNCH CHNH )的中心离子配位数为___________。(Cr与O、N均形成
3 2 2 2 2 2
了配位键)
(4)在银氨溶液中,1 mol[Ag(NH )]+中含___________molσ键。
3 2
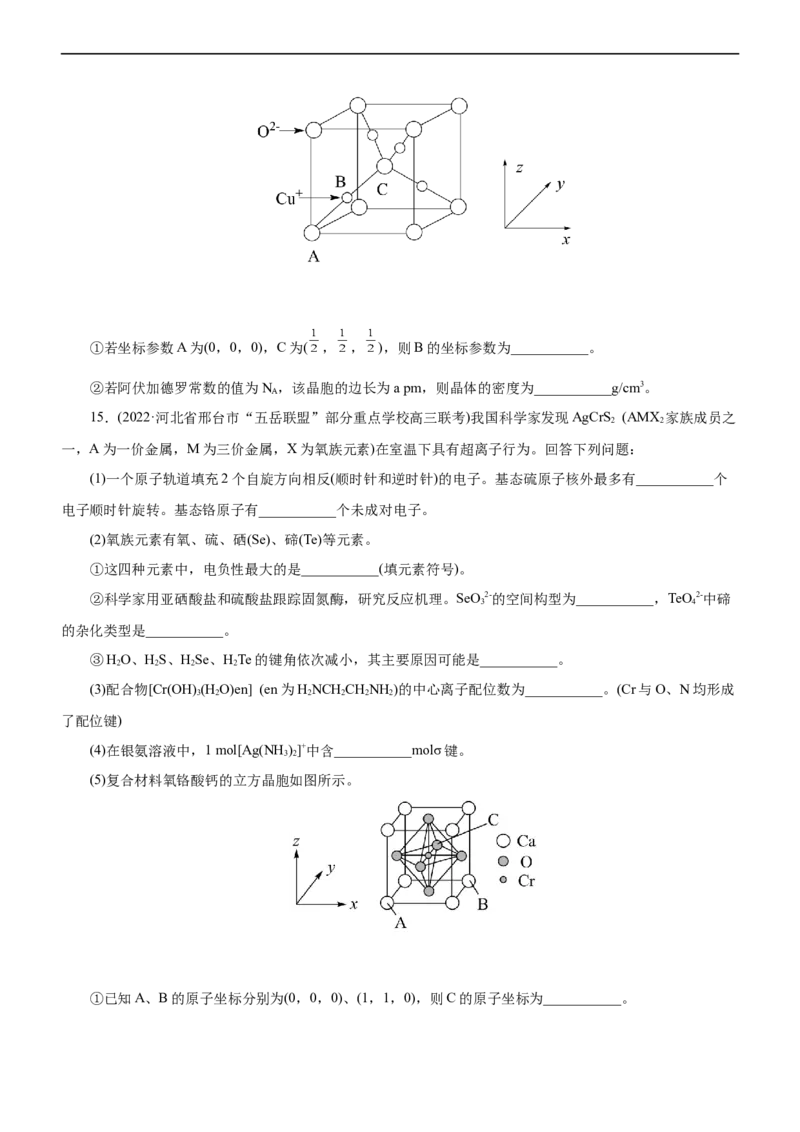
(5)复合材料氧铬酸钙的立方晶胞如图所示。
①已知A、B的原子坐标分别为(0,0,0)、(1,1,0),则C的原子坐标为___________。②1个钙原子与___________个氧原子等距离且最近。
③该晶体密度为___________ g· cm-3 (列出计算式即可)。已知钙和氧的最近距离为a nm,N 代表阿伏加
A
德罗常数。
16.(2023·湘豫名校联盟高三联考)新型半导体材料如碳化硅(SiC)、氮化镓(GaN)等在国防技术、航空航天
及5G技术等领域扮演着重要的角色。回答下列问题:
(1)基态Si原子中,核外电子占据的最高能层的符号为___________,占据最高能级的电子的电子云轮廓图
形状为___________;基态Ga原子的核外电子排布为[Ar]3d104s24p1,其转化为下列激发态时,吸收能量最少的
是___________(填选项字母)。
A.[Ar]
B.[Ar]
C.[Ar]
D.[Ar]
(2)C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子
结构分析,其原因为___________。
(3)GaCl 的熔点为77.9℃,GaF 的熔点为1000℃,试分析GaCl 熔点低于GaF 的原因为___________;气
3 3 3 3
态GaCl 常以二聚体形式存在,二聚体中各原子均满足8e-结构,据此写出二聚体的结构式为___________。
3
(4)B和Mg形成的化合物刷新了金属化合物超导温度的最高记录。该化合物的晶体结构单元如图所示,其
中Mg原子间形成正六棱柱,6个B原子分别位于六个三棱柱体心。则该化合物的化学式可表示为___________;
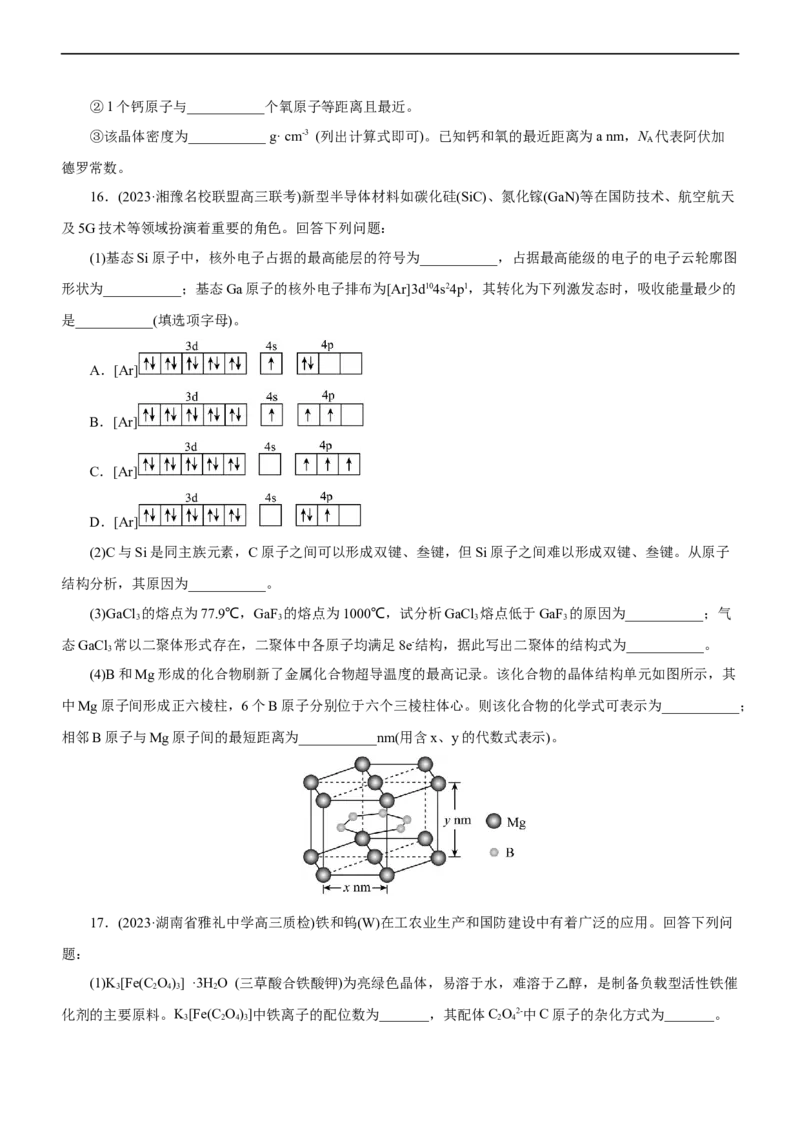
相邻B原子与Mg原子间的最短距离为___________nm(用含x、y的代数式表示)。
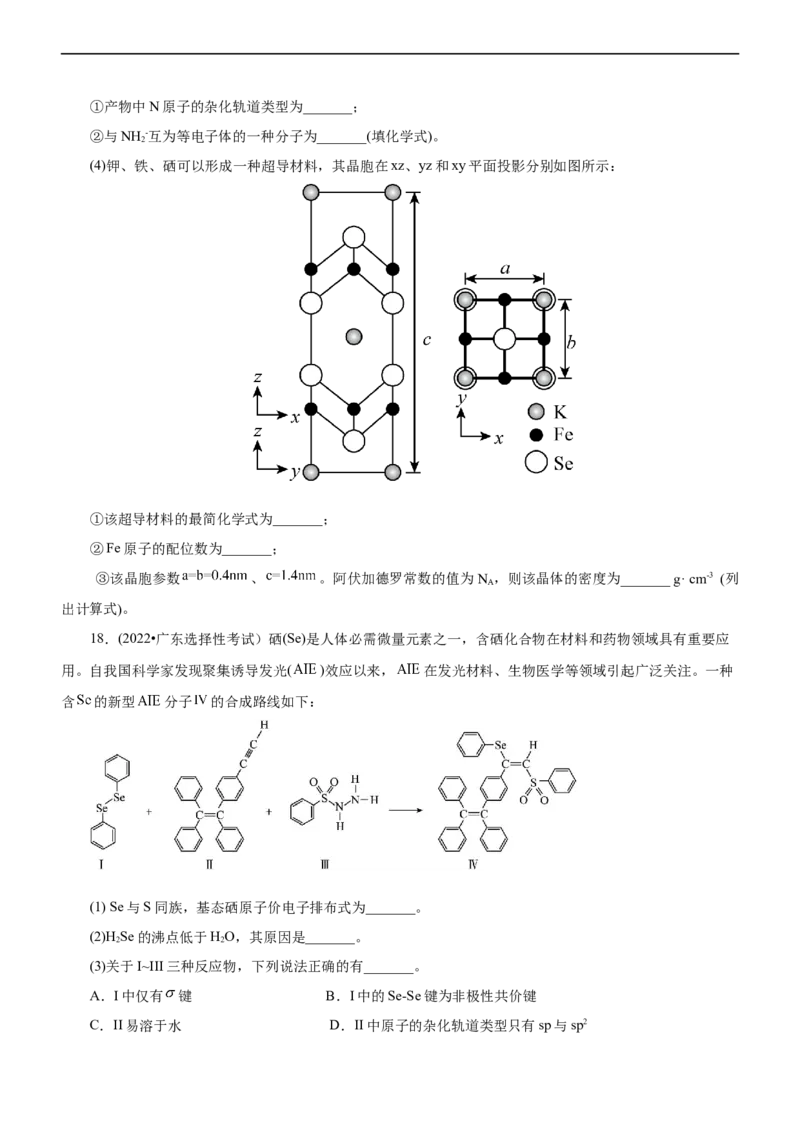
17.(2023·湖南省雅礼中学高三质检)铁和钨(W)在工农业生产和国防建设中有着广泛的应用。回答下列问
题:
(1)K [Fe(C O)] ·3H O (三草酸合铁酸钾)为亮绿色晶体,易溶于水,难溶于乙醇,是制备负载型活性铁催
3 2 4 3 2
化剂的主要原料。K[Fe(C O)]中铁离子的配位数为_______,其配体C O2-中C原子的杂化方式为_______。
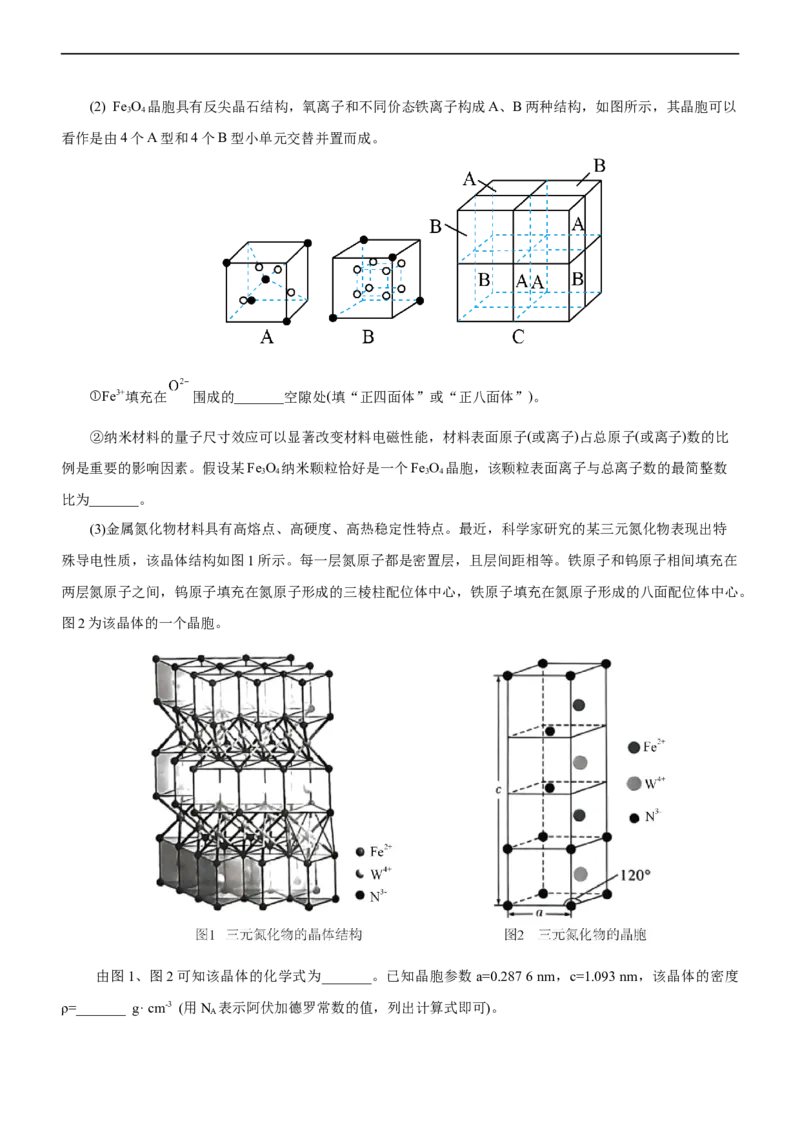
3 2 4 3 2 4(2) Fe O 晶胞具有反尖晶石结构,氧离子和不同价态铁离子构成A、B两种结构,如图所示,其晶胞可以
3 4
看作是由4个A型和4个B型小单元交替并置而成。
①Fe3+填充在 围成的_______空隙处(填“正四面体”或“正八面体”)。
②纳米材料的量子尺寸效应可以显著改变材料电磁性能,材料表面原子(或离子)占总原子(或离子)数的比
例是重要的影响因素。假设某Fe O 纳米颗粒恰好是一个Fe O 晶胞,该颗粒表面离子与总离子数的最简整数
3 4 3 4
比为_______。
(3)金属氮化物材料具有高熔点、高硬度、高热稳定性特点。最近,科学家研究的某三元氮化物表现出特
殊导电性质,该晶体结构如图1所示。每一层氮原子都是密置层,且层间距相等。铁原子和钨原子相间填充在
两层氮原子之间,钨原子填充在氮原子形成的三棱柱配位体中心,铁原子填充在氮原子形成的八面配位体中心。
图2为该晶体的一个晶胞。
由图1、图2可知该晶体的化学式为_______。已知晶胞参数a=0.287 6 nm,c=1.093 nm,该晶体的密度
ρ=_______ g· cm-3 (用N 表示阿伏加德罗常数的值,列出计算式即可)。
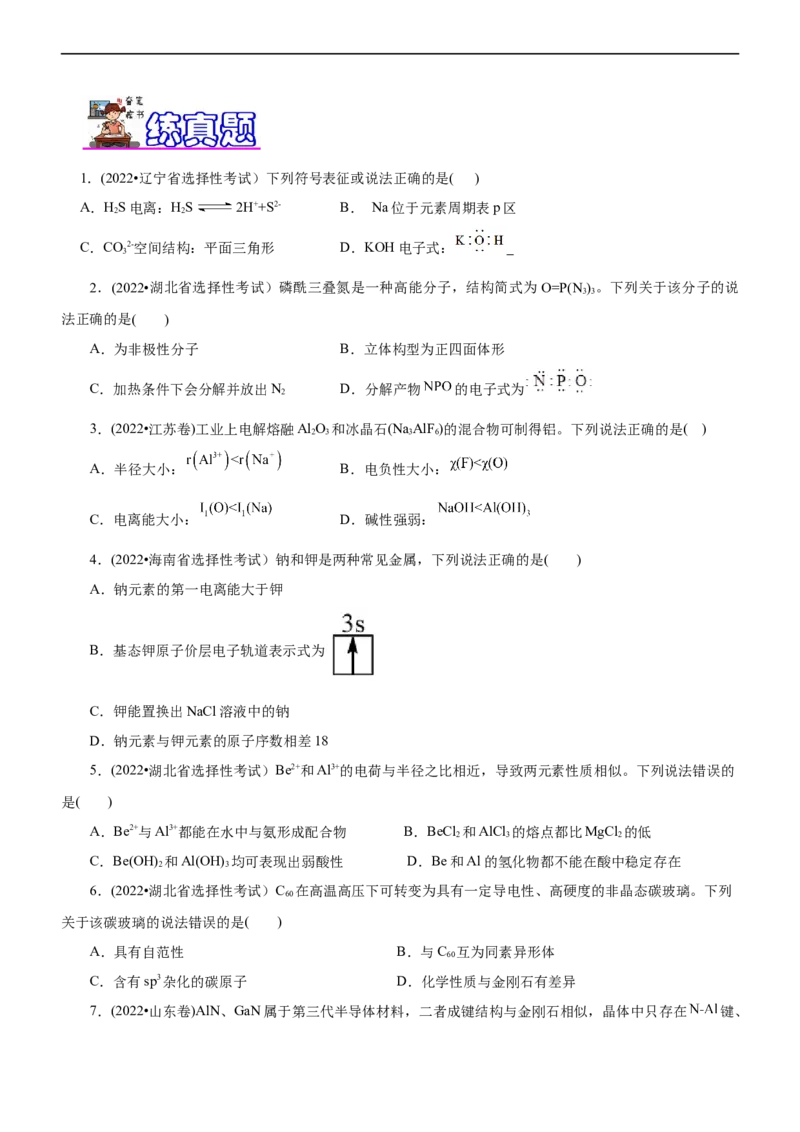
A1.(2022•辽宁省选择性考试)下列符号表征或说法正确的是( )
A.HS电离:HS 2H++S2- B. Na位于元素周期表p区
2 2
C.CO2-空间结构:平面三角形 D.KOH电子式:
3
2.(2022•湖北省选择性考试)磷酰三叠氮是一种高能分子,结构简式为 O=P(N ) 。下列关于该分子的说
3 3
法正确的是( )
A.为非极性分子 B.立体构型为正四面体形
C.加热条件下会分解并放出N D.分解产物 的电子式为
2
3.(2022•江苏卷)工业上电解熔融Al O 和冰晶石(Na AlF)的混合物可制得铝。下列说法正确的是( )
2 3 3 6
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
4.(2022•海南省选择性考试)钠和钾是两种常见金属,下列说法正确的是( )
A.钠元素的第一电离能大于钾
B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠
D.钠元素与钾元素的原子序数相差18
5.(2022•湖北省选择性考试)Be2+和Al3+的电荷与半径之比相近,导致两元素性质相似。下列说法错误的
是( )
A.Be2+与Al3+都能在水中与氨形成配合物 B.BeCl 和AlCl 的熔点都比MgCl 的低
2 3 2
C.Be(OH) 和Al(OH) 均可表现出弱酸性 D.Be和Al的氢化物都不能在酸中稳定存在
2 3
6.(2022•湖北省选择性考试)C 在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下列
60
关于该碳玻璃的说法错误的是( )
A.具有自范性 B.与C 互为同素异形体
60
C.含有sp3杂化的碳原子 D.化学性质与金刚石有差异
7.(2022•山东卷)AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在 键、键。下列说法错误的是( )
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化 D.晶体中所有原子的配位数均相同
8.(2021•湖北选择性考试)金属Na溶解于液氨中形成氨合钠离子和氨合电子,向该溶液中加入穴醚类配
体L,得到首个含碱金属阴离子的金黄色化合物[NaL]+Na-。下列说法错误的是( )
A.Na的半径比F的大 B.Na的还原性比Na的强
C.Na的第一电离能比H的大 D.该事实说明Na也可表现非金属性
9.(2022•海南省选择性考试)(双选)已知CHCOOH+Cl ClCH COOH+HCl,ClCH COOH的酸性
3 2 2 2
比CHCOOH强。下列有关说法正确的是( )
3
A.HCl的电子式为 B.Cl-Cl键的键长比I-I键短
C.CHCOOH分子中只有σ键 D.ClCH COOH的酸性比ICHCOOH强
3 2 2
10.(2022•江苏卷)下列说法正确的是( )
A.金刚石与石墨烯中的C-C-C夹角都为
B.SiH、SiCl 都是由极性键构成的非极性分子
4 4
C.锗原子( Ge)基态核外电子排布式为4s24p2
32
D.ⅣA族元素单质的晶体类型相同
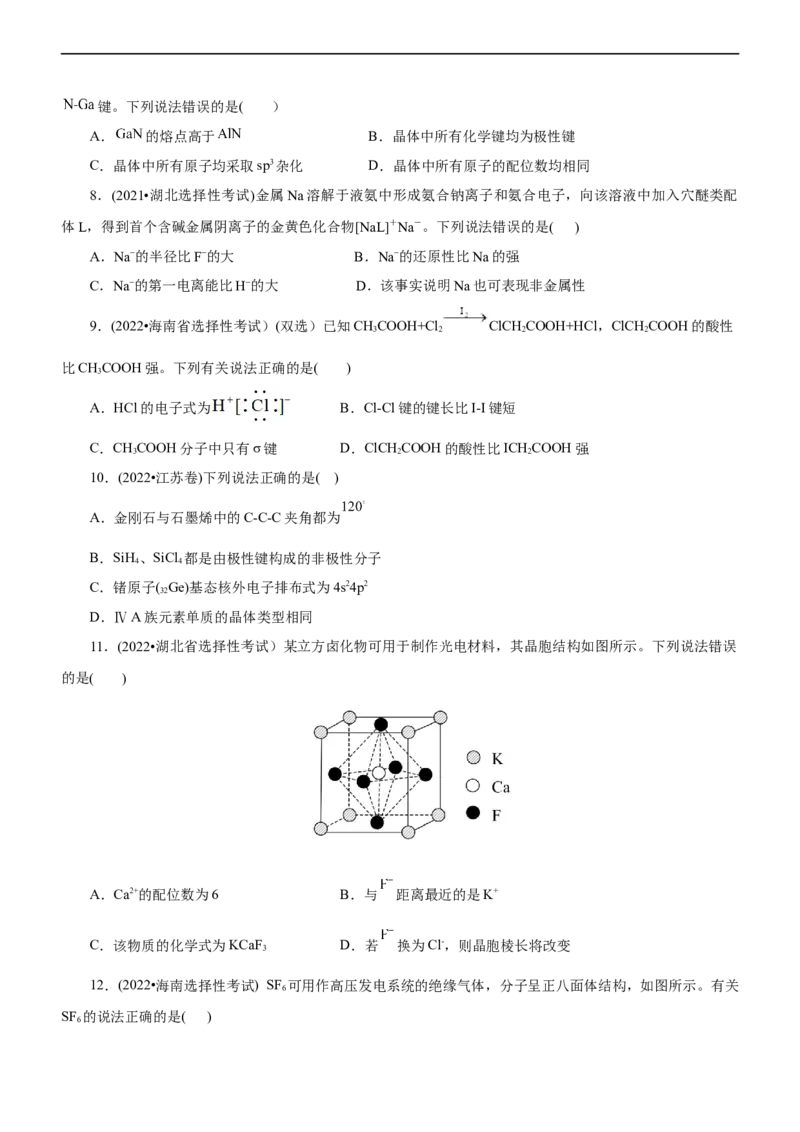
11.(2022•湖北省选择性考试)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误
的是( )
A.Ca2+的配位数为6 B.与 距离最近的是K+
C.该物质的化学式为KCaF D.若 换为Cl-,则晶胞棱长将改变
3
12.(2022•海南选择性考试) SF 可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关
6
SF 的说法正确的是( )
6A.是非极性分子 B.键角 都等于90°
C. 与 之间共用电子对偏向S D. 原子满足8电子稳定结构
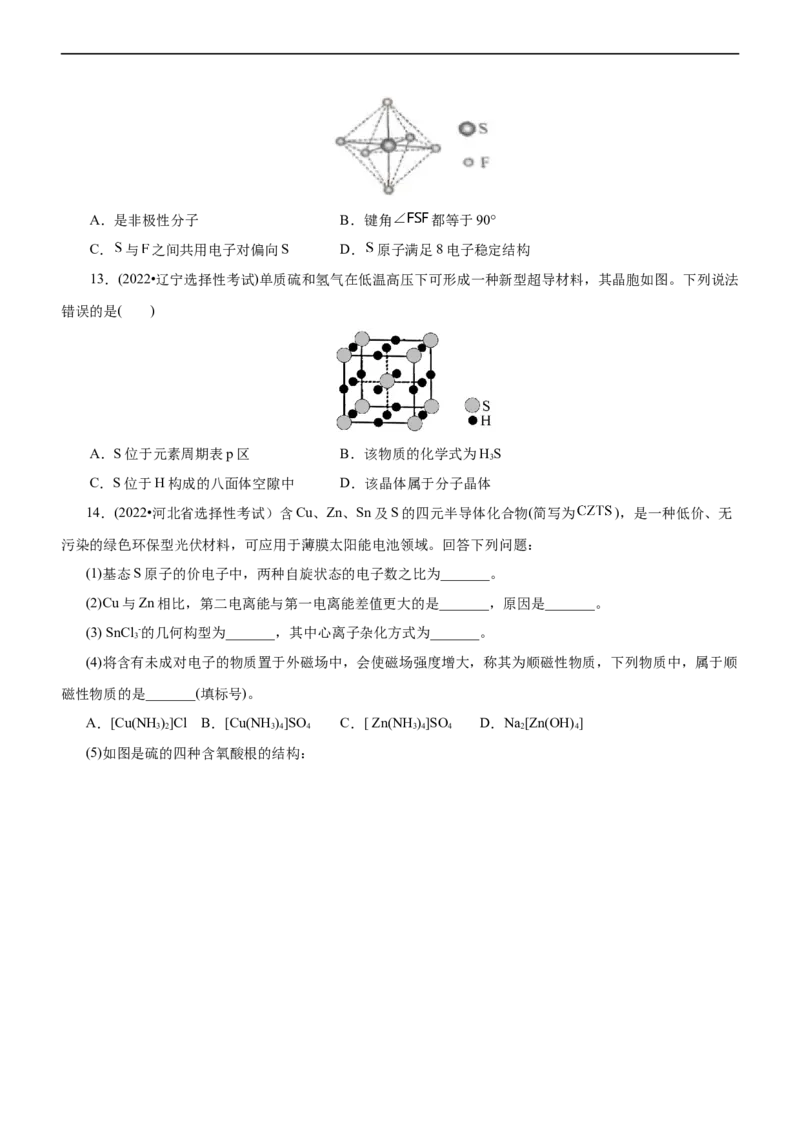
13.(2022•辽宁选择性考试)单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列说法
错误的是( )
A.S位于元素周期表p区 B.该物质的化学式为HS
3
C.S位于H构成的八面体空隙中 D.该晶体属于分子晶体
14.(2022•河北省选择性考试)含Cu、Zn、Sn及S的四元半导体化合物(简写为 ),是一种低价、无
污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_______。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是_______,原因是_______。
(3) SnCl -的几何构型为_______,其中心离子杂化方式为_______。
3
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺
磁性物质的是_______(填标号)。
A.[Cu(NH )]Cl B.[Cu(NH )]SO C.[ Zn(NH )]SO D.Na[Zn(OH) ]
3 2 3 4 4 3 4 4 2 4
(5)如图是硫的四种含氧酸根的结构:根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO -的是_______(填标号)。理由是_______。
4
本题暂无(6)问
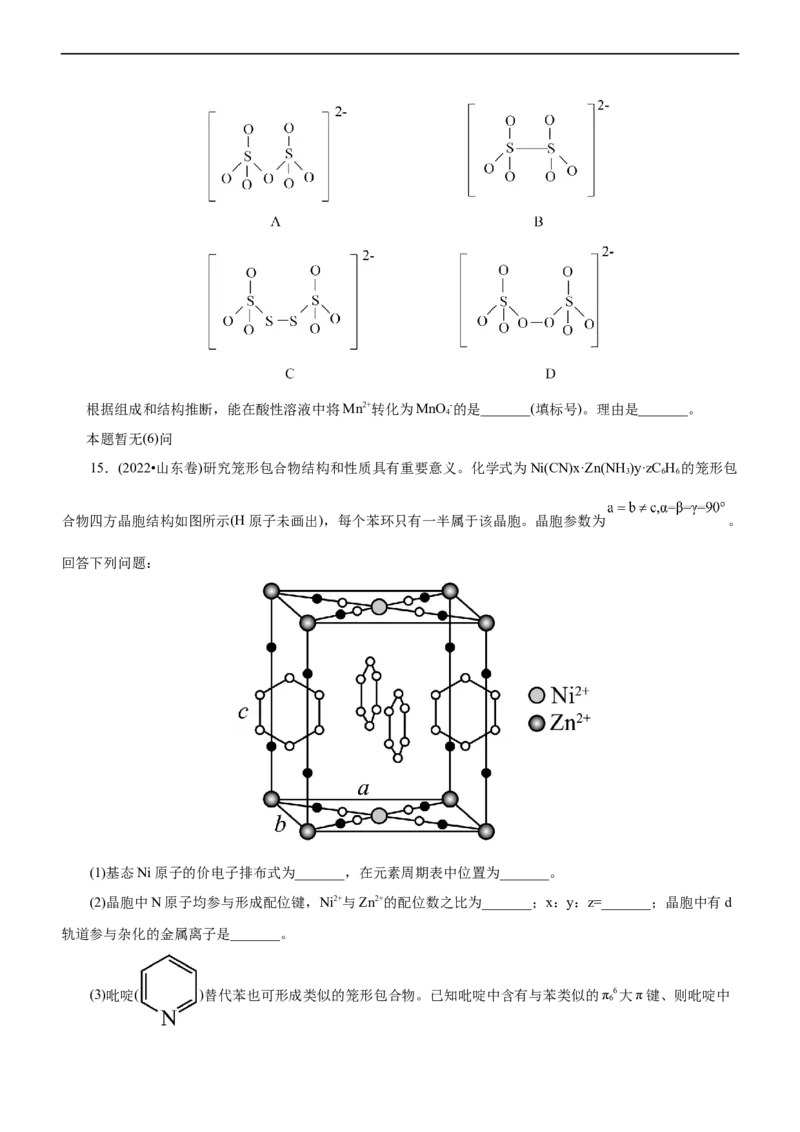
15.(2022•山东卷)研究笼形包合物结构和性质具有重要意义。化学式为Ni(CN)x·Zn(NH )y·zC H 的笼形包
3 6 6
合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为 。
回答下列问题:
(1)基态Ni原子的价电子排布式为_______,在元素周期表中位置为_______。
(2)晶胞中N原子均参与形成配位键,Ni2+与Zn2+的配位数之比为_______;x:y:z=_______;晶胞中有d
轨道参与杂化的金属离子是_______。
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的π 6大π键、则吡啶中
6N原子的价层孤电子对占据_______(填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①_______,②_______。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中碱性
最弱的是_______。
16.(2022•北京卷)FeSO ·7H O失水后可转为FeSO ·H O,与FeS 可联合制备铁粉精(Fe O)和HSO 。
4 2 4 2 2 x y 2 4
I. FeSO ·H O结构如图所示。
4 2
(1) Fe2+价层电子排布式为___________。
(2)比较SO 2-和HO分子中的键角大小并给出相应解释:___________。
4 2
(3)H O与Fe2+、SO 2-和HO的作用分别为___________。
2 4 2
II.FeS 晶胞为立方体,边长为 ,如图所示。
2
(4)①与Fe2+紧邻的阴离子个数为___________。
②晶胞的密度为 ___________ 。
(5)以FeS 为燃料,配合FeSO ·H O可以制备铁粉精(Fe O)和HSO 。结合图示解释可充分实现能源和资
2 4 2 x y 2 4
源有效利用的原因为___________。17.(2022•湖南选择性考试)铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广
泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态 原子的核外电子排布式为 [Ar]_______;
②该新药分子中有_______种不同化学环境的C原子;
③比较键角大小:气态SeO 分子_______ SeO 2-离子(填“>”“<”或“=”),原因是_______。
3 3
(2)富马酸亚铁(FeC HO)是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H,将N3-转化为NH -,
2 2
反应过程如图所示:①产物中N原子的杂化轨道类型为_______;
②与NH -互为等电子体的一种分子为_______(填化学式)。
2
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数 、 。阿伏加德罗常数的值为N ,则该晶体的密度为_______ g· cm-3 (列
A
出计算式)。
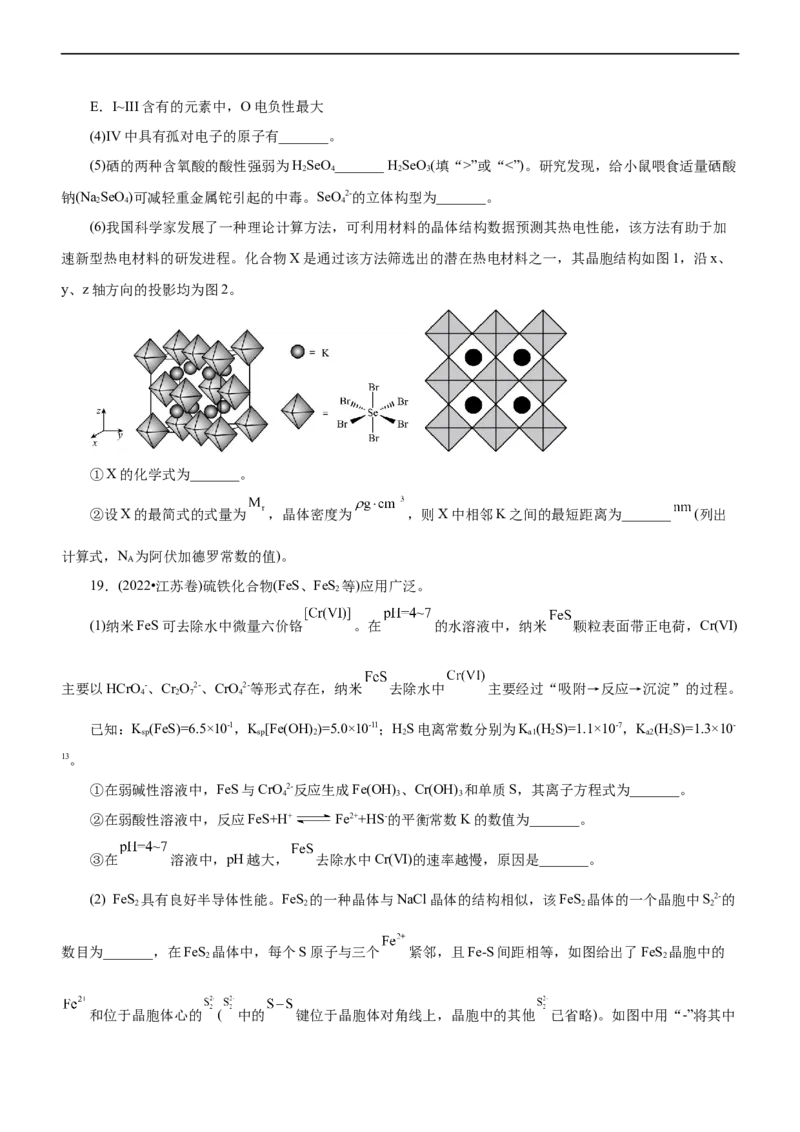
18.(2022•广东选择性考试)硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应
用。自我国科学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起广泛关注。一种
含 的新型 分子 的合成路线如下:
(1) Se与S同族,基态硒原子价电子排布式为_______。
(2)H Se的沸点低于HO,其原因是_______。
2 2
(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有 键 B.I中的Se-Se键为非极性共价键
C.II易溶于水 D.II中原子的杂化轨道类型只有sp与sp2E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为HSeO_______ H SeO(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸
2 4 2 3
钠(Na SeO)可减轻重金属铊引起的中毒。SeO2-的立体构型为_______。
2 4 4
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加
速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、
y、z轴方向的投影均为图2。
①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______ (列出
计算式,N 为阿伏加德罗常数的值)。
A
19.(2022•江苏卷)硫铁化合物(FeS、FeS 等)应用广泛。
2
(1)纳米FeS可去除水中微量六价铬 。在 的水溶液中,纳米 颗粒表面带正电荷,Cr(VI)
主要以HCrO -、CrO2-、CrO 2-等形式存在,纳米 去除水中 主要经过“吸附→反应→沉淀”的过程。
4 2 7 4
已知:K (FeS)=6.5×10-1,K [Fe(OH) )=5.0×10-11;HS电离常数分别为K (H S)=1.1×10-7,K (H S)=1.3×10-
sp sp 2 2 a1 2 a2 2
13。
①在弱碱性溶液中,FeS与CrO 2-反应生成Fe(OH) 、Cr(OH) 和单质S,其离子方程式为_______。
4 3 3
②在弱酸性溶液中,反应FeS+H+ Fe2++HS-的平衡常数K的数值为_______。
③在 溶液中,pH越大, 去除水中Cr(VI)的速率越慢,原因是_______。
(2) FeS 具有良好半导体性能。FeS 的一种晶体与NaCl晶体的结构相似,该FeS 晶体的一个晶胞中S2-的
2 2 2 2
数目为_______,在FeS 晶体中,每个S原子与三个 紧邻,且Fe-S间距相等,如图给出了FeS 晶胞中的
2 2
和位于晶胞体心的 ( 中的 键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来_______。
(3) FeS、FeS在空气中易被氧化,将FeS 在空气中氧化,测得氧化过程中剩余固体的质量与起始FeS 的
2 2 2
质量的比值随温度变化的曲线如图所示。800℃时,FeS 氧化成含有两种元素的固体产物为_______(填化学式,
2
写出计算过程)。