文档内容
专题 15 物质结构与性质
1.原子结构与元素的性质
(1)了解原子核外电子的能级分布,能用电子排布式表示常见元素(1~36号)原子核外电子
的排布。了解原子核外电子的运动状态;
(2)了解元素电离能的含义,并能用以说明元素的某些性质;
(3)了解原子核外电子在一定条件下会发生跃迁,了解其简单应用;
(4)了解电负性的概念,知道元素的性质与电负性的关系。
2.化学键与物质的性质
(1)理解离子键的形成,能根据离子化合物的结构特征解释其物理性质;
(2)了解共价键的主要类型σ键和π键,能用键能、键长、键角等说明简单分子的某些性
考纲 质;
(3)了解简单配合物的成键情况;
(4)了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系;
(5)理解金属键的含义,能用金属键理论解释金属的一些物理性质;
(6)了解杂化轨道理论及常见的杂化轨道类型(sp,sp2,sp3),能用价层电子对互斥理论或
者杂化轨道理论推测常见的简单分子或者离子的空间结构。
3.分子间作用力与物质的性质
(1)了解化学键和分子间作用力的区别;
(2)了解氢键的存在对物质性质的影响,能列举含有氢键的物质;
(3)了解分子晶体与原子晶体、离子晶体、金属晶体的结构粒子、粒子间作用力的区别。
《物质结构与性质》许多省市列入必考题,题目一般是以元素推断或某主族元素为背
景,以“拼盘”形式呈现,各小题之间相对独立,主要考查原子结构与性质、分子结构
与性质、晶体结构与性质。试题背景新颖,注重体现科学新成果或新发现,更注重“结
考情预测 构决定性质”思想的树立,考查空间想象能力。在原子结构部分主要命题点有电子排布
式或排布图的书写,电离能、电负性大小的比较与判断;在分子结构部分主要命题点有
化学键类型的判断,分子构型的判断,中心原子杂化方式的判断;在晶体结构部分主要
命题点有晶体类型的判断,晶体结构的计算等。
核心素养 宏观辨识与微观探析 证据推理与模型认知高频考点一 原子结构与性质
1.原子结构与化学键
(1)微粒间“三个”数量关系
中性原子:核电荷数=核内质子数=核外电子数=原子序数
阴离子:核外电子数=质子数+所带的电荷数
阳离子:核外电子数=质子数-所带的电荷数
(2)“四同”的判断方法——关键是抓住描述的对象
①同位素——原子,如1 H、2 H、3 H。
1 1 1
②同素异形体——单质,如O 与O,金刚石与石墨,红磷与白磷。
2 3
③同系物——有机化合物,如CHCH、CHCHCH。
3 3 3 2 3
④同分异构体——化合物,如正戊烷与新戊烷。
(3)10e-、18e-微粒10电子体和18电子体是元素推断题的重要突破口。
以Ne为中心记忆10电子体:
Ne
以Ar为中心记忆18电子体:
Ar
此外,由10电子体中的CH 、NH 、HO、HF失去一个H原子后的剩余部分如—CH 、—NH 、—OH、
4 3 2 3 2
—F等为9电子体,两两组合得到的物质如CHCH、CHOH、HO、NH、F 等为18电子体。
3 3 3 2 2 2 4 2
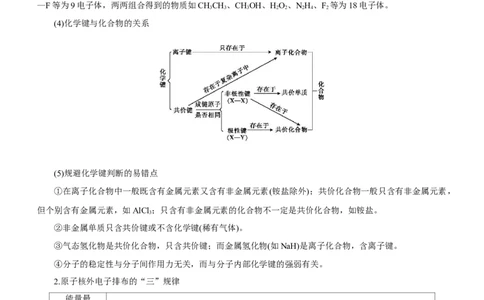
(4)化学键与化合物的关系
(5)规避化学键判断的易错点
①在离子化合物中一般既含有金属元素又含有非金属元素(铵盐除外);共价化合物一般只含有非金属元素,
但个别含有金属元素,如AlCl ;只含有非金属元素的化合物不一定是共价化合物,如铵盐。
3
②非金属单质只含共价键或不含化学键(稀有气体)。
③气态氢化物是共价化合物,只含共价键;而金属氢化物(如NaH)是离子化合物,含离子键。
④分子的稳定性与分子间作用力无关,而与分子内部化学键的强弱有关。
2.原子核外电子排布的“三”规律
能量最
原子核外电子总是先占据能量最低的原子轨道
低原理
泡利原理 每个原子轨道上最多只能容纳2个自旋状态相反的电子
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,
洪特规则
而且自旋状态相同
3.基态原子核外电子排布的表示方法
表示方法 含义 举例原子或离子结构
表示核外电子分层排布和核内质子数
示意图
··
电子式 表示原子最外层电子数目
·Cl·
·
··
S:1s22s22p63s23p4或[Ne]3s23p4
核外电子排布式表示每个能级上排布的电子数
S2-:1s22s22p63s23p6
电子排布图
表示每个原子轨道中电子的运动状态
(轨道表示式)
价电子排布式或 S:3s23p4
表示价电子的排布
排布图
Fe:3d64s2
4.电离能及其应用
(1)电离能的变化规律
①同周期从左到右(ⅠA族→0族),第一电离能呈增大的趋势。但第ⅡA族(ns2np0)和第ⅤA族(ns2np3),因
为p轨道处于全空或半充满状态,比较稳定,所以其第一电离能大于同周期右侧相邻的第ⅢA族或第ⅥA族
元素,如第一电离能:Mg>Al、P>S。
②逐级电离能逐渐增大(Ir(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl);r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)。
“三看”核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。
例:r(Cl-)>r(Cl);r(Fe2+)>r(Fe3+)。
8.金属性、非金属性强弱的判断
【典例剖析】【例1】(2022•辽宁省选择性考试)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子
均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是( )
A.X能与多种元素形成共价键 B.简单氢化物沸点:
C.第一电离能: D.电负性:
【答案】B
【解析】短周期元素X、Y、Z、W、Q原子序数依次增大,W简单离子在同周期离子中半径最小,说明W
为第三周期元素Al。短周期元素的基态原子中有两个单电子,可分类讨论:①为第二周期元素时,最外层电
子排布为2s22p2或2s22p4,即C或O;②为第三周期元素时,最外层电子排布为3s23p2或3s23p4,即Si或S。Q
与Z同主族,结合原子序数大小关系可知,则X、Z、Q分别为C、O和S,则Y为N。A项,X为C,能与多
种元素(H、O、N、P、S等)形成共价键,A正确;B项,Z和Q形成的简单氢化物为HO和HS,由于HO分
2 2 2
子间能形成氢键,故HO沸点高于HS,B错误;C项,Y为N,Z为O,N的最外层p轨道电子为半充满结构,
2 2
比较稳定,故其第一电离能比O大,C正确;D项,W为Al,Z为O,O的电负性更大,D正确;故选B。
【例2】(2021•山东卷)X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合
物能以[XY ]+[XY ]-的形式存在。下列说法错误的是( )
4 6
A.原子半径:X>Y B.简单氢化物的还原性:X>Y
C.同周期元素形成的单质中Y氧化性最强 D.同周期中第一电离能小于X的元素有4种
【答案】D
【解析】Y位于第三周期,且最高正价与最低负价的代数和为6,则Y是Cl元素,由X、Y形成的阴离子
和阳离子知,X与Y容易形成共价键,根据化合物的形式知X是P元素。A项,P与Cl在同一周期,则P半
径大,即X>Y,A项不符合题意;B项,两者对应的简单氢化物分别是PH 和HCl,半径是P3->Cl-,所以PH
3 3
的失电子能力强,还原性强,即X>Y,B项不符合题意;C项,同周期元素从左往右,金属性减弱,非金属性
增强,各元素对应的金属单质还原性减弱,非金属单质的氧化性增强,所以Cl 的氧化性最强,C项不符合题
2
意;D项,同一周期,从左到右,第一电离能呈现增大的趋势,第VA族元素的第一电离能大于相邻元素的第
一电离能;所以第三周期第一电离能从小到大依次为Na、Al、Mg、Si、S、P、Cl,所以有5种,D项符合题
意;故选D。
【变式探究】
1.主族元素的原子可失去最外层电子形成阳离子,主族元素的原子也可得到电子填充在最外层形成阴离
子。下列各原子或离子的电子排布式错误的是( )
A.Ca2+ 1s22s22p63s23p6 B.F- 1s22s22p5 C.S 1s22s22p63s23p4 D.Ar 1s22s22p63s23p6
【答案】B
【解析】首先写出各原子的正确的电子排布式:Ca 1s22s22p63s23p64s2,F 1s22s22p5,S 1s22s22p63s23p4,Ar1s22s22p63s23p6,A 中生成 Ca2+失去了 4s 轨道上的 2 个电子,B 中得 1 个电子进入 2p 轨道,电子排布为
1s22s22p6。
2.已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为
B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的原子外围电子排布式为5s25p1
【答案】D
【解析】A中只能说明该元素的L层有8个电子,无法确定其在周期表中的位置;某些非金属元素有多种
化合价,+4价不一定是其最高化合价,无法确定;C中根据最外层电子数只能确定族序数,无法确定周期数;
D可确定该元素在第五周期第ⅢA族。
3.现有主族元素X、Y、Z,X原子的最外层电子排布式为ns1,Y原子M能层的p能级上有4个电子,Z
原子的最外层p能级上也有4个电子,且Z原子的核外电子数比Y原子少8个。由这三种元素组成的化合物不
可能是( )
A.XYZ B.XYZ C.XYZ D.XYZ
2 3 2 4 2 2 3 4
【答案】D
【解析】因为X原子的最外层电子排布式为ns1,故X位于ⅠA族,化合价为+1价;根据Y原子M能层
的p能级上有4个电子,可知其电子排布式为1s22s22p63s23p4,故Y为S;又因为Z原子的最外层p能级上也有
4个电子,说明Z和S为同一主族,又知Z原子的核外电子数比Y原子少8个,故Z为O。元素X、Y、Z可
以组成HSO 、NaSO 、KSO 等,A符合;也可以组成 HSO 、NaSO 、KSO 等,B符合;还可以组成
2 3 2 3 2 3 2 4 2 4 2 4
NaSO、KSO 等,C符合。
2 2 3 2 2 3
4.(2020•山东卷)短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数是其最高能
级电子数的2倍,Z可与X形成淡黄色化合物ZX,Y、W最外层电子数相同。下列说法正确的是( )
2 2
A.第一电离能:W>X>Y>Z B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z D.氢化物水溶液的酸性:Y>W
【答案】C
【解析】四种短周期主族元素,基态X原子的电子总数是其最高能级电子数的2倍,设若X为第二周期元
素原子,则X可能为Be或O,若X为第三周期元素原子,则均不满足题意,Z与X能形成ZX 的淡黄色化合
2 2
物,该淡黄色固体为NaO,则X为O元素,Z为Na元素;Y与W的最外层电子数相同,则Y为F元素,W
2 2
为Cl元素。A项,同一周期从左向右第一电离能总趋势为逐渐增大,同一主族从上到下第一电离能逐渐减小,
故四种元素中第一电离能从大到小的顺序为F>O>Cl>Na,A错误;B项,单质的氧化性越强,简单离子的
还原性越弱,O、F、Cl三种元素中F 的氧化性最强O 的氧化性最弱,故简单离子的还原性O2->Cl->F-,B错
2 2
误;C项,电子层数越多简单离子半径越大,相同结构的离子,原子序数越大半径越小,故四种元素中离子半径从大到小的顺序为Cl->O2->F->Na+,C正确;D项,F元素的非金属性强于Cl元素,则形成氢化物后F原
子束缚H原子的能力强于Cl原子,在水溶液中HF不容易发生电离,故HCl的酸性强于HF,D错误;故选
C。
5.(2023·江苏省南通市海安区高三期中)当汽车遭受一定碰撞力量以后,安全气囊中的物质会发生剧烈的
反应:NaN +KNO =K O+Na O+N↑(未配平),生成大量气体。下列说法正确的是( )
3 3 2 2 2
A.半径大小:r(Na+)χ(O)
C.电离能大小:I1(Na)>I1(O) D.碱性强弱:KOH氢键>范德华力
组成和结构相似的物质,
A—H…B中形成氢键元素的电
影响因素 相对分子质量越大,范德 原子半径
负性(A、B的电负性)
华力越大
对性质 影响物质的熔点、沸点、 分子间氢键使熔点、沸点升
键能越大,稳定性越强
的影响 溶解度等物理性质 高,溶解度增大
5.配位化合物
配合物的组成 [中心离子(配体)][外界]
n
典型配合物 Cu(NH )SO Fe(SCN) Ag(NH)OH
3 4 4 3 3 2
中心离子 Cu2+ Fe3+ Ag+
中心离子结构特点 一般是金属离子,特别是过渡金属离子,必须有空轨道
配体 NH SCN- NH
3 3
配体结构特点 分子或离子,必须含有孤对电子(如NH 、HO、CO、Cl-、SCN-等)
3 2
配位数(n) 4 3 2
外界 SO 2- 无 OH-
4
颜色 深蓝色 血红色 无色
配离子所含化学键 配体通过配位键与中心离子结合
配合物所含化学键 配位键、离子键;配体或外界中可能还含有共价键
配合物的常见性质 属于离子化合物,多数能溶解、能电离,多数有颜色
是过渡金属和一氧化碳配位形成的配合物,如四羰基镍[Ni(CO) ]。在许多有机化
金属羰基配合物 4
合物的合成反应中,金属羰基配合物常常作为这些反应的催化剂
二茂铁的结构为一个铁原子处在两个平行的环戊二烯的环之间。在固体状态下,
两个茂环相互错开成全错位构型,温度升高时则绕垂直轴相对转动。二茂铁的化
二茂铁 学性质稳定,类似芳香族化合物
6.超分子
(1)定义:有两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
注意:超分子定义中分子是广义的,其中包括离子。
(2)特征:分子识别和自组装。【典例剖析】
【例1】(2022•辽宁省选择性考试)理论化学模拟得到一种N +离子,结构如图。下列关于该离子的说法错
13
误的是( )
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
【答案】B
【解析】A项,由N +的结构式可知,所有N原子均满足8电子稳定结构,A正确;B项,中心N原子为
13
sp3杂化,与中心N原子直接相连的N原子为sp2杂化,与端位N原子直接相连的N原子为sp杂化,端位N原
子为sp2杂化,则N原子的杂化方式有3种,B错误;C项,中心N原子为sp3杂化,则其空间结构为四面体形,
C正确;D项,N +中含叠氨结构( ),常温下不稳定,D正确;故选B。
13
【例2】 (2022•海南选择性考试)关于NH 性质的解释合理的是( )
3
选项 性质 解释
A 比PH 容易液化 NH 分子间的范德华力更大
3 3
B 熔点高于PH N-H键的键能比P-H大
3
C 能与Ag以配位键结合 NH 中氮原子有孤电子对
3
D 氨水中存在NH + NH ·H O是离子化合物
4 3 2
【答案】C
【解析】A项,NH 和PH 都属于同一主族是氢化物,分子晶体的沸点与其相对分子质量成正比,但氨气
3 3
中含有氢键, PH 不含氢键,氢键的存在导致氨气的沸点升高,故A错误;B项,NH 熔点高于PH ,是因为
3 3 3
氨气中含有氢键,氢键的存在导致氨气的熔点升高,不是N-H键的键能比P-H大,故B错误;C项,NH 中氮
3
原子有孤电子对,使Ag+和NH 以配位键结合形成[Ag(NH)]+,故C正确;D项,NH ·H O是共价化合物,是
3 3 2 3 2
弱碱,在水溶液中部分电离出NH +和OH-,故D错误;故选C。
4
【变式探究】
1.(2023·海南省琼海市嘉积中学高三期中)氯元素有多种化合价,可形成ClO、Cl-、ClO-、ClO -、ClO -、
2 2 3
ClO -等微粒。下列说法错误的是( )
4A.ClO -、ClO -、ClO -中Cl原子的杂化方式相同
2 3 4
B.基态Cl原子核外电子的空间运动状态有9种
C.键角:ClO ->ClO ->ClO -
2 3 4
D.ClO的空间构型为V形
2
【答案】C
【解析】A项,ClO -的结构式为: ,ClO -的结构式为: ,ClO -的结构式为
2 3 4
,VSEPR模型均为四面体,因此Cl的杂化方式都是sp3,A正确;B项,量子力学把电子在原
子核外的一个空间运动状态称为一个原子轨道,基态Cl原子的核外电子排布式为:1s22s22p63s23p5,s能级各有
一个轨道,p能级各有3个轨道,共9个轨道。因此基态Cl原子的核外电子的空间运动状态有9种,B正确;
C项,三种离子的Cl原子均为sp3杂化,ClO -空间结构呈V形,键角为105 ,ClO -空间结构呈三角锥形,键
2 3
角为107 ,ClO -空间结构呈四面体形,键角为109 28 ,键角关系为:ClO -<ClO -<ClO -,C错误;D项,
4 2 3 4
ClO中心原子为O原子,杂化方式为sp3,结构式为 ,因此空间构型为形,D正确;故选
2
C。
2.(2022·湖北省鄂东南省级示范高中高三联考)乙二胺四乙酸又叫EDTA,是化学中一种良好的配合剂,
形成的配合物又叫螯合物。 在配合滴定中经常用到,一般是测定金属离子的含量。已知:EDTA配离子
结构如图。下列叙述错误的是( )A.EDTA中氮原子杂化方式sp3
B.M元素可以是Cu、 或
C.M元素的配位数是6
D.EDTANa-Fe(III)的化学键有:σ键、配位键、π键和离子键
【答案】B
【解析】A项,根据该配离子结构,氮原子成四个单键(有1个配位键),属于杂化方式sp3,故A正确;B
项,依图可知,M的配位数为6,而Cu的配位数为4,故B项错误;C项,根据该配离子结构,M元素的配
位数是6,故C正确;D项,EDTANa-Fe(III)是离子化合物,含有离子键;阴离子是复杂离子,含有共价单键、
共价双键,单键为σ键、双键含σ键、π键,铁离子含有空轨道,与之结合的氮原子、氧原子含有孤电子对,
与铁离子形成配位键,故D正确;故选B。
3.三草酸合铁酸钾可用氯化铁与草酸钾混合直接合成:
FeCl +3KC O===K [Fe(C O)]+3KCl
3 2 2 4 3 2 4 3
(1)FeCl 中铁离子基态核外电子排布式为________。
3
(2)上述反应涉及的主族元素中,第一电离能最小的是________(填元素符号)。
(3)K [Fe(C O)]中化学键的类型有________。
3 2 4 3
(4)草酸(H C O)中C原子的杂化类型为________,1 mol草酸(H C O)中含有σ键的数目为________。
2 2 4 2 2 4
(5)与C O互为等电子体的一种分子为________(填化学式)。
2
【答案】(1)[Ar]3d5或1s22s22p63s23p63d5
(2)K (3)离子键、共价键、配位键 (4)sp2 7N (5)N O
A 2 4
【解析】(1)铁的原子序数为26,其基态原子的电子排布式为[Ar]3d64s2或1s22s22p63s23p63d64s2,则Fe3+基
态核外电子排布式为[Ar]3d5或1s22s22p63s23p63d5。(2)上述反应涉及的主族元素有Cl、K、C、O,第一电离能
最小(金属性最强)的为 K。(3)配合物 K[Fe(C O)]中化学键有离子键、共价键、配位键。(4)先画出草酸
3 2 4 3
(H C O)的结构( ),草酸分子中碳原子的杂化方式为sp2;1分子草酸中含有7个σ键,则1 mol草酸
2 2 4
(H C O)中含有σ键的数目为7N 。(5)根据“等价找邻”的方法确定C O的等电子体分子有NO 等。
2 2 4 A 2 2 4
4.W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在
考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质在高空大气层中
保护人类免遭太阳光中紫外线的强烈侵袭;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色
的ZO和黑色的ZO两种氧化物。
2
(1)Y3+基态电子排布式可表示为________。(2)MX的空间构型是________(用文字描述)。
(3)M可形成多种氢化物,其中MH 的碱性强于MH 的原因是_______________________________。
3 2 4
(4)根据等电子原理,WX分子的结构式为________。
(5)1 mol WX 中含有的键数目为________。
2
(6)H X分子中X原子轨道的杂化类型为________。
2
【答案】(1)1s22s22p63s23p63d3或[Ar]3d3 (2)平面三角形
(3)N H 分子中N为-2价,而NH 分子中N为-3价,电负性更大,导致N原子的孤电子对更易提供出
2 4 3
来与H+结合或碱性更强
(4)C≡O (5)2N (6)sp3杂化
A
【解析】W的一种核素在考古时常用来鉴定一些文物的年代,故W为C元素;M的氧化物是导致酸雨的
主要物质之一,则M为N元素或S元素;X的某一种单质在高空大气层中保护人类免遭太阳光中紫外线的强
烈侵袭,则X是O元素,故M为N元素;Y的基态原子核外有6个原子轨道处于半充满状态,则Y的价电子
排布式为3d54s1,故Y为Cr元素,Z能形成红色的ZO和黑色的ZO两种氧化物,故Z为Cu元素。(1)由上述
2
推断可知,Y3+为Cr3+,基态电子排布式可表示为1s22s22p63s23p63d3或[Ar]3d3。(2)NO中,键数为3,孤电子对
数为(5+1-3×2)/2=0,所以其空间构型为平面三角形。(3)从化合价角度分析:NH 分子中N为-2价,而
2 4
NH 分子中N为-3价,电负性更大,导致N原子的孤电子对更易提供出来与H+结合,故碱性更强。(4)CO与
3
N 是等电子体,化学结构相似,所以CO的结构式类似于N ,存在叁键结构,故为 。(5)CO 分子中存
2 2 2
在2个碳氧双键,每个双键都有1个键,故1 mol CO 分子中存在2N 个键。(6)H O分子中,O的键数为
2 A 2
2,孤电子对数为(6-2)/2=2,故HX分子中X原子轨道的杂化类型为sp3杂化。
2
1.键的极性与分子极性的关系
类型 实例 两个键之间的夹角 键的极性 分子的极性 空间构型
X H、N - 非极性键 非极性分子 直线型
2 2 2
XY HCl、NO - 极性键 极性分子 直线型
CO、CS 180° 极性键 非极性分子 直线型
2 2
XY (X Y) SO 120° 极性键 极性分子 三角形
2 2 2
HO、HS 104.5° 极性键 极性分子 V形
2 2
BF 120° 极性键 非极性分子 平面三角形
3
XY
3
NH 107.3° 极性键 非极性分子 三角锥形
3
XY CH、CCl 109.5° 极性键 非极性分子 正四面体
4 4 4
2.中心原子杂化类型和分子空间构型的相互判断分子(A为中 中心原子杂化 中心原子孤电
分子构型 示例
心原子) 方式 子对数
sp 0 直线形 BeCl
2
AB sp2 1 V形 SO
2 2
sp3 2 V形 HO
2
sp2 0 平面三角形 BF
3
AB
3
sp3 1 三角锥形 NH
3
AB sp3 0 正四面体形 CH
4 4
3.常见等电子体
粒子 通式 价电子总数 立体构型
CO、SCN-、NO、N、NO、COS、CS AX 16e- 直线形
2 2 2 2
CO、NO、SO AX 24e- 平面三角形
3 3
SO 、O、NO AX 18e- V形
2 3 2
SO、PO AX 32e- 正四面体形
4
PO、SO、ClO AX 26e- 三角锥形
3
CO、N、C AX 10e- 直线形
2
CH、NH AX 8e- 正四面体形
4 4
高频考点三 晶体结构与性质
1.常见原子晶体结构分析
晶体 晶体结构 结构分析
(1)每个碳与相邻4个碳以共价键结合,形成正四面体结构,键角均为109°28′
(2)每个金刚石晶胞中含有8个碳原子,最小的碳环为6元环,并且不在同一
平面(实际为椅式结构),碳原子为sp3杂化
(3)每个碳原子被12个六元环共用,每个共价键被6个六元环共用,一个六元
金刚石
1
原子半径(r)与边
2
环实际拥有 个碳原子
长(a)的关系:
(4)C原子数与C—C键数之比为1∶2,12g金刚石中有2 mol共价键
√3
a=8r
(5)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)SiO 晶体中最小的环为12元环,即:每个12元环上有6个O,6个Si
2
(2)每个Si与4个O以共价键结合,形成正四面体结构,每个正四面体占有1
个Si,4个“O”,n(Si)∶n(O)=1∶2
SiO (3)每个Si原子被12个十二元环共用,每个O原子被 6个十二元环共用
2
(4)每个SiO 晶胞中含有8个Si原子,含有16个O原子
2
(5)硅原子与Si—O共价键之比为1:4,1mol Si O 晶体中有4mol共价键
2
(6)密度= (a为晶胞边长,N 为阿伏加德罗常数)
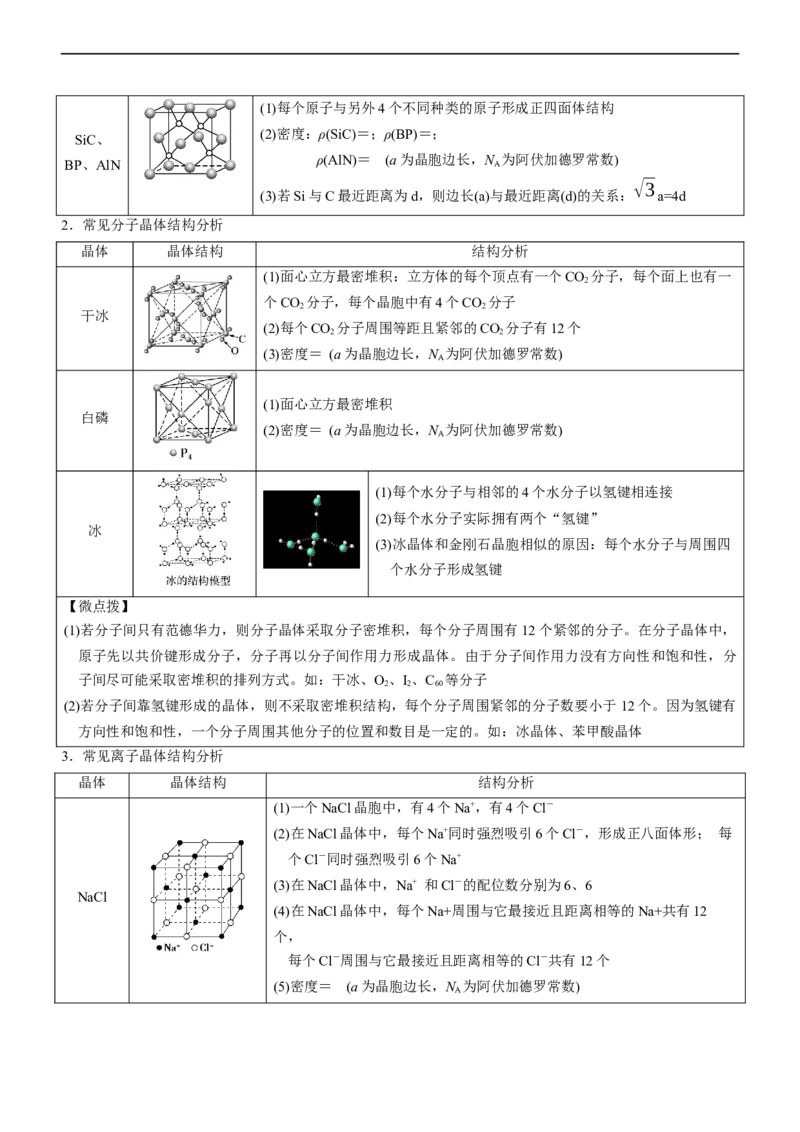
A(1)每个原子与另外4个不同种类的原子形成正四面体结构
(2)密度:ρ(SiC)=;ρ(BP)=;
SiC、
BP、AlN
ρ(AlN)= (a为晶胞边长,N
A
为阿伏加德罗常数)
√3
(3)若Si与C最近距离为d,则边长(a)与最近距离(d)的关系: a=4d
2.常见分子晶体结构分析
晶体 晶体结构 结构分析
(1)面心立方最密堆积:立方体的每个顶点有一个CO 分子,每个面上也有一
2
个CO 分子,每个晶胞中有4个CO 分子
2 2
干冰
(2)每个CO 分子周围等距且紧邻的CO 分子有12个
2 2
(3)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)面心立方最密堆积
白磷
(2)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个水分子与相邻的4个水分子以氢键相连接
(2)每个水分子实际拥有两个“氢键”
冰
(3)冰晶体和金刚石晶胞相似的原因:每个水分子与周围四
个水分子形成氢键
【微点拨】
(1)若分子间只有范德华力,则分子晶体采取分子密堆积,每个分子周围有12个紧邻的分子。在分子晶体中,
原子先以共价键形成分子,分子再以分子间作用力形成晶体。由于分子间作用力没有方向性和饱和性,分
子间尽可能采取密堆积的排列方式。如:干冰、O、I、C 等分子
2 2 60
(2)若分子间靠氢键形成的晶体,则不采取密堆积结构,每个分子周围紧邻的分子数要小于 12个。因为氢键有
方向性和饱和性,一个分子周围其他分子的位置和数目是一定的。如:冰晶体、苯甲酸晶体
3.常见离子晶体结构分析
晶体 晶体结构 结构分析
(1)一个NaCl晶胞中,有4个Na+,有4个Cl-
(2)在NaCl晶体中,每个Na+同时强烈吸引6个Cl-,形成正八面体形; 每
个Cl-同时强烈吸引6个Na+
(3)在NaCl晶体中,Na+ 和Cl-的配位数分别为6、6
NaCl
(4)在NaCl晶体中,每个Na+周围与它最接近且距离相等的Na+共有12
个,
每个Cl-周围与它最接近且距离相等的Cl-共有12个
(5)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A(1)一个CsCl晶胞中,有1个Cs+,有1个Cl-
(2)在CsCl晶体中,每个Cs+同时强烈吸引8个Cl-,即:Cs+的配位数为8,
每个Cl- 同时强烈吸引8个Cs+,即:Cl-的配位数为8
CsCl (3)在CsCl晶体中,每个Cs+周围与它最接近且距离相等的Cs+共有6个,形
成正八面体形,在CsCl晶体中,每个Cl-周围与它最接近且距离相等的
Cl-共有6个
(4)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)1个ZnS晶胞中,有4个S2-,有4个Zn2+
ZnS (2)Zn2+的配位数为4,S2-的配位数为4
(3)密度=
(1)1个CaF 的晶胞中,有4个Ca2+,有8个F-
2
(2)CaF 晶体中,Ca2+和F-的配位数不同,Ca2+配位数是8,F-的配位数是
2
CaF
2
4
(3)密度=
离子晶体的配位数 离子晶体中与某离子距离最近的异性离子的数目叫该离子的配位数
(1)正、负离子半径比:AB型离子晶体中,阴、阳离子的配位数相等,但
影响离子晶体配位数的因素 正、负离子半径比越大,离子的配位数越大。如:ZnS、NaCl、CsCl
(2)正、负离子的电荷比。如:CaF 晶体中,Ca2+和F-的配位数不同
2
4.常见金属晶体结构分析
(1)金属晶体的四种堆积模型分析
体心立方堆积 (钾 面心立方最密堆积(铜
堆积模型 简单立方堆积 六方最密堆积(镁型)
型) 型)
晶胞
代表金属 Po Na K Fe Cu Ag Au Mg Zn Ti
配位数 6 8 12 12
晶胞占有的原
1 2 4 6或2
子数
原子半径(r)与
立方体边长为 a=2r √3 a=4r √2 a=4r ——
(a)的关系
2.物质熔、沸点高低的比较
一般情况下,原子晶体>离子晶体>分子晶体,如:金刚石>NaCl>Cl ;金属晶体>分子晶体,如:Na>Cl 。
2 2(金属晶体熔、沸点有的很高,如钨、铂等,有的则很低,如汞等)
原子晶体 →→,如:金刚石>石英>晶体硅
一般地说,阴阳离子的电荷数越多,离子半径越小,离子键越强,晶格能越大,熔、沸点就
离子晶体
越高。如:MgO>MgCl ,NaCl>CsCl
2
金属离子半径越小,离子所带电荷数越多,其形成的金属键越强,金属单质的熔、沸点就越
金属晶体
高,如Al>Mg>Na
①分子间作用力越大,物质的熔、沸点越高;具有分子间氢键的分子晶体熔、沸点反常的
高。如HO>HTe>HSe>HS
2 2 2 2
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如SnH >GeH >SiH>
4 4 4
分子晶体 CH
4
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔沸点越高,如CO>
N
2
在同分异构体中,一般支链越多,熔、沸点越低,如正戊烷>异戊烷>新戊烷
【典例剖析】
【例1】(2022•山东卷)Cu Se是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组
2-x
成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是( )
A.每个Cu Se晶胞中Cu2+个数为x
2-x
B.每个NaSe晶胞完全转化为Cu Se晶胞,转移电子数为8
2 2-x
C.每个NaCuSe晶胞中0价Cu原子个数为1-x
D.当NaCu Se转化为NaCuSe时,每转移 电子,产生(1-x)mol原子
y 2-x
【答案】D
【解析】A项,由Cu Se晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的铜
2-x
离子和亚铜离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化合价
代数和为0可得2a+b=4×2,解得a=4x,故A错误;B项,由NaSe转化为Cu Se的电极反应式为NaSe-e-+(2-
2 2-x 2
x)Cu=Cu Se+Na+,由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中含有4个
2-xNaSe,转移电子数为4,故B错误;C项,由NaCuSe晶胞结构可知,位于顶点和面心的硒离子个数为8×
2
+6× =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数为(4-4x),故C错误;D项,由题意可知,
NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+ Na+=NaCuSe+(1-x)Cu,所以每转移(1-y)电子,
y 2-x y 2-x
产生(1-x)mol铜,故D正确;故选D。
【例2】 (2022•湖北选择性考试)某立方晶系的锑钾(Sb-K)合金可作为钾离子电池的电极材料,图a为该合
金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是( )
A.该晶胞的体积为 B.K和Sb原子数之比为3:1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 pm
【答案】B
【解析】该晶胞的边长为a×1010 cm,故晶胞的体积为(a×1010 cm)3=a3×1030 cm3,A项错误;该晶胞中K
的个数为12×+9=12,Sb的个数为8×+6×=4,故K和Sb原子个数之比为3:1,B项正确;以面心处Sb为研
究对象,与Sb最邻近的K原子数为8,C项错误;K和Sb的最短距离为晶胞体对角线长度的,即 pm,
D项错误。
【变式探究】
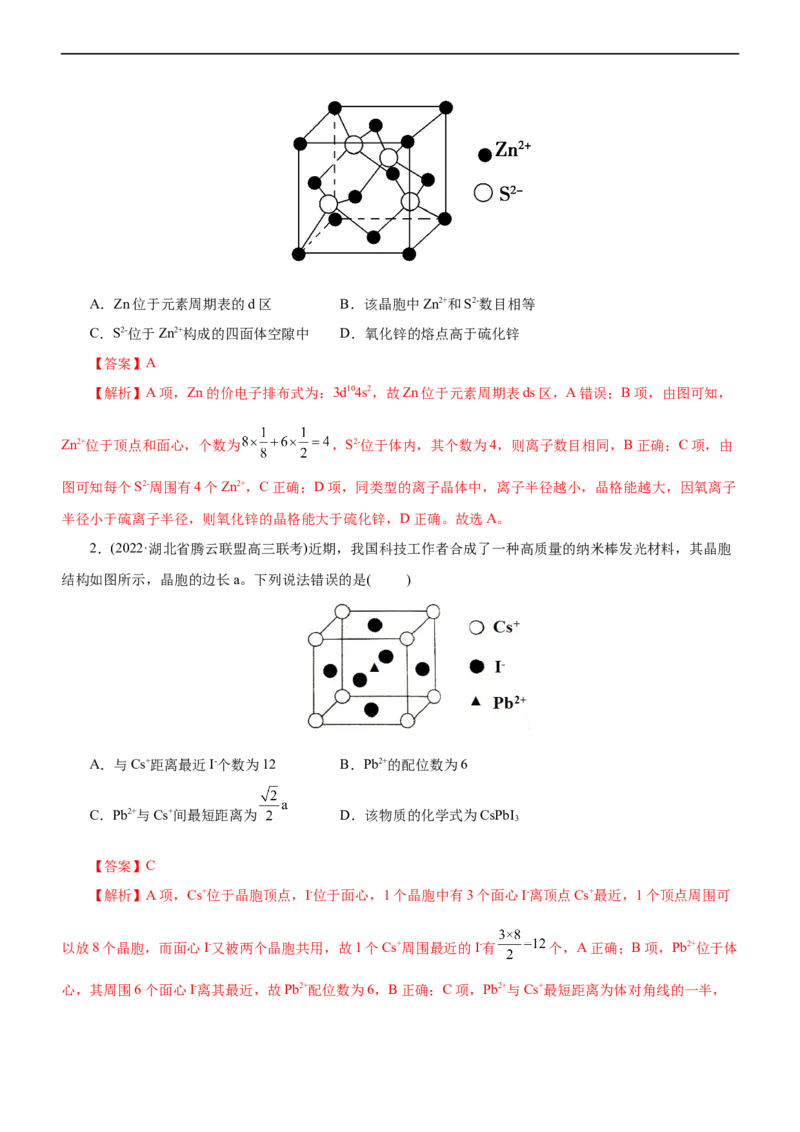
1.(2022·辽宁省名校联盟高三联合考试)锌与硫所形成化合物晶体的晶胞如图所示。下列判断错误的是(
)A.Zn位于元素周期表的d区 B.该晶胞中Zn2+和S2-数目相等
C.S2-位于Zn2+构成的四面体空隙中 D.氧化锌的熔点高于硫化锌
【答案】A
【解析】A项,Zn的价电子排布式为:3d104s2,故Zn位于元素周期表ds区,A错误;B项,由图可知,
Zn2+位于顶点和面心,个数为 ,S2-位于体内,其个数为4,则离子数目相同,B正确;C项,由
图可知每个S2-周围有4个Zn2+,C正确;D项,同类型的离子晶体中,离子半径越小,晶格能越大,因氧离子
半径小于硫离子半径,则氧化锌的晶格能大于硫化锌,D正确。故选A。
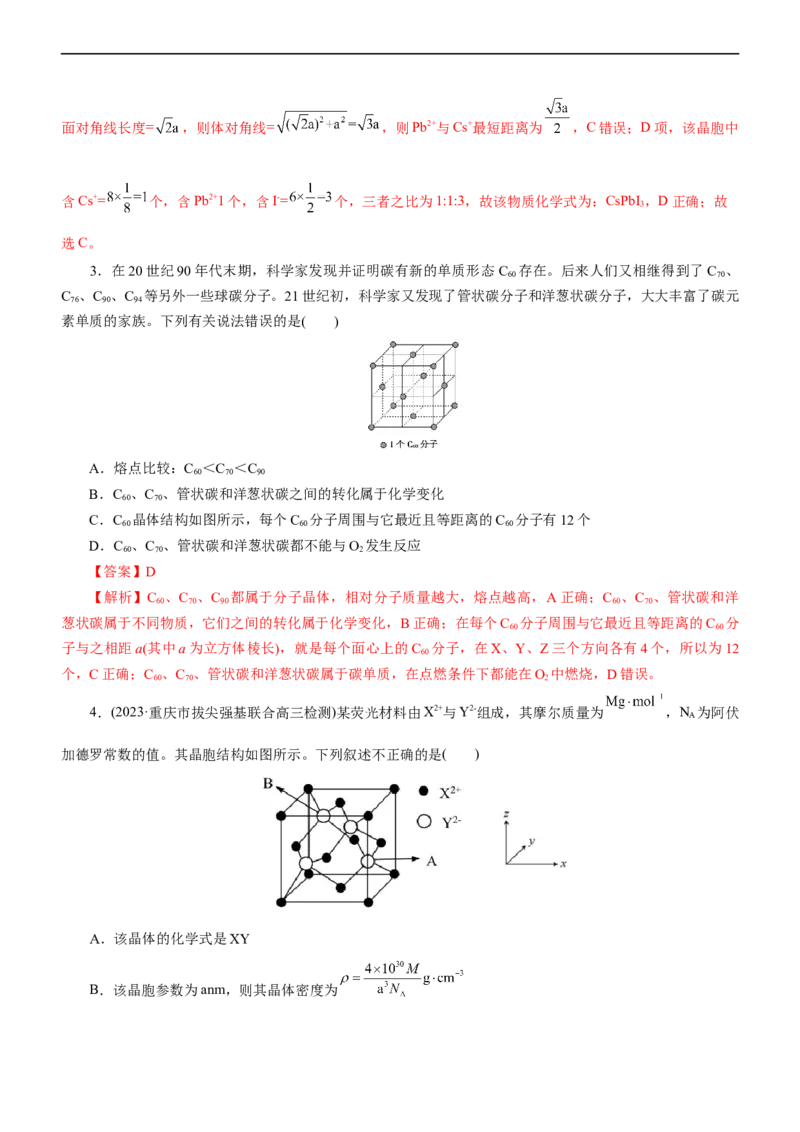
2.(2022·湖北省腾云联盟高三联考)近期,我国科技工作者合成了一种高质量的纳米棒发光材料,其晶胞
结构如图所示,晶胞的边长a。下列说法错误的是( )
A.与Cs+距离最近I-个数为12 B.Pb2+的配位数为6
C.Pb2+与Cs+间最短距离为 D.该物质的化学式为CsPbI
3
【答案】C
【解析】A项,Cs+位于晶胞顶点,I-位于面心,1个晶胞中有3个面心I-离顶点Cs+最近,1个顶点周围可
以放8个晶胞,而面心I-又被两个晶胞共用,故1个Cs+周围最近的I-有 个,A正确;B项,Pb2+位于体
心,其周围6个面心I-离其最近,故Pb2+配位数为6,B正确;C项,Pb2+与Cs+最短距离为体对角线的一半,面对角线长度= ,则体对角线= ,则Pb2+与Cs+最短距离为 ,C错误;D项,该晶胞中
含Cs+= 个,含Pb2+1个,含I-= 个,三者之比为1:1:3,故该物质化学式为:CsPbI ,D正确;故
3
选C。
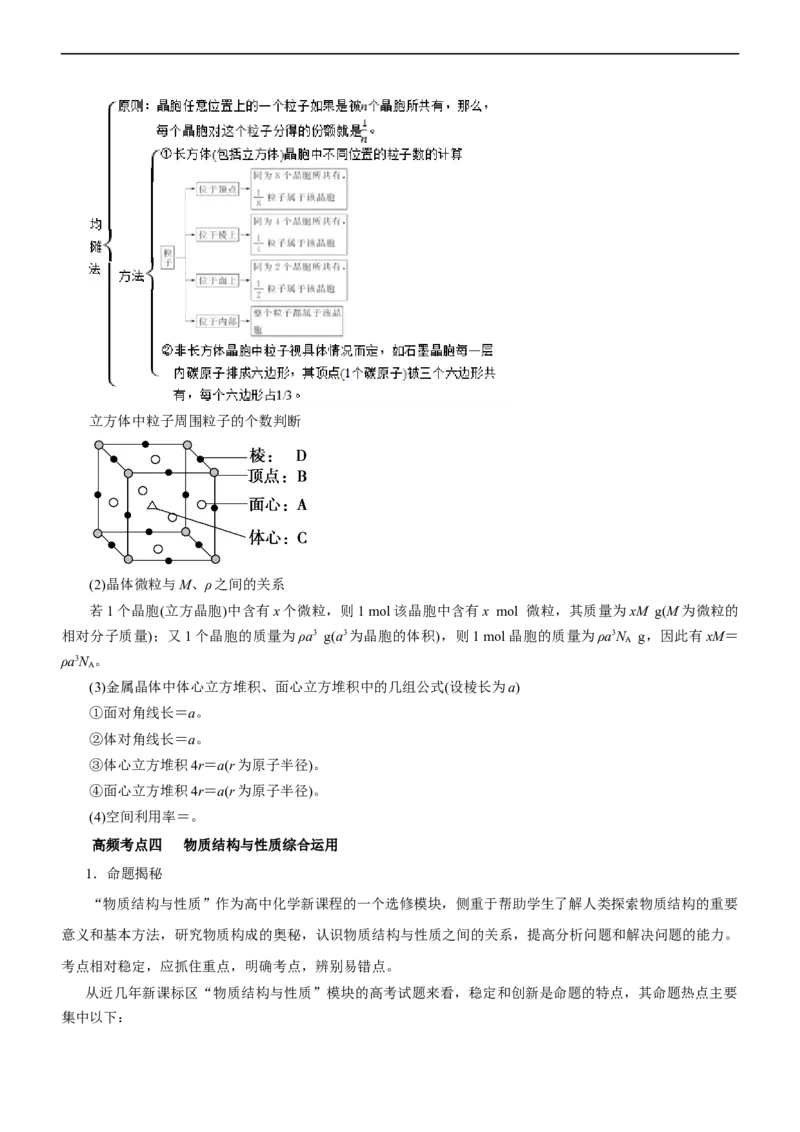
3.在20世纪90年代末期,科学家发现并证明碳有新的单质形态C 存在。后来人们又相继得到了C 、
60 70
C 、C 、C 等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰富了碳元
76 90 94
素单质的家族。下列有关说法错误的是( )
A.熔点比较:C <C <C
60 70 90
B.C 、C 、管状碳和洋葱状碳之间的转化属于化学变化
60 70
C.C 晶体结构如图所示,每个C 分子周围与它最近且等距离的C 分子有12个
60 60 60
D.C 、C 、管状碳和洋葱状碳都不能与O 发生反应
60 70 2
【答案】D
【解析】C 、C 、C 都属于分子晶体,相对分子质量越大,熔点越高,A正确;C 、C 、管状碳和洋
60 70 90 60 70
葱状碳属于不同物质,它们之间的转化属于化学变化,B正确;在每个C 分子周围与它最近且等距离的C 分
60 60
子与之相距a(其中a为立方体棱长),就是每个面心上的C 分子,在X、Y、Z三个方向各有4个,所以为12
60
个,C正确;C 、C 、管状碳和洋葱状碳属于碳单质,在点燃条件下都能在O 中燃烧,D错误。
60 70 2
4.(2023·重庆市拔尖强基联合高三检测)某荧光材料由X2+与Y2-组成,其摩尔质量为 ,N 为阿伏
A
加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是( )
A.该晶体的化学式是XY
B.该晶胞参数为anm,则其晶体密度为C.X2+的配位数是4,Y2-的配位数也是4
D.若A点的原子坐标为 ,则B点的原子坐标为
【答案】B
【解析】A项,由晶胞图可知,1个晶胞中含有X2+的个数为 ,Y2-个数为4,X2+与Y2-个数
比为1:1,因此该晶体的化学式是XY,故A项正确;B项,1个晶胞中含有4个XY,即1个晶胞的质量为
,晶胞体积为 ,因此晶体密度 ,故B项错误;C项,由图可知,距离
X2+最近且等距的Y2-有4个,距离Y2-最近且等距的X2+有4个,故C项正确;D项,若A点的原子坐标为
,则原点位于左下前X2+的顶点,该晶胞自下至上可分为4层(X2+-Y2--X2+-Y2--X2+),同理从左至右也可
分为4层(X2+-Y2--X2+-Y2--X2+),因此B点的原子坐标为 ,故D项正确;故选B。
晶体结构的相关计算
(1)晶胞中粒子数目的计算——均摊法立方体中粒子周围粒子的个数判断
(2)晶体微粒与M、ρ之间的关系
若1个晶胞(立方晶胞)中含有x个微粒,则1 mol该晶胞中含有x mol 微粒,其质量为xM g(M为微粒的
相对分子质量);又1个晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3N g,因此有xM=
A
ρa3N 。
A
(3)金属晶体中体心立方堆积、面心立方堆积中的几组公式(设棱长为a)
①面对角线长=a。
②体对角线长=a。
③体心立方堆积4r=a(r为原子半径)。
④面心立方堆积4r=a(r为原子半径)。
(4)空间利用率=。
高频考点四 物质结构与性质综合运用
1.命题揭秘
“物质结构与性质”作为高中化学新课程的一个选修模块,侧重于帮助学生了解人类探索物质结构的重要
意义和基本方法,研究物质构成的奥秘,认识物质结构与性质之间的关系,提高分析问题和解决问题的能力。
考点相对稳定,应抓住重点,明确考点,辨别易错点。
从近几年新课标区“物质结构与性质”模块的高考试题来看,稳定和创新是命题的特点,其命题热点主要
集中以下:(1)原子结构与性质:基态原子核外电子排布、第一电离能和电负性递变规律等;
(2)分子结构与性质:共价键类型的判断、原子轨道杂化类型、分子构型判断等;
(3)晶体结构与性质:晶体类型的判断、晶体熔沸点高低的比较、氢键对溶解性的影响、晶体密度和晶体
参数的计算、晶体空间利用率的计算等。该知识点的试题能很好地考查考生的空间想象能力,具有很高的区分
度,是“物质的结构与性质”选考题中的必考点。
从题型上看,一般给出一定的知识背景,然后设置3~4个小问题,每一个小题考查相应的知识要点仍是
今后命题的基本模式。
2.突破考点
(1)原子结构与性质。原子核外电子排布式(价电子排布式)、杂化方式、化学键类型、晶体结构、配合物、
电负性、电离能大小的比较、等电子体知识等。
(2)分子结构与性质。分子的成键方式、空间构型、杂化类型、价层电子对理论的计算与应用等方面,
(3)晶体结构与性质。做到识图、辨图、析图,最后深刻记忆,如金刚石、二氧化硅、氯化钠、氯化铯、
氟化钙、干冰等;对于金属晶体的四种堆积模型,要理清半径和晶胞棱长的关系,学会空间利用率的计算方法。
【典例剖析】
【例1】(2022•全国乙卷)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a. 1s22s22p43s1 b. 1s22s22p43d2 c. 1s22s12p5 d. 1s22s22p33p2
(2)①一氯乙烯(C HCl)分子中,C的一个_______杂化轨道与Cl的3p 轨道形成C-Cl_______键,并且Cl的
2 3 x
3p 轨道与C的2p 轨道形成3中心4电子的大π键 。
x x
②一氯乙烷(C HCl)、一氯乙烯(C HCl)、一氯乙炔(C HCl)分子中,C-Cl键长的顺序是_______,理由:
2 5 2 3 2
(ⅰ)C的杂化轨道中s成分越多,形成的 键越强:(ⅱ)_______。
(3)卤化物CsICl 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。解释X的熔
2
点比Y高的原因_______。
(4) α-AgI晶体中 离子作体心立方堆积(如图所示),Ag+主要分布在由I-构成的四面体、八面体等空隙中。
在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因此,α-AgI晶体在电池中可作为_______。已知阿伏加德罗常数为N ,则α-AgI晶体的摩尔体积V =_______ m3/mol (列出算式)。
A m
【答案】(1) ad d
(2) sp2 σ 一氯乙烷>一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的C-Cl键的键长
越短
(3) CsCl CsCl为离子晶体,ICl为分子晶体
(4)电解质
【解析】(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5。a项,1s22s22p43s1,基态氟原子2p能
级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;b项,1s22s22p43d2,核外共10个电子,不是
氟原子,b错误;c项,1s22s12p5,核外共8个电子,不是氟原子,c错误;d项,1s22s22p33p2,基态氟原子2p
能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d正确;故选ad;而同一原子3p能级的能量比3s
能级的能量高,因此能量最高的是1s22s22p33p2,故选d。(2)①一氯乙烯的结构式为 ,碳为
双键碳,采取sp2杂化,因此C的一个sp2杂化轨道与Cl的3p 轨道形成C-Clσ键。②C的杂化轨道中s成分越
x
多,形成的C-Cl键越强,C-Cl键的键长越短,一氯乙烷中碳采取sp3杂化,一氯乙烯中碳采取sp2杂化,一氯
乙炔中碳采取sp杂化,sp杂化时p成分少,sp3杂化时p成分多,因此三种物质中C-Cl键键长顺序为:一氯乙
烷>一氯乙烯>一氯乙炔,同时Cl参与形成的大π键越多,形成的C-Cl键的键长越短,一氯乙烯中Cl的3p 轨
x
道与C的2p 轨道形成3中心4电子的大π键( ),一氯乙炔中Cl的3p 轨道与C的2p 轨道形成2套3中心
x x x4电子的大π键( ),因此三种物质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔。(3)CsICl 发生非
2
氧化还原反应,各元素化合价不变,生成无色晶体和红棕色液体,则无色晶体为CsCl,红棕色液体为ICl,而
CsCl为离子晶体,熔化时,克服的是离子键,ICl为分子晶体,熔化时,克服的是分子间作用力,因此CsCl
的熔点比ICl高。(4)由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是
优良的离子导体,在电池中可作为电解质;每个晶胞中含碘离子的个数为8× +1=2个,依据化学式AgI可知,
银离子个数也为2个,晶胞的物质的量n= mol= mol,晶胞体积V=a3pm3=(504×10-12)3m3,则α-AgI晶体
的摩尔体积V = = = m3/mol。
m
【例2】(2022•海南省选择性考试)以Cu O、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的
2
优势。回答问题:
(1)基态O原子的电子排布式_______,其中未成对电子有_______个。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______。
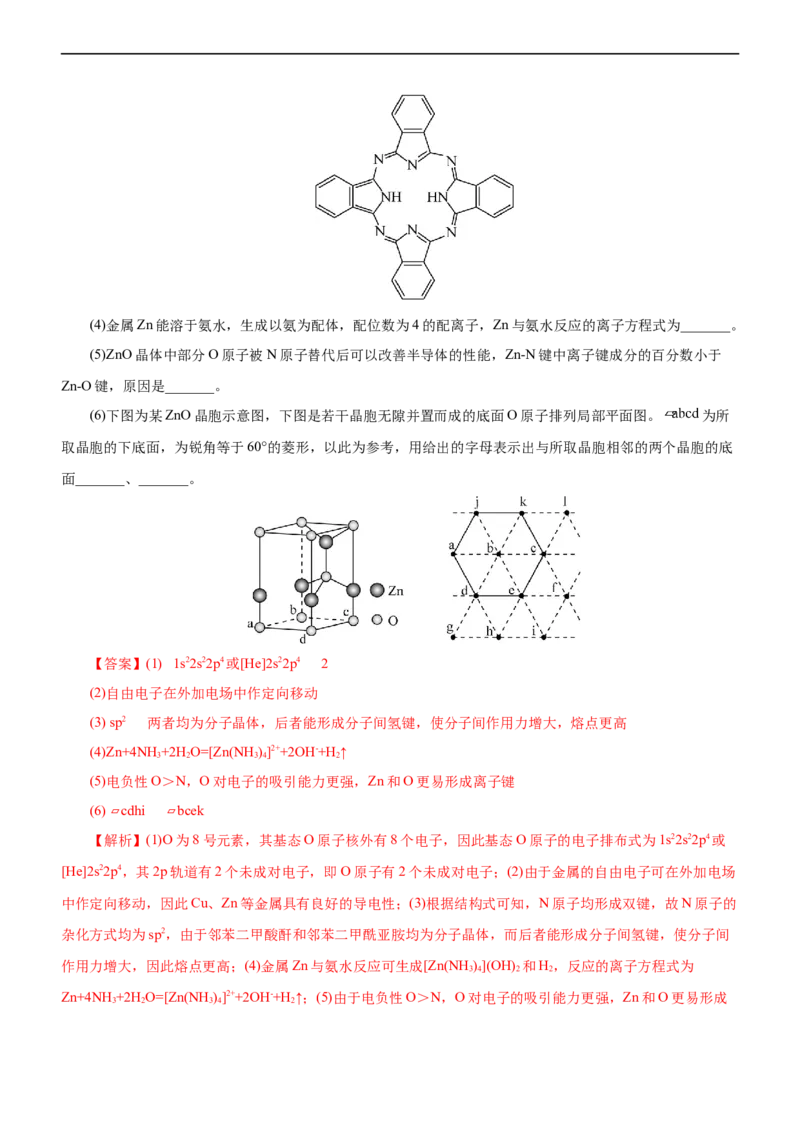
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子
共平面,所有N原子的杂化轨道类型相同,均采取_______杂化。邻苯二甲酸酐( )和邻苯二甲酰亚胺(
)都是合成酞菁的原料,后者熔点高于前者,主要原因是_______。(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于
Zn-O键,原因是_______。
(6)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。 为所
取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底
面_______、_______。
【答案】(1) 1s22s22p4或[He]2s22p4 2
(2)自由电子在外加电场中作定向移动
(3) sp2 两者均为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高
(4)Zn+4NH+2H O=[Zn(NH )]2++2OH-+H ↑
3 2 3 4 2
(5)电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键
(6) ▱cdhi ▱bcek
【解析】(1)O为8号元素,其基态O原子核外有8个电子,因此基态O原子的电子排布式为1s22s22p4或
[He]2s22p4,其2p轨道有2个未成对电子,即O原子有2个未成对电子;(2)由于金属的自由电子可在外加电场
中作定向移动,因此Cu、Zn等金属具有良好的导电性;(3)根据结构式可知,N原子均形成双键,故N原子的
杂化方式均为sp2,由于邻苯二甲酸酐和邻苯二甲酰亚胺均为分子晶体,而后者能形成分子间氢键,使分子间
作用力增大,因此熔点更高;(4)金属Zn与氨水反应可生成[Zn(NH )](OH) 和H,反应的离子方程式为
3 4 2 2
Zn+4NH +2H O=[Zn(NH )]2++2OH-+H ↑;(5)由于电负性O>N,O对电子的吸引能力更强,Zn和O更易形成
3 2 3 4 2离子键,因此Zn—N键中离子键成分的百分数小于Zn—O键;(6)根据晶胞示意图,一个晶胞中8个O原子位
于晶胞的顶点,1个O原子位于晶胞体内,4个Zn原子位于晶胞的棱上,1个Zn原子位于晶胞体内,棱上的3
个Zn原子和体内的Zn原子、O原子形成四面体结构,则于其相邻的晶胞与该晶胞共用bc和cd,则相邻的两
个晶胞的底面为▱cdhi和▱bcek。
【变式探究】
1.(2022•全国甲卷)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现
了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )的共聚物(ETFE)制成。回
2 2 2 2
答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
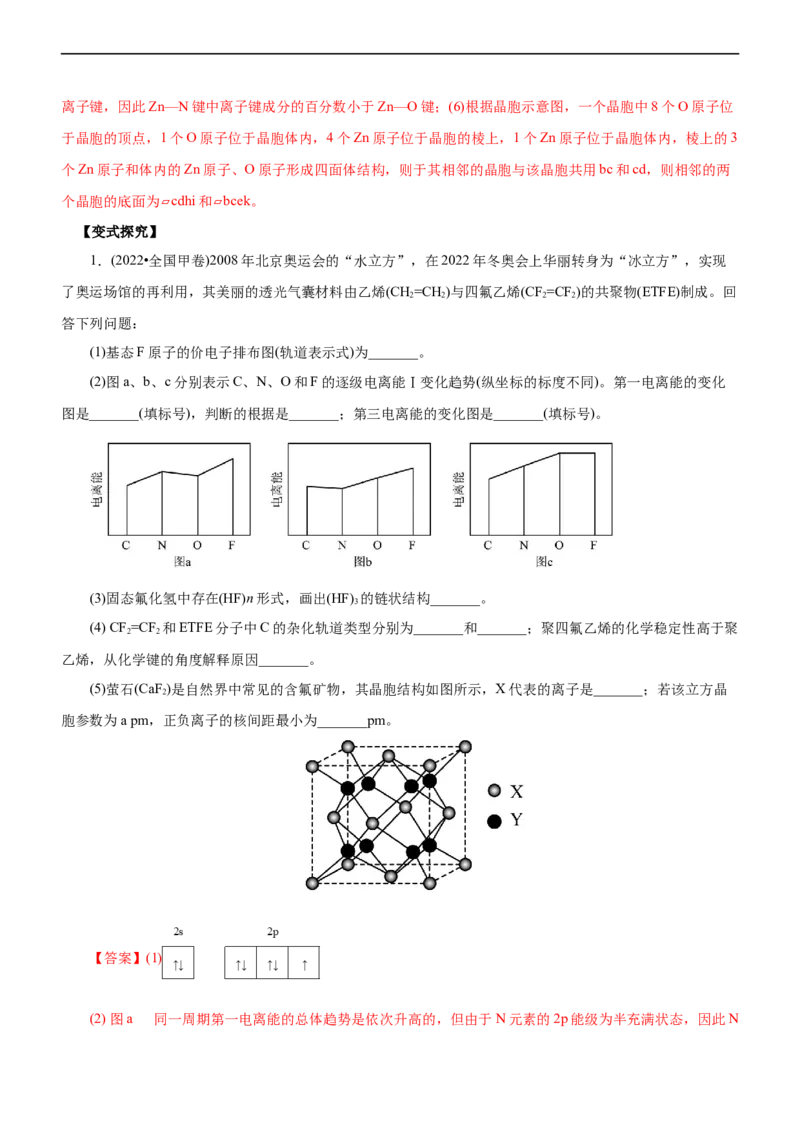
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化
图是_______(填标号),判断的根据是_______;第三电离能的变化图是_______(填标号)。
(3)固态氟化氢中存在(HF)n形式,画出(HF) 的链状结构_______。
3
(4) CF =CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的化学稳定性高于聚
2 2
乙烯,从化学键的角度解释原因_______。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______;若该立方晶
2
胞参数为a pm,正负离子的核间距最小为_______pm。
【答案】(1)
(2) 图a 同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高 图b
(3)
(4) sp2 sp3 C-F键的键能大于聚乙烯中C-H的键能,键能越大,化学性质越稳定
(5) Ca2+ a pm
【解析】根据基态原子的电子表示式书写价电子排布式;根据电离能的排布规律分析电离能趋势和原因;
根据氢键的表示方法书写(HF) 的结构;根据键能影响物质稳定性的规律分析两种物质的稳定性差异;根据均
3
摊法计算晶胞中各粒子的个数,判断粒子种类。(1)F为第9号元素其电子排布为1s22s22p5,则其价电子排布图
为 。(2)C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次
升高的,但由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因此C、N、
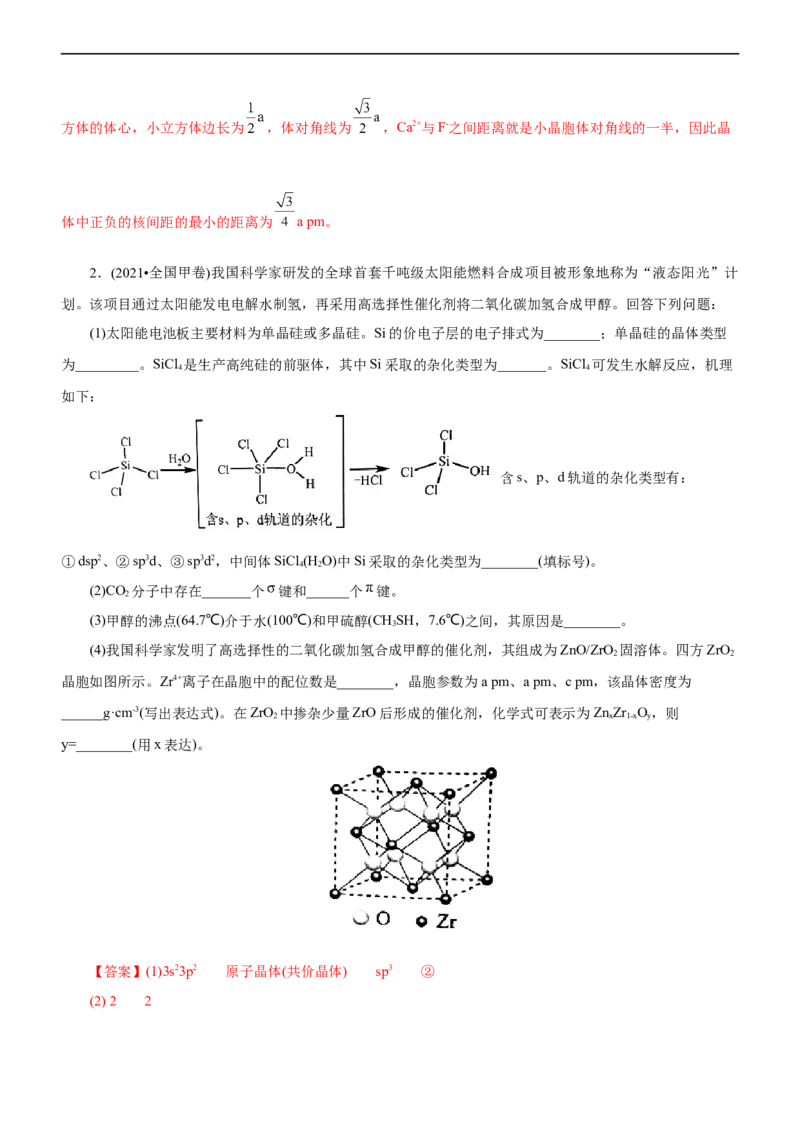
O、F四种元素的第一电离能从小到大的顺序为CC>H 54(3)①O Mg GeO ② ×1021
2 4
【解析】(1)Si位于周期表中第3周期第ⅣA族,基态原子的价电子排布式为3s23p2,则基态Si原子的价
电子排布图为: ;晶体硅、碳化硅均属于原子晶体,原子半径:Si>C,键长:C﹣
Si<Si﹣Si,则键能:C﹣Si>Si﹣Si,所以熔点:碳化硅>晶体硅,晶体硅和碳化硅熔点较高的是 SiC;
(2)①0℃为273K,呈液态的物质是:熔点<273K<沸点;根据表中数据知,SiF 的熔沸点都比273K低,而
4
SiBr 和SiI 的熔沸点都比273K高,只有SiCl 的熔点低于273K,沸点高于273K;根据表中数据知,其熔沸点
4 4 4
依次升高,这4种物质熔沸点都较低,说明为分子晶体,且都不含有氢键,结构相似的分子晶体熔沸点与分子
间作用力成正比,其相对分子质量依次增大,分子间作用力逐渐增强,所以其熔沸点依次升高;根据价层电子
1
对互斥理论,SiX 分子的中心原子的价层电子对数个数为 4+ (4﹣4×1)=4,则分子空间构型为正四面体构型;
4
2
②甲基的C原子形成4个σ键,无孤电子对,C原子价层电子对个数是4,为sp3杂化;环上C原子形成3个σ
键,无孤电子对,价层电子对个数是3,为sp2杂化;元素非金属性越强,其电负性越大,元素的非金属性大
小:N>C>H,则电负性大小顺序为N>C>H;共价单键为σ键、共价双键中含有1个σ键、1个π键,配位
键为 σ 键,则 中含有 12 个 σ 键,则 1 个 分子中含有
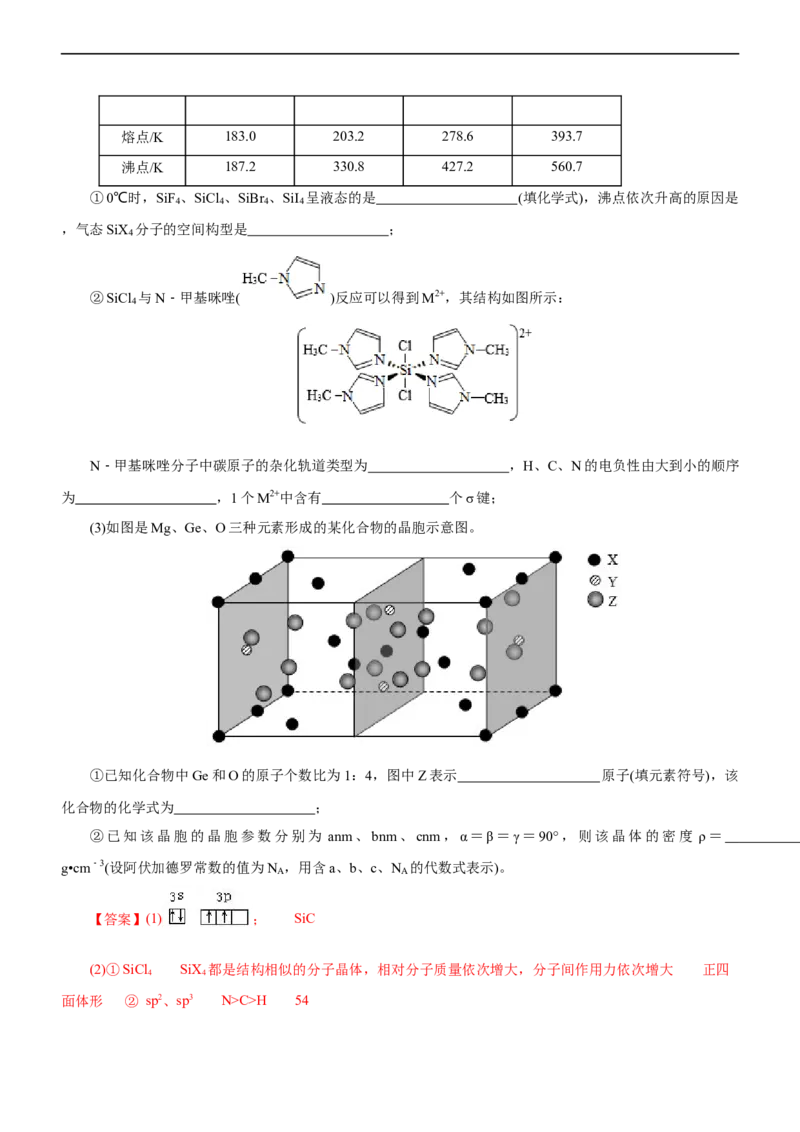
12×4+6=54个σ键,则1mol该物质中含有54molσ键;(3)①根据如图所示晶胞,根据均摊法,Z球位于晶胞
内,位于晶胞的内部,含有4+4+4+4=16个;Y球有4个位于晶胞内,X球位于顶点的有8个,位于4条棱心
1 1 1
的有4个,上下面心上各有2个,晶胞内有5个,则晶胞中共含有的X为8× +4× +4× +5=8个;已知
8 4 2
化合物中Ge和O的原子个数比为1:4,则为1:4比例的为X:Z,所以图中Z表示O原子,Y表示Ge原子,
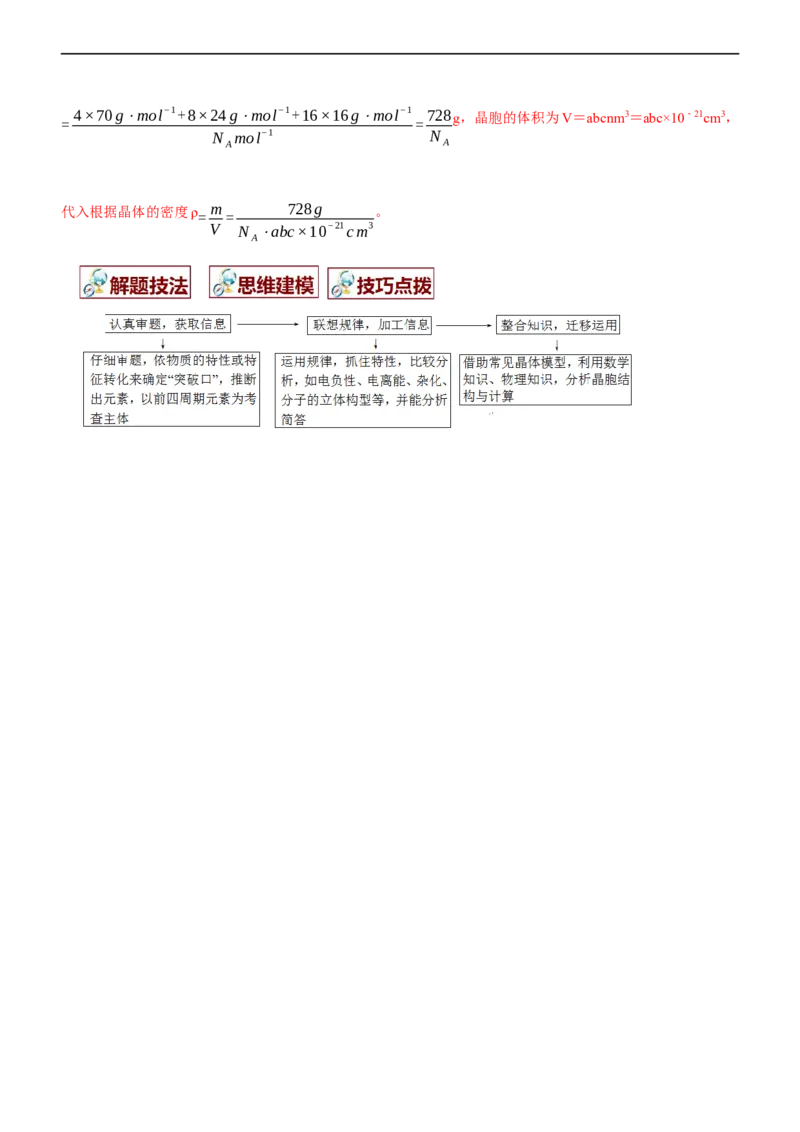
X 表 示 Mg 原 子 , 则 该 化 合 物 的 化 学 式 为 Mg GeO ; ② 晶 胞 的 总 质 量 为 m
2 44×70g⋅mol−1+8×24g⋅mol−1+16×16g⋅mol−1 728g,晶胞的体积为V=abcnm3=abc×10﹣21cm3,
= =
N mol−1 N
A A
代入根据晶体的密度ρ= m
=
728g 。
V N ⋅abc×10−21cm3
A