文档内容
专题 16 化学实验综合题
2020年高考真题
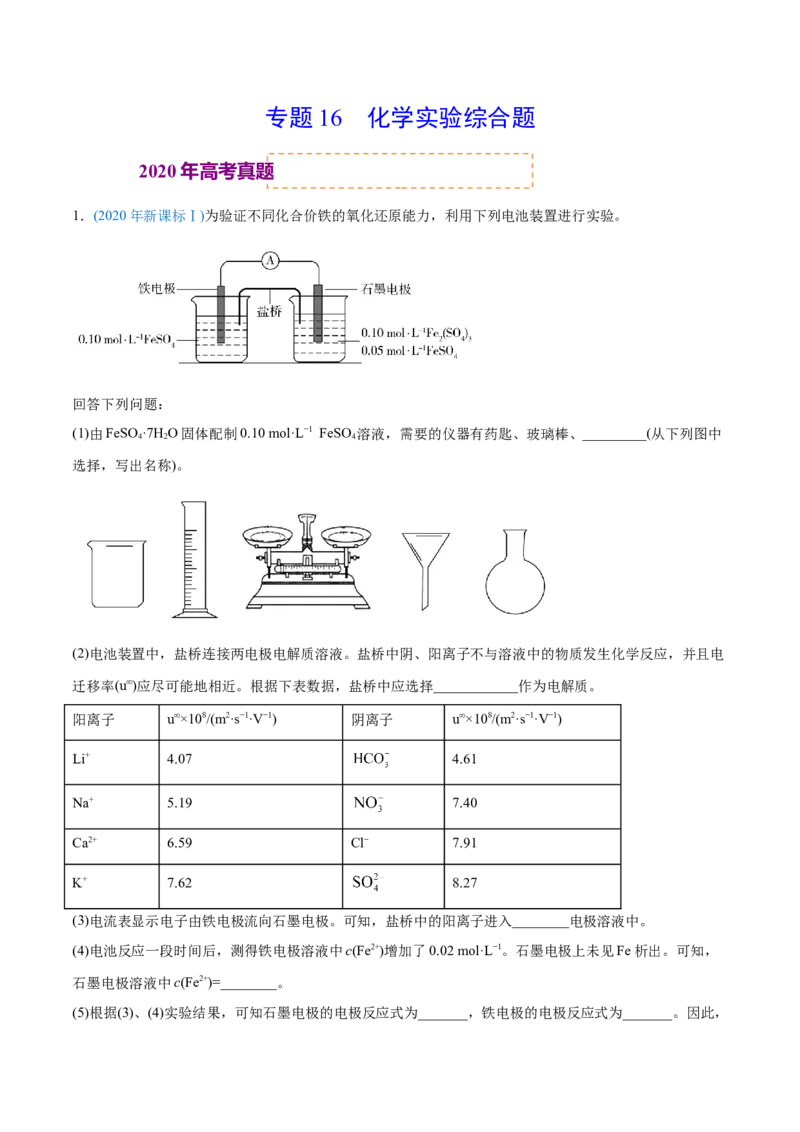
1.(2020年新课标Ⅰ)为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
回答下列问题:
(1)由FeSO ·7H O固体配制0.10 mol·L−1 FeSO 溶液,需要的仪器有药匙、玻璃棒、_________(从下列图中
4 2 4
选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电
迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择____________作为电解质。
阳离子 u∞×108/(m2·s−1·V−1) 阴离子 u∞×108/(m2·s−1·V−1)
Li+ 4.07 4.61
Na+ 5.19 7.40
Ca2+ 6.59 Cl− 7.91
K+ 7.62 8.27
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L−1。石墨电极上未见Fe析出。可知,
石墨电极溶液中c(Fe2+)=________。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为_______,铁电极的电极反应式为_______。因此,验证了Fe2+氧化性小于________,还原性小于________。
(6)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡一段时间,铁电
4 2 4 3
极表面被刻蚀活化。检验活化反应完成的方法是_______。
2.(2020年新课标Ⅱ)苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
+KMnO → + MnO +HCl→ +KCl
4 2
相对分 密度/
名称 熔点/℃ 沸点/℃ 溶解性
子质量
(g·mL−1)
不溶于水,易溶
甲苯 92 −95 110.6 0.867
于乙醇
苯甲 122.4(100℃左右 微溶于冷水,易
122 248 ——
酸 开始升华) 溶于乙醇、热水
实验步骤:
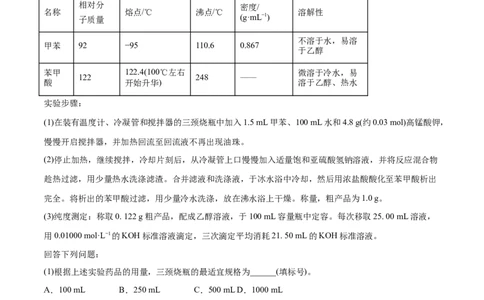
(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,
慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物
趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出
完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25. 00 mL溶液,
用0.01000 mol·L−1的KOH标准溶液滴定,三次滴定平均消耗21. 50 mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为______(填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)在反应装置中应选用______冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完
成,其判断理由是______。
(3)加入适量饱和亚硫酸氢钠溶液的目的是___________;该步骤亦可用草酸在酸性条件下处理,请用反应
的离子方程式表达其原理__________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是_______。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是_______。
(6)本实验制备的苯甲酸的纯度为_______;据此估算本实验中苯甲酸的产率最接近于_______(填标号)。A.70% B.60% C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中__________的方法提纯。
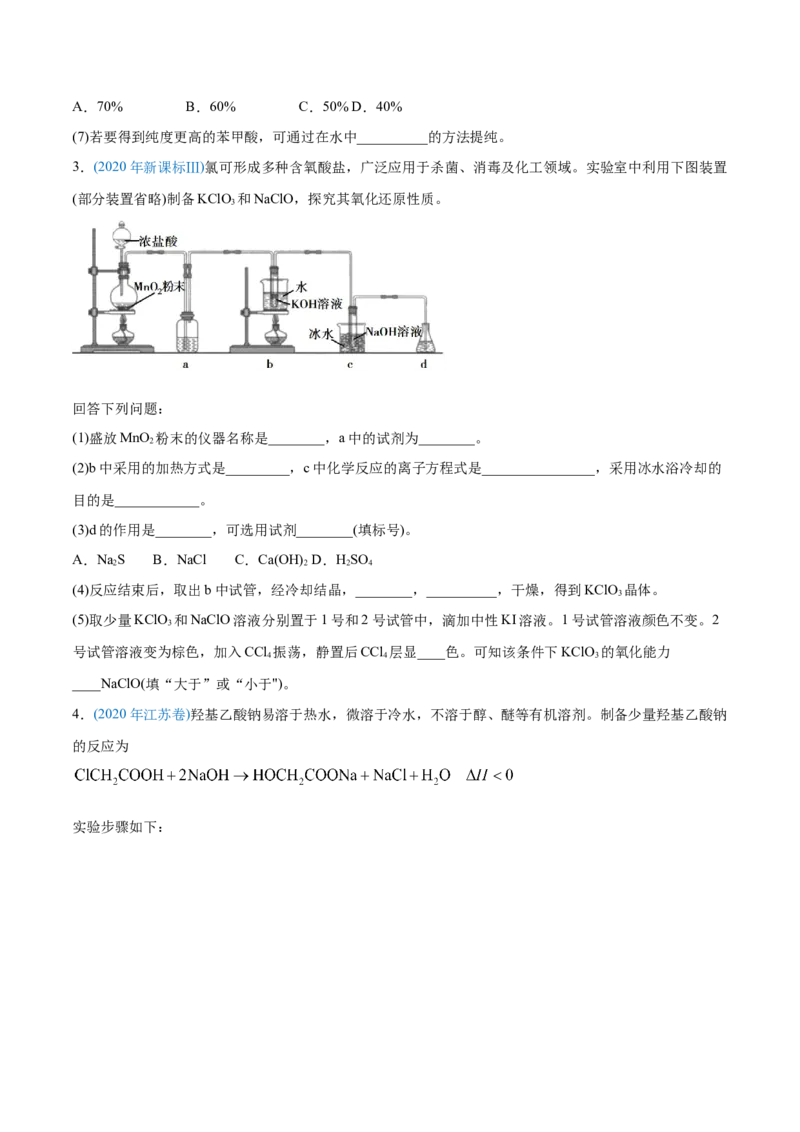
3.(2020年新课标Ⅲ)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置
(部分装置省略)制备KClO 和NaClO,探究其氧化还原性质。
3
回答下列问题:
(1)盛放MnO 粉末的仪器名称是________,a中的试剂为________。
2
(2)b中采用的加热方式是_________,c中化学反应的离子方程式是________________,采用冰水浴冷却的
目的是____________。
(3)d的作用是________,可选用试剂________(填标号)。
A.NaS B.NaCl C.Ca(OH) D.HSO
2 2 2 4
(4)反应结束后,取出b中试管,经冷却结晶,________,__________,干燥,得到KClO 晶体。
3
(5)取少量KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2
3
号试管溶液变为棕色,加入CCl 振荡,静置后CCl 层显____色。可知该条件下KClO 的氧化能力
4 4 3
____NaClO(填“大于”或“小于")。
4.(2020年江苏卷)羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。制备少量羟基乙酸钠
的反应为
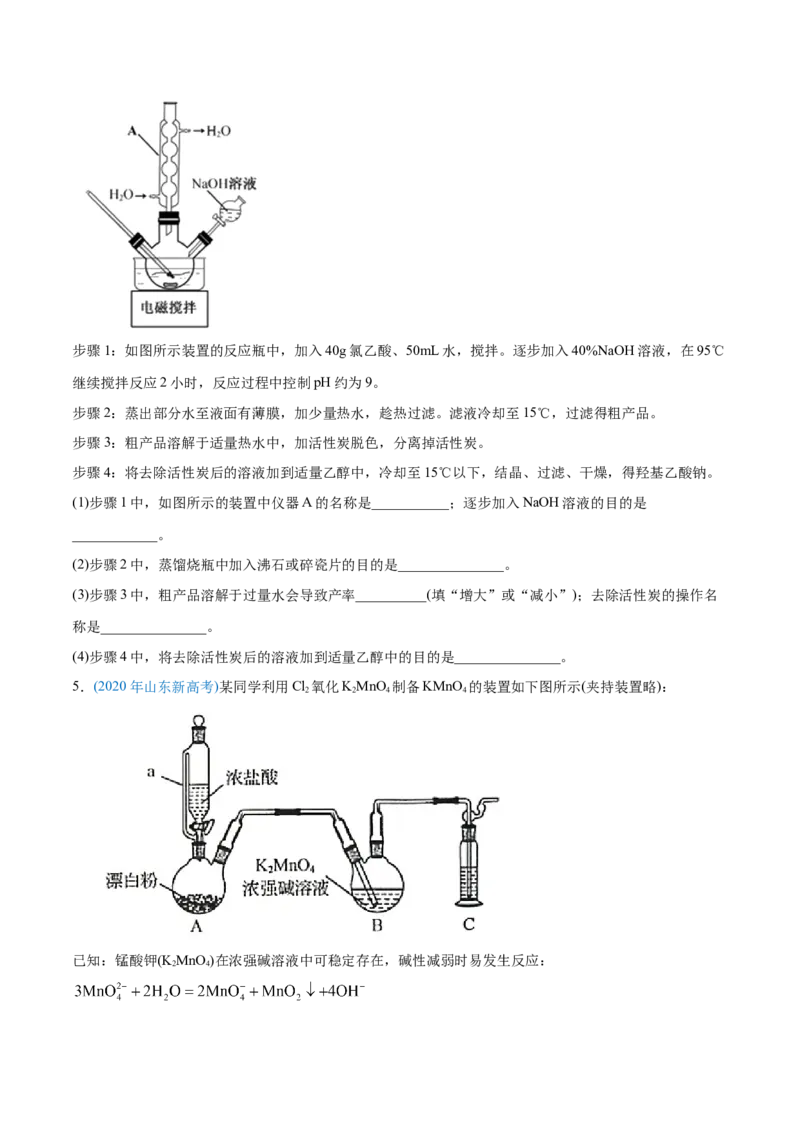
实验步骤如下:步骤1:如图所示装置的反应瓶中,加入40g氯乙酸、50mL水,搅拌。逐步加入40%NaOH溶液,在95℃
继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是___________;逐步加入NaOH溶液的目的是
____________。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是_______________。
(3)步骤3中,粗产品溶解于过量水会导致产率__________(填“增大”或“减小”);去除活性炭的操作名
称是_______________。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是_______________。
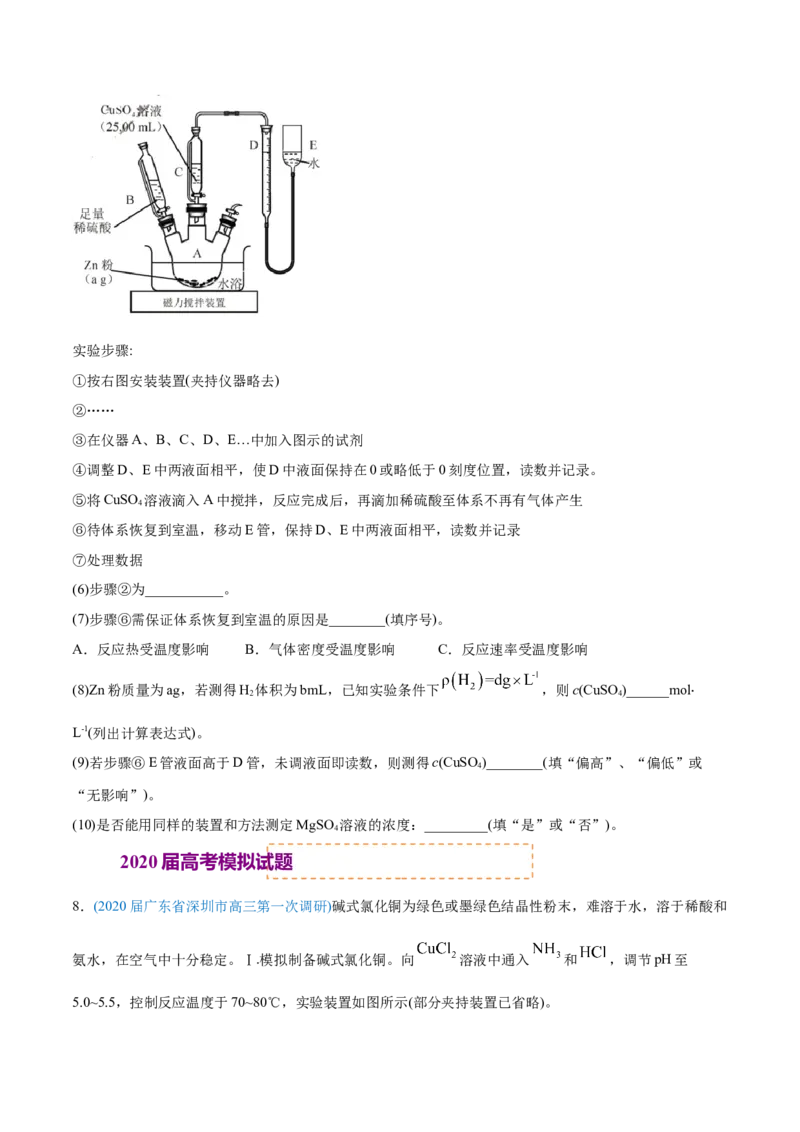
5.(2020年山东新高考)某同学利用Cl 氧化KMnO 制备KMnO 的装置如下图所示(夹持装置略):
2 2 4 4
已知:锰酸钾(K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4回答下列问题:
(1)装置A中a的作用是______________;装置C中的试剂为________________;装置A中制备Cl 的化学
2
方程为______________。
(2)上述装置存在一处缺陷,会导致KMnO 产率降低,改进的方法是________________。
4
(3)KMnO 常作氧化还原滴定的氧化剂,滴定时应将KMnO 溶液加入___________(填“酸式”或“碱式”)
4 4
滴定管中;在规格为50.00mL的滴定管中,若KMnO 溶液起始读数为15.00mL,此时滴定管中KMnO 溶
4 4
液的实际体积为______________(填标号)。
A.15.00 mL B.35.00mL C.大于35.00mL D.小于15.00m1
(4)某FeC O﹒2HO样品中可能含有的杂质为Fe (C O)、HC O﹒2HO,采用KMnO 滴定法测定该样品
2 4 2 2 2 4 3 2 2 4 2 4
的组成,实验步骤如下:
Ⅰ.取mg样品于锥形瓶中,加入稀HSO 溶解,水浴加热至75℃。用 c mol﹒L-1的KMnO 溶液趁热滴定至
2 4 4
溶液出现粉红色且30s内不褪色,消耗KMnO 溶液VmL。
4 1
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀HSO 酸化后,在75℃继续用KMnO 溶液
2 4 4
滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO 溶液VmL。
4 2
样品中所含 的质量分数表达式为_________________。
下列关于样品组成分析的说法,正确的是__________(填标号)。
A. 时,样品中一定不含杂质
B. 越大,样品中 含量一定越高
C.若步骤I中滴入KMnO 溶液不足,则测得样品中Fe元素含量偏低
4
D.若所用KMnO 溶液实际浓度偏低,则测得样品中Fe元素含量偏高
4
6.(2020年7月浙江选考)硫代硫酸钠在纺织业等领域有广泛应用。某兴趣小组用下图装置制备
。合成反应:
滴定反应:
已知: 易溶于水,难溶于乙醇, 开始失结晶水。
实验步骤:
Ⅰ. 制备:装置A制备的 经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液 约
为7时,停止通入 气体,得产品混合溶液。
Ⅱ.产品分离提纯:产品混合溶液经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到 产品。
Ⅲ.产品纯度测定:以淀粉作指示剂,用 产品配制的溶液滴定碘标准溶液至滴定终点,计
算 含量。
请回答:
(1)步骤Ⅰ:单向阀的作用是______;装置C中的反应混合溶液 过高或过低将导致产率降低,原因是
_______。
(2)步骤Ⅱ:下列说法正确的是_____。
A 快速蒸发溶液中水分,可得较大晶体颗粒
B 蒸发浓缩至溶液表面出现品晶膜时,停止加热
C 冷却结晶后的固液混合物中加入乙醇可提高产率D 可选用冷的 溶液作洗涤剂
(3)步骤Ⅲ
①滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→(______)→(______)→(______)→(______)→(______)→开始滴定。
A 烘干 B 装入滴定液至零刻度以上 C 调整滴定液液面至零刻度或零刻度以下D 用洗耳球吹出润洗液
E 排除气泡 F 用滴定液润洗2至3次 G 记录起始读数
②装标准碘溶液的碘量瓶(带瓶塞的锥形瓶)在滴定前应盖上瓶塞,目的是______。
③滴定法测得产品中 含量为 ,则 产品中可能混有的物质是
________。
7.(2020年天津卷)为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
4
Ⅰ.甲方案
实验原理:
实验步骤:
(1)判断 沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO )=________mol‧L-1。
4
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )_________(填“偏高”、“偏低”或“无影
4
响”)。
Ⅱ.乙方案
实验原理: ,实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
4
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
A.反应热受温度影响 B.气体密度受温度影响 C.反应速率受温度影响
(8)Zn粉质量为ag,若测得H 体积为bmL,已知实验条件下 ,则c(CuSO )______mol‧
2 4
L-1(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )________(填“偏高”、“偏低”或
4
“无影响”)。
(10)是否能用同样的装置和方法测定MgSO 溶液的浓度:_________(填“是”或“否”)。
4
2020届高考模拟试题
8.(2020届广东省深圳市高三第一次调研)碱式氯化铜为绿色或墨绿色结晶性粉末,难溶于水,溶于稀酸和
氨水,在空气中十分稳定。Ⅰ.模拟制备碱式氯化铜。向 溶液中通入 和 ,调节pH至
5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。(1)仪器X的名称是________,其主要作用有导气、________。
(2)实验室利用装置A制 ,发生反应的化学方程式为________。
(3)反应过程中,在三颈烧瓶内除观察到溶液蓝绿色褪去,还可能观察到的现象是________、________、
________。
(4)若体系 过高会导致碱式氯化铜的产量_______(填“偏高”、“偏低”或“无影响”)。
(5)反应结束后,将三颈瓶中的混合物过滤,从滤液中还可以获得的副产品是________(填化学式),经提纯
得产品无水碱式氯化铜。
Ⅱ.无水碱式氯化铜组成的测定。称取产品 ,加硝酸溶解,并加水定容至200mL,得到待测液。
(6)铜的测定:取20.00mL测液,经测定, 浓为 。则称取的样品中
________mol。
(7)采用沉淀滴定法测定氯:用 标准溶液滴定过量的 ,实验如图:
①滴定时,应选用下列哪种物质作为指示剂________(填标号)。
A. B. C.②重复实验操作三次,消耗 溶液的体积平均为10.00mL。则称取的样品中
______mol。
(8)根据上述实验结果可推知无水碱式氯化铜的化学式为________。
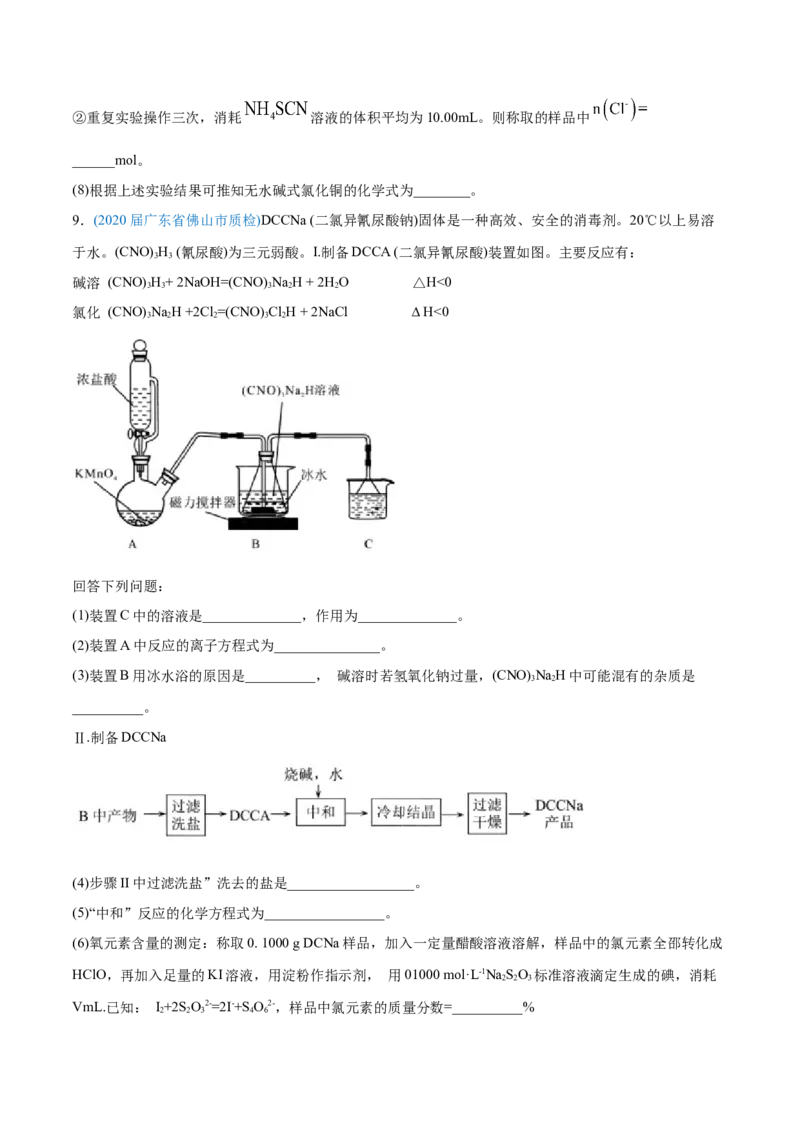
9.(2020届广东省佛山市质检)DCCNa (二氯异氰尿酸钠)固体是一种高效、安全的消毒剂。20℃以上易溶
于水。(CNO) H (氰尿酸)为三元弱酸。I.制备DCCA (二氯异氰尿酸)装置如图。主要反应有:
3 3
碱溶 (CNO) H+ 2NaOH=(CNO) NaH + 2HO △H<0
3 3 3 2 2
氯化 (CNO) NaH +2Cl =(CNO) ClH + 2NaCl ∆ H<0
3 2 2 3 2
回答下列问题:
(1)装置C中的溶液是______________,作用为______________。
(2)装置A中反应的离子方程式为_______________。
(3)装置B用冰水浴的原因是__________, 碱溶时若氢氧化钠过量,(CNO) NaH中可能混有的杂质是
3 2
__________。
Ⅱ.制备DCCNa
(4)步骤II中过滤洗盐”洗去的盐是__________________。
(5)“中和”反应的化学方程式为_________________。
(6)氧元素含量的测定:称取0. 1000 g DCNa样品,加入一定量醋酸溶液溶解,样品中的氯元素全邵转化成
HClO,再加入足量的KI溶液,用淀粉作指示剂, 用01000 mol·L-1NaSO 标准溶液滴定生成的碘,消耗
2 2 3
VmL.已知: I+2S O2-=2I-+S O2-,样品中氯元素的质量分数=__________%
2 2 3 4 610.(2020届广东省茂名市高三二模)二甲基砜是合成人体胶原蛋白的必要物质。实验室用二甲基硫醚为原
料合成二甲基砜的新方法为:反应 i:(CH)S+HO→(CH)SO+H O
3 2 2 2 3 2 2
反应 ii: 。
二甲基亚枫
二甲基硫醚(CH)S 二甲基砜(CH)SO
3 2 (CH)SO 3 2 2
3 2
密度 0.85 g·cm-3 1.10 g·cm-3 ——
熔点/沸点 -83.2℃/37.5℃ 18.4℃/189℃ 111℃/238℃
溶解性 不溶于水 易溶于水、乙醇 易溶于水、乙醇
具体流程如下:
回答下列问题:
(1)反应装置如图所示,仪器 B 的名称是_____,其作用是_____。
(2)第①步反应温度不高于 40 ℃的原因是_____;该步骤反应完全的现象是_____。
(3)第②步先将 A 中滴加剩余的 HO 全部加入三颈烧瓶中,然后加热发生反应 ii。该反应的化学方程式
2 2
为_____。
(4)第③步的实验操作为_____、过滤、低温干燥,得到二甲基砜产品。
(5)二甲基砜传统的生产工艺是由 HNO 氧化(CH)S 生成(CH)SO,然后用 NaOH 中和、精馏,制得精
3 3 2 3 2
品(CH)SO,最后再经氧化制得(CH)SO 。该新方法与传统硝酸氧化法比的优点有_____(至少回答 2 点)。
3 2 3 2 2
(6)该实验中制得二甲基砜 19.176g。二甲基砜的产率为_____。
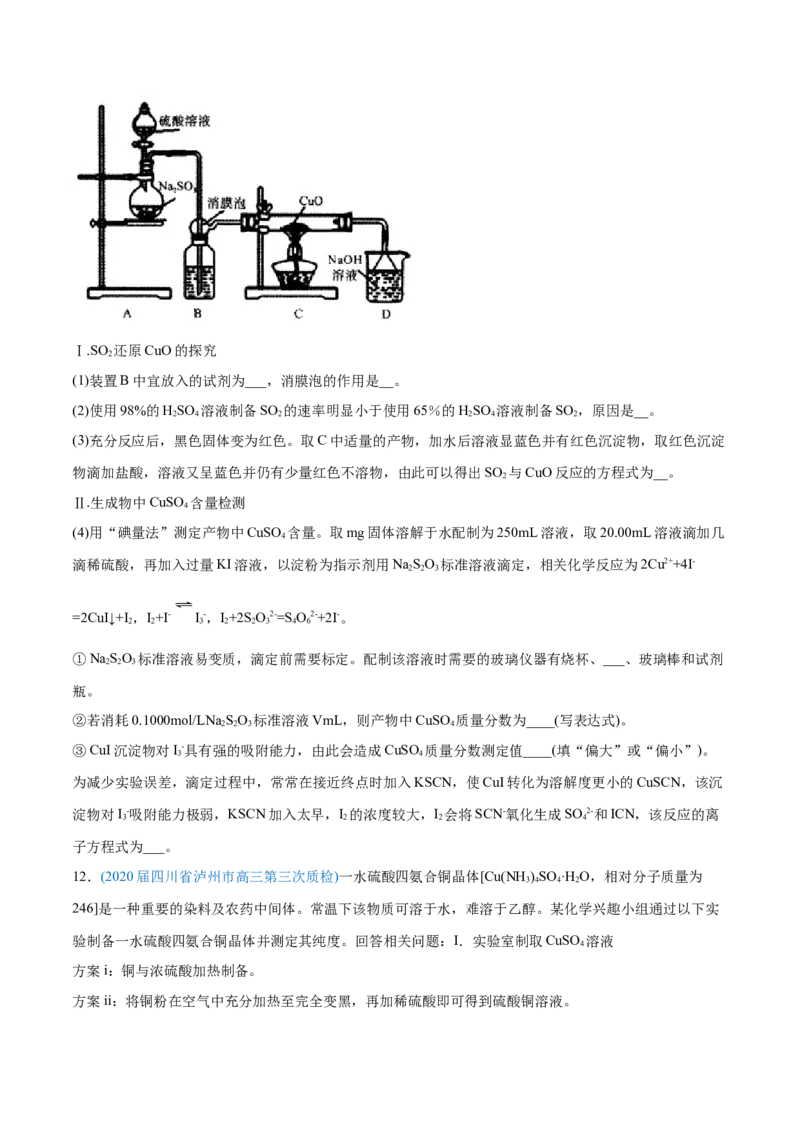
11.(2020届安徽省合肥市高三线上考试)实验室利用如图装置探究SO 还原CuO,并进一步检测产物含量。
2
已知Cu O+2H+=Cu+Cu2++H O。回答下列相关问题:
2 2Ⅰ.SO 还原CuO的探究
2
(1)装置B中宜放入的试剂为___,消膜泡的作用是__。
(2)使用98%的HSO 溶液制备SO 的速率明显小于使用65%的HSO 溶液制备SO ,原因是__。
2 4 2 2 4 2
(3)充分反应后,黑色固体变为红色。取C中适量的产物,加水后溶液显蓝色并有红色沉淀物,取红色沉淀
物滴加盐酸,溶液又呈蓝色并仍有少量红色不溶物,由此可以得出SO 与CuO反应的方程式为__。
2
Ⅱ.生成物中CuSO 含量检测
4
(4)用“碘量法”测定产物中CuSO 含量。取mg固体溶解于水配制为250mL溶液,取20.00mL溶液滴加几
4
滴稀硫酸,再加入过量KI溶液,以淀粉为指示剂用NaSO 标准溶液滴定,相关化学反应为2Cu2++4I-
2 2 3
=2CuI↓+I ,I+I- I-,I+2S O2-=S O2-+2I-。
2 2 3 2 2 3 4 6
①NaSO 标准溶液易变质,滴定前需要标定。配制该溶液时需要的玻璃仪器有烧杯、___、玻璃棒和试剂
2 2 3
瓶。
②若消耗0.1000mol/LNa SO 标准溶液VmL,则产物中CuSO 质量分数为____(写表达式)。
2 2 3 4
③CuI沉淀物对I-具有强的吸附能力,由此会造成CuSO 质量分数测定值____(填“偏大”或“偏小”)。
3 4
为减少实验误差,滴定过程中,常常在接近终点时加入KSCN,使CuI转化为溶解度更小的CuSCN,该沉
淀物对I-吸附能力极弱,KSCN加入太早,I 的浓度较大,I 会将SCN-氧化生成SO 2-和ICN,该反应的离
3 2 2 4
子方程式为___。
12.(2020届四川省泸州市高三第三次质检)一水硫酸四氨合铜晶体[Cu(NH )SO ·H O,相对分子质量为
3 4 4 2
246]是一种重要的染料及农药中间体。常温下该物质可溶于水,难溶于乙醇。某化学兴趣小组通过以下实
验制备一水硫酸四氨合铜晶体并测定其纯度。回答相关问题:I.实验室制取CuSO 溶液
4
方案i:铜与浓硫酸加热制备。
方案ii:将铜粉在空气中充分加热至完全变黑,再加稀硫酸即可得到硫酸铜溶液。(1)请写出方案i反应的化学方程式____,其缺点是____(写1点)。
(2)实际生产中方案ii常常有紫红色固体未反应,猜想原因可能是____。
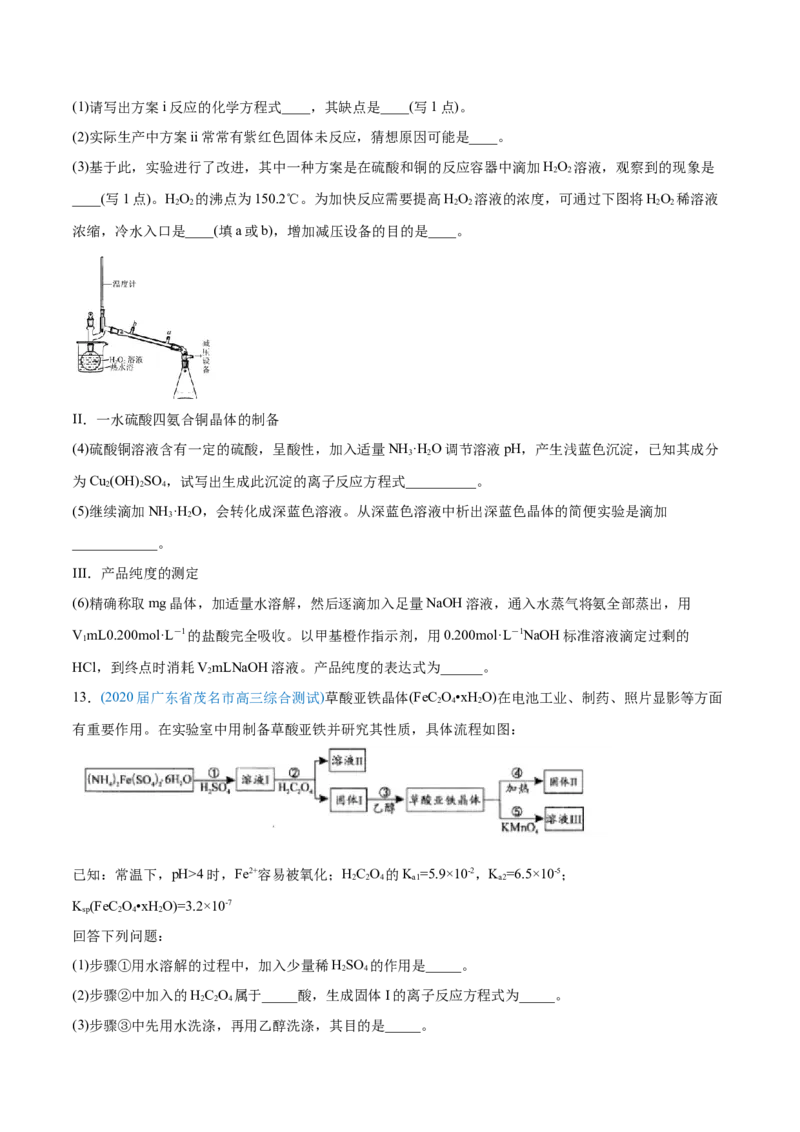
(3)基于此,实验进行了改进,其中一种方案是在硫酸和铜的反应容器中滴加HO 溶液,观察到的现象是
2 2
____(写1点)。HO 的沸点为150.2℃。为加快反应需要提高HO 溶液的浓度,可通过下图将HO 稀溶液
2 2 2 2 2 2
浓缩,冷水入口是____(填a或b),增加减压设备的目的是____。
II.一水硫酸四氨合铜晶体的制备
(4)硫酸铜溶液含有一定的硫酸,呈酸性,加入适量NH ·H O调节溶液pH,产生浅蓝色沉淀,已知其成分
3 2
为Cu (OH) SO ,试写出生成此沉淀的离子反应方程式__________。
2 2 4
(5)继续滴加NH ·H O,会转化成深蓝色溶液。从深蓝色溶液中析出深蓝色晶体的简便实验是滴加
3 2
____________。
III.产品纯度的测定
(6)精确称取mg晶体,加适量水溶解,然后逐滴加入足量NaOH溶液,通入水蒸气将氨全部蒸出,用
VmL0.200mol·L-1的盐酸完全吸收。以甲基橙作指示剂,用0.200mol·L-1NaOH标准溶液滴定过剩的
1
HCl,到终点时消耗VmLNaOH溶液。产品纯度的表达式为______。
2
13.(2020届广东省茂名市高三综合测试)草酸亚铁晶体(FeC O•xH O)在电池工业、制药、照片显影等方面
2 4 2
有重要作用。在实验室中用制备草酸亚铁并研究其性质,具体流程如图:
已知:常温下,pH>4时,Fe2+容易被氧化;HC O 的K =5.9×10-2,K =6.5×10-5;
2 2 4 a1 a2
K (FeC O•xH O)=3.2×10-7
sp 2 4 2
回答下列问题:
(1)步骤①用水溶解的过程中,加入少量稀HSO 的作用是_____。
2 4
(2)步骤②中加入的HC O 属于_____酸,生成固体I的离子反应方程式为_____。
2 2 4
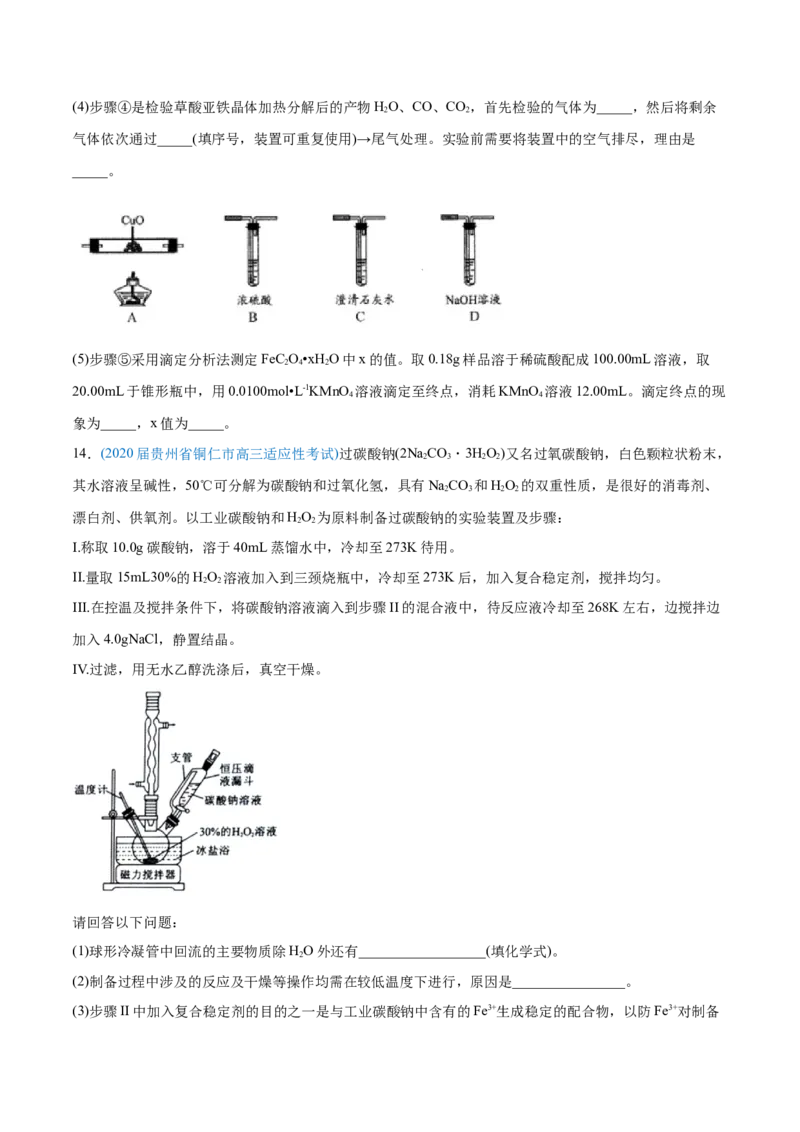
(3)步骤③中先用水洗涤,再用乙醇洗涤,其目的是_____。(4)步骤④是检验草酸亚铁晶体加热分解后的产物HO、CO、CO,首先检验的气体为_____,然后将剩余
2 2
气体依次通过_____(填序号,装置可重复使用)→尾气处理。实验前需要将装置中的空气排尽,理由是
_____。
(5)步骤⑤采用滴定分析法测定FeC O•xH O中x的值。取0.18g样品溶于稀硫酸配成100.00mL溶液,取
2 4 2
20.00mL于锥形瓶中,用0.0100mol•L-1KMnO 溶液滴定至终点,消耗KMnO 溶液12.00mL。滴定终点的现
4 4
象为_____,x值为_____。
14.(2020届贵州省铜仁市高三适应性考试)过碳酸钠(2Na CO・3HO)又名过氧碳酸钠,白色颗粒状粉末,
2 3 2 2
其水溶液呈碱性,50℃可分解为碳酸钠和过氧化氢,具有NaCO 和HO 的双重性质,是很好的消毒剂、
2 3 2 2
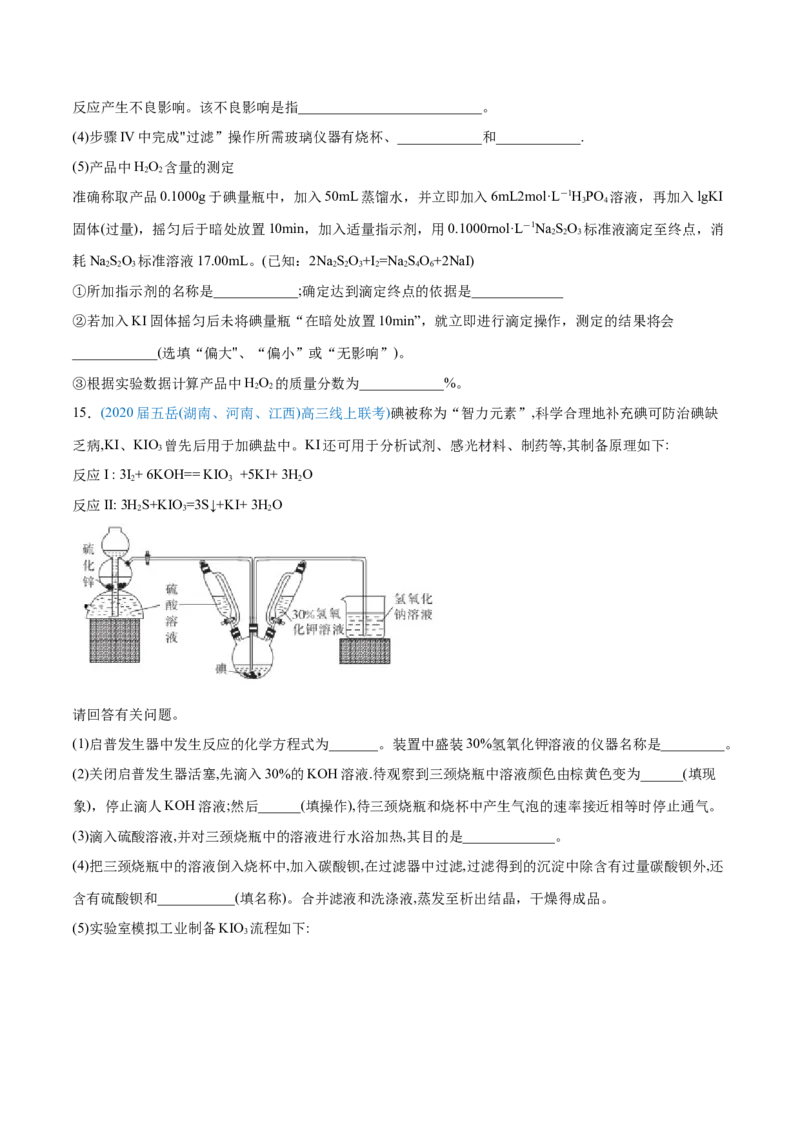
漂白剂、供氧剂。以工业碳酸钠和HO 为原料制备过碳酸钠的实验装置及步骤:
2 2
I.称取10.0g碳酸钠,溶于40mL蒸馏水中,冷却至273K待用。
II.量取15mL30%的HO 溶液加入到三颈烧瓶中,冷却至273K后,加入复合稳定剂,搅拌均匀。
2 2
III.在控温及搅拌条件下,将碳酸钠溶液滴入到步骤II的混合液中,待反应液冷却至268K左右,边搅拌边
加入4.0gNaCl,静置结晶。
IV.过滤,用无水乙醇洗涤后,真空干燥。
请回答以下问题:
(1)球形冷凝管中回流的主要物质除HO外还有__________________(填化学式)。
2
(2)制备过程中涉及的反应及干燥等操作均需在较低温度下进行,原因是________________。
(3)步骤II中加入复合稳定剂的目的之一是与工业碳酸钠中含有的Fe3+生成稳定的配合物,以防Fe3+对制备反应产生不良影响。该不良影响是指__________________________。
(4)步骤IV中完成"过滤”操作所需玻璃仪器有烧杯、____________和____________.
(5)产品中HO 含量的测定
2 2
准确称取产品0.1000g于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2mol·L-1HPO 溶液,再加入lgKI
3 4
固体(过量),摇匀后于暗处放置10min,加入适量指示剂,用0.1000rnol·L-1NaSO 标准液滴定至终点,消
2 2 3
耗NaSO 标准溶液17.00mL。(已知:2NaSO+I =Na SO+2NaI)
2 2 3 2 2 3 2 2 4 6
①所加指示剂的名称是____________;确定达到滴定终点的依据是_____________
②若加入KI固体摇匀后未将碘量瓶“在暗处放置10min”,就立即进行滴定操作,测定的结果将会
____________(选填“偏大"、“偏小”或“无影响”)。
③根据实验数据计算产品中HO 的质量分数为____________%。
2 2
15.(2020届五岳(湖南、河南、江西)高三线上联考)碘被称为“智力元素”,科学合理地补充碘可防治碘缺
乏病,KI、KIO 曾先后用于加碘盐中。KI还可用于分析试剂、感光材料、制药等,其制备原理如下:
3
反应I : 3I + 6KOH== KIO +5KI+ 3H O
2 3 2
反应II: 3H S+KIO =3S↓+KI+ 3H O
2 3 2
请回答有关问题。
(1)启普发生器中发生反应的化学方程式为_______。装置中盛装30%氢氧化钾溶液的仪器名称是_________。
(2)关闭启普发生器活塞,先滴入30%的KOH溶液.待观察到三颈烧瓶中溶液颜色由棕黄色变为______(填现
象),停止滴人KOH溶液;然后______(填操作),待三颈烧瓶和烧杯中产生气泡的速率接近相等时停止通气。
(3)滴入硫酸溶液,并对三颈烧瓶中的溶液进行水浴加热,其目的是_____________。
(4)把三颈烧瓶中的溶液倒入烧杯中,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还
含有硫酸钡和___________(填名称)。合并滤液和洗涤液,蒸发至析出结晶,干燥得成品。
(5)实验室模拟工业制备KIO 流程如下:
3几种物质的溶解度见下表:
①由上表数据分析可知,“操作a”为__________________。
②用惰性电极电解KI溶液也能制备KIO ,与电解法相比,上述流程制备KIO 的缺点是____________。
3 3
(6)某同学测定.上述流程生产的KIO 样品的纯度。
3
取1.00 g样品溶于蒸馏水中并用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加2.0 mol●L-1
NaSO 溶液,恰好完全反应时共消耗12. 60 mL Na SO 溶液。该样品中KIO 的质量分数为_______(已知反
2 2 3 2 2 3 3
应:I +2Na SO=2NaI+Na SO)。
2 2 2 3 2 4 6
16.(2020届河北省名校联盟高三联考)实验室以VO 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体
2 5
{(NH )[(VO) (CO)(OH) ] ·10H O},其流程如图:VO VOCl 溶液 氧钒(Ⅳ)碱式
4 5 6 3 4 9 2 2 5 2
碳酸铵晶体
(1)“还原”过程中的还原剂是__(填化学式)。
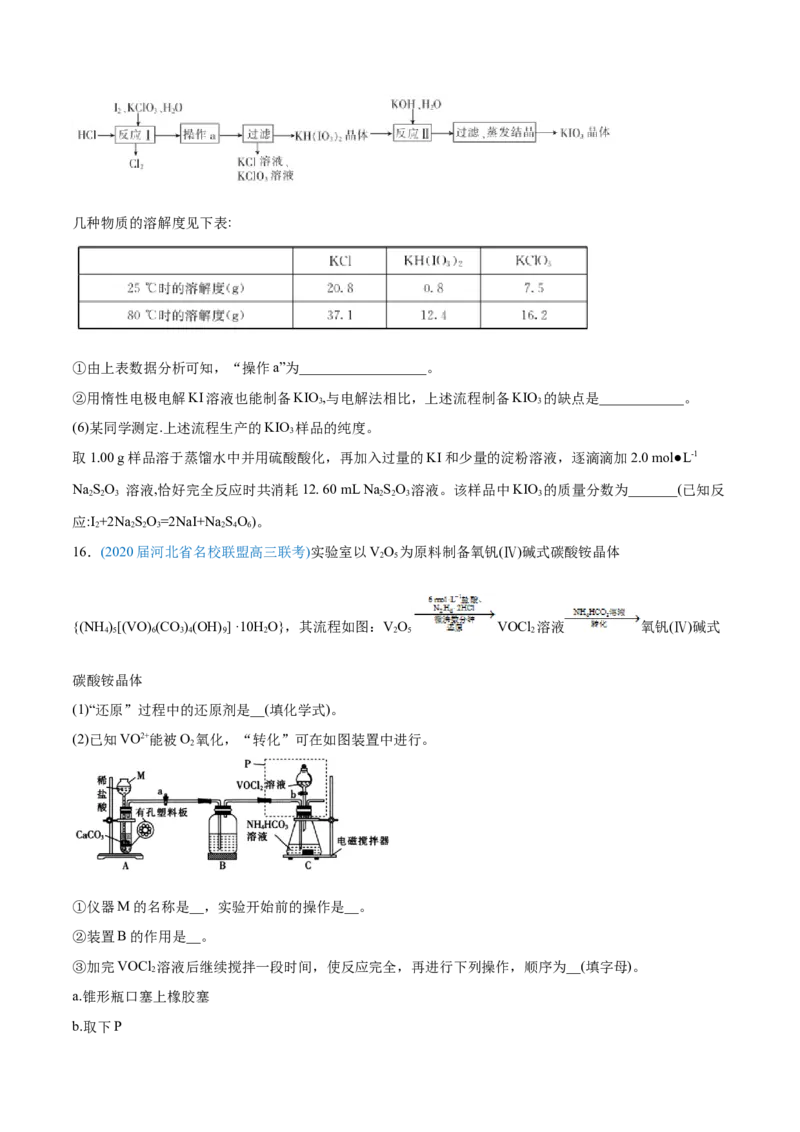
(2)已知VO2+能被O 氧化,“转化”可在如图装置中进行。
2
①仪器M的名称是__,实验开始前的操作是__。
②装置B的作用是__。
③加完VOCl 溶液后继续搅拌一段时间,使反应完全,再进行下列操作,顺序为__(填字母)。
2
a.锥形瓶口塞上橡胶塞
b.取下Pc.将锥形瓶置于干燥器中,静置过滤
④得到紫红色晶体,抽滤,并用饱和NH HCO 溶液洗涤3次,用无水乙醇洗涤2次,再用乙醚洗涤2次,
4 3
抽干称重。用饱和NH HCO 溶液洗涤除去的阴离子主要是__(填离子符号),用无水乙醇洗涤的目的是__。
4 3
⑤称量mg产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol·L-1KMnO 溶液至稍过量,
4
充分反应后继续滴加1%的NaNO 溶液至稍过量,再用尿素除去过量NaNO ,最后用
2 2
cmol·L-1(NH )Fe(SO ) 标准溶液滴定至终点(已知滴定反应为VO ++Fe2++2H+=VO2++Fe3++H O),消耗标准溶
4 2 4 2 2 2
液的体积为VmL。若(NH )Fe(SO ) 标准溶液部分变质,会使测定结果___(填“偏高”“偏低”或“无影
4 2 4 2
响”),产品中钒的质量分数为__(以VO2+的量进行计算,列出计算式)。
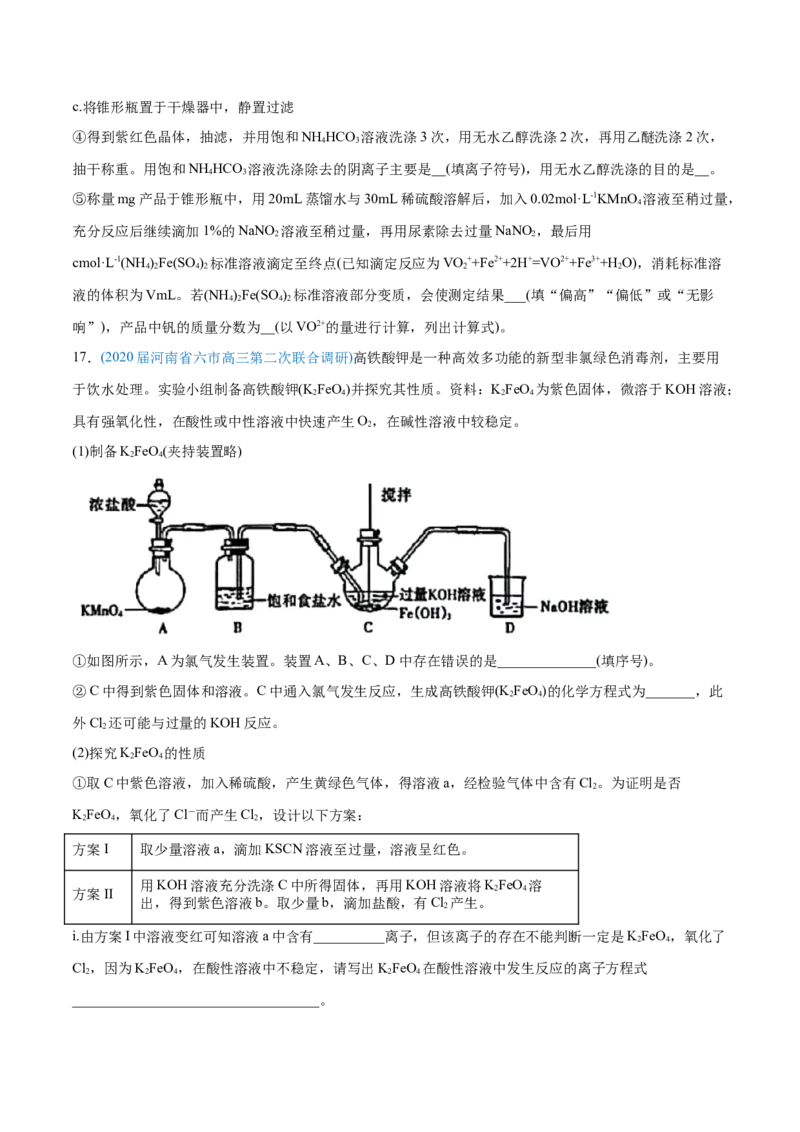
17.(2020届河南省六市高三第二次联合调研)高铁酸钾是一种高效多功能的新型非氯绿色消毒剂,主要用
于饮水处理。实验小组制备高铁酸钾(K FeO)并探究其性质。资料:KFeO 为紫色固体,微溶于KOH溶液;
2 4 2 4
具有强氧化性,在酸性或中性溶液中快速产生O,在碱性溶液中较稳定。
2
(1)制备KFeO(夹持装置略)
2 4
①如图所示,A为氯气发生装置。装置A、B、C、D中存在错误的是______________(填序号)。
②C中得到紫色固体和溶液。C中通入氯气发生反应,生成高铁酸钾(K FeO)的化学方程式为_______,此
2 4
外Cl 还可能与过量的KOH反应。
2
(2)探究KFeO 的性质
2 4
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl。为证明是否
2
KFeO,氧化了Cl-而产生Cl,设计以下方案:
2 4 2
方案I 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将KFeO 溶
方案II 2 4
出,得到紫色溶液b。取少量b,滴加盐酸,有Cl 产生。
2
i.由方案I中溶液变红可知溶液a中含有__________离子,但该离子的存在不能判断一定是KFeO,氧化了
2 4
Cl,因为KFeO,在酸性溶液中不稳定,请写出KFeO 在酸性溶液中发生反应的离子方程式
2 2 4 2 4
___________________________________。ii.方案Ⅱ可证明KFeO,氧化了Cl-.用KOH溶液洗涤的目的是_______________。
2 4
②根据KFeO 的制备实验得出:氧化性Cl_____FeO2- (填“>”或“<”),而方案Ⅱ实验表明,Cl 和
2 4 2 4 2
FeO2-的氧化性强弱关系恰好相反,原因是_______________。
4
(3)若在制备装置C中加入Fe(OH) 的质量为14.0g,充分反应后经过滤、洗涤、干燥得KFeO 固体19.3g,
3 2 4
则KFeO 的产率为______________。
2 4
18.(2020届福建省厦门市高三质检)次硫酸氢钠甲醛(aNaHSO •bHCHO•cH O)在印染、医药以及原子能工
2 2
业中应用广泛。以NaSO 、SO 、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
2 3 2
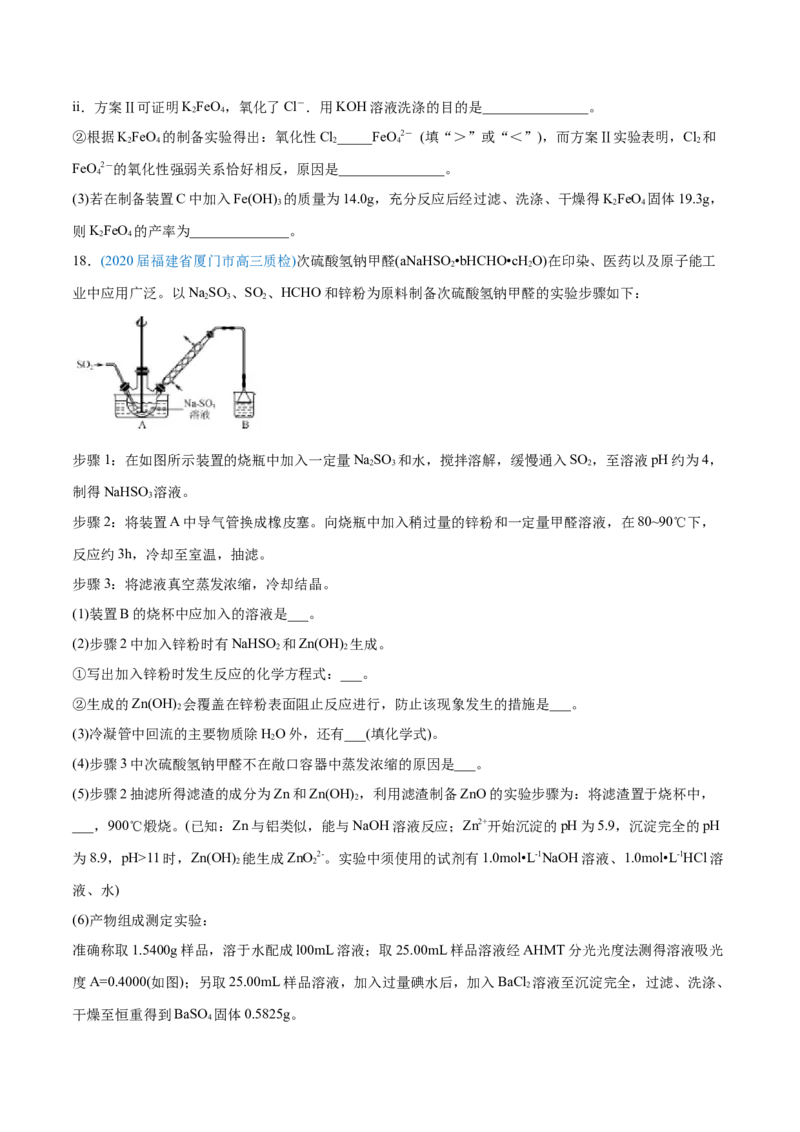
步骤1:在如图所示装置的烧瓶中加入一定量NaSO 和水,搅拌溶解,缓慢通入SO ,至溶液pH约为4,
2 3 2
制得NaHSO 溶液。
3
步骤2:将装置A中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,
反应约3h,冷却至室温,抽滤。
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B的烧杯中应加入的溶液是___。
(2)步骤2中加入锌粉时有NaHSO 和Zn(OH) 生成。
2 2
①写出加入锌粉时发生反应的化学方程式:___。
②生成的Zn(OH) 会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施是___。
2
(3)冷凝管中回流的主要物质除HO外,还有___(填化学式)。
2
(4)步骤3中次硫酸氢钠甲醛不在敞口容器中蒸发浓缩的原因是___。
(5)步骤2抽滤所得滤渣的成分为Zn和Zn(OH) ,利用滤渣制备ZnO的实验步骤为:将滤渣置于烧杯中,
2
___,900℃煅烧。(已知:Zn与铝类似,能与NaOH溶液反应;Zn2+开始沉淀的pH为5.9,沉淀完全的pH
为8.9,pH>11时,Zn(OH) 能生成ZnO2-。实验中须使用的试剂有1.0mol•L-1NaOH溶液、1.0mol•L-1HCl溶
2 2
液、水)
(6)产物组成测定实验:
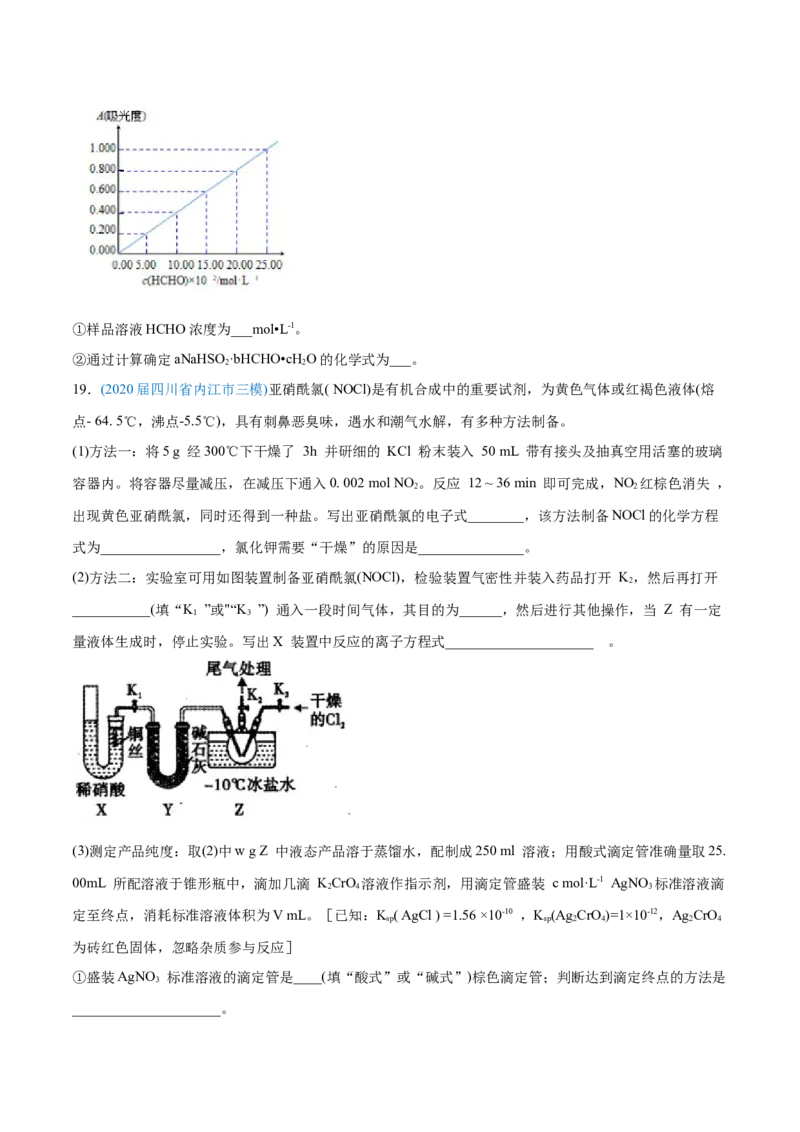
准确称取1.5400g样品,溶于水配成l00mL溶液;取25.00mL样品溶液经AHMT分光光度法测得溶液吸光
度A=0.4000(如图);另取25.00mL样品溶液,加入过量碘水后,加入BaCl 溶液至沉淀完全,过滤、洗涤、
2
干燥至恒重得到BaSO 固体0.5825g。
4①样品溶液HCHO浓度为___mol•L-1。
②通过计算确定aNaHSO ·bHCHO•cH O的化学式为___。
2 2
19.(2020届四川省内江市三模)亚硝酰氯( NOCl)是有机合成中的重要试剂,为黄色气体或红褐色液体(熔
点- 64. 5℃,沸点-5.5℃),具有刺鼻恶臭味,遇水和潮气水解,有多种方法制备。
(1)方法一:将5 g 经300℃下干燥了 3h 并研细的 KCl 粉末装入 50 mL 带有接头及抽真空用活塞的玻璃
容器内。将容器尽量减压,在减压下通入0. 002 mol NO 。反应 12 ~ 36 min 即可完成,NO 红棕色消失 ,
2 2
出现黄色亚硝酰氯,同时还得到一种盐。写出亚硝酰氯的电子式________,该方法制备NOCl的化学方程
式为_________________,氯化钾需要“干燥”的原因是_______________。
(2)方法二:实验室可用如图装置制备亚硝酰氯(NOCl),检验装置气密性并装入药品打开 K,然后再打开
2
___________(填“K ”或"“K ”) 通入一段时间气体,其目的为______,然后进行其他操作,当 Z 有一定
1 3
量液体生成时,停止实验。写出X 装置中反应的离子方程式_____________________ 。
(3)测定产品纯度:取(2)中w g Z 中液态产品溶于蒸馏水,配制成250 ml 溶液;用酸式滴定管准确量取25.
00mL 所配溶液于锥形瓶中,滴加几滴 KCrO 溶液作指示剂,用滴定管盛装 c mol·L-1 AgNO 标准溶液滴
2 4 3
定至终点,消耗标准溶液体积为V mL。[已知:K ( AgCl ) =1.56 ×10-10 ,K (Ag CrO)=1×10-12,Ag CrO
sp sp 2 4 2 4
为砖红色固体,忽略杂质参与反应]
①盛装AgNO 标准溶液的滴定管是____(填“酸式”或“碱式”)棕色滴定管;判断达到滴定终点的方法是
3
_____________________。②该产品纯度为_____________(用代数式表示)。
20.(2020届四川省成都市6月三诊)高铁酸钾(K FeO)是一种新型绿色、高效的水处理剂,对病毒的去除率
2 4
可达99.95%。已知KFeO 在低于常温的碱性环境中稳定,酸性条件下,其氧化性强于KMnO 、Cl 等。某
2 4 4 2
小组设计制备KFeO 并测定其纯度的实验步骤如下:
2 4
I.制备次氯酸钾。在搅拌和冰水浴条件下,将Cl 通入浓KOH溶液,同时补加一定量KOH,产生了大量白
2
色沉淀,抽滤后得到浓KClO滤液。
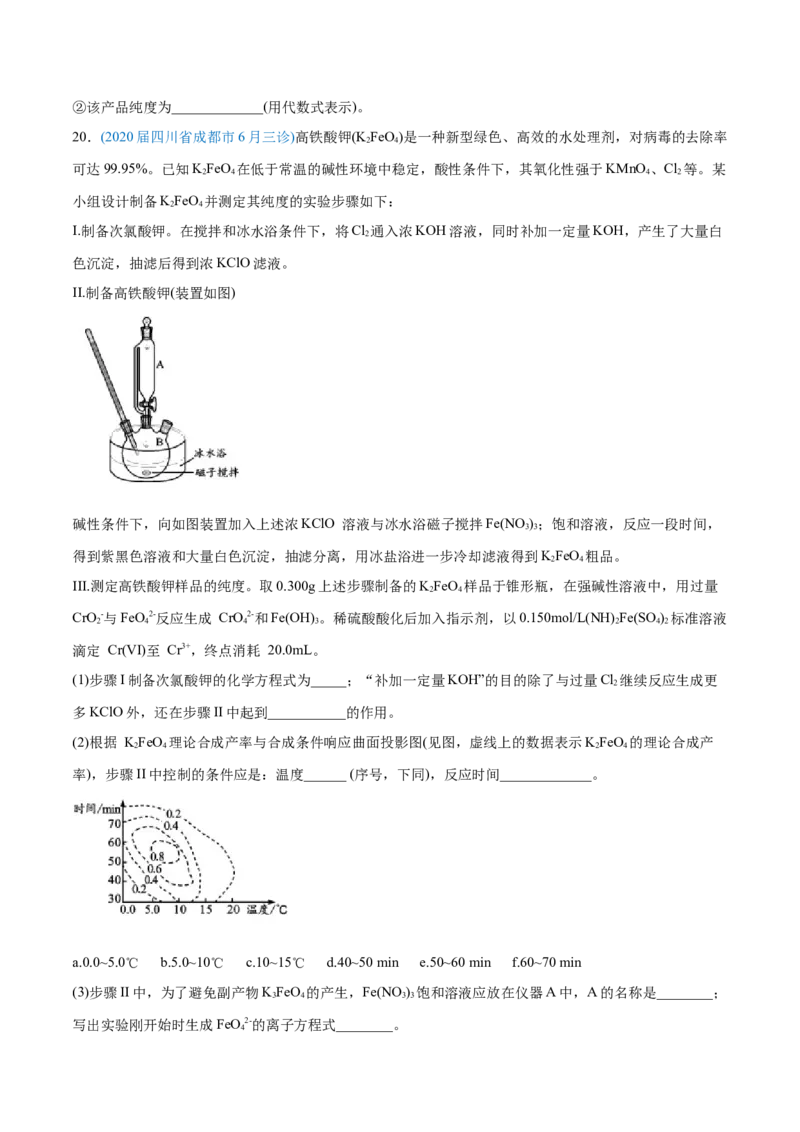
II.制备高铁酸钾(装置如图)
碱性条件下,向如图装置加入上述浓KClO 溶液与冰水浴磁子搅拌Fe(NO );饱和溶液,反应一段时间,
3 3
得到紫黑色溶液和大量白色沉淀,抽滤分离,用冰盐浴进一步冷却滤液得到KFeO 粗品。
2 4
III.测定高铁酸钾样品的纯度。取0.300g上述步骤制备的KFeO 样品于锥形瓶,在强碱性溶液中,用过量
2 4
CrO-与FeO2-反应生成 CrO2-和Fe(OH) 。稀硫酸酸化后加入指示剂,以0.150mol/L(NH)Fe(SO ) 标准溶液
2 4 4 3 2 4 2
滴定 Cr(VI)至 Cr3+,终点消耗 20.0mL。
(1)步骤I制备次氯酸钾的化学方程式为_____;“补加一定量KOH”的目的除了与过量Cl 继续反应生成更
2
多KClO外,还在步骤II中起到___________的作用。
(2)根据 KFeO 理论合成产率与合成条件响应曲面投影图(见图,虚线上的数据表示KFeO 的理论合成产
2 4 2 4
率),步骤II中控制的条件应是:温度______ (序号,下同),反应时间_____________。
a.0.0~5.0℃ b.5.0~10℃ c.10~15℃ d.40~50 min e.50~60 min f.60~70 min
(3)步骤II中,为了避免副产物KFeO 的产生,Fe(NO ) 饱和溶液应放在仪器A中,A的名称是________;
3 4 3 3
写出实验刚开始时生成FeO2-的离子方程式________。
4(4)根据步骤皿I的测定数据,计算高铁酸钾样品纯度为_____(保留3位有效数字)。
(5)为探究酸性条件下FeO2-氧化性强弱,甲同学取步骤II所得KFeO 粗品加入到少量盐酸中,观察到产生
4 2 4
黄绿色气体,经检验气体为Cl。该现象能否证明“酸性条件下FeO2-氧化性强于Cl”,并说明理由
2 4 2
_______________________________。
21.(2020届江西省九江市十校模考)实验室用酸性蚀刻废液(含 等)和碱性蚀刻废液
[NH +、Cu(NH )2+ 、NH ·H O等]制备CuI(白色固体)的实验流程如下:
4 3 4 3 2
(1)步骤Ⅰ中发生了多个反应,其中 与盐酸反应生成Cu(OH)Cl的离子方程式为____。
(2)步骤Ⅳ需控制pH为1~2,80 ℃下进行,合适的加热方式是____。
(3)步骤Ⅴ的具体步骤是蒸发浓缩、______、____。
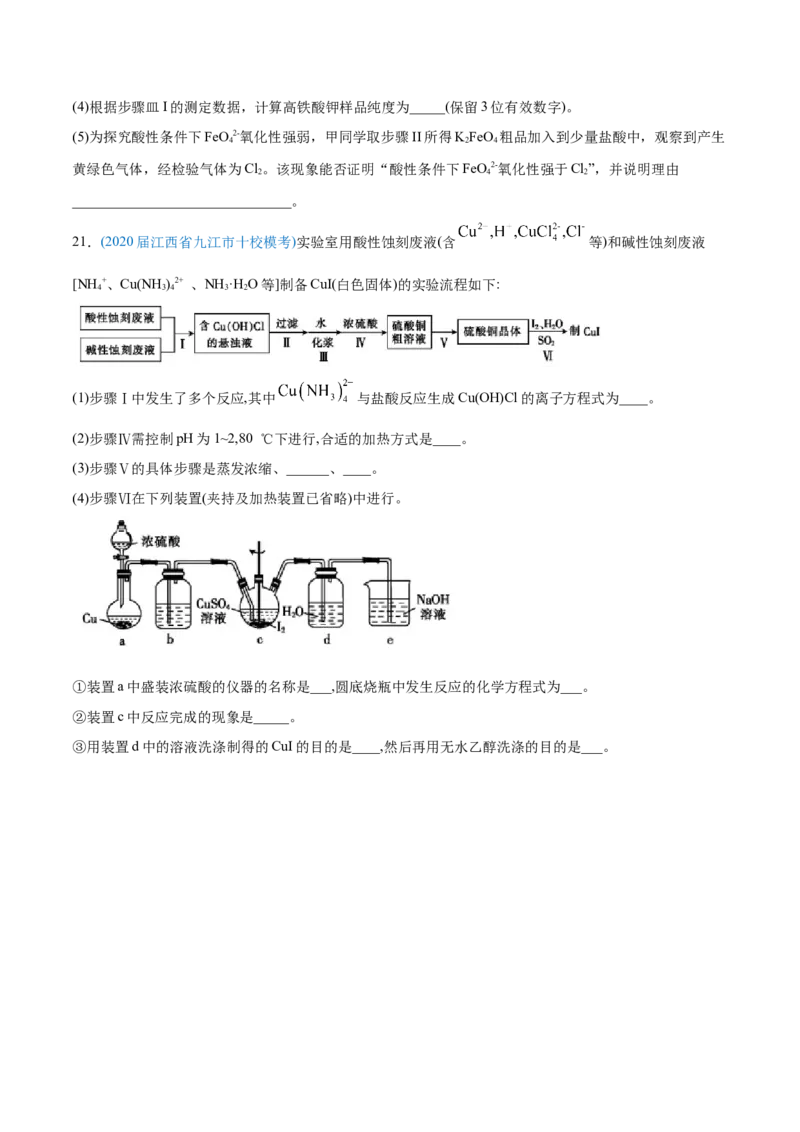
(4)步骤Ⅵ在下列装置(夹持及加热装置已省略)中进行。
①装置a中盛装浓硫酸的仪器的名称是___,圆底烧瓶中发生反应的化学方程式为___。
②装置c中反应完成的现象是_____。
③用装置d中的溶液洗涤制得的CuI的目的是____,然后再用无水乙醇洗涤的目的是___。