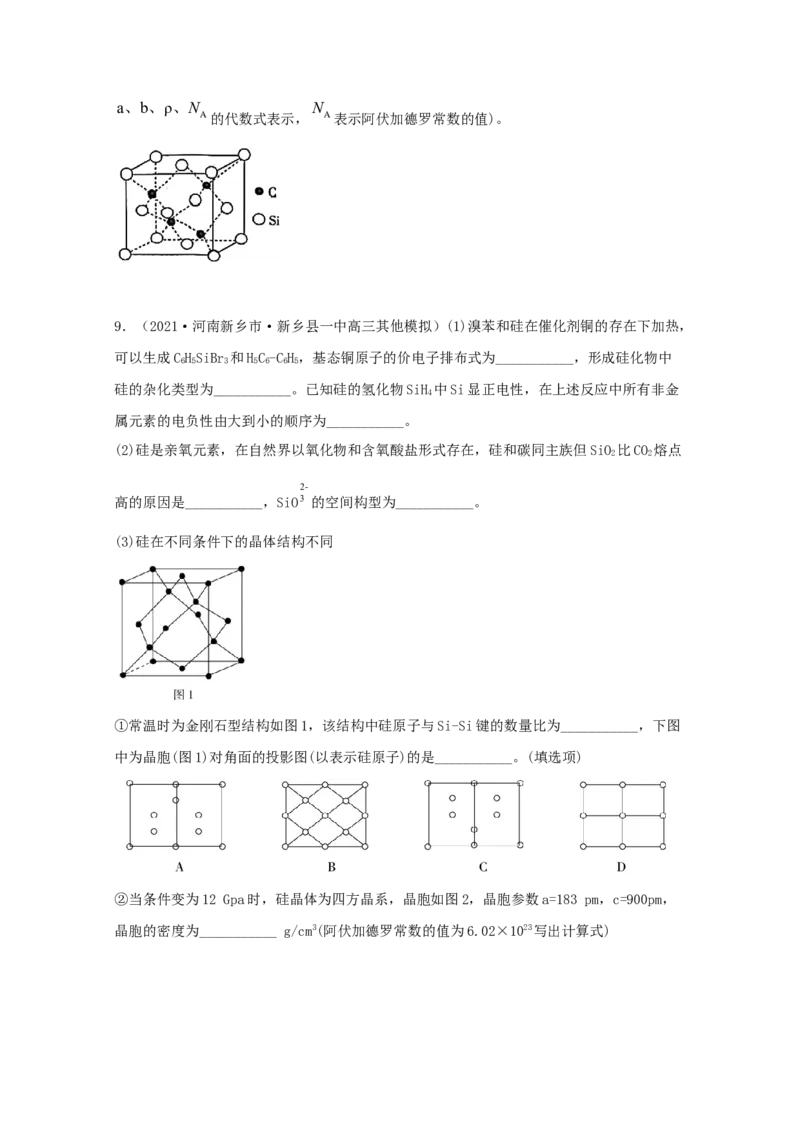
文档内容
专题 18 选修 3 物质结构与性质
2021年化学高考题
1.(2021·山东高考真题)非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有__种。
(2)O、F、Cl电负性由大到小的顺序为__;OF 分子的空间构型为__;OF 的熔、沸点__(填
2 2
“高于”或“低于”)ClO,原因是___。
2
(3)Xe是第五周期的稀有气体元素,与F形成的XeF 室温下易升华。XeF 中心原子的价层电
2 2
子对数为___,下列对XeF 中心原子杂化方式推断合理的是___(填标号)。
2
A.sp B.sp2 C.sp3 D.sp3d
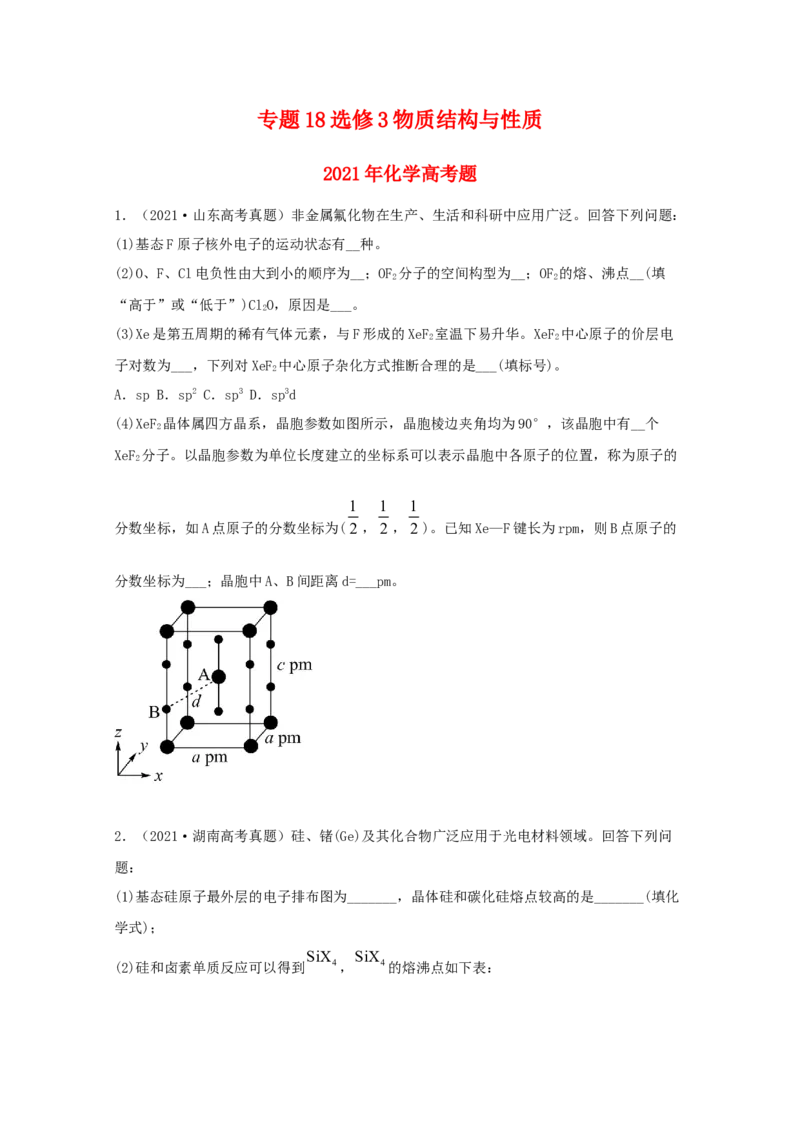
(4)XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有__个
2
XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的
2
1 1 1
分数坐标,如A点原子的分数坐标为(2 ,2 ,2 )。已知Xe—F键长为rpm,则B点原子的
分数坐标为___;晶胞中A、B间距离d=___pm。
2.(2021·湖南高考真题)硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问
题:
(1)基态硅原子最外层的电子排布图为_______,晶体硅和碳化硅熔点较高的是_______(填化
学式);
SiX SiX
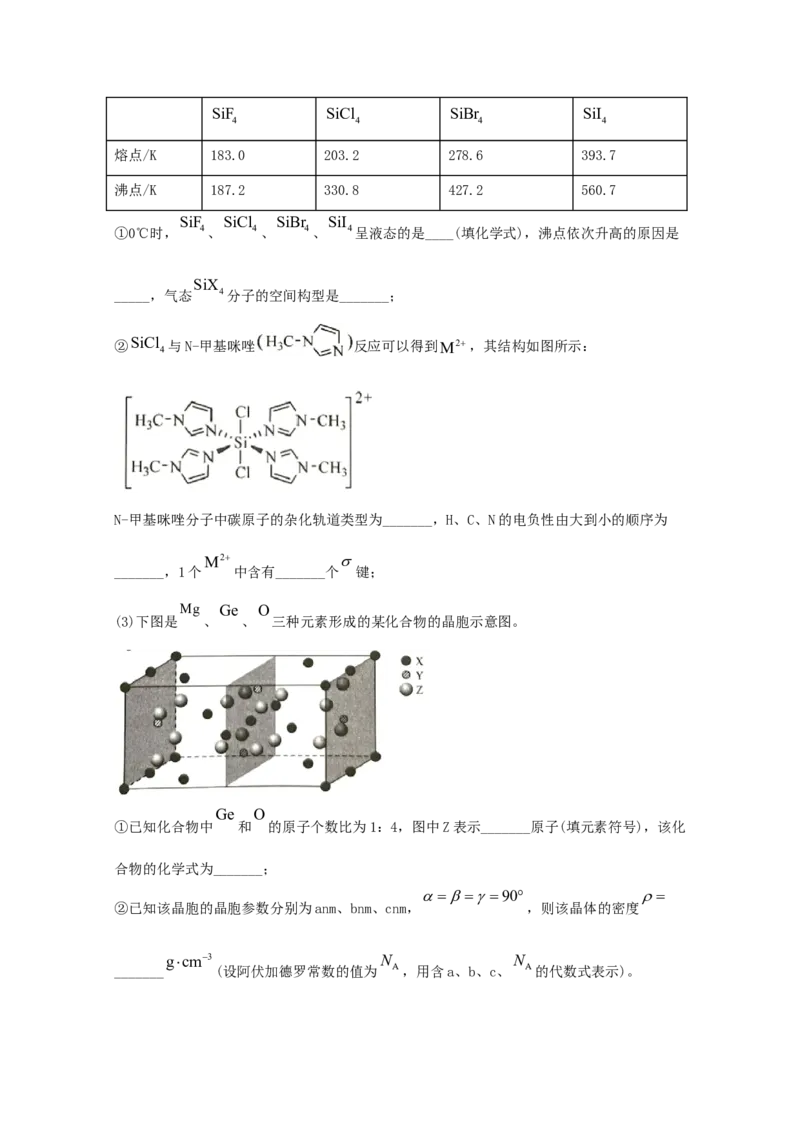
(2)硅和卤素单质反应可以得到 4, 4的熔沸点如下表:SiF SiCl SiBr SiI
4 4 4 4
熔点/K 183.0 203.2 278.6 393.7
沸点/K 187.2 330.8 427.2 560.7
SiF SiCl SiBr SiI
①0℃时, 4、 4、 4、 4呈液态的是____(填化学式),沸点依次升高的原因是
SiX
_____,气态 4分子的空间构型是_______;
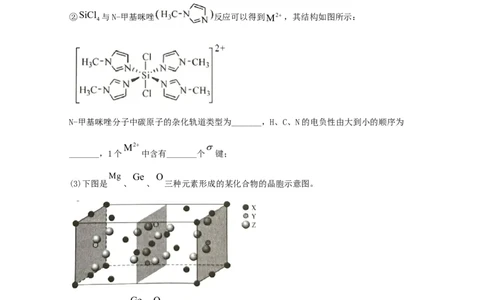
②SiCl 与N-甲基咪唑 反应可以得到M2,其结构如图所示:
4
N-甲基咪唑分子中碳原子的杂化轨道类型为_______,H、C、N的电负性由大到小的顺序为
M2
_______,1个 中含有_______个 键;
Mg Ge O
(3)下图是 、 、 三种元素形成的某化合物的晶胞示意图。
Ge O
①已知化合物中 和 的原子个数比为1:4,图中Z表示_______原子(填元素符号),该化
合物的化学式为_______;
90
②已知该晶胞的晶胞参数分别为anm、bnm、cnm, ,则该晶体的密度
gcm3 N N
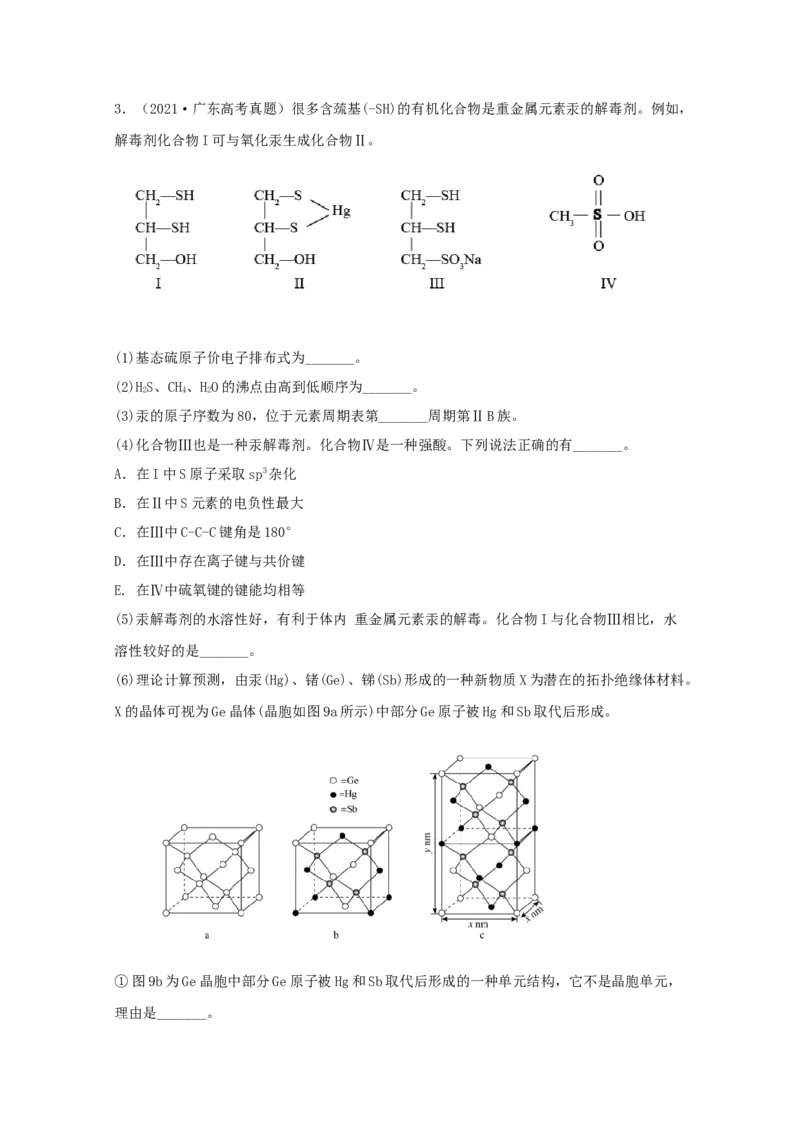
_______ (设阿伏加德罗常数的值为 A,用含a、b、c、 A的代数式表示)。3.(2021·广东高考真题)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,
解毒剂化合物I可与氧化汞生成化合物Ⅱ。
(1)基态硫原子价电子排布式为_______。
(2)HS、CH、HO的沸点由高到低顺序为_______。
2 4 2
(3)汞的原子序数为80,位于元素周期表第_______周期第ⅡB族。
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______。
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等
(5)汞解毒剂的水溶性好,有利于体内 重金属元素汞的解毒。化合物I与化合物Ⅲ相比,水
溶性较好的是_______。
(6)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。
X的晶体可视为Ge晶体(晶胞如图9a所示)中部分Ge原子被Hg和Sb取代后形成。
①图9b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,
理由是_______。②图9c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_______;该晶胞中粒子个数比
Hg:Ge:Sb = _______。
③设X的最简式的式量为M,则X晶体的密度为_______g/cm3(列出算式)。
r
4.(2021·全国高考真题)我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象
地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二
氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排式为________;单
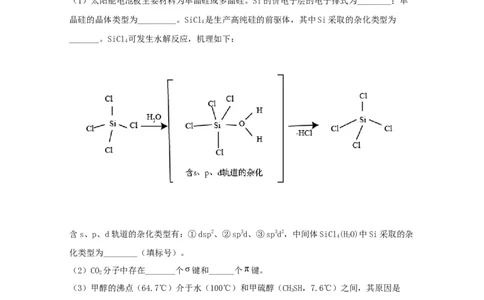
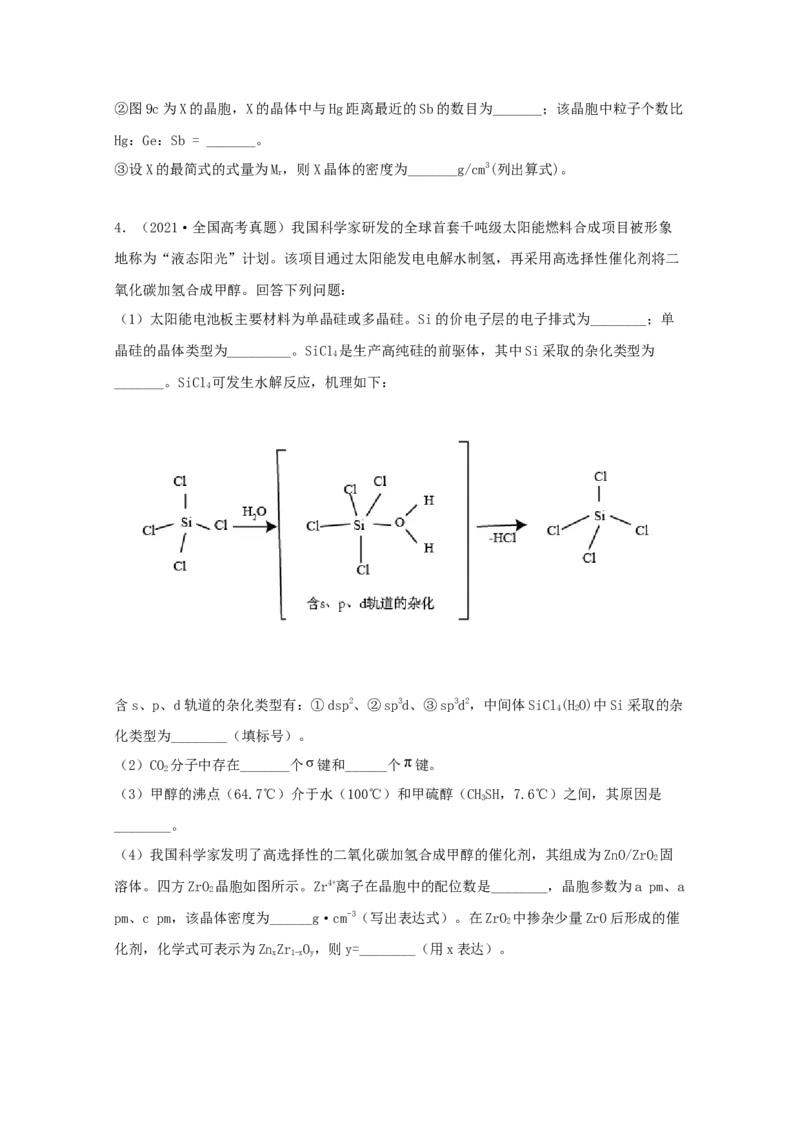
晶硅的晶体类型为_________。SiCl 是生产高纯硅的前驱体,其中Si采取的杂化类型为
4
_______。SiCl 可发生水解反应,机理如下:
4
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl(HO)中Si采取的杂
4 2
化类型为________(填标号)。
(2)CO 分子中存在_______个σ键和______个 π 键。
2
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CHSH,7.6℃)之间,其原因是
3
________。
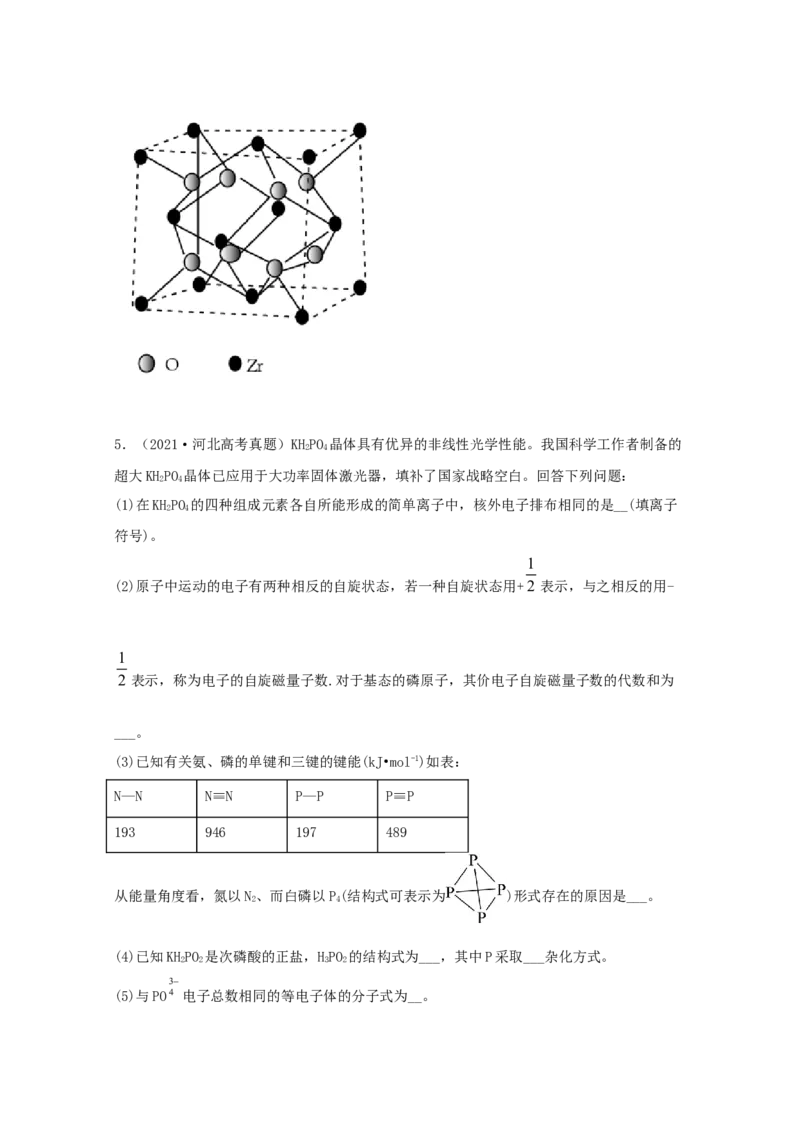
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO 固
2
溶体。四方ZrO 晶胞如图所示。Zr4+离子在晶胞中的配位数是________,晶胞参数为a pm、a
2
pm、c pm,该晶体密度为______g·cm-3(写出表达式)。在ZrO 中掺杂少量ZrO后形成的催
2
化剂,化学式可表示为ZnZr O,则y=________(用x表达)。
x 1-x y5.(2021·河北高考真题)KHPO 晶体具有优异的非线性光学性能。我国科学工作者制备的
2 4
超大KHPO 晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
2 4
(1)在KHPO 的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是__(填离子
2 4
符号)。
1
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+2 表示,与之相反的用-
1
2 表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为
___。
(3)已知有关氨、磷的单键和三键的键能(kJ•mol-1)如表:
N—N N≡N P—P P≡P
193 946 197 489
从能量角度看,氮以N、而白磷以P(结构式可表示为 )形式存在的原因是___。
2 4
(4)已知KHPO 是次磷酸的正盐,HPO 的结构式为___,其中P采取___杂化方式。
2 2 3 2
3
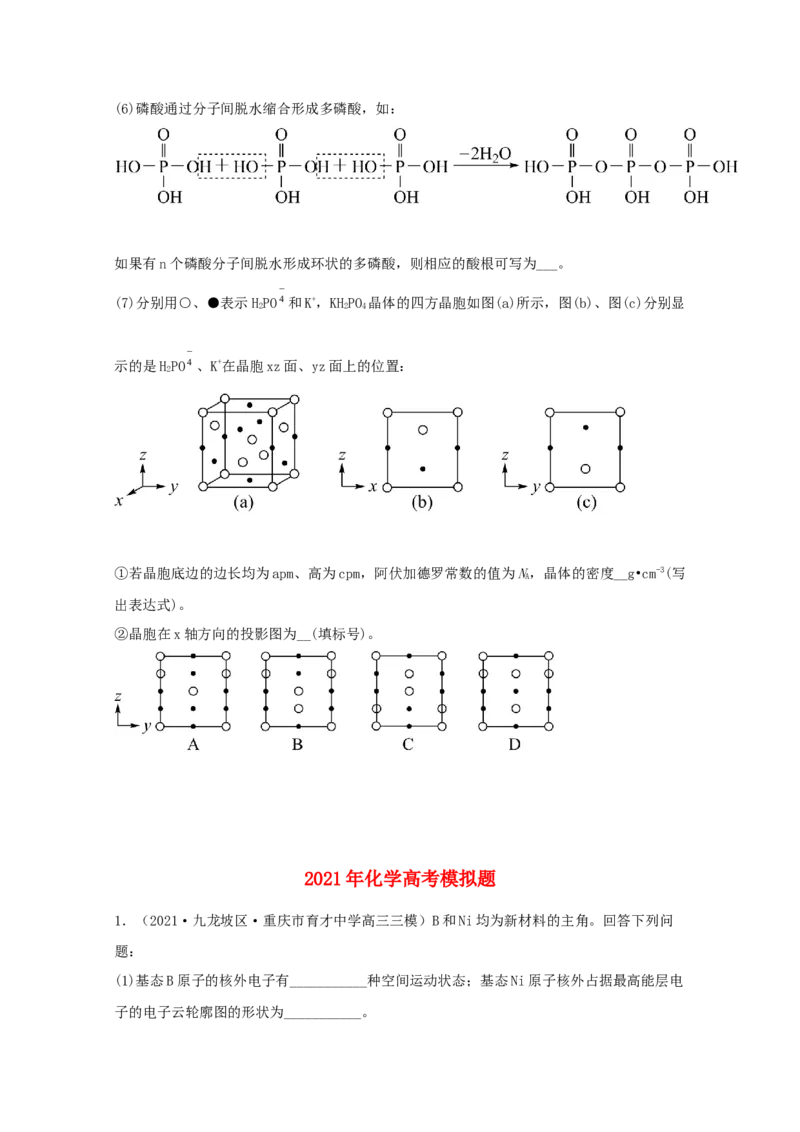
(5)与PO4 电子总数相同的等电子体的分子式为__。(6)磷酸通过分子间脱水缩合形成多磷酸,如:
如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为___。
(7)分别用○、●表示HPO4和K+,KHPO 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显
2 2 4
示的是HPO4、K+在晶胞xz面、yz面上的位置:
2
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为N,晶体的密度__g•cm-3(写
A
出表达式)。
②晶胞在x轴方向的投影图为__(填标号)。
2021年化学高考模拟题
1.(2021·九龙坡区·重庆市育才中学高三三模)B和Ni均为新材料的主角。回答下列问
题:
(1)基态B原子的核外电子有___________种空间运动状态;基态Ni原子核外占据最高能层电
子的电子云轮廓图的形状为___________。(2)硼的卤化物的沸点如表所示:
BBr
卤化物 BF BCl
3 3
3
沸
-100.3 12.5 90
点/℃
解释表中卤化物之间沸点差异的原因___________。
(3)镍及其化合物常用作有机合成的催化剂,如Ni(PPh),其中Ph表示苯基,PPh 表示分子,
3 2 3
PPh 的空间构型为___________;Ni(PPh) 晶体中存在的化学键类型有___________(填字母)。
3 3 2
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
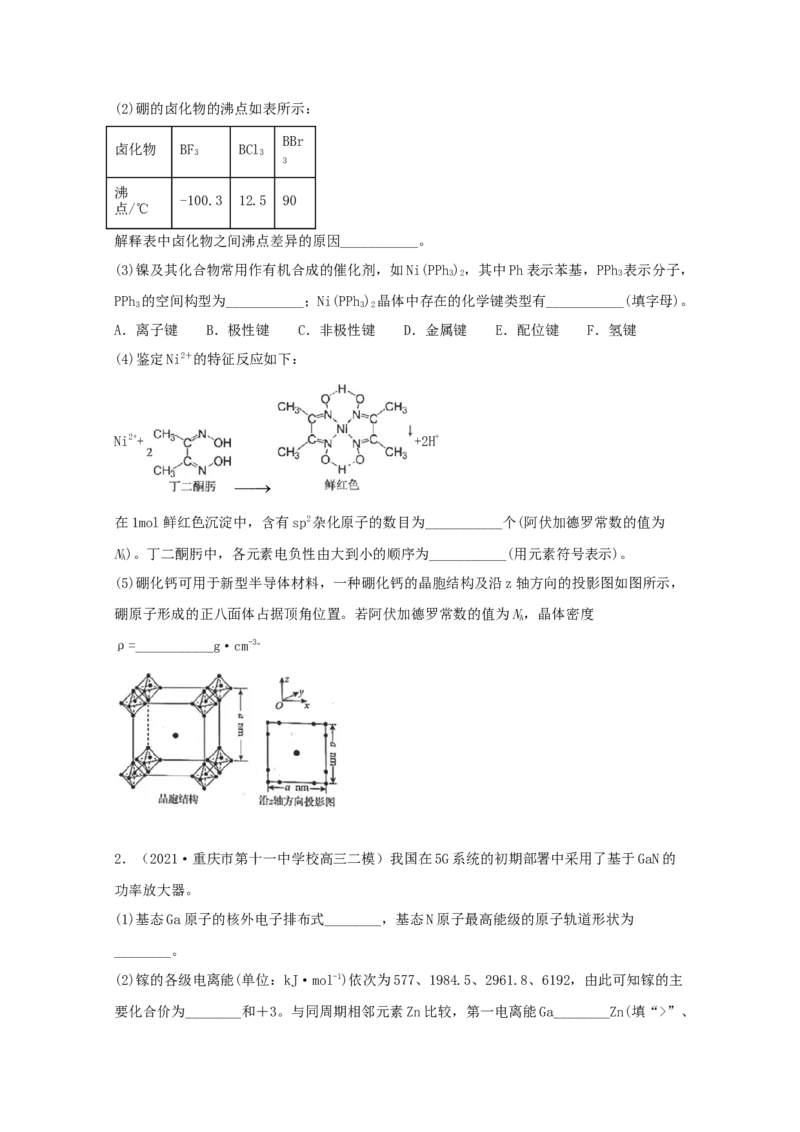
(4)鉴定Ni2+的特征反应如下:
Ni2++ +2H+
在1mol鲜红色沉淀中,含有sp2杂化原子的数目为___________个(阿伏加德罗常数的值为
N)。丁二酮肟中,各元素电负性由大到小的顺序为___________(用元素符号表示)。
A
(5)硼化钙可用于新型半导体材料,一种硼化钙的晶胞结构及沿z轴方向的投影图如图所示,
硼原子形成的正八面体占据顶角位置。若阿伏加德罗常数的值为N,晶体密度
A
ρ=___________g·cm-3。
2.(2021·重庆市第十一中学校高三二模)我国在5G系统的初期部署中采用了基于GaN的
功率放大器。
(1)基态Ga原子的核外电子排布式________,基态N原子最高能级的原子轨道形状为
________。
(2)镓的各级电离能(单位:kJ·mol-1)依次为577、1984.5、2961.8、6192,由此可知镓的主
要化合价为________和+3。与同周期相邻元素Zn比较,第一电离能Ga________Zn(填“>”、“<”或“=”),理由是________。
(3)已知氮化硼、氮化铝、氮化镓的熔点如下表。从结构的角度分析它们熔点不同的原因是
________。
物质 BN AlN GaN
熔点/℃ 3000 2249 1700
(4)GaN可由非极性分子三甲基镓(CH)Ga和NH 发生系列反应制得。GaN晶胞结构如图1所示,
3 3 3
(CH)Ga和GaN中Ga原子的杂化方式分别为________、________。
3 3
(5)图1的六棱柱底边边长为a cm,阿伏加德罗常数的值为N。晶胞中每个Ga原子周围最近
A
的Ga原子数目为________。从GaN晶体中“分割”出的平行六面体如图2,若该平行六面体
2a3 cm3
的体积为 ,则GaN晶体的密度为________g·cm-3(用含a、N 的代数式表示)。
A
3.(2021·青海西宁市·高三二模)磷及其化合物在工农业生产中都有重要作用。
(1)磷原子核外电子排布式为_______。
(2)羟基磷灰石[Ca(PO)OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为
5 4 3
PO3-
_______, 4 的空间构型为_______,该化合物中所含元素电负性最大的是_______。
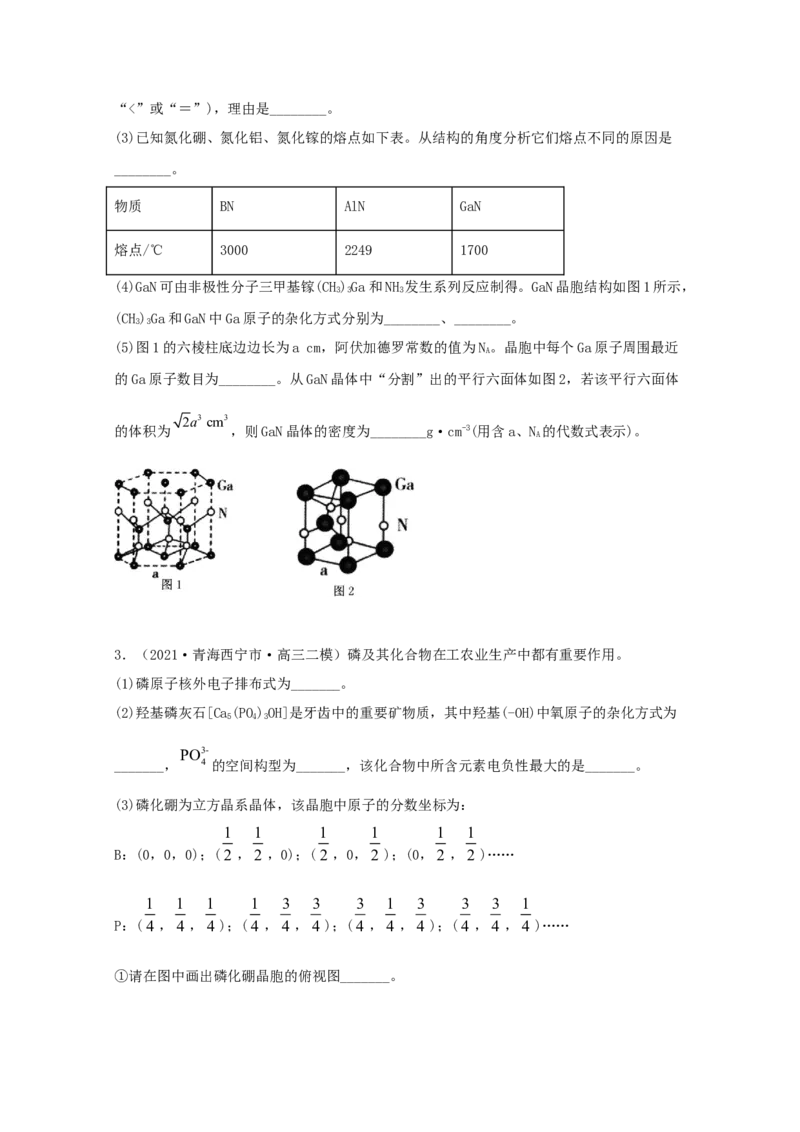
(3)磷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
1 1 1 1 1 1
B:(0,0,0);(2 ,2 ,0);(2 ,0,2 );(0,2 ,2 )……
1 1 1 1 3 3 3 1 3 3 3 1
P:(4 ,4 ,4 );(4 ,4 ,4 );(4 ,4 ,4 );(4 ,4 ,4 )……
①请在图中画出磷化硼晶胞的俯视图_______。②与每个磷原子紧邻的硼原子有_______个,与每个硼原子紧邻的硼原子有_______个。
(4)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如图所示。该磷钇矿的化学式为_______,
PO3-
与 4 互为等电子体的阴离子有_______(写出一种离子符号)。已知晶胞参数a=0.69nm,
c=0.60nm,阿伏加德罗常数的值为N,则该磷钇矿的密度为_______g·cm-3(列出计算式)。
A
4.(2021·青海高三三模)第四周期过渡元素单质及其化合物在生活、生产中有广泛应用。
回答下列问题:
(1)Co3+的一种配离子[Co(N)(NH)]2+中,Co3+的配位数是___________,配位体NH 的空间
3 3 5 3
构型为___________。
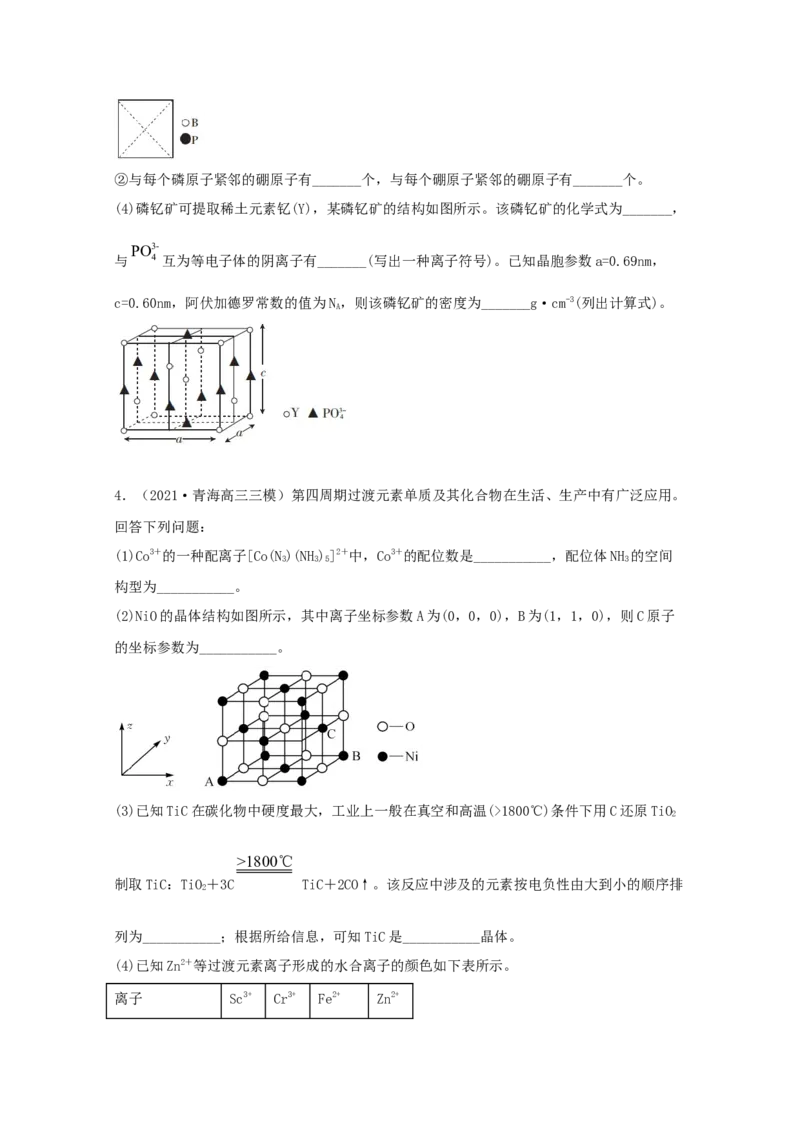
(2)NiO的晶体结构如图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C原子
的坐标参数为___________。
(3)已知TiC在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原TiO
2
>1800℃
制取TiC:TiO+3C TiC+2CO↑。该反应中涉及的元素按电负性由大到小的顺序排
2
列为___________;根据所给信息,可知TiC是___________晶体。
(4)已知Zn2+等过渡元素离子形成的水合离子的颜色如下表所示。
离子 Sc3+ Cr3+ Fe2+ Zn2+无
水合离子的颜色 绿色 浅绿色 无色
色
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因:___________。
(5)VO 是一种常见的催化剂,在合成硫酸、硝酸中起到非常重要的作用。五氧化二钒的结构
2 5
式为( ),则该结构中σ键与π键个数之比为___________。VO 溶解在NaOH
2 5
3- 3-
溶液中,可得到钒酸钠(NaVO)。VO4 与PO4 的空间构型相同,其中V原子的杂化方式为
3 4
___________。
CuFeS
5.(2021·全国高三零模)黄铜矿(主要成分为 2)是一种天然矿石。中国在商代或更
早就掌握了由它冶炼铜的技术。医药上,黄铜矿有促进骨折愈合的作用。请回答下列问题:
Cu Cu2
(1)基态 比 稳定的原因是______。
H SO
SO2
(2) 2 3中的阴离子的空间构型为______,与 4 互为等电子体的离子是______(写出一
种化学式即可)。
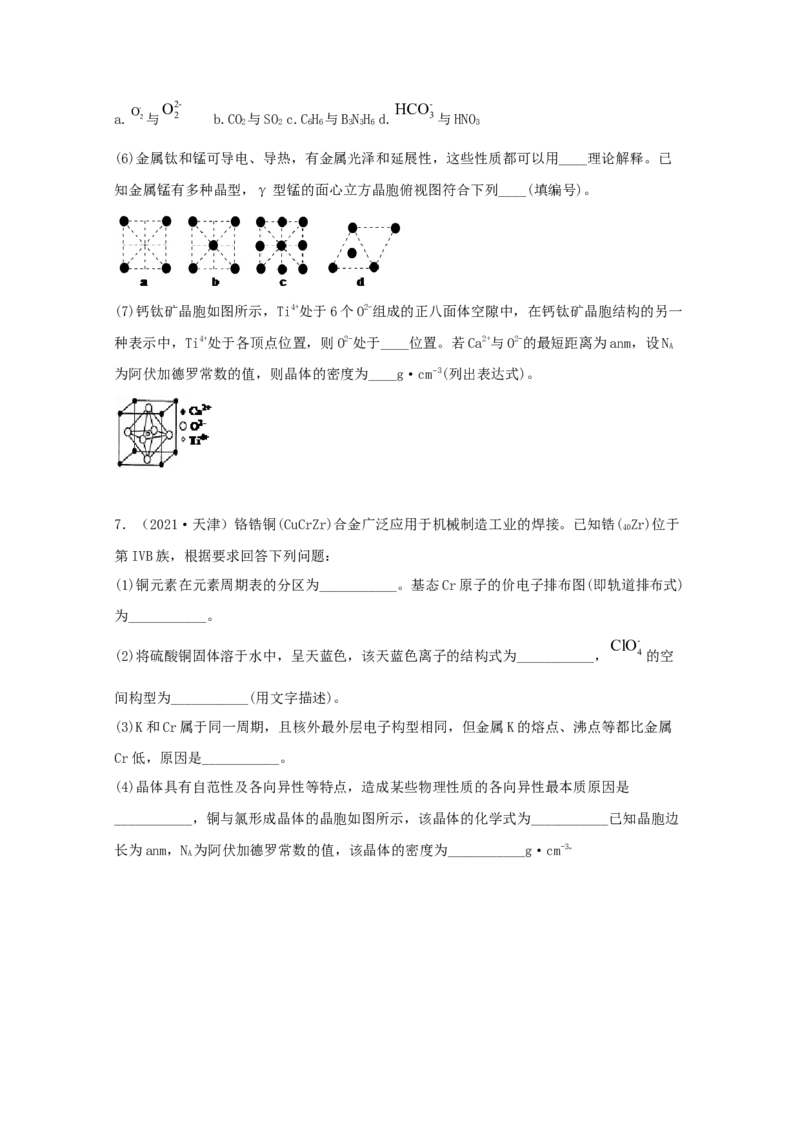
(3)图为某阳离子的结构,加热时该离子先失去的配位体是______(填化学式),原因是
______。
CuFeS
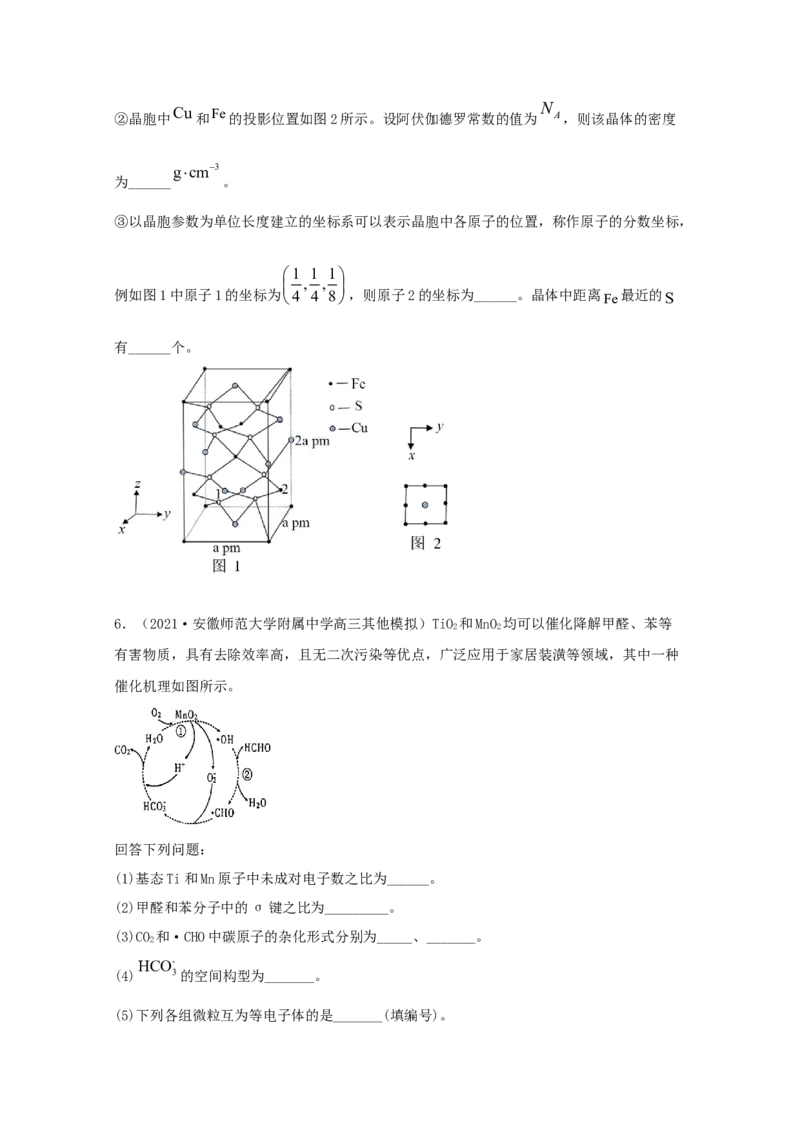
(4)四方晶系的 2晶胞结构如图1所示。
CuFeS S
① 2中各元素电负性数值从小到大的顺序为______,晶胞中 原子的杂化方式为
______。N
②晶胞中 Cu 和 Fe 的投影位置如图2所示。设阿伏伽德罗常数的值为 A,则该晶体的密度
gcm3
为______ 。
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,
1 1 1
, ,
例如图1中原子1的坐标为4 4 8,则原子2的坐标为______。晶体中距离 Fe 最近的S
有______个。
6.(2021·安徽师范大学附属中学高三其他模拟)TiO 和MnO 均可以催化降解甲醛、苯等
2 2
有害物质,具有去除效率高,且无二次污染等优点,广泛应用于家居装潢等领域,其中一种
催化机理如图所示。
回答下列问题:
(1)基态Ti和Mn原子中未成对电子数之比为______。
(2)甲醛和苯分子中的σ键之比为_________。
(3)CO 和·CHO中碳原子的杂化形式分别为_____、_______。
2
HCO-
(4) 3的空间构型为_______。
(5)下列各组微粒互为等电子体的是_______(填编号)。O-
O2- HCO-
a. 2与 2 b.CO 与SO c.CH 与BNH d. 3与HNO
2 2 6 6 3 3 6 3
(6)金属钛和锰可导电、导热,有金属光泽和延展性,这些性质都可以用____理论解释。已
知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列____(填编号)。
(7)钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的正八面体空隙中,在钙钛矿晶胞结构的另一
种表示中,Ti4+处于各顶点位置,则O2-处于____位置。若Ca2+与O2-的最短距离为anm,设N
A
为阿伏加德罗常数的值,则晶体的密度为____g·cm−3(列出表达式)。
7.(2021·天津)铬锆铜(CuCrZr)合金广泛应用于机械制造工业的焊接。已知锆( Zr)位于
40
第IVB族,根据要求回答下列问题:
(1)铜元素在元素周期表的分区为___________。基态Cr原子的价电子排布图(即轨道排布式)
为___________。
ClO-
(2)将硫酸铜固体溶于水中,呈天蓝色,该天蓝色离子的结构式为___________, 4的空
间构型为___________(用文字描述)。
(3)K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属
Cr低,原因是___________。
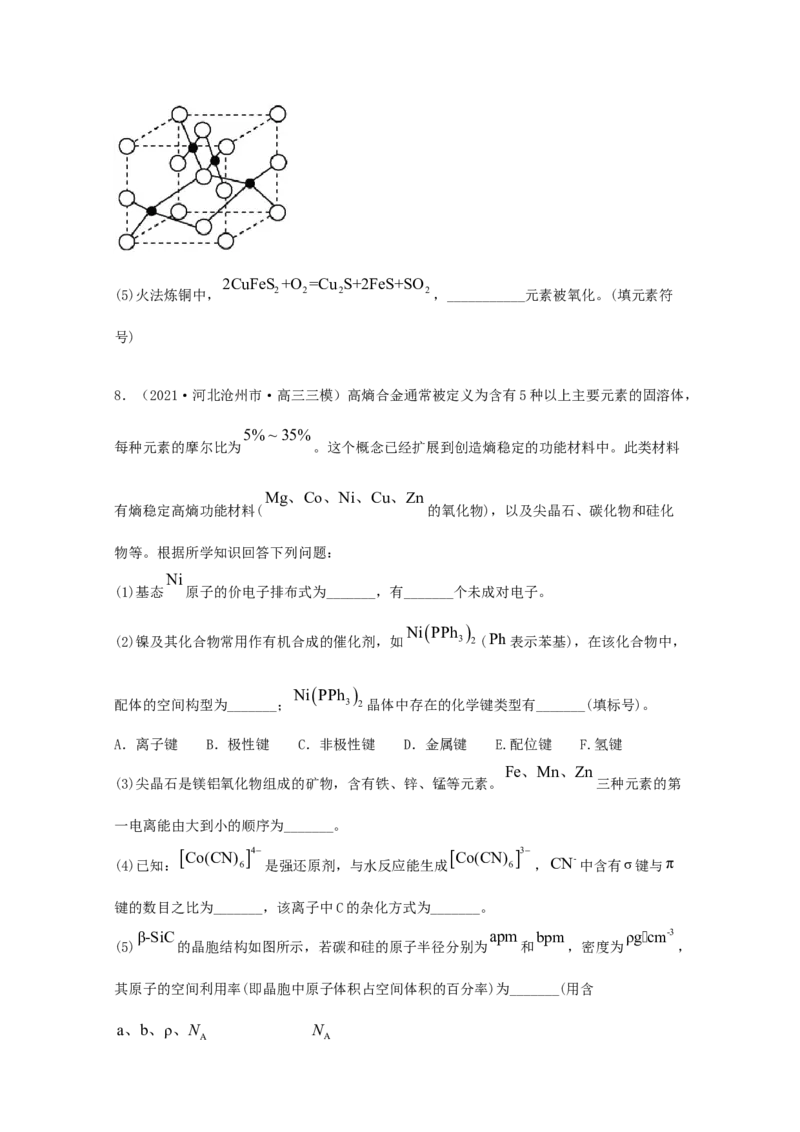
(4)晶体具有自范性及各向异性等特点,造成某些物理性质的各向异性最本质原因是
___________,铜与氯形成晶体的晶胞如图所示,该晶体的化学式为___________已知晶胞边
长为anm,N 为阿伏加德罗常数的值,该晶体的密度为___________g·cm-3。
A2CuFeS +O =Cu S+2FeS+SO
(5)火法炼铜中, 2 2 2 2,___________元素被氧化。(填元素符
号)
8.(2021·河北沧州市·高三三模)高熵合金通常被定义为含有5种以上主要元素的固溶体,
5%~35%
每种元素的摩尔比为 。这个概念已经扩展到创造熵稳定的功能材料中。此类材料
Mg、Co、Ni、Cu、Zn
有熵稳定高熵功能材料( 的氧化物),以及尖晶石、碳化物和硅化
物等。根据所学知识回答下列问题:
Ni
(1)基态 原子的价电子排布式为_______,有_______个未成对电子。
NiPPh
(2)镍及其化合物常用作有机合成的催化剂,如 3 2(Ph表示苯基),在该化合物中,
NiPPh
配体的空间构型为_______; 3 2晶体中存在的化学键类型有_______(填标号)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
Fe、Mn、Zn
(3)尖晶石是镁铝氧化物组成的矿物,含有铁、锌、锰等元素。 三种元素的第
一电离能由大到小的顺序为_______。
(4)已知:
Co(CN)
6
4
是强还原剂,与水反应能生成
Co(CN)
6
3
,CN-中含有σ键与π
键的数目之比为_______,该离子中C的杂化方式为_______。
β-SiC apm bpm ρgcm-3
(5) 的晶胞结构如图所示,若碳和硅的原子半径分别为 和 ,密度为 ,
其原子的空间利用率(即晶胞中原子体积占空间体积的百分率)为_______(用含
a、b、ρ、N N
A Aa、b、ρ、N N
A的代数式表示, A表示阿伏加德罗常数的值)。
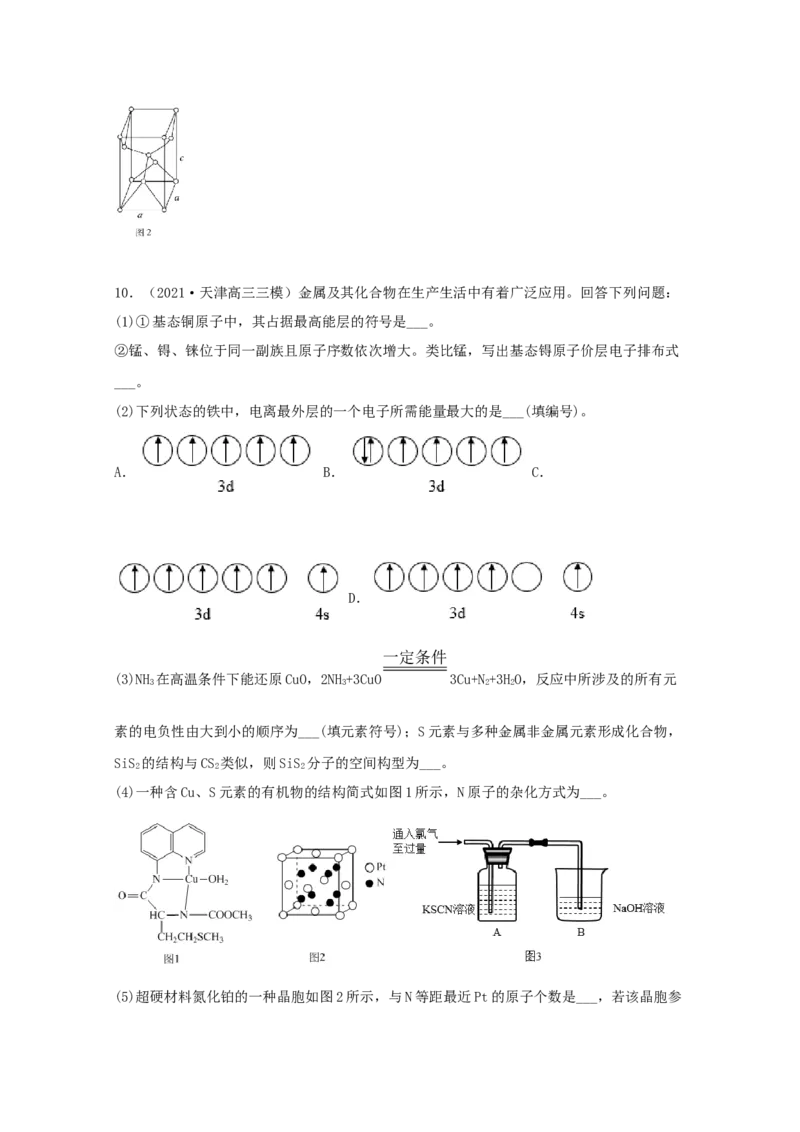
9.(2021·河南新乡市·新乡县一中高三其他模拟)(1)溴苯和硅在催化剂铜的存在下加热,
可以生成CHSiBr 和HC-CH,基态铜原子的价电子排布式为___________,形成硅化物中
6 5 3 5 6 6 5
硅的杂化类型为___________。已知硅的氢化物SiH 中Si显正电性,在上述反应中所有非金
4
属元素的电负性由大到小的顺序为___________。
(2)硅是亲氧元素,在自然界以氧化物和含氧酸盐形式存在,硅和碳同主族但SiO 比CO 熔点
2 2
2-
高的原因是___________,SiO3 的空间构型为___________。
(3)硅在不同条件下的晶体结构不同
①常温时为金刚石型结构如图1,该结构中硅原子与Si-Si键的数量比为___________,下图
中为晶胞(图1)对角面的投影图(以表示硅原子)的是___________。(填选项)
②当条件变为12 Gpa时,硅晶体为四方晶系,晶胞如图2,晶胞参数a=183 pm,c=900pm,
晶胞的密度为___________ g/cm3(阿伏加德罗常数的值为6.02×1023写出计算式)10.(2021·天津高三三模)金属及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)①基态铜原子中,其占据最高能层的符号是___。
②锰、锝、铼位于同一副族且原子序数依次增大。类比锰,写出基态锝原子价层电子排布式
___。
(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是___(填编号)。
A. B. C.
D.
一定条件
(3)NH 在高温条件下能还原CuO,2NH+3CuO 3Cu+N+3HO,反应中所涉及的所有元
3 3 2 2
素的电负性由大到小的顺序为___(填元素符号);S元素与多种金属非金属元素形成化合物,
SiS 的结构与CS 类似,则SiS 分子的空间构型为___。
2 2 2
(4)一种含Cu、S元素的有机物的结构简式如图1所示,N原子的杂化方式为___。
(5)超硬材料氮化铂的一种晶胞如图2所示,与N等距最近Pt的原子个数是___,若该晶胞参数为apm,密度为ρg·cm-3,则阿伏加德罗常数(N)为___mol-1(用含a、ρ的式子表示,并
A
化成最简)
(6)Cl 可氧化KSCN溶液。查阅资料可知SCN-中氮元素转化为NO3 。如图3所示,取A中溶液
2
于试管中,加入用HCl酸化的BaCl 溶液,产生白色沉淀。写出SCN-与Cl 反应的离子方程式
2 2
为___。
11.(2021·天津高三一模)乙炔是有机合成工业的一种重要原料。工业上曾用焦碳制备电
石(CaC),再与水反应制备乙炔。
2
(1)焦炭、金刚石和C 都是碳的单质。已知金刚石中碳碳键的键长为154.45pm,C 中碳碳键
60 60
的健长为140~145pm,二者比较熔点高的是___,理由是___。
(2)乙炔与氢氰酸反应可得丙烯腈(HC=CH—C≡N)。丙烯腈分子中碳原子轨道杂化类型是___,
2
该分子中σ键与π键个数比为___。
(3)将乙炔通入[Cu(NH)]Cl溶液生成CuC 红棕色沉淀。Cu+基态核外电子排布式为___。
3 2 2 2
[Cu(NH)]Cl的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:
3 2
___。
(4)CaC 的电子式为____。乙炔中混有的HS气体可用CuSO 溶液吸收,反应方程式为___。
2 2 4
C2
(5)CaC 晶体的晶胞结构与NiCl晶体相似,但CaC 晶体中哑铃形 2 的存在,使晶胞沿一个
2 2
2
方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距高相等且最近的C2 有___个。已知CaC 晶
2
2
体密度为ρg·cm-3,晶胞中两个C2 的最近距离为acm,阿伏加德罗常数值为N。则CaC 晶
A 2
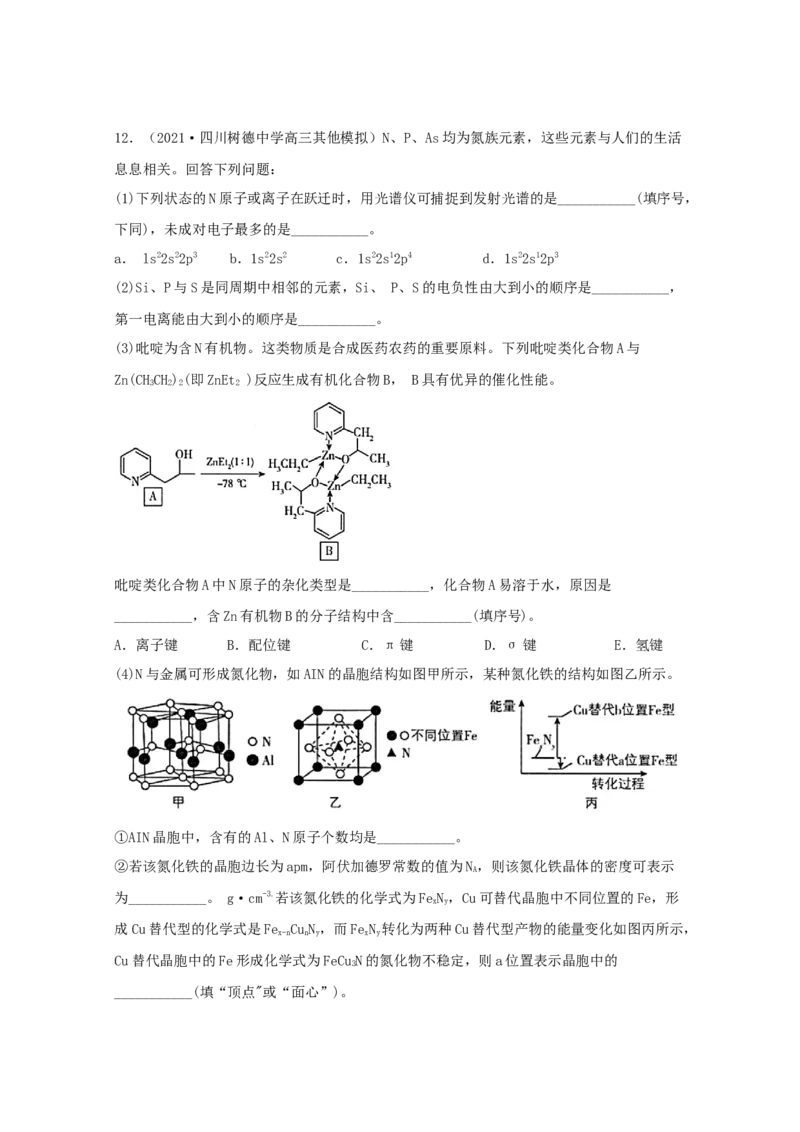
胞中棱长h=___cm。12.(2021·四川树德中学高三其他模拟)N、P、As均为氮族元素,这些元素与人们的生活
息息相关。回答下列问题:
(1)下列状态的N原子或离子在跃迁时,用光谱仪可捕捉到发射光谱的是___________(填序号,
下同),未成对电子最多的是___________。
a. ls22s22p3 b.1s22s2 c.1s22s12p4 d.1s22s12p3
(2)Si、P与S是同周期中相邻的元素,Si、 P、S的电负性由大到小的顺序是___________,
第一电离能由大到小的顺序是___________。
(3)吡啶为含N有机物。这类物质是合成医药农药的重要原料。下列吡啶类化合物A与
Zn(CHCH)(即ZnEt )反应生成有机化合物B, B具有优异的催化性能。
3 2 2 2
吡啶类化合物A中N原子的杂化类型是___________,化合物A易溶于水,原因是
___________,含Zn有机物B的分子结构中含___________(填序号)。
A.离子键 B.配位键 C.π键 D.σ键 E.氢键
(4)N与金属可形成氮化物,如AIN的晶胞结构如图甲所示,某种氮化铁的结构如图乙所示。
①AIN晶胞中,含有的Al、N原子个数均是___________。
②若该氮化铁的晶胞边长为apm,阿伏加德罗常数的值为N,则该氮化铁晶体的密度可表示
A
为___________。 g·cm-3.若该氮化铁的化学式为FeN,Cu可替代晶胞中不同位置的Fe,形
x y
成Cu替代型的化学式是Fe CuN,而FeN 转化为两种Cu替代型产物的能量变化如图丙所示,
x-n n y x y
Cu替代晶胞中的Fe形成化学式为FeCuN的氮化物不稳定,则a位置表示晶胞中的
3
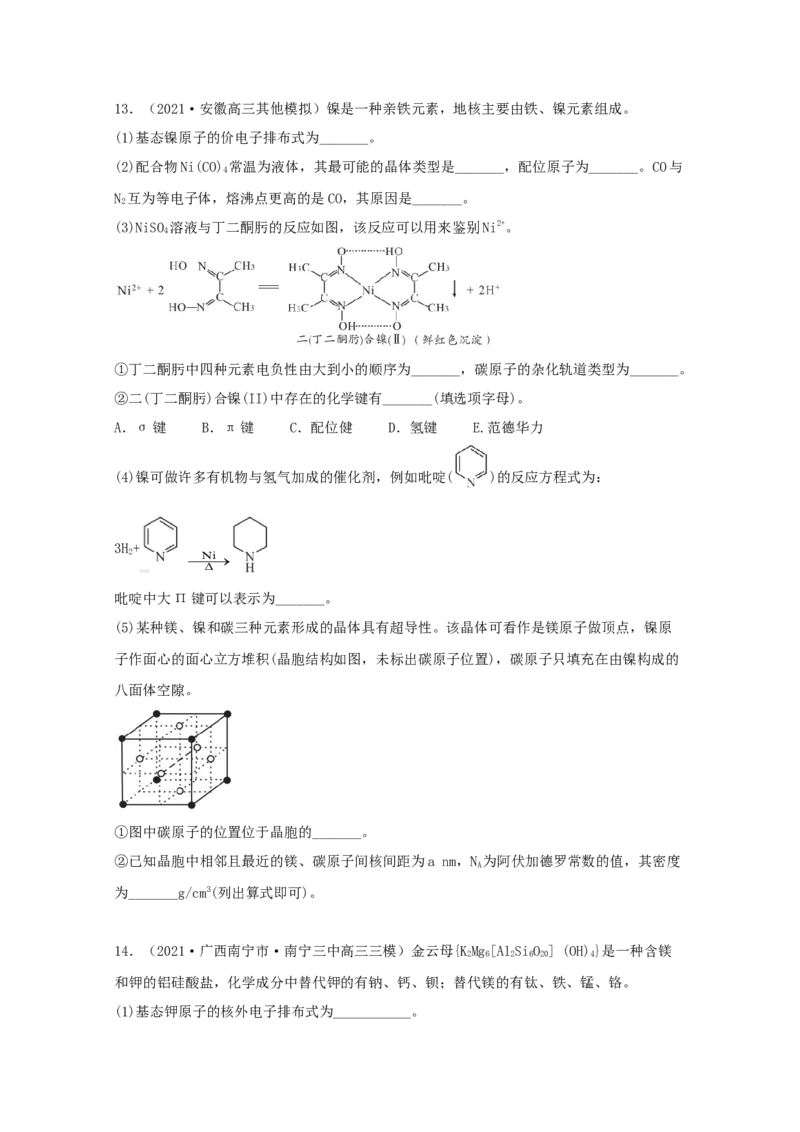
___________(填“顶点"或“面心”)。13.(2021·安徽高三其他模拟)镍是一种亲铁元素,地核主要由铁、镍元素组成。
(1)基态镍原子的价电子排布式为_______。
(2)配合物Ni(CO) 常温为液体,其最可能的晶体类型是_______,配位原子为_______。CO与
4
N 互为等电子体,熔沸点更高的是CO,其原因是_______。
2
(3)NiSO 溶液与丁二酮肟的反应如图,该反应可以用来鉴别Ni2+。
4
①丁二酮肟中四种元素电负性由大到小的顺序为_______,碳原子的杂化轨道类型为_______。
②二(丁二酮肟)合镍(II)中存在的化学键有_______(填选项字母)。
A.σ键 B.π键 C.配位健 D.氢键 E.范德华力
(4)镍可做许多有机物与氢气加成的催化剂,例如吡啶( )的反应方程式为:
3H+
2 Ni
Δ
吡啶中大Π键可以表示为_______。
(5)某种镁、镍和碳三种元素形成的晶体具有超导性。该晶体可看作是镁原子做顶点,镍原
子作面心的面心立方堆积(晶胞结构如图,未标出碳原子位置),碳原子只填充在由镍构成的
八面体空隙。
①图中碳原子的位置位于晶胞的_______。
②已知晶胞中相邻且最近的镁、碳原子间核间距为a nm,N 为阿伏加德罗常数的值,其密度
A
为_______g/cm3(列出算式即可)。
14.(2021·广西南宁市·南宁三中高三三模)金云母{KMg[AlSiO ] (OH)}是一种含镁
2 6 2 6 20 4
和钾的铝硅酸盐,化学成分中替代钾的有钠、钙、钡;替代镁的有钛、铁、锰、铬。
(1)基态钾原子的核外电子排布式为___________。(2)钡元素在周期表中位于___________ (填“s”“d”或“p”) 区。
(3) Mg、Al、 K的第一电离能由小到大的顺序是___________。
(4)镁、钙、钡均为第IIA族元素。
①MgO、CaO、BaO 中硬度最小的是___________。
②CaO的晶体结构与氯化钠的晶体结构类型相同,则与O2-距离最近的Ca2+数目为___________。
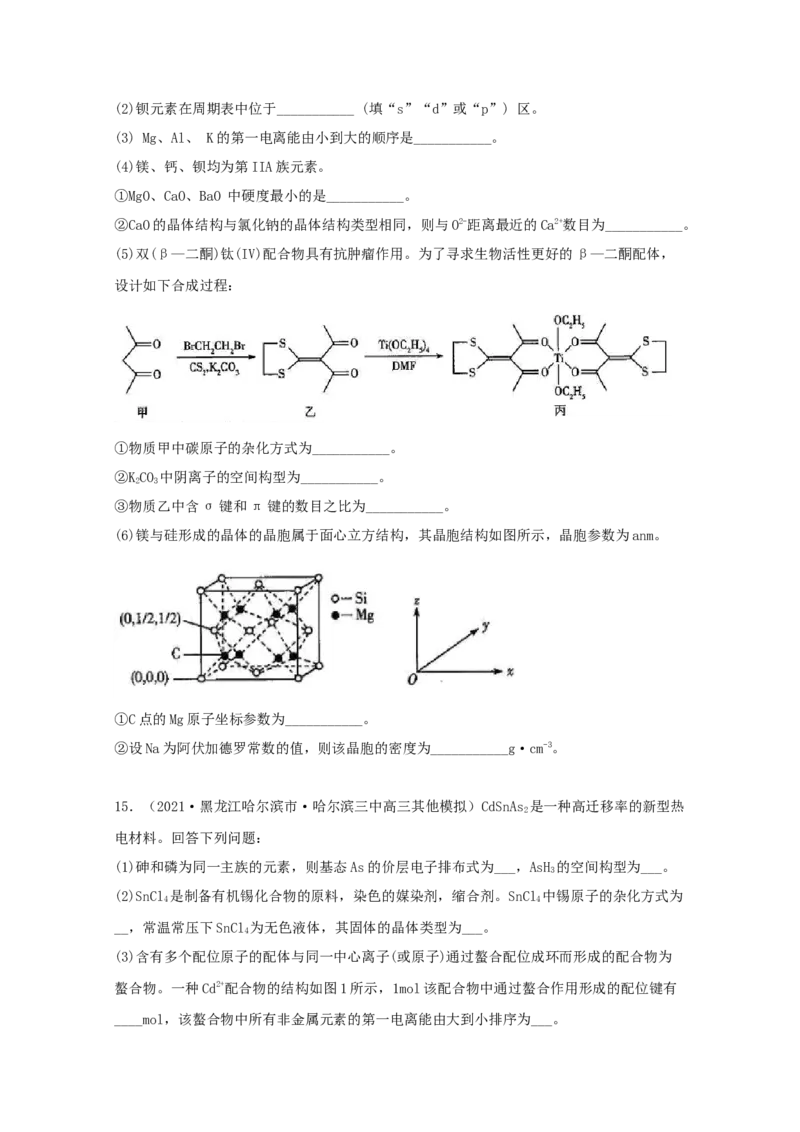
(5)双(β—二酮)钛(IV)配合物具有抗肿瘤作用。为了寻求生物活性更好的β—二酮配体,
设计如下合成过程:
①物质甲中碳原子的杂化方式为___________。
②KCO 中阴离子的空间构型为___________。
2 3
③物质乙中含σ键和π键的数目之比为___________。
(6)镁与硅形成的晶体的晶胞属于面心立方结构,其晶胞结构如图所示,晶胞参数为anm。
①C点的Mg原子坐标参数为___________。
②设Na为阿伏加德罗常数的值,则该晶胞的密度为___________g·cm-3。
15.(2021·黑龙江哈尔滨市·哈尔滨三中高三其他模拟)CdSnAs 是一种高迁移率的新型热
2
电材料。回答下列问题:
(1)砷和磷为同一主族的元素,则基态As的价层电子排布式为___,AsH 的空间构型为___。
3
(2)SnCl 是制备有机锡化合物的原料,染色的媒染剂,缩合剂。SnCl 中锡原子的杂化方式为
4 4
__,常温常压下SnCl 为无色液体,其固体的晶体类型为___。
4
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为
螯合物。一种Cd2+配合物的结构如图1所示,1mol该配合物中通过螯合作用形成的配位键有
____mol,该螯合物中所有非金属元素的第一电离能由大到小排序为___。(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐
标。四方晶系CdSnAs 的晶胞结构如图2所示,晶胞每个棱夹角均为90度。已知晶胞参数如
2
图,则图中紧邻Cd与As间的距离为___pm,晶胞密度为_______g/pm3。(N 表示阿伏伽德罗常
A
数)
16.(2021·长沙市明德中学高三三模)近日,某科研团队成功合成了Ni—Fe双原子催化剂
(Ni/Fe—C—N),并应用于高效催化CO 还原。回答下列问题:
2
(1)基态铁原子的价电子轨道排布图为_______。
(2)C、N、O三种元素的第一电离能由大到小的顺序为_______。
(3)过渡金属配合物Ni(CO) 的中心原子价电子数与CO提供配位的电子总数之和为18,则
n
n=_______;该化合物易溶于苯及四氯化碳等有机溶剂,原因是_______。
(4)二茂铁的结构为 ,由Fe2+和 (环戊二烯基负离子)构成。一个 中σ键总数为
_______,C原子的杂化轨道类型为_______。
(5)某C、Fe合金的晶胞结构如图所示:
该合金的化学式为_______,若该晶体的晶胞参数为apm、bpm、cpm,α=β=γ=90o,密度为
ρg·cm-3,则N为_______(写出计算式即可)。
A
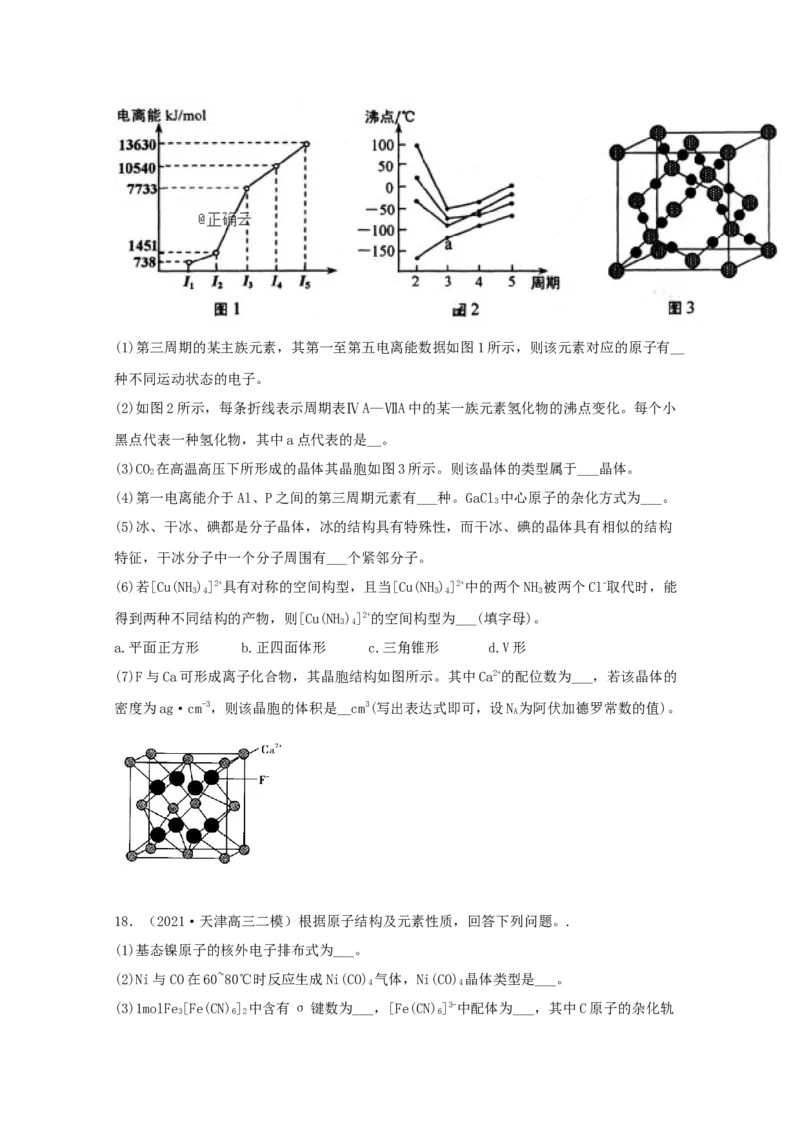
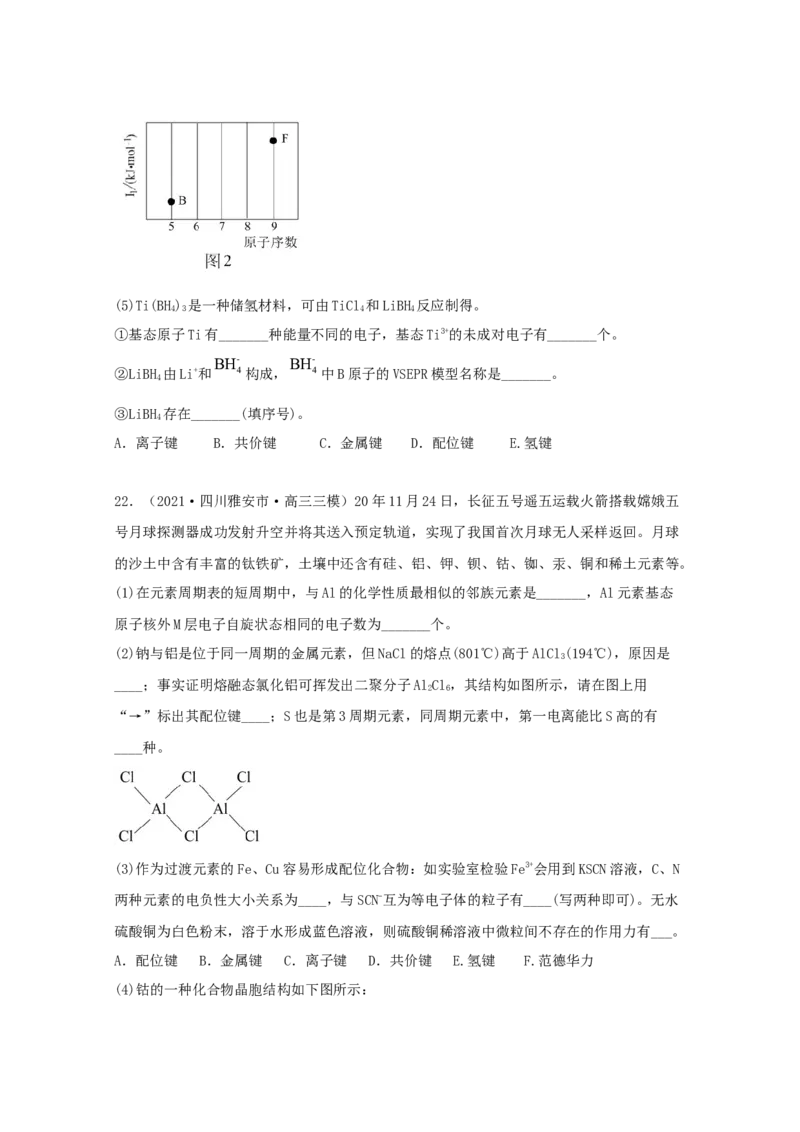
17.(2021·天津高三三模)请回答以下问题:(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有__
种不同运动状态的电子。
(2)如图2所示,每条折线表示周期表ⅣA—ⅦA中的某一族元素氢化物的沸点变化。每个小
黑点代表一种氢化物,其中a点代表的是__。
(3)CO 在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于___晶体。
2
(4)第一电离能介于Al、P之间的第三周期元素有___种。GaCl 中心原子的杂化方式为___。
3
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构
特征,干冰分子中一个分子周围有___个紧邻分子。
(6)若[Cu(NH)]2+具有对称的空间构型,且当[Cu(NH)]2+中的两个NH 被两个Cl-取代时,能
3 4 3 4 3
得到两种不同结构的产物,则[Cu(NH)]2+的空间构型为___(填字母)。
3 4
a.平面正方形 b.正四面体形 c.三角锥形 d.V形
(7)F与Ca可形成离子化合物,其晶胞结构如图所示。其中Ca2+的配位数为___,若该晶体的
密度为ag·cm-3,则该晶胞的体积是__cm3(写出表达式即可,设N 为阿伏加德罗常数的值)。
A
18.(2021·天津高三二模)根据原子结构及元素性质,回答下列问题。.
(1)基态镍原子的核外电子排布式为___。
(2)Ni与CO在60~80℃时反应生成Ni(CO) 气体,Ni(CO) 晶体类型是___。
4 4
(3)1molFe[Fe(CN)] 中含有σ键数为___,[Fe(CN)]3-中配体为___,其中C原子的杂化轨
3 6 2 6道类型为___。
(4)已知无水硫酸铜为白色粉末,溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间
作用力有:___。
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 E.范德华力
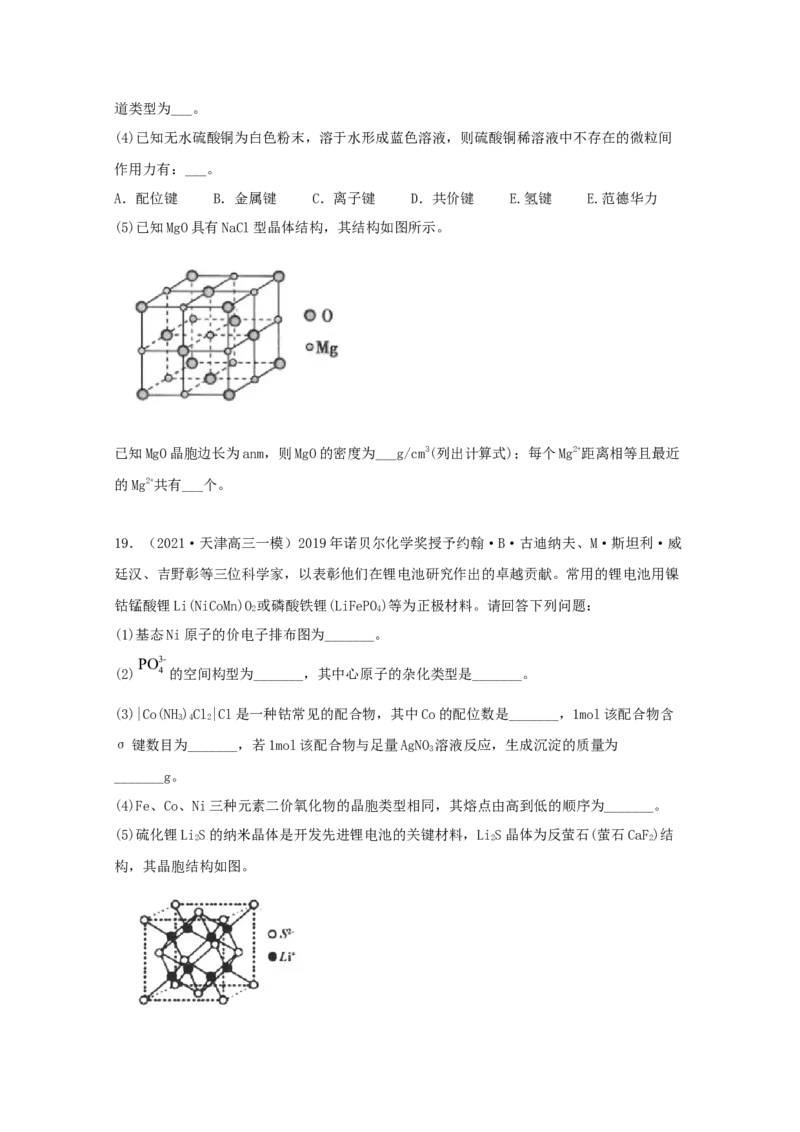
(5)已知MgO具有NaCl型晶体结构,其结构如图所示。
已知MgO晶胞边长为anm,则MgO的密度为___g/cm3(列出计算式);每个Mg2+距离相等且最近
的Mg2+共有___个。
19.(2021·天津高三一模)2019年诺贝尔化学奖授予约翰·B·古迪纳夫、M·斯坦利·威
廷汉、吉野彰等三位科学家,以表彰他们在锂电池研究作出的卓越贡献。常用的锂电池用镍
钴锰酸锂Li(NiCoMn)O 或磷酸铁锂(LiFePO)等为正极材料。请回答下列问题:
2 4
(1)基态Ni原子的价电子排布图为_______。
PO3-
(2) 4 的空间构型为_______,其中心原子的杂化类型是_______。
(3)|Co(NH)Cl|Cl是一种钴常见的配合物,其中Co的配位数是_______,1mol该配合物含
3 4 2
σ键数目为_______,若1mol该配合物与足量AgNO 溶液反应,生成沉淀的质量为
3
_______g。
(4)Fe、Co、Ni三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为_______。
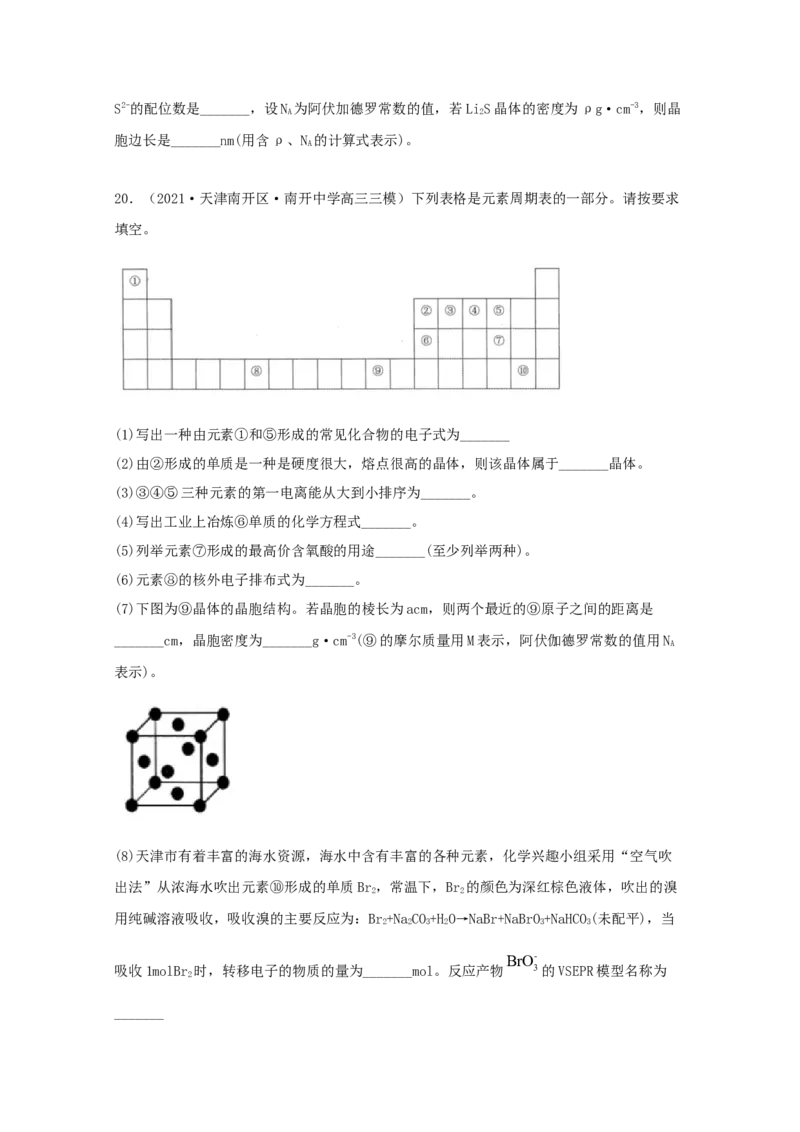
(5)硫化锂LiS的纳米晶体是开发先进锂电池的关键材料,LiS晶体为反萤石(萤石CaF)结
2 2 2
构,其晶胞结构如图。S2-的配位数是_______,设N 为阿伏加德罗常数的值,若LiS晶体的密度为ρg·cm-3,则晶
A 2
胞边长是_______nm(用含ρ、N 的计算式表示)。
A
20.(2021·天津南开区·南开中学高三三模)下列表格是元素周期表的一部分。请按要求
填空。
(1)写出一种由元素①和⑤形成的常见化合物的电子式为_______
(2)由②形成的单质是一种是硬度很大,熔点很高的晶体,则该晶体属于_______晶体。
(3)③④⑤三种元素的第一电离能从大到小排序为_______。
(4)写出工业上冶炼⑥单质的化学方程式_______。
(5)列举元素⑦形成的最高价含氧酸的用途_______(至少列举两种)。
(6)元素⑧的核外电子排布式为_______。
(7)下图为⑨晶体的晶胞结构。若晶胞的棱长为acm,则两个最近的⑨原子之间的距离是
_______cm,晶胞密度为_______g·cm-3(⑨的摩尔质量用M表示,阿伏伽德罗常数的值用N
A
表示)。
(8)天津市有着丰富的海水资源,海水中含有丰富的各种元素,化学兴趣小组采用“空气吹
出法”从浓海水吹出元素⑩形成的单质Br,常温下,Br 的颜色为深红棕色液体,吹出的溴
2 2
用纯碱溶液吸收,吸收溴的主要反应为:Br+NaCO+HO→NaBr+NaBrO+NaHCO(未配平),当
2 2 3 2 3 3
BrO-
吸收1molBr 时,转移电子的物质的量为_______mol。反应产物 3的VSEPR模型名称为
2
_______21.(2021·天津和平区·耀华中学高三二模)(1)金属氢化物是具有良好发展前景的储氢
材料。
①LiH中,离子半径Li+_______(填“>”、“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如下表所示:
I I I I I
1 2 3 4 5
I/kJ·mol-1 738 1451 7733 10540 13630
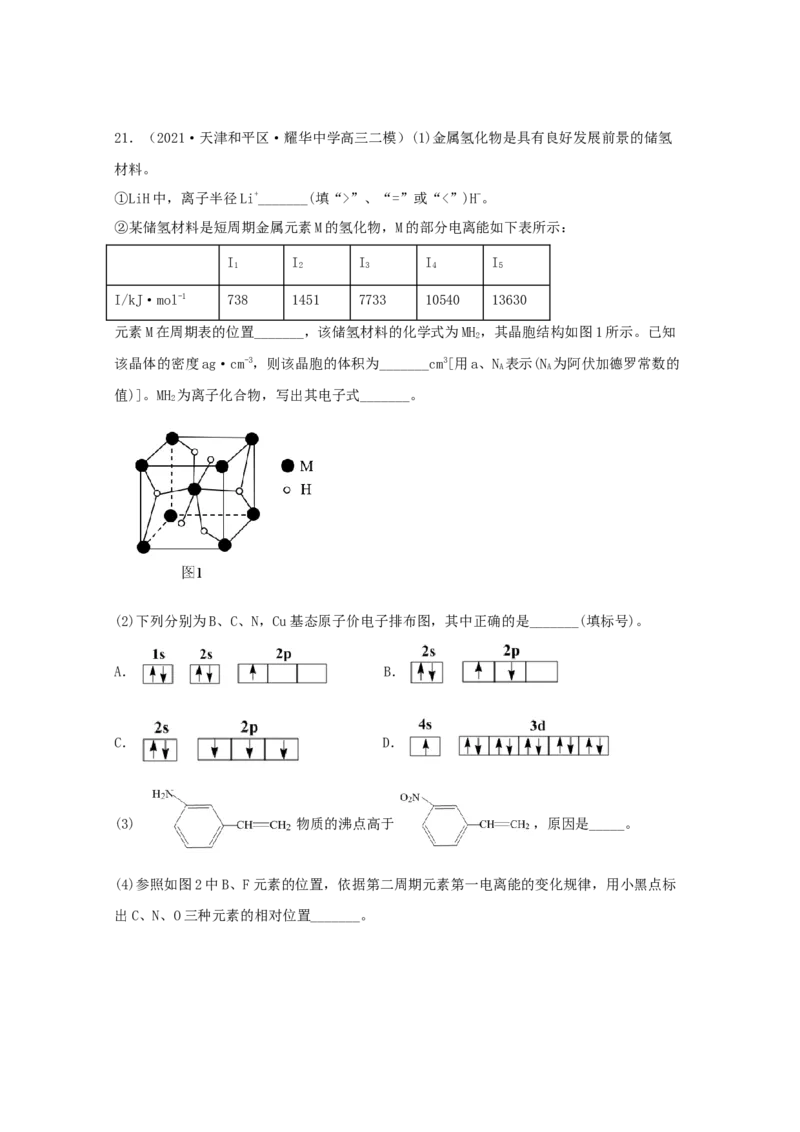
元素M在周期表的位置_______,该储氢材料的化学式为MH,其晶胞结构如图1所示。已知
2
该晶体的密度ag·cm-3,则该晶胞的体积为_______cm3[用a、N 表示(N 为阿伏加德罗常数的
A A
值)]。MH 为离子化合物,写出其电子式_______。
2
(2)下列分别为B、C、N,Cu基态原子价电子排布图,其中正确的是_______(填标号)。
A. B.
C. D.
(3) 物质的沸点高于 ,原因是_____。
(4)参照如图2中B、F元素的位置,依据第二周期元素第一电离能的变化规律,用小黑点标
出C、N、O三种元素的相对位置_______。(5)Ti(BH) 是一种储氢材料,可由TiCl 和LiBH 反应制得。
4 3 4 4
①基态原子Ti有_______种能量不同的电子,基态Ti3+的未成对电子有_______个。
BH- BH-
②LiBH 由Li+和 4构成, 4中B原子的VSEPR模型名称是_______。
4
③LiBH 存在_______(填序号)。
4
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
22.(2021·四川雅安市·高三三模)20年11月24日,长征五号遥五运载火箭搭载嫦娥五
号月球探测器成功发射升空并将其送入预定轨道,实现了我国首次月球无人采样返回。月球
的沙土中含有丰富的钛铁矿,土壤中还含有硅、铝、钾、钡、钴、铷、汞、铜和稀土元素等。
(1)在元素周期表的短周期中,与Al的化学性质最相似的邻族元素是_______,Al元素基态
原子核外M层电子自旋状态相同的电子数为_______个。
(2)钠与铝是位于同一周期的金属元素,但NaCl的熔点(801℃)高于AlCl(194℃),原因是
3
____;事实证明熔融态氯化铝可挥发出二聚分子AlCl,其结构如图所示,请在图上用
2 6
“→”标出其配位键____;S也是第3周期元素,同周期元素中,第一电离能比S高的有
____种。
(3)作为过渡元素的Fe、Cu容易形成配位化合物:如实验室检验Fe3+会用到KSCN溶液,C、N
两种元素的电负性大小关系为____,与SCN-互为等电子体的粒子有____(写两种即可)。无水
硫酸铜为白色粉末,溶于水形成蓝色溶液,则硫酸铜稀溶液中微粒间不存在的作用力有___。
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
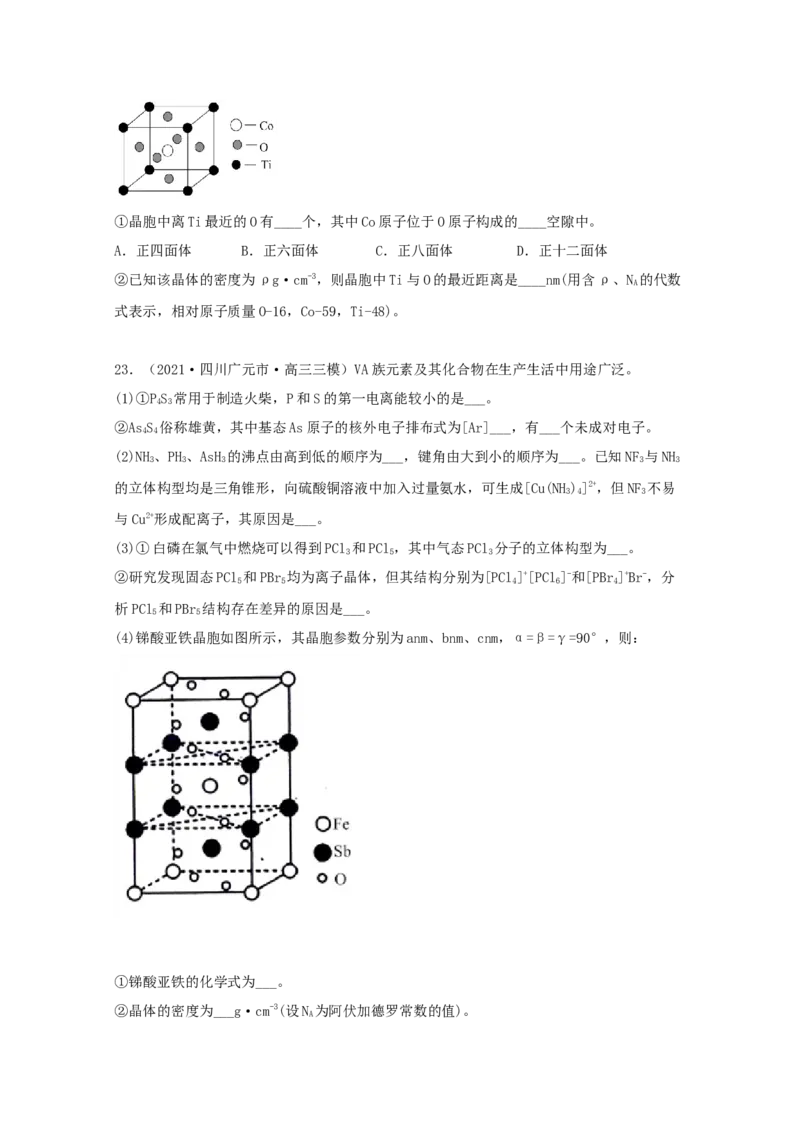
(4)钴的一种化合物晶胞结构如下图所示:①晶胞中离Ti最近的O有____个,其中Co原子位于O原子构成的____空隙中。
A.正四面体 B.正六面体 C.正八面体 D.正十二面体
②已知该晶体的密度为ρg·cm-3,则晶胞中Ti与O的最近距离是____nm(用含ρ、N 的代数
A
式表示,相对原子质量O-16,Co-59,Ti-48)。
23.(2021·四川广元市·高三三模)VA族元素及其化合物在生产生活中用途广泛。
(1)①PS 常用于制造火柴,P和S的第一电离能较小的是___。
4 3
②AsS 俗称雄黄,其中基态As原子的核外电子排布式为[Ar]___,有___个未成对电子。
4 4
(2)NH、PH、AsH 的沸点由高到低的顺序为___,键角由大到小的顺序为___。已知NF 与NH
3 3 3 3 3
的立体构型均是三角锥形,向硫酸铜溶液中加入过量氨水,可生成[Cu(NH)]2+,但NF 不易
3 4 3
与Cu2+形成配离子,其原因是___。
(3)①白磷在氯气中燃烧可以得到PCl 和PCl,其中气态PCl 分子的立体构型为___。
3 5 3
②研究发现固态PCl 和PBr 均为离子晶体,但其结构分别为[PCl]+[PCl]-和[PBr]+Br-,分
5 5 4 6 4
析PCl 和PBr 结构存在差异的原因是___。
5 5
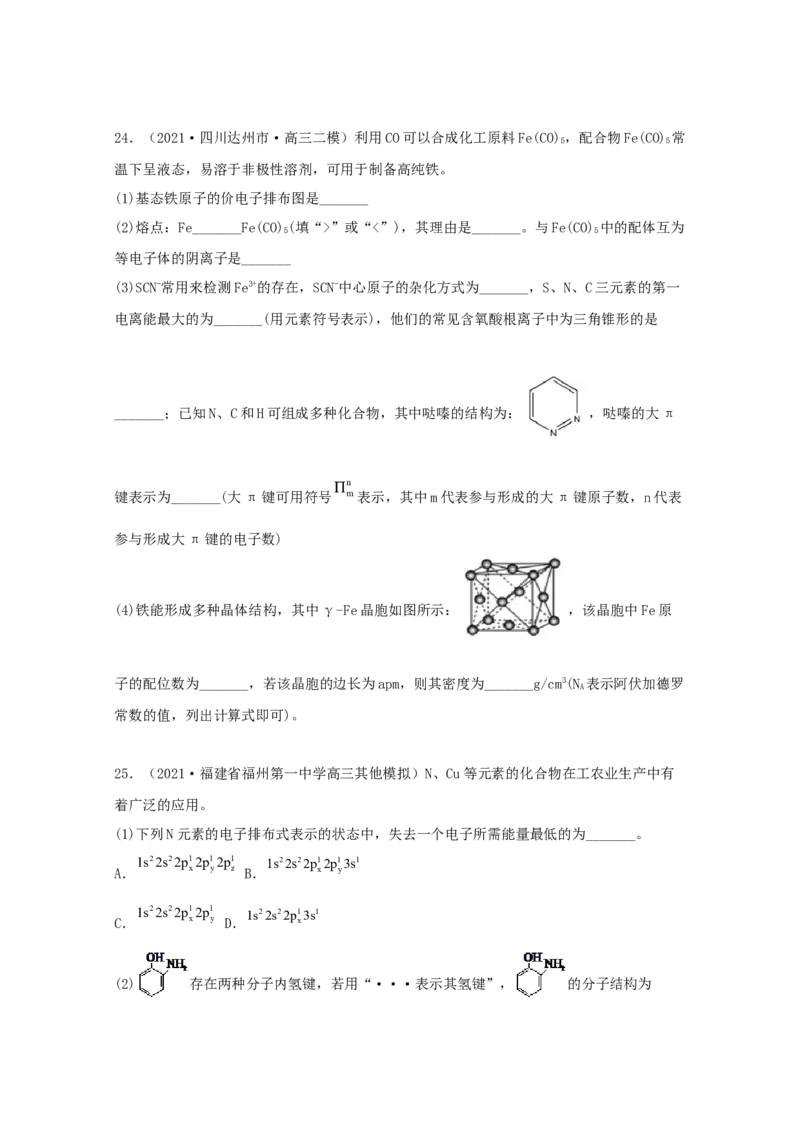
(4)锑酸亚铁晶胞如图所示,其晶胞参数分别为anm、bnm、cnm,α=β=γ=90°,则:
①锑酸亚铁的化学式为___。
②晶体的密度为___g·cm-3(设N 为阿伏加德罗常数的值)。
A24.(2021·四川达州市·高三二模)利用CO可以合成化工原料Fe(CO),配合物Fe(CO) 常
5 5
温下呈液态,易溶于非极性溶剂,可用于制备高纯铁。
(1)基态铁原子的价电子排布图是_______
(2)熔点:Fe_______Fe(CO)(填“>”或“<”),其理由是_______。与Fe(CO) 中的配体互为
5 5
等电子体的阴离子是_______
(3)SCN-常用来检测Fe3+的存在,SCN-中心原子的杂化方式为_______,S、N、C三元素的第一
电离能最大的为_______(用元素符号表示),他们的常见含氧酸根离子中为三角锥形的是
_______;已知N、C和H可组成多种化合物,其中哒嗪的结构为: ,哒嗪的大π
Πn
键表示为_______(大π键可用符号 m表示,其中m代表参与形成的大π键原子数,n代表
参与形成大π键的电子数)
(4)铁能形成多种晶体结构,其中γ-Fe晶胞如图所示: ,该晶胞中Fe原
子的配位数为_______,若该晶胞的边长为apm,则其密度为_______g/cm3(N 表示阿伏加德罗
A
常数的值,列出计算式即可)。
25.(2021·福建省福州第一中学高三其他模拟)N、Cu等元素的化合物在工农业生产中有
着广泛的应用。
(1)下列N元素的电子排布式表示的状态中,失去一个电子所需能量最低的为_______。
1s22s22p12p12p1 1s22s22p12p13s1
A. x y z B. x y
1s22s22p12p1 1s22s22p13s1
C. x y D. x
(2) 存在两种分子内氢键,若用“···表示其氢键”, 的分子结构为_______。
(3)基态Cu2+价电子的空间运动状态有_______种。
(4) 分子中采取 杂化的原子有_______。(填原子符号)
sp3
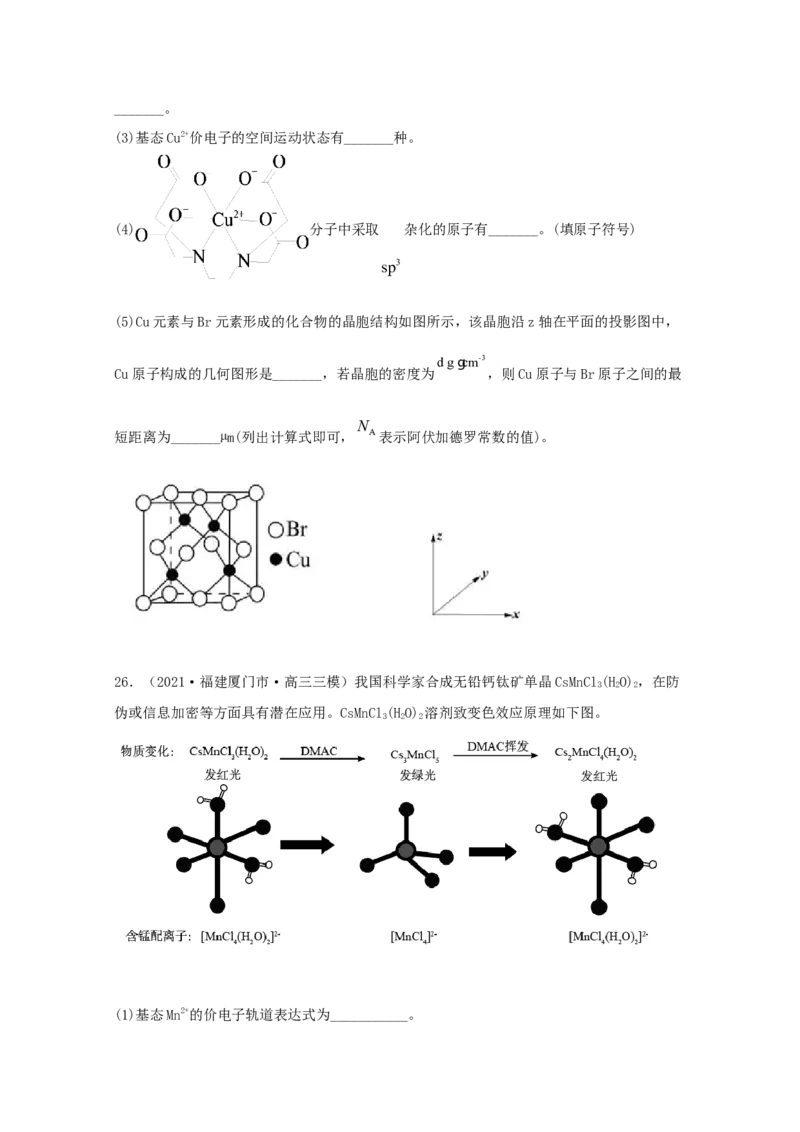
(5)Cu元素与Br元素形成的化合物的晶胞结构如图所示,该晶胞沿z轴在平面的投影图中,
dggcm-3
Cu原子构成的几何图形是_______,若晶胞的密度为 ,则Cu原子与Br原子之间的最
N
短距离为_______µm(列出计算式即可, A表示阿伏加德罗常数的值)。
26.(2021·福建厦门市·高三三模)我国科学家合成无铅钙钛矿单晶CsMnCl(HO),在防
3 2 2
伪或信息加密等方面具有潜在应用。CsMnCl(HO) 溶剂致变色效应原理如下图。
3 2 2
(1)基态Mn2+的价电子轨道表达式为___________。(2)CsMnCl(HO) 中,主族元素的电负性从大到小的顺序为___________。
3 2 2
(3)变色过程,锰离子的配位数___________(填“有”或“没有”)发生变化。
(4)从结构角度分析DMAC[结构简式为(CH)NCOCH]能使含锰配离子发生变化的原因
3 2 3
___________。
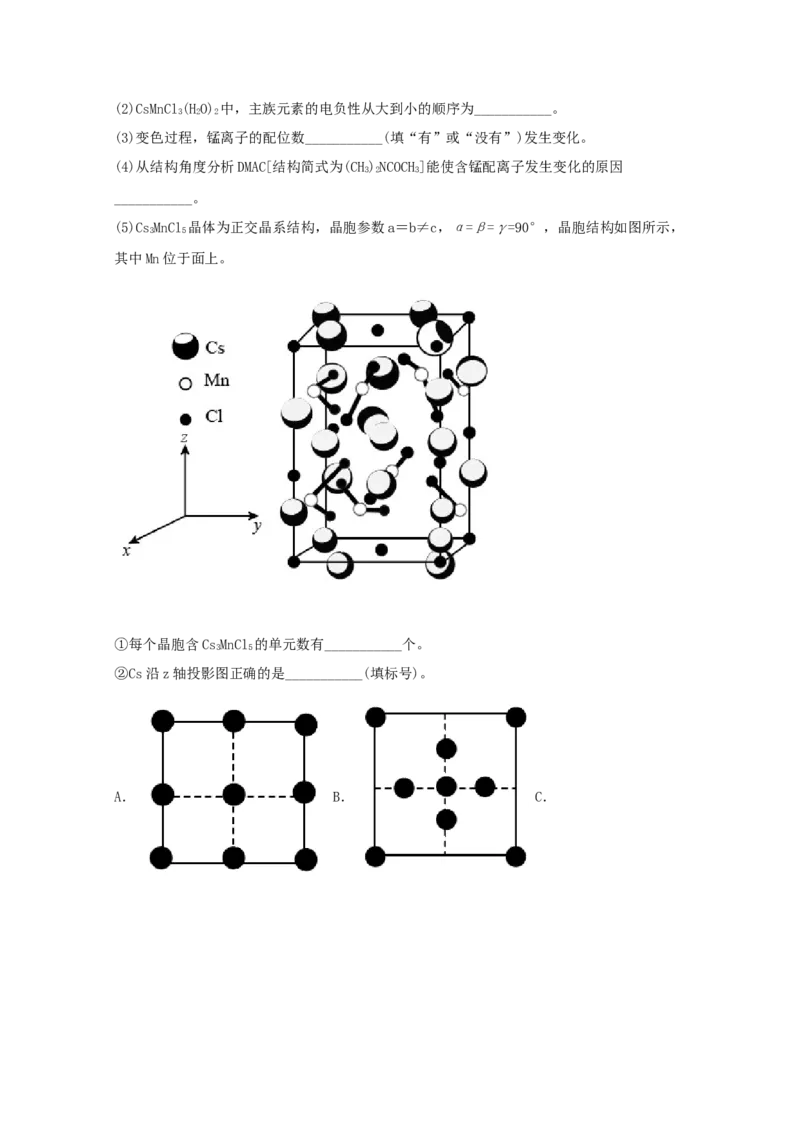
(5)CsMnCl 晶体为正交晶系结构,晶胞参数a=b≠c,α=β=γ=90°,晶胞结构如图所示,
3 5
其中Mn位于面上。
①每个晶胞含CsMnCl 的单元数有___________个。
3 5
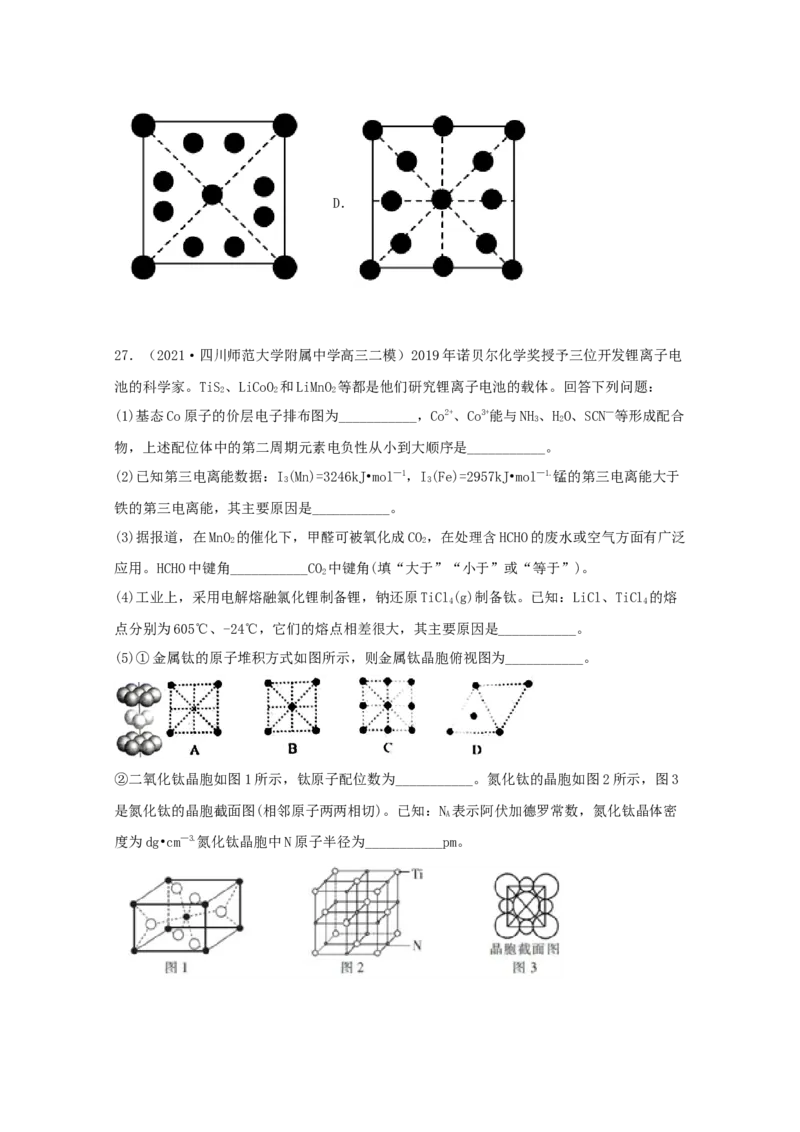
②Cs沿z轴投影图正确的是___________(填标号)。
A. B. C.D.
27.(2021·四川师范大学附属中学高三二模)2019年诺贝尔化学奖授予三位开发锂离子电
池的科学家。TiS、LiCoO 和LiMnO 等都是他们研究锂离子电池的载体。回答下列问题:
2 2 2
(1)基态Co原子的价层电子排布图为___________,Co2+、Co3+能与NH、HO、SCN—等形成配合
3 2
物,上述配位体中的第二周期元素电负性从小到大顺序是___________。
(2)已知第三电离能数据:I(Mn)=3246kJ•mol—1,I(Fe)=2957kJ•mol—1.锰的第三电离能大于
3 3
铁的第三电离能,其主要原因是___________。
(3)据报道,在MnO 的催化下,甲醛可被氧化成CO,在处理含HCHO的废水或空气方面有广泛
2 2
应用。HCHO中键角___________CO 中键角(填“大于”“小于”或“等于”)。
2
(4)工业上,采用电解熔融氯化锂制备锂,钠还原TiCl(g)制备钛。已知:LiCl、TiCl 的熔
4 4
点分别为605℃、-24℃,它们的熔点相差很大,其主要原因是___________。
(5)①金属钛的原子堆积方式如图所示,则金属钛晶胞俯视图为___________。
②二氧化钛晶胞如图1所示,钛原子配位数为___________。氮化钛的晶胞如图2所示,图3
是氮化钛的晶胞截面图(相邻原子两两相切)。已知:N 表示阿伏加德罗常数,氮化钛晶体密
A
度为dg•cm—3.氮化钛晶胞中N原子半径为___________pm。二、工业流程题
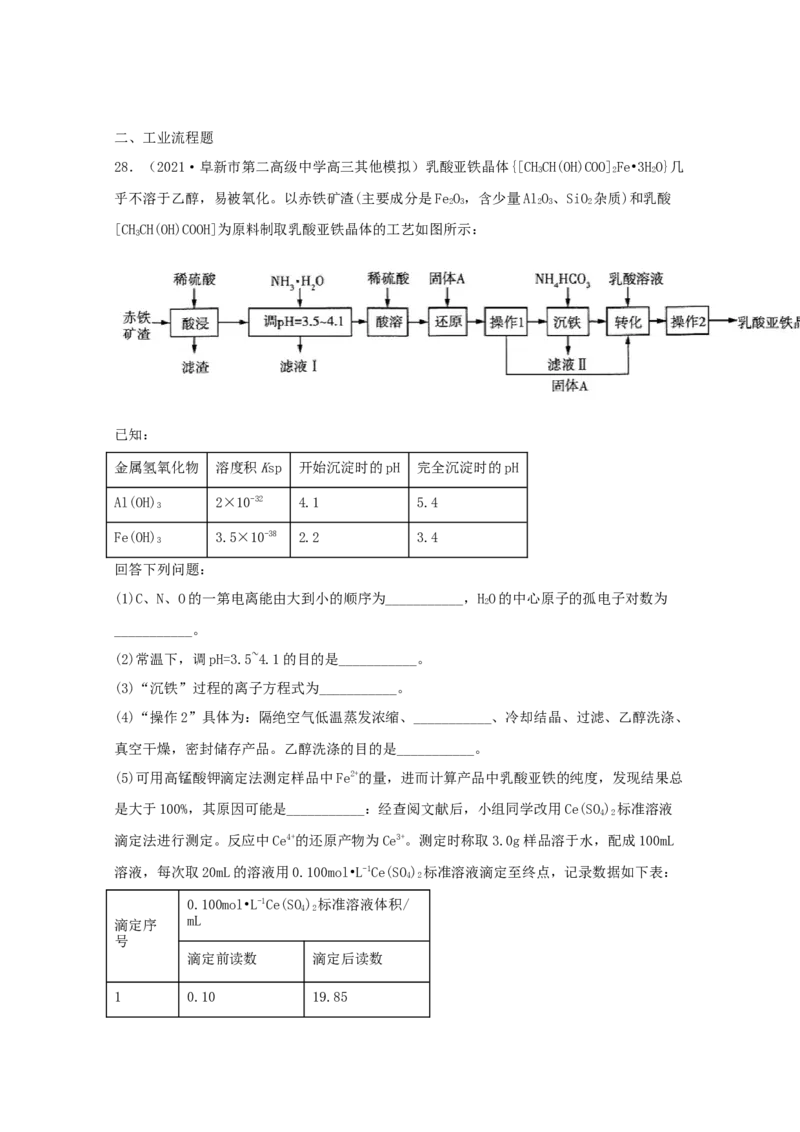
28.(2021·阜新市第二高级中学高三其他模拟)乳酸亚铁晶体{[CHCH(OH)COO]Fe•3HO}几
3 2 2
乎不溶于乙醇,易被氧化。以赤铁矿渣(主要成分是FeO,含少量AlO、SiO 杂质)和乳酸
2 3 2 3 2
[CHCH(OH)COOH]为原料制取乳酸亚铁晶体的工艺如图所示:
3
已知:
金属氢氧化物 溶度积Ksp 开始沉淀时的pH 完全沉淀时的pH
Al(OH) 2×10-32 4.1 5.4
3
Fe(OH) 3.5×10-38 2.2 3.4
3
回答下列问题:
(1)C、N、O的一第电离能由大到小的顺序为___________,HO的中心原子的孤电子对数为
2
___________。
(2)常温下,调pH=3.5~4.1的目的是___________。
(3)“沉铁”过程的离子方程式为___________。
(4)“操作2”具体为:隔绝空气低温蒸发浓缩、___________、冷却结晶、过滤、乙醇洗涤、
真空干燥,密封储存产品。乙醇洗涤的目的是___________。
(5)可用高锰酸钾滴定法测定样品中Fe2+的量,进而计算产品中乳酸亚铁的纯度,发现结果总
是大于100%,其原因可能是___________:经查阅文献后,小组同学改用Ce(SO) 标准溶液
4 2
滴定法进行测定。反应中Ce4+的还原产物为Ce3+。测定时称取3.0g样品溶于水,配成100mL
溶液,每次取20mL的溶液用0.100mol•L-1Ce(SO) 标准溶液滴定至终点,记录数据如下表:
4 2
0.100mol•L-1Ce(SO) 标准溶液体积/
4 2
mL
滴定序
号
滴定前读数 滴定后读数
1 0.10 19.852 0.12 21.32
3 1.05 20.70
则产品中乳酸亚铁晶体的纯度为___________。