文档内容
专题 30 水的电离和溶液的 pH
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 水的电离与离子积常数
考点二 溶液的酸碱性、pH计算
考点三 酸碱中和滴定及其应用
考点一 水的电离与离子积常数
1.(2023春·青海西宁·高三统考开学考试)25℃时,用NaOH标准溶液滴定100mL0.1mol•L-1KHA溶液
(HA的K =1.1×10-3,K =4.0×10-7),混合溶液中水电离出的c(OH-)与加入NaOH溶液体积之间的关系如图
2 a1 a2
所示。下列有关说法正确的是
A.X点溶液呈碱性
B.Y点与W点溶液中水的电离程度不同
C.根据以上信息可以判断V=100
1
D.Z点对应溶液中存在c(OH-)=c(H+)+2c(HA)+c(HA-)
2
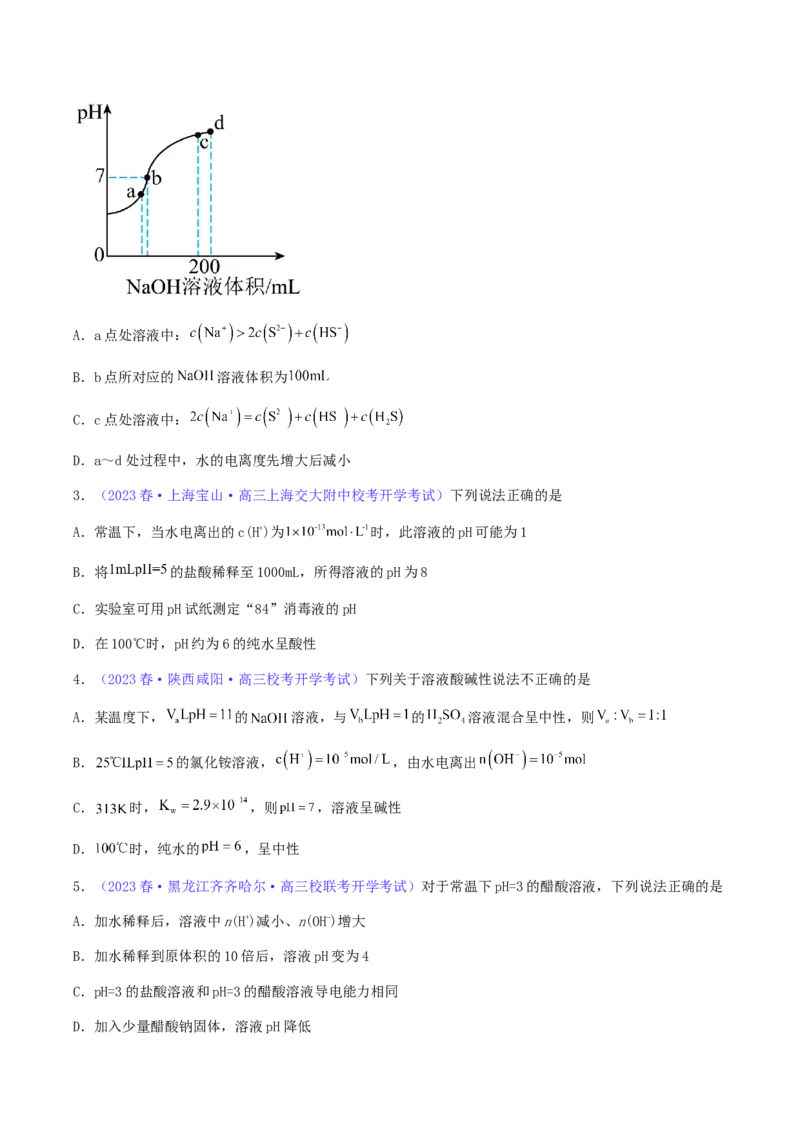
2.(2023秋·河南开封·高三开封市第二十五中学校考开学考试)常温下,向 溶液
中滴加 的 溶液。实验过程中, 溶液的pH与所滴加的 溶液体积的关系如图所示。
已知常温下 的 , 。下列说法正确的是
1
原创精品资源学科网独家享有版权,侵权必究!A.a点处溶液中:
B.b点所对应的 溶液体积为
C.c点处溶液中:
D.a~d处过程中,水的电离度先增大后减小
3.(2023春·上海宝山·高三上海交大附中校考开学考试)下列说法正确的是
A.常温下,当水电离出的c(H+)为 时,此溶液的pH可能为1
B.将 的盐酸稀释至1000mL,所得溶液的pH为8
C.实验室可用pH试纸测定“84”消毒液的pH
D.在100℃时,pH约为6的纯水呈酸性
4.(2023春·陕西咸阳·高三校考开学考试)下列关于溶液酸碱性说法不正确的是
A.某温度下, 的 溶液,与 的 溶液混合呈中性,则
B. 的氯化铵溶液, ,由水电离出
C. 时, ,则 ,溶液呈碱性
D. 时,纯水的 ,呈中性
5.(2023春·黑龙江齐齐哈尔·高三校联考开学考试)对于常温下pH=3的醋酸溶液,下列说法正确的是
A.加水稀释后,溶液中n(H+)减小、n(OH-)增大
B.加水稀释到原体积的10倍后,溶液pH变为4
C.pH=3的盐酸溶液和pH=3的醋酸溶液导电能力相同
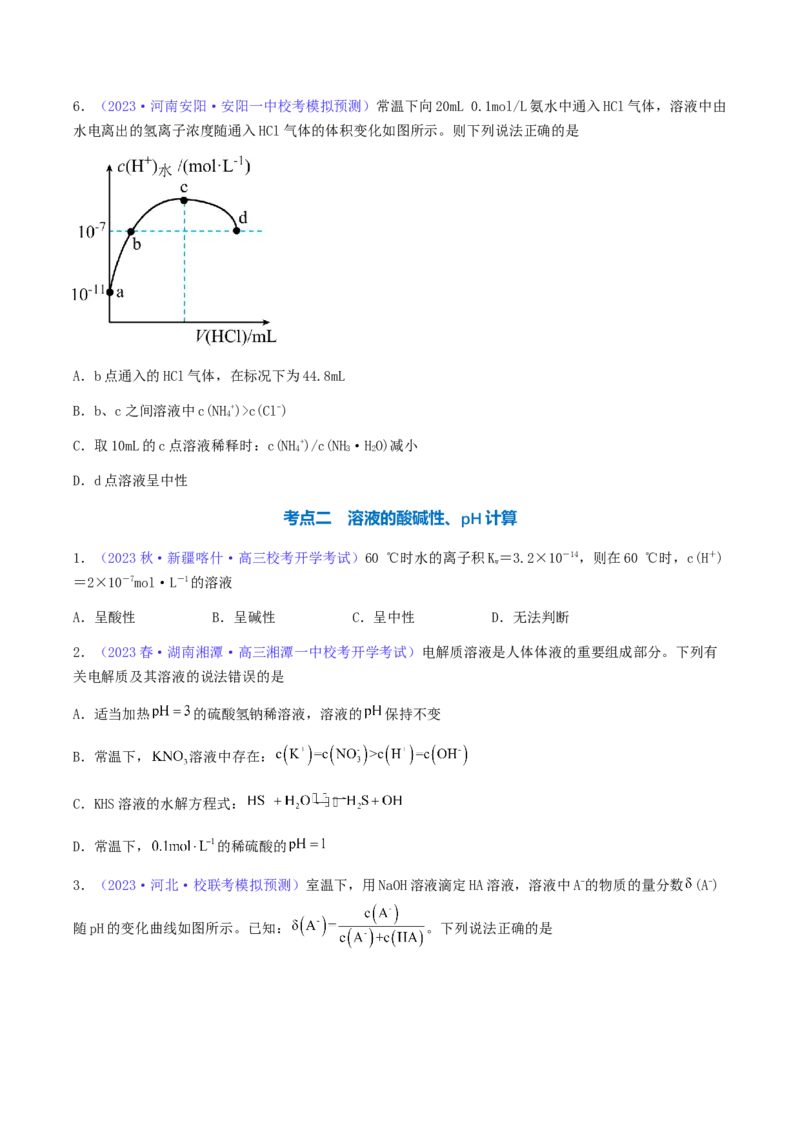
D.加入少量醋酸钠固体,溶液pH降低6.(2023·河南安阳·安阳一中校考模拟预测)常温下向20mL 0.1mol/L氨水中通入HCl气体,溶液中由
水电离出的氢离子浓度随通入HCl气体的体积变化如图所示。则下列说法正确的是
A.b点通入的HCl气体,在标况下为44.8mL
B.b、c之间溶液中c(NH+)>c(Cl-)
4
C.取10mL的c点溶液稀释时:c(NH+)/c(NH·HO)减小
4 3 2
D.d点溶液呈中性
考点二 溶液的酸碱性、pH计算
1.(2023秋·新疆喀什·高三校考开学考试)60 ℃时水的离子积K=3.2×10-14,则在60 ℃时,c(H+)
w
=2×10-7mol·L-1的溶液
A.呈酸性 B.呈碱性 C.呈中性 D.无法判断
2.(2023春·湖南湘潭·高三湘潭一中校考开学考试)电解质溶液是人体体液的重要组成部分。下列有
关电解质及其溶液的说法错误的是
A.适当加热 的硫酸氢钠稀溶液,溶液的 保持不变
B.常温下, 溶液中存在:
C.KHS溶液的水解方程式:
D.常温下, 的稀硫酸的
3.(2023·河北·校联考模拟预测)室温下,用NaOH溶液滴定HA溶液,溶液中A-的物质的量分数 (A-)
随pH的变化曲线如图所示。已知: 。下列说法正确的是A.K的数量级为10-3
a
B.PH与pK之间满足关系式:
a
C.X点为滴定终点
D. 时,溶液呈碱性
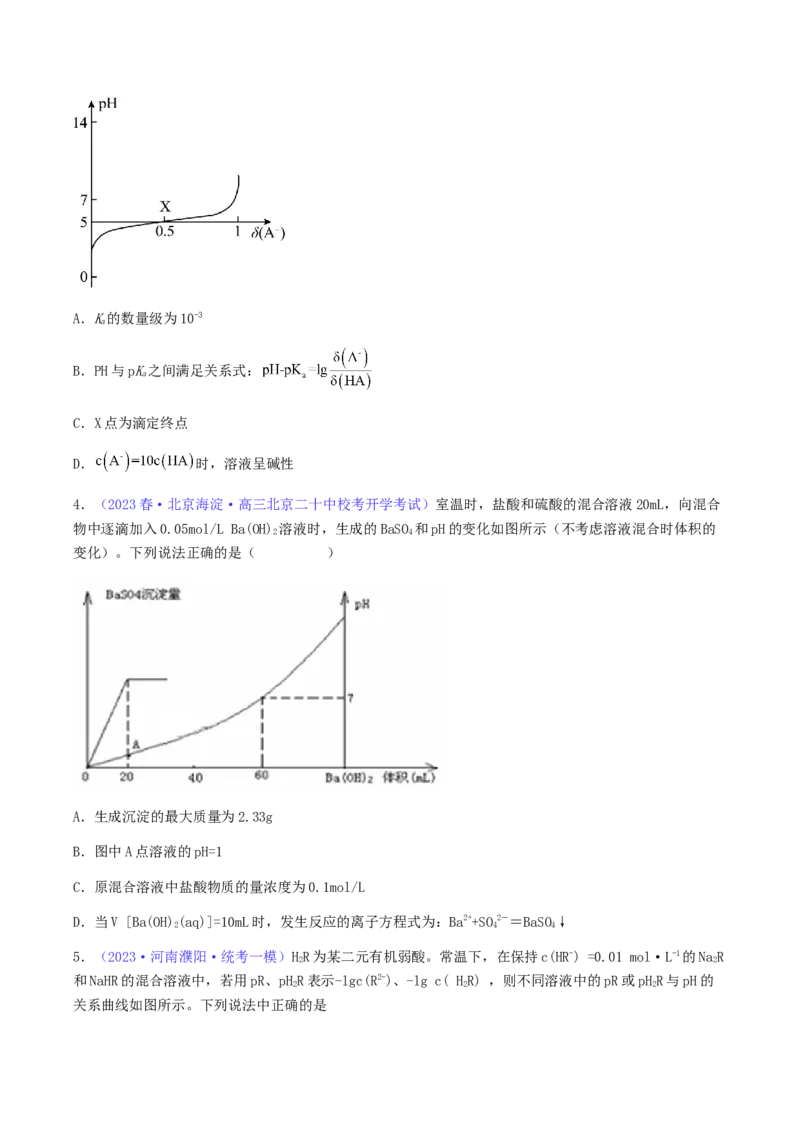
4.(2023春·北京海淀·高三北京二十中校考开学考试)室温时,盐酸和硫酸的混合溶液20mL,向混合
物中逐滴加入0.05mol/L Ba(OH) 溶液时,生成的BaSO 和pH的变化如图所示(不考虑溶液混合时体积的
2 4
变化)。下列说法正确的是( )
A.生成沉淀的最大质量为2.33g
B.图中A点溶液的pH=1
C.原混合溶液中盐酸物质的量浓度为0.1mol/L
D.当V [Ba(OH)(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO2-=BaSO↓
2 4 4
5.(2023·河南濮阳·统考一模)HR为某二元有机弱酸。常温下,在保持c(HR-) =0.01 mol·L-1的NaR
2 2
和NaHR的混合溶液中,若用pR、pHR表示-lgc(R2-)、-lg c( HR) ,则不同溶液中的pR或pHR与pH的
2 2 2
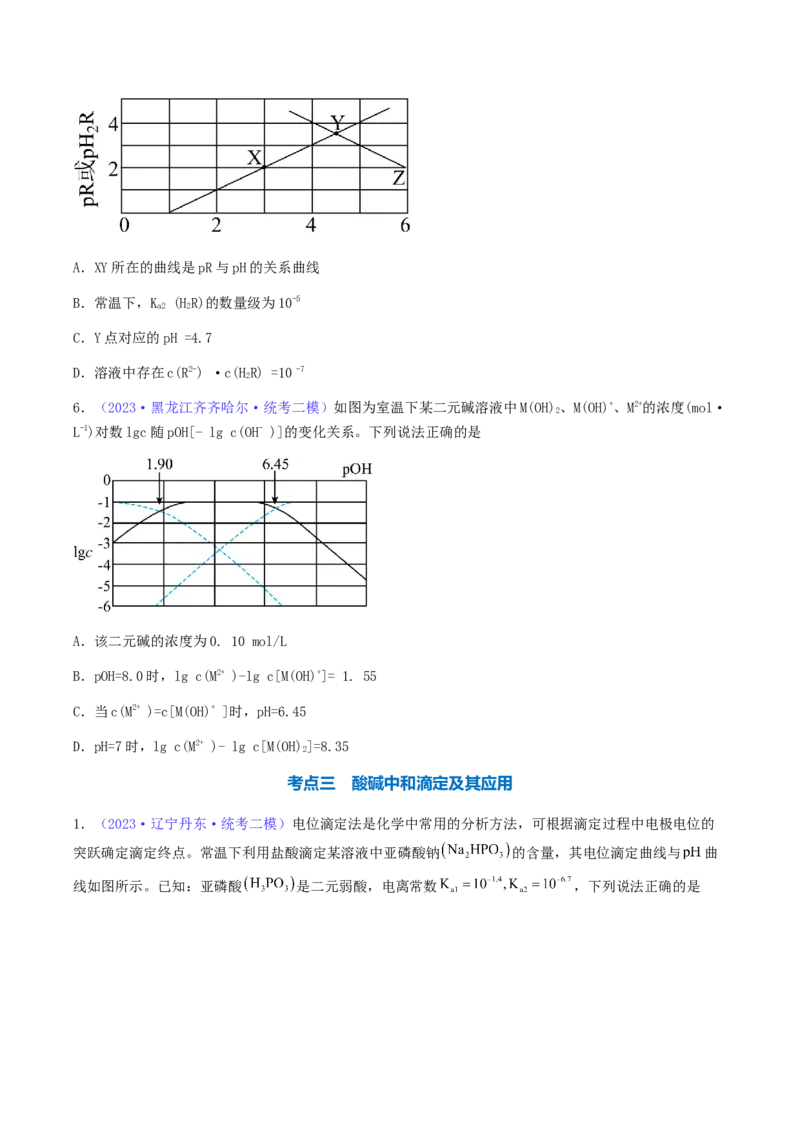
关系曲线如图所示。下列说法中正确的是A.XY所在的曲线是pR与pH的关系曲线
B.常温下,K (HR)的数量级为10-5
a2 2
C.Y点对应的pH =4.7
D.溶液中存在c(R2-) ·c(HR) =10 -7
2
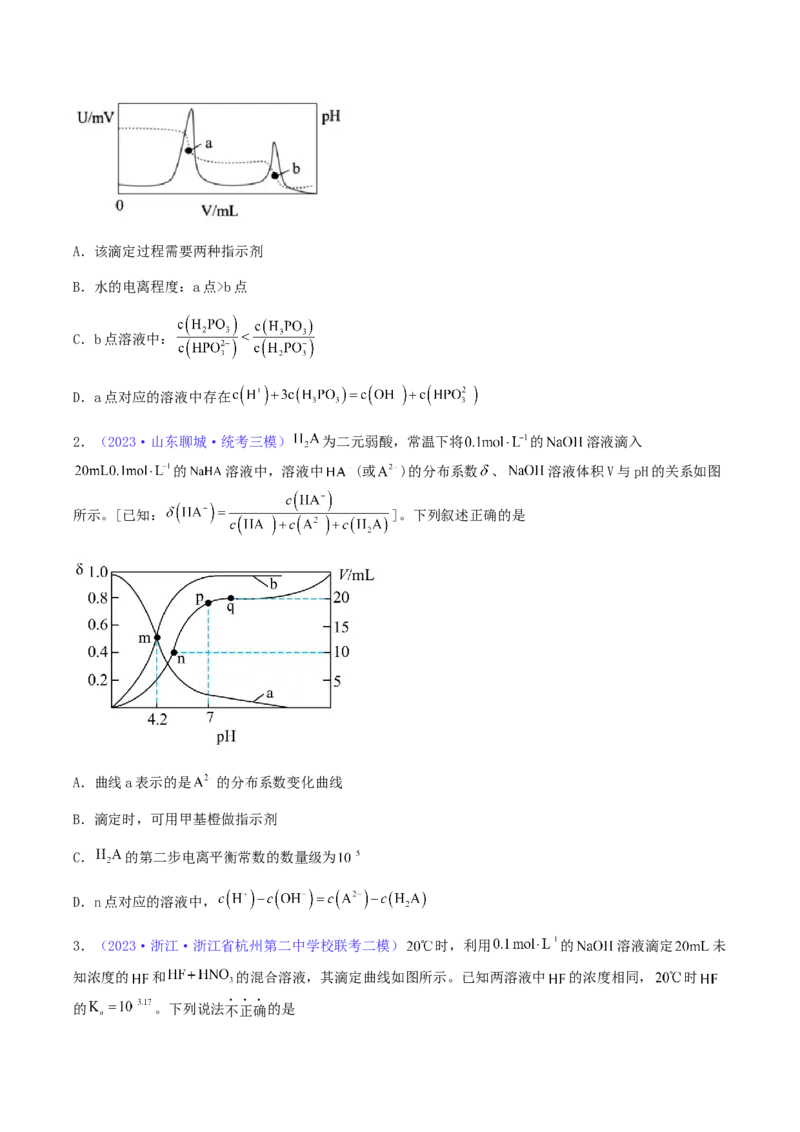
6.(2023·黑龙江齐齐哈尔·统考二模)如图为室温下某二元碱溶液中M(OH)、M(OH)+、M2+的浓度(mol·
2
L-1)对数lgc随pOH[- lg c(OH- )]的变化关系。下列说法正确的是
A.该二元碱的浓度为0. 10 mol/L
B.pOH=8.0时,lg c(M2+ )-lg c[M(OH)+]= 1. 55
C.当c(M2+ )=c[M(OH)+ ]时,pH=6.45
D.pH=7时,lg c(M2+ )- lg c[M(OH)]=8.35
2
考点三 酸碱中和滴定及其应用
1.(2023·辽宁丹东·统考二模)电位滴定法是化学中常用的分析方法,可根据滴定过程中电极电位的
突跃确定滴定终点。常温下利用盐酸滴定某溶液中亚磷酸钠 的含量,其电位滴定曲线与 曲
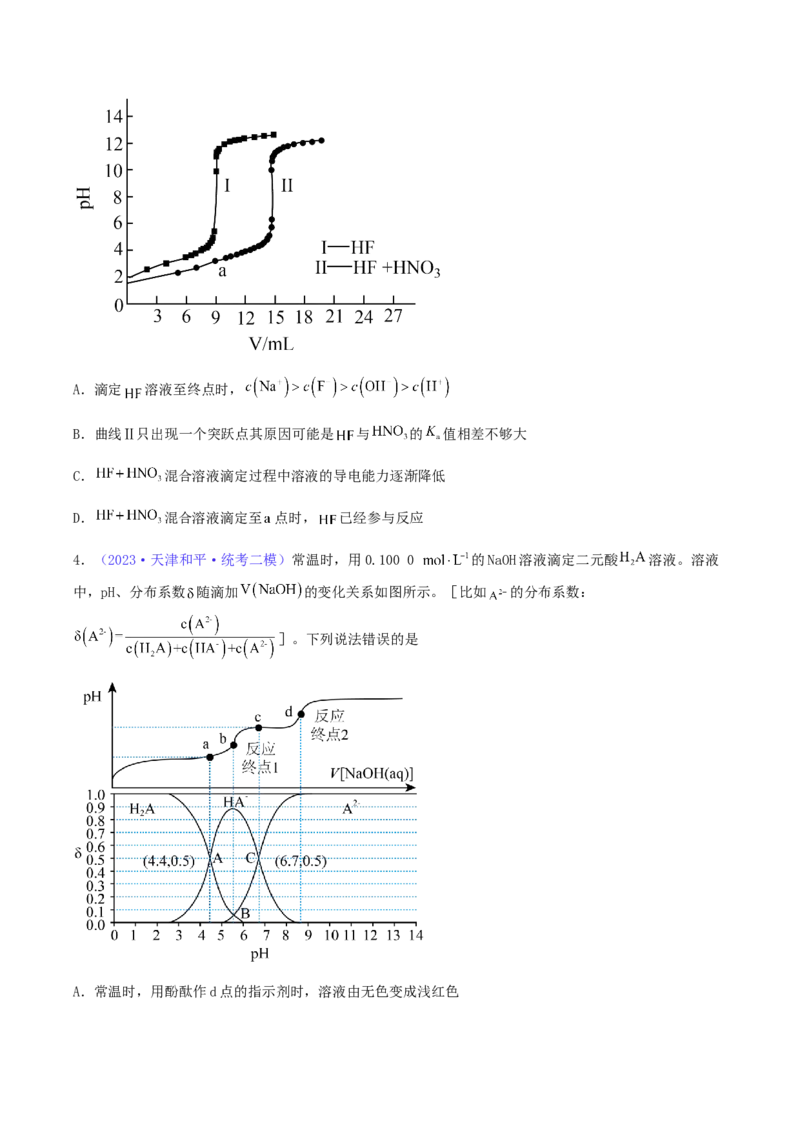
线如图所示。已知:亚磷酸 是二元弱酸,电离常数 ,下列说法正确的是A.该滴定过程需要两种指示剂
B.水的电离程度:a点>b点
C.b点溶液中:
D.a点对应的溶液中存在
2.(2023·山东聊城·统考三模) 为二元弱酸,常温下将 的 溶液滴入
的 溶液中,溶液中 (或 )的分布系数 、 溶液体积V与pH的关系如图
所示。[已知: ]。下列叙述正确的是
A.曲线a表示的是 的分布系数变化曲线
B.滴定时,可用甲基橙做指示剂
C. 的第二步电离平衡常数的数量级为
D.n点对应的溶液中,
3.(2023·浙江·浙江省杭州第二中学校联考二模) 时,利用 的 溶液滴定 未
知浓度的 和 的混合溶液,其滴定曲线如图所示。已知两溶液中 的浓度相同, 时
的 。下列说法不正确的是A.滴定 溶液至终点时,
B.曲线Ⅱ只出现一个突跃点其原因可能是 与 的 值相差不够大
C. 混合溶液滴定过程中溶液的导电能力逐渐降低
D. 混合溶液滴定至 点时, 已经参与反应
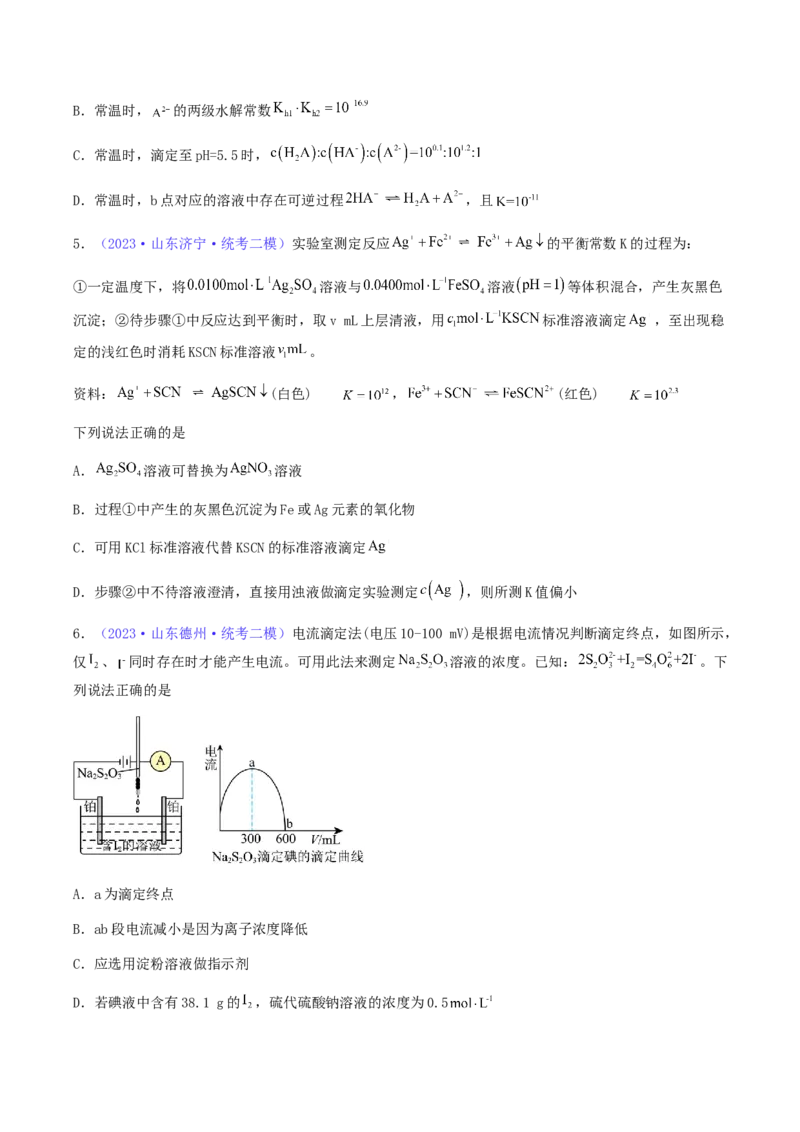
4.(2023·天津和平·统考二模)常温时,用0.100 0 的NaOH溶液滴定二元酸 溶液。溶液
中,pH、分布系数 随滴加 的变化关系如图所示。[比如 的分布系数:
]。下列说法错误的是
A.常温时,用酚酞作d点的指示剂时,溶液由无色变成浅红色B.常温时, 的两级水解常数
C.常温时,滴定至pH=5.5时,
D.常温时,b点对应的溶液中存在可逆过程 ,且
5.(2023·山东济宁·统考二模)实验室测定反应 的平衡常数K的过程为:
①一定温度下,将 溶液与 溶液 等体积混合,产生灰黑色
沉淀;②待步骤①中反应达到平衡时,取v mL上层清液,用 标准溶液滴定 ,至出现稳
定的浅红色时消耗KSCN标准溶液 。
资料: (白色) , (红色)
下列说法正确的是
A. 溶液可替换为 溶液
B.过程①中产生的灰黑色沉淀为Fe或Ag元素的氧化物
C.可用KCl标准溶液代替KSCN的标准溶液滴定
D.步骤②中不待溶液澄清,直接用浊液做滴定实验测定 ,则所测K值偏小
6.(2023·山东德州·统考二模)电流滴定法(电压10-100 mV)是根据电流情况判断滴定终点,如图所示,
仅 、 同时存在时才能产生电流。可用此法来测定 溶液的浓度。已知: 。下
列说法正确的是
A.a为滴定终点
B.ab段电流减小是因为离子浓度降低
C.应选用淀粉溶液做指示剂
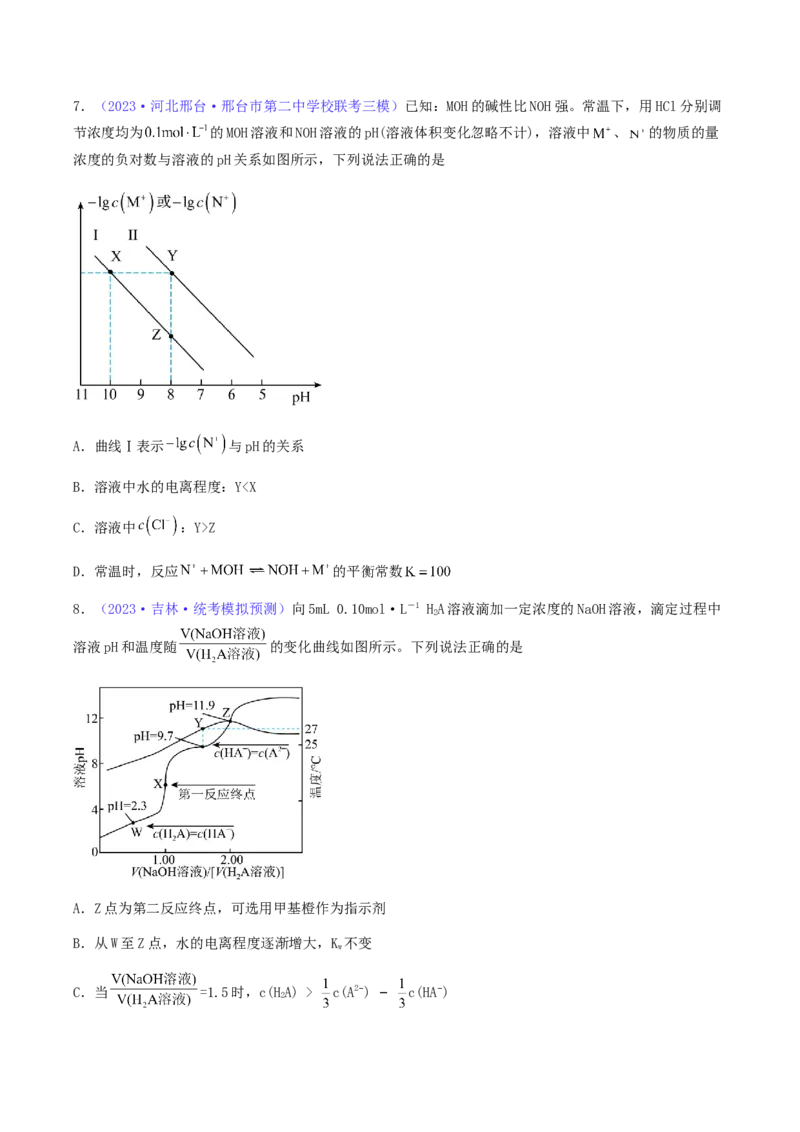
D.若碘液中含有38.1 g的 ,硫代硫酸钠溶液的浓度为0.57.(2023·河北邢台·邢台市第二中学校联考三模)已知:MOH的碱性比NOH强。常温下,用HCl分别调
节浓度均为 的MOH溶液和NOH溶液的pH(溶液体积变化忽略不计),溶液中 、 的物质的量
浓度的负对数与溶液的pH关系如图所示,下列说法正确的是
A.曲线Ⅰ表示 与pH的关系
B.溶液中水的电离程度:YZ
D.常温时,反应 的平衡常数
8.(2023·吉林·统考模拟预测)向5mL 0.10mol·L-1 HA溶液滴加一定浓度的NaOH溶液,滴定过程中
2
溶液pH和温度随 的变化曲线如图所示。下列说法正确的是
A.Z点为第二反应终点,可选用甲基橙作为指示剂
B.从W至Z点,水的电离程度逐渐增大,K 不变
w
C.当 =1.5时,c(HA) > c(A2−) − c(HA−)
2D.25 ℃时,HA的电离常数K =10-2.3,K =10-9.7
2 a1 a2