文档内容
表格型实验方案的评价
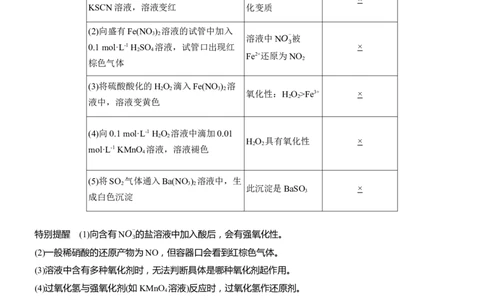
1.氧化性、还原性强弱探究
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)将Fe(NO ) 样品溶于稀硫酸,滴加 Fe(NO ) 晶体已氧
3 2 3 2
×
KSCN溶液,溶液变红 化变质
(2)向盛有Fe(NO ) 溶液的试管中加入
3 2 溶液中NO-
被
3
0.1 mol·L-1 H SO 溶液,试管口出现红 ×
2 4
Fe2+还原为NO
2
棕色气体
(3)将硫酸酸化的H O 滴入Fe(NO ) 溶
2 2 3 2
氧化性:H O >Fe3+ ×
2 2
液中,溶液变黄色
(4)向0.1 mol·L-1 H O 溶液中滴加0.01
2 2
H O 具有氧化性 ×
2 2
mol·L-1 KMnO 溶液,溶液褪色
4
(5)将SO 气体通入Ba(NO ) 溶液中,生
2 3 2
此沉淀是BaSO ×
3
成白色沉淀
特别提醒
(1)向含有NO-
的盐溶液中加入酸后,会有强氧化性。
3
(2)一般稀硝酸的还原产物为NO,但容器口会看到红棕色气体。
(3)溶液中含有多种氧化剂时,无法判断具体是哪种氧化剂起作用。
(4)过氧化氢与强氧化剂(如KMnO 溶液)反应时,过氧化氢作还原剂。
4
2.电解质强弱探究
判断(填
探究方案 探究目的
“√”或“×”)
(1)室温下,用pH计测量醋酸溶液、盐酸
CH COOH是弱电解质 ×
3
的pH,比较溶液pH大小
(2)室温下,用pH试纸测得CH COONa HNO 2 电离出H+的能力比
3 ×
溶液的pH约为9,NaNO 溶液的pH约 CH 3 COOH强
2为8
特别提醒 应比较同温度、同浓度、同类型的电解质。
3.通过现象判断酸性强弱
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)向Na CO 溶液中加入冰醋酸,将产生的气 酸性:醋酸>碳
2 3
×
体直接通入苯酚钠溶液中,溶液变浑浊 酸>苯酚
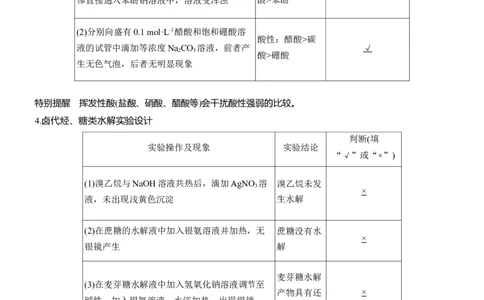
(2)分别向盛有0.1 mol·L-1醋酸和饱和硼酸溶
酸性:醋酸>碳
液的试管中滴加等浓度Na CO 溶液,前者产 √
2 3
酸>硼酸
生无色气泡,后者无明显现象
特别提醒 挥发性酸(盐酸、硝酸、醋酸等)会干扰酸性强弱的比较。
4.卤代烃、糖类水解实验设计
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)溴乙烷与NaOH溶液共热后,滴加AgNO 溶 溴乙烷未发
3
×
液,未出现浅黄色沉淀 生水解
(2)在蔗糖的水解液中加入银氨溶液并加热,无 蔗糖没有水
×
银镜产生 解
麦芽糖水解
(3)在麦芽糖水解液中加入氢氧化钠溶液调节至
产物具有还 ×
碱性,加入银氨溶液,水浴加热,出现银镜
原性
特别提醒 ①水解液要先中和,后加检验试剂。②麦芽糖水解时,由于麦芽糖自身具有还原性,故无法根
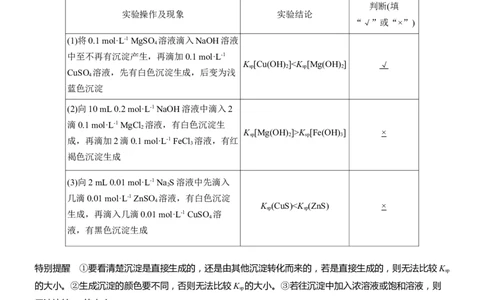
据是否有银镜(或砖红色沉淀)产生来判断麦芽糖是否水解。5.有关K 的判断
sp
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)将0.1 mol·L-1 MgSO 溶液滴入NaOH溶液
4
中至不再有沉淀产生,再滴加0.1 mol·L-1
K [Cu(OH) ]K [Fe(OH) ] ×
sp 2 sp 3
成,再滴加2滴0.1 mol·L-1 FeCl 溶液,有红
3
褐色沉淀生成
(3)向2 mL 0.01 mol·L-1 Na S溶液中先滴入
2
几滴0.01 mol·L-1 ZnSO 溶液,有白色沉淀
4
K (CuS)K(C H OH)
a1 2 3 a 6 5
气体
光洁的铜丝灼烧后,趁热插 铜丝由黑色变
C 乙醇具有氧化性
入2 mL乙醇中 为红色
向CH COOH溶液中加入
3
D CH COONH 固体,测量溶液 pH变大 CH COONH 溶液呈碱性
3 4 3 4
pH变化
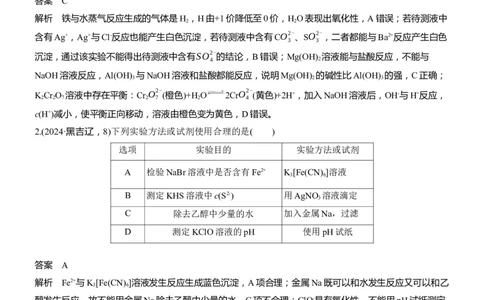
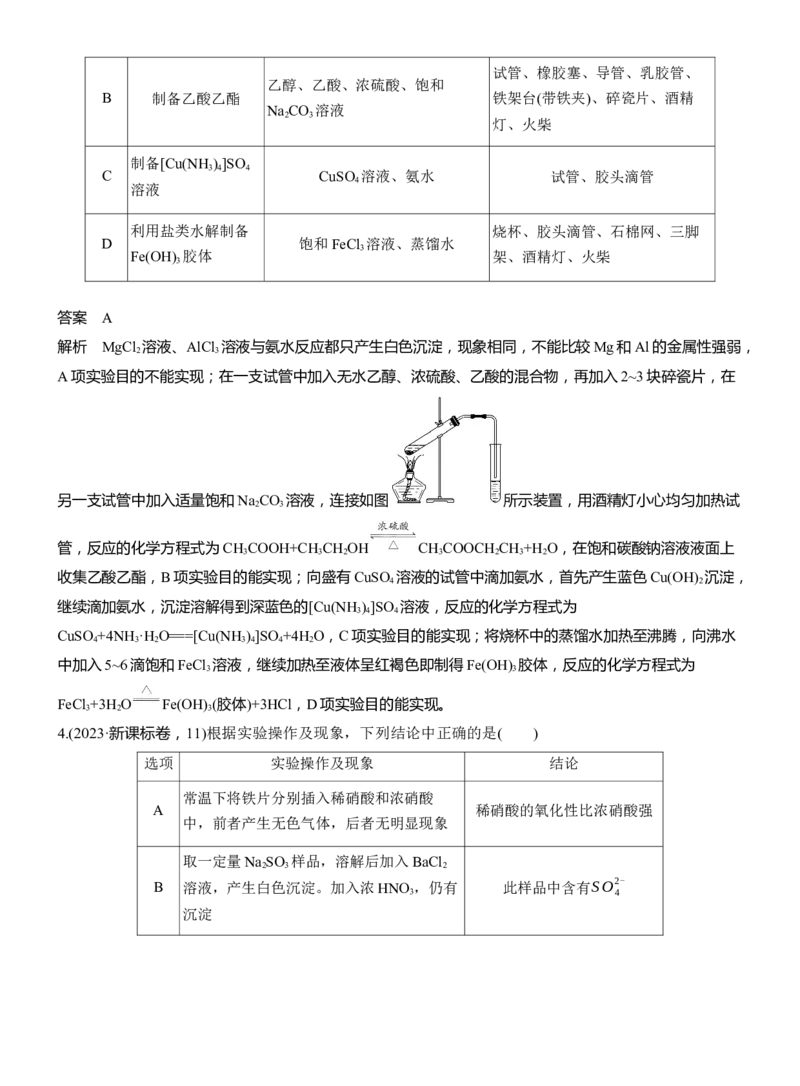
答案 B解析 溴乙烷不能电离出Br-,与硝酸银溶液不反应,溶液分层,上层为无色溶液,A错误;铜与氧气反应
生成氧化铜,氧化铜可氧化乙醇生成乙醛,则乙醇具有还原性,C错误;CH COONH 溶液为中性,
3 4
CH COONH 固体溶于水电离出的醋酸根离子可抑制醋酸的电离,溶液的pH变大,D错误。
3 4
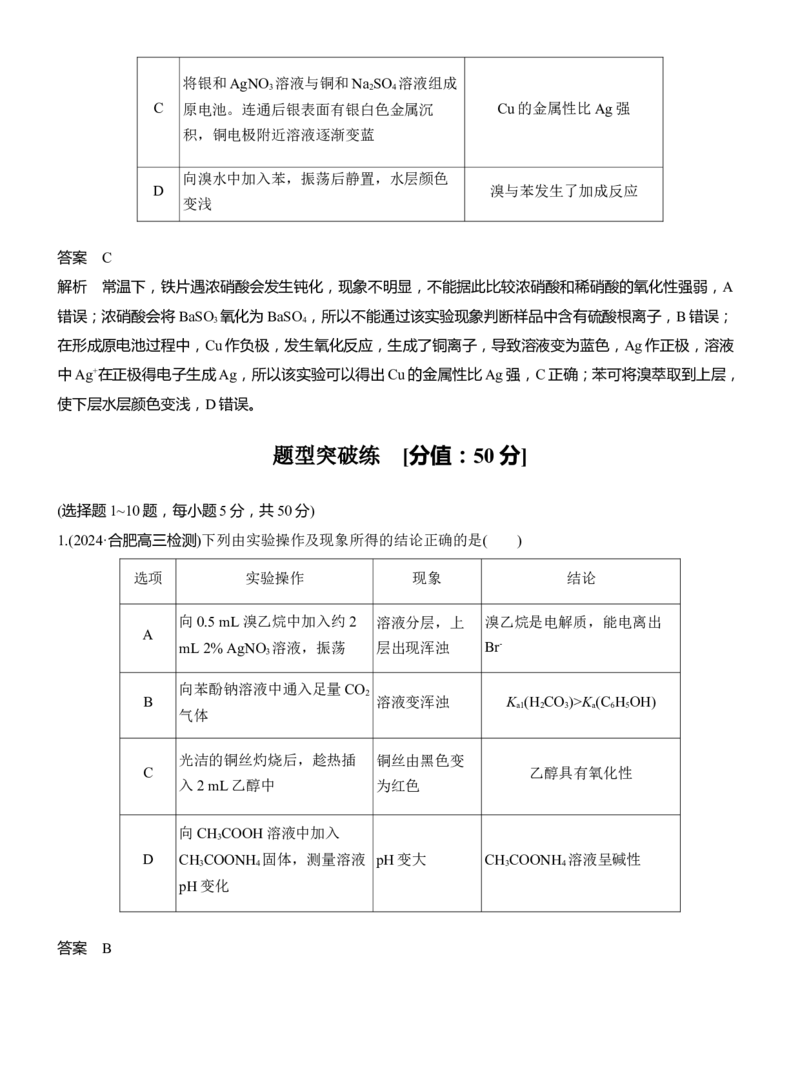
2.(2024·安徽江淮十校联考)下列实验操作、现象均正确,且能得到相应实验结论的是( )
选项 实验操作 实验现象 实验结论
向0.1 mol·L-1 HI溶液中滴加几滴淀粉溶
A 溶液出现蓝色 氧化性:Fe3+>I
2
液,再滴加几滴0.1 mol·L-1 Fe(NO ) 溶液
3 3
B 将Ag O分别加入浓氨水和稀硝酸中 Ag O均溶解 Ag O属于两性氧化物
2 2 2
向蔗糖溶液中加入稀硫酸并加热一段时
C 无银镜产生 蔗糖未水解
间,然后滴加银氨溶液
向浓度均为0.1 mol·L-1的MgSO 和CuSO
4 4
先观察到有蓝色
D 的混合溶液中逐滴加入0.01 mol·L-1的 K [Cu(OH) ]K sp [Cu(OH) 2 ]
2浓度的CuSO 溶液,先生成白色沉淀,后生成
4
蓝色沉淀
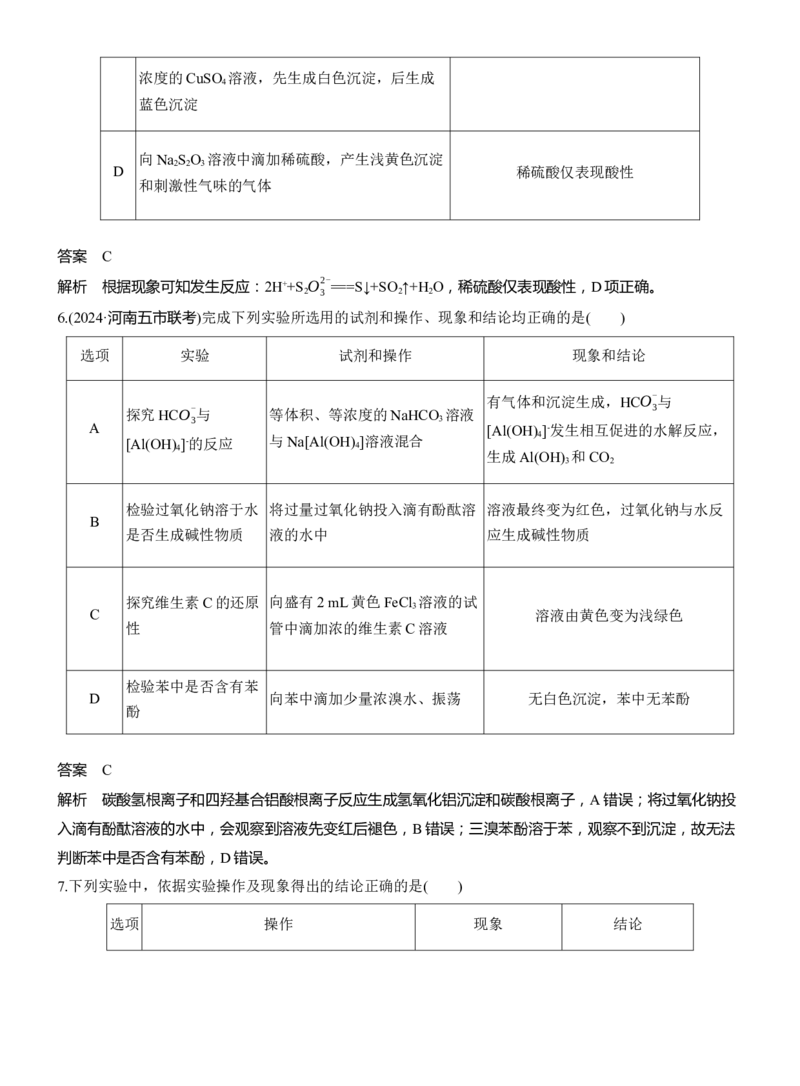
向Na S O 溶液中滴加稀硫酸,产生浅黄色沉淀
2 2 3
D 稀硫酸仅表现酸性
和刺激性气味的气体
答案 C
解析 根据现象可知发生反应:2H++S
O2-
===S↓+SO ↑+H O,稀硫酸仅表现酸性,D项正确。
2 3 2 2
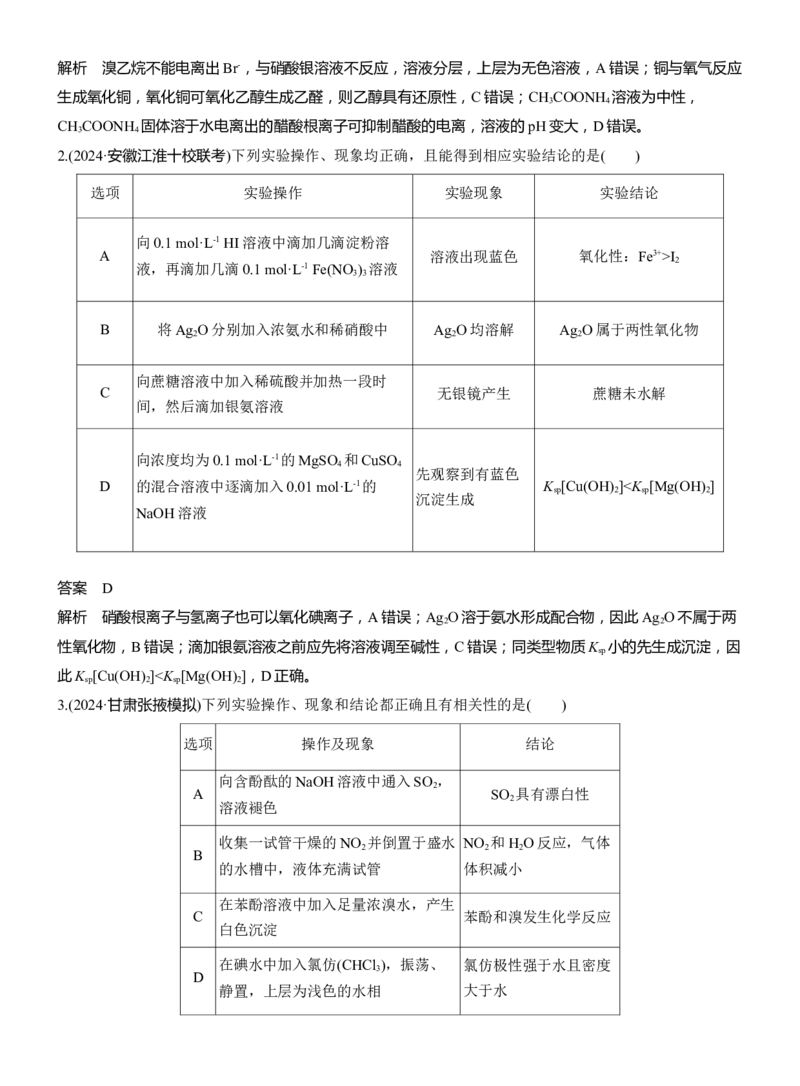
6.(2024·河南五市联考)完成下列实验所选用的试剂和操作、现象和结论均正确的是( )
选项 实验 试剂和操作 现象和结论
有气体和沉淀生成,HCO-
与
探究HCO-
与 等体积、等浓度的NaHCO 溶液
3
3 3
A [Al(OH) ]-发生相互促进的水解反应,
[Al(OH) 4 ]-的反应 与Na[Al(OH) 4 ]溶液混合 4
生成Al(OH) 和CO
3 2
检验过氧化钠溶于水 将过量过氧化钠投入滴有酚酞溶 溶液最终变为红色,过氧化钠与水反
B
是否生成碱性物质 液的水中 应生成碱性物质
探究维生素C的还原 向盛有2 mL黄色FeCl 溶液的试
3
C 溶液由黄色变为浅绿色
性 管中滴加浓的维生素C溶液
检验苯中是否含有苯
D 向苯中滴加少量浓溴水、振荡 无白色沉淀,苯中无苯酚
酚
答案 C
解析 碳酸氢根离子和四羟基合铝酸根离子反应生成氢氧化铝沉淀和碳酸根离子,A错误;将过氧化钠投
入滴有酚酞溶液的水中,会观察到溶液先变红后褪色,B错误;三溴苯酚溶于苯,观察不到沉淀,故无法
判断苯中是否含有苯酚,D错误。
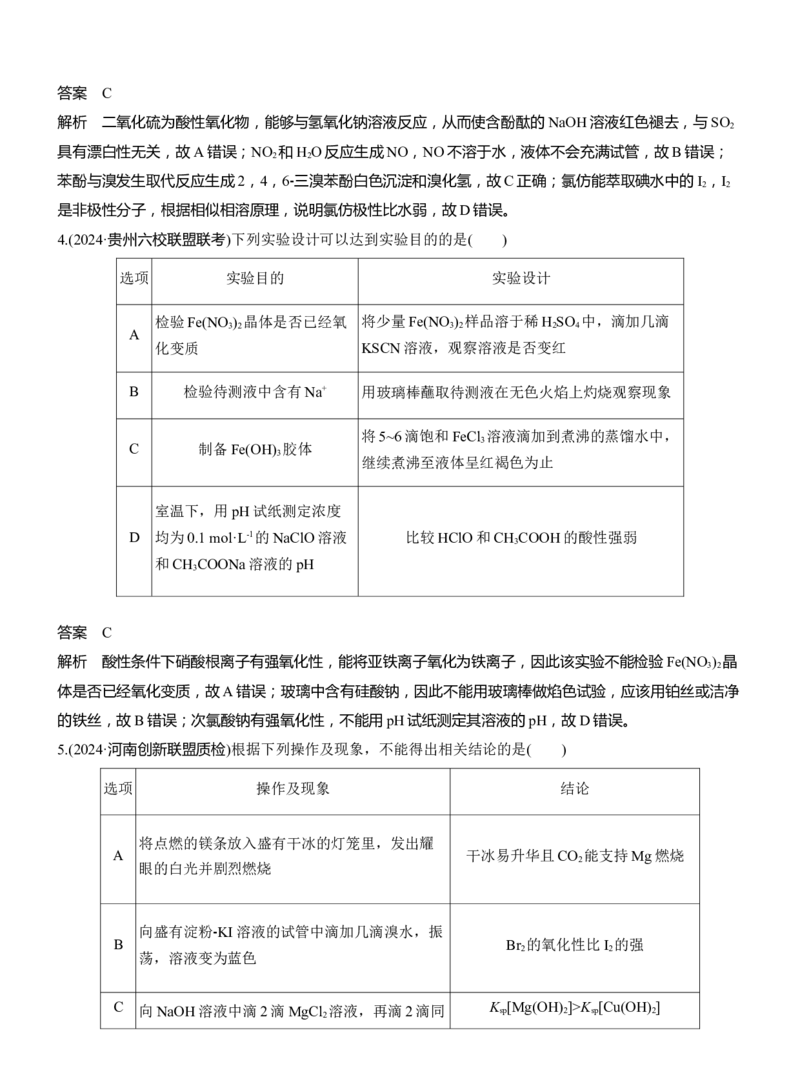
7.下列实验中,依据实验操作及现象得出的结论正确的是( )
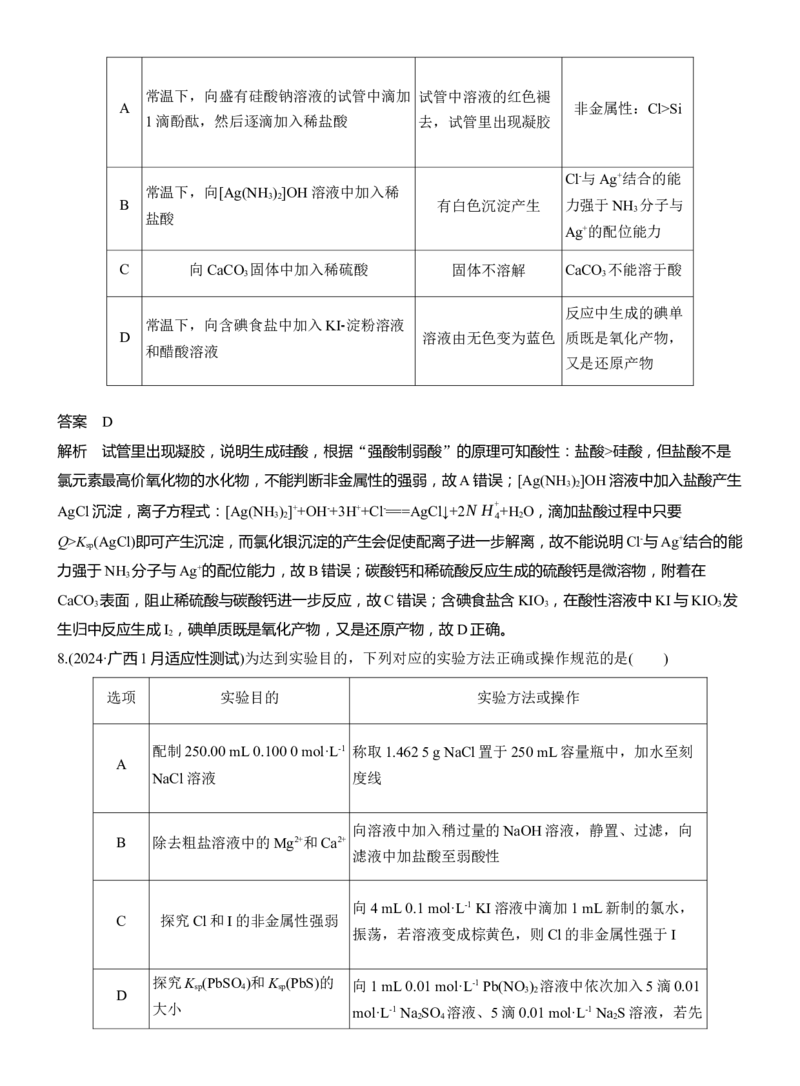
选项 操作 现象 结论常温下,向盛有硅酸钠溶液的试管中滴加 试管中溶液的红色褪
A 非金属性:Cl>Si
1滴酚酞,然后逐滴加入稀盐酸 去,试管里出现凝胶
Cl-与Ag+结合的能
常温下,向[Ag(NH ) ]OH溶液中加入稀
3 2
B 有白色沉淀产生 力强于NH 分子与
3
盐酸
Ag+的配位能力
C 向CaCO 固体中加入稀硫酸 固体不溶解 CaCO 不能溶于酸
3 3
反应中生成的碘单
常温下,向含碘食盐中加入KI⁃ 淀粉溶液
D 溶液由无色变为蓝色 质既是氧化产物,
和醋酸溶液
又是还原产物
答案 D
解析 试管里出现凝胶,说明生成硅酸,根据“强酸制弱酸”的原理可知酸性:盐酸>硅酸,但盐酸不是
氯元素最高价氧化物的水化物,不能判断非金属性的强弱,故A错误;[Ag(NH ) ]OH溶液中加入盐酸产生
3 2
AgCl沉淀,离子方程式:[Ag(NH ) ]++OH-+3H++Cl-===AgCl↓+2N H+ +H O,滴加盐酸过程中只要
3 2 4 2
Q>K (AgCl)即可产生沉淀,而氯化银沉淀的产生会促使配离子进一步解离,故不能说明Cl-与Ag+结合的能
sp
力强于NH 分子与Ag+的配位能力,故B错误;碳酸钙和稀硫酸反应生成的硫酸钙是微溶物,附着在
3
CaCO 表面,阻止稀硫酸与碳酸钙进一步反应,故C错误;含碘食盐含KIO ,在酸性溶液中KI与KIO 发
3 3 3
生归中反应生成I ,碘单质既是氧化产物,又是还原产物,故D正确。
2
8.(2024·广西1月适应性测试)为达到实验目的,下列对应的实验方法正确或操作规范的是( )
选项 实验目的 实验方法或操作
配制250.00 mL 0.100 0 mol·L-1 称取1.462 5 g NaCl置于250 mL容量瓶中,加水至刻
A
NaCl溶液 度线
向溶液中加入稍过量的NaOH溶液,静置、过滤,向
B 除去粗盐溶液中的Mg2+和Ca2+
滤液中加盐酸至弱酸性
向4 mL 0.1 mol·L-1 KI溶液中滴加1 mL新制的氯水,
C 探究Cl和I的非金属性强弱
振荡,若溶液变成棕黄色,则Cl的非金属性强于I
D 探究K sp (PbSO 4 )和K sp (PbS)的 向1 mL 0.01 mol·L-1 Pb(NO 3 ) 2 溶液中依次加入5滴0.01
大小 mol·L-1 Na SO 溶液、5滴0.01 mol·L-1 Na S溶液,若先
2 4 2观察到白色沉淀再观察到黑色沉淀,则
K (PbSO )>K (PbS)
sp 4 sp
答案 C
解析 配制250.00 mL 0.100 0 mol·L-1NaCl溶液时,称取的氯化钠固体应先在烧杯中溶解,再转移至容量瓶
中定容,A错误;向溶液中加入稍过量的NaOH溶液,除去粗盐溶液中的Mg2+,还需向溶液中加入
Na CO 溶液除去Ca2+,过滤后再向滤液中加入适量盐酸除去过量的NaOH和Na CO ,B错误;向1 mL
2 3 2 3
0.01 mol·L-1 Pb(NO ) 溶液中依次加入5滴0.01 mol·L-1 Na SO 溶液、5滴0.01 mol·L-1Na S溶液,Pb(NO )
3 2 2 4 2 3 2
过量,若先观察到白色沉淀PbSO ,再观察到黑色沉淀PbS,则不能确定发生了沉淀转化,无法得到
4
K (PbSO )>K (PbS),D错误。
sp 4 sp
9.(2024·河北沧州模拟)下列实验操作、现象及得出的结论均正确的是( )
选项 实验操作、现象 实验结论
0.1 mol·L-1的NaHCO 溶液与0.1 mol·L-1的
A 3 结合H+能力:[Al(OH) ]->CO2-
4 3
Na[Al(OH) ]溶液等体积混合,产生白色沉淀
4
将补铁口服液(含维生素C)滴入酸性KMnO 溶液,
4
B 补铁口服液中含有Fe2+
紫红色褪去
C 将久置的Na O 加入稀盐酸中,产生气泡 Na O 已经变质
2 2 2 2
取两份新制氯水,分别滴加AgNO
3
溶液和淀粉 ⁃KI溶
D 氯气与水的反应存在限度
液,前者有白色沉淀,后者溶液变蓝
答案 A
解析 等物质的量浓度、等体积的NaHCO 溶液与Na[Al(OH) ]溶液混合,产生白色沉淀,发生反应:
3 4
[Al(OH) ]-+HCO- ===Al(OH) ↓+CO2- +H O,说明结合H+能力:[Al(OH) ]->CO2- ,A正确;维生素C也能
4 3 3 3 2 4 3
使酸性KMnO 溶液褪色,B错误;盐酸可与Na O 反应,反应的化学方程式为
4 2 2
2Na O +4HCl===4NaCl+2H O+O ↑,C错误;新制氯水中的Cl 和HClO都能与KI反应生成使淀粉变蓝色
2 2 2 2 2
的碘,则溶液变蓝色不能说明溶液中存在氯气分子,无法证明氯气与水的反应存在限度,D错误。
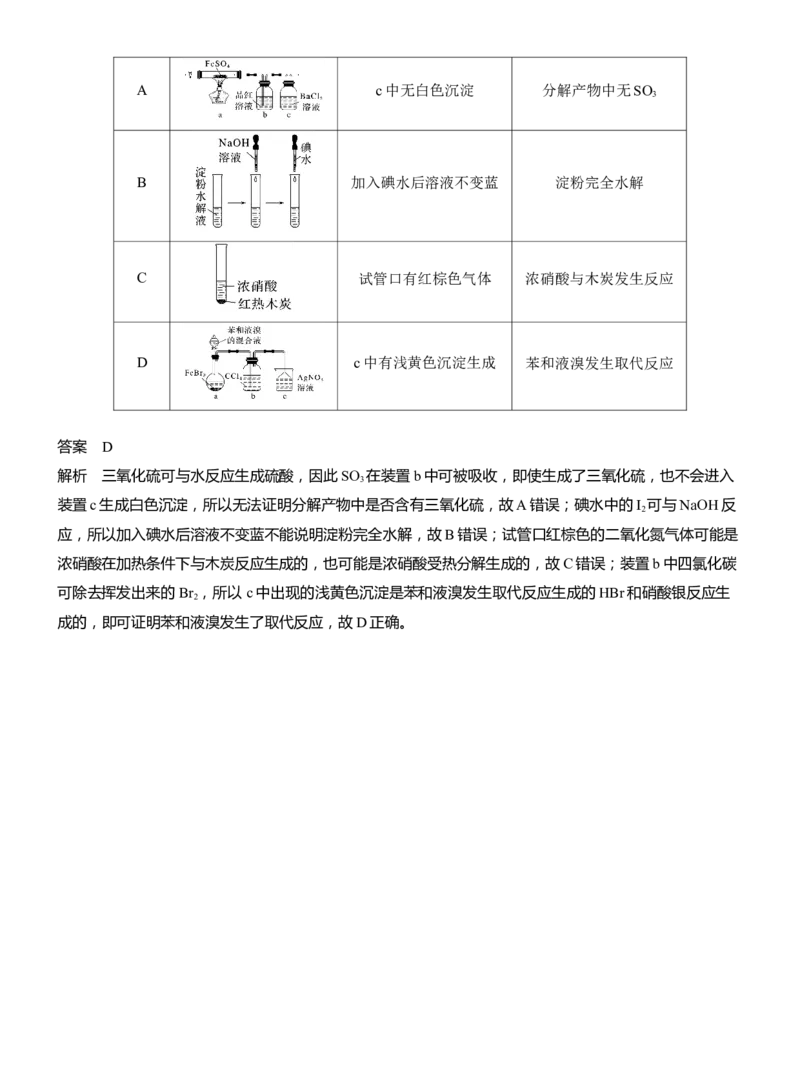
10.(2024·福建漳州高三检测)下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论A c中无白色沉淀 分解产物中无SO
3
B 加入碘水后溶液不变蓝 淀粉完全水解
C 试管口有红棕色气体 浓硝酸与木炭发生反应
D c中有浅黄色沉淀生成 苯和液溴发生取代反应
答案 D
解析 三氧化硫可与水反应生成硫酸,因此SO 在装置b中可被吸收,即使生成了三氧化硫,也不会进入
3
装置c生成白色沉淀,所以无法证明分解产物中是否含有三氧化硫,故A错误;碘水中的I 可与NaOH反
2
应,所以加入碘水后溶液不变蓝不能说明淀粉完全水解,故B错误;试管口红棕色的二氧化氮气体可能是
浓硝酸在加热条件下与木炭反应生成的,也可能是浓硝酸受热分解生成的,故C错误;装置b中四氯化碳
可除去挥发出来的Br ,所以 c中出现的浅黄色沉淀是苯和液溴发生取代反应生成的HBr和硝酸银反应生
2
成的,即可证明苯和液溴发生了取代反应,故D正确。