文档内容
无机化工微流程
1.题型特点
(1)核心元素转化过程中条件控制、定性及定量关系判断。
(2)过渡金属元素价态变化特点、形成氢氧化物沉淀的条件、形成配合物的性质等。
(3)物质分离提纯中涉及仪器使用、操作注意事项的判断等。
(4)绿色化学思想的考查,主要是废物的再利用、循环物质的判断等。
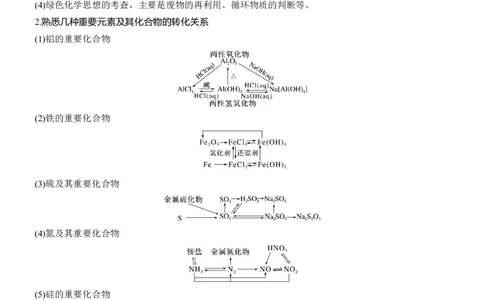
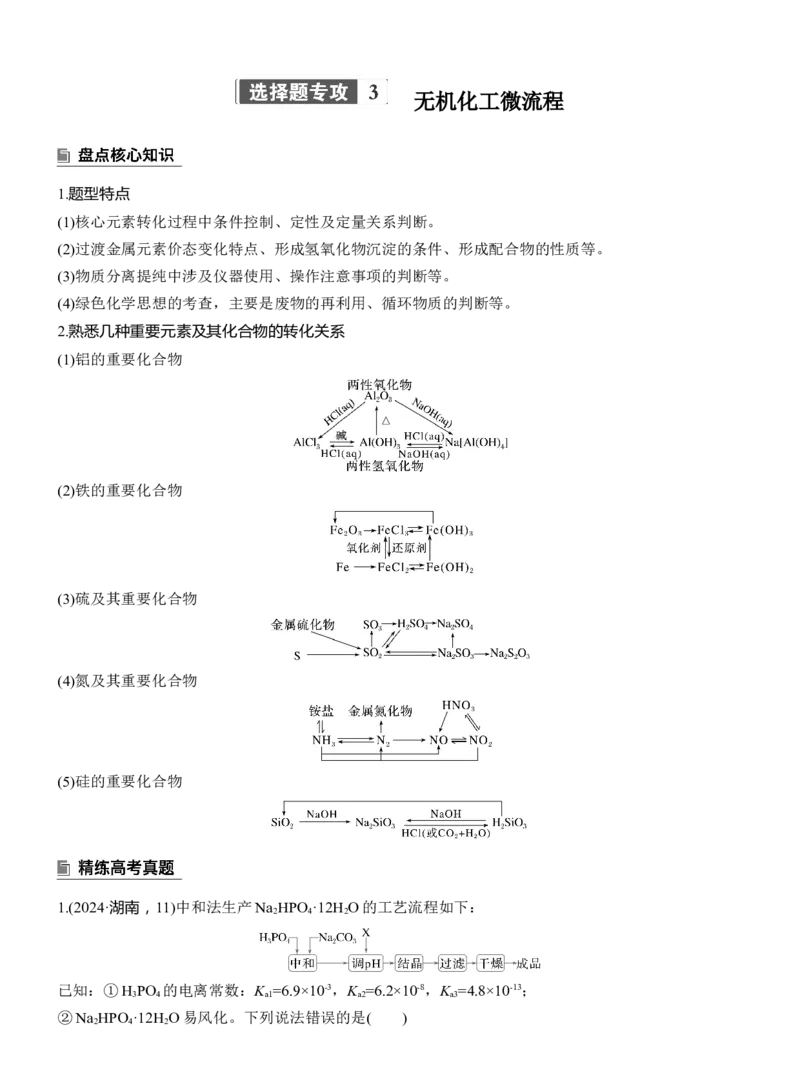
2.熟悉几种重要元素及其化合物的转化关系
(1)铝的重要化合物
(2)铁的重要化合物
(3)硫及其重要化合物
(4)氮及其重要化合物
(5)硅的重要化合物
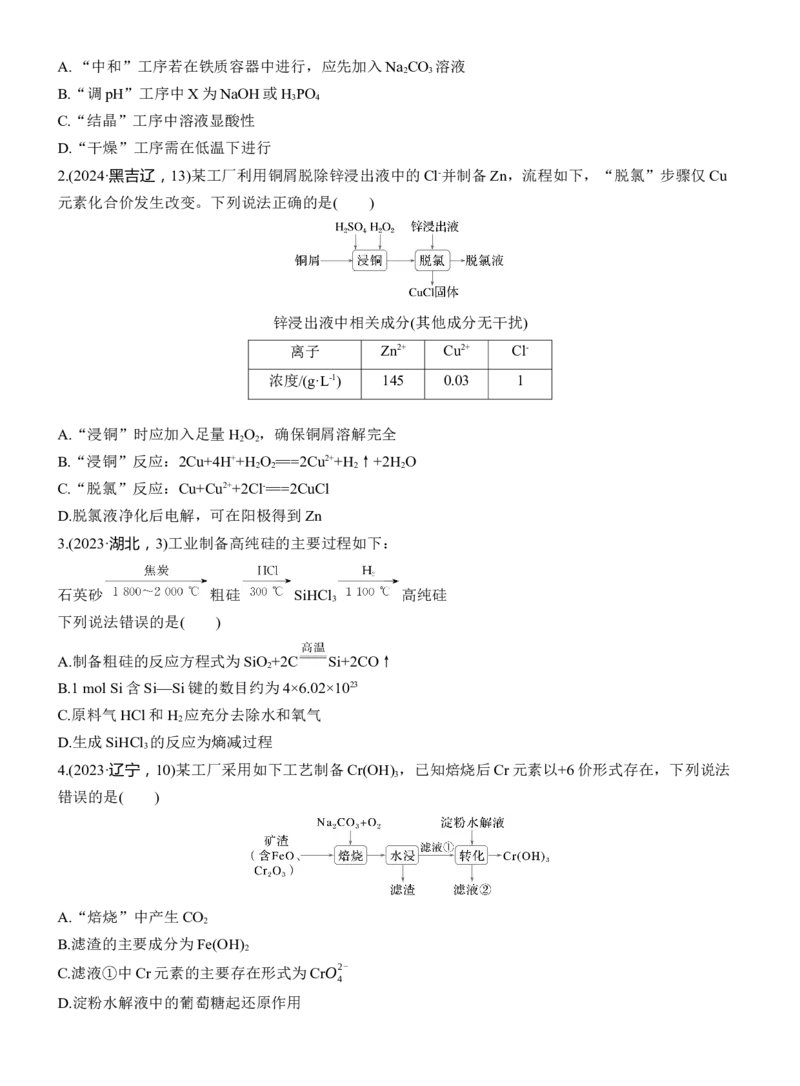
1.(2024·湖南,11)中和法生产Na HPO ·12H O的工艺流程如下:
2 4 2
已知:①H PO 的电离常数:K =6.9×10-3,K =6.2×10-8,K =4.8×10-13;
3 4 a1 a2 a3
②Na HPO ·12H O易风化。下列说法错误的是( )
2 4 2A. “中和”工序若在铁质容器中进行,应先加入Na CO 溶液
2 3
B.“调pH”工序中X为NaOH或H PO
3 4
C.“结晶”工序中溶液显酸性
D.“干燥”工序需在低温下进行
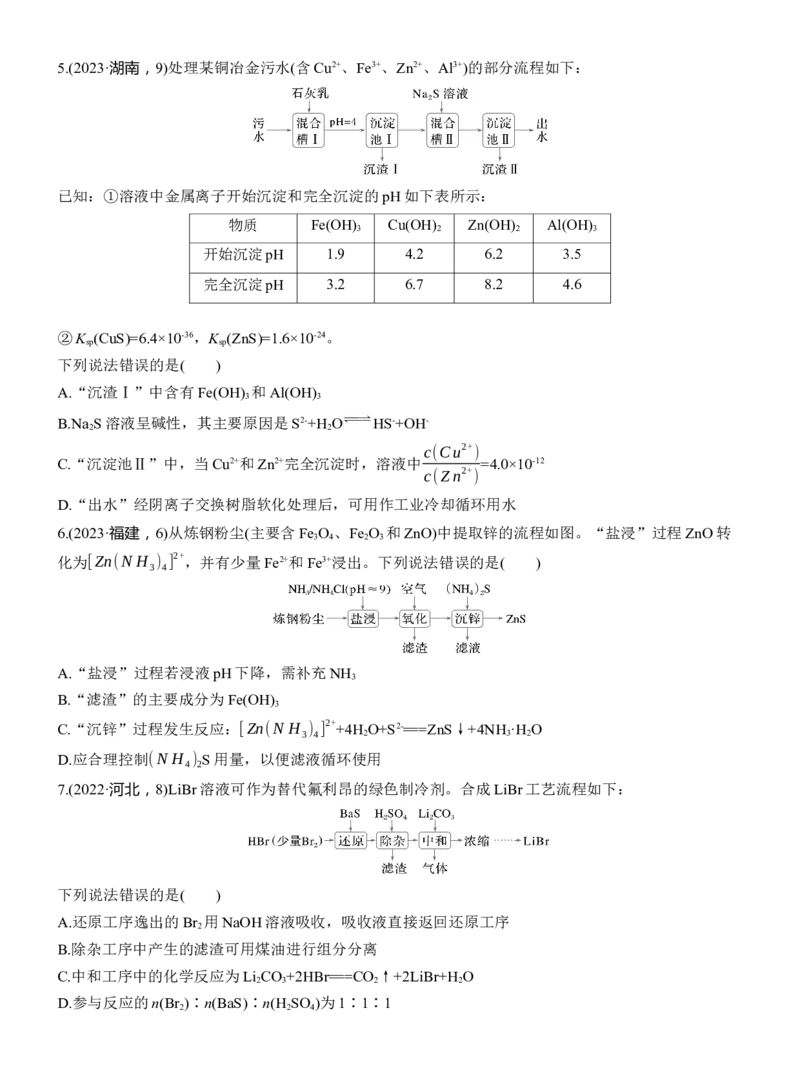
2.(2024·黑吉辽,13)某工厂利用铜屑脱除锌浸出液中的Cl-并制备Zn,流程如下,“脱氯”步骤仅Cu
元素化合价发生改变。下列说法正确的是( )
锌浸出液中相关成分(其他成分无干扰)
离子 Zn2+ Cu2+ Cl-
浓度/(g·L-1) 145 0.03 1
A.“浸铜”时应加入足量H O ,确保铜屑溶解完全
2 2
B.“浸铜”反应:2Cu+4H++H O ===2Cu2++H ↑+2H O
2 2 2 2
C.“脱氯”反应:Cu+Cu2++2Cl-===2CuCl
D.脱氯液净化后电解,可在阳极得到Zn
3.(2023·湖北,3)工业制备高纯硅的主要过程如下:
石英砂 粗硅 SiHCl 高纯硅
3
下列说法错误的是( )
A.制备粗硅的反应方程式为SiO +2C Si+2CO↑
2
B.1 mol Si含Si—Si键的数目约为4×6.02×1023
C.原料气HCl和H 应充分去除水和氧气
2
D.生成SiHCl 的反应为熵减过程
3
4.(2023·辽宁,10)某工厂采用如下工艺制备Cr(OH) ,已知焙烧后Cr元素以+6价形式存在,下列说法
3
错误的是( )
A.“焙烧”中产生CO
2
B.滤渣的主要成分为Fe(OH)
2
C.滤液①中Cr元素的主要存在形式为CrO2-
4
D.淀粉水解液中的葡萄糖起还原作用5.(2023·湖南,9)处理某铜冶金污水(含Cu2+、Fe3+、Zn2+、Al3+)的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
物质 Fe(OH) Cu(OH) Zn(OH) Al(OH)
3 2 2 3
开始沉淀pH 1.9 4.2 6.2 3.5
完全沉淀pH 3.2 6.7 8.2 4.6
②K (CuS)=6.4×10-36,K (ZnS)=1.6×10-24。
sp sp
下列说法错误的是( )
A.“沉渣Ⅰ”中含有Fe(OH) 和Al(OH)
3 3
B.Na S溶液呈碱性,其主要原因是S2-+H O HS-+OH-
2 2
c(Cu2+
)
C.“沉淀池Ⅱ”中,当Cu2+和Zn2+完全沉淀时,溶液中 =4.0×10-12
c(Zn2+
)
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
6.(2023·福建,6)从炼钢粉尘(主要含Fe O 、Fe O 和ZnO)中提取锌的流程如图。“盐浸”过程ZnO转
3 4 2 3
化为[Zn(N H ) ] 2+ ,并有少量Fe2+和Fe3+浸出。下列说法错误的是( )
3 4
A.“盐浸”过程若浸液pH下降,需补充NH
3
B.“滤渣”的主要成分为Fe(OH)
3
C.“沉锌”过程发生反应:[Zn(N H ) ] 2+ +4H O+S2-===ZnS↓+4NH ·H O
3 4 2 3 2
D.应合理控制(N H ) S用量,以便滤液循环使用
4 2
7.(2022·河北,8)LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为Li CO +2HBr===CO ↑+2LiBr+H O
2 3 2 2
D.参与反应的n(Br )∶n(BaS)∶n(H SO )为1∶1∶1
2 2 4答案精析
精练高考真题
1.C [铁是较活泼金属,可与H PO 反应生成氢气,故“中和”工序若在铁质容器中进行,应先加入
3 4
Na CO 溶液,A正确;若“中和”工序加入的Na CO 过量,则需要加入酸性物质来调节pH,为了不引入
2 3 2 3
新杂质,可加入H PO ;若“中和”工序加入H PO 过量,则需要加入碱性物质来调节pH,为了不引入新
3 4 3 4
K
杂质,可加入NaOH,B正确;“结晶”工序中的溶液为饱和Na HPO 溶液,HPO2- 的水解常数K = w =
2 4 4 h K
a2
1.0×10-14
≈1.6×10-7>K ,Na HPO 的水解程度大于其电离程度,溶液显碱性,C错误;由于
6.2×10-8 a3 2 4
Na HPO ·12H O易风化失去结晶水,故“干燥”工序需要在低温下进行,D正确。]
2 4 2
2.C [“浸铜”步骤中,铜屑不能溶解完全,Cu在“脱氯”步骤还需要充当还原剂,故A错误;“浸铜”
时,铜屑中加入H SO 和H O 得到Cu2+,反应的离子方程式为Cu+2H++H O ===Cu2++2H O,故B错误;
2 4 2 2 2 2 2
“脱氯”步骤中,“浸铜”后的溶液中加入锌浸出液,仅Cu元素的化合价发生改变,得到CuCl固体,即
Cu的化合价升高,Cu2+的化合价降低,发生归中反应,离子方程式为Cu+Cu2++2Cl-===2CuCl,故C正确;
脱氯液净化后电解,Zn2+应在阴极得到电子变为Zn,故D错误。]
3.B [在晶体硅中,每个Si与其周围的4个Si形成共价键并形成立体空间网状结构,因此,平均每个Si形
成2个共价键,1 mol Si含Si—Si的数目约为2×6.02×1023,B说法错误;SiHCl 易水解,氢气中混有氧气
3
易爆炸,原料气HCl和H 应充分去除水和氧气,C说法正确;Si+3HCl SiHCl +H ,该反应是气体分
2 3 2
子数减少的反应,因此,生成SiHCl 的反应为熵减过程,D说法正确。]
3
4.B
5.D [当pH=1.9时氢氧化铁开始沉淀,当pH=3.5时氢氧化铝开始沉淀,当pH=4时,则会生成氢氧化铝和
氢氧化铁,即“沉渣Ⅰ”中含有Fe(OH) 和Al(OH) ,A正确;硫化钠溶液中的硫离子可以水解,产生氢氧
3 3
根离子,使溶液显碱性,其第一步水解的离子方程式为S2-+H O HS-+OH-,B正确;当铜离子和锌离子
2
c(Cu2+ ) c(Cu2+ )·c(S2- ) K (CuS)
sp
完全沉淀时,则硫化铜和硫化锌都达到了沉淀溶解平衡,则 = = =
c(Zn2+ ) c(Zn2+ )·c(S2- ) K (ZnS)
sp
6.4×10-36
=4.0×10-12,C正确;“出水”中除含有阴离子外,还含有大量的Na+、Ca2+等,故只经阴离子交
1.6×10-24
换树脂软化处理后,不可用作工业冷却循环用水,D错误。]
6.B [“盐浸”过程ZnO转化为[Zn(N H ) ] 2+ ,发生反应:ZnO+2NH +2N H+ ===[Zn(N H ) ] 2+ +H O,
3 4 3 4 3 4 2
根据题中信息可知,Fe O 、Fe O 只有少量溶解,通入空气氧化后Fe2+和Fe3+转化为Fe(OH) ;“沉锌”过
2 3 3 4 3
程发生反应:[Zn(N H ) ] 2+ +4H O+S2-===ZnS↓+4NH ·H O,经洗涤干燥后得到产物ZnS及滤液。“盐
3 4 2 3 2
浸”过程中消耗氨,浸液pH下降,需补充NH ,A正确;由分析可知,“滤渣”的主要成分为Fe O 和
3 3 4Fe O ,只含少量的Fe(OH) ,B错误;“沉锌”过程发生反应:[Zn(N H ) ] 2+ +4H O+S2-
2 3 3 3 4 2
===ZnS↓+4NH ·H O,C正确。]
3 2
7.A [由流程可知,氢溴酸中含有少量的溴,加入硫化钡将溴还原生成溴化钡和硫,再加入硫酸除杂,得
到的滤渣为硫酸钡和硫;加入碳酸锂进行中和,得到的溴化锂溶液经浓缩等操作后得到产品溴化锂。还原
工序逸出的Br 用NaOH溶液吸收,吸收液中含有溴化钠和次溴酸钠等物质,若直接返回还原工序,则产
2
品中会有一定量的溴化钠,导致产品的纯度降低,A错误;除杂工序中产生的滤渣为硫酸钡和硫,硫可溶
于煤油,而硫酸钡不溶于煤油,因此可用煤油进行组分分离,B正确;中和工序中,碳酸锂和氢溴酸发生
反应生成溴化锂、二氧化碳和水,C正确;根据得失电子守恒可知,溴和硫化钡反应时物质的量之比为
1∶1;根据硫酸钡的化学组成及钡元素守恒可知,n(BaS)∶n(H SO )为1∶1,因此,参与反应的
2 4
n(Br )∶n(BaS)∶n(H SO )为1∶1∶1,D正确。]
2 2 4