文档内容
专题五 元素的综合推断
【考情分析】
命题点 三年考情 分析解读
2017课标Ⅱ·T ,2016 高考考纲要求“根据图表、数据等所给
9
课标Ⅰ·T , 背景材料,分析有关现象的变化规律”,
8
原子结构推断 此类型的考题常受命题者的青睐。命题
2015课标Ⅰ·T ,2015
8 形式通常有两种:一种是通过观察、比
课标Ⅱ·T
10 较图表中数据的变化趋势,总结出有关
规律,再运用于解题过程中。第二种是
元素周期律推 2017课标Ⅲ·T ,2016
12
以文字形式给出,先进行元素的推断,
断 课标Ⅲ·T
12
再以所得元素为载体进行有关知识的
2017课标Ⅰ·T ,2016 考查,赋分一般6分,本部分试题难度
物质综合推断 12
课标Ⅱ·T 中等,本部分内容是高考考查的重点。
9
1.结构与位置互推是解题的核心
(1)掌握四个关系式:①电子层数=周期数;②质子数=原子序数;③最外层电子
数=主族序数;④主族元素的最高正价=主族序数(O、F除外),负价=主族序数
-8。
(2)熟练掌握周期表的结构及周期表中的一些特殊规律:①“凹”型结构的“三
短四长,七主七副八零完”;②各周期元素种类;③稀有气体的原子序数及在周期
表中的位置;④同主族上下相邻元素原子序数的关系。
2.性质与位置互推是解题的关键
熟悉元素周期表中同周期、同主族元素性质的递变规律,主要包括:(1)元素的金
属性、非金属性;(2)气态氢化物的稳定性;(3)最高价氧化物对应水化物的酸碱
性;(4)金属与水或酸反应置换H 的难易程度。
2
3.结构和性质的互推是解题的要素
(1)电子层数和最外层电子数决定元素原子的金属性和非金属性;(2)同主族元素
最外层电子数相同,化学性质相似;(3)正确推断原子半径和离子半径的大小及结
构特点;(4)判断元素金属性和非金属性的强弱。
4.关系总结5.解题模板:“两步”快速突破元素推断题
考点指导1 依据原子结构特点推断元素
【典例1】 (2019·重庆适应性测试)短周期元素a、b、c、d的原子序数依次增大,
c、a、b最外层电子数为等差数列,公差为2,a、c的价电子数之和为6,d的核外电
子数等于b的核外电子数加8。下列叙述错误的是( )
A.a和b可形成气态化合物
B.c的原子半径小于d的原子半径
C.b和c形成的化合物为离子化合物
D.a和d最高价氧化物的水化物均呈酸性
[师生互动]
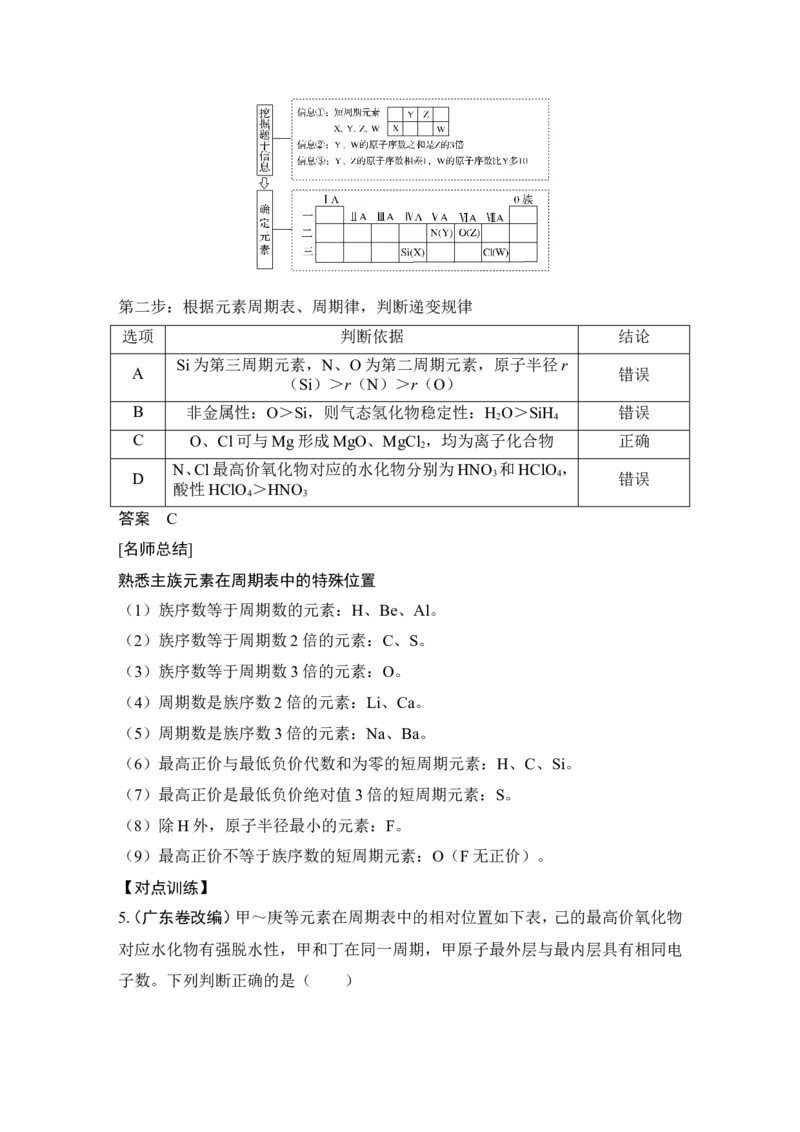
第一步:挖掘题干信息,确定元素名称
第二步:根据元素周期表、周期律,判断结论选项 判断依据 结论
A C、O可以形成气态化合物CO、CO 等 正确
2
B Mg、S同周期,原子半径:Mg>S 错误
C MgO为离子化合物 正确
C、S的最高价氧化物的水化物分别为H CO 、H SO ,呈
D 2 3 2 4 正确
酸性
答案 B
[名师总结]
1.“阴三、阳四”规律:某元素阴离子最外层电子数与次外层相同,该元素位于第
三周期;若为阳离子,则位于第四周期。
2.“阴上、阳下”规律:电子层结构相同的离子,若电性相同,则位于同周期,若电
性不同,则阳离子位于阴离子的下一周期。
【对点训练】
1(. 2018·课标全国Ⅰ,12)主族元素W、X、Y、Z的原子序数依次增加,且均不大于
20。W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫
酸反应,其生成物可腐蚀玻璃。下列说法正确的是( )
A.常温常压下X的单质为气态
B.Z的氢化物为离子化合物
C.Y和Z形成的化合物的水溶液呈碱性
D.W与Y具有相同的最高化合价
解析 本题考查元素推断、元素化合物的结构与性质、化合价规律和特例。氢氟酸
可腐蚀玻璃,根据题意可知W是F,与其同主族的Y是Cl;实验室中用CaF 与浓
2
H SO 反应制取HF,故Z是Ca;W、X、Z最外层电子数之和为10,则X是Na。钠
2 4
单质常温常压下是固体,A错误;CaH 是由Ca2+与H-构成的离子化合物,B正确
2
CaCl 溶液呈中性,C错误;F是非金属性最强的元素,没有正化合价,氯元素的最
2
高化合价是+7价,D错误。
答案 B
2(. 2018·课标全国Ⅱ,10)W、X、Y和Z为原子序数依次增大的四种短周期元素。
W与X可生成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z
原子最外层的电子数与W的电子总数相同。下列叙述正确的是( )
A.X与其他三种元素均可形成两种或两种以上的二元化合物B.Y与其他三种元素分别形成的化合物中只含有离子键
C.四种元素的简单离子具有相同的电子层结构
D.W的氧化物对应的水化物均为强酸
解析 由题意可推出W是氮元素,X是氧元素,Y是钠元素,Z是氯元素。O能与
N形成NO、NO 、N O 等化合物,O与Na能形成Na O和Na O ,O与Cl能形成
2 2 5 2 2 2
ClO 、Cl O 等化合物,A项正确;Na与N、Cl形成的化合物只含离子键,而Na与
2 2 7
O形成的Na O 中既含离子键又含共价键,B项错误;N3-、O2-、Na+均含10个电
2 2
子,而Cl-含18个电子,C项错误;N元素的最高价氧化物对应的水化物HNO 为
3
强酸,而该选项中没有指明是N元素的最高价氧化物对应的水化物,D项错误。
答案 A
考点指导2 依据元素及其化合物的性质推断
【典例2】 A 、 B 、 C 、 D 是原子序数依次增大的四种短周期元素 ①,甲、乙、丙、丁、
戊是由其中的两种或三种元素组成的化合物②, 辛是由 C 元素形成的单质 ③。已知:
常温下 0.1 mol/L 丁溶液的 pH 为 1 3④,甲、乙、丙、丁、戊、辛物质间可发生如图所
示转化。
则下列说法不正确的是( )
A.原子半径:D>B>C
B.元素的非金属性:B>C>A
C.A、B、C、D形成的化合物中既含有离子键又含有共价键
D.A分别与B、C、D形成的简单化合物中,A与B形成的简单化合物的熔点最低
[师生互动]
第一步:挖掘题干信息,确定元素第二步:根据元素周期表、周期律,判断递变规律
选项 判断依据 结论
A 原子半径:Na>C>O 正确
B 非金属性:O>C>H 错误
四种元素可形成NaHCO ,既有离子键又有共
C 3 正确
价键
D CH 、H O、NaH中,CH 为气体熔点最低 正确
4 2 4
答案 B
[名师总结]
常见元素及其化合物的特性
(1)形成化合物种类最多的元素或单质是自然界中硬度最大的物质的元素或气态
氢化物中氢的质量分数最大的元素:C。
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。
(3)地壳中含量最多的元素或气态氢化物的沸点最高的元素或氢化物在通常情况
下呈液态的元素:O。
(4)地壳中含量最多的金属元素:Al。
(5)最活泼的非金属元素或无正价的元素或无含氧酸的非金属元素或无氧酸(气
态氢化物)可腐蚀玻璃的元素或气态氢化物最稳定的元素或阴离子的还原性最弱
的元素:F。
(6)最活泼的金属元素或最高价氧化物对应水化物碱性最强的元素或阳离子的氧
化性最弱的元素:Cs。(7)最易着火的非金属元素的单质,其元素是:P。
(8)焰色反应呈黄色的元素:Na。
(9)焰色反应呈紫色(透过蓝色钴玻璃观察)的元素:K。
(10)单质密度最小的元素:H,密度最小的金属元素:Li。
(11)常温下单质呈液态的非金属元素:Br;金属元素:Hg。
(12)最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素:Al。
(13)元素的气态氢化物和它的最高价氧化物对应水化物起化合反应的元素:N;
能起氧化还原反应的元素:S。
(14)元素的气态氢化物能和它的氧化物在常温下反应生成该元素单质的元素:S。
(15)元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
(16)常见的一种元素存在几种单质的元素:C、P、O、S,其中一种同素异形体易着
火的元素:P。
【对点训练】
3(. 2018·课标全国Ⅲ,13)W、X、Y、Z均为短周期元素且原子序数依次增大,元素
X和Z同族。盐YZW与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作
用,可得到含YZW的溶液。下列说法正确的是( )
A.原子半径大小为WCl>O>F,A项错误;HF是弱酸,HCl
为强酸,酸性:HFNH ,正确;B项,O2-、Na+均具有Ne的电
2 3
子层结构,B正确;C项,Na S溶液因S2-水解呈碱性,蓝色石蕊试纸不变色,错误;
2
D项,S和O同属于第ⅥA族,S与Na同属于第三周期,正确。
答案 C
考点指导3 依据元素周期表的“片段结构”推断元素
【典例3】 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知
Y、W的原子序数之和是Z的3倍,下列说法正确的是( )
Y Z
X W
A.原子半径:X<Y<Z
B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
[师生互动]
第一步:挖掘题干信息,确定元素第二步:根据元素周期表、周期律,判断递变规律
选项 判断依据 结论
Si为第三周期元素,N、O为第二周期元素,原子半径r
A 错误
(Si)>r(N)>r(O)
B 非金属性:O>Si,则气态氢化物稳定性:H O>SiH 错误
2 4
C O、Cl可与Mg形成MgO、MgCl ,均为离子化合物 正确
2
N、Cl最高价氧化物对应的水化物分别为HNO 和HClO ,
D 3 4 错误
酸性HClO >HNO
4 3
答案 C
[名师总结]
熟悉主族元素在周期表中的特殊位置
(1)族序数等于周期数的元素:H、Be、Al。
(2)族序数等于周期数2倍的元素:C、S。
(3)族序数等于周期数3倍的元素:O。
(4)周期数是族序数2倍的元素:Li、Ca。
(5)周期数是族序数3倍的元素:Na、Ba。
(6)最高正价与最低负价代数和为零的短周期元素:H、C、Si。
(7)最高正价是最低负价绝对值3倍的短周期元素:S。
(8)除H外,原子半径最小的元素:F。
(9)最高正价不等于族序数的短周期元素:O(F无正价)。
【对点训练】
5.(广东卷改编)甲~庚等元素在周期表中的相对位置如下表,己的最高价氧化物
对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电
子数。下列判断正确的是( )A.丙与戊的原子序数相差28
B.气态氢化物的稳定性:庚<己<戊
C.常温下,甲和乙的单质均能与水剧烈反应
D.丁的单质可用于制造光导纤维
解析 己的最高价氧化物对应水化物有强脱水性,则己为S;由元素在周期表中的
相对位置可推断:丙为B、丁为Si、庚为F。因甲和丁在同一周期,且甲原子最外层
与最内层具有相同电子数,则甲为Mg,乙为Ca。A.丙为B,原子序数为5,而戊位
于P的下方,其原子序数比P的原子序数大18,即戊的原子序数为33,则丙与戊
的原子序数相差28,正确。B.同周期元素自左向右,元素的非金属性逐渐增强;同
主族元素自上而下,元素的非金属性逐渐减弱,因此元素的非金属性:庚>己>戊,
元素的非金属性越强,其气态氢化物的稳定性越强,故气态氢化物稳定性:庚>己
>戊。C.常温下,甲(Mg)与水反应缓慢,加热时反应较快。D.可用于制造光导纤维
的为SiO ,不是单质Si,错误。
2
答案 A
6(. 浙江高考)如表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元
素原子的核电荷数为X元素的2倍。下列说法正确的是( )
X
Y Z W
T
A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次增大
B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物
的酸性依次增强
C.YX 晶体熔化、液态WX 汽化均需克服分子间作用力
2 3
D.根据元素周期律,可以推测T元素的单质具有半导体特性,T X 具有氧化性和
2 3
还原性
解析 由题干信息和元素在周期表中的相对位置可知,X、W分别为O和S;则Y
为Si、Z为P、T为As。X、W、Z气态氢化物的热稳定性依次减弱,A项错误;自然界中存在磷单质、硫单质,B项错误;SiO 是原子晶体,SO 是分子晶体,前者熔化
2 3
时需要破坏共价键,后者汽化只需要破坏分子间作用力,C项错误;As处在金属和
非金属交界处,所以As具有半导体特性,As的最高化合价为+5,而As O 中As
2 3
为+3价,所以As O 既具有氧化性,又具有还原性,D项正确。
2 3
答案 D
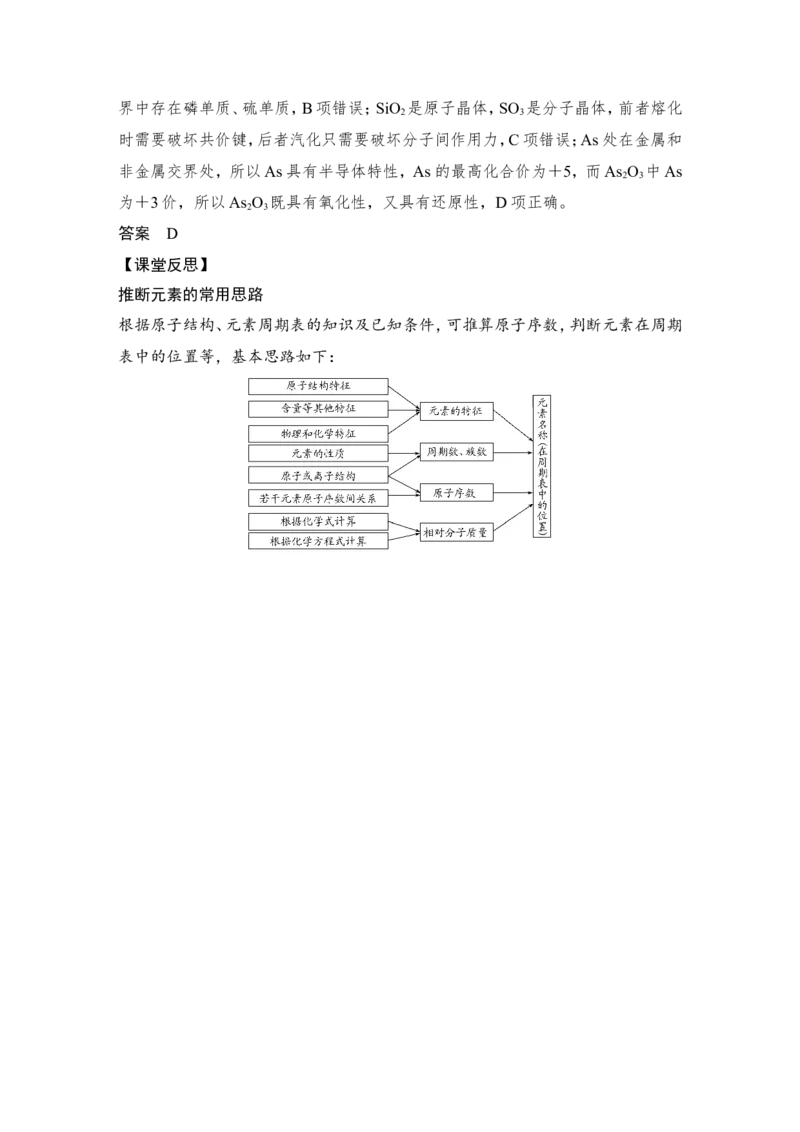
【课堂反思】
推断元素的常用思路
根据原子结构、元素周期表的知识及已知条件,可推算原子序数,判断元素在周期
表中的位置等,基本思路如下: