文档内容
电离平衡、水解平衡及沉淀溶解平衡的分析应用
(选择题1~6题,每小题3分,7~14题,每小题4分,共50分)
1.(2024·天津红桥区高三模拟)白醋是烹调中的酸味辅料,能改善调节人体的新陈代谢,其主要成分
CH COOH为一元弱酸。25 ℃时,下列有关说法正确的是( )
3
A.pH=3的CH COOH溶液中,存在c(H+)=c(CH COOH)+c(CH COO-)
3 3 3
B.pH=7的CH COONH 溶液中,c(CH COO-)=c(N H+ )>c(H+)=c(OH-)
3 4 3 4
C.pH=5的CH COOH溶液中,水电离产生的c(H+)=10-5 mol·L-1
3
D.pH=10的CH COONa溶液中,c(CH COO-)>c(Na+)>c(OH-)>c(H+)
3 3
2.(2024·天津南开区高三模拟)室温下,对于100 mL pH=3 CH COOH溶液,下列判断正确的是( )
3
c(CH COO- )
A.加入少量水,溶液中 3 减小
c(CH COOH)
3
B.与100 mL pH=11 NaOH溶液混合后pH>7
C.溶液中粒子浓度大小关系:c(H+)=c(CH COOH)+c(CH COO-)+c(OH-)
3 3
D.滴加0.1 mol·L-1 CH COONa溶液至c(CH COO-)=c(Na+)时,溶液呈中性
3 3
3.(2024·南京模拟)下列关于电解质溶液的说法不正确的是( )
A.室温下,0.1 mol·L-1弱酸HA的pH=3,HA的电离度为1%
B.室温下,5×10-4 mol·L-1Na SO 稀溶液中,c(Na+)∶c(OH-)=500∶1
2 4
C.室温下,c(OH-)=100c(H+)的NH ·H O溶液的pH=8
3 2
c(Cl- )-c(N H+ )
D.室温下,加水稀释NH Cl溶液, 4 保持不变
4 c(N H+ )·c(OH- )
4
4.(2024·广州统考模拟)常温下,乳酸(用HL表示)的K=1.4×10-4,乳酸和氢氧化钠溶液反应生成乳酸钠(用
a
NaL表示)。下列说法正确的是( )
A.NaL水溶液呈中性
B.0.01 mol·L-1 HL溶液的pH=2
C.0.01 mol·L-1 HL溶液中,c(L-)>c(HL)
D.0.01 mol·L-1 NaL溶液中,c(Na+)=c(L-)+c(HL)
5.(2024·广东统考模拟)安息香酸(HR)是最简单的一元芳香酸,其钠盐(用NaR表示)的水溶液呈碱性。已知
常温下,K(HR)>K (H CO )。下列说法正确的是( )
a a1 2 3
A.常温下,0.001 mol·L-1 HR水溶液的pH=3
B.向NaR水溶液中加水稀释,溶液的pH升高
C.NaR水溶液中,c(HR)+c(H+)=c(R-)+c(OH-)
D.常温下,NaR溶液的碱性比同浓度的NaHCO 溶液弱
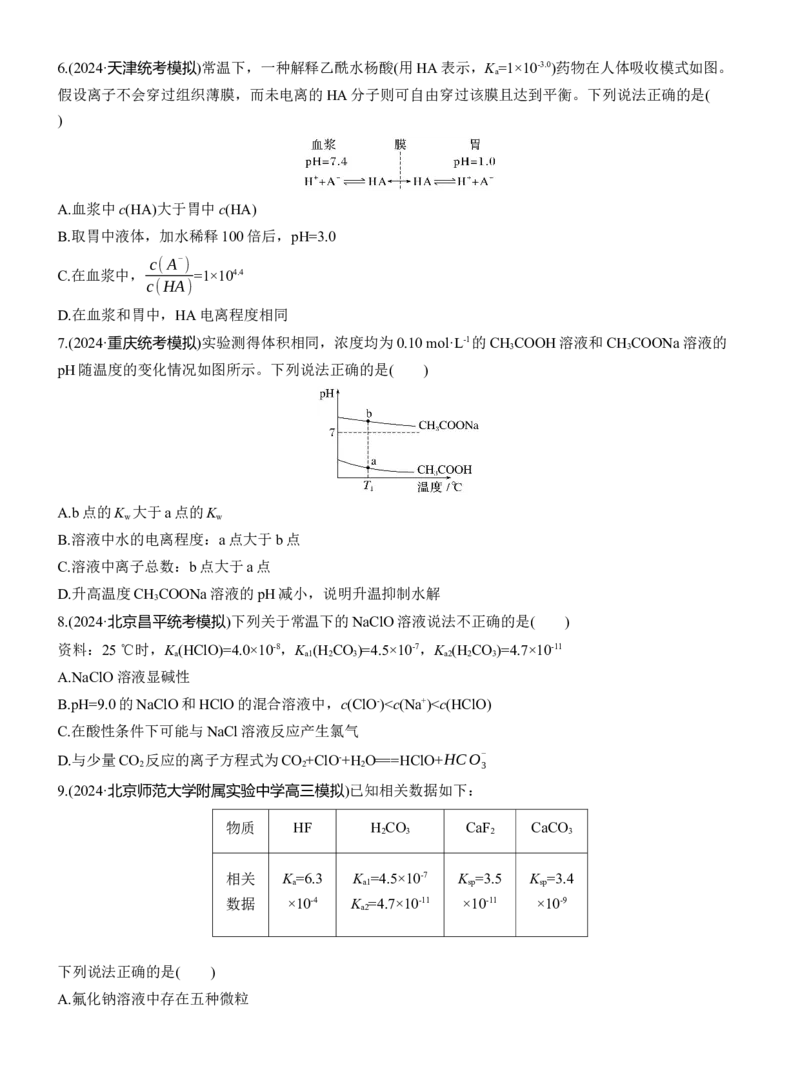
36.(2024·天津统考模拟)常温下,一种解释乙酰水杨酸(用HA表示,K=1×10-3.0)药物在人体吸收模式如图。
a
假设离子不会穿过组织薄膜,而未电离的HA分子则可自由穿过该膜且达到平衡。下列说法正确的是(
)
A.血浆中c(HA)大于胃中c(HA)
B.取胃中液体,加水稀释100倍后,pH=3.0
c(A-
)
C.在血浆中, =1×104.4
c(HA)
D.在血浆和胃中,HA电离程度相同
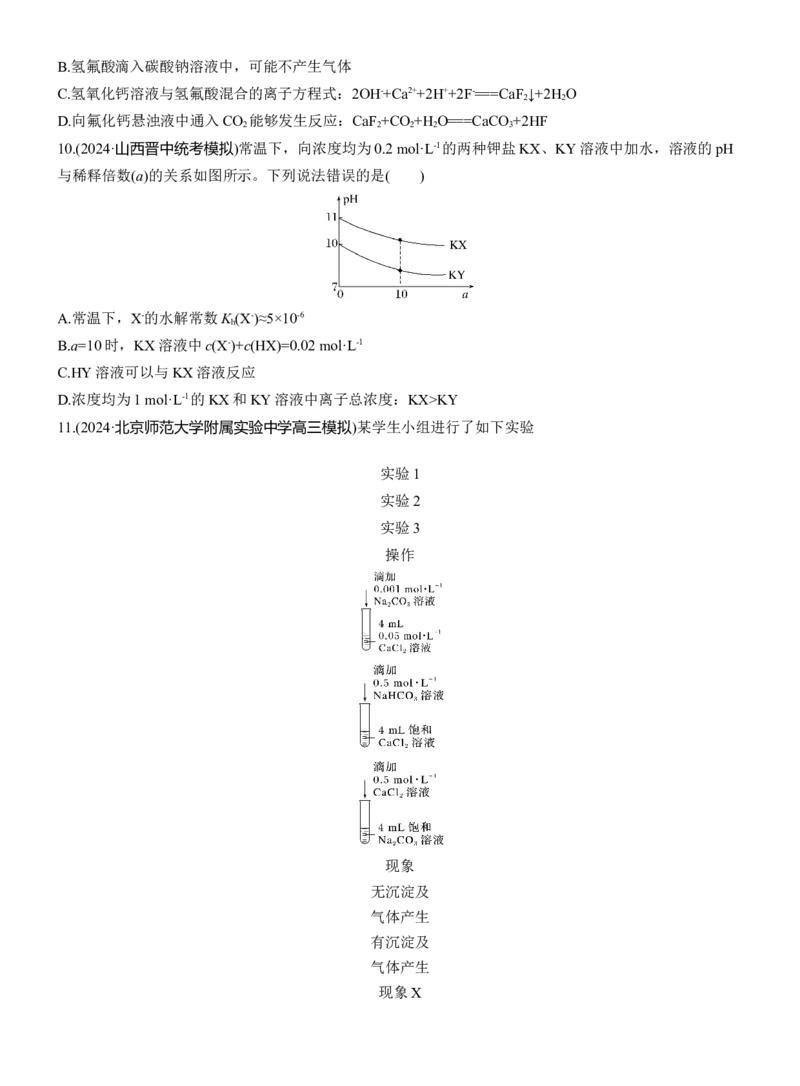
7.(2024·重庆统考模拟)实验测得体积相同,浓度均为0.10 mol·L-1的CH COOH溶液和CH COONa溶液的
3 3
pH随温度的变化情况如图所示。下列说法正确的是( )
A.b点的K 大于a点的K
w w
B.溶液中水的电离程度:a点大于b点
C.溶液中离子总数:b点大于a点
D.升高温度CH COONa溶液的pH减小,说明升温抑制水解
3
8.(2024·北京昌平统考模拟)下列关于常温下的NaClO溶液说法不正确的是( )
资料:25 ℃时,K(HClO)=4.0×10-8,K (H CO )=4.5×10-7,K (H CO )=4.7×10-11
a a1 2 3 a2 2 3
A.NaClO溶液显碱性
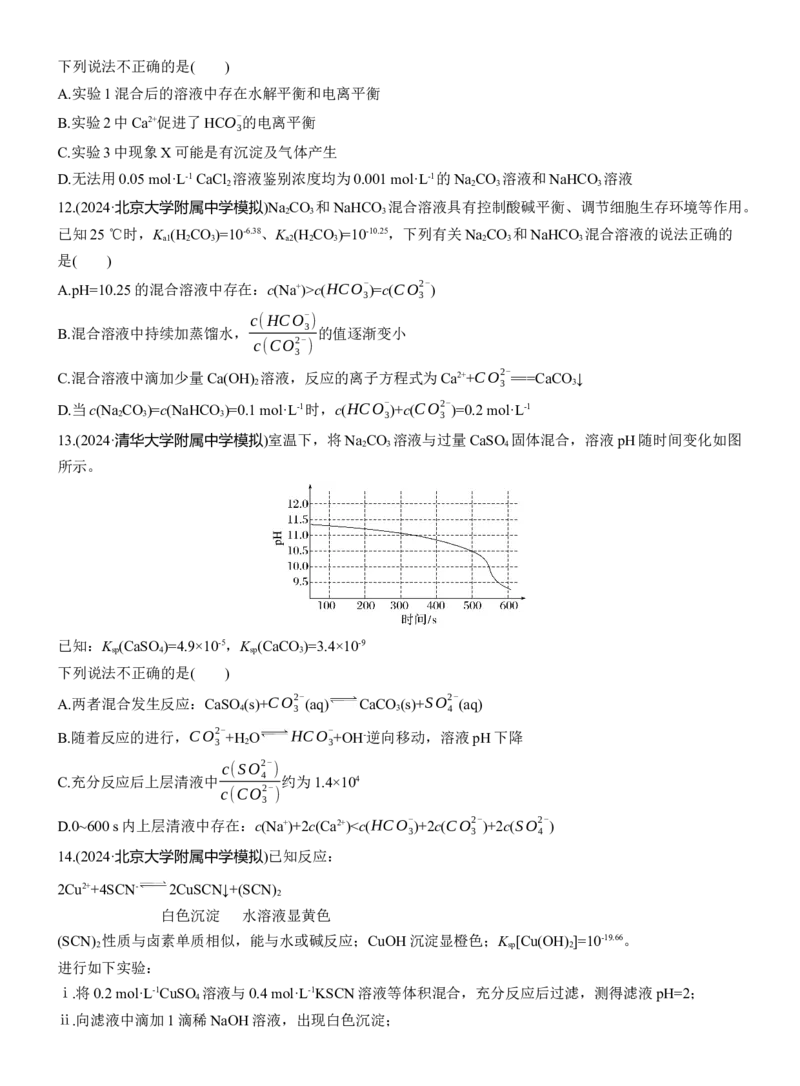
B.pH=9.0的NaClO和HClO的混合溶液中,c(ClO-)KY
11.(2024·北京师范大学附属实验中学高三模拟)某学生小组进行了如下实验
实验1
实验2
实验3
操作
现象
无沉淀及
气体产生
有沉淀及
气体产生
现象X下列说法不正确的是( )
A.实验1混合后的溶液中存在水解平衡和电离平衡
B.实验2中Ca2+促进了HCO-
的电离平衡
3
C.实验3中现象X可能是有沉淀及气体产生
D.无法用0.05 mol·L-1 CaCl 溶液鉴别浓度均为0.001 mol·L-1的Na CO 溶液和NaHCO 溶液
2 2 3 3
12.(2024·北京大学附属中学模拟)Na CO 和NaHCO 混合溶液具有控制酸碱平衡、调节细胞生存环境等作用。
2 3 3
已知25 ℃时,K (H CO )=10-6.38、K (H CO )=10-10.25,下列有关Na CO 和NaHCO 混合溶液的说法正确的
a1 2 3 a2 2 3 2 3 3
是( )
A.pH=10.25的混合溶液中存在:c(Na+)>c(HCO- )=c(CO2-
)
3 3
c(HCO-
)
3
B.混合溶液中持续加蒸馏水, 的值逐渐变小
c(CO2-
)
3
C.混合溶液中滴加少量Ca(OH) 溶液,反应的离子方程式为Ca2++CO2- ===CaCO ↓
2 3 3
D.当c(Na CO )=c(NaHCO )=0.1 mol·L-1时,c(HCO- )+c(CO2- )=0.2 mol·L-1
2 3 3 3 3
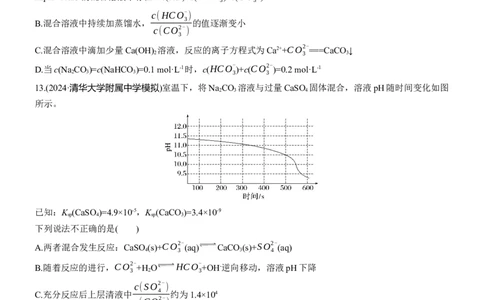
13.(2024·清华大学附属中学模拟)室温下,将Na CO 溶液与过量CaSO 固体混合,溶液pH随时间变化如图
2 3 4
所示。
已知:K (CaSO )=4.9×10-5,K (CaCO )=3.4×10-9
sp 4 sp 3
下列说法不正确的是( )
A.两者混合发生反应:CaSO
(s)+CO2-
(aq) CaCO
(s)+SO2-
(aq)
4 3 3 4
B.随着反应的进行,CO2-
+H O
HCO-
+OH-逆向移动,溶液pH下降
3 2 3
c(SO2-
)
C.充分反应后上层清液中 4 约为1.4×104
c(CO2-
)
3
D.0~600
s内上层清液中存在:c(Na+)+2c(Ca2+)K (CuSCN)
sp 2 sp
C.ⅲ中出现蓝色沉淀时,该平衡可能发生逆向移动
D.无论ⅱ还是ⅲ,随着NaOH溶液的加入,c[(SCN) ]始终降低
2答案精析
1.B
c(CH COO- )·c(H+ ) c(CH COO- )
2.D [醋酸K= 3 ,温度不变,其K 不变,加水后c(H+)减小,故 3 增
a c(CH COOH) a c(CH COOH)
3 3
大,A错误;pH=11 NaOH溶液c(NaOH)=10-3 mol·L-1,CH COOH是弱酸,只有很少部分发生电离,故
3
pH=3 CH COOH溶液c(CH COOH)远大于10-3 mol·L-1,等体积混合后,醋酸过量,溶液为酸性,pH<7,B
3 3
错误;由电荷守恒:c(H+)=c(CH COO-)+c(OH-),C错误。]
3
c(H+
)
3.B [室温下,0.1 mol·L-1弱酸HA的pH=3,c(H+)=10-3 mol·L-1,由HA H++A-,电离度α=
c
×100%=1%,A项正确;5×10-4 mol·L-1Na SO 溶液中,c(Na+)=10-3 mol·L-1,溶液呈中性,c(OH-)=10-7
2 4
mol·L-1,c(Na+)∶c(OH-)=10 000∶1,B项错误;K =c(H+)·c(OH-)=10-14,又c(OH-)=100c(H+),所以
w
c(Cl- )-c(N H+ ) c(N H ·H O) 1
4 3 2
c(H+)=10-8 mol·L-1,pH=8,C项正确;由元素守恒可知, = = ,室
c(N H+ )·c(OH- ) c(N H+ )·c(OH- ) K
4 4 b
c(Cl- )-c(N H+ )
4
温下,加水稀释NH Cl溶液, 保持不变,D项正确。]
4 c(N H+ )·c(OH- )
4
c(H+ )·c(L- ) c2 (H+ )
4.D [NaL是强碱弱酸盐,水解显碱性,A错误;K= = =1.4×10-4,c(H+)≈1.18×10-3
a c(HL) 0.01
mol·L-1,pH≈2.93,B错误;HL微弱电离,c(L-)3,A错误;NaR水溶液
中由于R-水解显碱性,加水稀释水解程度变大,但是碱性变弱,溶液的pH减小,B错误;NaR水溶液中
的质子守恒为c(HR)+c(H+)=c(OH-),C错误;已知K(HR)>K (H CO ),HR酸性比碳酸强,根据越弱越水
a a1 2 3
解,同浓度的NaHCO 溶液水解程度大,碱性强,D正确。]
3
6.C [根据题意,未电离的HA分子可自由穿过组织薄膜,所以血浆中c(HA)等于胃中c(HA),故A错误;
取胃中液体,HA是弱酸,加水稀释100倍后,电离平衡正向移动,pH<3.0,故B错误;在血浆中,
c(A- ) K 1×10-3.0
= a = =1×104.4,故C正确;氢离子抑制HA电离,在血浆和胃中的pH不同,HA电离
c(HA) c(H+ ) 1×10-7.4
程度不相同,故D错误。]
7.C [K 只与温度有关,a、b两点的温度相同,所以K 相等,故A错误;a点醋酸电离出的H+抑制水的
w w
电离,b点溶质是醋酸钠,由于CH COO-水解,促进水的电离,所以溶液中水的电离程度:a点小于b点,
3
故B错误;b点的溶质为CH COONa,CH COONa是盐,完全电离:CH COONa===CH COO-+Na+,由醋
3 3 3 3
酸根离子的水解CH COO-+H O CH COOH+OH-可知,水解生成的氢氧根离子的物质的量等于消耗的醋
3 2 3酸根离子,由于水解程度很小,水解后溶液中离子的总物质的量基本维持不变,而a点的CH COOH是弱
3
电解质,电离程度小,则其离子总数少,故C正确;盐类水解是吸热反应,升高温度促进水解,即升温
CH COO-+H O CH COOH+OH-平衡右移,所以升高温度CH COONa溶液中氢氧根离子浓度增大,升温
3 2 3 3
时K 也增大,导致氢离子浓度增大,pH减小,故D错误。]
w
c(ClO- )·c(H+
)
8.B [NaClO为强碱弱酸盐,故NaClO溶液显碱性,故A正确;K(HClO)= =4.0×10-8,当
a c(HClO)
c(ClO-
)
4.0×10-8 4.0×10-8
pH=9.0时, = = =40,c(HClO)HClO>HCO-
2 2 2 3 3
,则与少量CO 反应的离子方程式为CO +ClO-+H
O===HClO+HCO-
,故D正确。]
2 2 2 3
9.B [氟化钠溶液中氟离子会发生水解反应生成HF和OH-,存在的微粒有Na+、F-、HF、OH-、H O和少
2
量的H+,共6种,A错误;根据表中数据可知,HF的电离平衡常数大于碳酸,所以将少量HF滴入碳酸钠
溶液中会生成碳酸氢钠,此时不产生气泡,若HF过量,则会生成气体,B正确;HF为弱酸,在离子方程
式中不能拆分,需保留化学式,C错误;碳酸的酸性弱于HF,所以不能发生上述反应,且碳酸钙可溶于
HF,产物不共存,D错误。]
10.D [0.2 mol·L-1的KX溶液中,c(OH-)=10-3 mol·L-1≈c(HX),X-+H O HX+OH-,K (X-)=
2 h
c(HX)·c(OH-
)
≈5×10-6,A项正确;a=10时c(K+)=0.02 mol·L-1,由元素守恒可知c(K+)=c(X-)+c(HX),B
c(X-
)
项正确;相同温度时等浓度的KX溶液的pH大于KY溶液的pH,说明X-水解能力强于Y-,酸性:
HY>HX,C项正确;由电荷守恒可知,两种盐溶液中分别存在:c(K+)+c(H+)=c(OH-)+c(X-),c(K+)
+c(H+)=c(OH-)+c(Y-),由于两种溶液中c(K+)相等而KX溶液中c(H+)较小,故离子总浓度KX较小,D项错
误。]
11.C [实验1混合后的溶液无沉淀及气体产生,溶液中存在碳酸根离子的水解平衡,水的电离平衡,A正
确;实验2中有沉淀及气体产生,钙离子结合了碳酸氢根离子电离产生的碳酸根离子,同时,碳酸氢根离
子电离产生的氢离子和另一个碳酸氢根离子结合生成水和二氧化碳,说明Ca2+促进了HCO-
的电离平衡,B
3
正确;由实验1和2可知,当钙离子浓度较小时,不容易和碳酸根离子结合生成沉淀,随着钙离子浓度增
大,会生成白色沉淀,但是没有气体产生,C错误;由实验1和2可知,当钙离子浓度较小时,不容易和
碳酸根离子结合生成沉淀,故无法用0.05 mol·L-1 CaCl 溶液鉴别浓度均为0.001 mol·L-1的Na CO 溶液和
2 2 3
NaHCO 溶液,D正确。]
3
c(H+ )·c(CO2-
)
12.A [混合溶液的pH为10.25,c(H+)=10-10.25 mol·L-1,K (H CO )=10-10.25=
3 ,则c(HCO-
a2 2 3 c(HCO-
)
3
3
)=c(CO2- ),即溶液中存在:c(Na+)>c(HCO- )=c(CO2- ),故A正确;随蒸馏水的不断加入,溶液中c(OH-)
3 3 3c(HCO- ) K (CO2- )
3 h 3
逐渐减小,碳酸根离子的水解平衡常数不变,则 = 的值逐渐增大,故B错误;混合溶
c(CO2-
)
c(OH-
)
3
液中滴加少量Ca(OH) 溶液,钙离子与氢氧根离子均要参与反应,故C错误;当c(Na CO )=c(NaHCO )=0.1
2 2 3 3
mol·L-1时,根据元素守恒有c(HCO- )+c(CO2-
)+c(H CO )=0.2 mol·L-1,故D错误。]
3 3 2 3
13.D [CaSO 微溶于水,CaCO 难溶于水,Na CO 溶液与过量CaSO 固体混合反应生成CaCO ,离子反应
4 3 2 3 4 3
为CaSO
(s)+CO2-
(aq) CaCO
(s)+SO2- (aq),随着反应的进行,c(CO2- )减小,使得CO2-
+H O
4 3 3 4 3 3 2
HCO- +OH-逆向移动,c(OH-)减小,pH减小,故A、B正确;充分反应后上层清液为碳酸钙和硫酸钙的饱
3
c(SO2- ) c(Ca2+ )·c(SO2- ) K (CaSO ) 4.9×10-5
4 4 sp 4
和溶液, = = = ≈1.4×104,故C正确;根据电荷守恒得:
c(CO2- ) c(Ca2+ )·c(CO2- ) K (CaCO ) 3.4×10-9
3 3 sp 3
c(Na+)+2c(Ca2+)+c(H+)=c(OH-)+c(HCO- )+2c(CO2- )+2c(SO2- ),0~600 s溶液呈碱性,c(OH-)>c(H+),则
3 3 4
c(Na+)+2c(Ca2+)>c(HCO- )+2c(CO2- )+2c(SO2-
),故D错误。]
3 3 4
14.B [将0.2 mol·L-1CuSO 溶液与0.4 mol·L-1KSCN溶液等体积混合,发生已知信息中的反应,故得到白色
4
沉淀,由于溶液中存在Cu2+和(SCN) ,故得到黄绿色溶液,故A正确;ⅱ中出现白色沉淀,说明(SCN) 与
2 2
NaOH反应导致平衡正向移动,但是c(OH-)与c(SCN-)大小未知,两个沉淀是不同类型的沉淀,故无法比较
K [Cu(OH) ]与K (CuSCN)大小,故B错误;继续滴加NaOH溶液,数滴后又出现蓝色沉淀,即Cu2+与
sp 2 sp
OH-反应,导致Cu2+浓度减小,上述平衡逆向移动,故C正确;ⅱ中加入NaOH溶液,(SCN) 与NaOH反
2
应导致平衡正向移动,根据勒夏特列原理,c[(SCN) ]仍然降低;ⅲ中随着NaOH溶液的加入,平衡逆向移
2
动,c[(SCN) ]降低,故D正确。]
2