文档内容
专题十二 化学反应速率与化学平衡
一、单选题
1.(2022秋·河南驻马店·高三统考期末)进入冬季后,某医院痛风门诊患者激增,医
生告知患者减少食用动物内脏和海鲜类,增加摄入含钾丰富的食物(如香蕉、西兰花)。
痛风的化学原理为 ,关节滑液中尿
酸钠(NaUr)晶体越多,病情越严重。下列有关说法错误的是
A.上述反应的△H>0
B.痛风患者应注意保暖
C.痛风患者需控制食盐的摄入量
D.痛风患者大量饮水可适当降低痛风的发病概率
【答案】A
【详解】A.根据题意,进入冬季后,当尿酸钠晶体越多时,病情越严重,即降低温
度,平衡向正反应方向进行,根据勒夏特列原理,正反应方向为放热反应,即ΔH<
0,故A说法错误;
B.患者保暖,相当于升高温度,根据选项A分析,升高温度,平衡向逆反应方向进
行,尿酸钠晶体减少,减轻病情,故B说法正确;
C.摄入食盐的量增大,c(Na+)增大,平衡向正反应方向进行,尿酸钠晶体增多,病情
加重,因此需要控制食盐摄入量,故C说法正确;
D.大量饮水,离子浓度降低,平衡向逆反应方向进行,人体内尿酸钠晶体含量减少,
降低病情,故D说法正确;
答案为A。
2.(2023·江苏·统考一模)HS和CO 反应生成的羰基硫(COS)用于粮食熏蒸,能防止
2 2
某些昆虫、线虫和真菌的危害。CO(g)+HS(g) COS(g)+H O(g) H>0,下列说法
2 2 2
△
正确的是
A.已知该反应在加热条件下能自发进行,则其 S>0
△
B.上述反应的平衡常数K=
C.上述反应中消耗1 mol H S,生成22.4 L水蒸气
2
D.实际应用中,通过增加HS的量来提高CO 转化率,能有效减少碳排放
2 2【答案】A
【详解】A.已知该反应在加热条件下能自发进行所以 ,因为
H>0,所以 S>0,A正确;
△ △
B.由反应方程式,结合平衡常数含义可知,上述反应的平衡常数K=
,B错误;
C.没有指明具体条件,不能确定气体的体积,C错误;
D.减少碳排放是指减少二氧化碳的生成,D错误;
故选A。
3.(2022秋·海南海口·高三校考期中)某温度下,在2L恒容密闭容器中加入
1molX(s)和3molY(g),发生反应: ,10min后达到平衡状
态。下列说法错误的是
A.容器内气体的密度不变时,反应达到平衡状态B.达到平衡时,存在v正(Y)=3v
逆(Z)
C.升高温度,正、逆反应速率均增大 D.改变温度,对平衡没有影响
【答案】D
【分析】化学平衡各组分的物质的量、质量、浓度均不变,同一组分的正逆反应速率
相等。
【详解】A.恒容密闭容器,容器内气体的密度不变时,气体质量不变,X为固体,根
据质量守恒定律可知,固体X质量不变,故反应达到平衡状态,A正确;
B.X(s)+3Y(g) Z(g)+M(g),化学反应速率之比等于化学计量数之比,则v正(Y)=3v正
(Z),达到平衡时⇌,当平衡时v正(Z)=v逆(Z),故v正(Y)=3v逆(Z),B正确;
C.升高温度,正、逆反应速率均增大,C正确;
D.勒夏特列原理,如果改变影响平衡的一个因素,平衡向着能够减弱这种改变的方
向移动;当温度升高,平衡向吸热方向移动,降低温度平衡向放热方向移动,D错误;
故答案为:D。
4.(2023秋·吉林长春·高三长春市第二中学校考期末)氢气能用于烟气的脱氮反应:
。某温度下,向2L恒容
密闭容器中充入0.2mol 和0.2molNO,经5min反应达到平衡,测得平衡体系中
2
原创精品资源学科网独家享有版权,侵权必究!。下列说法正确的是
A.使用高效催化剂能提高NO的平衡转化率
B.在0~5min内,
C.保持其他条件不变,增大 ,逆反应速率减小,平衡正向移动
D.保持其他条件不变向容器中再充入0.2mol 和0.2molNO,NO的平衡转化率增大
【答案】D
【详解】A.催化剂只能改变反应速率,不能影响平衡,使用高效催化剂不能提高NO
的平衡转化率,故A错误;
B.反应经5min达到平衡,n(N )=0.05mol ,则消耗NO的物质的量为0.1mol,在
2
0~5min内, v(NO)= =0.01mol⋅L-1⋅min-1,故B错误;
C.保持其他条件不变,增大 c(H ) ,正反应速率瞬间增大,平衡正向移动,生成了
2
生成物,氮气和水蒸气浓度也增大,则逆反应速率随之增大,故C错误;
D.保持其他条件不变向容器中再充入0.2mol H 和0.2molNO,按原比例再加反应物,
2
相当于增大压强,平衡正向移动,NO的平衡转化率增大,故D正确;
故选D。
5.(2023秋·江苏苏州·高三常熟中学校考期末)已知反应
; 可用于粗硅的提纯。下列关
于该反应的说法正确的是
A.该反应在任何条件下均能自发进行
B.该反应的平衡常数表达式为
C.升高温度可以提高反应物的平衡转化率
D.反应每放出 热量,需断裂 键
【答案】B
【详解】A.该反应是一个熵减的反应,需满足 才能自发进行,故A错误;
B.因为Si为固体,不计入平衡常数计算,因此反应的平衡常数表达式为K=,故B正确;
C.该反应为放热反应,升高温度平衡向吸热方向进行,即逆向进行,将降低反应物的
平衡转化率,故C错误;
D.晶体硅是空间网状结构,每个硅原子连接周围4个硅原子,所以每个Si—Si键由
两个Si原子共同构成,故1单位硅单质有2单位Si—Si键,则每反应1 mol Si需断裂2
mol Si—Si键,故D错误;
故答案选:B。
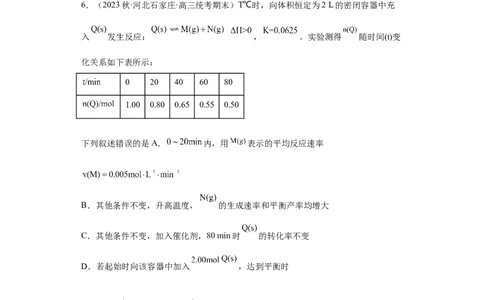
6.(2023秋·河北石家庄·高三统考期末)T℃时,向体积恒定为2 L的密闭容器中充
入 发生反应: , 。实验测得 随时间(t)变
化关系如下表所示:
0 20 40 60 80
1.00 0.80 0.65 0.55 0.50
下列叙述错误的是A. 内,用 表示的平均反应速率
B.其他条件不变,升高温度, 的生成速率和平衡产率均增大
C.其他条件不变,加入催化剂,80 min时 的转化率不变
D.若起始时向该容器中加入 ,达到平衡时
【答案】D
【详解】A. 内,消耗Q为0.2mol,则用 表示的平均反应速率
,A正确;
B.反应为吸热反应,其他条件不变,升高温度,反应速率增大且平衡正向移动,则导
4
原创精品资源学科网独家享有版权,侵权必究!致 的生成速率和平衡产率均增大,B正确;
C.80 min时 反应0.5mol,则生成MN均为0.5mol;
,此时 ,则80 min时反应达
到平衡状态;其他条件不变,加入催化剂,反应速率加快,则80 min时 一定达到
平衡,故其转化率不变,C正确;
D.Q为固体,增加量不影响平衡移动,结合C分析可知,达到平衡时M浓度仍为
,D错误;
故选D。
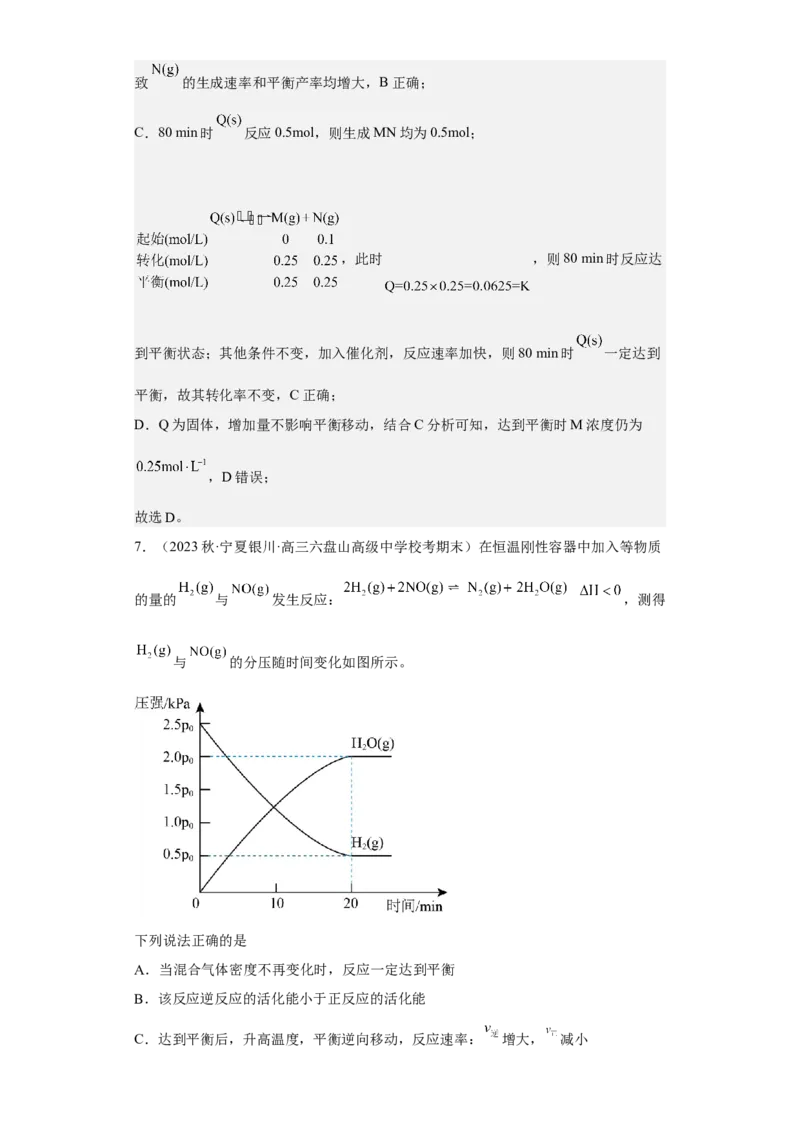
7.(2023秋·宁夏银川·高三六盘山高级中学校考期末)在恒温刚性容器中加入等物质
的量的 与 发生反应: ,测得
与 的分压随时间变化如图所示。
下列说法正确的是
A.当混合气体密度不再变化时,反应一定达到平衡
B.该反应逆反应的活化能小于正反应的活化能
C.达到平衡后,升高温度,平衡逆向移动,反应速率: 增大, 减小D.体系中混合气体总物质的量:
【答案】D
【详解】A.该刚性容器的体积不变,反应体系中各物质均为气体,混合气体的质量
不变,则容器中气体的密度始终不变,气体密度不再变化时,反应不一定达到平衡,
故A错误;
B.该反应的 ,且 则 ,即该反应逆反应的活化能大于正反应
的活化能,故B错误;
C.达到平衡后,升高温度,平衡逆向移动,反应速率: , 都增大,故C错误;
D.由图可知,初始状态时 ,达到平衡时 ,
,则 ,恒温恒容条件下,气体的物质的量之比等
于压强之比,即体系中气体总物质的量:
,故D正确;
故选D。
8.(2023秋·天津河北·高三统考期末)含硫矿物是多种化工生产的原料,主要有硫磺、
黄铁矿( )、辉铜矿( )、明矾 、绿矾( )、胆矾
( )、重晶石( )等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿
煅烧时可发生反应: 。 直接排放会造成环境污染,可将
其转化,或用石灰乳、 等物质进行回收再利用。对于反应
,下列说法正确的是
A.该反应
6
原创精品资源学科网独家享有版权,侵权必究!B.反应平衡常数
C.其他条件一定,增大体系的压强可以增大反应的平衡转化率
D.其他条件一定,升高温度可以增大反应的平衡常数
【答案】C
【详解】A.由反应可知,反应后气体分子数减小,则 ,A错误;
B.由反应式可知,平衡常数为 ,B错误;
C.增大压强,平衡正向进行,增大了平衡转化率,C正确;
D.该反应为放热反应,升高温度,反应逆向进行,平衡常数减小,D错误;
故答案为:C。
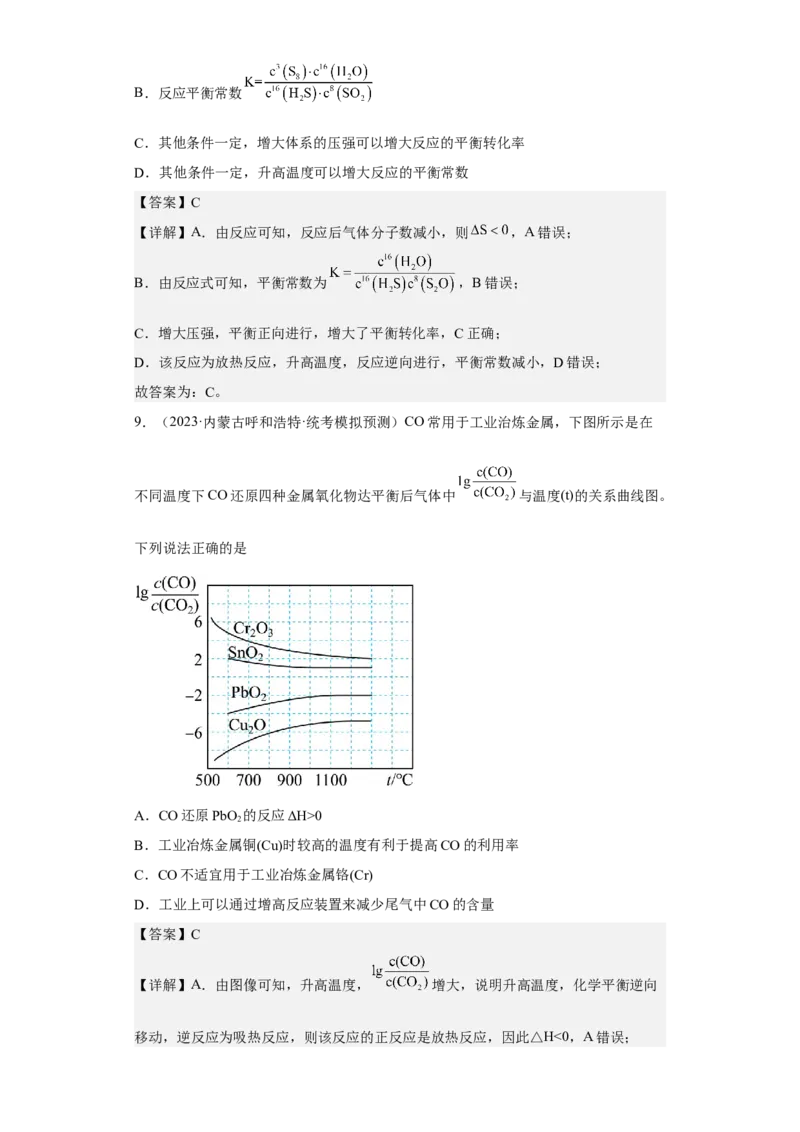
9.(2023·内蒙古呼和浩特·统考模拟预测)CO常用于工业治炼金属,下图所示是在
不同温度下CO还原四种金属氧化物达平衡后气体中 与温度(t)的关系曲线图。
下列说法正确的是
A.CO还原PbO 的反应ΔH>0
2
B.工业冶炼金属铜(Cu)时较高的温度有利于提高CO的利用率
C.CO不适宜用于工业冶炼金属铬(Cr)
D.工业上可以通过增高反应装置来减少尾气中CO的含量
【答案】C
【详解】A.由图像可知,升高温度, 增大,说明升高温度,化学平衡逆向
移动,逆反应为吸热反应,则该反应的正反应是放热反应,因此△H<0,A错误;B.由图像可知温度越高, 越大,说明在较高温度时平衡逆向移动,不利于
提高CO的利用率,B错误;
C.由图像可知用CO工业冶炼金属铬时, 一直很高,说明CO转化率很低,
因此不适合冶炼铬,C正确;
D.通过增高反应装置,可以增大CO与铁矿石的接触,但不能影响平衡移动,CO的
利用率不变,因此不能减少尾气中CO的含量,D错误;
故选C。
10.(2023秋·吉林长春·高三长春市第二中学校考期末)NO和 混合后可发生反应:
① 、② ,反应体系中含氮物质的物质
的量浓度c随着时间t的变化曲线如图所示。下列说法正确的是
A.c为 随t的变化曲线
B. 时,
C. 时刻, 的消耗速率大于生成速率
D. 时,反应①和②均达到化学平衡状态
【答案】C
【分析】NO和 混合后可发生反应:① 、②
8
原创精品资源学科网独家享有版权,侵权必究!,反应过程中NO浓度减小,NO 浓度先增大后减小,NO 浓度
2 2 4
一直增大,a、b、c分别代表NO、NO 、NO 的浓度随t的变化曲线,以此解答。
2 2 4
【详解】A.根据题给反应,结合题图中各物质浓度变化情况可知,a、b、c分别代表
NO、NO 、NO 的浓度随t的变化曲线,A说法错误;
2 2 4
B.根据物料守恒可知,任意时刻c(NO) +c(NO) +2c(NO)= C ,B说法错误;
2 2 4 0
C.由题图可知,t 时刻以后,NO 的浓度在减小,故此时NO 的消耗速率大于生成速
2 2 2
率,C说法正确;
D. 时NO 的浓度不变,说明反应②达到化学平衡状态,反应①不是可逆反应,没
2 4
有平衡状态,故D错误;
故选C。
11.(2022秋·北京房山·高三统考期末)一定条件下,在容积相等的两个恒温恒容密
闭容器中加入一定量的一氧化碳和水蒸气,发生反应:CO(g)+HO(g) CO(g)
2 2
+H (g) H=-41kJ•mol-1,达平衡后获得数据如表。下列说法不正确的是
2
△
起始时各物质的物质的量/
容器编 mol 达到平衡的时 达到平衡时体系能量的
号 间/min 变化
CO HO CO H
2 2 2
① 1 4 0 0 t 放出32.8kJ热量
1
② 2 8 0 0 t 放出QkJ热量
2
A.①中反应达平衡时,CO的转化率为80% B.该温度下,②中反应的平衡常数K=1
C.Q大于65.6 D.反应开始进行时,反应速率②>①
【答案】C
【详解】A. ,说明消耗1molCO,反
应放出41kJ热量,容器①达到平衡时放出32.8kJ热量,32.8则消耗CO物质的量为
,CO的转化率为 ,A正确;
B.化学平衡常数只与温度有关,容器①、②温度相同,则化学平衡常数相等,根据容
器①数据,列化学平衡三段式:,B正确;
C.反应前后气体体积不变,反应①②是等效平衡,则容器②消耗CO物质的量为
1.6mol,放热的热量Q = 1.6mol x 41kJ/mol = 65.6kJ,C错误;
D.起始时,容器②的浓度大于容器①,浓度越大,反应速率越快,则反应开始进行
时,反应速率②>①,D正确;
故选C。
12.(2023秋·吉林长春·高三长春市第二中学校考期末)利用反应
H<0,可减少汽车尾气对大气的污染。该
△
反应的速率方程可表示为 、 ,其中
、 分别为正、逆反应的速率常数(与温度有关),lgk与 的关系如图所示:
下列说法正确的是
A.升高温度,v 减小、v 增大 B.曲线②代表lgk
正 逆 正
C.该反应易在高温下自发进行 D. ℃时,该反应的平衡常数K为10
【答案】D
10
原创精品资源学科网独家享有版权,侵权必究!【详解】A.升高温度,v 增大、v 也增大,A错误;
正 逆
B.该反应的正反应为放热反应,降低温度,正、逆反应速率减小,k 、k 也减小,
正 逆
由于温度对吸热反应影响更大,所以化学平衡正向移动,则k >k ,所以曲线③代
正 逆
表lgk ,曲线④代表lgk ,B错误;
正 逆
C.该反应的正反应是气体体积减小的放热 H<0, S<0,因此反应易在低温下自发
进行,C错误; △ △
D. , ,当v =v 时,反应处于平衡
正 逆
状态, = , ,根据选项
B分析可知曲线③代表lgk ,曲线④代表lgk ,在 ℃,lgk =a-0.1,lgk =a-1.1,
正 逆 正 逆
所以即lgk -lgk =1=lgK,故K=10,D正确;
正 逆
故合理选项是D。
13.(2023秋·海南·高三统考期末)一定温度下,在某密闭容器中的 和 发生下
列反应,并达到平衡状态:
。下列说法正确的是
A.升高温度,
B.加入 ,平衡正向移动,平衡常数增大
C.使用合适的催化剂,可提高 的平衡转化率
D.压缩容器的容积,平衡时 的物质的量增大
【答案】D
【详解】A.该反应的正反应为放热反应,升高温度,正、逆反应速率都加快,但正
反应速率加快的倍数小于逆反应速率加快的倍数,即v <v ,平衡逆向移动,A项错
正 逆
误;
B.加入CO(g),平衡正向移动,平衡常数与浓度无关,平衡常数不变,B项错误;
2C.使用合适的催化剂,能加快反应速率,缩短达到平衡的时间,但不能使平衡发生移
动,不能提高CO 的平衡转化率,C项错误;
2
D.该反应的正反应气体体积减小,压缩容器的容积,增大压强,平衡正向移动,平
衡时CHOH(g)的物质的量增大,D项正确;
3
答案选D。
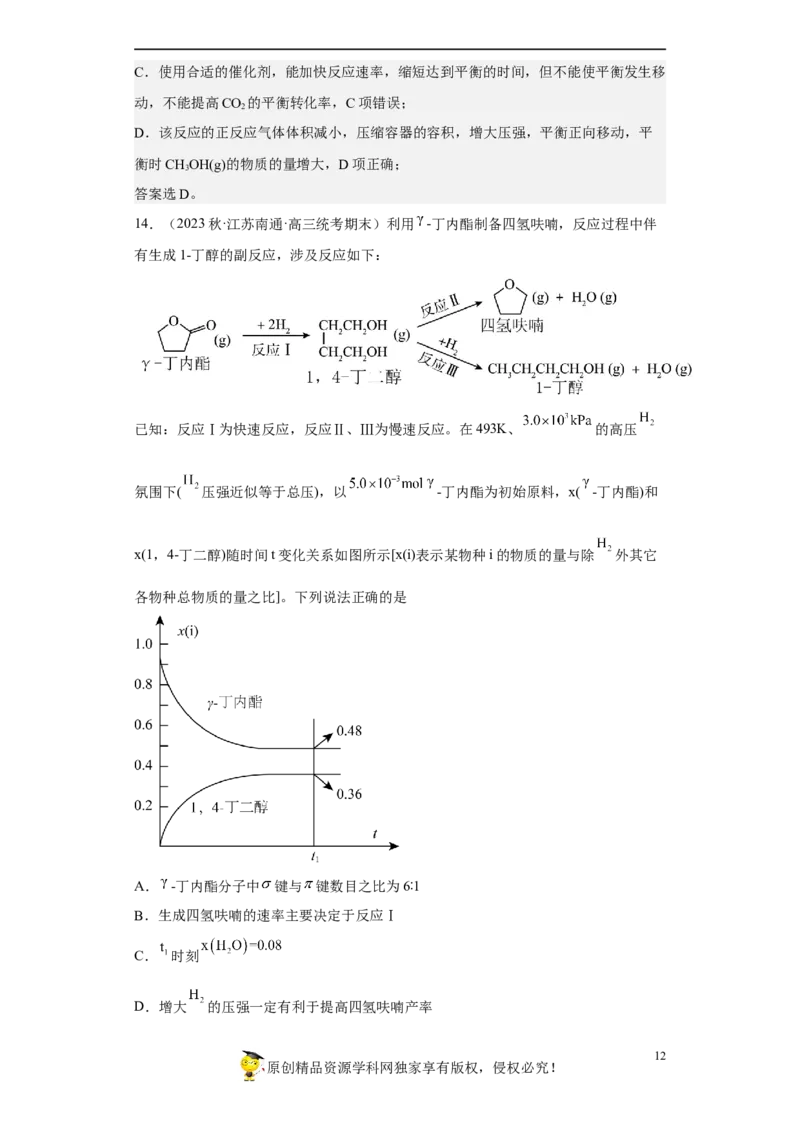
14.(2023秋·江苏南通·高三统考期末)利用 -丁内酯制备四氢呋喃,反应过程中伴
有生成1-丁醇的副反应,涉及反应如下:
已知:反应Ⅰ为快速反应,反应Ⅱ、Ⅲ为慢速反应。在493K、 的高压
氛围下( 压强近似等于总压),以 -丁内酯为初始原料,x( -丁内酯)和
x(1,4-丁二醇)随时间t变化关系如图所示[x(i)表示某物种i的物质的量与除 外其它
各物种总物质的量之比]。下列说法正确的是
A. -丁内酯分子中 键与 键数目之比为6∶1
B.生成四氢呋喃的速率主要决定于反应Ⅰ
C. 时刻
D.增大 的压强一定有利于提高四氢呋喃产率
12
原创精品资源学科网独家享有版权,侵权必究!【答案】C
【详解】A.根据 以及有机物中碳成键特点可知,σ键和π键个数比为
12∶1,故A错误;
B.化学反应的决速步是由慢反应决定的,生成四氢呋喃决速步为反应Ⅱ,故B错误;
C.以γ-丁内酯为原料,根据反应Ⅰ、Ⅱ、Ⅲ可知,体系总物质的量增加量正好是1,
4-丁二醇参与反应Ⅱ、Ⅲ的量,也正好是HO(g)的物质的量,设t 时γ-丁内酯消耗
2 1
amol,1,4-丁二醇消耗为bmol,则体系总物质的量为(5.0×10-3+b)mol,根据图像可知,
=0.48, =0.36,解得a= ,b= ,则t 时刻
1
x(H O)= =0.08,故C正确;
2
D.因反应在高压氢气氛围下进行,增大氢气压强,体系压强增大,平衡逆向进行,
不利于四氢呋喃的生成,故D错误;
答案为C。
15.(2023秋·吉林长春·高三长春市第二中学校考期末)一定条件下,分别向体积为
1L的密闭容器中充入气体,发生反应: ,测得实验①、②、③反
应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是
实验 充入气体量 反应过程条件
① 2molX+1molY 恒温
② 1molZ 恒温
③ 1molZ 绝热A.曲线Ⅰ对应实验① B.正反应为放热反应
C.气体的总物质的量: D.b点平衡常数比c点平衡常数小
【答案】C
【详解】A.恒温恒容条件下,气体的压强之比等于气体物质的量之比,故起始时实
验②与实验③的压强相等,实验①的压强是实验②与实验③的3倍,则曲线Ⅰ对应实
验①,故A正确;
B.实验①与实验②的温度相等,根据等效平衡可知,实验①与实验②最终会达到相同
的平衡状态,故曲线II对应实验②,则曲线III对应实验③,实验②与实验③充入的Z
一样多,实验③比实验②达到平衡所用的时间长,则实验③温度较低,反应速率较慢,
说明Z生成X和Y是吸热反应,则正反应为放热反应,故B正确;
C.根据pV=nRT,c、d两点的压强相同,V相同,由于从逆向建立平衡,逆向是吸热,
c点的温度比d点低,则c点的气体物质的量更多,故气体的总物质的量: ,故
C错误;
D.若都在恒温条件进行,根据B的分析,反应为放热反应,c点温度较低,所以达到
平衡时③(c)比①或②(b)更往正向移动,K更大,D正确;
故选C。
16.(2023秋·河南商丘·高三商丘市回民中学校考期末)一定条件下向某密闭容器中
加入 、 和一定量的B三种气体,图1表示各物质浓度随时间的变化关
系,图2表示速率随时间的变化关系, 时刻各改变一种条件,且改变的
条件均不同。若 时刻改变的条件是压强,则下列说法错误的是
A.若 ,则前 的平均反应速率
14
原创精品资源学科网独家享有版权,侵权必究!B.该反应的化学方程式为
C. 时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度
D.B的起始物质的量为
【答案】C
【分析】t 时正、逆反应速率中只有其中一个增大,应是改变某一物质的浓度,t 时改
2 4
变的条件为减小压强,说明反应前后气体的体积相等,t 时正逆反应速率都增大,应是
5
升高温度,由图甲可知,t 时到达平衡,△c(A)=0.09mol/L,△c(C)=0.06mol/L,二者
1
化学计量数之比为0.09:0.06=3:2,则B为生成物,反应方程式为3A(g) B(g)
+2C(g),结合浓度的变化解答该题。
【详解】A.若t=15s,生成物C在t∼t 时间段的平均反应速率为:v =
1 0 1
=0.004 mol L﹣1 s﹣1,A正确;
B.由以上分析可知反应的化学方程式为:3A(g) B(g)+2C(g),B正确;
C.t 时刻该变外界条件,其中某方向速率一瞬间不发生变化,另一方向化学反应速率
2
增大,故t 时刻该变的外加条件为增大反应物浓度,t 时刻错误该变外界条件,化学反
2 3
应速率均增大,且正逆化学反应速率相等,故t 时刻该变的外界条件可以是加入催化
3
剂或压缩体积加压或充入适量A、B、C,t 时刻后正逆化学反应速率均增大,其该变
5
外界条件可能为升温、充入相关参加反应的物质,C错误;
D.该反应的方程式为3A(g) B(g)+2C(g),根据方程式可知消耗0.09mol/L的A,则
生成0.03mol/L的B,容器的体积为2L,生成B的物质的量为
,平衡时B的物质的量为
,所以起始时B的物质的量为
0.1mol−0.06mol=0.04mol,D正确;
故答案为:C。
二、原理综合题
17.(2023秋·河南驻马店·高三河南省上蔡第一高级中学统考期末)二氧化碳加氢合
成甲醇是人工合成淀粉的首要步骤之一,同时也是实现碳中和的重要途径。该过程总
反应为CO(g)+3H(g) CHOH(g)+HO(g) H=-49.4kJ·mol-1。在特定催化剂条件下,
2 2 3 2
其反应机理如下: △Ⅰ.CO (g)+H(g) CO(g)+HO(g) H
2 2 2 1
Ⅱ.CO(g)+2H
2
(g) CH
3
OH(g) H
2
=△-90.3 kJ·mol-1
回答以下问题: △
(1) H=_______kJ·mol-1。
1
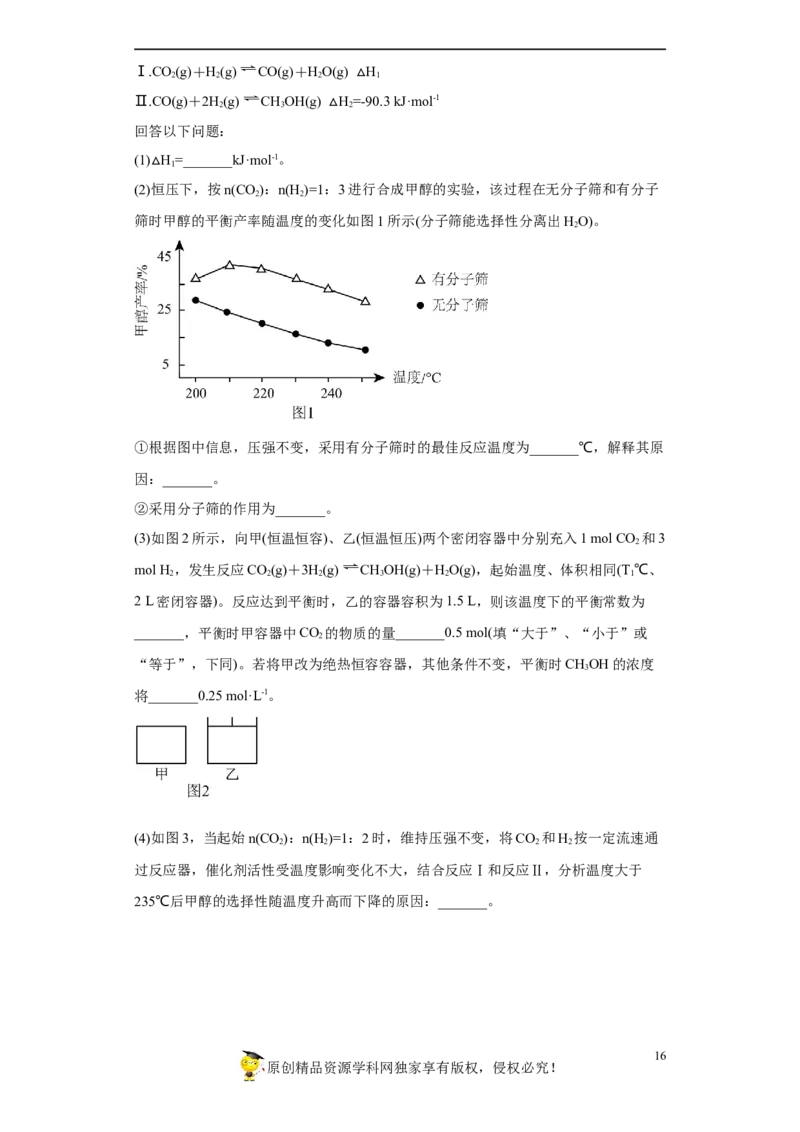
(2)△恒压下,按n(CO
2
):n(H
2
)=1:3进行合成甲醇的实验,该过程在无分子筛和有分子
筛时甲醇的平衡产率随温度的变化如图1所示(分子筛能选择性分离出HO)。
2
①根据图中信息,压强不变,采用有分子筛时的最佳反应温度为_______℃,解释其原
因:_______。
②采用分子筛的作用为_______。
(3)如图2所示,向甲(恒温恒容)、乙(恒温恒压)两个密闭容器中分别充入1 mol CO 和3
2
mol H,发生反应CO(g)+3H(g) CHOH(g)+HO(g),起始温度、体积相同(T ℃、
2 2 2 3 2 1
2 L密闭容器)。反应达到平衡时,乙的容器容积为1.5 L,则该温度下的平衡常数为
_______,平衡时甲容器中CO 的物质的量_______0.5 mol(填“大于”、“小于”或
2
“等于”,下同)。若将甲改为绝热恒容容器,其他条件不变,平衡时CHOH的浓度
3
将_______0.25 mol·L-1。
(4)如图3,当起始n(CO):n(H )=1:2时,维持压强不变,将CO 和H 按一定流速通
2 2 2 2
过反应器,催化剂活性受温度影响变化不大,结合反应Ⅰ和反应Ⅱ,分析温度大于
235℃后甲醇的选择性随温度升高而下降的原因:_______。
16
原创精品资源学科网独家享有版权,侵权必究!【答案】(1)+40.9
(2) 210 开始时温度低,反应速率慢,生成物(H O)还很少,分子筛的作用不明显,
2
随着产物增多,分子筛作用明显增强;210℃以后,温度对平衡的影响超过分子筛的作
用 分子筛从反应体系中不断分离出HO,减少了生成物,平衡正向移动,甲
2
醇产率升高
(3) (或0.33) 大于 小于
(4)反应I为吸热反应,反应II为放热反应,温度大于235℃时,随温度升高,反应I向
正反应方向进行,反应II向逆反应方向进行,故甲醇的选择性随温度升高而降低
【详解】(1)根据盖斯定律可知,反应I=总反应-反应II,则 H= H- H=(-49.4)-
1 2
( -90.3)=+40.9 kJ·mol-1; △ △ △
(2)①由图可知,压强不变,采用有分子筛时在温度210℃时甲醇的平衡产率最大,
则最佳反应温度为210℃;其原因是:开始时温度低,反应速率慢,生成物(H O)还很
2
少,分子筛的作用不明显,随着产物增多,分子筛作用明显增强;210℃以后,温度对
平衡的影响超过分子筛的作用;
②采用分子筛的作用为:分子筛从反应体系中不断分离出HO,减少了生成物,平衡
2
正向移动,甲醇产率升高;
(3)恒温恒压时,体积之比等于物质的量之比,即 ,由此计算可得,平衡后,
乙容器中气体的总物质的量为3mol,据此列出三段式:,则(1-x)+(3-3x)+x+x=3,
计算可得x=0.5,则该温度下的平衡常数为 ,
甲容器为恒温恒容条件,随着反应的进行,压强减小,CO 的转化率下降,故CO 的
2 2
物质的量大于0.5mol;若将甲改为绝热容器,此时容器内温度上升,CO 的转化率下
2
降,平衡时CHOH的浓度小于0.25mol/L;
3
(4)温度大于235℃后甲醇的选择性随温度升高而下降的原因:反应I为吸热反应,
反应II为放热反应,温度大于235℃时,随温度升高,反应I向正反应方向进行,反应
II向逆反应方向进行,故甲醇的选择性随温度升高而降低。
18.(2022秋·河南·高三校联考专题练习)近年来,全球丙烯需求快速增长,研究丙
烷制丙烯有着重要的意义。相关反应有:
I.C H 在无氧条件下直接脱氢:C H(g) C H(g)+H(g) H=+124kJ•mol-1
3 8 3 8 3 6 2 1
△
II.逆水煤气变换:CO(g)+H(g) CO(g)+HO(g) H
2 2 2 2
△
III.CO 氧化C H 脱氢制取丙烯:C H(g)+CO (g) C H(g)+CO(g)+HO(g) H
2 3 8 3 8 2 3 6 2 3
△
已知:CO和H 的燃烧热分别为-283.0kJ•mol-1、-285.8kJ•mol-1;
2
HO(g)=H O(l) H=-44kJ•mol-1
2 2
(1)反应II的 H△2 =______。
(2)下列说法正△确的是______。
A.升高温度反应I的平衡常数增大
B.选择合适的催化剂可提高丙烷平衡转化率
C.若反应II能自发,则 S<0
D.恒温恒压下,通入水蒸△气有利于提高丙烷转化率
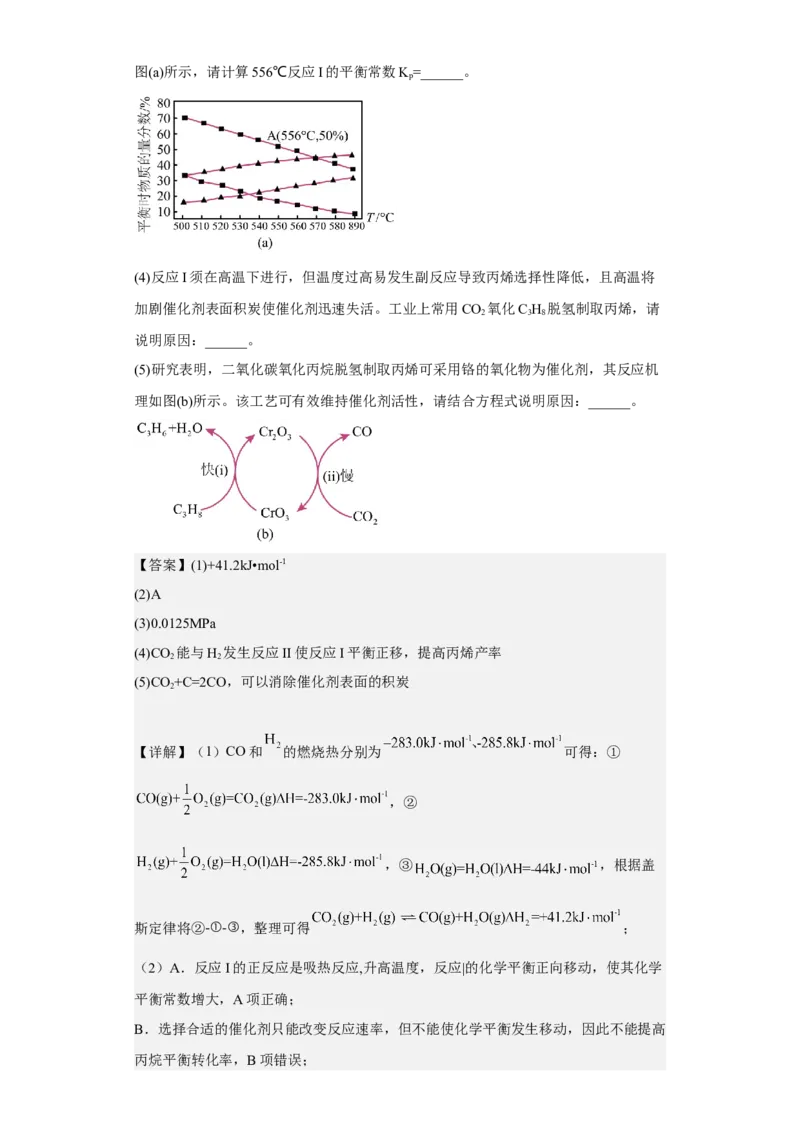
(3)对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常
数,记作K,如p(B)=p•x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。
p
在不同压强下(0.1MPa、0.01MPa),反应I中丙烷和丙烯的物质的量分数随温度变化如
18
原创精品资源学科网独家享有版权,侵权必究!图(a)所示,请计算556℃反应I的平衡常数K=______。
p
(4)反应I须在高温下进行,但温度过高易发生副反应导致丙烯选择性降低,且高温将
加剧催化剂表面积炭使催化剂迅速失活。工业上常用CO 氧化C H 脱氢制取丙烯,请
2 3 8
说明原因:______。
(5)研究表明,二氧化碳氧化丙烷脱氢制取丙烯可采用铬的氧化物为催化剂,其反应机
理如图(b)所示。该工艺可有效维持催化剂活性,请结合方程式说明原因:______。
【答案】(1)+41.2kJ•mol-1
(2)A
(3)0.0125MPa
(4)CO 能与H 发生反应II使反应I平衡正移,提高丙烯产率
2 2
(5)CO +C=2CO,可以消除催化剂表面的积炭
2
【详解】(1)CO和 的燃烧热分别为 可得:①
,②
,③ ,根据盖
斯定律将②-①-③,整理可得 ;
(2)A.反应I的正反应是吸热反应,升高温度,反应|的化学平衡正向移动,使其化学
平衡常数增大,A项正确;
B.选择合适的催化剂只能改变反应速率,但不能使化学平衡发生移动,因此不能提高
丙烷平衡转化率,B项错误;C.根据(1)计算可知反应|I热化学方程式为
该反应的正反应是吸热反应,若
△S < 0则△G=△H - T△S> 0,反应不能自发进行,C项错误;
D.该反应的正反应是气体体积增大的反应,在恒温恒压下通入水蒸气,体系的体积
增大,化学平衡逆向移动,不利于提高丙烷转化率,D项错误;
答案选A。
(3)反应I的正反应是气体体积增大的吸热反应,在压强不变时,升温,化学平衡正向
移动, 的物质的量分数减小;在温度不变时,加压,化学平衡逆向移动, 的物
质的量分数增大,所以A点表示0.1 MPa、556 ℃时 平衡时的物质的量分数,则
平衡时物质的量分数均为25%,
;
(4)工业上常用 氧化 ,脱氢制取丙烯,这是由于 能与 发生反应,使反
应I平衡正向移动,从而提高丙烯产率。
(5)该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,这是由于C能够与
反应生成CO,使C脱离催化剂表面;
19.(2022秋·天津河北·高三天津十四中校考期末)利用甲醇 制备一些高附
加值产品,是目前研究的热点。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ.
反应Ⅱ.
反应Ⅲ.
20
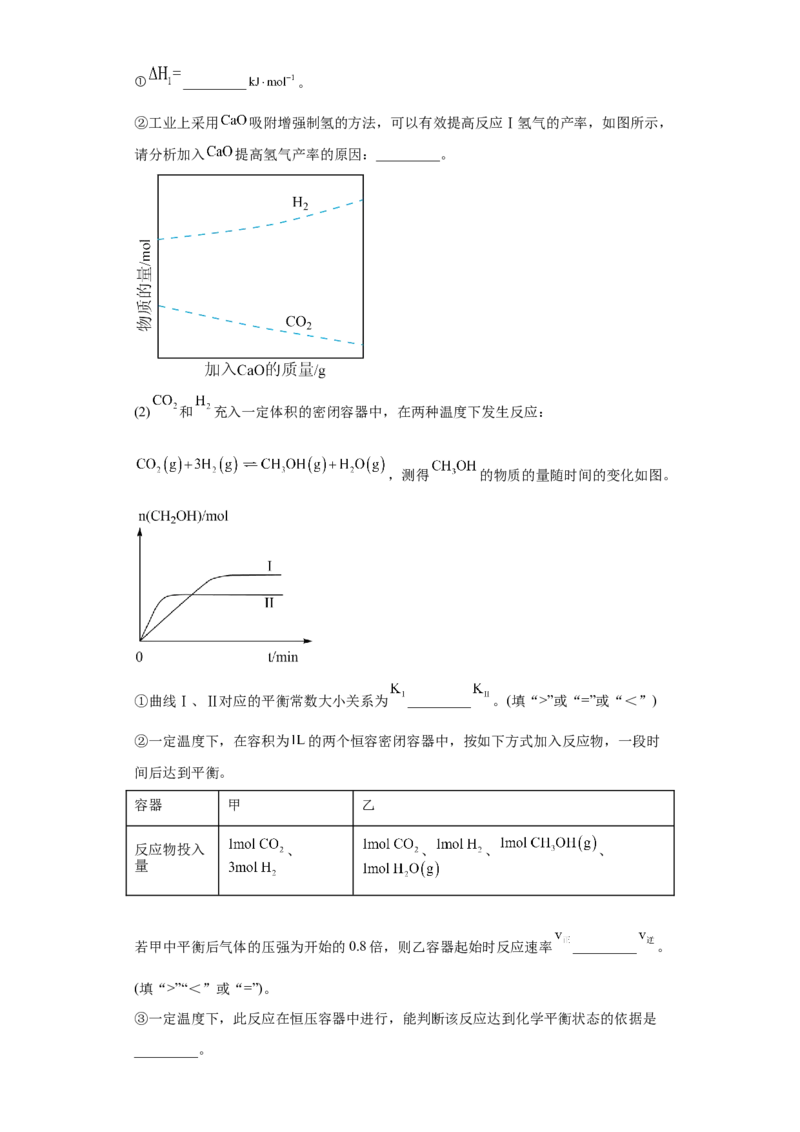
原创精品资源学科网独家享有版权,侵权必究!① _________ 。
②工业上采用 吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,
请分析加入 提高氢气产率的原因:_________。
(2) 和 充入一定体积的密闭容器中,在两种温度下发生反应:
,测得 的物质的量随时间的变化如图。
①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为 _________ 。(填“>”或“=”或“<”)
②一定温度下,在容积为 的两个恒容密闭容器中,按如下方式加入反应物,一段时
间后达到平衡。
容器 甲 乙
反应物投入 、 、 、 、
量
若甲中平衡后气体的压强为开始的0.8倍,则乙容器起始时反应速率 _________ 。
(填“>”“<”或“=”)。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是
_________。a.容器中压强不变
b. 的体积分数不变
c.
d.容器中密度不变
e.2个 断裂的同时有3个 断裂
(3)已知电离常数 : , : , ,则
向 溶液中通入少量 时的离子方程式为_________。
(4)利用人工光合作用,借助太阳能使 和 转化为 ,如图所示,在催化
剂b表面发生的电极反应为:_________。
【答案】(1) b—a CaO消耗CO,生成物CO 的浓度减小,平衡向正反应方向移
2 2
动,氢气的产率增大
(2) > < bd
(3)CO +CN—+H O=HCN+HCO
2 2
(4)CO +2H++2e—=HCOOH
2
【详解】(1)①由盖斯定律可知,反应Ⅲ—反应Ⅱ可得反应Ⅰ,则ΔH=ΔH—ΔH=(b
1 3 2
—a)kj/mol,故答案为:b—a;
②二氧化碳能与氧化钙反应生成碳酸钙,则加入氧化钙可以使反应Ⅰ生成的二氧化碳
浓度减小,平衡向正反应方向移动,氢气的产率增大,故答案为:CaO消耗CO,生
2
成物CO 的浓度减小,平衡向正反应方向移动,氢气的产率增大;
2
(2)①由图可知,曲线Ⅱ达到平衡达到平衡所需时间小于曲线Ⅰ,甲醇的物质的量小
于曲线Ⅰ说明反应温度Ⅱ大于Ⅰ,平衡向逆反应方向移动,该反应为放热反应,所以
22
原创精品资源学科网独家享有版权,侵权必究!化学平衡常数K 大于K ,故答案为:>;
I II
②设甲中平衡水蒸气的浓度为amol,由题意可建立如下三段式:
由平衡后气体的压强为开始的0.8倍可得: = ,解得a=0.4,则平衡时二氧化碳、
氢气、甲醇、水蒸气的浓度分别为0.6mol/L、1.8mol/L、0.4mol/L、0.4mol/L,反应的
平衡常数K= ≈0.046,容器乙中的浓度熵Q= =1>K,所以反应向正反应方
c
向进行,正反应速率大于逆反应速率,故答案为:>;
③a.恒压容器中混合气体的压强始终不变,则容器中压强不变不能说明正逆反应速率
相等,无法判断反应是否达到平衡,故错误;
b.氢气的体积分数不变说明正逆反应速率相等,反应已达到平衡,故正确;
c. 不能说明正逆反应速率相等,无法判断反应是否达到平衡,故
错误;
d.由质量守恒定律可知,反应前后气体的质量相等,该反应是气体体积减小的反应,
反应中气体体积减小,混合气体的密度增大,则容器中密度不变说明正逆反应速率相
等,反应已达到平衡,故正确;
e.2个 断裂的同时有3个 断裂均代表正反应速率,不能说明正逆反应速率
相等,无法判断反应是否达到平衡,故错误;
故选bd;
(3)由电离常数可知,氢氰酸的电离程度大于碳酸氢根离子,小于碳酸,所以由强酸
制弱酸的原理可知,氰化钾溶液与二氧化碳反应生成氢氰酸和碳酸氢钾,反应的离子
方程式为CO+CN—+H O=HCN+HCO ,故答案为:CO+CN—+H O=HCN+HCO ;
2 2 2 2
(4)由图中电子移动方向可知,催化剂b为原电池的正极,酸性条件下二氧化碳在正
极得到电子发生还原反应生成甲酸,电极反应式为CO+2H++2e—=HCOOH,故答案为:
2
CO+2H++2e—=HCOOH。
2
20.(2022秋·陕西西安·高三统考期末)习近平主席在第75届联合国大会提出我国要
实现2030年碳达峰、2060年碳中和的目标。因此 的捕获、利用与封存成为科学家研究的重要课题。研究表明 和 在催化剂存在下可发生反应制得合成气:
。回答下列问题:
(1)已知 、 和 的燃烧热 分别为 、
和 。上述反应的焓变 _________ 。
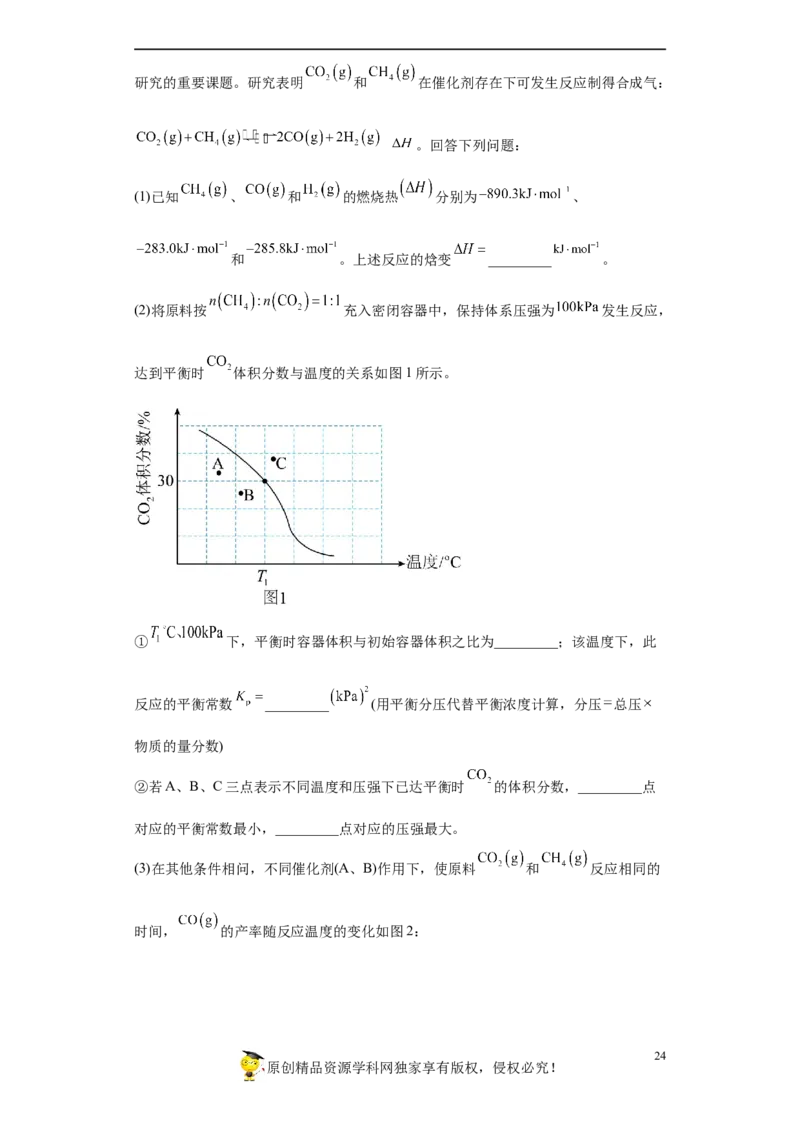
(2)将原料按 充入密闭容器中,保持体系压强为 发生反应,
达到平衡时 体积分数与温度的关系如图1所示。
① 下,平衡时容器体积与初始容器体积之比为_________;该温度下,此
反应的平衡常数 _________ (用平衡分压代替平衡浓度计算,分压 总压
物质的量分数)
②若A、B、C三点表示不同温度和压强下已达平衡时 的体积分数,_________点
对应的平衡常数最小,_________点对应的压强最大。
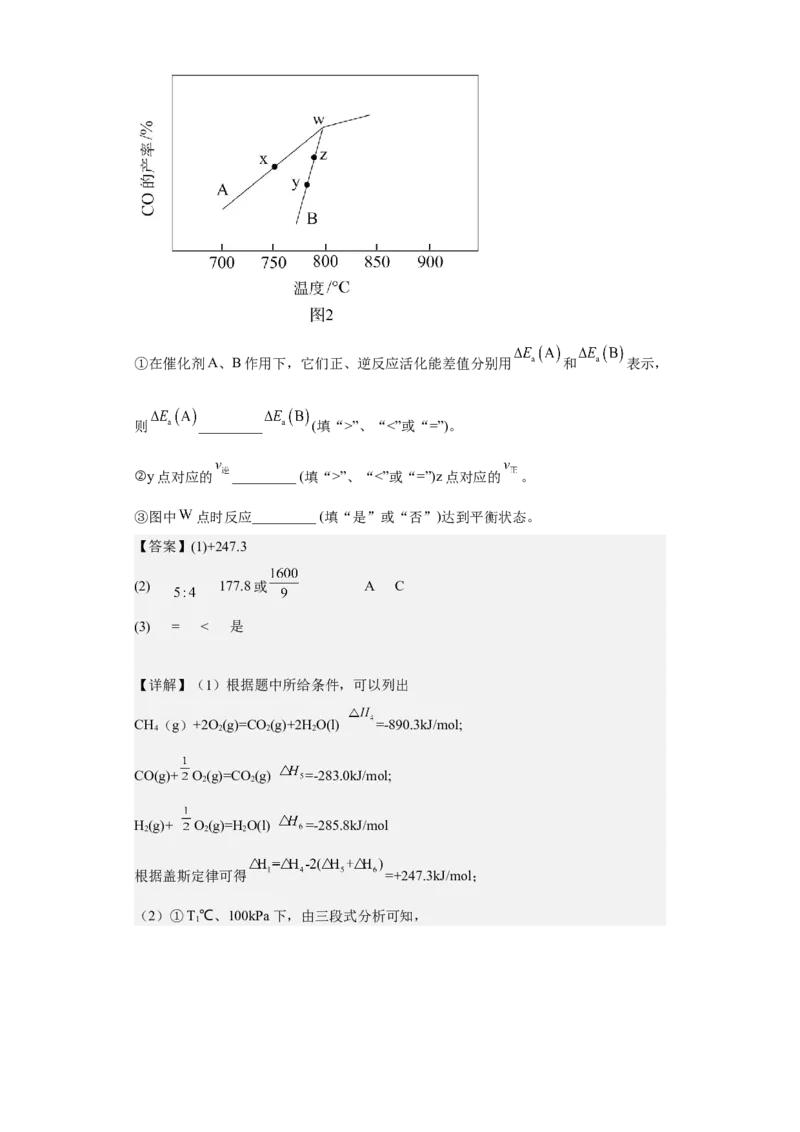
(3)在其他条件相问,不同催化剂(A、B)作用下,使原料 和 反应相同的
时间, 的产率随反应温度的变化如图2:
24
原创精品资源学科网独家享有版权,侵权必究!①在催化剂A、B作用下,它们正、逆反应活化能差值分别用 和 表示,
则 _________ (填“>”、“<”或“=”)。
②y点对应的 _________ (填“>”、“<”或“=”)z点对应的 。
③图中 点时反应_________ (填“是”或“否”)达到平衡状态。
【答案】(1)+247.3
(2) 177.8或 A C
(3) = < 是
【详解】(1)根据题中所给条件,可以列出
CH(g)+2O (g)=CO (g)+2HO(l) =-890.3kJ/mol;
4 2 2 2
CO(g)+ O(g)=CO (g) =-283.0kJ/mol;
2 2
H(g)+ O(g)=HO(l) =-285.8kJ/mol
2 2 2
根据盖斯定律可得 =+247.3kJ/mol;
(2)①T℃、100kPa下,由三段式分析可知,
1,根据气体的体积分数即为物质的
量分数,故有: =30%,即得:x=0.25a,n(初始气体):n(平衡时气体)=2a:
(2a+2x)=2a:(2a+2×0.25a)=4:5,同温同压,体积之比等于物质的量之比,平衡时容器
体积与初始容器体积之比为5:4;该温度下,CH、CO、CO、H 的平衡分压分别为:
4 2 2
p(CH)= p(CO )= = =30kPa,,p(CO)=p(H )= =
4 2 2
=20kPa,此反应的平衡常数Kp= = =
(kPa)2,故答案为:5:4; ;
②若A、B、C三点表示不同温度和压强下已达平衡时CO 的体积分数,由于平衡常数
2
仅仅是温度的函数,且该反应正反应是一个吸热反应,升高温度平衡正向移动,平衡
常数增大,A点对应的平衡常数最小;该反应增大压强平衡逆向移动,CO 的体积分
2
数增大,故C点对应CO 的体积分数大,温度高,压强最大,故答案为:A;C;
2
(3)①在催化剂A、B作用下,它们正、逆反应活化能差值即该反应的反应热 ,
催化剂影响反应速率但不影响反应的焓变,分别用E(A)、E(B)表示,则E(A)=E(B),
故答案为:=;
②由图可知,y点对应的温度低于z点对应的温度,温度越高反应速率越快,故y点对
应的 <z点对应的 ,故答案为:<;
(逆) (正)
③催化剂改变反应速率,但不影响平衡状态,W点及之后升温,一氧化碳的产率相同,
说明反应已达到平衡。
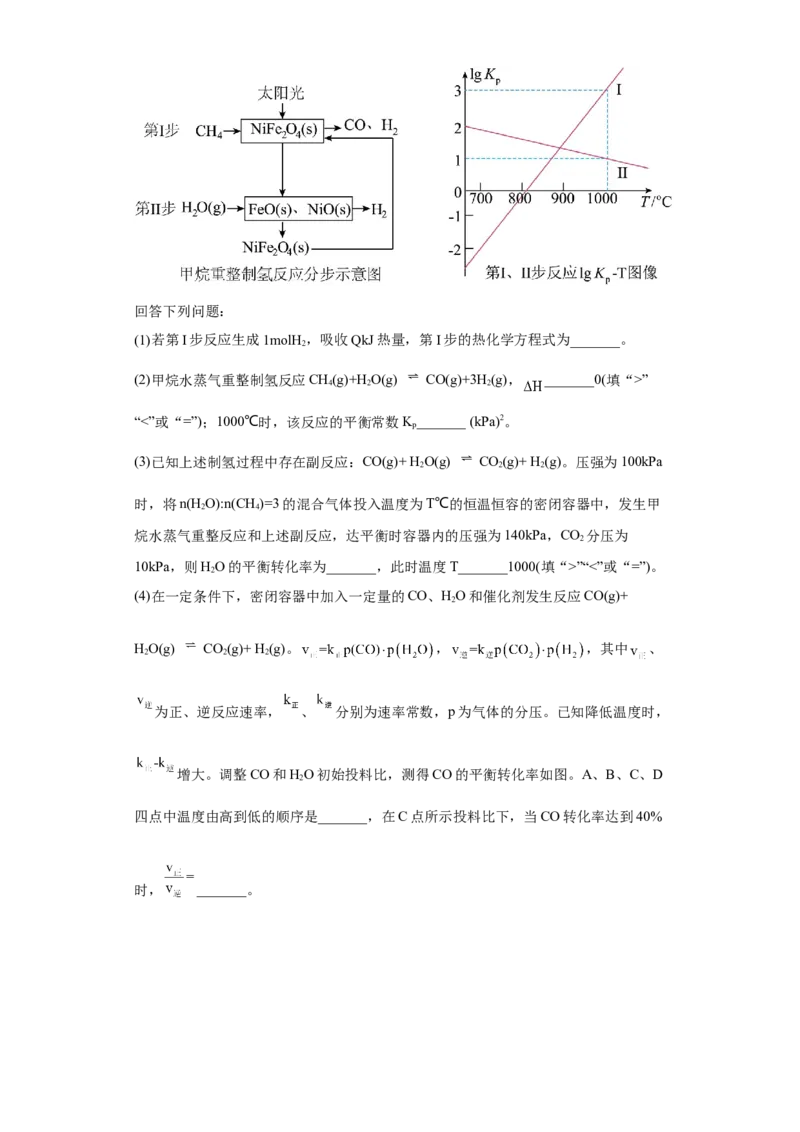
21.(2023秋·山东烟台·高三统考期末)一种利用太阳能催化甲烷水蒸气重整制氢反
应原理及各步反应以气体分压(单位为)表示的平衡常数与温度T变化关系如图所示。
26
原创精品资源学科网独家享有版权,侵权必究!回答下列问题:
(1)若第I步反应生成1molH ,吸收QkJ热量,第I步的热化学方程式为_______。
2
(2)甲烷水蒸气重整制氢反应CH(g)+HO(g) CO(g)+3H(g), _______0(填“>”
4 2 2
“<”或“=”);1000℃时,该反应的平衡常数K_______ (kPa)2。
p
(3)已知上述制氢过程中存在副反应:CO(g)+ H O(g) CO(g)+ H (g)。压强为100kPa
2 2 2
时,将n(H O):n(CH )=3的混合气体投入温度为T℃的恒温恒容的密闭容器中,发生甲
2 4
烷水蒸气重整反应和上述副反应,达平衡时容器内的压强为140kPa,CO 分压为
2
10kPa,则HO的平衡转化率为_______,此时温度T_______1000(填“>”“<”或“=”)。
2
(4)在一定条件下,密闭容器中加入一定量的CO、HO和催化剂发生反应CO(g)+
2
HO(g) CO(g)+ H (g)。 , ,其中 、
2 2 2
为正、逆反应速率, 、 分别为速率常数,p为气体的分压。已知降低温度时,
增大。调整CO和HO初始投料比,测得CO的平衡转化率如图。A、B、C、D
2
四点中温度由高到低的顺序是_______,在C点所示投料比下,当CO转化率达到40%
时, _______。【答案】(1)
(2) >
(3) >
(4) B> A>C>D
【详解】(1)第I步反应为甲烷和 反应生成 、 、一氧化碳和氢气,
若生成1molH ,吸收QkJ热量,第I步的热化学方程式为
2
;
(2)由图可知,第Ⅱ步的反应为 ,
反应I+反应Ⅱ得: ,则反应的 ,则
1000℃时,该反应的平衡常数 (kPa)2;由图可知, 斜率更大受温
度影响更大且随温度升高而变大,故 也随温度升高而变大,升高温度平衡正向移动,
则反应为吸热反应,焓变大于零;
(3)压强为100kPa时,将n(H O):n(CH )=3的混合气体投入温度为T℃的恒温恒容的
2 4
密闭容器中,则水、甲烷初始压强分别为25kPa、75kPa;副反应为气体分子数不变的
反应,不会改变压强,重整反应为气体分子数增加2的反应,达平衡时容器内的压强
为140kPa,则反应甲烷压强为(140kPa-100kPa)÷2=20 kPa;
28
原创精品资源学科网独家享有版权,侵权必究!则HO的平衡转化率为 ;由三段式可知,此时重整反应的
2
,重整反应为吸热反应,K值变大,则温
度升高,故温度T大于1000。
(4)已知降低温度时, 增大,则说明正反应速率增大,反应正向进行,为放热
反应;增加一氧化碳的投料会降低一氧化碳的转化率、降低温度平衡正向移动会提高
一氧化碳的转化率,故温度A大于C大于D;投料比相同,B点转化率更低,则温度
B大于A;故A、B、C、D四点中温度由高到低的顺序是B> A>C>D;
在C点所示投料比下,若一氧化碳和水的投料浓度均为1mol/L,一氧化碳的平衡转化
率为50%:
此时 = , ,
;
当CO转化率达到40%时:。
30
原创精品资源学科网独家享有版权,侵权必究!