文档内容
专题十 工艺流程题
必备知识 解读
一、高考精细审题
一.题干信息提供
1.描述:提供如下信息
①原料 :原料中有哪些元素及元素以何种化合物或单质形式存在。
②制备目标产品
③工艺过程中未知的陌生反应的产物和一些除杂信息。
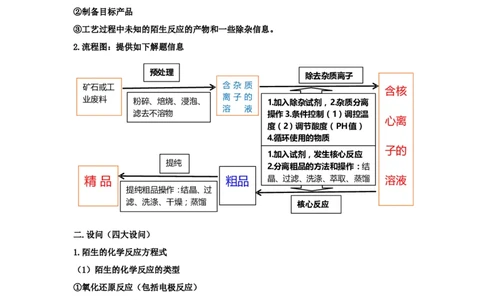
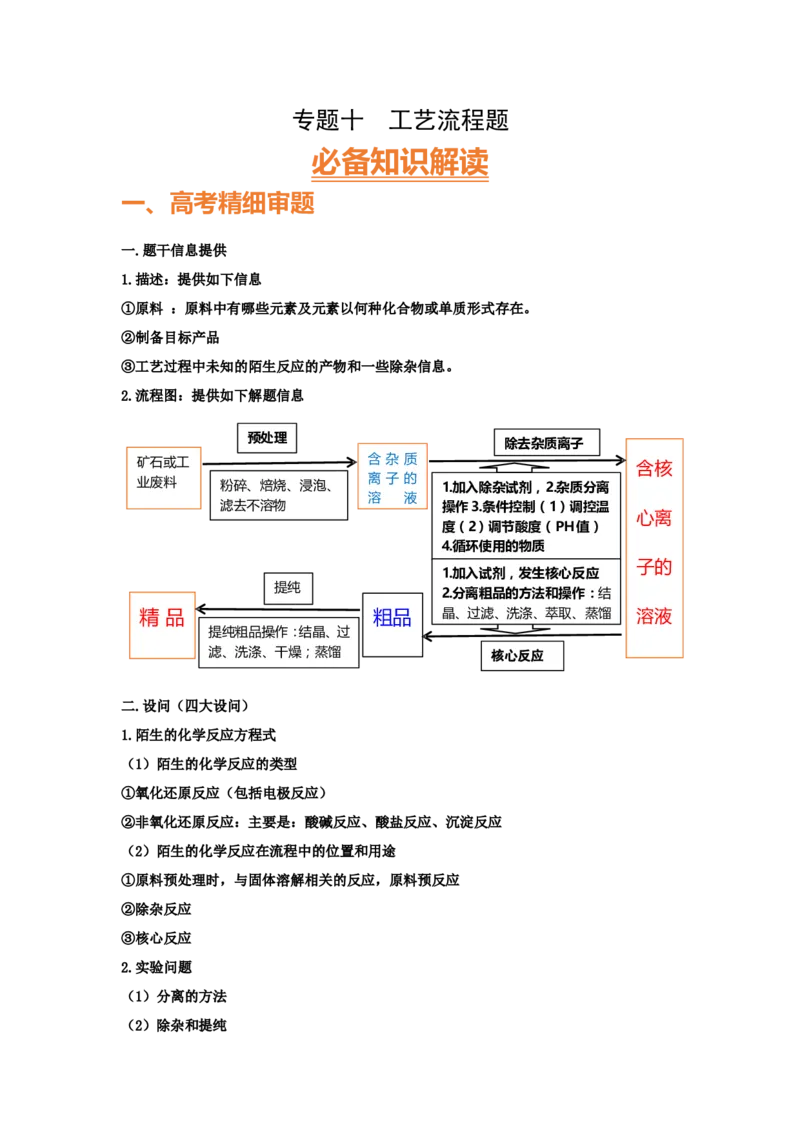
2.流程图:提供如下解题信息
预处理
除去杂质离子
矿石或工 含 杂 质
含核
业废料 粉碎、焙烧、浸泡、 离 子 的 1.加入除杂试剂,2.杂质分离
溶 液
滤去不溶物 操作3.条件控制(1)调控温
心离
度(2)调节酸度(PH值)
4.循环使用的物质
子的
1.加入试剂,发生核心反应
提纯
2.分离粗品的方法和操作:结
精 品 粗品 晶、过滤、洗涤、萃取、蒸馏 溶液
提纯粗品操作:结晶、过
滤、洗涤、干燥;蒸馏 核心反应
二.设问(四大设问)
1.陌生的化学反应方程式
(1)陌生的化学反应的类型
①氧化还原反应(包括电极反应)
②非氧化还原反应:主要是:酸碱反应、酸盐反应、沉淀反应
(2)陌生的化学反应在流程中的位置和用途
①原料预处理时,与固体溶解相关的反应,原料预反应
②除杂反应
③核心反应
2.实验问题
(1)分离的方法
(2)除杂和提纯(3)控制条件的方法
3.原因分析
(1)加入试剂的原因
(2)升温或降温的原因
(3)加入过量试剂的原因
(4)摩擦试管壁或其它操作的原因
4.计算问题
(1)PH值的计算
(2)浓度的计算
(3)电化学计算
(4)产品纯度或原料利用率的计算
二、考题流程四步
第一步.原料预处理
第二步.预处理得到的溶液,进行离子除杂,得到核心离子
第三步.核心离子溶液中加入试剂。经过核心反应得到粗品
第四步.粗品提纯得到精品产物
应考能力 解 密
问题一.原料预处理
一、表面处理
1.除去油污:碱煮水洗、灼烧
2.除氧化膜:打磨、化学方法。
二、细化(粉碎)处理
1.粉碎或研磨:增大固液(或固气或固固)接触面积,加快反应(溶解)速率,增大原料
的转化率(或浸取率),提高原料利用率。
2.喷洒、雾化(用多孔分散器):增大气--液接触面积,加快反应(溶解)速率,增大原
料的转化率(或浸取率),提高原料利用率。
三、灼烧、焙烧或煅烧处理
1.焙烧的目的:
(1)除掉油污、有机物或某些可燃杂质。(2)空气氧化某种元素,使它转化为某气体或某种产物,再加酸溶解。
(3)原料之间高温下反应。如:MnO 和FeS
2
2.有时要书写焙烧的化学方程式。如:CuFeS 灼烧氧化为SO、CuO、FeO。
2 2 2 3
四、溶浸(溶解)处理
1.增 大 原 料 浸 出 率 (或)浸 出速 率) 的 措 施 :
(1) 浸 出 率: 浸 出 的有用成份占总原料的比例
搅 拌、 升 高 温 度 、减小 气 体 的 流 速 ( 浓 度 、 压 强 ) ,粉碎、
增 大 气 液 或 固 液 接 触 面 积增加浓度 、延 长 浸 出 时 间
(2)浸 出速 率:浸 出快慢
搅 拌 、 升 高 温 度 、 恰当的气 体 流 速 ( 浓 度 、 压 强 ) , 粉碎、增 大
气 液 或 固 液 接 触 面 积增加浓度
2.水溶
煅烧处理后,原料发生变化,产生能溶于水或有水参加能发生反应的物质,就要水溶解。
3.碱溶的目的:
(1)除去油污
(2)除去金属铝、SiO 等杂质(与NaOH反应)
2
4.酸浸的目的:
(1)溶解、去氧化物(膜)、调节pH促进水解(生成沉淀)
(2)酸与矿石中的盐、金属氧化物发生反应;
(3)加入氧化剂或还原剂,作酸性介质。
五、生成目标产物中有用的离子,要书写预处理化学方程式。
矿石或废料的煅烧、酸溶、碱溶时的反应
1.矿石或废料的煅烧:一般是易被空气氧化或易分解的矿物,如:含硫矿石,硫被氧化成
SO.所加的原料之间,也可以发生反应。
2
2.酸溶:与酸能发生反应的矿石或废料:金属氧化物或金属弱酸盐,有些两性的金属高价
产物,题目会告知。如:CaF(PO) 与HSO 反应。
5 4 3 2 4
3.碱溶:“碱作用”还可以除去油污、除去铝片氧化物、溶解铝、二氧化硅,主要是铝和
二氧化硅与NaOH反应。
4.所加的原料之间,也可以发生反应,如:软锰矿与硫铁矿石(MnO 和FeS)
2 2
问题二.预处理得到的溶液,进行离子除杂,得到核心离子
一.加入试剂
1.某试剂的作用:1)调节PH值。
2)做氧化剂:如:HO、MnO、KMnO、KCIO
2 2 2 4 3
3)做还原剂:如:NaSO
2 3
4)做沉淀剂:如:F-(沉淀Ca2+、Mg2+离子)、S2-(沉淀Cu2+、Zn2+离子)
5)可循环使用的试剂:在流程中出现两次,一次使用、一次产出。
2.试剂的用量调控
(1)用量过多:浪费试剂 溶液的PH可能发生变化发生付反应后续处理浪费其它的试剂。
(2)用量过少:反应不充分或沉淀不彻底反应速率不快
3.加入方式:分步多次加入,利于充分反应。
二.控制条件
(一)温度控制
1.加 热 的 目 的 :
(1)煮沸蒸馏水是为了赶走水中的氧气。
(2)有时产生沉淀时加热,为了防止产生胶体,不利于沉淀生成。
(3)促进有利水解
(4)加快反应速率
2.加热的方式
(1)水浴:温度在100 ℃以下,易于控制温度,且受热均匀。
(2)油浴:温度在98 ℃以上,易于控制温度,且受热均匀。
(3)保温回流:让反应物充分反应,提高产率。
3.温度过高:从如下五个方面考滤后果。
(1) 温度太高,会消耗更多的资源,成本高。
(2) 温度太高,可能会导致催化剂失活,相同时间内的转化率变小。
(3) 温度升高,平衡向逆向移动,转化率变小。正反应是放热反应。
(4) 温度升高,某些物质会分解。如HO、NHHO、NHHCO
2 2 3 2 4 3
(5) 温度升高,某些物质会挥发。如HO、NHHO、
2 2 3 2
(6) 温度升高,促进不利水解
(7) 温度升高,促进不利付反应
4.温度过低:从如下三个方面考滤后果。
(1)温度太低,化学反应速率慢,但是,转化率可能高。
(2)温度太低,不该析出的物质,可能从溶液中析出晶体。
(3)温度太低,某些物质的状态可能会发生变化。(二).酸碱性控制
1.调节PH的目的:生成沉淀,除去杂质。
(1)调控水解,使某些离子沉淀如Fe3+(生成Fe(OH)、下同)、Cu2+、Al3+。
3
(2)保留某些物质使其转化为PH范围内的离子状态、不产生沉淀。
2.调节PH的试剂:
(1)酸性溶液要调节PH:只要能和酸反应的都可以。
如:单质:Zn、Fe、Al都行,能和H+反应的金属。
化合物:氧化锌、氧化铁、氧化铝、氧化铜、氢氧化物、碳酸盐、氢氧化钠、氨水。
(2)如果调节PH时,目标产物是沉淀,与加入的试剂中离子无关的,可以用:氢氧化
钠、氨水。
(3)如果目标产物不是沉淀,而是从溶液中析出的晶体,就不能引入新的杂质,要加入需
要保留的金属离子的氧化物、氢氧化物、碳酸盐、碱式碳酸盐。
三、杂质的分离
(一)固体-液体分离
1.滤渣成份:
(1)题目告知的沉淀。
(2)滤渣是不和酸反应的物质:SiO、MnO、S
2 2
(3)被C或CO还原的铜。
(4)若溶液中有Ca2+,和硫酸反应产生的CaSO。和碳酸钠反应产生的CaCO
4 . 3
(5) 调节PH产生的氢氧化铁、氢氧化铝、氢氧化铜。
(6)不与碱溶液反应的金属氧化物
2.过滤的方法-除去被沉淀的离子
(1)常温常压过渡
(2)趁热过滤(保温漏斗):以保证溶液中的某些杂质物质不析出。
(3)加速过渡(抽滤、减压过渡):加快过滤的速率。
3.检 验 溶 液 中 离 子 是 否 沉 淀 完 全 的 方 法 :
将 溶 液 静 置 一 段 时 间 后 , 向 上 层 清 液 中 滴 入 对 应 的 沉 淀 剂 (
必 要 时 先 加 酸 酸 化 排 除 其 他 离 子 的 干 扰 ) , 若 无 沉 淀 生 成
, 则 离 子 沉 淀 完 全 ( 写 出 详 细 的 操 作 、 现 象 、 结 论 )
4.促进沉淀析出的方法:
(1)摩察试管内壁,防止形成胶体,利于沉淀析出。
(2)升高温度,防止形成胶体,利于沉淀析出。(3)加入过量的电解质溶液,使胶体形成沉淀。
(二)液体-液体
1.蒸馏:分离沸点不同的两种相溶的液体。
2.萃取-反萃取-分液
四.书写除杂反应方程式:如:NaF除去Ca2+、Mg2+。
问题三.核心离子溶液中加入试剂。经过核心反应得到粗品
一、加入试剂,发生核心反应,书写核心反应方程式
1.流程中的非氧化还原反应:元素化合价无变化则为非氧化还原反应,遵循质量守恒定
律。要求写离子方程式。主要有:酸碱反应、酸盐反应、沉淀反应。
如:用碳酸铵溶液与含硫酸镁的溶液反应生成Mg(OH)∙MgCO,这就是碱式碳酸镁沉淀,要
2 3
写沉镁过程的离子反应;硫酸亚铁溶液加入碳酸氢钠反应的离子方程式。
又如:NaFeO 转化为KFeO 的反应:KFeO 的溶解度比NaFeO 的溶解度小。
2 4 2 4 2 4 2 4
2.化工流程中陌生氧化还原反应方程式的书写
化工流程中陌生化还原反应的书写思路 :元素化合价有变化则为氧化还原反应,除遵循质
量守恒外,还要遵循得 失电子守恒规律。最后根据题目要求写出化学方程式或离子方
程式(需要遵循 电荷守恒规律)即可。
氧化还原反应方程式的书写: 首先确定“两剂两产物”,即氧化剂、还原剂、氧化产物和
还原产物。接下来三步配平方程式。
①根据化合价升降法配平两剂两产物;
②氧化剂和还原剂中的元素与还原产物、氧化产物中的元素对应配平;
③如是离子方程式,要根据电荷守恒补充 H+和 OH-;
根据原子守恒补充 HO 配平氢元素,最后配平所有原子。
2
二.分离粗品的方法和操作
1.从 滤 液 中 提 取 一 般 晶 体 的 方 法:
晶体类型: 溶 解 度 随 温 度 升 高 而 增 大 的 晶 体 ,带结晶水,易水解的晶
体 ,易分解的 晶 体 ,
结晶方法:蒸 发 浓 缩 < 至 有 晶 膜 出 现 >、 冷 却 结 晶 、 过 滤 、 洗 涤 (
冰 水 洗 、 热 水 洗 、 乙 醇 洗 ) 、 干 燥
2.从 滤 液 中 提 取晶体的另一种 的 方 法:
晶体类型: 溶 解 度 受 温 度 影 响 较 小 或 随 温 度 升 高 而 减 小 的 晶 体 ,
如 NaC l
结晶方法: 蒸 发结晶 、 趁热 过 滤 <如 果 温 度 下 降 , 杂 质 也 会 以 晶 体的 形 式 析 出 来 >、 洗 涤 、 干 燥
问题四.粗品提纯得到精品产物
一.电化提纯:
通过电解法提纯,要书写电极反应
二.目标产物过滤后,需要洗涤。
1. 洗 涤 的 目 的 :提纯目标产物
洗掉沉淀或者晶体表面可能吸附的可溶性离子.
尽量减少沉淀或者晶体的损失。
2.检 验 沉 淀 是 否 洗 涤 干 净 的 方 法 :
取最后一次洗涤液,加入一种试剂,这种试剂,能够与溶液中存在并且有可能被沉淀吸附
的离子反应生成沉淀。所以,要明确沉淀从什么溶液中析出。往往要检验的是:
SO2-、Cl-。
4
3.洗涤试剂:
(1)乙醇洗涤:
降 低 被 洗 涤 物 质 的 溶 解 度 , 减 少 被 洗 涤 物 质 的 溶 解 损 耗 , 得
到 较 干 燥 的 产 物
快速除去表面水份,减少晶体损失。
(2)冷水:
洗 去 晶 体 表 面 的 杂 质 离 子 并 降 低 被 洗 涤 物 质 的 溶 解 度 , 减 少
其 在 洗 涤 过 程 中 的 溶 解 损 耗,提高产率。
防水解
(3)用某种溶液洗涤:
减少固体在水中的溶解度;
除去杂质,与溶液中的某些离子可以反应,以洗掉某些物质。
(4)有机溶剂: 减 少 产 品的 溶 解 损 耗 ,提高产率。防止产品可能的水解。
4.怎样洗沉淀:在过滤器中直接洗。
在过滤器中加少量水,使水浸没沉淀,等水滤下,反复操作2-3次即可。
三.蒸馏:粗液体产物提纯方法,是蒸馏
四.重结晶:固体产物提纯方法,是重结晶
问题五、计算问题一、计算控制条件中的相关数据
1.M(OH) 悬浊液中K 、K、pH之间的关系:
n sp W
M(OH)(s) Mn+(aq)+nOH-(aq)
n
K =c(Mn+)·cn(OH-)= c(OH-)·cn(OH-)=cn+1(OH-) = 1( K )n+1。
sp W
n n n 10-pH
由此可求:
已知Ks和离子浓度,求开始沉淀时的PH值
已知Ks和完全沉淀时的离子浓度(小于10-5),求开始沉淀时的PH值
已知完全沉淀时的PH值,求离子浓度
2.已知两个Ks和离子浓度,求一个离子完全沉淀(开始沉淀)时,另一离子的浓度
M(OH)(s) Mn+(aq)+nOH-(aq) K =c(Mn+)·cn(OH-)
n spM(OH)n
N(OH)(s) Nn+(aq)+nOH-(aq) K =c(Nn+)·cn(OH-)
n spNOH)n
两个Ksp都有OH-,已知其一可求另外一个离子浓度
3.沉淀转化的计算
二.计算纯度、原料利用率
产品的纯净质量
(1)纯度= ×100%
粗产品的质量
原料的转化质量
(2)原料利用率= ×100%
原料的总质量
三.电化学和氧化还原反应的计算
(1)根据得失电子守恒关系建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:
(式中M为金属,n为其离子的化合价数值)
(2)根据得失电子守恒关系可以计算氧化剂、还原剂、氧化产物、还原产物的物质的量的
比以及质量
高考实例剖析高考实例剖析--
高考怎么考《工艺流程题》,根据高考指挥棒来学习《工艺流程题》
【高考实例一】
ZnSO
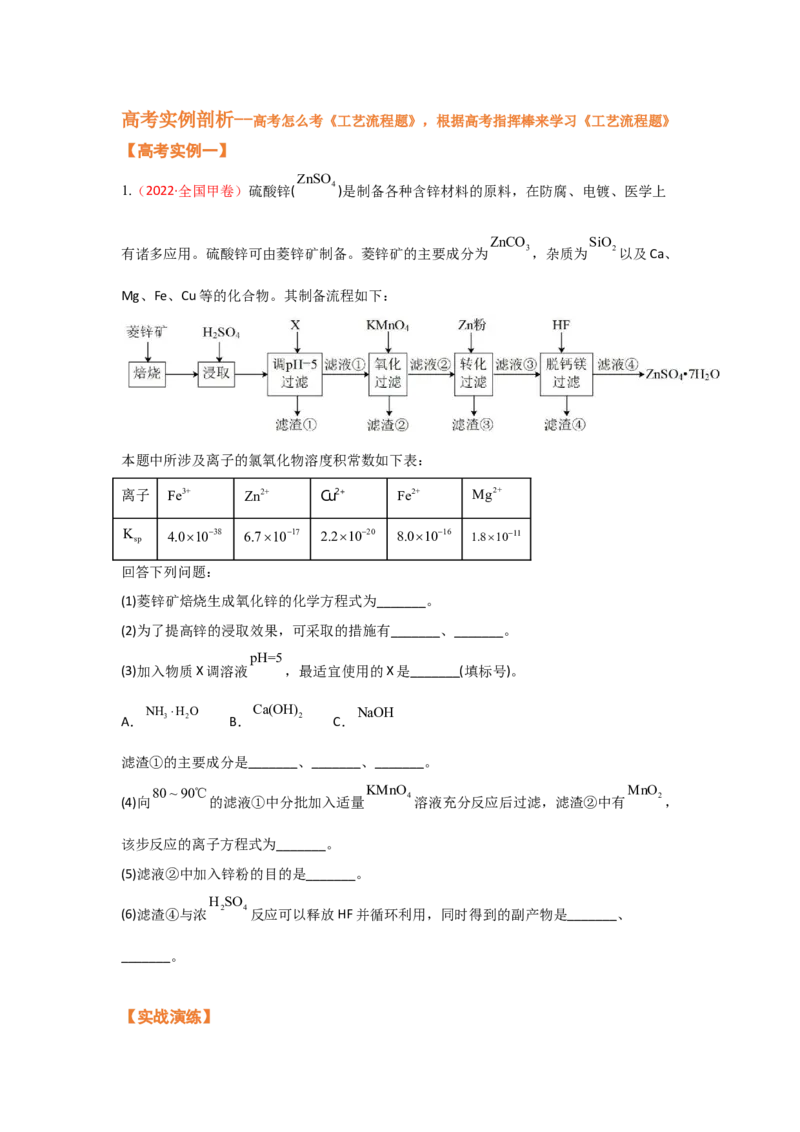
1.(2022·全国甲卷)硫酸锌( 4 )是制备各种含锌材料的原料,在防腐、电镀、医学上
ZnCO SiO
有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 3,杂质为 2以及Ca、
Mg、Fe、Cu等的化合物。其制备流程如下:
本题中所涉及离子的氯氧化物溶度积常数如下表:
离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+
K
sp
4.01038 6.71017 2.21020 8.01016 1.81011
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
pH=5
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
NH H O Ca(OH) NaOH
A. 3 2 B. 2 C.
滤渣①的主要成分是_______、_______、_______。
80~90℃ KMnO MnO
(4)向 的滤液①中分批加入适量 4溶液充分反应后过滤,滤渣②中有 2,
该步反应的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
H SO
(6)滤渣④与浓 2 4反应可以释放HF并循环利用,同时得到的副产物是_______、
_______。
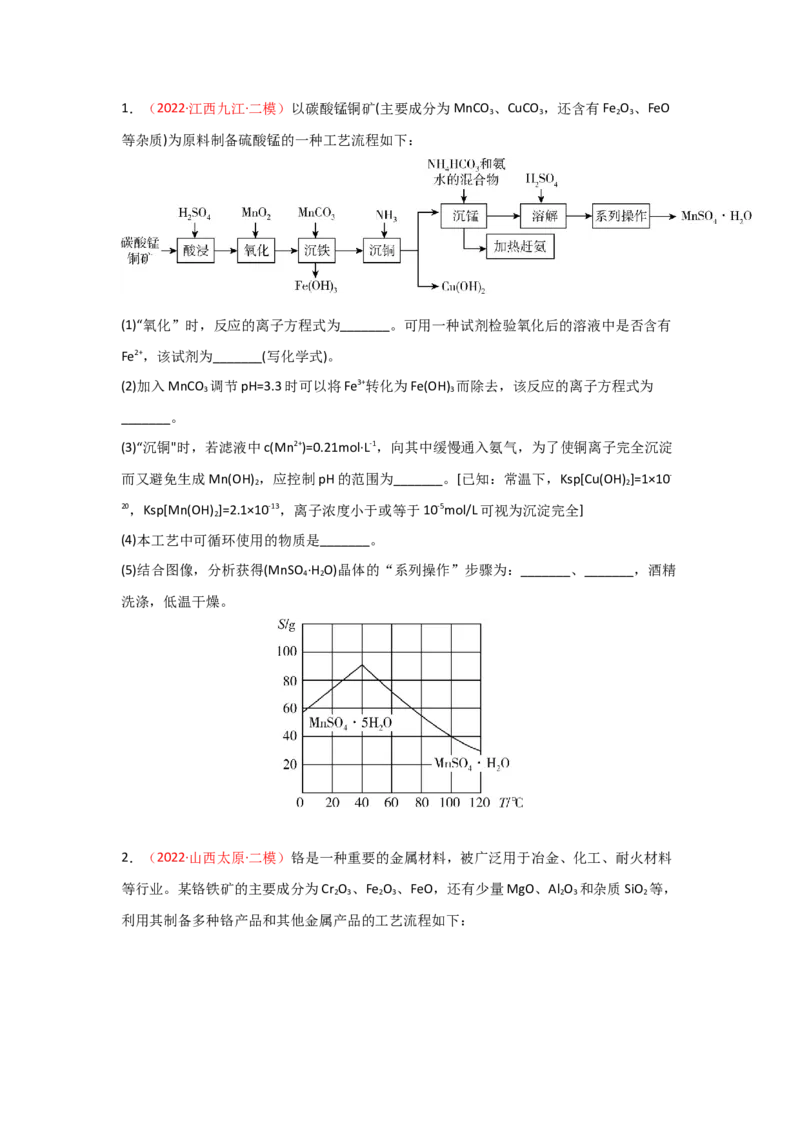
【实战演练】1.(2022·江西九江·二模)以碳酸锰铜矿(主要成分为MnCO 、CuCO ,还含有Fe O 、FeO
3 3 2 3
等杂质)为原料制备硫酸锰的一种工艺流程如下:
(1)“氧化”时,反应的离子方程式为_______。可用一种试剂检验氧化后的溶液中是否含有
Fe2+,该试剂为_______(写化学式)。
(2)加入MnCO 调节pH=3.3时可以将Fe3+转化为Fe(OH) 而除去,该反应的离子方程式为
3 3
_______。
(3)“沉铜"时,若滤液中c(Mn2+)=0.21mol·L-1,向其中缓慢通入氨气,为了使铜离子完全沉淀
而又避免生成Mn(OH) ,应控制pH的范围为_______。[已知:常温下,Ksp[Cu(OH) ]=1×10-
2 2
20,Ksp[Mn(OH) ]=2.1×10-13,离子浓度小于或等于10-5mol/L可视为沉淀完全]
2
(4)本工艺中可循环使用的物质是_______。
(5)结合图像,分析获得(MnSO ·H O)晶体的“系列操作”步骤为:_______、_______,酒精
4 2
洗涤,低温干燥。
2.(2022·山西太原·二模)铬是一种重要的金属材料,被广泛用于冶金、化工、耐火材料
等行业。某铬铁矿的主要成分为Cr O 、Fe O 、FeO,还有少量MgO、Al O 和杂质SiO 等,
2 3 2 3 2 3 2
利用其制备多种铬产品和其他金属产品的工艺流程如下:已知:Al O +Na CO 2NaAlO +CO ↑ SiO +Na CO Na SiO +CO ↑
2 3 2 3 2 2 2 2 3 2 3 2
回答下列问题:
(1)步骤①发生的主要反应为FeO+Cr O +Na CO +NaNO Na CrO +Fe O +NaNO +A↑,反应
2 3 2 3 3 2 4 2 3 2
时应选用何种材质的容器?_______(填字母)。
A.塑料 B.刚玉 C.铁 D.石英
(2)步骤②的操作是_______,“滤渣 2”是Al(OH) 和_______。 写出过量物质A与“滤液
3
1"中溶质生成Al(OH) 的离子方程式:_______。
3
(3)“滤液2”中的Na CrO 需要用H SO 酸化,用离子方程式表示该反应:_______。
2 4 2 4
(4)制取高纯铬常用电解法和铝热法,铝热法的缺点是_______。步骤④是在隔绝空气条件
下,除生成Cr O 外,还生成了Na CO 和CO,若该反应中有3 mol Na Cr O 参加反应,则转
2 3 2 3 2 2 7
移的电子为_______mol。
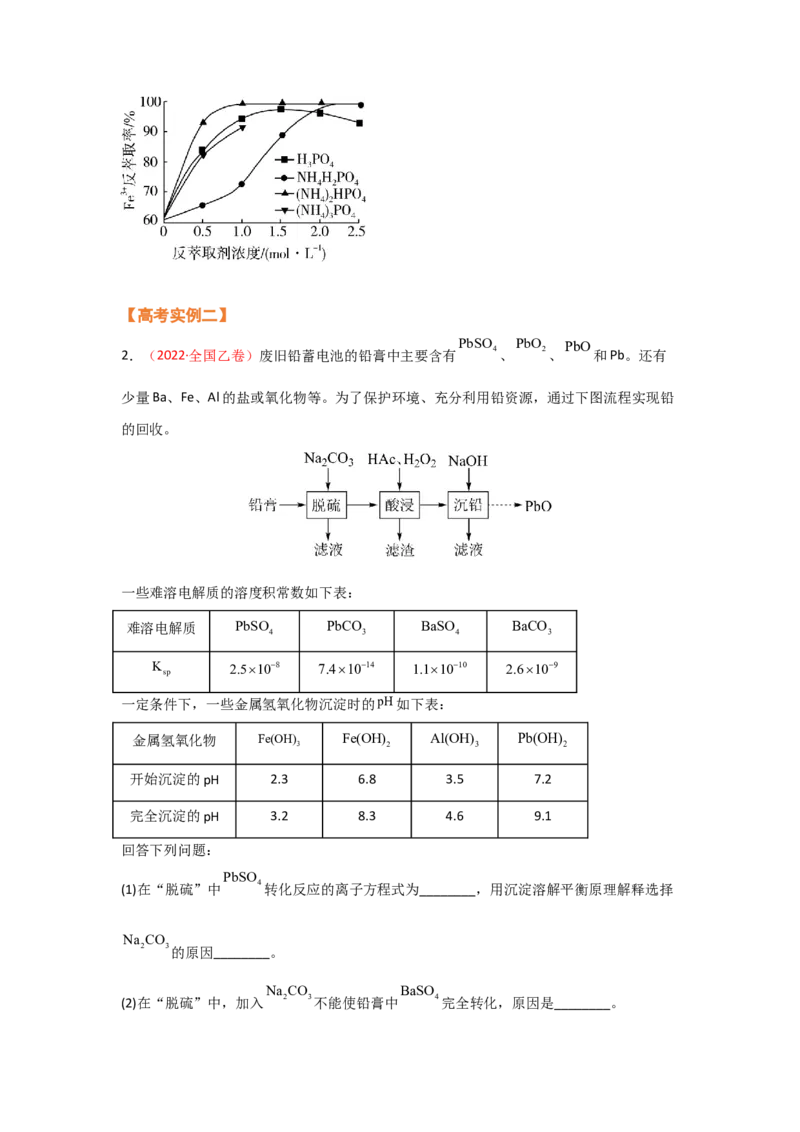
(5)“滤渣1”中铁元素含量较高,具有回收价值。为回收金属,需要将含Fe3+的有机相进行反
萃取。在有机相中Fe3+质量浓度为22.8 g/L、有机相与水相的体积比(V:V)=1:1、反萃取
o a
时间为20min、反萃取温度为25°C条件下,不同浓度的4种反萃取剂对Fe3+反萃取率的影
响实验结果如图所示。当反萃取剂的浓度均为0.5 mol·L-1时,反萃取效果最好的是_______
(填化学式),在实际操作中需在该反萃取剂中加入一定量H PO 溶液,其目的是_______ ;
3 4
但H PO 浓度不宜过大,其原因是_______。[已知:(NH ) HPO 溶液pH=7.8 ~8.2]
3 4 4 2 4【高考实例二】
PbSO PbO PbO
2.(2022·全国乙卷)废旧铅蓄电池的铅膏中主要含有 4、 2、 和Pb。还有
少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅
的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5108 7.41014 1.11010 2.6109
sp
一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH)
3 2 3 2
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
PbSO
(1)在“脱硫”中 4转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择
Na CO
2 3的原因________。
Na CO BaSO
(2)在“脱硫”中,加入 2 3不能使铅膏中 4完全转化,原因是________。HAc H O
(3)在“酸浸”中,除加入醋酸( ),还要加入 2 2。
H O
(ⅰ)能被 2 2氧化的离子是________;
H O Pb(Ac)
(ⅱ)
2 2促进了金属Pb在醋酸中转化为 2,其化学方程式为________;
H O PbO Pb(Ac) H O
(ⅲ)
2 2也能使 2转化为 2, 2 2的作用是________。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是________。
(5)“沉铅”的滤液中,金属离子有________。
【实战演练】
1.(2022·陕西汉中·二模)我国发现超级铼矿,铼(Re)是一种熔点高、耐磨、耐腐蚀的金
属,广泛用于航天航空等领域。工业上用富铼渣(含ReS )制得铼粉,其工艺流程如下图所
2
示:
回答下列问题:
(1)铼不溶于盐酸,可溶于稀硝酸生成强酸高铼酸(HReO ),请写出反应的离子方程式
4
_______。
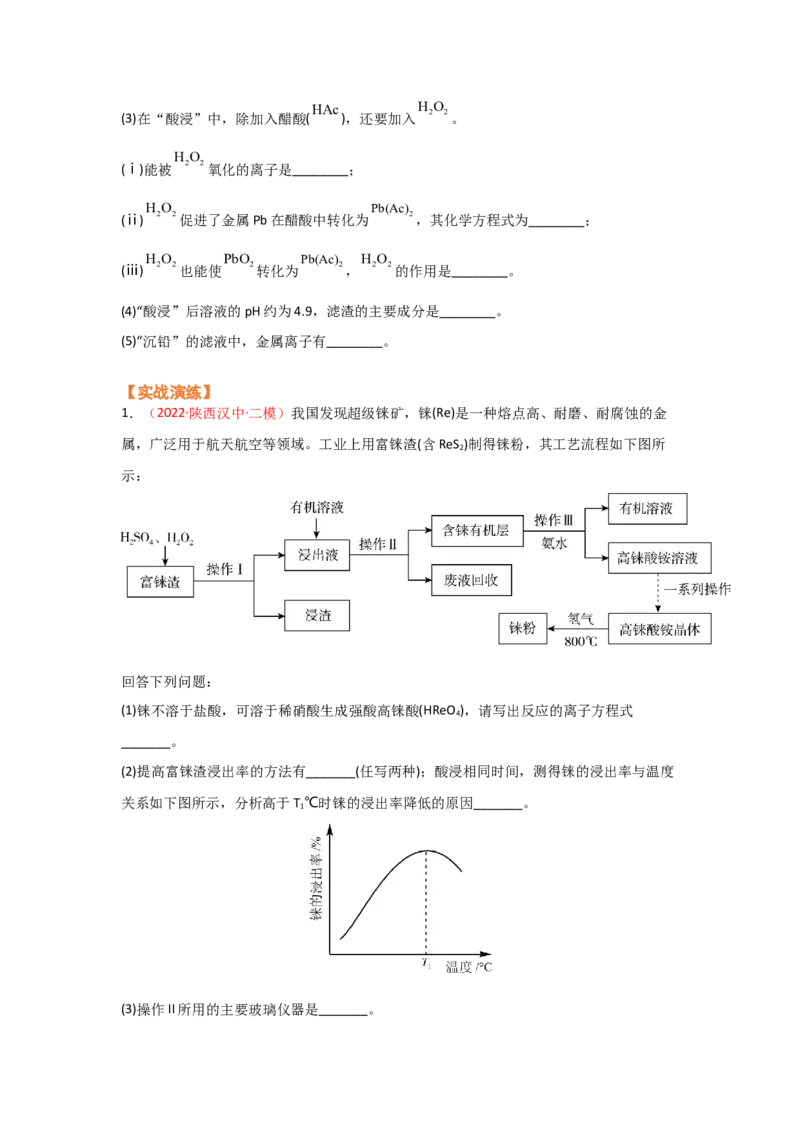
(2)提高富铼渣浸出率的方法有_______(任写两种);酸浸相同时间,测得铼的浸出率与温度
关系如下图所示,分析高于T ℃时铼的浸出率降低的原因_______。
1
(3)操作II所用的主要玻璃仪器是_______。(4)高铼酸铵和氢气制取单质铼的化学方程式为_______;此反应过程中,实际消耗H 的量
2
大于理论值,其原因是_______。
(5)由高铼酸铵溶液获得高铼酸铵晶体的一系列操作为_______、洗涤、干燥。
(6)整个工艺流程中除有机溶液可循环利用外,还有_______。
2.(2022·陕西渭南·二模)金属钪可用作宇航材料、火箭和飞机的制造材料;氧化钪可提
高计算机记忆元件性能。赤泥是铝土矿加工过程中产生的废料,含有丰富的钪元素,另含
有Fe O 、SiO 、Al O 等氧化物。一种从赤泥中提取氧化钪的工艺流程如图所示(P O 是一种
2 3 2 2 3 2 4
磷酸酯萃取剂)。
回答下列问题:
(1)写出赤泥经盐酸处理后所得“浸渣”与强碱溶液反应的离子方程式____。
(2)赤泥“酸浸”时温度过高,酸浸速率反而下降,其原因是____。
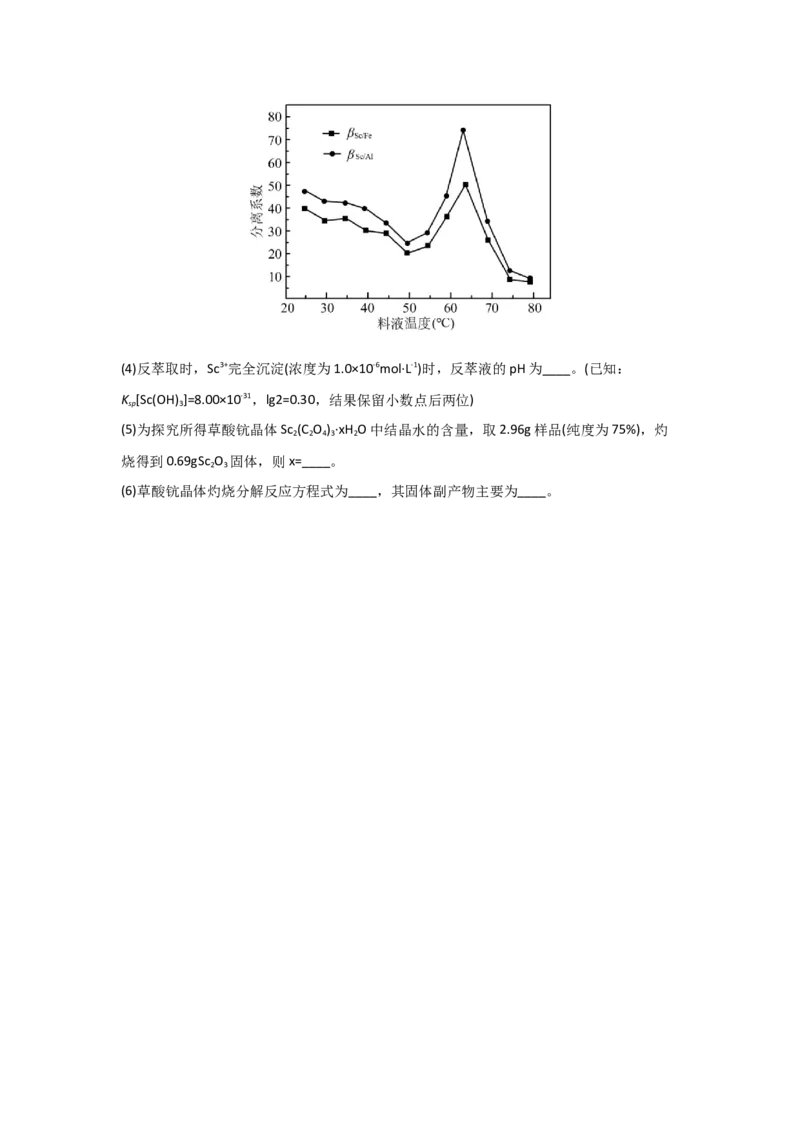
(3)P O 萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P O 最佳浓度及
2 4 2 4
料液温度分别为____、____;萃取后“盐酸洗涤”的目的是____。P O 浓度对萃取率的影
2 4
响如表:
试验编号 P O 浓度/% 分相情况 钪萃取率/% 铁萃取率/%
2 4
1-1 1 分相快 90.76 15.82
1-2 2 分相容易 91.53 19.23
1-3 3 分相容易 92.98 13.56
1-4 4 有第三相 90.69 30.12
1-5 5 轻微乳化 91.74 39.79
料液温度对分离系数的影响如图:(4)反萃取时,Sc3+完全沉淀(浓度为1.0×10-6mol·L-1)时,反萃液的pH为____。(已知:
K [Sc(OH) ]=8.00×10-31,lg2=0.30,结果保留小数点后两位)
sp 3
(5)为探究所得草酸钪晶体Sc (C O ) ·xH O中结晶水的含量,取2.96g样品(纯度为75%),灼
2 2 4 3 2
烧得到0.69gSc O 固体,则x=____。
2 3
(6)草酸钪晶体灼烧分解反应方程式为____,其固体副产物主要为____。