文档内容
电极反应式的书写及电化学计算
1.分析电化学装置的物质变化书写电极反应式
(1)确定装置类型
原电池:外接用电器、电压表、负载等;
电解池:外接电源或题干给出信息;
二次电池:放电为原电池、充电为电解池。
(2)“四步法”书写电极反应式
2.已知总反应式,书写电极反应式
(1)书写三步骤
步骤一:根据电池总反应式,标出电子转移的方向和数目(ne-)。
步骤二:找出正(阴)、负(阳)极,失电子的电极为负(阳)极;确定溶液的酸碱性。
步骤三:写电极反应式。
负(阳)极反应:还原剂-ne-===氧化产物
正(阴)极反应:氧化剂+ne-===还原产物
(2)书写技巧
若某电极反应式较难写出时,可先写出较易的电极反应式,然后根据得失电子守恒,用总反应式减去
较易的电极反应式,即可得出较难写出的电极反应式。
3.守恒法在电化学计算中的应用
(1)电子守恒和电荷守恒列关系式
①电子守恒:两极得失电子数相等。
②电荷守恒:1个电子对应1个正电荷(或负电荷)。4
③常用关系式:O ~4e-~4Ag~2Cu~2H ~2Cl ~4OH-~4H+~ Mn+。
2 2 2 n
(2)几个注意问题
①气体体积相关计算时,必须注明标准状况。
②计算含交换膜电化学装置中某一区域质量变化,注意离子的迁移。
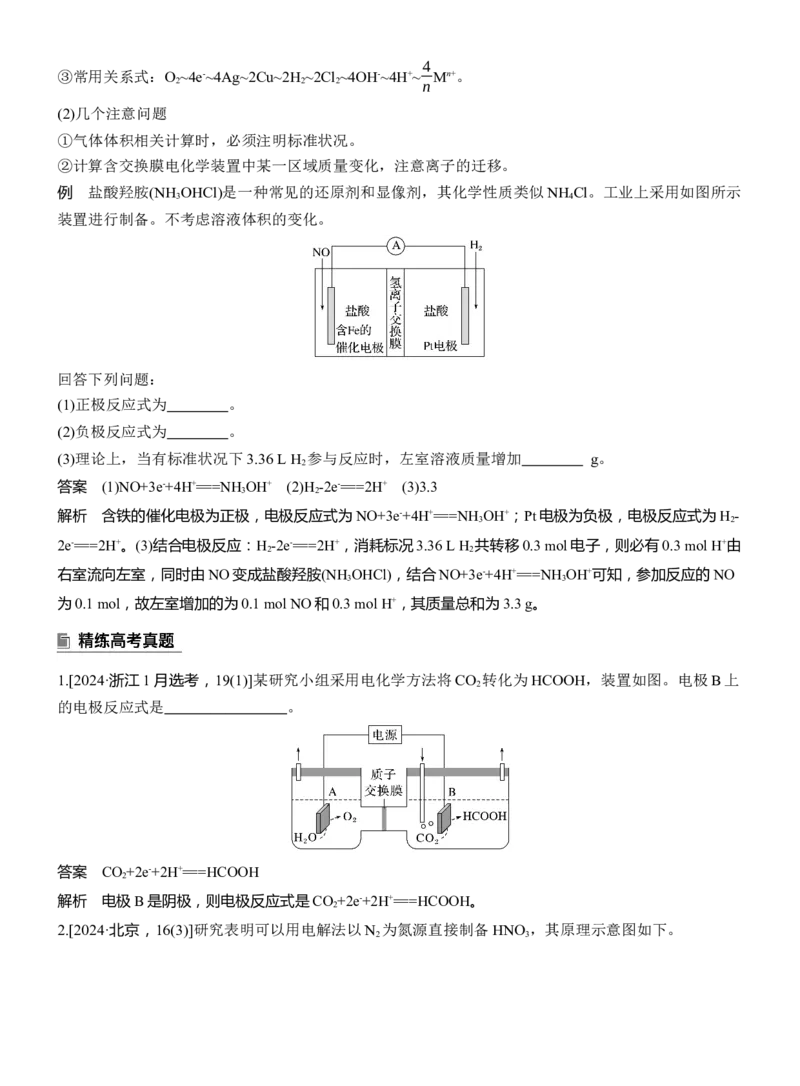
例 盐酸羟胺(NH OHCl)是一种常见的还原剂和显像剂,其化学性质类似NH Cl。工业上采用如图所示
3 4
装置进行制备。不考虑溶液体积的变化。
回答下列问题:
(1)正极反应式为 。
(2)负极反应式为 。
(3)理论上,当有标准状况下3.36 L H 参与反应时,左室溶液质量增加 g。
2
答案 (1)NO+3e-+4H+===NH OH+ (2)H -2e-===2H+ (3)3.3
3 2
解析 含铁的催化电极为正极,电极反应式为NO+3e-+4H+===NH OH+;Pt电极为负极,电极反应式为H -
3 2
2e-===2H+。(3)结合电极反应:H -2e-===2H+,消耗标况3.36 L H 共转移0.3 mol电子,则必有0.3 mol H+由
2 2
右室流向左室,同时由NO变成盐酸羟胺(NH OHCl),结合NO+3e-+4H+===NH OH+可知,参加反应的NO
3 3
为0.1 mol,故左室增加的为0.1 mol NO和0.3 mol H+,其质量总和为3.3 g。
1.[2024·浙江1月选考,19(1)]某研究小组采用电化学方法将CO 转化为HCOOH,装置如图。电极B上
2
的电极反应式是 。
答案 CO +2e-+2H+===HCOOH
2
解析 电极B是阴极,则电极反应式是CO +2e-+2H+===HCOOH。
2
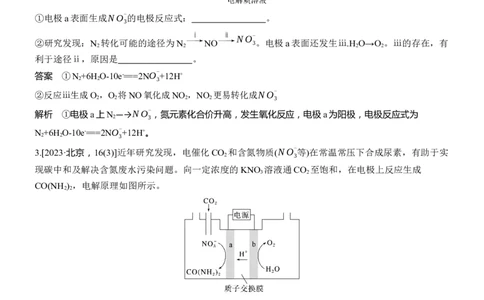
2.[2024·北京,16(3)]研究表明可以用电解法以N 为氮源直接制备HNO ,其原理示意图如下。
2 3①电极a表面生成NO-
的电极反应式: 。
3
NO-
②研究发现:N 转化可能的途径为N NO 3。电极a表面还发生ⅲ.H O→O 。ⅲ的存在,有
2 2 2 2
利于途径ⅱ,原因是 。
答案 ①N +6H
O-10e-===2NO-
+12H+
2 2 3
②反应ⅲ生成O ,O 将NO氧化成NO ,NO
更易转化成NO-
2 2 2 2 3
解析 ①电极a上N
―→NO-
,氮元素化合价升高,发生氧化反应,电极a为阳极,电极反应式为
2 3
N +6H O-10e-===2NO- +12H+。
2 2 3
3.[2023·北京,16(3)]近年研究发现,电催化CO
和含氮物质(NO-
等)在常温常压下合成尿素,有助于实
2 3
现碳中和及解决含氮废水污染问题。向一定浓度的KNO 溶液通CO 至饱和,在电极上反应生成
3 2
CO(NH ) ,电解原理如图所示。
2 2
①电极b是电解池的 极。
②电解过程中生成尿素的电极反应式是 。
答案 ①阳
②2NO-
+16e-+CO +18H+===CO(NH ) +7H O
3 2 2 2 2
解析 ①电极b上发生H O失电子生成O 的氧化反应,是电解池的阳极。②a极硝酸根离子得电子转化为
2 2
尿素,再结合酸性环境可分析出电极反应式。
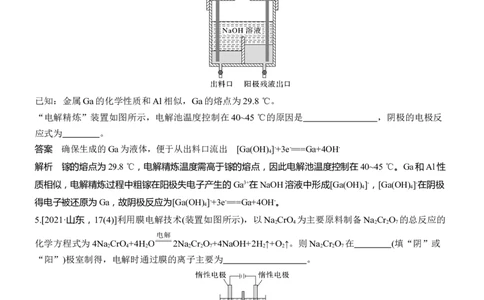
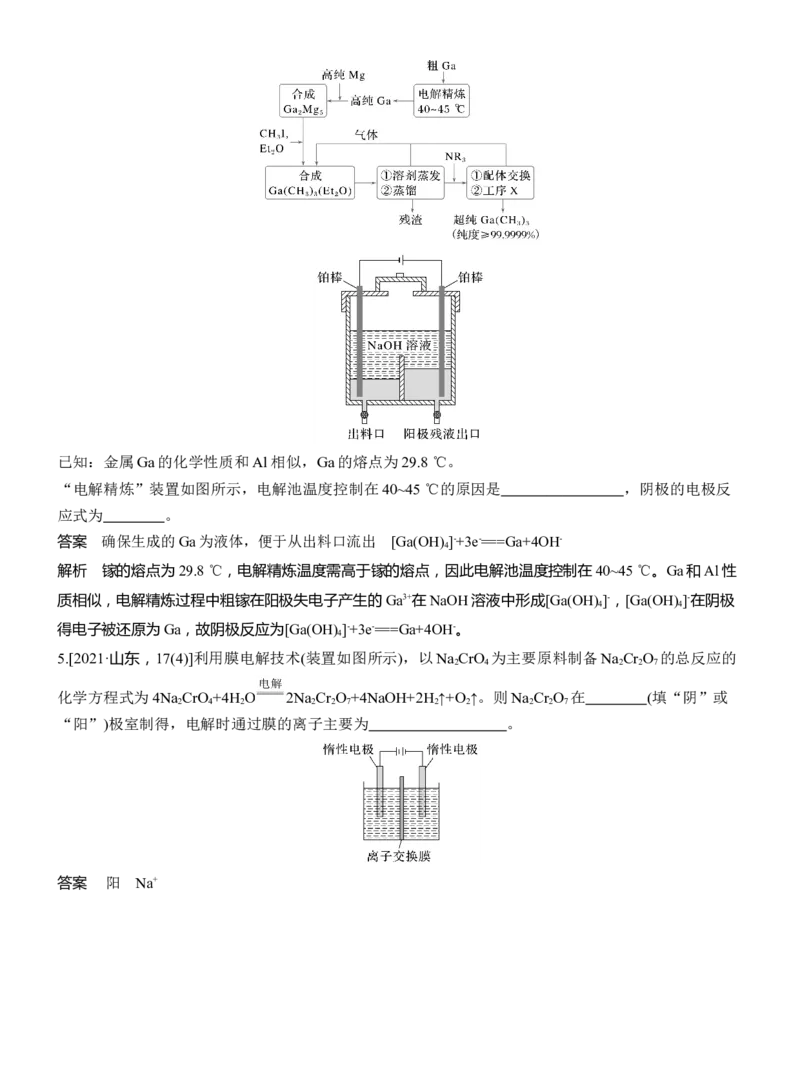
4.[2023·湖南,17(2)]工业上以粗镓为原料,制备超纯Ga(CH ) 的工艺流程如下:
3 3已知:金属Ga的化学性质和Al相似,Ga的熔点为29.8 ℃。
“电解精炼”装置如图所示,电解池温度控制在40~45 ℃的原因是 ,阴极的电极反
应式为 。
答案 确保生成的Ga为液体,便于从出料口流出 [Ga(OH) ]-+3e-===Ga+4OH-
4
解析 镓的熔点为29.8 ℃,电解精炼温度需高于镓的熔点,因此电解池温度控制在40~45 ℃。Ga和Al性
质相似,电解精炼过程中粗镓在阳极失电子产生的Ga3+在NaOH溶液中形成[Ga(OH) ]-,[Ga(OH) ]-在阴极
4 4
得电子被还原为Ga,故阴极反应为[Ga(OH) ]-+3e-===Ga+4OH-。
4
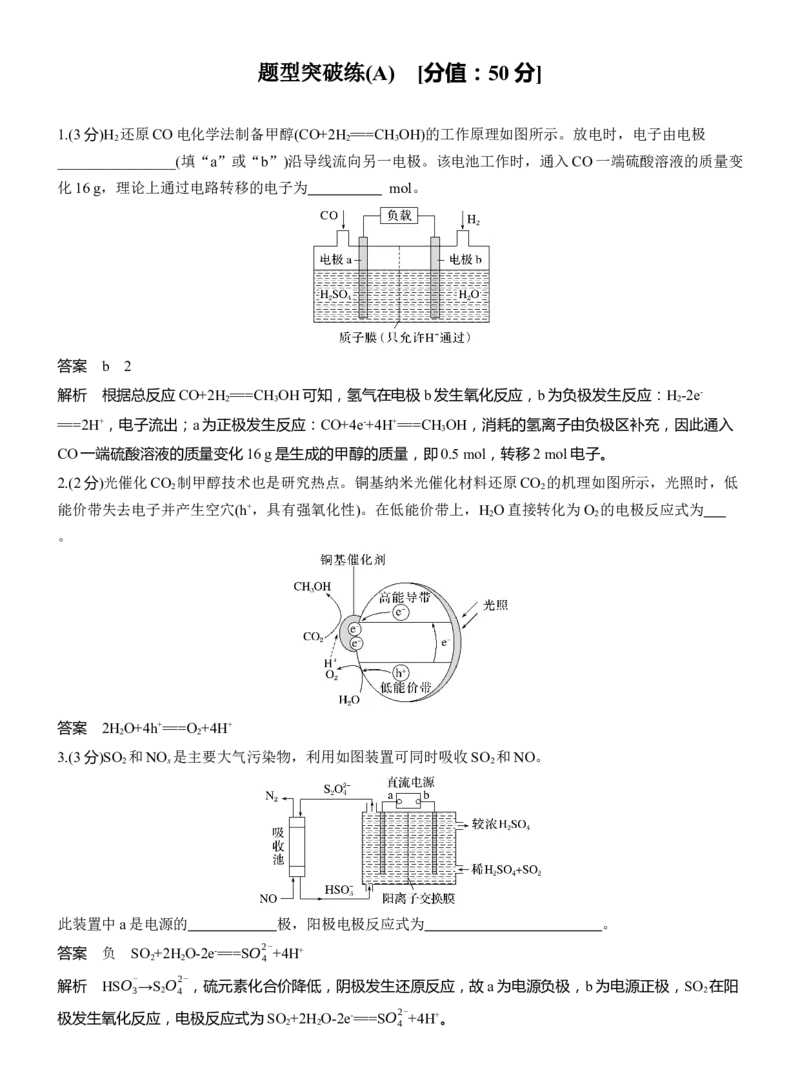
5.[2021·山东,17(4)]利用膜电解技术(装置如图所示),以Na CrO 为主要原料制备Na Cr O 的总反应的
2 4 2 2 7
化学方程式为4Na CrO +4H O 2Na Cr O +4NaOH+2H ↑+O ↑。则Na Cr O 在 (填“阴”或
2 4 2 2 2 7 2 2 2 2 7
“阳”)极室制得,电解时通过膜的离子主要为 。
答案 阳 Na+题型突破练(A) [分值:50 分]
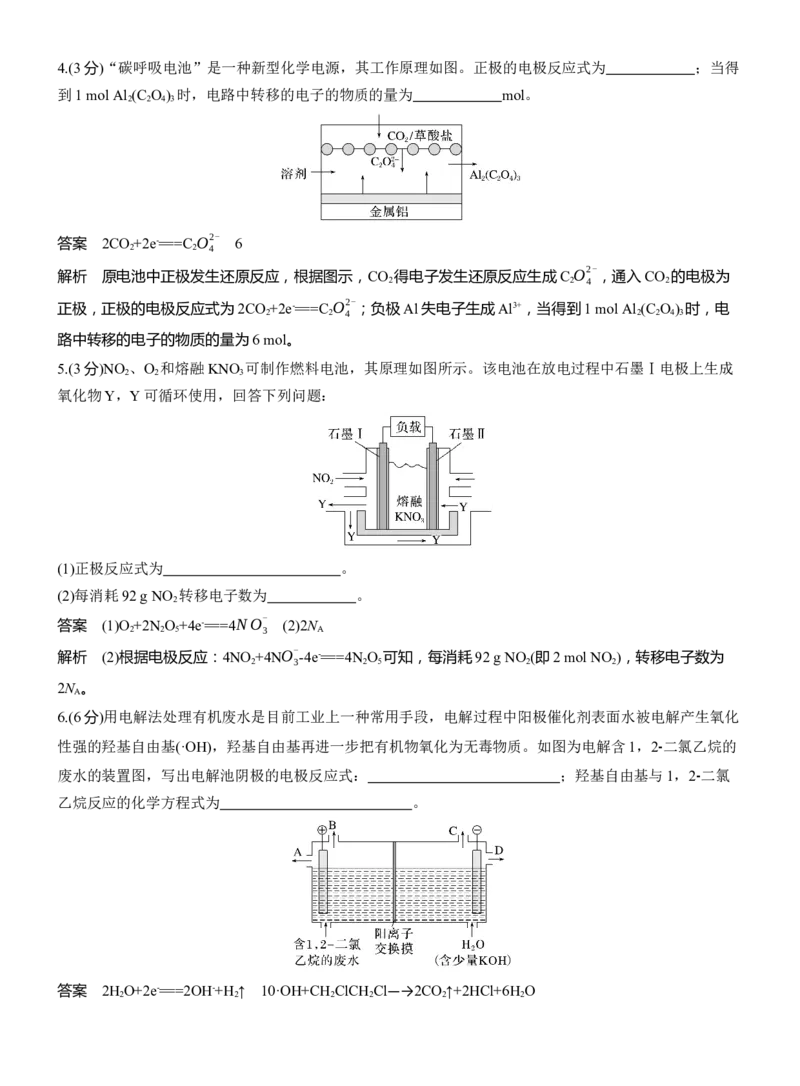
1.(3分)H 还原CO电化学法制备甲醇(CO+2H ===CH OH)的工作原理如图所示。放电时,电子由电极
2 2 3
________________(填“a”或“b”)沿导线流向另一电极。该电池工作时,通入CO一端硫酸溶液的质量变
化16 g,理论上通过电路转移的电子为 mol。
答案 b 2
解析 根据总反应CO+2H ===CH OH可知,氢气在电极b发生氧化反应,b为负极发生反应:H -2e-
2 3 2
===2H+,电子流出;a为正极发生反应:CO+4e-+4H+===CH OH,消耗的氢离子由负极区补充,因此通入
3
CO一端硫酸溶液的质量变化16 g是生成的甲醇的质量,即0.5 mol,转移2 mol电子。
2.(2分)光催化CO 制甲醇技术也是研究热点。铜基纳米光催化材料还原CO 的机理如图所示,光照时,低
2 2
能价带失去电子并产生空穴(h+,具有强氧化性)。在低能价带上,H O直接转化为O 的电极反应式为
2 2
。
答案 2H O+4h+===O +4H+
2 2
3.(3分)SO 和NO 是主要大气污染物,利用如图装置可同时吸收SO 和NO。
2 x 2
此装置中a是电源的 极,阳极电极反应式为 。
答案 负 SO +2H
O-2e-===SO2-
+4H+
2 2 4
解析
HSO-
→S
O2-
,硫元素化合价降低,阴极发生还原反应,故a为电源负极,b为电源正极,SO 在阳
3 2 4 2
极发生氧化反应,电极反应式为SO +2H
O-2e-===SO2-
+4H+。
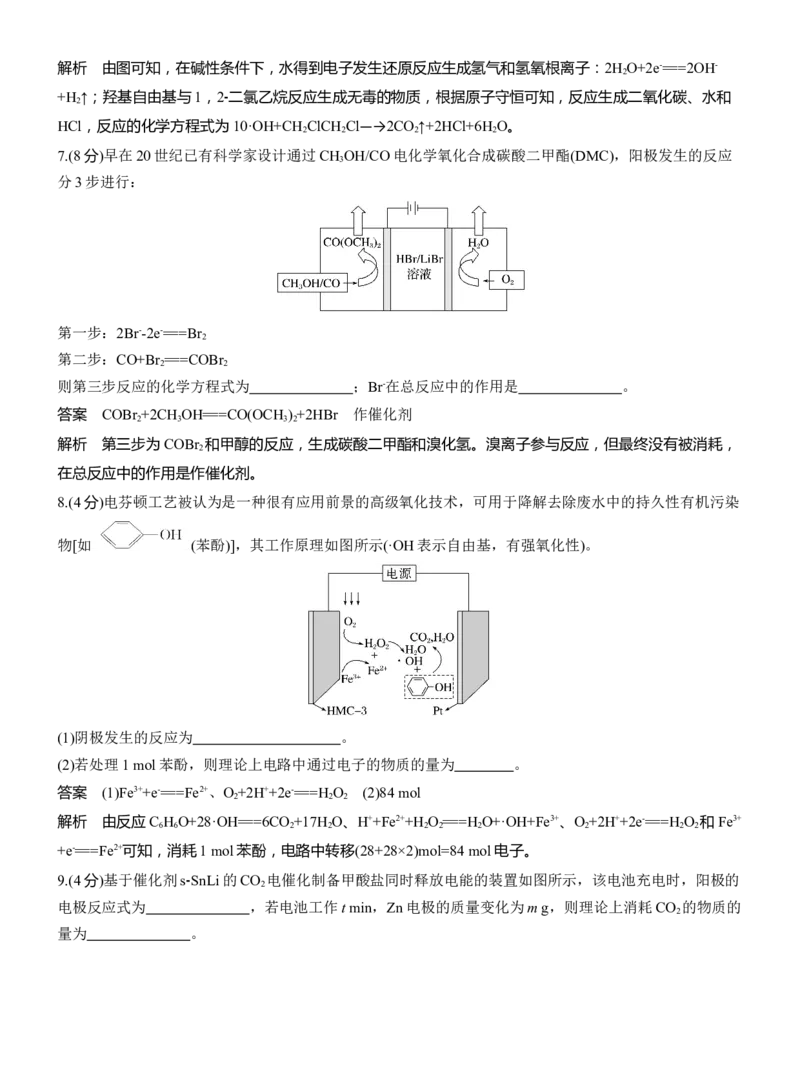
2 2 44.(3分)“碳呼吸电池”是一种新型化学电源,其工作原理如图。正极的电极反应式为 ;当得
到1 mol Al (C O ) 时,电路中转移的电子的物质的量为 mol。
2 2 4 3
答案 2CO +2e-===C
O2-
6
2 2 4
解析 原电池中正极发生还原反应,根据图示,CO 得电子发生还原反应生成C
O2-
,通入CO 的电极为
2 2 4 2
正极,正极的电极反应式为2CO +2e-===C
O2-
;负极Al失电子生成Al3+,当得到1 mol Al (C O ) 时,电
2 2 4 2 2 4 3
路中转移的电子的物质的量为6 mol。
5.(3分)NO 、O 和熔融KNO 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成
2 2 3
氧化物Y,Y可循环使用,回答下列问题:
(1)正极反应式为 。
(2)每消耗92 g NO 转移电子数为 。
2
答案 (1)O +2N O
+4e-===4NO-
(2)2N
2 2 5 3 A
解析 (2)根据电极反应:4NO
+4NO-
-4e-===4N O 可知,每消耗92 g NO (即2 mol NO ),转移电子数为
2 3 2 5 2 2
2N 。
A
6.(6分)用电解法处理有机废水是目前工业上一种常用手段,电解过程中阳极催化剂表面水被电解产生氧化
性强的羟基自由基(·OH),羟基自由基再进一步把有机物氧化为无毒物质。如图为电解含1,2⁃ 二氯乙烷的
废水的装置图,写出电解池阴极的电极反应式: ;羟基自由基与1,2⁃ 二氯
乙烷反应的化学方程式为 。
答案 2H O+2e-===2OH-+H ↑ 10·OH+CH ClCH Cl―→2CO ↑+2HCl+6H O
2 2 2 2 2 2解析 由图可知,在碱性条件下,水得到电子发生还原反应生成氢气和氢氧根离子:2H O+2e-===2OH-
2
+H
2
↑;羟基自由基与1,2⁃二氯乙烷反应生成无毒的物质,根据原子守恒可知,反应生成二氧化碳、水和
HCl,反应的化学方程式为10·OH+CH ClCH Cl―→2CO ↑+2HCl+6H O。
2 2 2 2
7.(8分)早在20世纪已有科学家设计通过CH OH/CO电化学氧化合成碳酸二甲酯(DMC),阳极发生的反应
3
分3步进行:
第一步:2Br--2e-===Br
2
第二步:CO+Br ===COBr
2 2
则第三步反应的化学方程式为 ;Br-在总反应中的作用是 。
答案 COBr +2CH OH===CO(OCH ) +2HBr 作催化剂
2 3 3 2
解析 第三步为COBr 和甲醇的反应,生成碳酸二甲酯和溴化氢。溴离子参与反应,但最终没有被消耗,
2
在总反应中的作用是作催化剂。
8.(4分)电芬顿工艺被认为是一种很有应用前景的高级氧化技术,可用于降解去除废水中的持久性有机污染
物[如 (苯酚)],其工作原理如图所示(·OH表示自由基,有强氧化性)。
(1)阴极发生的反应为 。
(2)若处理1 mol苯酚,则理论上电路中通过电子的物质的量为 。
答案 (1)Fe3++e-===Fe2+、O +2H++2e-===H O (2)84 mol
2 2 2
解析 由反应C H O+28·OH===6CO +17H O、H++Fe2++H O ===H O+·OH+Fe3+、O +2H++2e-===H O 和Fe3+
6 6 2 2 2 2 2 2 2 2
+e-===Fe2+可知,消耗1 mol苯酚,电路中转移(28+28×2)mol=84 mol电子。
9.(4分)基于催化剂s⁃SnLi的CO
2
电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的
电极反应式为 ,若电池工作t min,Zn电极的质量变化为m g,则理论上消耗CO 的物质的
2
量为 。m
答案 4OH--4e-===2H O+O ↑ mol
2 2 65
解析 由题中图像可知,电池充电时,阳极上氢氧根离子发生氧化反应,失去电子生成氧气,电极反应式
为4OH--4e-===2H O+O ↑;电池工作时,负极反应:Zn-2e-===Zn2+,正极反应:CO +2e-+H O===HCOO-
2 2 2 2
m
+OH-,由转移电子守恒可知,n(CO )=n(Zn)= mol。
2 65
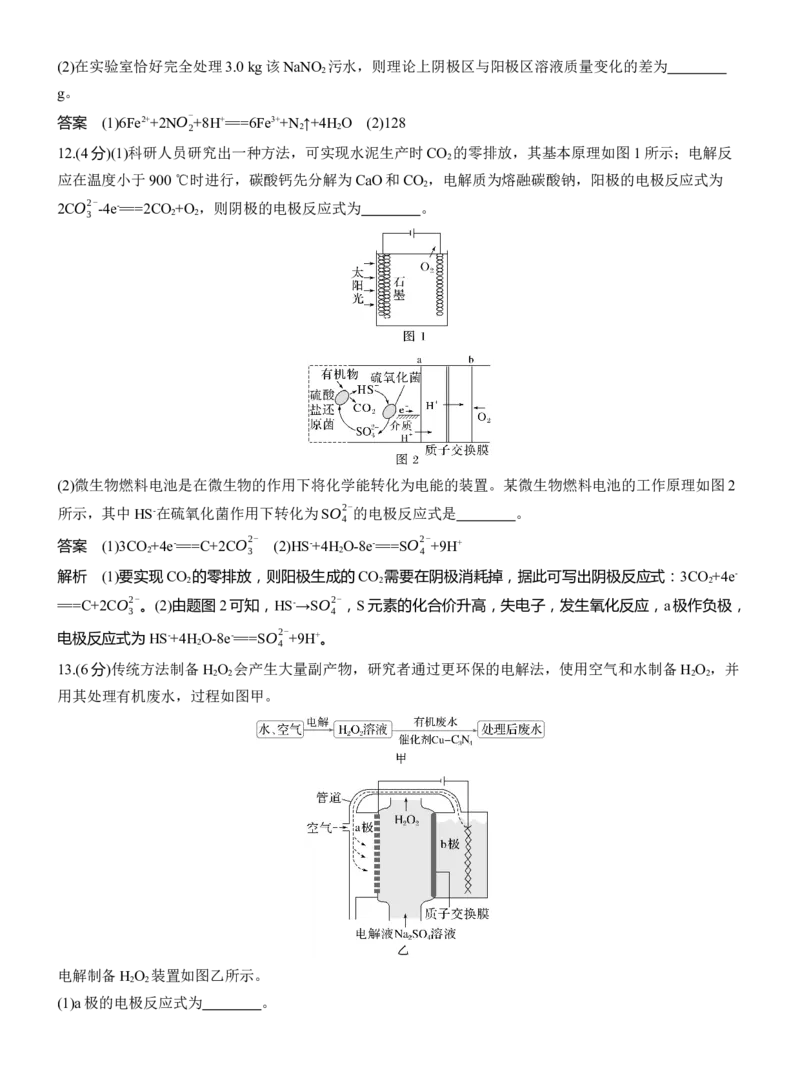
10.(6分)合成氨也可以通过电化学过程实现,其装置如图所示。
(1)导线中电子流动方向为 。
(2)生成NH 的电极反应式为 。
3
(3)若惰性电极2的电流效率η为75%,则惰性电极2处N 与NH 的物质的量之比为 (η=
2 3
电极上目标产物的实际质量
×100%)。
电极上目标产物的理论质量
答案 (1)惰性电极2到电源正极、电源负极到惰性电极1 (2)3H -6e-+2N3-===2NH (3)1∶6
2 3
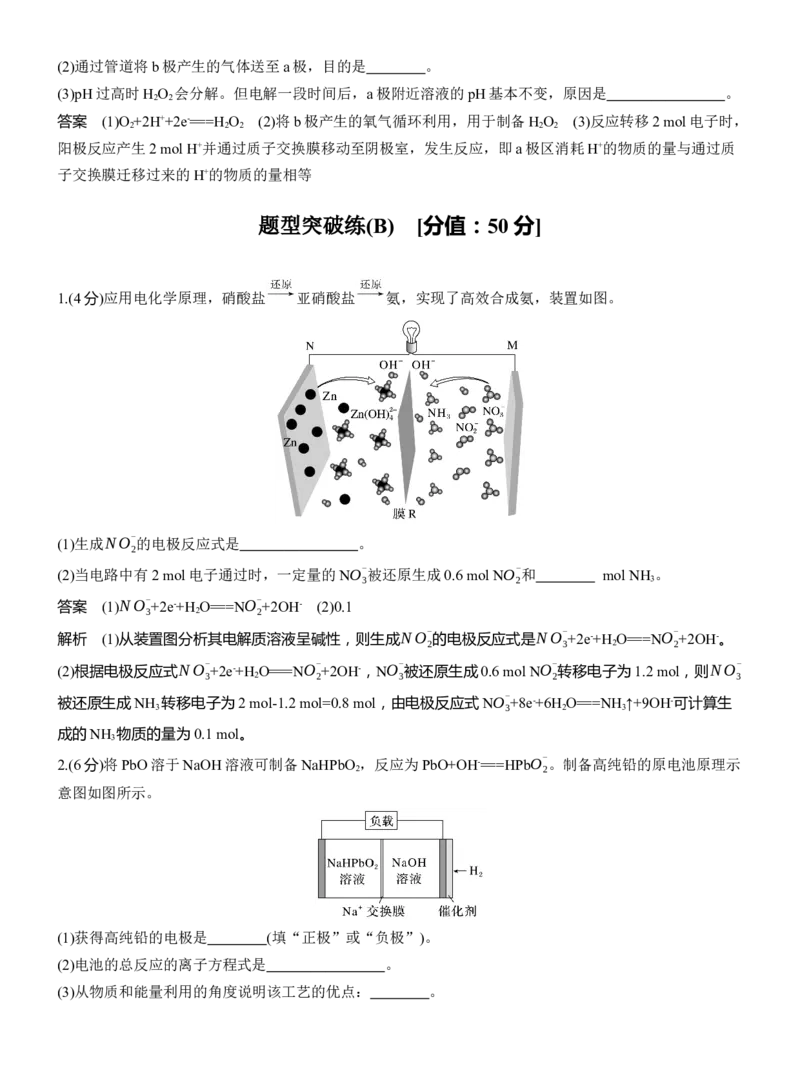
11.(4分)经测定污水里NaNO 含量为4.6%,科研人员研究发现可用如图所示的装置处理污水中的NaNO ,
2 2
原理是利用Fe2+把NO-
还原成N 。
2 2
(1)阳极附近溶液中发生反应的离子方程式为 。(2)在实验室恰好完全处理3.0 kg该NaNO 污水,则理论上阴极区与阳极区溶液质量变化的差为
2
g。
答案
(1)6Fe2++2NO-
+8H+===6Fe3++N ↑+4H O (2)128
2 2 2
12.(4分)(1)科研人员研究出一种方法,可实现水泥生产时CO 的零排放,其基本原理如图1所示;电解反
2
应在温度小于900 ℃时进行,碳酸钙先分解为CaO和CO ,电解质为熔融碳酸钠,阳极的电极反应式为
2
2CO2- -4e-===2CO +O ,则阴极的电极反应式为 。
3 2 2
(2)微生物燃料电池是在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图2
所示,其中HS-在硫氧化菌作用下转化为SO2-的电极反应式是 。
4
答案 (1)3CO
+4e-===C+2CO2-
(2)HS-+4H
O-8e-===SO2-
+9H+
2 3 2 4
解析 (1)要实现CO 的零排放,则阳极生成的CO 需要在阴极消耗掉,据此可写出阴极反应式:3CO +4e-
2 2 2
===C+2CO2- 。(2)由题图2可知,HS-→SO2-
,S元素的化合价升高,失电子,发生氧化反应,a极作负极,
3 4
电极反应式为HS-+4H
O-8e-===SO2-
+9H+。
2 4
13.(6分)传统方法制备H O 会产生大量副产物,研究者通过更环保的电解法,使用空气和水制备H O ,并
2 2 2 2
用其处理有机废水,过程如图甲。
电解制备H O 装置如图乙所示。
2 2
(1)a极的电极反应式为 。(2)通过管道将b极产生的气体送至a极,目的是 。
(3)pH过高时H O 会分解。但电解一段时间后,a极附近溶液的pH基本不变,原因是 。
2 2
答案 (1)O +2H++2e-===H O (2)将b极产生的氧气循环利用,用于制备H O (3)反应转移2 mol电子时,
2 2 2 2 2
阳极反应产生2 mol H+并通过质子交换膜移动至阴极室,发生反应,即a极区消耗H+的物质的量与通过质
子交换膜迁移过来的H+的物质的量相等
题型突破练(B) [分值:50 分]
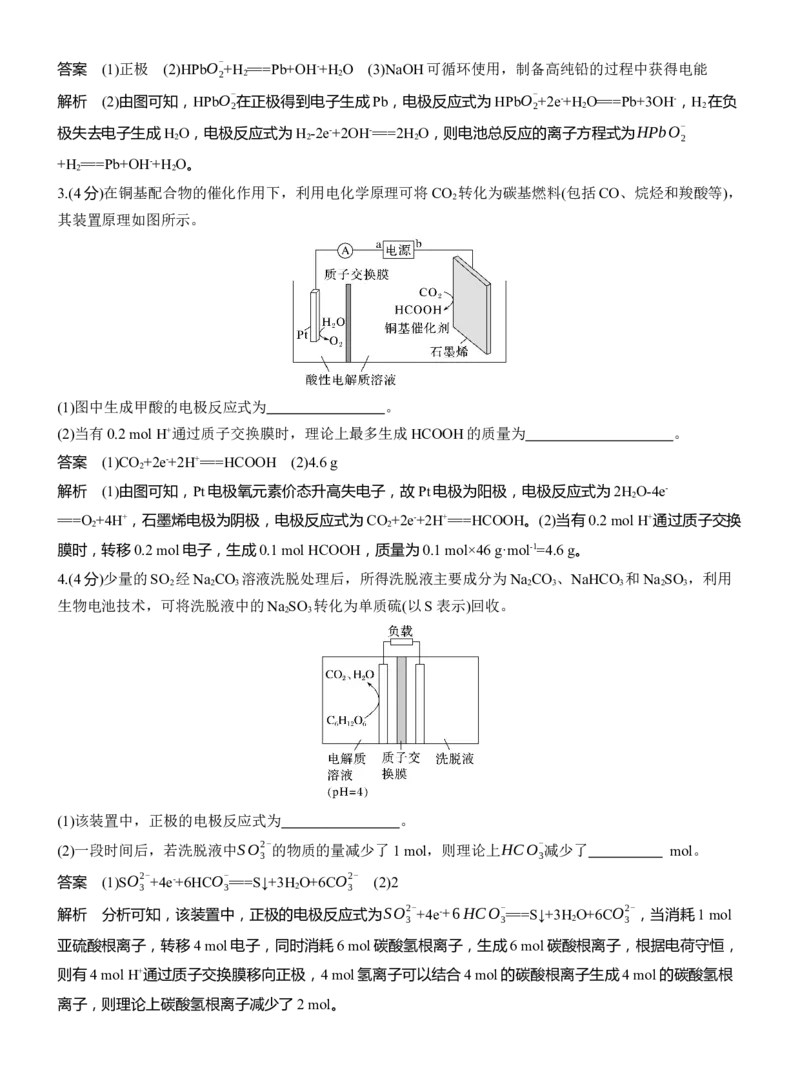
1.(4分)应用电化学原理,硝酸盐 亚硝酸盐 氨,实现了高效合成氨,装置如图。
(1)生成NO-
的电极反应式是 。
2
(2)当电路中有2
mol电子通过时,一定量的NO-
被还原生成0.6 mol
NO-
和 mol NH 。
3 2 3
答案
(1)NO-
+2e-+H
O===NO-
+2OH- (2)0.1
3 2 2
解析
(1)从装置图分析其电解质溶液呈碱性,则生成NO- 的电极反应式是NO-
+2e-+H
O===NO-
+2OH-。
2 3 2 2
(2)根据电极反应式NO-
+2e-+H
O===NO- +2OH-,NO-
被还原生成0.6 mol
NO-
转移电子为1.2
mol,则NO-
3 2 2 3 2 3
被还原生成NH 转移电子为2 mol-1.2 mol=0.8
mol,由电极反应式NO-
+8e-+6H O===NH ↑+9OH-可计算生
3 3 2 3
成的NH 物质的量为0.1 mol。
3
2.(6分)将PbO溶于NaOH溶液可制备NaHPbO
,反应为PbO+OH-===HPbO-
。制备高纯铅的原电池原理示
2 2
意图如图所示。
(1)获得高纯铅的电极是 (填“正极”或“负极”)。
(2)电池的总反应的离子方程式是 。
(3)从物质和能量利用的角度说明该工艺的优点: 。答案 (1)正极
(2)HPbO-
+H ===Pb+OH-+H O (3)NaOH可循环使用,制备高纯铅的过程中获得电能
2 2 2
解析
(2)由图可知,HPbO- 在正极得到电子生成Pb,电极反应式为HPbO-
+2e-+H O===Pb+3OH-,H 在负
2 2 2 2
极失去电子生成H O,电极反应式为H -2e-+2OH-===2H
O,则电池总反应的离子方程式为HPbO-
2 2 2 2
+H ===Pb+OH-+H O。
2 2
3.(4分)在铜基配合物的催化作用下,利用电化学原理可将CO 转化为碳基燃料(包括CO、烷烃和羧酸等),
2
其装置原理如图所示。
(1)图中生成甲酸的电极反应式为 。
(2)当有0.2 mol H+通过质子交换膜时,理论上最多生成HCOOH的质量为 。
答案 (1)CO +2e-+2H+===HCOOH (2)4.6 g
2
解析 (1)由图可知,Pt电极氧元素价态升高失电子,故Pt电极为阳极,电极反应式为2H O-4e-
2
===O +4H+,石墨烯电极为阴极,电极反应式为CO +2e-+2H+===HCOOH。(2)当有0.2 mol H+通过质子交换
2 2
膜时,转移0.2 mol电子,生成0.1 mol HCOOH,质量为0.1 mol×46 g·mol-1=4.6 g。
4.(4分)少量的SO 经Na CO 溶液洗脱处理后,所得洗脱液主要成分为Na CO 、NaHCO 和Na SO ,利用
2 2 3 2 3 3 2 3
生物电池技术,可将洗脱液中的Na SO 转化为单质硫(以S表示)回收。
2 3
(1)该装置中,正极的电极反应式为 。
(2)一段时间后,若洗脱液中SO2-的物质的量减少了1 mol,则理论上HCO- 减少了 mol。
3 3
答案
(1)SO2- +4e-+6HCO-
===S↓+3H
O+6CO2-
(2)2
3 3 2 3
解析
分析可知,该装置中,正极的电极反应式为SO2- +4e-+6HCO-
===S↓+3H
O+6CO2-
,当消耗1 mol
3 3 2 3
亚硫酸根离子,转移4 mol电子,同时消耗6 mol碳酸氢根离子,生成6 mol碳酸根离子,根据电荷守恒,
则有4 mol H+通过质子交换膜移向正极,4 mol氢离子可以结合4 mol的碳酸根离子生成4 mol的碳酸氢根
离子,则理论上碳酸氢根离子减少了2 mol。5.(3分)纯净的硫化锌是半导体锂离子电池负极材料。在充电过程中发生合金化反应生成LiZn(合金相),同
时负极材料晶胞的组成变化如图所示。
充电过程中ZnS到LiZnS的电极反应式为
x y
(x和y用具体数字表示)。
答案 4ZnS+6Li++6e-===3Zn+4Li Zn S
1.5 0.25
1 1
解析 由均摊法可知,LiZnS中Li+和Zn2+共有7个,S2-有8× +6× =4个,由化合价代数和为零可知,
x y 8 2
LiZnS的化学式为Li Zn S。根据题干信息在“充电过程中,发生合金化反应生成LiZn(合金相)”,故
x y 1.5 0.25
ZnS负极充电时得电子有Zn生成,故充电时的电极反应为4ZnS+6Li++6e-===3Zn+4Li Zn S。
1.5 0.25
6.(4分)晶体Ⅱ可作电池正极材料,通过Zn2+在晶体Ⅱ中嵌入和脱嵌,实现电极材料充放电的原理如图所示。
“ⅱ”代表电池 (填“充电”或“放电”)过程,“ⅲ”的电极反应式为 。
答案 放电 ZnMn O-2xe-=== Mn O+xZn2+
x 0.61 0.39 0.61 0.39
7.(4分)科学家通过使用双极膜电渗析法来捕获和转化海水中的CO ,其原理如图所示。
2
(1)写出与电源正极相连的一极上的电极反应式: 。
(2)下列说法正确的是 (填字母)。
A.循环液1和循环液2中的阴离子种类相同
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜C.水的电离程度:处理后海水1>处理后海水2
D.该方法可以同时将海水进行淡化
答案 (1)Fe(CN) 4- -e-===Fe(CN) 3- (2)A
6 6
解析 (1)由图分析可知,电极X中Fe化合价降低,得到电子,作阴极,与电源负极相连;电极Y中Fe化
合价升高,失去电子,作阳极,与电源正极相连;与电源正极相连的一极上的电极反应式为Fe(CN) 4- -e-
6
===Fe(CN) 3- 。(2)由①可知电极X为阴极,电极反应式为Fe(CN) 3- +e-===Fe(CN) 4- ,电极Y为阳极,电
6 6 6
极反应式为Fe(CN) 4- -e-===Fe(CN) 3- ,则循环液1和2中均含有Fe(CN) 3- 和Fe(CN) 4- ,A项正确;由
6 6 6 6
电极X反应可知,循环液1中负电荷数增加,为平衡溶液中电荷,则海水中的钠离子应通过隔膜 1移向电
极X;由电极Y反应可知,循环液 2中负电荷数减少,为平衡溶液中电荷,则循环液中钾离子应通过隔膜
2进入左室,这样才能保持循环液中的离子不出现交换,隔膜1、2都为阳离子交换膜,B项错误;海水经
处理,HCO-
转换为CO ,CO 的水溶液呈弱酸性,会抑制水的电离,而酸化海水经处理,CO 转化为
3 2 2 2
HCO- ,HCO-
易水解,故水的电离程度:处理后海水1<处理后海水2,C项错误。
3 3
8.(4分)新能源的利用对实现“碳中和”也有重要意义。搭载钠离子电池的新能源汽车,动力充足、冬天也
无需频繁充电。第二代钠离子电池是以硬碳(C)为基底材料的嵌钠硬碳(NaC)和锰基高锰普鲁士白
y x y
Na Mn[Mn(CN) ]为电极的一种新型二次电池,在充放电过程中,Na+在两个电极之间往返嵌入和脱嵌。其
2 6
工作原理如图所示。
若用该钠离子电池给铅酸蓄电池充电,普鲁士白电极连接 (填“Pb”或“PbO ”)极,钠离子电池
2
负极的电极反应式为 。
答案 PbO NaC-xe-===C+xNa+
2 x y y
解析 给铅酸蓄电池充电时,普鲁士白为正极,连接铅酸蓄电池的PbO 电极,负极为嵌钠硬碳,电极反应
2
式为NaC-xe-===C+xNa+。
x y y
9.(3分)通过氢电极增压法可使氧化锌进一步制得单质锌(如图),储罐内ZnO溶解后形成[Zn(OH) ]2-,电解
4
池中发生总反应的离子方程式为 。答案 H +[Zn(OH) ]2- Zn+2H O+2OH-
2 4 2
解析 由图示可知,左侧电极为电解池的阳极,碱性条件下氢气在阳极失去电子发生氧化反应生成水,右
侧电极为阴极,[Zn(OH) ]2-在阴极得到电子发生还原反应生成锌和氢氧根离子,则电解池的总反应为H +
4 2
[Zn(OH) ]2- Zn+2H O+2OH-。
4 2
10.(3分)基于电化学原理,我国科学家利用固体氧化物电解池实现高选择性C H 电化学脱氢制
3 8
CH ==CHCH 的工艺,装置如图,则C H 生成CH ==CHCH 的电极反应式为 。
2 3 3 8 2 3
答案 C H +O2--2e-===CH ==CHCH +H O
3 8 2 3 2
11.(4分)微生物燃料电池的一种重要应用是废水处理中实现碳氮联合转化为CO 和N ,如图所示,其中
2 2
1,2为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。
(1)正极的电极反应式是 。
(2)协同转化总反应中当有标准状况下44.8 L N 生成时转移电子数是 。
2
答案
(1)2NO-
+12H++10e-===N ↑+6H O (2)44N
3 2 2 A
解析 (1)由图可知,正极的硝酸根离子得到电子在酸性条件下发生还原反应生成氮气,电极反应式是
2NO-
+12H++10e-===N ↑+6H O。(2)协同转化总反应为醋酸根离子、铵根离子、氧气反应生成二氧化碳、
3 2 2
氮气和水:4CH
COO-+4NH+
+11O ===8CO ↑+2N ↑+14H O,电子转移为11O ~44e-~2N ,标准状况下44.8
3 4 2 2 2 2 2 2
L N (为2 mol)生成时转移电子44 mol,个数是44N 。
2 A
12.(7分)中科院研究出首例在室温条件超快传输的氢负离子导体LaH,某小组据此设计了如图装置,以电
x
化学方法进行反应:CO (g)+3H (g) CH OH(g)+H O(g) ΔH=-49.5 kJ·mol-1。
2 2 3 2
(1)电极a为电源的 (填“正极”或“负极”)。(2)生成CH OH的电极反应式为 。
3
(3)若反应:CO (g)+H (g) CO(g)+H O(g) ΔH=+41.2 kJ·mol-1(副反应)也同时发生,出口Ⅱ为CO、
2 2 2
CH OH、CO 的混合气,且n(CO)∶n(CH OH)=1∶3,则惰性电极2的电流效率η为 (η=
3 2 3
利用的电量
×100%)。
总的电子电量
答案 (1)负极 (2)CO -6e-+6H-===CH OH+H O (3)90%
2 3 2
解析 (1)由信息可知,电解池装置中的离子导体可以传输氢负离子,氢气在惰性电极1上放电生成氢负离
子,氢负离子在惰性电极2上失电子变为氢原子,然后氢原子将二氧化碳还原为甲醇和水,则电极a为电
源的负极。(2)在惰性电极2上氢负离子失电子变为氢原子,然后氢原子将二氧化碳还原为甲醇和水,根据
得失电子守恒和电荷守恒配平电极反应式:CO -6e-+6H-===CH OH+H O。(3)若副反应也同时发生,出口Ⅱ
2 3 2
为CO、CH OH、CO 的混合气,且n(CO)∶n(CH OH)=1∶3,假设生成1 mol CO和3 mol CH OH,转移电
3 2 3 3
3mol×6
子1 mol×2+3 mol×6=20 mol,则惰性电极2的电流效率η为 ×100%=90%。
20mol