文档内容
章末综合检测(十) 化学实验
一、选择题:本题包括6小题,每小题只有一个选项最符合题意。
1.(2021·广东执信中学等三校联考)实验室中下列做法错误的是( )
A.用冷水贮存白磷
B.用浓硫酸干燥二氧化硫
C.用二氧化碳灭火器扑灭金属钾的燃烧
D.用酒精灯直接加热蒸发皿
C [金属钾着火燃烧生成KO 等,可与CO 反应放出O,故不能用二氧化碳灭火器灭
2 2 2 2
火,C错误。]
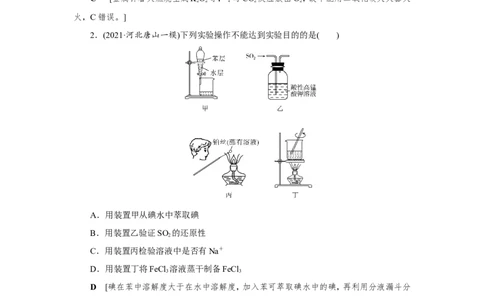
2.(2021·河北唐山一模)下列实验操作不能达到实验目的的是( )
A.用装置甲从碘水中萃取碘
B.用装置乙验证SO 的还原性
2
C.用装置丙检验溶液中是否有Na+
D.用装置丁将FeCl 溶液蒸干制备FeCl
3 3
D [碘在苯中溶解度大于在水中溶解度,加入苯可萃取碘水中的碘,再利用分液漏斗分
液,A正确;SO 通入酸性KMnO 溶液,溶液褪色,MnO被SO 还原为Mn2+,体现SO 的还原
2 4 2 2
性,B正确;铂丝蘸取溶液进行焰色反应,火焰若呈黄色,则含Na+,否则不含,C正确;加入
促进FeCl 的水解,不能得到FeCl ,另外蒸发要在蒸发皿中进行,D错误。]
3 3
3.(2021·湖南名校教育联合体联考)以下除杂方法(括号内为少量杂质)中,正确的是(
)
选项 被提纯的物质 除杂试剂 分离方法
A HS(HCl) CuSO 溶液 洗气
2 4
B CO(HCl) 饱和NaCO 溶液 洗气
2 2 3C O(N ) 炽热的铜网 —
2 2
D NaBr溶液(NaI) 溴的CCl 溶液 分液
4
D [H S与CuSO 溶液反应生成CuS沉淀,A错误;CO、HCl都与NaCO 溶液反应,应
2 4 2 2 3
选用饱和NaHCO 溶液,B错误;N 与灼热的铜不反应,O 与灼热的铜反应生成CuO,C错误;
3 2 2
Br 的氧化性强于I,Br 将NaI氧化生成I,并利用CCl 萃取、分液,保留水层即可,D正确。]
2 2 2 2 4
4.(2021·江苏苏州调研)根据下列实验操作和现象所得出的结论正确的是( )
选项 实验操作和现象 结论
NaSO 样品溶于水,加入硝酸酸化的Ba(NO ) 溶液,
A 2 3 3 2 NaSO 样品中含有NaSO
有白色沉淀产生 2 3 2 4
向KI溶液中滴入少量新制氯水和四氯化碳,振荡、
B I-的还原性强于Cl-
静置,溶液下层呈紫红色
室温下,向浓度均为0.1 mol·L-1的BaCl 和CaCl 混
C 2 2 白色沉淀是BaCO
合溶液中加入NaCO 溶液,出现白色沉淀 3
2 3
向苯和液溴的混合物中加入铁粉,将气体通入硝酸银
D 苯与Br 发生取代反应
溶液中,有淡黄色沉淀产生 2
B [硝酸可将NaSO 氧化为NaSO ,原样品中有无NaSO 实验现象一样,因此由操作
2 3 2 4 2 4
和现象不能证明NaSO 样品中含有NaSO ,A错误;向KI溶液中滴入少量新制氯水发生反
2 3 2 4
应Cl +2I—===2Cl-+I ,由还原剂的还原性大于还原产物的还原性可知I-的还原性强于Cl
2 2
-,加入四氯化碳后发生萃取,密度大的有机层处于溶液下层呈紫红色,有碘生成,碘离子被
氯气氧化,由操作和现象能证明I-的还原性强于Cl-,B正确;CaCl 溶液与NaCO 反应生成
2 2 3
的CaCO 也是白色沉淀,由操作和现象无法证明白色沉淀是BaCO ,C错误;液溴易挥发,进
3 3
入硝酸银溶液与水反应生成溴离子,再与硝酸银反应生成淡黄色沉淀,由操作和现象不能证
明苯与Br 发生取代反应,D错误。]
2
5.(2021·河南鹤壁检测)由AlCl 溶液制备AlCl ·6H O的装置如下图,下列说法错误的是
3 3 2
( )
A.通入HCl的作用是抑制AlCl 水解和降低AlCl 溶解度,使其以AlCl ·6H O晶体形式
3 3 3 2
析出
B.抽滤后洗涤时,合适的洗涤剂是饱和氯化铝溶液C.将AlCl ·6H O加热脱水,即可得到无水AlCl
3 2 3
D.为得到纯净的AlCl ·6H O,宜采用的干燥方式是用滤纸吸干
3 2
C [Al3+会发生水解反应:Al3++3H
2
O⇌Al(OH)
3
+3H+,通入HCl可以抑制Al3+的水解,
增大了溶液中Cl-的浓度,降低AlCl 溶解度,有利于AlCl •6HO结晶,A正确;增大氯离子
3 3 2
浓度可防止晶体溶解而损失,合适的洗涤剂为饱和氯化铝溶液,B正确;加热促进AlCl 水解
3
生成氢氧化铝,将AlCl ·6HO加热脱水不能得到无水AlCl ,C错误;由于AlCl •6HO受热
3 2 3 3 2
易分解,所以不能使用烘干的方式干燥,可以使用滤纸吸干的方式干燥晶体,D正确。]
6.(2021·湖南长沙检测)某化学兴趣小组从含有KI、KNO 等成分的工业废水中回收I 和
3 2
KNO,其流程如下:
3
下列说法正确的是( )
A.步骤1中有机相应从分液漏斗下端放出,无机相从上口倒出
B.步骤2分离方法为过滤
C.步骤3可在装置 中完成
D.步骤4中,将溶液蒸发至只剩少量水时,用余热蒸干
C [苯的密度小于水的密度,步骤1中有机相在上层,无机相在下层,故分液时,无机
相从下端放出,有机相从上口倒出,A错误;步骤2从有机相分离苯和粗碘的方法为蒸馏,B
错误;碘易升华,步骤3利用粗碘制取精碘可采用升华-凝华的方法,C正确;KNO 的溶解
3
度受温度影响较大,从溶液中获得KNO 晶体,采用蒸发浓缩、冷却结晶的方法,D错误。]
3
二、非选择题:本题包括3小题。
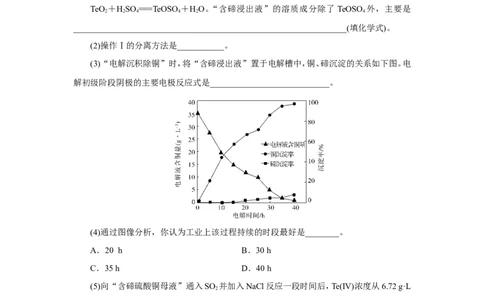
7.(2021·湖北襄阳等四地联考)碲及其化合物具有许多优良性能,被广泛用于冶金、化工、
医药卫生等工业领域。工业上用铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)经如
下工艺流程得到粗碲。已知TeOSO 为正盐。
4
(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应:Cu Te+2O===2CuO
2 2
+TeO ;
2
TeO +HSO ===TeOSO +HO。“含碲浸出液”的溶质成分除了TeOSO 外,主要是
2 2 4 4 2 4
________________________________________________________________(填化学式)。
(2)操作Ⅰ的分离方法是___________。
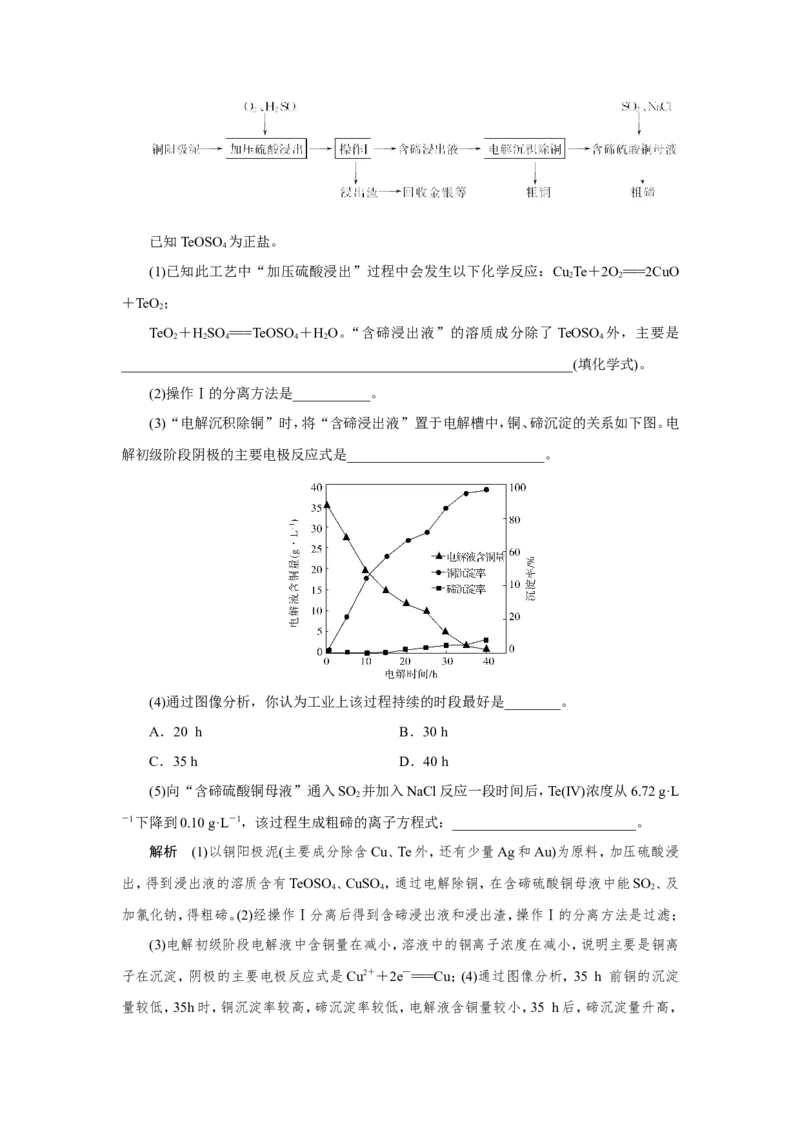
(3)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电
解初级阶段阴极的主要电极反应式是____________________________。
(4)通过图像分析,你认为工业上该过程持续的时段最好是________。
A.20 h B.30 h
C.35 h D.40 h
(5)向“含碲硫酸铜母液”通入SO 并加入NaCl反应一段时间后,Te(IV)浓度从6.72 g·L
2
-1下降到0.10 g·L-1,该过程生成粗碲的离子方程式:__________________________。
解析 (1)以铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)为原料,加压硫酸浸
出,得到浸出液的溶质含有TeOSO、CuSO ,通过电解除铜,在含碲硫酸铜母液中能SO 、及
4 4 2
加氯化钠,得粗碲。(2)经操作Ⅰ分离后得到含碲浸出液和浸出渣,操作Ⅰ的分离方法是过滤;
(3)电解初级阶段电解液中含铜量在减小,溶液中的铜离子浓度在减小,说明主要是铜离
子在沉淀,阴极的主要电极反应式是Cu2++2e—===Cu;(4)通过图像分析,35 h 前铜的沉淀
量较低,35h时,铜沉淀率较高,碲沉淀率较低,电解液含铜量较小,35 h后,碲沉淀量升高,故工业上该过程持续的时段最好是35 h;(5)向“含碲硫酸铜母液”通入SO 并加入NaCl反
2
应一段时间后,Te(Ⅳ)浓度从6.72 g·L-1下降到0.10 g·L-1,该过程是Te(Ⅳ)被二氧化硫还原
为粗碲,二氧化硫被氧化成硫酸根,根据电荷守恒和质量守恒写出生成粗碲的离子方程式:
TeO2++2SO +3HO===Te↓+2SO+6H+。
2 2
答案 (1)CuSO (2)过滤 (3)Cu2++2e—===Cu
4
(4) C (5)TeO2++2SO +3HO===Te↓+2SO+6H+
2 2
8.(2021·山东德州检测)甘氨酸亚铁[(NH CHCOO)Fe]是新一代畜禽饲料补铁添加剂。
2 2 2
某实验小组以硫酸亚铁为铁源制备甘氨酸亚铁,其简要流程如下。
已知相关物质的信息如下:
甘氨酸 柠檬酸 甘氨酸亚铁
(NH CHCOOH) (3羟基1,3,5戊三酸) [(NH CHCOO)Fe]
2 2 2 2 2
浅黄褐绿色结晶粉末,易溶于
水,难溶于乙醇,结构如下
图:
易溶于水,微溶于乙醇,具有 易溶于水和乙醇,具有较强的
两性 酸性和还原性
回答下列问题:
(1)步骤(a)中加入铁粉的作用是___________________________________________;
写出生成沉淀的化学方程式:_________________________________________。
(2)步骤(b)中为了提高甘氨酸亚铁的产率,需要控制溶液的pH在5.5~6.0之间,pH过低
甘氨酸亚铁产率将下降,其原因为___________________________________;柠檬酸的作用
包括________(填字母)。
A.调节溶液的pH
B.除去步骤(a)中加入的铁粉
C.防止Fe2+被氧化
D.促进沉淀的溶解,加快反应速率
(3)步骤(b)中趁热过滤的目的是_________________________________________。
(4)步骤(c)中加入乙醇的目的是__________________________________________。
(5)产品中Fe2+含量的检测:称取m g样品溶解于适量蒸馏水中,配制成100.0 mL溶液。用移液管取出25.00 mL溶液于锥形瓶中,向其中加入一定量混酸X进行酸化,用c mol·L-1
的KMnO 标准溶液滴定至终点,消耗KMnO 溶液的体积为V mL。
4 4
①混酸X可以是________(填字母)。
A.HCl和HSO B.HCl和HPO
2 4 3 4
C.HSO 和HPO D.HSO 和HNO
2 4 3 4 2 4 3
E.HCl和HNO
3
②滴定终点的现象为_____________________________________________________。
③据此计算Fe2+的质量分数为____________________________________________。
解析 (1)Fe2+在空气中易被氧化,加入Fe粉可防止其被氧化;Fe2+与HCO电离出的CO
结合,H+再和过量的HCO反应生成CO。
2
(2)NH CHCOOH中有碱性基团—NH ,可以和H+反应,故pH应控制在5.5~6.0之间。
2 2 2
(4)甘氨酸亚铁难溶于乙醇,加入乙醇可降低其损失。
(5)①HCl有还原性、HNO 有氧化性,两者都会影响滴定结果,故选C;③由关系式MnO
3
~5Fe2+可得n(Fe2+)=5cV×10-3mol,则Fe2+的质量分数为×100%=×100%。
答案 (1)防止Fe2+被氧化
FeSO +2NH HCO ===FeCO ↓+(NH )SO +HO+CO↑
4 4 3 3 4 2 4 2 2
(2)H+会与NH CHCOOH反应,不利于甘氨酸亚铁的生成 ACD
2 2
(3)除去铁粉,减少因温度降低甘氨酸亚铁析出带来的损失
(4)降低甘氨酸亚铁的损失
(5)①C ②当滴入最后一滴标准溶液时,溶液变为紫色或浅紫色,且半分钟内不变色
③×100%
9.(2021·四川仁寿一中检测)为了探究乙二酸的不稳定性、弱酸性和还原性,某化学兴趣
小组设计如下实验。
查阅资料乙二酸俗称草酸,草酸晶体(H C O·2H O)在100 ℃时开始升华,157 ℃时大量
2 2 4 2
升华并开始分解;草酸蒸气在低温下迅速冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清
石灰水变浑浊。
Ⅰ.乙二酸的不稳定性:根据草酸晶体的组成,猜想其受热分解产物为CO、CO 和HO。
2 2
(1)请用下列装置组成一套探究并验证其产物的实验装置。请回答下列问题:①装置的连接顺序为:A→D→____→____→F→E→C→G。
②装置中冰水混合物的作用是__________________________________________。
③整套装置存在不合理之处为___________________________________________。
Ⅱ.乙二酸的弱酸性:
该小组同学为验证草酸性质需0.1 mol/L的草酸溶液480 mL。
(2)配制该溶液需要草酸晶体为____ g。
(3)为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是____________。
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定0.1 mol/L草酸溶液的pH
C.将草酸溶液加入NaCO 溶液中,有CO 放出
2 3 2
D.测定草酸钠溶液的pH
(4)该小组同学将0.1 mol/L草酸溶液和0.1 mol/L的NaOH等体积混合后,测定反应后溶
液呈酸性,则所得溶液中各离子浓度由大到小的顺序为______________________________
________________________。
Ⅲ.乙二酸的还原性:
(5)该小组同学向用硫酸酸化的KMnO 溶液中滴入过量的草酸溶液,发现酸性KMnO
4 4
溶液褪色,从而判断草酸具有较强的还原性,该反应的离子方程式为__________________
______________________________________________________。
解析 (1)①根据草酸晶体的组成,猜想其受热分解产物为CO、CO和HO,由于草酸晶
2 2
体(HC O•2HO)在100 ℃时开始升华,157 ℃时大量升华并开始分解,草酸蒸气在低温下可
2 2 4 2
冷凝为固体,所以生成的气体中含有草酸蒸气,草酸蒸气能使澄清石灰水变浑浊,检验产物
时可用冰水混合物使草酸冷凝以除去草酸干扰,因为检验二氧化碳需要氢氧化钙溶液,溶液中含有水分,所以要先用无水硫酸铜检验水蒸气;用CuO检验CO,CO生成二氧化碳,为防
止CO生成的CO 干扰产物中CO 的检验,所以要先检验CO、后检验CO,故顺序为用D检
2 2 2
验水、用B冷却得到草酸晶体、用G检验二氧化碳、用F吸收二氧化碳、用E干燥CO、用C
氧化CO、再用G检验产物二氧化碳,排列顺序是A→D→B→G→F→E→C→G;
②冰水混合物的作用是除去产物中草酸蒸气,防止干扰实验,故需除去草酸蒸气,防止
干扰实验;③CO有毒,不能直接排空,所以要有尾气处理装置,而图中没有CO尾气处理装
置。
(2)配制480 mL 0.1 mol•L-1的草酸溶液需要500 mL容量瓶,则需要草酸晶体质量=
cVM=0.1 mol/L×0.5 L×126 g/mol=6.3 g;
(3)将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色,说明草酸具有酸性,但不能说明
草酸部分电离,所以不能证明草酸是弱酸,A错误;测定0.1 mol·L-1草酸溶液的pH,如果溶
液中氢离子浓度小于草酸浓度的2倍,就说明草酸部分电离为弱电解质,B正确;将草酸溶液
加入NaCO 溶液中,有CO 放出,说明草酸酸性大于碳酸,但不能说明草酸部分电离,则不
2 3 2
能证明草酸是弱酸,C错误;测定草酸钠溶液的pH,如果草酸钠是强酸强碱盐,溶液呈中性,
如果草酸钠是弱酸强碱盐,溶液呈碱性,所以能证明草酸是否是弱电解质,D正确。
(4)二者恰好反应生成NaHC O,混合溶液呈酸性,则c(H+)>c(OH-),Na+不水解、HC O
2 4 2
水解,则c(Na+)>c(HC O),溶液呈酸性说明HC O电离程度大于水解程度,所以溶液中c(H
2 2
+)>c(C O),溶液呈酸性则c(OH-)浓度最小,则溶液中离子浓度大小顺序是c(Na+)>
2
c(HC O)>c(H+)>c(C O)>c(OH-);
2 2
(5)酸性条件下,KMnO 具有强氧化性,酸性KMnO 溶液和草酸发生氧化还原反应而使
4 4
酸性高锰酸钾溶液褪色,Mn元素化合价由+7价变为+2价,则C元素生成稳定氧化物
CO ,根据转移电子相等、原子守恒、电荷守恒,书写方程式为2MnO+5HC O +6H+
2 2 2 4
===2Mn2++10CO↑+8HO。
2 2
答案 (1)①B G ②除去草酸蒸气,防止干扰实验 ③没有CO尾气处理装置
(2)6.3 (3)BD (4)c(Na+)>c(HC O)>c(H+)>c(C O)>c(OH-)
2 2
(5)2MnO+5HC O+6H+===2Mn2++10CO↑+8HO
2 2 4 2 2