文档内容
专题突破(十) 水溶液中离子平衡的两类特殊图像及分析
近几年,高考试题中关于水溶液中离子平衡的图像考查较多,两类特殊图像(对数图像、
分布系数图像)更是备受命题专家的青睐,此类试题的信息量较大,且都隐藏于图像中,对考
生的综合能力要求较高,体现《中国高考评价体系》对以解决实际问题为核心的实践操作能
力的要求,要求考生合理分析图像,识别有效证据,获取有效信息,科学推理论证,处理转化
数据,能够有效解决有关电解质溶液图像的实际问题。
1.对数图像
(1)对数图像的含义
将溶液中某一微粒的浓度[如c(A)]或某些微粒浓度的比值取常用对数,即lg c(A)或lg,
与溶液中的pH或溶液的体积等关系作出的图像称为对数图像。图中数据的含义为:
①若c(A)=1时,lgc(A)=0。
②若c(A)>1时,lg c(A)取正值且c(A)越大,lg c(A)越大。
③若c(A)<1时,lg c(A)取负值,且c(A)越大,lg c(A)越大,但数值越小。
(2)常考对数图像的类型
图像种类 具体类型 含义 变化规律
生成物与反应物离子浓 lg越大,反应向正反应方
lg
度比的常用对数 向进行的程度越大
稀释后与稀释前体积比
对数图像 lg lg越大,稀释程度越大
的常用对数
氢离子与氢氧根离子浓 AG越大,酸性越强,中性
AG=lg
度比的常用对数 时,=1
氢离子浓度的常用对数 pH越大,c(H+)越小,溶
pH=-lg c(H+)
负值 液的碱性越强
负对数图像
C 离子浓度的常用对数
pC=-lg c(C) pC越大,c(C)越小
负值
2.分布系数图像
分布曲线是指以pH为横坐标,分布系数即组分的平衡浓度占总浓度的分数为纵坐标,
分布系数与溶液pH之间的关系曲线。
一元弱酸(以CHCOOH
举例 3 二元酸(以草酸为例) 三元酸(以HPO 为例)
为例) 3 4弱电解质
分布系数
图
δ 为 HC O 分布系 δ 为HPO 分布系数、δ
0 2 2 4 0 3 4 1
δ、δ 分别为CHCOOH、 数、δ 为HC O分布系 为HPO分布系数、δ 为
δ 0 1 3 1 2 2 2
CHCOO-分布系数 数、δ 为C O分布系 HPO分布系数、δ 为PO
3 2 2 3
数 分布系数
当溶液的pH=2时,δ=
当pH<pK 时,主要存在 当溶液的pH=1.2时 0
a δ,pH=7.1时δ=δ,pH
形式是CHCOOH;当pH δ =δ ,pH=4.2时δ 1 1 2
3 0 1 1 =12.2时δ=δ;当pH<
>pK 时,主要存在形式 =δ,当pH<1.2 时, 2 3
a 2 2时,HPO 占优势;在2
是CHCOO-。δ 与δ 曲 HC O 占优势;在1.2 3 4
含义 3 0 1 2 2 4 <pH<7.1 区间,HPO
线相交在δ=δ=0.5处, <pH<4.2 区间 , 2
0 1 占优势;在 7.1<pH<
此 时 c(CHCOOH) = HC O 占优势,而当
3 2 12.2区间,HPO占优势;
c(CHCOO-),即 pH= pH>4.2时,C O为主
3 2 而当pH>12.2时,PO为
pK 要存在形式
a 主要存在形式
pH由2到6发生反应的
pH由4到6发生反应 pH由11到14发生反应
离子方程 离子方程式:CHCOOH
3 的离子方程式:HC O 的离子方程式:HPO+
式 +OH-===CH COO-+ 2
3 +OH-===C O+HO OH-===PO+HO
HO 2 2 2
2
K(CHCOOH)=,从图可
3 K (H C O)=,从图可
知 , c(CHCOO - ) = 2 2 2 4 K (H PO )=,从图可知,
3 知,c(C O)=c(HC O) 3 3 4
c(CHCOOH)时,pH=pK 2 2 c(HPO)=c(PO)时 pH=
求lg K 3 时pH=4.2,K =c(H
=4.76。K(CHCOOH)= 2 12.2,K =c(H+)=10-
3 +)=10-4. 2,lg K =- 3
c(H + ) = 10 - 4.76 , lg 2 12.2,lg K=-12.2
4.2 a
K(CHCOOH)=-4.76
3
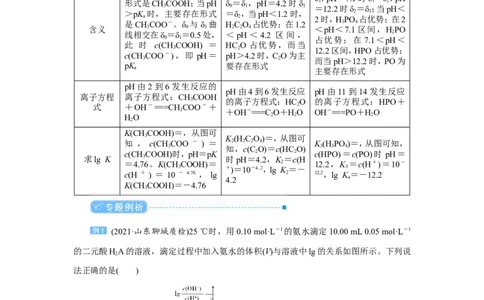
(2021·山东聊城质检)25 ℃时,用0.10 mol·L-1的氨水滴定10.00 mL 0.05 mol·L-1
的二元酸HA的溶液,滴定过程中加入氨水的体积(V)与溶液中lg的关系如图所示。下列说
2
法正确的是( )
A.H
2
A的电离方程式为H
2
A⇌H++HA-
B.B点溶液中,水电离出氢离子浓度为1.0×10-8 mol·L-1C.C点溶液中,c(NH)+c(NH ·H O)=2c(A2-)
3 2
D.25 ℃时,氨水的电离平衡常数为K =
b
D [25 ℃时,A点lg=-12,结合K =c(OH-)·c(H+)=1×10-14,解得c(H+)=0.1
w
mol/L,说明0.05 mol HA完全电离,则电离方程式为HA===2H++A2-,A错误。B点加入
2 2
10 mL氨水,恰好完全反应生成(NH )A,此时lg=-2,则有c(H+)=1×10-6mol/L,而H+全
4 2
部来源于水的电离,故水电离出的c(H+)=1×10-6mol/L,B错误。C点溶液是(NH )A和
4 2
NH ·HO混合液,lg=0,则有c(OH-)=c(H+),根据电荷守恒可得:c(H+)+c(NH)=c(OH-)
3 2
+2c(A2-),则有c(NH)=2c(A2-),C错误。C点溶液中c(NH)=2c(A2-)=0.1 mol/L×,由
c(NH)+c(NH ·HO)=0.1 mol/L×可得,c(NH ·HO)=0.1 mol/L×;C点溶液lg=0,c(OH
3 2 3 2
-)=c(H+)=10-7 mol/L,求出25℃时NH ·HO的电离常数为K =,D正确。]
3 2 b
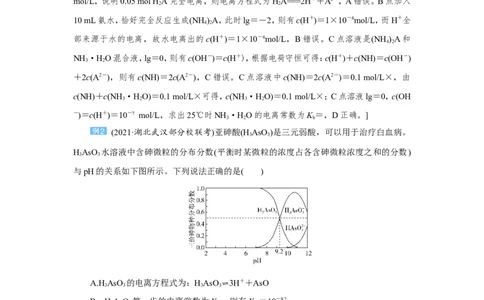
(2021·湖北武汉部分校联考)亚砷酸(H AsO )是三元弱酸,可以用于治疗白血病。
3 3
HAsO 水溶液中含砷微粒的分布分数(平衡时某微粒的浓度占各含砷微粒浓度之和的分数)
3 3
与pH的关系如下图所示。下列说法正确的是( )
A.H
3
AsO
3
的电离方程式为:H
3
AsO 3⇌3H++AsO
B.HAsO 第一步的电离常数为K ,则有K =10-9.2
3 3 a1 a1
C.HAsO 溶液的pH约为9.2
3 3
D.pH=12时,溶液中c(H AsO)+2c(HAsO)+3c(AsO)+c(OH-)=c(H+)
2B [由图可知,HAsO 水溶液中存在HAsO 、HAsO、HAsO等,则HAsO 是三元弱酸,
3 3 3 3 2 3 3
分步发生电离,以第一步电离为主,电离方程式为H
3
AsO 3⇌H++H
2
AsO,A错误。H
3
AsO
3
第
一步的电离常数为K =,由图可知,HAsO 和HAsO的分布分数相等时,溶液的pH=9.2,
a1 3 3 2
即c(H AsO )=c(H AsO)时c(H+)=10-9.2 mol·L-1,则有K = c(H+)=10-9.2,B正确。HAsO
3 3 2 a1 3 3
溶液呈酸性,则其pH<7,C错误。pH=12时,HAsO 溶液中加入NaOH溶液等碱液,结合电
3 3
荷守恒推知,溶液中c(H AsO)+2c(HAsO)+3c(AsO)+c(OH-)>c(H+),D错误。]
2
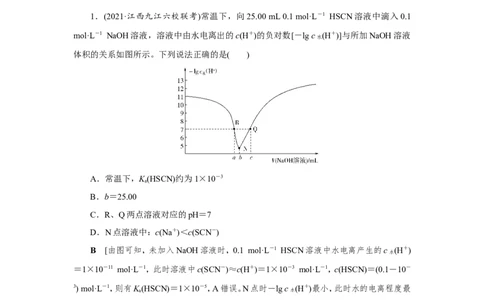
1.(2021·江西九江六校联考)常温下,向25.00 mL 0.1 mol·L-1 HSCN溶液中滴入0.1
mol·L-1 NaOH溶液,溶液中由水电离出的c(H+)的负对数[-lg c (H+)]与所加NaOH溶液
水
体积的关系如图所示。下列说法正确的是( )
A.常温下,K(HSCN)约为1×10-3
a
B.b=25.00
C.R、Q两点溶液对应的pH=7
D.N点溶液中:c(Na+)<c(SCN-)
B [由图可知,未加入NaOH溶液时,0.1 mol·L-1 HSCN溶液中水电离产生的c (H+)
水
=1×10-11 mol·L-1,此时溶液中c(SCN-)≈c(H+)=1×10-3 mol·L-1,c(HSCN)=(0.1-10-
3) mol·L-1,则有K(HSCN)=1×10-5,A错误。N点时-lg c (H+)最小,此时水的电离程度最
a 水
大,说明HSCN和NaOH溶液恰好完全反应生成NaSCN,由于两溶液的浓度相同,则有b=
25.00,B正确。图中R点溶液呈中性,N点HSCN与NaOH溶液恰好完全反应,Q点NaOH溶
液过量,此时溶液为NaSCN和NaOH的混合溶液,溶液呈碱性,C错误。N点为NaSCN溶液,
由于SCN-发生水解而使溶液呈碱性,则有c(OH-)>c(H+);据电荷守恒可得关系:c(Na+)+
c(H+)=c(SCN-)+ c(OH-),则有c(Na+)>c(SCN-), D错误。]
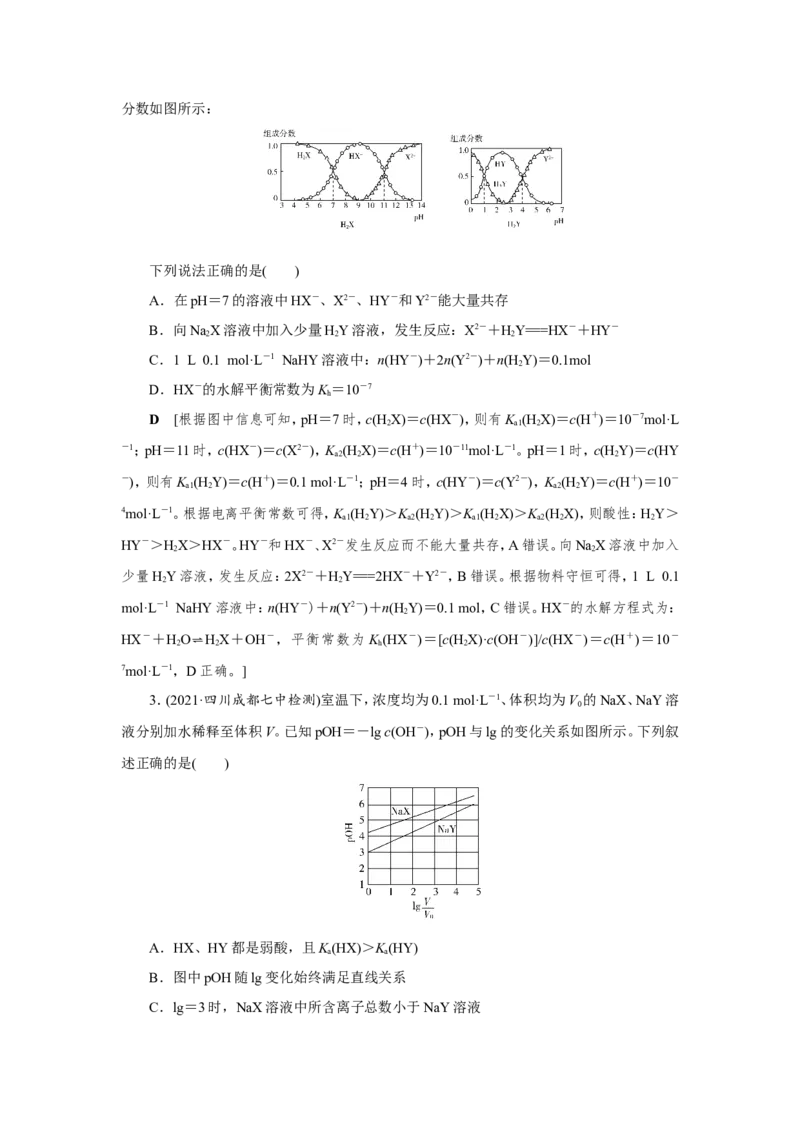
2.(2021·山西汾阳中学检测)HX和HY均为二元弱酸,常温下,将NaOH溶液分别滴加
2 2
到HX和HY的溶液中,不同pH环境下不同形态的粒子(即酸、酸式酸根、酸根离子)的组成
2 2分数如图所示:
下列说法正确的是( )
A.在pH=7的溶液中HX-、X2-、HY-和Y2-能大量共存
B.向NaX溶液中加入少量HY溶液,发生反应:X2-+HY===HX-+HY-
2 2 2
C.1 L 0.1 mol·L-1 NaHY溶液中:n(HY-)+2n(Y2-)+n(H Y)=0.1mol
2
D.HX-的水解平衡常数为K =10-7
h
D [根据图中信息可知,pH=7时,c(H X)=c(HX-),则有K (H X)=c(H+)=10-7mol·L
2 a1 2
-1;pH=11时,c(HX-)=c(X2-),K (H X)=c(H+)=10-11mol·L-1。pH=1时,c(H Y)=c(HY
a2 2 2
-),则有K (H Y)=c(H+)=0.1 mol·L-1;pH=4时,c(HY-)=c(Y2-),K (H Y)=c(H+)=10-
a1 2 a2 2
4mol·L-1。根据电离平衡常数可得,K (H Y)>K (H Y)>K (H X)>K (H X),则酸性:HY>
a1 2 a2 2 a1 2 a2 2 2
HY->HX>HX-。HY-和HX-、X2-发生反应而不能大量共存,A错误。向NaX溶液中加入
2 2
少量HY溶液,发生反应:2X2-+HY===2HX-+Y2-,B错误。根据物料守恒可得,1 L 0.1
2 2
mol·L-1 NaHY溶液中:n(HY-)+n(Y2-)+n(H Y)=0.1 mol,C错误。HX-的水解方程式为:
2
HX-+H
2
O⇌H
2
X+OH-,平衡常数为K
h
(HX-)=[c(H
2
X)·c(OH-)]/c(HX-)=c(H+)=10-
7mol·L-1,D正确。]
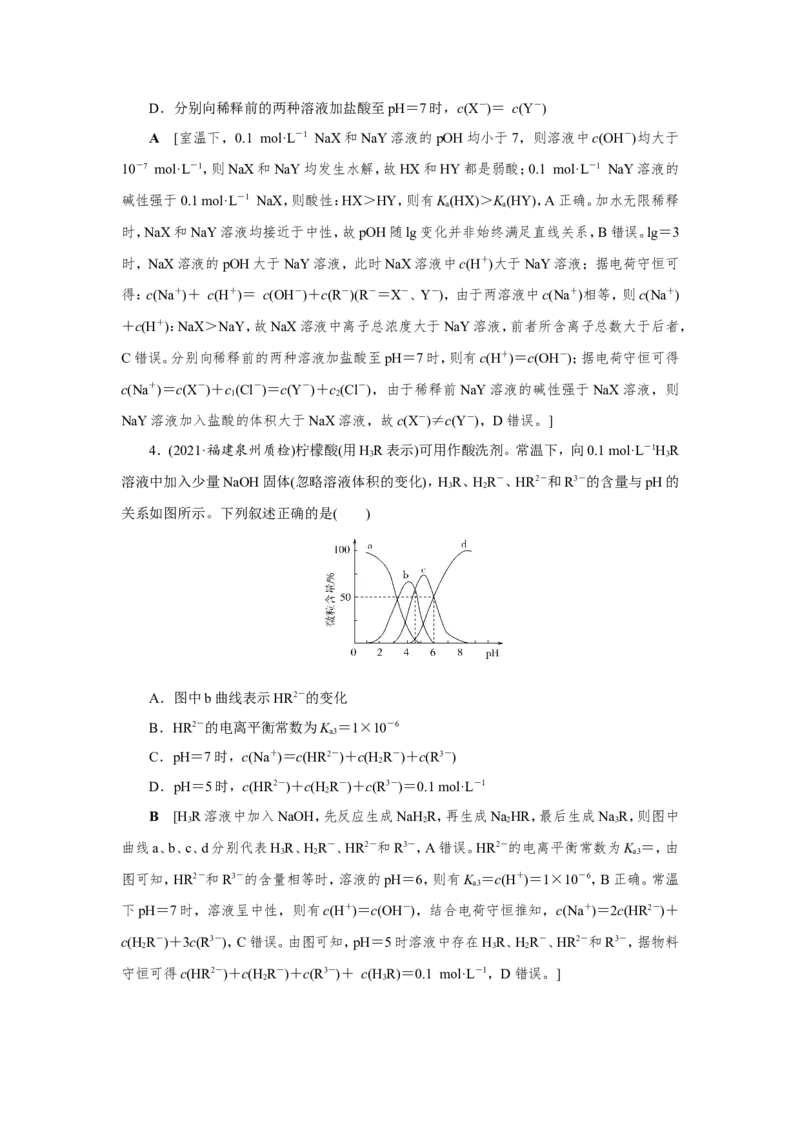
3.(2021·四川成都七中检测)室温下,浓度均为0.1 mol·L-1、体积均为V 的NaX、NaY溶
0
液分别加水稀释至体积V。已知pOH=-lg c(OH-),pOH与lg的变化关系如图所示。下列叙
述正确的是( )
A.HX、HY都是弱酸,且K(HX)>K(HY)
a a
B.图中pOH随lg 变化始终满足直线关系
C.lg=3时,NaX溶液中所含离子总数小于NaY溶液D.分别向稀释前的两种溶液加盐酸至pH=7时,c(X-)= c(Y-)
A [室温下,0.1 mol·L-1 NaX和NaY溶液的pOH均小于7,则溶液中c(OH-)均大于
10-7 mol·L-1,则NaX和NaY均发生水解,故HX和HY都是弱酸;0.1 mol·L-1 NaY溶液的
碱性强于0.1 mol·L-1 NaX,则酸性:HX>HY,则有K(HX)>K(HY),A正确。加水无限稀释
a a
时,NaX和NaY溶液均接近于中性,故pOH随lg变化并非始终满足直线关系,B错误。lg=3
时,NaX溶液的pOH大于NaY溶液,此时NaX溶液中c(H+)大于NaY溶液;据电荷守恒可
得:c(Na+)+ c(H+)= c(OH-)+c(R-)(R-=X-、Y-),由于两溶液中c(Na+)相等,则c(Na+)
+c(H+):NaX>NaY,故NaX溶液中离子总浓度大于NaY溶液,前者所含离子总数大于后者,
C错误。分别向稀释前的两种溶液加盐酸至pH=7时,则有c(H+)=c(OH-);据电荷守恒可得
c(Na+)=c(X-)+c(Cl-)=c(Y-)+c(Cl-),由于稀释前NaY溶液的碱性强于NaX溶液,则
1 2
NaY溶液加入盐酸的体积大于NaX溶液,故c(X-)≠c(Y-),D错误。]
4.(2021·福建泉州质检)柠檬酸(用HR表示)可用作酸洗剂。常温下,向0.1 mol·L-1HR
3 3
溶液中加入少量NaOH固体(忽略溶液体积的变化),HR、HR-、HR2-和R3-的含量与pH的
3 2
关系如图所示。下列叙述正确的是( )
A.图中b曲线表示HR2-的变化
B.HR2-的电离平衡常数为K =1×10-6
a3
C.pH=7时,c(Na+)=c(HR2-)+c(H R-)+c(R3-)
2
D.pH=5时,c(HR2-)+c(H R-)+c(R3-)=0.1 mol·L-1
2
B [H R溶液中加入NaOH,先反应生成NaH R,再生成NaHR,最后生成NaR,则图中
3 2 2 3
曲线a、b、c、d分别代表HR、HR-、HR2-和R3-,A错误。HR2-的电离平衡常数为K =,由
3 2 a3
图可知,HR2-和R3-的含量相等时,溶液的pH=6,则有K =c(H+)=1×10-6,B正确。常温
a3
下pH=7时,溶液呈中性,则有c(H+)=c(OH-),结合电荷守恒推知,c(Na+)=2c(HR2-)+
c(H R-)+3c(R3-),C错误。由图可知,pH=5时溶液中存在HR、HR-、HR2-和R3-,据物料
2 3 2
守恒可得c(HR2-)+c(H R-)+c(R3-)+ c(H R)=0.1 mol·L-1,D错误。]
2 3