文档内容
专题突破卷 01 化学计量
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列对摩尔(mol)的有关说法中不正确的是
A.摩尔是一个单位而非物理量
B.氧气的摩尔质量就是其相对分子质量
C.1mol任何气体所含气体的分子数目都相等
D.0.5molH 约含有6.02×1023个原子
2
2.下列说法中正确的是
A.硫酸的摩尔质量是98g B.2molCl-的质量是71g
C.氮气的摩尔质量是14g/mol D.1mol氯气的质量是35.5g
3.某物质在一定条件下加热分解,产物都是气体。分解方程式为2A B+2C+2D。测得生成的混合气体
的平均相对分子质量为2a,则A的相对分子质量为
A.7a B.5a C.2.5a D.2a
4.下列叙述正确的是
A. 的质量为16 g∙mol−1
B. 离子中的电子数约为 个
C. 的摩尔质量是32g
D. 含有氢原子数目为1mol
5.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,2.24LSO 中含氧原子数为0.3N
3 A
B.1 mol Na O 中,含有阴阳离子总数为4N
2 2 A
C.28 g N 与足量H 反应转移电子数6N
2 2 A
D.1mol C H (纯净物)最多含4N 个甲基
5 12 A6.氯碱工业通过电解饱和食盐水制备氯气: ;下列有关氯碱工业
的说法不正确的是
A.工业上可利用生成的 和 制盐酸
B.每生成1 mol 转移电子数约为
C.获得的主要产品除 外,还有烧碱和
D.工业上可用澄清石灰水吸收 联合生产漂白粉
7.关于0.1 mol·L-1 HNO 溶液的叙述错误的是
3
A.1 L该溶液中含有HNO 的质量为6.3 g
3
B.0.5 L该溶液中氢离子的物质的量浓度为0.1 mol·L-1
C.从1 L该溶液中取出100 mL,则取出溶液中HNO 的物质的量浓度为0.01 mol·L-1
3
D.取该溶液10 mL,加水稀释至100 mL后HNO 的物质的量浓度为0.01 mol·L-1
3
8.二氧化氯 是一种优良的消毒剂,可用氯酸钠和双氧水在酸性条件下反应制备:
(未配平)。下列说法正确的是
A.每转移1mol电子,生成标准状况下11.2L
B. 是氧化剂,发生氧化反应
C. 是还原产物
D.产物中 与 的物质的量之比为1∶2
9.已知Q与R的摩尔质量之比为9:22,在反应X+2Y=Q +R中,当1.6gX与一定量Y完全反应后,生成
4.4gR,则参与反应的Y和生成物Q的质量之比为
A.46:9 B.32:9 C.23:9 D.16:9
10.实验中需用 的 溶液950mL,配制时应选用的容量瓶的规格和称取 的质量分别为
A.1000mL,212g B.950mL,201.4g C.1000mL,201.4g D.500mL,100.7g
11.N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.0.1 mol·L-1的NH HCO 溶液与NaOH溶液等体积混合并加热,产生的氨气标况下2.24L
4 3
B.标况下,1molN 和O 的混合气体总体积约为22.4L
2 2
C.常温常压下,2.8gCO和C H 的混合气体中含有的分子数目为0.1 N
2 4 A
D.39.0gNa O 与足量水完全反应,转移的电子数为0.5 N
2 2 A
12.下列说法正确的是
A.同温同压下甲烷和氧气的密度之比为2∶1
B.1g甲烷和1g氧气的原子数之比为5∶1
C.等物质的量的甲烷和氧气的质量之比为2∶1
D.在标准状况下等质量的甲烷和氧气的体积之比为1∶2
13.在 、 、 的混合溶液中, 、 、 的物质的量浓度之比为1∶2∶4,现加入适量
的铁粉,充分反应后使溶液中三种离子的物质的量浓度之比变为9∶3∶1,则原溶液中的Fe与参与反应的铁
粉物质的量比为
A.3∶5 B.4∶5 C.6∶5 D.5∶4
14.N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.0.1molCl 与0.2molCH 光照充分反应生成HCl分子数为0.1N
2 4 A
B.1LpH=12的氨水中加入足量盐酸,生成NH +数为0.01N
4 A
C.100g 34%的HO 中加入MnO 充分反应转移电子数为2N
2 2 2 A
D.0.1mol乙醇与0.1mol乙酸在浓硫酸作用下充分反应生成乙酸乙酯分子数为0.1 N
A
15.配制一定物质的量浓度的NaCl溶液,下列操作会使溶液浓度偏高是
A.定容至液面最高处与刻度线相平 B.溶解NaCl时烧杯中有少量蒸馏水
C.转移时没有洗涤烧杯和玻璃棒 D.少量NaCl固体残留在称量纸上
二、非选择题(本题包括4小题,共55分)
16.(16分)回答下列问题
(1)0.5mol水中含有___________个水分子;9g水与___________g硫酸所含的分子数相等。
(2)100mL0.2mol/LNa SO 溶液中Na+的物质的量浓度为___________。
2 4
(3)标准状况下,和2molNH 含有相同氢原子数的CH 的体积为___________。
3 4
(4)从1LAl (SO ) 溶液中取出100mL,向其中加入200mL0.9mol·L-1的BaCl 溶液恰好使SO 完全沉淀,则
2 4 3 2原溶液中Al3+的物质的量浓度为___________。
(5)12.4gNa R含0.4molNa+,则NaR的摩尔质量为___________,R的相对原子质量为___________。
2 2
(6)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造
空气”的质量是4.8g,其中氧气和氦气的分子数之比是___________。
17.(15分)现有16.0 g CO和CO 的混合气体,在标准状况下其体积为8.96 L。请回答下列问题:
2
(1)该混合气体的平均摩尔质量为___________。
(2)混合气体中碳原子的个数为___________(用N 表示阿伏加德罗常数的值)。
A
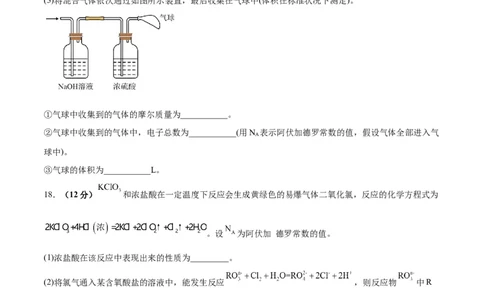
(3)将混合气体依次通过如图所示装置,最后收集在气球中(体积在标准状况下测定)。
①气球中收集到的气体的摩尔质量为___________。
②气球中收集到的气体中,电子总数为___________(用N 表示阿伏加德罗常数的值,假设气体全部进入气
A
球中)。
③气球的体积为___________L。
18.(12分) 和浓盐酸在一定温度下反应会生成黄绿色的易爆气体二氧化氯,反应的化学方程式为
。设 为阿伏加 德罗常数的值。
(1)浓盐酸在该反应中表现出来的性质为_________。
(2)将氯气通入某含氧酸盐的溶液中,能发生反应 ,则反应物 中R
元素的化合价是_________;当反应消耗0.25mol氯气时,转移电了的数目为_______。
(3)根据世界环保联盟的要求, 将逐渐取代 成为自来水的消毒剂。工业上常用 溶液和
溶液混合并加入 酸化制得 ,且产物中有 ,则在该反应中, 和 的
物质的量之比为______。
18.(12分)实验室欲用 固体配制 的 溶液 。(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ③冷却 ②摇动
正确的操作顺序为______。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、______。
(2)某同学欲称量 的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯
的实际质量为______ ,要完成本实验该同学应称出______ 。
(3)使用容量瓶前必须进行的一步操作是______。
(4)在配制过程中,其他操作都是正确的,下列操作会使浓度偏高的是______(填序号)。
A 所用 已经潮解
B 向容量瓶中加水未到刻度线
C 有少量 溶液残留在烧杯里
D 用带游码的托盘天平称 ( 以下用游码)时误用了“左码右物”方法