文档内容
专题突破卷 01 化学物质及其变化
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一项是符合题目要求的)
1.2023年诺贝尔化学奖授予发现和合成量子点材料的三位科学家。将富含维生素、蛋白质、糖类的有机
物经高温碳化后可以获得直径为2~10nm碳量子点材料。下列说法正确的是
A.维生素、蛋白质、糖类组成元素相同
B.碳量子点材料属于有机高分子材料
C.高温碳化有机物属于物理变化
D.将碳量子点材料分散到溶液中所形成的分散系为胶体
【答案】D
【解析】A.维生素、糖类组成元素相同,都含碳、氢、氧元素,蛋白质除含碳、氢、氧元素以外,还含
有氮元素,故A错误;
B.碳量子点材料是碳单数,不属于有机高分子材料,故B错误;
C.高温碳化有机物是将有机物变为碳,属于化学变化,故C错误;
D.碳量子点材料直径为2~10nm,将碳量子点材料分散到溶液中所形成的分散系为胶体,故D正确。
综上所述,答案为D。
2.下列各组物质的分类都正确的是(括号里的是类别)
A.NaClO(碱式盐)、 (碱)、 (离子化合物)、玻璃钢(金属材料)
B.液氨(氢化物)、 (铵盐)、 (含氧酸)、NaOH(强碱)
C.HCl(共价化合物)、 (羧酸)、 (碱性氧化物)、 (卤代烃)
D. (酸性氧化物)、 (有机物)、CO(有机物)、 (酯)
【答案】B
【分析】碱是电离出的阴离子都是氢氧根离子的化合物;盐是由金属阳离子或铵根离子和酸根离子构成的
化合物;氧化物是含有两种元素一种为氧元素的化合物;能和碱反应生成盐和水的氧化物属于酸性氧化物;
能和酸反应生成盐和水的氧化物属于碱性氧化物;
【解析】A.NaClO为正盐;乙醇不是碱,是有机物;硫酸为共价化合物;玻璃钢属于复合材料,A错误;B.液氨是一种物质组成属于纯净物、由氢和氮元素组成、属于氢化物;NH Cl含有铵根离子,属于铵盐;
4
HNO 是含氧酸;NaOH属于强碱,B正确;
3
C. 和水生成氢氧化钠和氧气,不是碱性氧化物,为过氧化物,C错误;
D.二氧化氮和水生成硝酸和NO,不是酸性氧化物;CO性质与无机物相似,属于无机物,D错误;
故选B。
3.下列说法正确的是
A.在同一化合物中,金属元素显正价,则非金属元素一定显负价
B.化学变化常伴随着发光,则有发光现象的变化一定是化学变化
C.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物
D.催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂
【答案】C
【解析】A.在同一化合物中,金属元素显正价,但是非金属元素不一定显负价,如碳酸钙中钙元素显+2
价,碳元素显+4价,A不符合题意;
B.化学变化常伴随着发光,但是有发光现象的变化不一定是化学变化,如电灯通电时发光放热,但是属
于物理变化,B不符合题意;
C.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物,C符合题意;
D.催化剂的质量在反应前后不变,但是在反应前后质量不变的物质不一定是该反应的催化剂,也可能是
不参与反应的杂质,D不符合题意;
故选C。
4.化学与生活、生产、科技密切相关。下列说法正确的是
A.葡萄糖酸 内酯常用作制豆腐的凝固剂
B.量子通信材料螺旋碳纳米管、石墨烯等纳米材料属于胶体
C.石油经干馏后可以获得汽油、煤油、柴油等轻质油
D.“嫦娥五号”使用的太阳能电池阵可将化学能转变成电能
【答案】A
【解析】A.葡萄糖酸 内酯白色结晶性粉末,在使用中常作为稳定凝固剂,A正确;
B.胶体是混合物,螺旋碳纳米管、石墨烯等纳米材料是纯净物,不属于胶体,B错误;
C.石油分馏可得石油气、汽油、煤油、柴油等,C错误;
D.太阳能电池是将光能转化为电能,D错误;
故选A。5.化学与生产、生活及社会发展密切相关。列说法不正确的是
A.德尔塔病毒能在空气中以气溶胶的形式传播,气溶胶属于胶体
B.用己烷萃取玉米胚芽中的油脂时发生了化学反应
C.橱窗所用有机玻璃为高分子化合物
D.家庭装修用水性涂料代替油性涂料有利于健康
【答案】B
【解析】A.胶体是分散质粒子大小在1nm到100nm的分散系,气溶胶属于胶体,A正确;
B.用己烷萃取玉米胚芽中的油脂是利用溶解度不同进行物质分离提纯的物理方法,B错误;
C.有机玻璃一般是聚甲基丙烯酸甲酯,为高分子化合物,C正确;
D.油性涂料由于不溶于水易溶于有机溶剂中,故油性涂料中含有有毒有害的有机溶剂如丙酮、苯等,故
家庭装修用水性涂料代替油性涂料有利于健康,D正确;
故选B。
6.科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是
A.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
B.发现了月壤中的“嫦娥石[(Ca Y)Fe(PO)]”:其成分属于无机盐
8 4 7
C.利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
【答案】C
【解析】A.电池是一种可以将其他能量转化为电能的装置,钙钛矿太阳能电池可以将太阳能转化为电能,
A正确;
B.嫦娥石因其含有Y、Ca、Fe等元素,属于无机化合物,又因含有磷酸根,是无机盐,B正确;
C.常见的脂肪酸有:硬脂酸(C H COOH)、油酸(C H COOH),二者相对分子质量虽大,但没有达到高
17 35 17 33
分子化合物的范畴,不属于有机高分子,C错误;
D.海水中含有大量的无机盐成分,可以将大多数物质腐蚀,而聚四氟乙烯塑料被称为塑料王,耐酸、耐
碱,不会被海水腐蚀,D正确;
故选:C。
7.下列物品为江苏各地特产,其主要化学成分不能与其他三种归为一类的是
A.东海水晶 B.宜兴紫砂壶 C.苏州丝绸 D.扬中玉雕
【答案】C
【分析】东海水晶、宜兴紫砂壶、扬中玉雕均属于硅酸盐制品,主要成分均为无机非金属材料,而苏州丝
绸属于天然有机高分子材料,主要成分为蛋白质。【解析】A.由分析可知,东海水晶属于无机非金属材料,A不符合题意;
B.由分析可知,宜兴紫砂壶属于无机非金属材料,B不符合题意;
C.由分析可知,苏州丝绸属于有机高分子材料,C符合题意;
D.由分析可知,扬中玉雕属于无机非金属材料,D不符合题意;
故答案为C。
8.甲醇是具有巨大应用潜力的绿色燃料。利用CO 催化氢化合成甲醇。下列说法正确的是
2
A.甲醇分子燃烧不排放CO B.合成反应类型为化合反应
2
C.甲醇比氢气更易储存和运输 D.常温常压下甲醇为气体
【答案】C
【解析】A.甲醇燃烧生成二氧化碳和水,故A错误;
B.合成反应反应式为CO+3H =CH OH+H O,生成两种物质,不是化合反应,故B错误;
2 2 3 2
C.甲醇为液体燃料,比氢气更易储存和运输,故C正确;
D.常温常压下,甲醇为液体,故D错误;
选C。
9.氮及其化合物的转化具有重要应用。下列说法不正确的是
A.常温下可以用铁制容器来盛装浓硝酸
B.工业制硝酸过程中的物质转化:
C.氮气、铵盐、亚硝酸盐、硝酸盐之间的转化构成了自然界“氮循环”的一部分
D.实验室用浓氨水、生石灰制备少量氨气:
【答案】B
【解析】A.常温下可以用铁制容器来盛装浓硝酸,会发生钝化,故A正确;
B.一氧化氮和水不反应,故B错误;
C.氮气、铵盐、亚硝酸盐、硝酸盐之间的转化构成了自然界“氮循环”的一部分,故C正确;
D.生石灰溶于水得到氢氧化钙、同时大量放热促使一水合氨分解,则反应实验室用浓氨水、生石灰制备
少量氨气: ,故D正确;
故选:B。
10.“臭碱”(主要成分是NaS)、“纯碱”是两种化工产品,下列说法错误的是
2
A.臭碱和纯碱都属于碱类 B.NaS在空气中易被氧化
2
C.可利用NaS溶液与稀硫酸反应制备HS D.臭碱可使氯水褪色
2 2【答案】A
【解析】A.臭碱的主要成分是NaS,纯碱的主要成分是NaCO,都属于盐类,A错误;
2 2 3
B.NaS中硫元素为-2价,处于最低价,在空气中易被氧化为硫单质,B正确;
2
C.可利用稀硫酸的强酸性与NaS溶液制备HS,C正确;
2 2
D.臭碱NaS中硫元素能被氯气氧化,D正确。
2
故选A。
11.在给定条件下,下列选项所示的物质间转化能实现的是
A.
B.
C.
D.
【答案】A
【解析】A.氯化镁溶液可以与石灰乳反应得到氢氧化镁沉淀,煅烧氢氧化镁可以分解生成氧化镁,故A
符合题意;
B.氯气与氢氧化钙反应生成次氯酸钙,次氯酸钙与过量SO 发生氧化还原反应,生成硫酸根和氯离子,
2
故B不符合题意;
C.铁与稀盐酸反应只能生成氯化亚铁,且氯化铁溶液蒸发过程中彻底水解得不到氯化铁固体,故C不符
合题意;
D.硫酸铜与氢氧化钠反应生成新制氢氧化铜,但是蔗糖中不含醛基是非还原糖,无法用新制氢氧化铜检
验,故D不符合题意;
综上所述答案为A。
12.在指定条件下,下列选项所示的物质间转化能实现的是
A. B.
C. D.
【答案】B
【解析】A. 硫在氧气中燃烧只能生成二氧化硫,故A错误;
B. 铁与氯气反应生成三氯化铁,故B正确;C. 二氧化硫与过量的氢氧化钠反应生成亚硫酸钠,故C错误;
D. 氯化铝与氨水反应只能生成氢氧化铝,故D错误;
故选B。
13.在给定条件下,下列选项所示的物质间转化能实现的是
A.
B.
C.
D.淀粉 葡萄糖
【答案】A
【解析】A.氨气催化氧化生成NO,NO与O 和HO反应生成硝酸可以实现,故A正确;
2 2
B.浓盐酸与MnO 要加热才能反应生成氯气,稀盐酸与MnO 不加热不反应,故B错误;
2 2
C.硫酸根离子与SO 不能生成S ,故C错误;
2
D.淀粉在酸性条件下加热水解生成葡萄糖,葡萄糖与银氨溶液反应需要在碱性条件下才能发生银镜反应,
故D错误;
答案选A。
14.化学与社会生活密切相关。下列有关说法错误的是
A.菏泽特产牡丹籽油属于高分子化合物
B.燃煤中加入CaO可以减少酸雨的形成
C.亚硝酸钠可用于一些肉制品的加工,发挥防腐作用
D.雾中汽车大灯前明亮的光路与肢体的丁达尔效应有关
【答案】A
【解析】A.牡丹籽油是一种优良的植物油脂,油脂的相对分子质量较小,不属于高分子化合物,故A错
误;
B.二氧化硫的排放是导致酸雨形成的重要因素,燃煤燃烧生成二氧化硫气体,但二氧化硫能与氧化钙、
氧气反应生成硫酸钙,所以燃煤中加入CaO 可以减少酸雨的形成,故B正确;
C.亚硝酸钠能防腐,能使肉类呈现新鲜的红色,生产加工腊肉、香肠等肉制品时添加适量的亚硝酸钠,
用作防腐剂,故C正确;
D.雾是胶体,雾中汽车大灯前明亮的光路是雾的丁达尔效应,故D正确;故选A。
二、非选择题(本题包括4小题,共58分)
15.(14分)牙膏是日常生活中常用的清洁用品,由粉状摩擦剂、湿润剂、表面活性剂、黏合剂、香料、
甜味剂及其他特殊成分构成。下表列出了三种牙膏中的摩擦剂。
牙膏 X牙膏 Y牙膏 Z牙膏
摩擦剂 氢氧化铝 碳酸钙 二氧化硅
_________
摩擦剂物质类别(指酸、碱、盐、氧化物) 盐 __________
_
(1)将上述摩擦剂所属物质的正确类别填入空格 、 。
(2)你推测上述三种摩擦剂都 (填“溶于”或者“不溶于”)水,理由是 。
(3)已知二氧化硅的化学式为SiO,该物质能与NaOH溶液反应,反应方程式为2NaOH+SiO=Na SiO+
2 2 2 3
HO,NaSiO 属于 (填“酸”“碱”或“盐”)类。非金属氧化物SO 也具有类似的性质,请你
2 2 3 2
写出SO 与NaOH溶液反应的化学方程式 。
2
【答案】(1) 碱 氧化物
(2) 不溶于 因为摩擦剂是通过牙刷的运动摩擦以清洁牙齿,所以均不溶于水
(3) 盐 2NaOH+SO =Na SO +HO
2 2 3 2
【解析】(1)氢氧化铝属于碱,二氧化硅为氧化物。
(2)上述三种摩擦剂都不溶于水,因为摩擦剂是通过牙刷的运动摩擦以清洁牙齿,所以均不溶于水。
(3)酸性氧化物和碱反应生成盐和水,NaSiO 属于盐,SO 也是酸性氧化物,与NaOH溶液反应生成亚
2 3 2
硫酸钠和水,反应的化学方程式为2NaOH+SO =Na SO +HO。
2 2 3 2
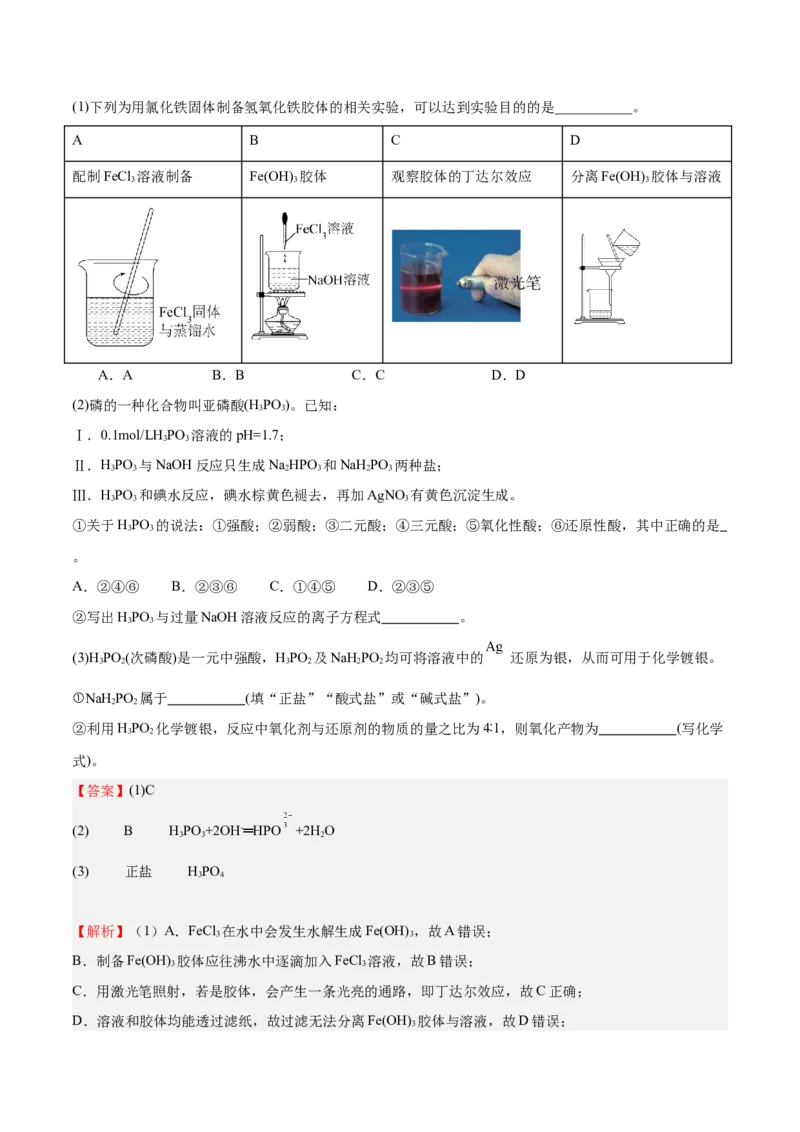
16.(14分)回答下列问题:(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
A B C D
配制FeCl 溶液制备 Fe(OH) 胶体 观察胶体的丁达尔效应 分离Fe(OH) 胶体与溶液
3 3 3
A.A B.B C.C D.D
(2)磷的一种化合物叫亚磷酸(H PO )。已知:
3 3
Ⅰ.0.1mol/LH PO 溶液的pH=1.7;
3 3
Ⅱ.HPO 与NaOH反应只生成NaHPO 和NaH PO 两种盐;
3 3 2 3 2 3
Ⅲ.HPO 和碘水反应,碘水棕黄色褪去,再加AgNO 有黄色沉淀生成。
3 3 3
①关于HPO 的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是
3 3
。
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出HPO 与过量NaOH溶液反应的离子方程式 。
3 3
(3)H PO (次磷酸)是一元中强酸,HPO 及NaH PO 均可将溶液中的 还原为银,从而可用于化学镀银。
3 2 3 2 2 2
①NaHPO 属于 (填“正盐”“酸式盐”或“碱式盐”)。
2 2
②利用HPO 化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为 (写化学
3 2
式)。
【答案】(1)C
(2) B H PO +2OH-═HPO +2H O
3 3 2
(3) 正盐 HPO
3 4
【解析】(1)A.FeCl 在水中会发生水解生成Fe(OH) ,故A错误;
3 3
B.制备Fe(OH) 胶体应往沸水中逐滴加入FeCl 溶液,故B错误;
3 3
C.用激光笔照射,若是胶体,会产生一条光亮的通路,即丁达尔效应,故C正确;
D.溶液和胶体均能透过滤纸,故过滤无法分离Fe(OH) 胶体与溶液,故D错误;
3故答案为:C。
(2)①由0.1mol/L H PO 溶液的pH=1.7,说明亚磷酸部分电离,则亚磷酸是弱酸;由HPO 与NaOH反应
3 3 3 3
只生成NaHPO 和NaH PO 两种盐,则说明亚磷酸是二元酸;由HPO 和碘水反应,碘水棕黄色褪去,再
2 3 2 3 3 3
加AgNO 有黄色沉淀生成,说明该反应中亚磷酸失电子作还原剂,所以亚磷酸有还原性,②③⑥正确,故
3
选B;
②H PO 与过量NaOH溶液反应的离子方程式为:HPO +2OH-═HPO +2H O,故答案为:B;HPO +2OH-
3 3 3 3 2 3 3
═HPO +2H O。
2
(3)①HPO 是一元弱酸,则NaH PO 为正盐,故答案为:正盐;
3 2 2 2
②该反应中银离子是氧化剂、HPO 是还原剂,氧化剂与还原剂的物质的量之比为4:1,根据转移电子相
3 2
等知,1molH PO 失去4mol电子,所以P元素为+5价,则氧化产物是HPO ,故答案为:HPO 。
3 2 3 4 3 4
17.(15分)2023年新冠肺炎疫情正在离我们远去,但是病毒仍然在不断变异,民众的防疫意识绝对不能
松懈。
(1)研究表明新冠病毒可通过气溶胶传播,口罩可以有效防止飞沫的传播。气溶胶属于 (填“胶
体”或“溶液”);常利用 鉴别溶液和胶体。
(2)常用的消毒剂有过氧化物、医用酒精以及含氯消毒剂等。常温下,NaO、乙醇、Cl、NaC1O溶液,其
2 2 2
中能导电的是 ,属于电解质的是 。
(3)目前使用的含氯消毒剂中被世界环保组织认定为安全高效的杀菌消毒剂是C1O。ClO 是一种黄绿色,
2 2
有刺激性气味的气体,熔点:-59℃,沸点:11.0℃。浓度>10%遇热、光照都会引起爆炸。遇到有机物也会
爆炸。
①欧洲一些国家用NaClO 氧化浓盐酸来制取ClO ,同时有Cl 生成,且Cl 的体积为ClO 的 。写出该反
3 2 2 2 2
应的化学反应方程式 。
②我国广泛采用将经干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO)的柱内得ClO 。写出化学反应方
2 2
程式 。和欧洲的方法相比,我国这一方法的主要优点是 。
③ClO 为高效低毒的消毒剂,其消毒的效率是Cl 的 倍。(消毒效率就是得到相同的电子数时消
2 2
毒剂的质量的大小关系)
【答案】(1) 胶体 丁达尔效应(2) NaClO溶液 NaO
2 2
(3) 生成的C1O
2
中不含Cl 杂质 2.63
2
【解析】(1)气溶胶属于胶体;常利用丁达尔效应鉴别溶液和胶体;
(2)结合物质自身性质可知能导电的有:NaClO溶液;电解质是指在水溶液或熔融状态下能导电的化合
物,则属于电解质的是:NaO;
2 2
(3)①用NaClO 氧化浓盐酸来制取ClO ,同时有Cl 生成,且Cl 的体积为ClO 的 ,根据得失电子守恒
3 2 2 2 2
及质量守恒定律,化学反应方程式: ;
②将经干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO)的柱内得ClO ,根据得失电子守恒及质量守恒
2 2
定律,化学反应方程式: ;该方法优点:生成的C1O 中不含Cl 杂质;
2 2
③ClO 和Cl 作消毒剂,反应后均被还原为Cl-,得到相同电子数时,物质的量之比:
2 2
,则质量分别为: , ,则
ClO 为高效低毒的消毒剂,其消毒的效率是Cl 的2.63倍;
2 2
18.(15分)I.“皮鞋很忙的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行
为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些
制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬会对人体造成伤害。明胶
是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是 价。 是一种酸根离子,则
属于 (填“酸”、“碱”、“盐”或“氧化物”)
(2)明胶的水溶液和 溶液共同具备的性质是 (填序号)
A.都不稳定,密封放置会产生沉淀
B.二者均有丁达尔效应
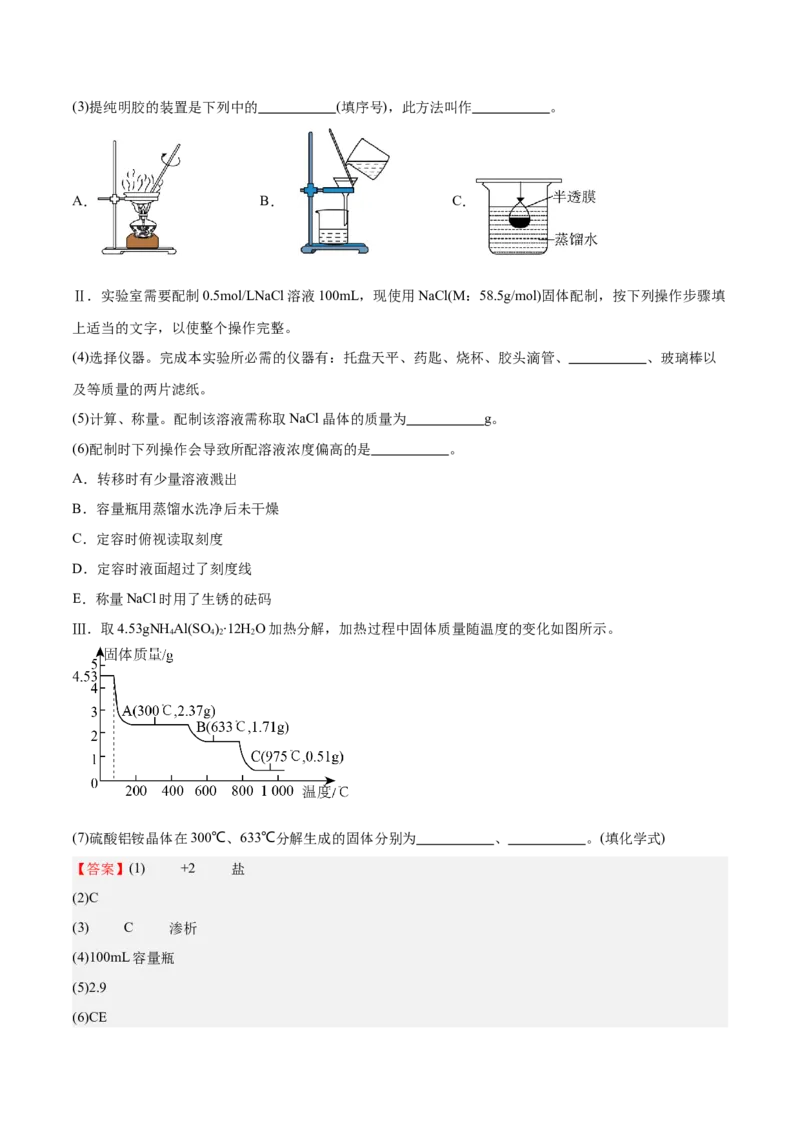
C.分散质粒子可通过滤纸(3)提纯明胶的装置是下列中的 (填序号),此方法叫作 。
A. B. C.
Ⅱ.实验室需要配制0.5mol/LNaCl溶液100mL,现使用NaCl(M:58.5g/mol)固体配制,按下列操作步骤填
上适当的文字,以使整个操作完整。
(4)选择仪器。完成本实验所必需的仪器有:托盘天平、药匙、烧杯、胶头滴管、 、玻璃棒以
及等质量的两片滤纸。
(5)计算、称量。配制该溶液需称取NaCl晶体的质量为 g。
(6)配制时下列操作会导致所配溶液浓度偏高的是 。
A.转移时有少量溶液溅出
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线
E.称量NaCl时用了生锈的砝码
Ⅲ.取4.53gNHAl(SO )∙12H O加热分解,加热过程中固体质量随温度的变化如图所示。
4 4 2 2
(7)硫酸铝铵晶体在300℃、633℃分解生成的固体分别为 、 。(填化学式)
【答案】(1) +2 盐
(2)C
(3) C 渗析
(4)100mL容量瓶
(5)2.9
(6)CE(7) NH Al(SO ) Al (SO )
4 4 2 2 4 3
【解析】(1) 中,氧元素的化合价是−2价,铬元素的化合价是+3价,根据化合物价态总和为0
得到铁元素化合价是+2价; 是由亚铁离子和 组成的盐,故答案为:+2;盐。
(2)A.胶体较稳定,溶液是稳定的,故A不符合题意;B.溶液无丁达尔效应,胶体有丁达尔效应,故
B不符合题意;C.胶粒和溶液都可透过滤纸,故C符合题意;综上所述,答案为C。
(3)提纯明胶是利用渗析法将胶体和溶液中水分子等小分子或离子能透过半透膜分离,装置为C;故答案
为:C;渗析。
(4)配制0.5mol/LNaCl溶液100mL,完成本实验所必需的仪器有:托盘天平、药匙、烧杯、胶头滴管、
100mL容量瓶、玻璃棒以及等质量的两片滤纸;故答案为:100mL容量瓶。
(5)配制该溶液需称取NaCl晶体的质量为0.5mol/L×0.1L×58.5g/mol=2.9g;故答案为:2.9。
(6)A.转移时有少量溶液溅出,溶质物质的量减少,导致所配溶液浓度偏低,故A不符合题意;B.容
量瓶未干燥对结果无影响,故B不符合题意;C.定容俯视刻度线,溶液体积偏少,所配溶液浓度偏高,
故C符合题意;D.称量时氯化钠和砝码放反使实际称量的氯化钠质量减小,所配溶液浓度偏低,故D不
符合题意;E.砝码生锈使实际称量的氯化钠质量增大,导致溶液浓度偏高,故E符合题意;综上所述,
答案为:CE。
(7)4.53gNHAl(SO )∙12H O物质的量为0.01mol,在A点质量为2.37g,质量减少2.16g,减去的质量刚
4 4 2 2
好等于水的质量,因此A点固体物质为NH Al(SO ),在633℃即B点质量为1.71g,从A点到B点氮元素
4 4 2
可能流失,根据铝守恒得到Al (SO ) 物质的量为0.005mol,其质量刚好为1.71g;故答案为:
2 4 3
NH Al(SO );Al (SO )。
4 4 2 2 4 3