文档内容
专题突破卷 09 水溶液中的离子反应与平衡
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列有关电解质溶液的说法正确的是
A.加水稀释,NaS溶液中离子浓度均减小
2
B.0.1 mol/L NaOH溶液中滴加等体积等浓度醋酸溶液,溶液的导电性增强
C.pH相同的①CHCOONa②NaHCO ③NaClO三种溶液的c(Na+):①>②>③
3 3
D.向0.1 mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH﹣)/c(NH·H O)增大
3 2
2.MOH强碱溶液和等体积、等浓度的HA弱酸溶液混合后,溶液中有关离子的浓度应满足的关系是
A.c(M+)>c(OH-)>c(A-)>c(H+) B.c(M+)>c(A-)>c(H+)>c(OH-)
C.c(M+)>c(A-)>c(OH-)>c(H+) D.c(M+)>c(H+)>c(A-)>c(OH-)
3.根据表中信息,判断0.10mol/L的下列各物质的溶液pH最大的是
酸 电离常数(常温下)
,
,
A. B.
C. D.
4.25℃时, 和 的沉淀溶解平衡曲线如图( 代表 或 )所示。下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.a点可表示 的饱和溶液
B.c点可表示 的过饱和溶液,达新平衡时可到达b点
C.d点时溶液中存在 (忽略单位)
D.用 溶液浸泡足量 ,会有部分 转化为
5.已知在100 ℃时水的离子积K =1×10-12,下列溶液的温度均为100 ℃。其中说法正确的是
w
A.0.005 mol·L-1的HSO 溶液,pH=2
2 4
B.0.001 mol·L-1的NaOH溶液,pH=11
C.0.005 mol·L-1的HSO 溶液与0.01 mol·L-1的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性
2 4
D.完全中和pH=3的HSO 溶液50 mL,需要pH=9的NaOH溶液100 mL
2 4
6.一定温度下, 体系中, 和 的关系如图所示。下列说法不正
确的是
A.AgCl溶于水形成的饱和溶液中:
B.b点溶液中加入少量 固体,会析出白色沉淀
C.d点溶液中加入少量AgCl固体, 和 均增大
D.a、b、c三点对应的AgCl的 不相等
7.在不同温度下,水达到电离平衡时 与 的关系如图所示。 时,将 的 溶
液和 的 溶液等体积混合后(混合后溶液的体积变化忽略不计),该溶液的 是
资料收集整理【淘宝店铺:向阳百分百】A.1.7 B.2 C.10 D.10.3
8.已知CaCO 的K =2.8×10-9,现将浓度为2×10-4mol•L-1的NaCO 溶液与CaCl 溶液等体积混合,若要产
3 sp 2 3 2
生沉淀,则所用CaCl 溶液的浓度至少应为
2
A.2.8×10-2mol•L-1 B.1.4×10-5mol•L-1 C.2.8×10-5mol•L-1 D.5.6×10-5mol•L-1
9.关于常温下pH为2的盐酸,下列叙述正确的是
A.将10mL,该溶液稀释至100mL后,
B.向该溶液中加入等体积pH为12的氨水恰好完全中和
C.该溶液中盐酸电离出的c(H+)与水电离出的c(H+)之比为
D.该溶液中由水电离出的 (H+)
10.下列有关中和滴定的说法正确的是
A.用25 mL滴定管进行中和滴定时,用去标准液的体积为21.7 mL
B.用标准KOH溶液滴定未知浓度的盐酸,配制标准溶液的KOH固体中有NaOH杂质,则结果偏高
C.用c mol/L酸性高锰酸钾溶液滴定V mL未知浓度的HC O 溶液至滴定终点,用去酸性高锰酸钾溶液
1 2 2 2 4
体积为V mL,则HC O 溶液的浓度为 mol/L
1 2 2 4
D.用未知浓度的盐酸滴定已知浓度的NaOH溶液时,若读数时,滴定前仰视,滴定到终点后俯视,会导
致测定结果偏高
11.室温下,向10mL 0.10mol•L-1的HX溶液中逐滴滴入0.20mol•L-1的YOH溶液,混合溶液的pH变化情
况如图所示(忽略溶液温度和体积变化)。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.HX是弱酸
B.M点对应的溶液中,c(Y+)>c(X-)
C.N点对应的溶液中,粒子浓度关系存在:c(Y+)+c(YOH)=2c(X-)
D.常温下,pH=5的YX溶液中,由水电离的c(H+)=1.0×10-9mol•L-1
12.有25mL0.1mol•L-1的三种溶液①NaCO 溶液;②CHCOONa溶液;③NaOH溶液,下列说法正确的
2 3 3
是
电离平衡常数 K K
a1 a2
HCO 4.5×10-7 4.7×10-11
2 3
CHCOOH 1.75×10-5 ——
3
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25mL0.1mol•L-1盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>②>①
13.室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。
下列说法正确的是
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
资料收集整理【淘宝店铺:向阳百分百】B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
14.常温下浓度均为0.1mol/L的四种盐溶液,其pH如表所示,下列说法正确的是
序号 ① ② ③ ④
溶液 CHCOONa NaHCO NaCO NaClO
3 3 2 3
pH 8.8 9.7 11.6 10.3
A.等浓度的CHCOOH和HClO溶液,pH小的是HClO
3
B.NaCO 和NaHCO 溶液中粒子种类不同
2 3 3
C.四种溶液中水的电离程度:①>②>④>③
D.NaHCO 溶液中:c(Na+)=c(CO )+c(HCO )+c(H CO)
3 2 3
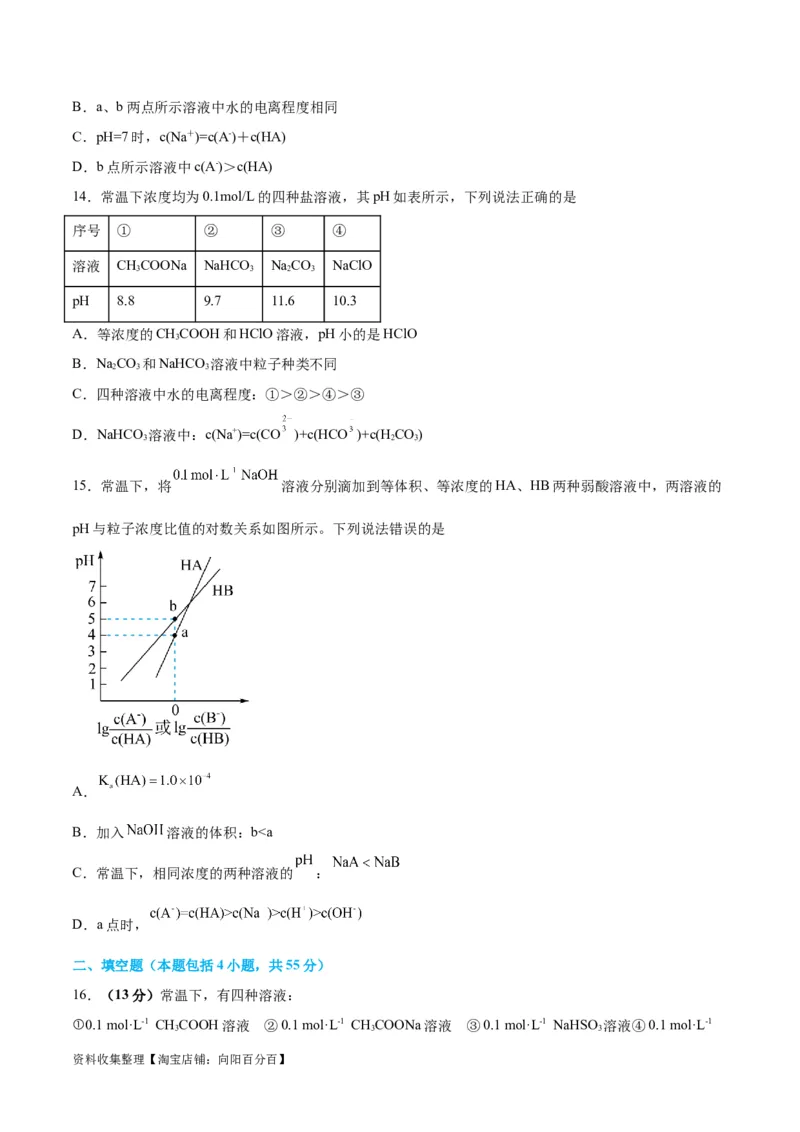
15.常温下,将 溶液分别滴加到等体积、等浓度的HA、HB两种弱酸溶液中,两溶液的
pH与粒子浓度比值的对数关系如图所示。下列说法错误的是
A.
B.加入 溶液的体积:b”“<”或“=”)7,溶液中离子的电荷守恒关系式是 。
(2)溶液②呈 (填“酸”“碱”或“中”)性。其原因是 (用离子方程式说明)。
(3)下列有关①和②两种溶液的说法正确的是 (填字母)。
a. 两种溶液中c(CHCOO-) 都小于0.1 mol·L-1
3
b. 两种溶液中c(CHCOO-) 都等于0.1 mol·L-1
3
c. CHCOOH溶液中c(CHCOO-) 小于CHCOONa溶液中c(CHCOO-)
3 3 3 3
(4)NaHCO 溶液的pH>7,NaHSO 溶液的pH<7,则,NaHCO 溶液中c(HCO) (填“>”“<”或“=”,
3 3 3 2 3
下同)c( ),NaHSO 溶液中c(HSO ) c( )
3 2 3
17.(14分)NH Al(SO ) 常作食品加工中的食品添加剂,用于焙烤食品;NH HSO 在分析试剂、医药、
4 4 2 4 4
电子工业中用途广泛。请回答下列问题:
(1)NH Al(SO ) 可作净水剂,其原理是 (用离子方程式说明)。
4 4 2
(2)相同条件下,0.1mol∙L-1NH Al(SO ) 溶液中的c( ) (填“等于”“大于”或“小
4 4 2
于”)0.1mol∙L-1NH HSO 溶液中的c( )。
4 4
(3)几种均为0.1mol∙L-1的电解质溶液的pH随温度变化的曲线如图所示。
①其中符合0.1mol∙L-1NH Al(SO ) 溶液的pH随温度变化的曲线是 (填罗马数字),导致NH Al(SO )
4 4 2 4 4 2
溶液的pH随温度变化的原因是 。
②20℃时,0.1mol∙L-1NH Al(SO ) 溶液中2c c 3cAl3= molL1。
4 4 2
(4)室温时,向100mL0.1mol∙L-1NH HSO 溶液中滴加0.1mol∙L-1NaOH溶液,溶液pH与加入NaOH溶液体积
4 4
的关系曲线如图乙所示。
资料收集整理【淘宝店铺:向阳百分百】试分析图中a、b、c、d四个点,水的电离程度最大的是 点;在b点,溶液中各离子浓度由大到小
的排列顺序是 。
18.(14分)I.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过 。处理含
镉废水可采用化学沉淀法。
(1)写出磷酸镉[ ]沉淀溶解平衡常数的表达式: 。
(2)一定温度下, 的 , 的 ,该温度下 [填“ ”或
“ ”]的饱和溶液中 浓度较大。
(3)向某含镉废水中加入 ,当 浓度达到 时,废水中 的浓度为 [已知:
],此时 (填“符合”或“不符合”)《生活饮用水卫生标准》。
II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时, ;酸碱指示剂百里酚蓝变色的pH范围如下:
pH 8.0~9.6
颜
黄色 绿色 蓝色
色
25℃时,向 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为 。
(5)常温下,向50mL 的 溶液中加入50mL 的盐酸,生成沉淀。已知该温度
下, ,忽略溶液体积的变化。
资料收集整理【淘宝店铺:向阳百分百】①反应后,溶液中 。
②反应后,溶液的 。
③如果向反应后的溶液中继续加入50mL 的盐酸, (填“有”或“无”)白色沉淀生成。
19.(14分)按要求回答下列问题
(1)一定温度下,现有a.盐酸,b.硫酸,c.醋酸三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序
是 (用a、b、c表示)
②当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是
(用a、b、c表示)
③当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H(相同状况),
2
则开始时反应速率的大小关系为 (用a、b、c表示)
(2)现用中和滴定法测定某烧碱溶液的浓度,有关数据记录如表:
所消耗盐酸标准液的体积
滴定序号 待测液体积
滴定前 滴定后 消耗的体积
1
2
3
①用 式滴定管盛装0.2500mol/L盐酸标准液。如图表示第二次滴定前后50mL滴定管中液面的位置。
该次滴定所用标准盐酸体积为 mL。
②现实验室中有石蕊和酚酞两种指示剂,该实验应选用 作指示剂。
资料收集整理【淘宝店铺:向阳百分百】③根据所给数据,该烧碱样品的物质的量浓度为 。
④若操作过程中滴加盐酸速度过快,未充分振荡,刚看到溶液变色,就立刻停止滴定,则会造成测定结果
(填“偏低”“偏高”或“无影响”)。
资料收集整理【淘宝店铺:向阳百分百】