文档内容
专题讲座(四)反应速率、平衡图像题解题策略
【化学学科素养】
化学反应速率和化学平衡图像分析类试题是高考的热点题型,该类试题经常涉及的图像类型有含量—
时间—温度(压强)图像、恒温、恒压曲线等,图像中蕴含着丰富的信息,具有简明、直观、形象的特点,
命题形式灵活,难度不大,解题的关键是根据反应特点,明确反应条件,认真分析图像,充分挖掘蕴含的
信息,紧扣化学原理,找准切入点解决问题。图像作为一种思维方法在解题过程中也有着重要作用,可以
将一些较为抽象的知识,转化为图像,然后进行解决。注意掌握从图像中获取有效信息,解答与化学反应
速率和化学平衡有关的问题,如反应速率、反应转化率、产率,提高转化率的措施等;从图表或图像中获
取信息,计算转化率、平衡常数等。
【必备知识解读】
1.含量—时间—温度(压强)图像
C%指生成物的质量分数,B%指反应物的质量分数。
【方法技巧】 “先拐先平,数值大”,即曲线先出现拐点的首先达到平衡,反应速率快,以此判断
温度或压强的高低。再依据外界条件对平衡的影响分析判断反应的热效应及反应前后气体体积的变化。
2.转化率(或浓度)—压强—温度图像α表示某反应物的转化率,c表示某反应物的平衡浓度。
图①,若p>p>p,则正反应为气体体积减小的反应,ΔH 0 ;
1 2 3
图②,若T>T,则正反应为放热反应。
1 2
[技法解读] “定一议二”,即把自变量(温度、压强)之一设为恒量,讨论另外两个变量的关系。
3.特殊图像
(1)对于化学反应:mA(g)+nB(g)pC(g)+qD(g),如图所示:M点前,表示从反应开始,v >v ;M
正 逆
点恰好达到平衡;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,平
衡左移,故正反应ΔH<0。
(2)对于化学反应:mA(g)+nB(g)pC(g)+qD(g),L线上所有的点都是平衡点(如图)。L线的左上方
(E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以E点满足v >v ;同理,L线的右下
正 逆
方(F点)满足v <v 。
正 逆
【关键能力拓展】
有关化学平衡、化学反应速率的图表题一直是高考关注的热点,在审题时,一般采用“看特点,识图
表,想原理,巧整合”四步法解答。
第一步:看特点。即分析可逆反应方程式,观察物质的状态、气态物质分子数的变化(正反应是气体分
子数增大的反应,还是气体分子数减小的反应)、反应热(正反应是放热反应,还是吸热反应)等。
第二步:识图像。即识别图像类型,横坐标和纵坐标的含义、线和点(平台、折线、拐点等)的关系。
利
用规律“先拐先平,数值大”判断,即曲线先出现拐点,先达到平衡,其温度、压强越大。第三步:联想化学反应速率、化学平衡移动原理,特别是影响因素及使用前提条件等。
[来源:学,科,网Z,X,X,K]
第四步:图表与原理整合。逐项分析图表,重点看图表是否符合可逆反应的特点、化学反应速率和化
学平衡原理。
【核心题型例解】
高频考点一 速率变化图像
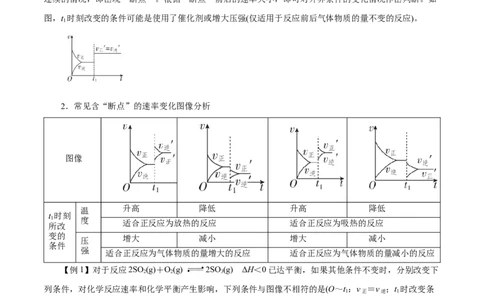
1.速率—时间图像“断点”分析
当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都可能使速率—时间图像的曲线出现不
连续的情况,即出现“断点”。根据“断点”前后的速率大小,即可对外界条件的变化情况作出判断。如
图,t 时刻改变的条件可能是使用了催化剂或增大压强(仅适用于反应前后气体物质的量不变的反应)。
1
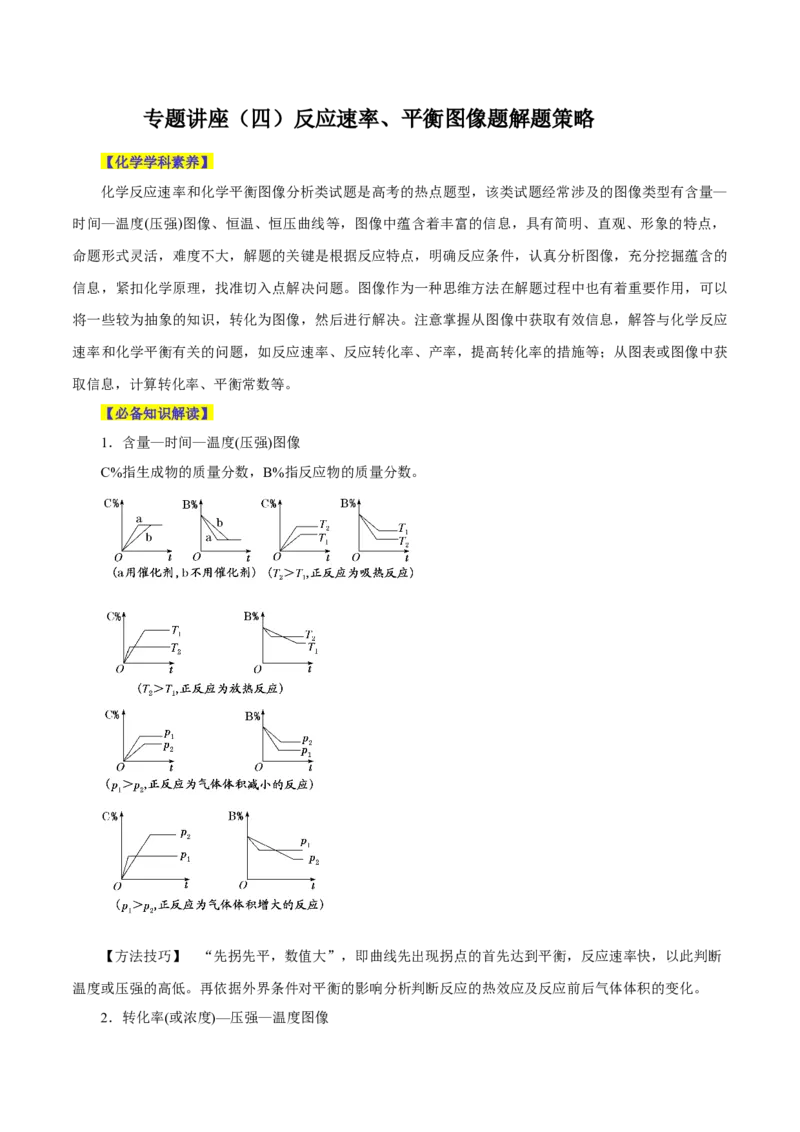
2.常见含“断点”的速率变化图像分析
图像
升高 降低 升高 降低
温
t 时刻
1 度
适合正反应为放热的反应 适合正反应为吸热的反应
所改
变的 增大 减小 增大 减小
压
条件
强
适合正反应为气体物质的量增大的反应 适合正反应为气体物质的量减小的反应
【例1】对于反应2SO (g)+O(g) 2SO (g) ΔH<0已达平衡,如果其他条件不变时,分别改变下
2 2 3
列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是(O~t:v =v ;t 时改变条
1 正 逆 1
件,t 时重新建立平衡)( )
2【答案】C
【解析】分析时要注意改变条件瞬间v 、v 的变化。增加O 的浓度,v 增大,v 瞬间不变,A正
正 逆 2 正 逆
确;增大压强,v 、v 都增大,v 增大的倍数大于v 增大的倍数,B正确;升高温度,v 、v 都瞬间增
正 逆 正 逆 正 逆
大,C错误;加入催化剂,v 、v 同时同倍数增大,D正确。
正 逆
高频考点二 物质的量(或浓度)—时间图像
将物质的量(或浓度)减少的物质作为反应物,将物质的量(或浓度)增加的物质作为产物;依据物质的转
化量之比一定等于方程式系数比来确定化学方程式。如:
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所
示。
则该反应的化学方程式为3X+Y 2Z,前2 min内v(X)=0.075 mol·L-1·min-1。
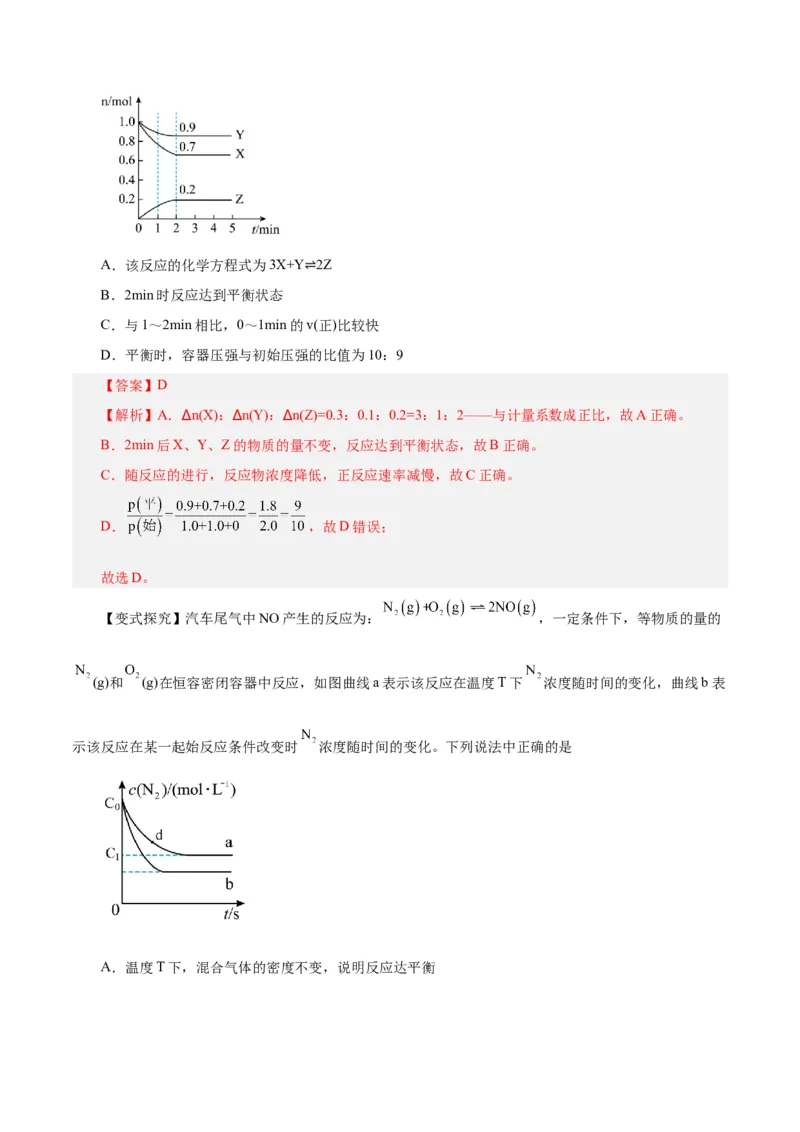
【例2】一定温度下,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如
图所示。下列说法错误的是A.该反应的化学方程式为3X+Y 2Z
B.2min时反应达到平衡状态 ⇌
C.与1~2min相比,0~1min的v(正)比较快
D.平衡时,容器压强与初始压强的比值为10:9
【答案】D
【解析】A.∆n(X):∆n(Y):∆n(Z)=0.3:0.1:0.2=3:1:2——与计量系数成正比,故A正确。
B.2min后X、Y、Z的物质的量不变,反应达到平衡状态,故B正确。
C.随反应的进行,反应物浓度降低,正反应速率减慢,故C正确。
D. ,故D错误;
故选D。
【变式探究】汽车尾气中NO产生的反应为: ,一定条件下,等物质的量的
(g)和 (g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下 浓度随时间的变化,曲线b表
示该反应在某一起始反应条件改变时 浓度随时间的变化。下列说法中正确的是
A.温度T下,混合气体的密度不变,说明反应达平衡B.温度T下,该反应的平衡常数
C.曲线a对应条件下,
D.曲线b对应的条件改变一定是升高温度
【答案】B
【解析】该反应是气体分子数不变得反应,反应前后气体的密度不变,不能作为平衡判断标志,故A
错误;温度T下,平衡时N、O、NO的浓度分别为:c、c、2(c -c ),该反应的平衡常数
2 2 1 1 0 1
,故B正确;曲线a对应条件下,d点没有平衡,正向进行, ,故
C错误;曲线b反应速率加快,平衡时N 浓度减小,若 改变的条件升高温度,故D错误;故选B。
2
高频考点三 转化率(或百分含量)—时间—温度(或压强)图像
已知不同温度或压强下,反应物的转化率α(或百分含量)与时间的关系曲线,推断温度的高低及反应的
热效应或压强的大小及气体物质间的化学计量数的关系。[以aA(g)+bB(g) cC(g)中反应物的转化率α
A
为例说明]
(1)“先拐先平,数值大”原则
分析反应由开始(起始物质相同时)达到平衡所用时间的长短可推知反应条件的变化。
①若为温度变化引起,温度较高时,反应达平衡所需时间短。如甲中T>T。
2 1
②若为压强变化引起,压强较大时,反应达平衡所需时间短。如乙中p>p。
1 2
③使用催化剂时,反应达平衡所需时间短。如图丙中a使用催化剂。
(2)正确掌握图像中反应规律的判断方法
①图甲中,T>T,升高温度,α 降低,平衡逆向移动,正反应为放热反应。
2 1 A
②图乙中,p>p,增大压强,α 升高,平衡正向移动,则正反应为气体分子数减小的反应。
1 2 A
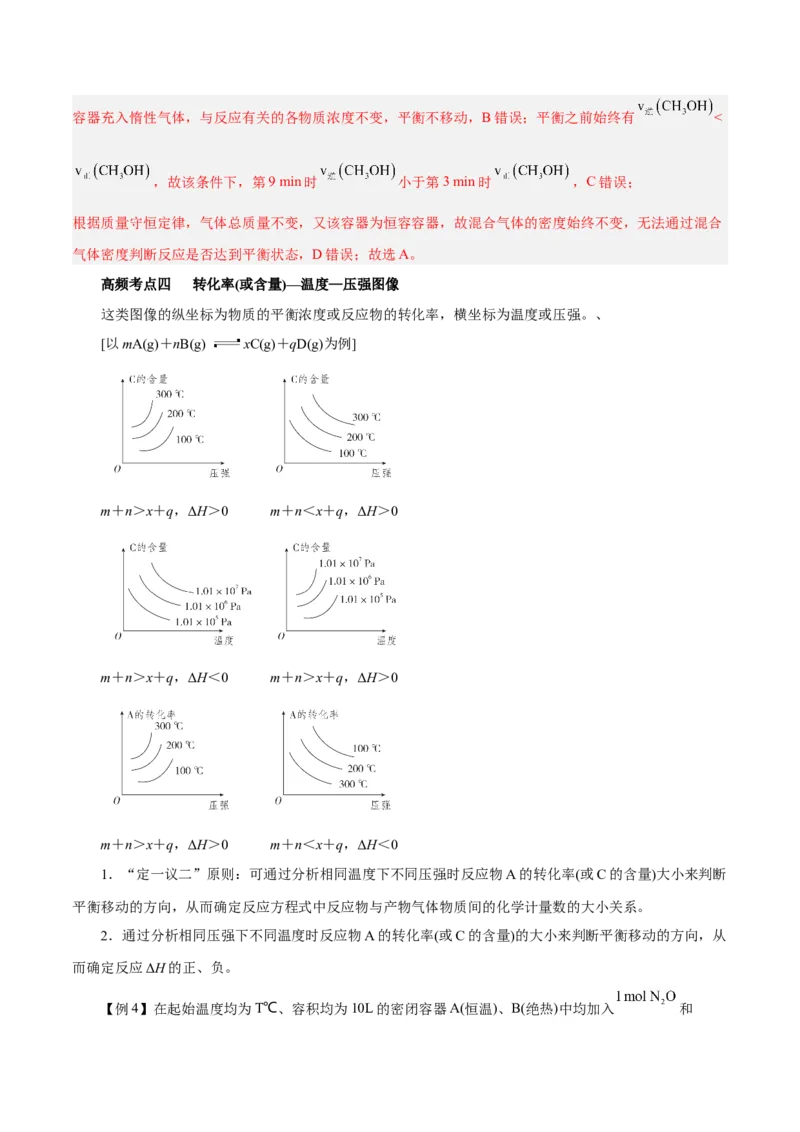
【例3】已知某可逆反应mA(g)+nB(g ) pC(g)在密闭容器中进行,如图表示在不同反应时间(t)时,
温度(T)和压强(p)与反应物B在混合气体中的体积分数[φ(B)]的关系曲线,由曲线分析,下列判断正确的是(
)A.T<T,p>p,m+n>p,放热反应
1 2 1 2
B.T>T,p <p,m+n>p,吸热反应
1 2 1 2
C.T<T,p>p,m+n<p,放热反应
1 2 1 2
D.T>T,p<p,m+n<p,吸热反应
1 2 1 2
【答案】D
【解析】由图可知,压强一定时,温度T 先达到平衡,故温度:T >T ,升高温度,B在混合气体中
1 1 2
的体积分数减小,说明平衡正向移动,正反应为吸热反应;温度一定时,压强 p 先达到平衡,故压强:p
2 1
<p ,增大压强,B在混合气体中的体积分数增大,说明平衡逆向移动,正反应为气体体积增大的反应,
2
则m+n<p。
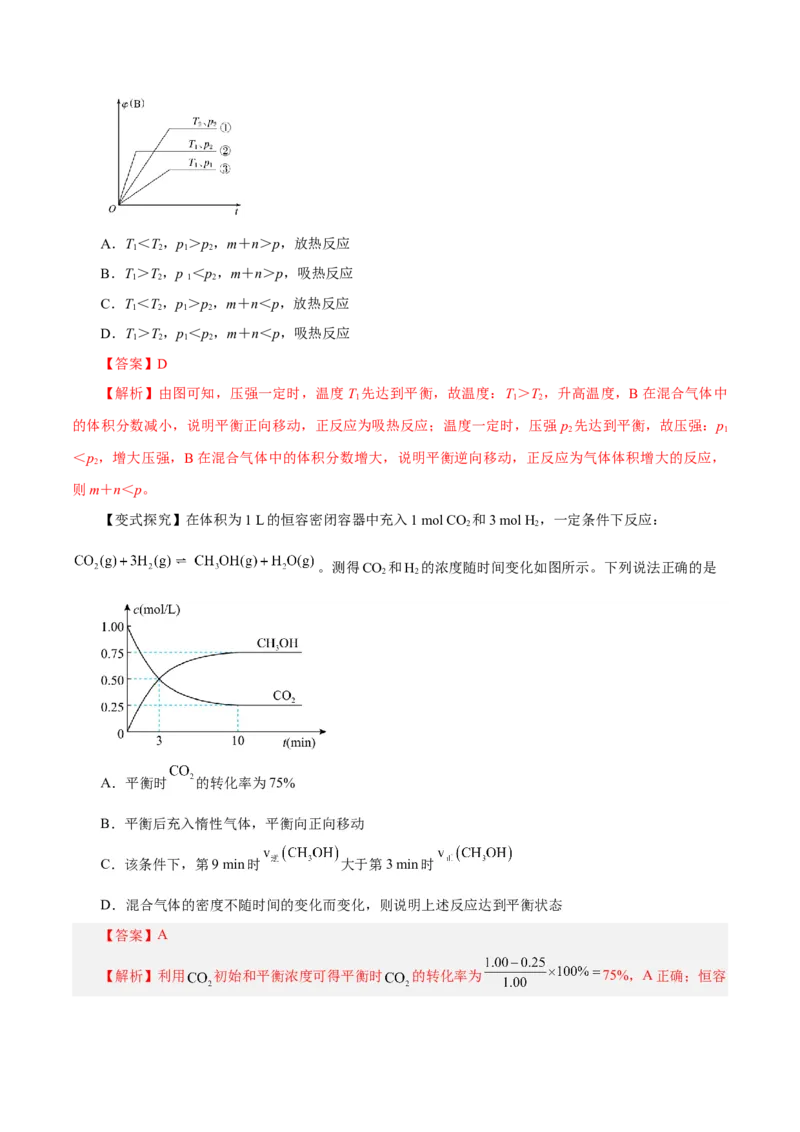
【变式探究】在体积为1 L的恒容密闭容器中充入1 mol CO 和3 mol H ,一定条件下反应:
2 2
。测得CO 和H 的浓度随时间变化如图所示。下列说法正确的是
2 2
A.平衡时 的转化率为75%
B.平衡后充入惰性气体,平衡向正向移动
C.该条件下,第9 min时 大于第3 min时
D.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
【答案】A
【解析】利用 初始和平衡浓度可得平衡时 的转化率为 75%,A正确;恒容容器充入惰性气体,与反应有关的各物质浓度不变,平衡不移动,B错误;平衡之前始终有 <
,故该条件下,第9 min时 小于第3 min时 ,C错误;
根据质量守恒定律,气体总质量不变,又该容器为恒容容器,故混合气体的密度始终不变,无法通过混合
气体密度判断反应是否达到平衡状态,D错误;故选A。
高频考点四 转化率(或含量)—温度—压强图像
这类图像的纵坐标为物质的平衡浓度或反应物的转化率,横坐标为温度或压强。、
[以mA(g)+nB(g) xC(g)+qD(g)为例]
m+n>x+q,ΔH>0 m+n<x+q,ΔH>0
m+n>x+q,ΔH<0 m+n>x+q,ΔH>0
m+n>x+q,ΔH>0 m+n<x+q,ΔH<0
1.“定一议二”原则:可通过分析相同温度下不同压强时反应物A的转化率(或C的含量)大小来判断
平衡移动的方向,从而确定反应方程式中反应物与产物气体物质间的化学计量数的大小关系。
2.通过分析相同压强下不同温度时反应物A的转化率(或C的含量)的大小来判断平衡移动的方向,从
而确定反应ΔH的正、负。
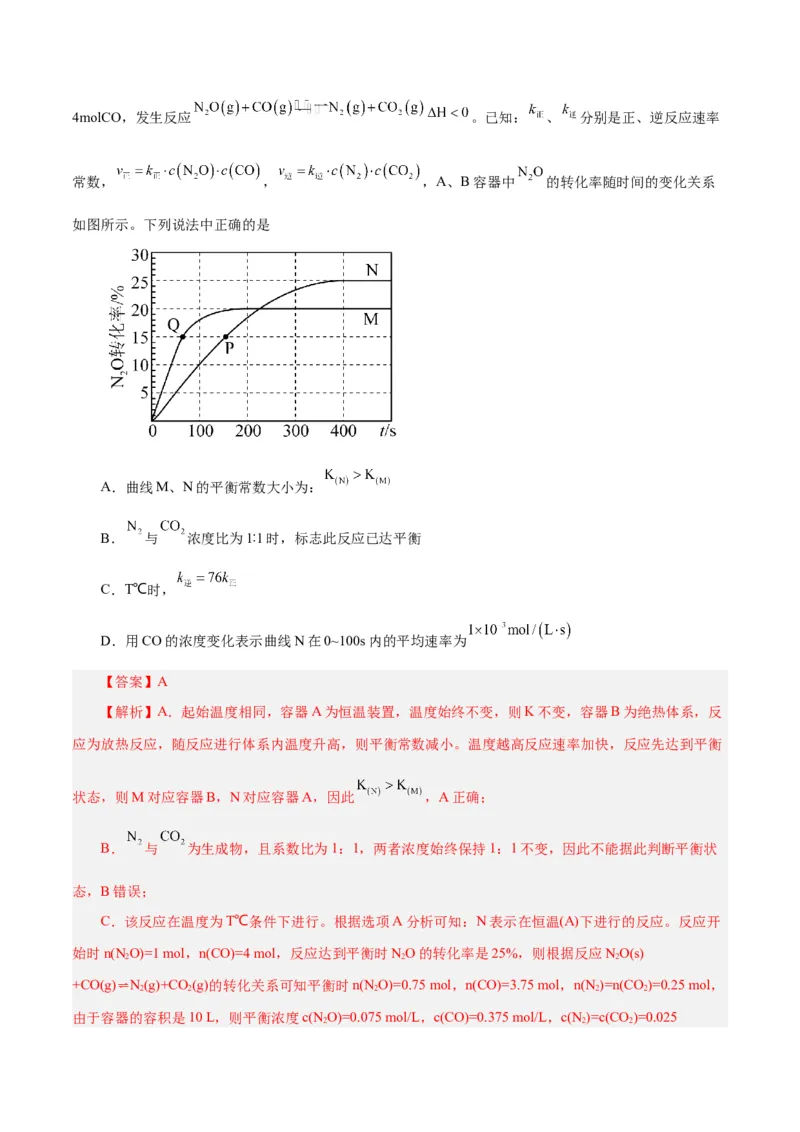
【例4】在起始温度均为T℃、容积均为10L的密闭容器A(恒温)、B(绝热)中均加入 和4molCO,发生反应 。已知: 、 分别是正、逆反应速率
常数, , ,A、B容器中 的转化率随时间的变化关系
如图所示。下列说法中正确的是
A.曲线M、N的平衡常数大小为:
B. 与 浓度比为1∶1时,标志此反应已达平衡
C.T℃时,
D.用CO的浓度变化表示曲线N在0~100s内的平均速率为
【答案】A
【解析】A.起始温度相同,容器A为恒温装置,温度始终不变,则K不变,容器B为绝热体系,反
应为放热反应,随反应进行体系内温度升高,则平衡常数减小。温度越高反应速率加快,反应先达到平衡
状态,则M对应容器B,N对应容器A,因此 ,A正确;
B. 与 为生成物,且系数比为1:1,两者浓度始终保持1:1不变,因此不能据此判断平衡状
态,B错误;
C.该反应在温度为T℃条件下进行。根据选项A分析可知:N表示在恒温(A)下进行的反应。反应开
始时n(N O)=1 mol,n(CO)=4 mol,反应达到平衡时NO的转化率是25%,则根据反应NO(s)
2 2 2
+CO(g)⇌N
2
(g)+CO
2
(g)的转化关系可知平衡时n(N
2
O)=0.75 mol,n(CO)=3.75 mol,n(N
2
)=n(CO
2
)=0.25 mol,
由于容器的容积是10 L,则平衡浓度c(NO)=0.075 mol/L,c(CO)=0.375 mol/L,c(N)=c(CO )=0.025
2 2 2mol/L,反应达到平衡时v =v ,k ∙c(NO) ∙c(CO)=k ∙c(N) ∙c(CO), = = =
正 逆 正 2 逆 2 2
,C错误;
D.0-100 s时NO的转化率为10 %,NO的反应量为l mol×10% =0.l mol,根据方程式中物质反应转
2 2
化关系可知CO的反应量为0.l mol,则用CO的浓度变化表示曲线N在0-100 s内的反应速率为v(CO)=
=1.0×10-4mol/(L⋅s),D错误;故选:A。
【变式探究】我国要在2030年前实现碳达峰,2060年前实现碳中和的目标。 还原为甲醇是人工
合成淀粉的第一步。 催化加氢主要反应有:
反应Ⅰ:
反应Ⅱ:
当压强分别为 、 时,将 与 以起始物质的量之比为1:3置于密闭容器中反应,不同温度下
平衡体系中 的转化率、 和 的选择性如图所示。
下列说法正确的是
A.若 ,则
B.曲线①表示 的选择性随温度的变化C.其他条件不变,升高温度, 的平衡转化率增大
D.相同温度下, 小于 ,且 下 的选择性小。
【答案】B
【解析】A.已知反应Ⅱ: ,若Ⅲ
,根据盖斯定律,由Ⅱ+Ⅲ得反应Ⅰ:
=-48.9kJ/mol,选项A错误;
B.反应Ⅰ是生成CHOH的反应,该反应是放热反应,温度越高,平衡逆向移动,CHOH的选择性
3 3
越低,反应Ⅱ是生成CO的反应,该反应是吸热反应,温度越高,平衡正向移动,则CO的选择性越高,
因此曲线①表示 的选择性,选项B正确;
C.反应Ⅰ是放热反应,反应Ⅱ是吸热反应,其他条件不变,升高温度, 的平衡转化率由反应Ⅰ
和反应Ⅱ共同判定,无法确定,选项C错误;
D.曲线①②表示 的选择性,增大压强有利于 的选择,故相同温度下, 大于 ,且
下 的选择性大,选项D错误;
答案选B。
【变式探究】探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以CO 、H 为
3 3 2 2
原料合成CHOH涉及的主要反应如下:
3
Ⅰ.CO (g)+3H(g ) CHOH(g)+HO(g) ΔH=-49.5 kJ·mol-1
2 2 3 2 1
Ⅱ.CO(g)+2H(g ) CHOH(g) ΔH=-90.4 kJ·mol-1
2 3 2
Ⅲ.CO (g)+H(g ) CO(g)+HO(g) ΔH=+40.9 kJ·mol-1
2 2 2 3
(1)不同压强下,按照n(CO)∶n(H )=1∶3投料,实验测定CO 的平衡转化率和CHOH的平衡产率随
2 2 2 3
温度的变化关系如图所示。已知:CO 的平衡转化率=×100%
2
CHOH的平衡产率=×100%
3
其中纵坐标表示CO 平衡转化率的是图________(填“甲”或“乙”);压强p、p、p 由大到小的顺序
2 1 2 3
为________;图乙中T 温度时,三条曲线几乎交于一点的原因是_______。
1
(2)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为________(填标号)。
2 3
A.低温、高压 B.高温、低压
C.低温、低压 D.高温、高压
【解析】(1)反应Ⅰ为放热反应,故低温阶段,温度越高,CO 的平衡转化率越低,而反应Ⅲ为吸热反
2
应,温度较高时,主要发生反应Ⅲ,则温度越高,CO 的平衡转化率越高,即图乙的纵坐标表示的是 CO
2 2
的平衡转化率。反应Ⅰ为气体分子数减少的反应,反应Ⅲ为气体分子数不变的反应,因此压强越大,CO
2
的平衡转化率越高,故压强由大到小的顺序是p 、p 、p 。反应Ⅲ为吸热反应,温度较高时,主要发生反
1 2 3
应Ⅲ,且反应Ⅲ反应前后气体分子数相等,故CO 的平衡转化率几乎不再受压强影响。(2)由上述分析知,
2
图甲、图乙的纵坐标分别表示CHOH的平衡产率、CO 的平衡转化率,且p >p >p ,分析图像可知,应
3 2 1 2 3
选择的反应条件为低温、高压,A项正确。
【答案】(1)乙 p 、p 、p T 时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡没有
1 2 3 1
影响
(2)A