文档内容
( )
昆明一中 2023 届高三第八次联考
化学参考答案
7 8 9 10 11 12 13
D B C B C A D
7.【答案】D
【解析】
铁的冶炼常用焦炭、CO等将铁矿石高温还原制得生铁,生铁可作炼钢原料,A选项说法正确;借助空
气把生铁中的碳、硫等部分除去,将含碳量降至2%以下,可实现“生铁炒钢”,B选项说法正确;生铁含
碳量高于2%,质硬而脆,熟铁含碳量低于0.03%,质柔不坚,生铁和熟铁混在一起冶炼,可使含碳量符合
钢的要求,C选项说法正确;“生铁先化,渗淋熟铁之中”说明生铁的熔点低于熟铁,但熟铁的含碳量低于
钢,D选项说法错误。
8.【答案】B
【解析】
脱水转化前有羰基、羟基、醚键三种官能团,脱水后增加了碳碳双键,官能团种类增加一种,A选项
说法错误;羟基或苯环均可发生取代反应,苯环和羰基均可发生加成反应,6-姜酚和6-姜烯酚都能被氧气
氧化,B选项说法正确;6-姜酚中结合羟基的饱和碳原子为手性碳,6-姜烯酚不含手性碳,C选项说法错误;
6-姜酚不具有顺反异构,D选项说法错误。
9.【答案】C
【解析】
将硫与热氢氧化钠溶液反应,硫歧化生成硫离子和亚硫酸根离子,A选项错误;将氯化铁溶液滴入碘化
钾溶液中,碘离子被氧化为碘单质,B选项错误;将少量甲酸钠溶液滴入溴水中,甲酸根离子被溴水氧化
为碳酸氢根离子,后者再与氧化还原过程中生成的氢离子结合放出二氧化碳,C选项正确;一水合氨不能
拆写成离子形式,D选项错误。
10.【答案】B
【解析】
盐溶液能使甲基橙变红色,不一定是强酸弱碱盐水解,可能是硫酸氢钠等强酸的酸式盐电离显酸性,A
选项结论不正确;某溶液中滴加酸性高锰酸钾溶液,紫色褪去并产生无色气体,该溶液可能是H O 溶液或
2 2
甲醛、甲酸、草酸等溶液,产生的气体可能是氧气或二氧化碳,B选项正确;向溶液中滴加盐酸酸化的氯
化钡溶液,产生白色沉淀,不能确定该沉淀是氯化银或硫酸钡,C选项错误;某化合物溶于盐酸或氢氧化
钠溶液均产生气体,可能是碳酸氢铵、硫化铵等挥发性弱酸的铵盐,不属于两性化合物,D选项错误。
11.【答案】C
【解析】
用氢氧化钠溶液滴定浓度相同的磷酸,V =V =20mL时,反应生成NaH PO ,溶液pH=4.7,说明磷
碱 酸 2 4
酸二氢根的电离程度大于水解程度,即 K >K /K ,可得 K ·K >K 。V =2V =40 mL 时,反应生成
a2 w a1 a1 a2 w 碱 酸
Na HPO ,溶液pH=9.7,说明磷酸一氢根的电离程度小于水解程度,即K <K /K ,可得K ·K <K ,A
2 4 a3 w a2 a2 a3 w
选项说法正确;a点为0.05mol·L−1NaH PO 溶液,c(Na+)=0.05mol·L−1最大,H PO-由于微弱电离和水解,
2 4 2 4
浓度稍小于c(Na+),c(H+)=10-4.7mol·L−1,在三者中最小,B选项说法正确;b点为Na HPO 溶液,根据元
2 4
素质量守恒可得:c(Na+)=2[c(H PO )+c(H PO-)+c(HPO2-)+c(PO3-)],C选项说法错误,符合题意;滴定时第
3 4 2 4 4 4
一次pH突变与甲基红的变色范围(4.4~6.2)吻合。第二次pH突变与酚酞的变色范围(8.2~10)吻合,指
示剂选择合理,D选项说法正确。
1昆明思塾升学高考补习学校 赵老师19984063112(微信同号)
12.【答案】A
【解析】
所含第二周期元素的第一电离能:F>N>O>C,A选项正确;三氟甲基中碳原子的轨道杂化类型为sp3,
B选项说法错误;基态碳原子中未成对电子数为2(2p能级的2个电子),少于氮2p能级上的3个未成对
电子(实际上未成对电子数最多的是铕,4f7),C选项说法错误;该配合物中配位原子是氧和氮,配位原子
数为2N+(2×3)O=8,D选项说法错误。
13.【答案】D
【解析】
在水溶液锌电池中锌作负极,氧化锰作正极,首次使用需将MnO氧化为产生锰空位的Mn V O,
0.61 Mn0.39
故需充电将MnO氧化激活,A选项叙述正确;①的电极反应式为MnO-0.78e−=Mn V O+0.39Mn2+
0.61 Mn0.39
,即充电使MnO氧化激活的电极反应,B选项叙述正确;该锌锰氧化物(Zn Mn V O)中锰的最低
x 0.61 Mn0.39
价态为+2,则x最大为0.39,若图中4个锌可能的位置全部被占据,则晶胞中锌离子数为4×1/2=2,达到
氧原子数的一半,则化学式为Zn Mn V O,超过x的最大值0.39,故锌可能的位置不可能都被占据,
0.5 0.61 Mn0.39
C选项叙述正确;理论上,1mol 晶体转移电子的物质的量③为2xmol≤①的0.78mol,D选项叙述错误,
符合题意。
27.(15分)
(1)Cu (OH) CO +4H+=2Cu2++CO ↑+3H O (2分)
2 2 3 2 2
(2)2.5V,3.0h (1分) 2H O-4e−=O ↑+4H+(2分) 取少量电解液于试管中,滴加铁
2 2
氰化钾溶液后未产生蓝色沉淀(2分,或取少量电解液调pH为3.5,过滤,向滤液中滴加KSCN溶液后不
变红,再滴加氯水后也不变红)
(3)溶解度最大的磷酸盐杂质(K 最大)CrPO 刚好完全沉淀时,c(PO3−)=1×10−17/1×10−5=1×10−12mol·L−1,
sp 4 4
c3(Ni2+)·c2(PO3−)=10−3×3×10−12×2=10−33<K [Ni (PO ) ]=5×10−31,不析出Ni (PO ) 沉淀(2分,合理即可)
4 sp 3 4 2 3 4 2
镍离子被絮状沉淀吸附(或镍离子与杂质离子形成磷酸盐共沉淀)(2分,合理即可)
(4)浸出(1分) b(1分)
(5) (2分)
28.(14分)
(1)硫氢化铵(1分)
△
(2)2NH Cl+Ca(OH) ==== CaCl +2NH ↑+2H O(2分) 碱石灰(1分)
4 2 2 3 2
(3)CS 层(1分) 使CS 与NH 接触充分,同时防止倒吸(2分)
2 2 3
(4)在D和E之间连接一个安全瓶(2分,合理即可) 冷却结晶(1分)
(5)加入半滴AgNO 溶液后,溶液红色褪去,且30秒内无变化(2分)
3
(6) (2分)
29.(14分)
(1)CH OH*=CO*+2H (g) ∆H=+65.7kJ·mol−1(2分) 179.6 (1分) +26.3(2分)解析:
3 2
根据CH OH*=CH OH(g)∆H >0,CO*=CO(g)∆H >0
3 3 1 2
可得CO*+CH OH(g)=CO(g)+CH OH* ∆H=∆H -∆H
3 3 2 1
再根据CH OH(g) CO(g)+2H (g)∆H=+92.0kJ·mol−1,CH OH*=CO*+2H (g)∆H=+65.7kJ·mol−1
3 2 3 2
可得CO*+CH OH(g)=CO(g)+CH OH* ∆H=(+92.0kJ·mol−1)-(+65.7kJ·mol−1)=+26.3kJ·mol−1
3 3
(2)①b(2分) c(2分)
解析:反应物水的转化率随x 增大而增大,则出口物料中x 将随x 增大而减小,故表示x 的是b;
甲醇进料 水 甲醇进料 水
三个反应都生成氢气,生成二氧化碳的是反应ii、iii,且生成二氧化碳的物质的量小于氢气,则x 大于
氢气
x ,故表示x 、x 的分别是a、c。
二氧化碳 氢气 二氧化碳
2昆明思塾升学高考补习学校 赵老师19984063112(微信同号)
大于(1分) x =x =0.5,出口时x <x ,说明甲醇的转化量大于水,
甲醇进料 水进料 甲醇 水
所以α 大于α(2分,合理即可)
甲醇 水
0.056×0.6462×p2 0.178×0.6463×p2 0.056×0.088
②[( 总)/( 总)]= <1(2分)
0.032 0.032×0.088 0.178×0.646
p ·p2 x p ·x2 p2 0.056×0.6462×p2
解析:Q = 一氧化碳 氢气= 一氧化碳 总 氢气 总= 总、
p反应i
p x p 0.032
甲醇 甲醇 总
p ·p3 x p ·x3 p3 0.178×0.6463×p2
Q = 二氧化碳 氢气= 二氧化碳 总 氢气 总= 总
p反应ii
p ·p x p ·x p 0.032×0.088
甲醇 水 甲醇 总 水 总
则 Q p反应i =[( 0.056×0.6462×p2 总)/( 0.178×0.6463×p2 总)]= 0.056×0.088 <1。
Q 0.032 0.032×0.088 0.178×0.646
p反应ii
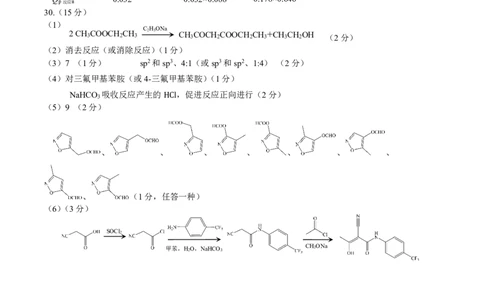
30.(15分)
(1)
2CH 3 COOCH 2 CH 3
C2H5ONa
CH 3 COCH 2 COOCH 2 CH 3 +CH 3 CH 2 OH (2分)
(2)消去反应(或消除反应)(1分)
(3)7 (1分) sp2和sp3、4:1(或sp3和sp2、1:4) (2分)
(4)对三氟甲基苯胺(或4-三氟甲基苯胺)(1分)
NaHCO 吸收反应产生的 ,促进反应正向进行(2分)
3
(5)9 (2分)
HCl
、 、 、 、 、 、 、
、 (1分,任答一种)
(6)(3分)
SOCl2
甲苯,H2O,NaHCO3 CH3ONa
3