文档内容
丰台区 2022~2023 学年度第一学期期末练习
高 三 化 学
2023.01
1.答题前,考生务必先将答题卡上的学校、班级、姓名、准考证号用黑色字迹签字笔填
写清楚,并认真核对条形码上的准考证号、姓名,在答题卡的“条形码粘贴区”贴好
考 条形码。
生 2.本次练习所有答题均在答题卡上完成。选择题必须使用2B铅笔以正确填涂方式将各
须 小题对应选项涂黑,如需改动,用橡皮擦除干净后再选涂其它选项。非选择题必须使
知 用标准黑色字迹签字笔书写,要求字体工整、字迹清楚。
3.请严格按照答题卡上题号在相应答题区内作答,超出答题区域书写的答案无效,在练
习卷、草稿纸上答题无效。
4.本练习卷满分共100分,作答时长90分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
第一部分(选择题 共 42 分)
本部分共 14 题,每题 3 分,共 42 分。在每题列出的四个选项中,选出最符合题目要求
的一项。
1.化学与生活密切相关。下列叙述正确的是
A.冰的密度比水小,是因为水分子内存在氢键
B.洁厕灵(主要成分为HCl)与84消毒液可以混用
C.镀锌铁制品的镀层破损后失去对铁制品的保护作用
D.利用紫外杀菌技术进行消毒,是为了使蛋白质变性
2.下列化学用语或图示表达不正确的是
...
A.HClO的电子式:
B.乙酸甲酯的结构简式:CH COOCH
3 3
C.乙烯的分子结构模型:
3s 3p
D.基态S原子的价层电子的轨道表示式:
3.下列有关性质的比较,不
.
能
.
用元素周期律解释的是
A.熔点:CO < SiO B.酸性:H SO > H PO
2 2 2 4 3 4
C.金属性:Na > Mg D.稳定性:H O > H S
2 2
高三化学 第1 页(共9页)4.下列反应的离子方程式正确的是
A.用饱和碳酸钠溶液处理水垢中的硫酸钙:CO2-+Ca2+=== CaCO ↓
3 3
B.NO 通入水中制硝酸:2NO +H O === H++NO- +NO↑
2 2 2 3
C.硫酸铜溶液中加少量的铁粉:3Cu2+ +2Fe === 2Fe3+ +3Cu
D.室温下用稀HNO
3
溶解铜:3Cu+2NO-
3
+ 8H+ === 3Cu2+ + 2NO↑+ 4H
2
O
5. N 为阿伏加德罗常数,下列说法正确的是
A
A.0.1 mol氨基(—NH )中含有N 个质子
2 A
B.14 g乙烯和丙烯的混合气体中所含碳氢键数为2 N
A
C.1.0 mol·L-1AlCl 溶液中,Cl-数目为3 N
3 A
D.电解熔融NaCl,阳极产生气体质量为7.1 g时,外电路中通过电子的数目为0.1 N
A
6.常温下,1体积水能溶解约700体积NH 。用圆底烧瓶收集NH 后进行如图所示实验,下
3 3
列分析正确的是
氨气
A.圆底烧瓶内形成喷泉现象,证明NH 与水发生了反应
3
B.喷泉停止后,圆底烧瓶内剩余少量气体,是因为NH 3 的 胶头滴管
溶解已达到饱和
止水夹
C.圆底烧瓶中的液体呈红色的原因是
NH +H O NH ·H O NH+ +OH-
水(含酚酞试剂)
3 2 3 2 4
D.取圆底烧瓶内部分液体,滴加盐酸至pH=7时,溶液中c(Cl-)>c(NH+ )
4
7.下列物质混合后,变化过程中不涉及氧化还原反应的是
...
A.FeCl 溶液使淀粉碘化钾试纸变蓝
3
B.将SO 通入到Ba(NO ) 溶液中,生成白色沉淀
2 3 2
C.向饱和食盐水中依次通入NH 、CO ,有晶体析出
3 2
D.石蕊溶液滴入氯水中,溶液变红,随后迅速褪色
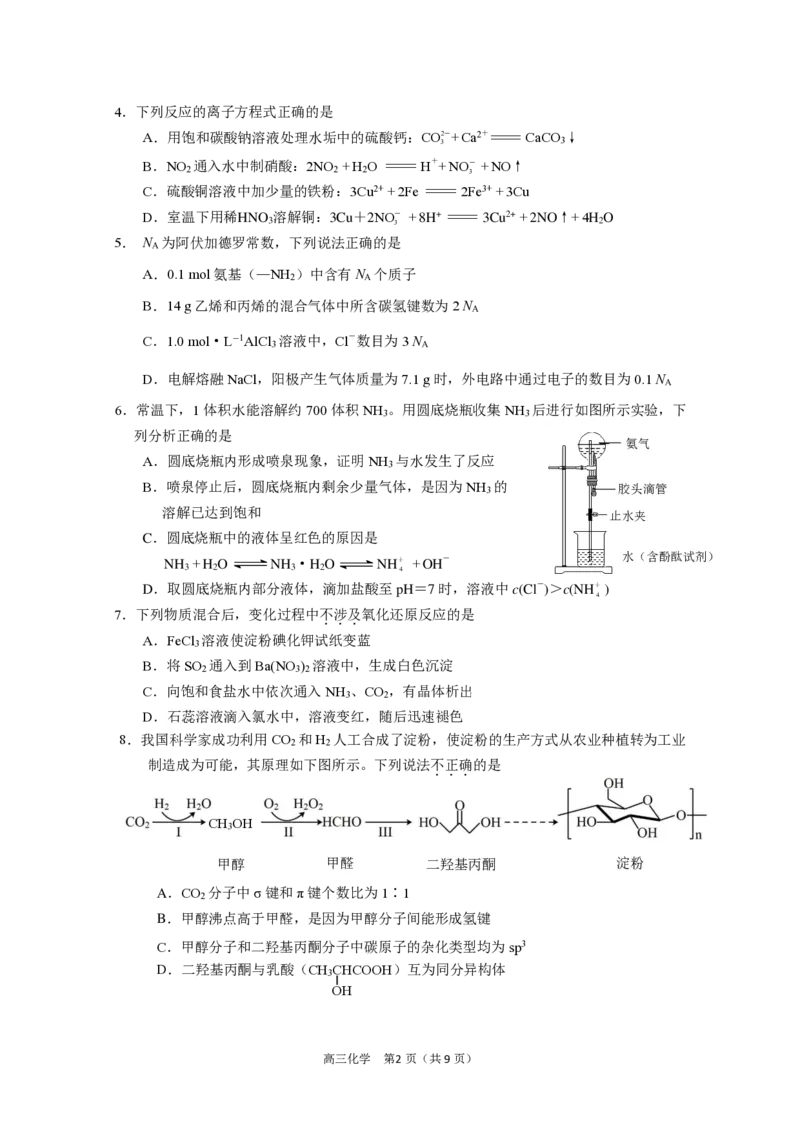
8.我国科学家成功利用CO 和H 人工合成了淀粉,使淀粉的生产方式从农业种植转为工业
2 2
制造成为可能,其原理如下图所示。下列说法不正确的是
...
CH OH
3
甲醇 甲醛 二羟基丙酮 淀粉
A.CO 分子中σ键和π键个数比为1∶1
2
B.甲醇沸点高于甲醛,是因为甲醇分子间能形成氢键
C.甲醇分子和二羟基丙酮分子中碳原子的杂化类型均为sp3
D.二羟基丙酮与乳酸(C H C H C O O H )互为同分异构体
3
OH
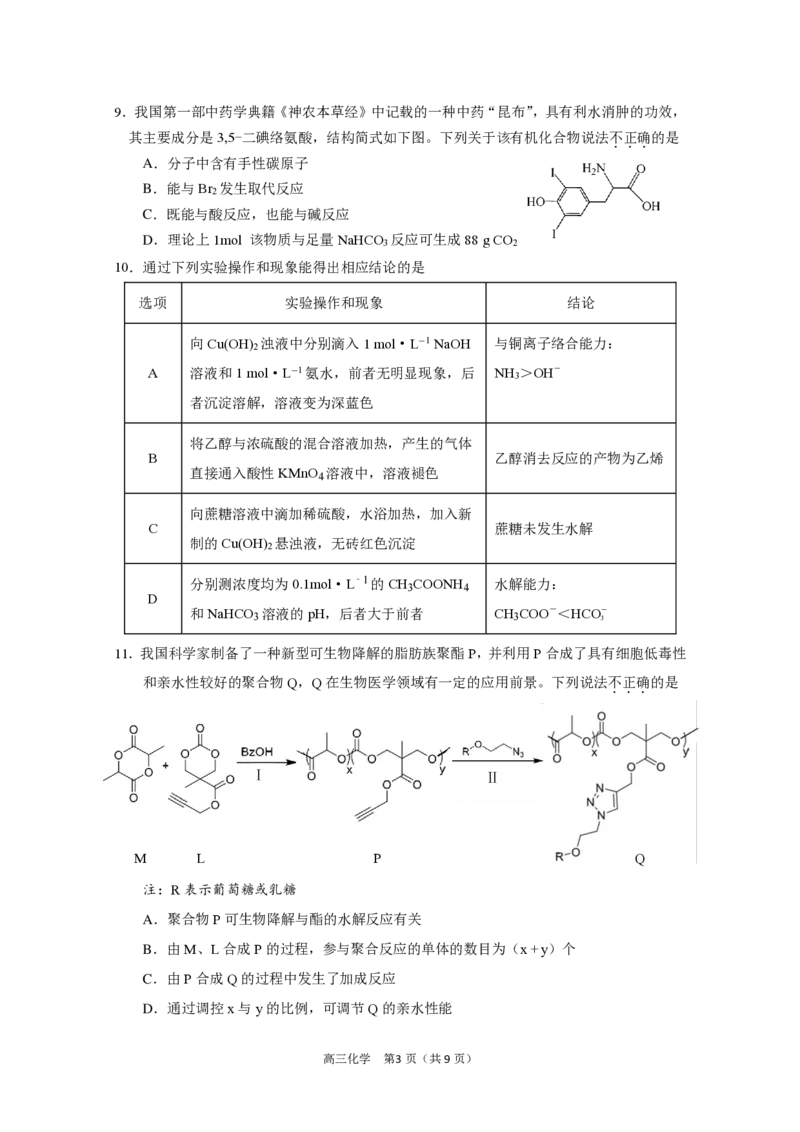
高三化学 第2 页(共9页)9.我国第一部中药学典籍《神农本草经》中记载的一种中药“昆布”,具有利水消肿的功效,
其主要成分是3,5-二碘络氨酸,结构简式如下图。下列关于该有机化合物说法不正确的是
...
A.分子中含有手性碳原子
B.能与Br 发生取代反应
2
C.既能与酸反应,也能与碱反应
D.理论上1mol 该物质与足量NaHCO 反应可生成88 g CO
3 2
10.通过下列实验操作和现象能得出相应结论的是
选项 实验操作和现象 结论
向Cu(OH) 浊液中分别滴入1 mol·L-1 NaOH 与铜离子络合能力:
2
A 溶液和1 mol·L-1氨水,前者无明显现象,后 NH >OH-
3
者沉淀溶解,溶液变为深蓝色
将乙醇与浓硫酸的混合溶液加热,产生的气体
B 乙醇消去反应的产物为乙烯
直接通入酸性KMnO 溶液中,溶液褪色
4
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新
C 蔗糖未发生水解
制的Cu(OH) 悬浊液,无砖红色沉淀
2
分别测浓度均为0.1mol·L﹣1的CH COONH 水解能力:
3 4
D
和NaHCO 溶液的pH,后者大于前者 CH COO-<HCO-
3 3 3
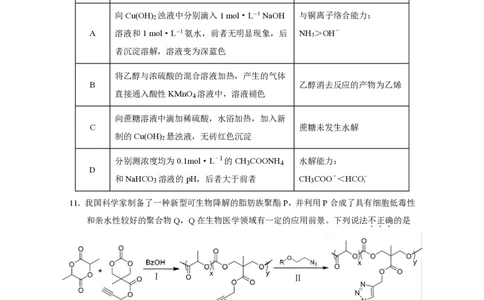
11.我国科学家制备了一种新型可生物降解的脂肪族聚酯P,并利用P合成了具有细胞低毒性
和亲水性较好的聚合物Q,Q在生物医学领域有一定的应用前景。下列说法不正确的是
...
Ⅰ Ⅱ
Q
M L P Q
注:R表示葡萄糖或乳糖
A.聚合物P可生物降解与酯的水解反应有关
B.由M、L合成P的过程,参与聚合反应的单体的数目为(x +y)个
C.由P合成Q的过程中发生了加成反应
D.通过调控x与y的比例,可调节Q的亲水性能
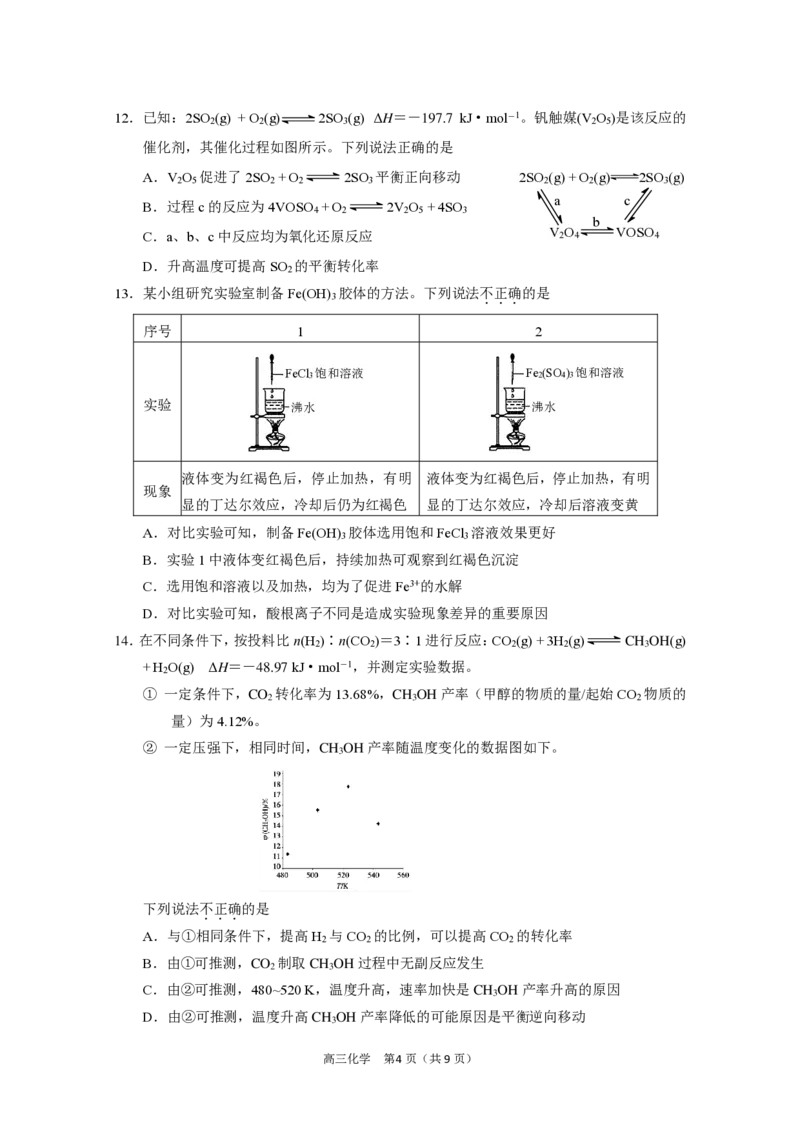
高三化学 第3 页(共9页)12.已知:2SO
2
(g) + O
2
(g) 2SO
3
(g) ΔH=-197.7 kJ·mol-1。钒触媒(V
2
O
5
)是该反应的
催化剂,其催化过程如图所示。下列说法正确的是
A.V O 促进了2SO +O 2SO 平衡正向移动 2SO (g) +O (g) 2SO (g)
2 5 2 2 3 2 2 3
a c
B.过程c的反应为4VOSO +O 2V O +4SO
4 2 2 5 3
b
C.a、b、c中反应均为氧化还原反应 V 2 O 4 VOSO 4
D.升高温度可提高SO 的平衡转化率
2
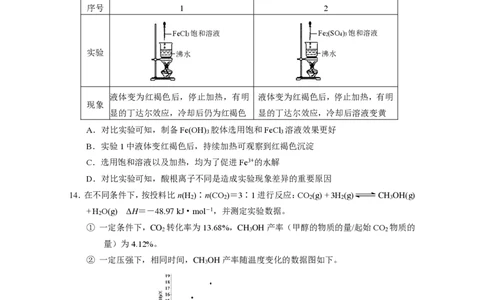
13.某小组研究实验室制备Fe(OH) 胶体的方法。下列说法不正确的是
3 ...
序号 1 2
FeCl3 饱和溶液 Fe2(SO4)3 饱和溶液
实验 沸水 沸水
液体变为红褐色后,停止加热,有明 液体变为红褐色后,停止加热,有明
现象
显的丁达尔效应,冷却后仍为红褐色 显的丁达尔效应,冷却后溶液变黄
A.对比实验可知,制备Fe(OH) 胶体选用饱和FeCl 溶液效果更好
3 3
B.实验1中液体变红褐色后,持续加热可观察到红褐色沉淀
C.选用饱和溶液以及加热,均为了促进Fe3+的水解
D.对比实验可知,酸根离子不同是造成实验现象差异的重要原因
14.在不同条件下,按投料比n(H )∶n(CO )=3∶1进行反应:CO (g) +3H (g) CH OH(g)
2 2 2 2 3
+H O(g) ΔH=-48.97 kJ·mol-1,并测定实验数据。
2
① 一定条件下,CO 转化率为13.68%,CH OH产率(甲醇的物质的量/起始CO 物质的
2 3 2
量)为4.12%。
② 一定压强下,相同时间,CH OH产率随温度变化的数据图如下。
3
下列说法不正确的是
...
A.与①相同条件下,提高H 与CO 的比例,可以提高CO 的转化率
2 2 2
B.由①可推测,CO 制取CH OH过程中无副反应发生
2 3
C.由②可推测,480~520 K,温度升高,速率加快是CH OH产率升高的原因
3
D.由②可推测,温度升高CH OH产率降低的可能原因是平衡逆向移动
3
高三化学 第4 页(共9页)第二部分(非选择题 共 58 分)
本部分共5题,共58分。
15.(10 分)ZnS、CdSe 均为重要的半导体材料,可应用于生物标记和荧光显示领域,并在
光电器件、生物传感和激光材料等方面也得到了广泛的应用。
(1)基态Zn原子的价层电子排布式为________。
(2) Se在周期表中的位置为________。
34
(3)S与P在周期表中是相邻元素,两者的第一电离能:S________P(填“>”、“<”或“=”),
解释其原因________。
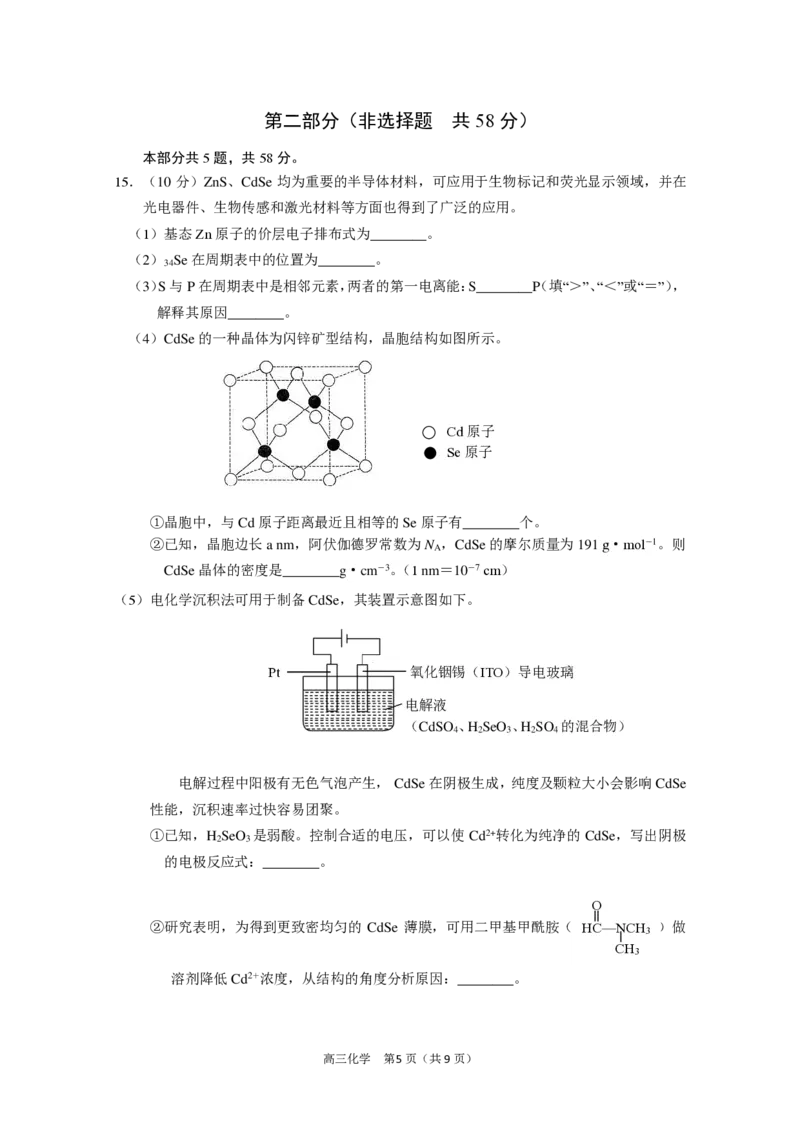
(4)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示。
Cd原子
Se原子
①晶胞中,与Cd原子距离最近且相等的Se原子有________个。
②已知,晶胞边长a nm,阿伏伽德罗常数为N ,CdSe的摩尔质量为191 g·mol-1。则
A
CdSe晶体的密度是________g·cm-3。(1 nm=10-7 cm)
(5)电化学沉积法可用于制备CdSe,其装置示意图如下。
Pt 氧化铟锡(ITO)导电玻璃
电解液
(CdSO 、H SeO 、H SO 的混合物)
4 2 3 2 4
电解过程中阳极有无色气泡产生, CdSe在阴极生成,纯度及颗粒大小会影响CdSe
性能,沉积速率过快容易团聚。
①已知,H SeO 是弱酸。控制合适的电压,可以使 Cd2+转化为纯净的 CdSe,写出阴极
2 3
的电极反应式:________。
O
②研究表明,为得到更致密均匀的 CdSe 薄膜,可用二甲基甲酰胺( H C — N C H )做
3
CH
3
溶剂降低Cd2+浓度,从结构的角度分析原因:________。
高三化学 第5 页(共9页)16.(11 分)煤焦油、煤和海砂中氯离子含量高会破坏金属的钝化膜,导致铁制设备和钢管
等被腐蚀。
(1)铁接触氧气和水后会发生电化学腐蚀,其负极的电极反应式为________。
(2)测定煤中氯离子含量的两种方法。
方法一:在高温下,通入水蒸气将煤样中无机盐转化为HCl,再滴定氯离子。
方法二:取a g煤样,处理后得到含氯离子的样品溶液,加入v mL b mol·L-1AgNO
1 3
溶液,以NH Fe(SO ) 作指示剂,用c mol·L-1 KSCN溶液滴定过量的AgNO 溶液,
4 4 2 3
共消耗KSCN溶液v mL。
2
已知:AgNO 能与KSCN反应生成AgSCN沉淀。
3
① 结合化学用语,从化学平衡的角度解释方法一中无机盐中 MgCl 生成 HCl 的原因
2
________。
②方法二中,滴定终点的现象为 。
③利用方法二,测得煤样中氯元素的质量分数为 。
(3)快速检测法测定海砂中氯离子含量的过程如下。
ⅰ.配制固定组分的铬酸银(Ag CrO )浑浊液;
2 4
ⅱ.将待测海砂样品与ⅰ中浑浊液混合,溶液的颜色会随着氯离子含量的变化而变化。
氯离子含量x x<0.001% 0.003%>x>0.001% x>0.003%
沉 淀 仍 然 砖红色沉淀部分变为白色, 砖红色沉淀完全变为白色,
ⅱ中现象
为砖红色 溶液逐渐转变为黄色 溶液完全转变为黄色
已知: K
sp
(Ag
2
CrO
4
)=c2 (Ag+)·c (CrO2
4
-) =1.1×10-12; K
sp
(AgCl)=1.8×10-10;
K CrO 溶液为黄色, Ag CrO 固体为砖红色。
2 4 2 4
①x<0.001% 时, 沉淀仍然为砖红色的原因是________。
②写出砖红色沉淀变为白色的离子方程式________。
高三化学 第6 页(共9页)17.(13分)抗肿瘤药物培美曲塞的前体N合成路线如下:
A Br2
B
C C2H5MgBr D E
C 2 H 4 C 2 H 2 THF C 2 HMgBr H+ C 4 H 6 O
J
C
12
H
12
O
3
F Br2 G 氧化 H 浓硫酸/△ I
H
C 7 H 8 FeBr3 C 7 H 7 Br C 7 H 5 O 2 Br 试剂a C 8 H 7 O 2 Br 2
试剂b M HBr L
一定条件 C 12 H 13 O 3 Br DBBA C 12 H 14 O 3
N K
O
HN
已知:ⅰ. 试剂b的结构简式为 H 2 N N NH 2
OO
ⅱ. R MRgMBgrB R r
T
1
H
R
T
H
F
1
H
H
F
R 1RM
1
gMBgrBr
H+
R 1RC
1
HC2HC
2
HC2HO
2
HOH
R 1 NH 2 ⅲ+. RRRR 1112 NNNCHHHH 22 O 2 +++ 一 RRR 定 222 条件 CCCHHHRROOO 11 一一一 NN 定定定 HH 条条条 2 件件件 C+HRRRR 2111 RNNNC 2 HHHHOCCC 一 HHH 定条 RRR 件 222 R 1 NH CH R 2
OH OOOHHH OH
(1)B→C反应所需的试剂和条件是________。
(2)E的结构简式是________。
(3)G的结构简式是________。H→I的化学方程式是________。
(4)下列关于J的说法正确的是________。
a.J分子中有三种官能团 b.可以与Na、NaOH、Br 发生反应
2
c.核磁共振氢谱有5组峰 d.由E和I生成J的反应类型是取代反应
(5)L中含氧官能团名称是_______。
(6)M→N的反应过程有HBr和H O生成,则M的结构简式是________。
2
(7)试剂b的一种合成路线如下。已知P中含—CH —结构,写出中间产物P、Q的结
2
构简式________、________。
+
加成 -C
2
H
5
OH 异构化
P Q
取 代
试剂b
高三化学 第7 页(共9页)18.(12分)富钴结壳浸出液分离MnSO 制备Mn O 的工业流程如下。
4 3 4
洗涤
固体X Fe
2
O
3
·xH
2
O
O2 、石灰乳
浸出液
固体Y
②
S
还
O
原
2 ① NaHS Mn 3 O 4
溶液1
富钴结壳 ③
⑤
无烟煤
焙烧
④
溶液2 MnSO
4
固体
已知:ⅰ.浸出液中主要含有的金属离子为:Ni2+、Co2+、Cu2+、Mn2+、Fe2+
ⅱ.25℃时,金属硫化物的溶度积常数。
金属硫化物 NiS CoS CuS MnS
K 3.98×10-20 5.01×10-22 7.94×10-37 3.16×10-11
sp
(1)过程①中,SO 还原得到的浸出液中含硫元素的阴离子主要为________。
2
(2)过程②中,Fe2+转化为Fe O ·xH O时,氧气和石灰乳的作用分别是________。
2 3 2
(3)固体Y中主要物质的化学式为________。
(4)已知,Mn2+在 pH=9.7 时完全沉淀转化为 Mn(OH) 。过程③中沉淀剂不选择 Na S
2 2
的原因可能是________。
(5)已知,温度高于 20℃时,MnSO 在水中的溶解度随温度升高迅速降低。过程④中,
4
采用的操作是________。
(6)过程⑤中发生下列反应。
C(s)+O (g) === CO (g) ΔH = -394 kJ·mol−1
2 2 1
1
C(s)+ O (g) === CO(g) ΔH = -111 kJ·mol−1
2 2 2
3MnSO (s) +2CO(g) === Mn O (s) +3SO (g) +2CO (g) ΔH
4 3 4 2 2 3
利用ΔH 和ΔH 计算ΔH 时,还需要利用________反应的ΔH。
1 2 3
(7)流程中可循环使用的物质是________。
高三化学 第8 页(共9页)19.(12分)某小组同学探究实验室配制银氨溶液并检验醛基的方法。
资料:ⅰ.AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的Ag O。
2
ⅱ.向硝酸银溶液中加入氨水,转化为 Ag O 的 AgNO 占参加反应的 AgNO 总量的百
2 3 3
分比最大不超过10%。
Ⅰ.在实验室配制银氨溶液的过程中,小组同学发现,所用试剂的配制方式和存放时间不
同,实验现象不同。(注:以下试剂若无特殊说明,均为新制)
序号 实验操作 实验现象
1 向1 mL 2%AgNO 溶液中逐滴加入2% 氨水 先产生棕色沉淀,后溶液变澄清
3
向1 mL 2%AgNO 溶液中逐滴加入在空气中 先产生白色沉淀,后溶液变澄清
3
2
存放一段时间的2% 氨水
向1 mL 2% AgNO(HNO 酸化)溶液中逐滴 溶液始终澄清
3 3
3
加入2% 氨水至过量
(1)NH 分子空间构型为________。
3
(2)结合资料ⅱ,写出实验1中加入少量氨水时发生的主要反应的离子方程式________。
(3)已知,实验2中白色沉淀加硝酸产生能使澄清石灰水变浑浊的无色气体,实验2中
白色沉淀的主要成分是________。
(4)对比实验1和3,分析实验3中“溶液始终澄清”的原因是________。
Ⅱ.用实验1配制出的银氨溶液检验醛基。
资料:可从电极反应角度分析物质氧化性和还原性的变化。
(5)银氨溶液与CH CHO的反应中,电极反应式:
3
还原反应:Ag+ + e- = Ag;氧化反应:________(碱性条件下)。
在此基础上设计并实施了以下实验。
序号 实验操作 实验现象
4 向银氨溶液中加入3滴CH CHO,水浴加热 产生银镜
3
5 向银氨溶液中加入1滴10% NaOH溶液后,滴入3滴CH CHO 产生银镜比实验4快
3
(6)实验 5 产生银镜比实验 4 快的可能原因是________。按照实验 5 的方法,将乙醛换
成丙酮,水浴加热后也能产生银镜。
综合上述实验,实验4是检验醛基的最合理方法。
高三化学 第9 页(共9页)丰台区 2022~2023 学年度第一学期期末练习
高三化学 参考答案
2023.01
第一部分(选择题 共 42 分)
1 2 3 4 5 6 7
D A A D B C C
8 9 10 11 12 13 14
C D A B B C B
第二部分(非选择题 共58分)
15.(10分)(1)3d104s2(1分)
(2) 第四周期VIA族(1分)
(3)< (1 分) P 的价电子排布式为 3s23p3,S 的价电子排布为 3s23p4,P 原子为
半充满结构,比较稳定,难失电子,第一电离能大。(1分)
(4)①4 (1分) ②764/(N ×a3×10-21) (2分)
A
(5)①H SeO +4H++Cd2++6e-=== CdSe↓+3H O (2分)
2 3 2
②二甲基甲酰胺中N原子有孤电子对,Cd2+有空轨道,可以形成配合物(1分)
16.(11分)(1)Fe-2e-=== Fe2+(2分)
(2)①MgCl +2H O Mg(OH) +2HCl,高温下HCl逸出,平衡正向移动。(2分)
2 2 2
② 溶液变为红色,半分钟不褪色(1分)
③ 35.5(v b- v c)×10-3 /a (2分)
1 2
(3)①氯离子含量低(浓度),Q=c( Cl-)· c(Ag+)<K (AgCl),达不到生成AgCl沉
sp
淀的条件。(2分)
②Ag CrO +2Cl-==== =2AgCl+CrO2- (2分)
2 4 4
17.(13分)
(1)NaOH/乙醇、△ (2分) (2) (1分)
CH
(3) 3 (1分)
Br
(2分)
浓硫酸
Br COOH + CH OH Br COOCH + H O
3 3 2
(4)a b d(2分)
(5)醛基 酯基(2分)
参考答案 第1页 共2页(6) (1分)
(7)CH CH OOC—CH —CN (1分) (1分)
3 2 2
18.(12分)(1)SO2- (1分)
4
(2)氧气是氧化剂,可将Fe2+氧化为Fe3+,石灰乳是沉淀剂,可调节PH使Fe3+沉淀
(2分)
(3)CoS、NiS、CuS(2分)
(4)Na S水解呈碱性,其碱性强于NaHS。可能会导致Mn2+转化为Mn(OH) 沉淀(2
2 2
分)
(5)蒸发、结晶(趁热过滤)(2分)
(6)3MnSO (s)=== Mn O (s) +3SO (g)+O (g) (2分)
4 3 4 2 2
(7)SO (1分)
2
19.(12分)(1)三角锥形(2分)
(2)Ag+ + 2NH •H O [Ag(NH ) ]+ +2H O(2分)
3 2 3 2 2
(3)Ag CO (2分)
2 3
(4) 加入氨水,发生反应:H+ + NH •H O === NH + + H O,c(NH +)增大,使平衡
3 2 4 2 4
NH •H O NH ++OH-逆向移动,c(OH-)减小,c(Ag+)•c(OH-)无法达到
3 2 4
K (AgOH),因此溶液始终澄清。(2分)
sp
(5) CH
3
CHO-2e-+3OH-=== CH
3
COO- + 2H
2
O(2分)
(6)加入1滴10%NaOH溶液,c(OH-)增大,乙醛还原性增强,反应速率加快。(2分)
参考答案 第2页 共2页