文档内容
培优训练8:新型电源及电解应用
1.(2019·湖南省郴州市高三一检,10)优质的锂碘电池可用于心脏起搏器延续患
者的生命,它的正极材料是聚2乙烯吡啶(简写P VP)和I 的复合物,电解质是固
2 2
态薄膜状的碘化锂,电池的总反应为2Li+P VP·nI ===P VP(· n-1)I +2LiI,则下
2 2 2 2
列说法正确的是( )
A.正极的反应为P VP·nI +2e-===P VP·(n-1)I +2I-
2 2 2 2
B.电池工作时,碘离子移向P VP极
2
C.聚2乙烯吡啶的复合物与有机物性质相似,因此聚2乙烯吡啶的复合物不会导电
D.该电池所产生的电压低,使用寿命比较短
解析 A.正极的反应为P VP·nI +2e-===P VP(· n-1)I +2I-,故A正确;B.P VP
2 2 2 2 2
极为正极,电池工作时,碘离子移向负极Li,故B错误;C.聚2乙烯吡啶的复合物
作正极,因此聚2乙烯吡啶的复合物可以导电,故C错误;D.锂的比能量高,该电
池使用寿命比较长,故D错误。故选A。
答案 A
2(. 2018·南昌NCS2018060项目一模,12)氨硼烷(NH ·BH )电池可在常温下工
3 3
作,装置如图所示。该电池工作时的总反应为:NH ·BH +3H O ===NH BO +
3 3 2 2 4 2
4H O。下列说法正确的是( )
2
A.正极附近溶液的pH减小
B.电池工作时,H+通过质子交换膜向负极移动
C.消耗3.1 g 氨硼烷,理论上通过内电路的电子为0.6 mol
D.负极电极反应为:NH ·BH +2H O-6e-===NH+BO+6H+
3 3 2
解析 根据电池总反应,正极上H O 发生还原反应:H O +2e-+2H+===2H O,
2 2 2 2 2
正极附近c(H+)减小,溶液pH增大,A项错误;原电池工作时,阳离子向正极移动,
故H+通过质子交换膜向正极移动,B项错误;NH ·BH 转化为NH BO ,N的化合
3 3 4 2
价不变,B的化合价升高,根据NH ·BH ――→NH BO ,消耗3.1 g氨硼烷(0.1
3 3 4 2mol),反应中转移0.6 mol电子,但电子不通过内电路,C项错误;根据电池总反应,
负极上氨硼烷发生氧化反应:NH ·BH +2H O-6e-===NH+BO+6H+,D项正确。
3 3 2
答案 D
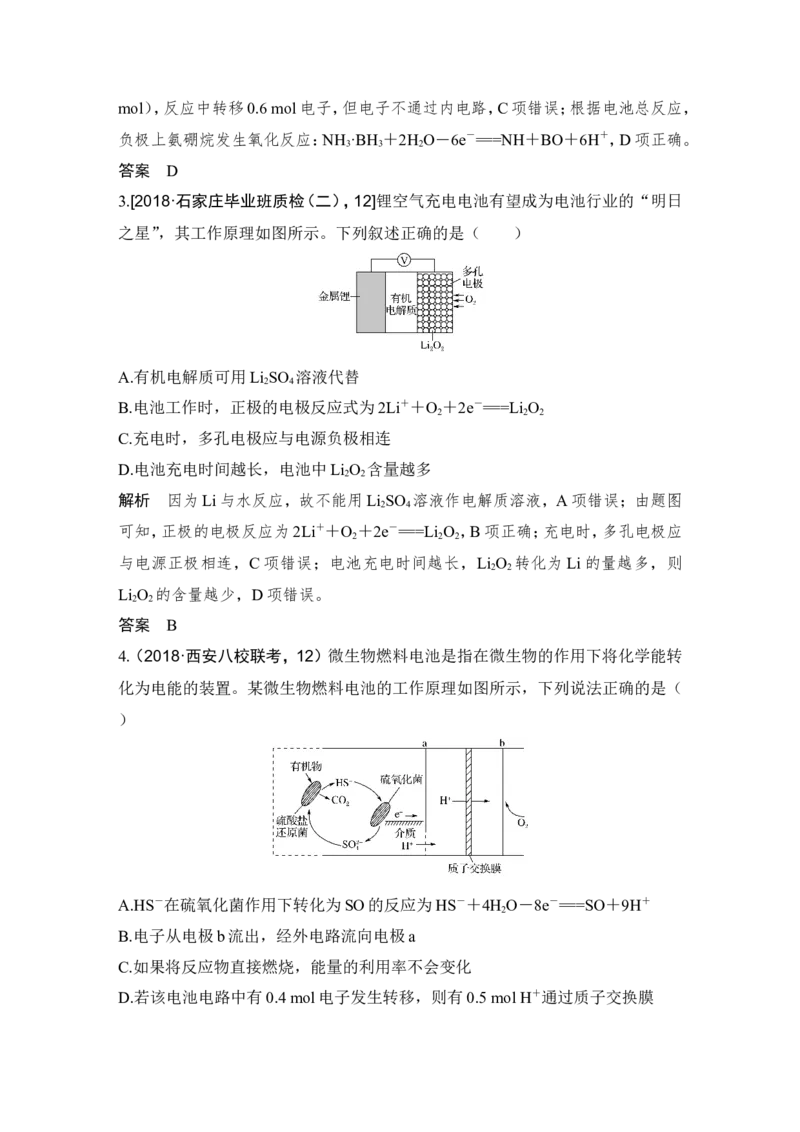
3.[2018·石家庄毕业班质检(二),12]锂空气充电电池有望成为电池行业的“明日
之星”,其工作原理如图所示。下列叙述正确的是( )
A.有机电解质可用Li SO 溶液代替
2 4
B.电池工作时,正极的电极反应式为2Li++O +2e-===Li O
2 2 2
C.充电时,多孔电极应与电源负极相连
D.电池充电时间越长,电池中Li O 含量越多
2 2
解析 因为Li与水反应,故不能用Li SO 溶液作电解质溶液,A项错误;由题图
2 4
可知,正极的电极反应为2Li++O +2e-===Li O ,B项正确;充电时,多孔电极应
2 2 2
与电源正极相连,C项错误;电池充电时间越长,Li O 转化为Li的量越多,则
2 2
Li O 的含量越少,D项错误。
2 2
答案 B
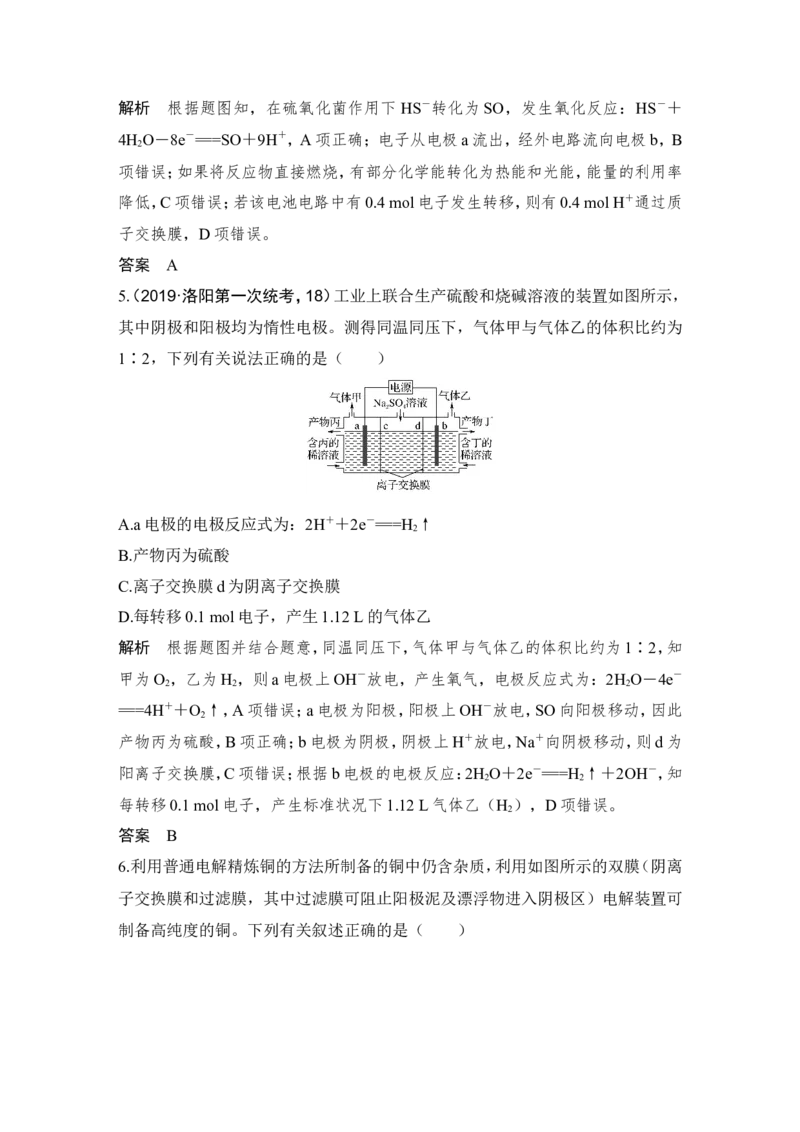
4.(2018·西安八校联考,12)微生物燃料电池是指在微生物的作用下将化学能转
化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是(
)
A.HS-在硫氧化菌作用下转化为SO的反应为HS-+4H O-8e-===SO+9H+
2
B.电子从电极b流出,经外电路流向电极a
C.如果将反应物直接燃烧,能量的利用率不会变化
D.若该电池电路中有0.4 mol电子发生转移,则有0.5 mol H+通过质子交换膜解析 根据题图知,在硫氧化菌作用下 HS-转化为SO,发生氧化反应:HS-+
4H O-8e-===SO+9H+,A项正确;电子从电极a流出,经外电路流向电极b,B
2
项错误;如果将反应物直接燃烧,有部分化学能转化为热能和光能,能量的利用率
降低,C项错误;若该电池电路中有0.4 mol电子发生转移,则有0.4 mol H+通过质
子交换膜,D项错误。
答案 A
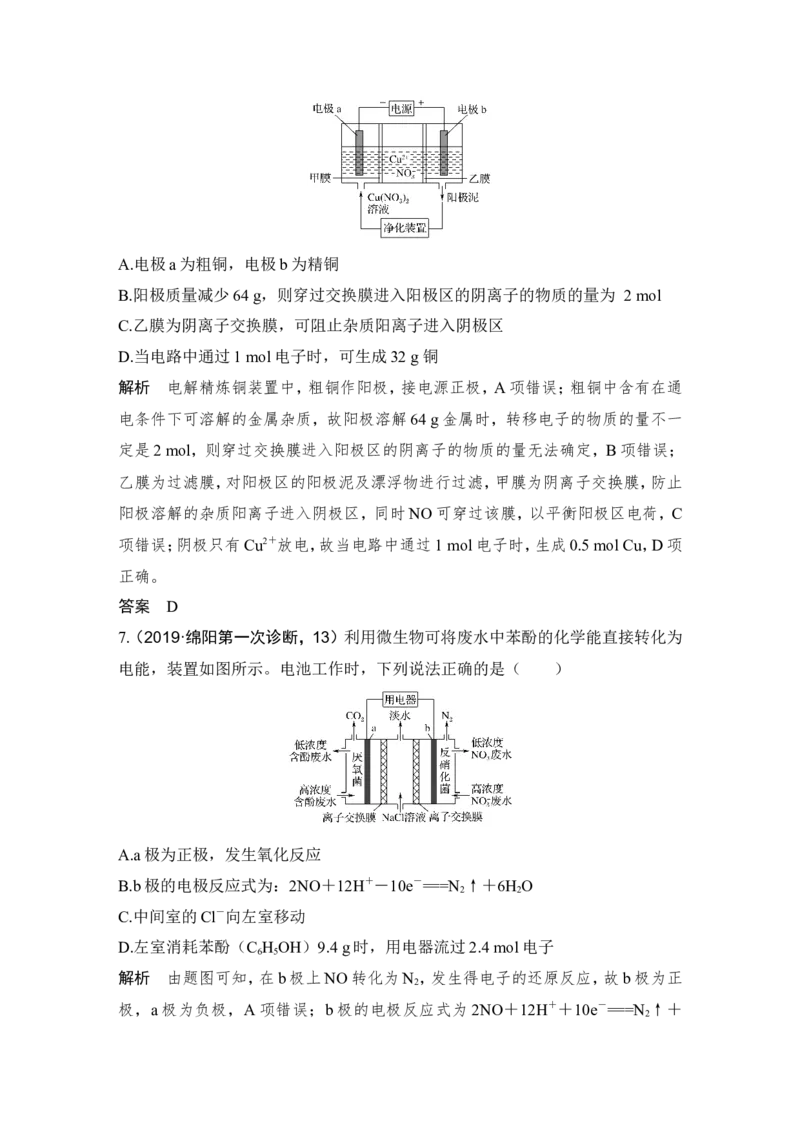
5(. 2019·洛阳第一次统考,18)工业上联合生产硫酸和烧碱溶液的装置如图所示,
其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为
1∶2,下列有关说法正确的是( )
A.a电极的电极反应式为:2H++2e-===H ↑
2
B.产物丙为硫酸
C.离子交换膜d为阴离子交换膜
D.每转移0.1 mol电子,产生1.12 L的气体乙
解析 根据题图并结合题意,同温同压下,气体甲与气体乙的体积比约为1∶2,知
甲为O ,乙为H ,则a电极上OH-放电,产生氧气,电极反应式为:2H O-4e-
2 2 2
===4H++O ↑,A项错误;a电极为阳极,阳极上OH-放电,SO向阳极移动,因此
2
产物丙为硫酸,B项正确;b电极为阴极,阴极上H+放电,Na+向阴极移动,则d为
阳离子交换膜,C项错误;根据b电极的电极反应:2H O+2e-===H ↑+2OH-,知
2 2
每转移0.1 mol电子,产生标准状况下1.12 L气体乙(H ),D项错误。
2
答案 B
6.利用普通电解精炼铜的方法所制备的铜中仍含杂质,利用如图所示的双膜(阴离
子交换膜和过滤膜,其中过滤膜可阻止阳极泥及漂浮物进入阴极区)电解装置可
制备高纯度的铜。下列有关叙述正确的是( )A.电极a为粗铜,电极b为精铜
B.阳极质量减少64 g,则穿过交换膜进入阳极区的阴离子的物质的量为 2 mol
C.乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区
D.当电路中通过1 mol电子时,可生成32 g 铜
解析 电解精炼铜装置中,粗铜作阳极,接电源正极,A项错误;粗铜中含有在通
电条件下可溶解的金属杂质,故阳极溶解64 g金属时,转移电子的物质的量不一
定是2 mol,则穿过交换膜进入阳极区的阴离子的物质的量无法确定,B项错误;
乙膜为过滤膜,对阳极区的阳极泥及漂浮物进行过滤,甲膜为阴离子交换膜,防止
阳极溶解的杂质阳离子进入阴极区,同时NO可穿过该膜,以平衡阳极区电荷,C
项错误;阴极只有Cu2+放电,故当电路中通过1 mol电子时,生成0.5 mol Cu,D项
正确。
答案 D
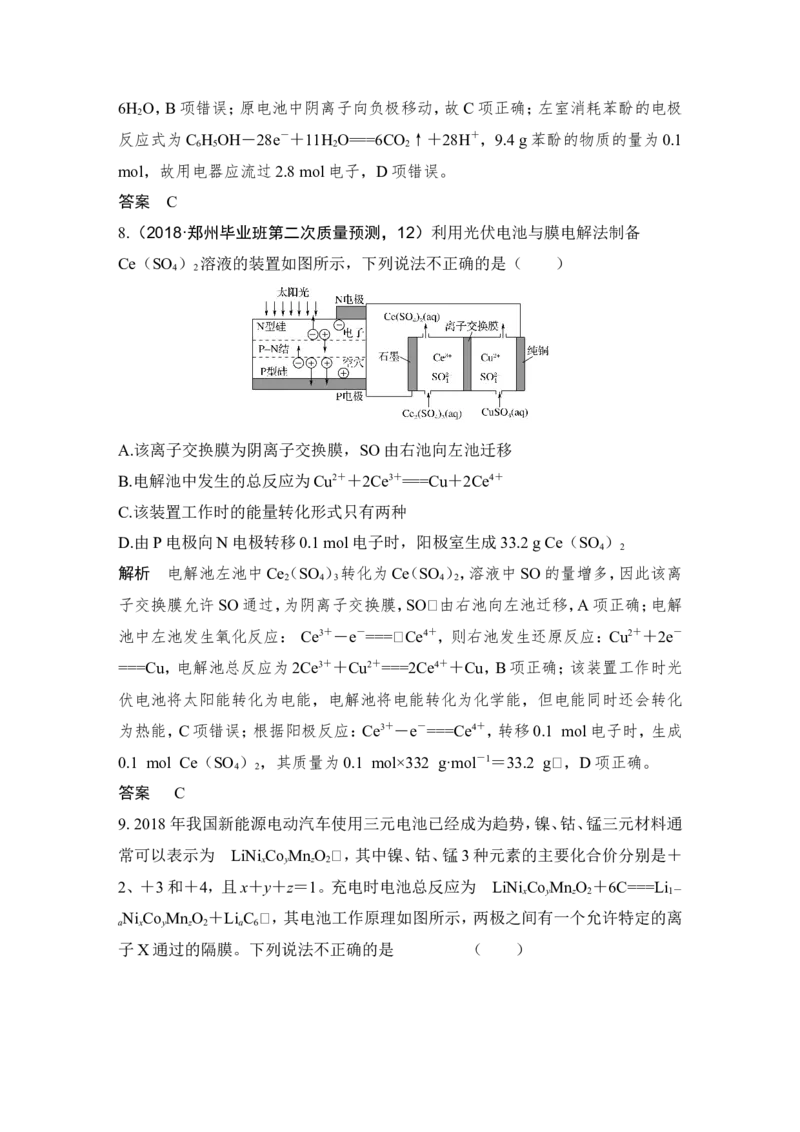
7.(2019·绵阳第一次诊断,13)利用微生物可将废水中苯酚的化学能直接转化为
电能,装置如图所示。电池工作时,下列说法正确的是( )
A.a极为正极,发生氧化反应
B.b极的电极反应式为:2NO+12H+-10e-===N ↑+6H O
2 2
C.中间室的Cl-向左室移动
D.左室消耗苯酚(C H OH)9.4 g时,用电器流过2.4 mol电子
6 5
解析 由题图可知,在b极上NO转化为N ,发生得电子的还原反应,故b极为正
2
极,a极为负极,A项错误;b极的电极反应式为2NO+12H++10e-===N ↑+
26H O,B项错误;原电池中阴离子向负极移动,故C项正确;左室消耗苯酚的电极
2
反应式为C H OH-28e-+11H O===6CO ↑+28H+,9.4 g苯酚的物质的量为0.1
6 5 2 2
mol,故用电器应流过2.8 mol电子,D项错误。
答案 C
8.(2018·郑州毕业班第二次质量预测,12)利用光伏电池与膜电解法制备
Ce(SO ) 溶液的装置如图所示,下列说法不正确的是( )
4 2
A.该离子交换膜为阴离子交换膜,SO由右池向左池迁移
B.电解池中发生的总反应为Cu2++2Ce3+===Cu+2Ce4+
C.该装置工作时的能量转化形式只有两种
D.由P电极向N电极转移0.1 mol电子时,阳极室生成33.2 g Ce(SO )
4 2
解析 电解池左池中Ce(SO )转化为Ce(SO ),溶液中SO的量增多,因此该离
2 4 3 4 2
子交换膜允许SO通过,为阴离子交换膜,SO由右池向左池迁移,A项正确;电解
池中左池发生氧化反应: Ce3+-e-===Ce4+,则右池发生还原反应:Cu2++2e-
===Cu,电解池总反应为2Ce3++Cu2+===2Ce4++Cu,B项正确;该装置工作时光
伏电池将太阳能转化为电能,电解池将电能转化为化学能,但电能同时还会转化
为热能,C项错误;根据阳极反应:Ce3+-e-===Ce4+,转移0.1 mol电子时,生成
0.1 mol Ce(SO ) ,其质量为0.1 mol×332 g·mol-1=33.2 g,D项正确。
4 2
答案 C
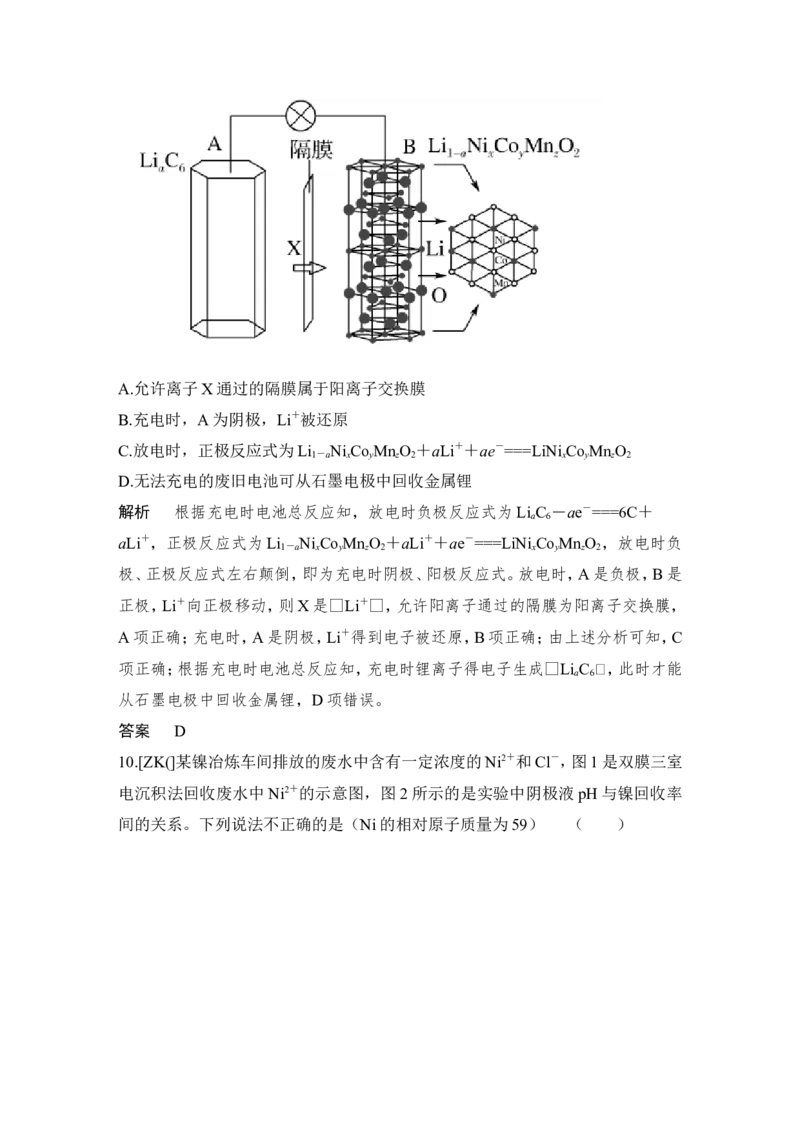
9. 2018年我国新能源电动汽车使用三元电池已经成为趋势,镍、钴、锰三元材料通
常可以表示为LiNi Co MnO ,其中镍、钴、锰3种元素的主要化合价分别是+
x y z 2
2、+3和+4,且x+y+z=1。充电时电池总反应为LiNi Co MnO +6C===Li
x y z 2 1-
Ni Co MnO +Li C ,其电池工作原理如图所示,两极之间有一个允许特定的离
a x y z 2 a 6
子X通过的隔膜。下列说法不正确的是 ( )A.允许离子X通过的隔膜属于阳离子交换膜
B.充电时,A为阴极,Li+被还原
C.放电时,正极反应式为Li Ni Co MnO +aLi++ae-===LiNi Co MnO
1-a x y z 2 x y z 2
D.无法充电的废旧电池可从石墨电极中回收金属锂
解析 根据充电时电池总反应知,放电时负极反应式为Li C -ae-===6C+
a 6
aLi+,正极反应式为Li Ni Co MnO +aLi++ae-===LiNi Co MnO ,放电时负
1-a x y z 2 x y z 2
极、正极反应式左右颠倒,即为充电时阴极、阳极反应式。放电时,A是负极,B是
正极,Li+向正极移动,则X是Li+,允许阳离子通过的隔膜为阳离子交换膜,
A项正确;充电时,A是阴极,Li+得到电子被还原,B项正确;由上述分析可知,C
项正确;根据充电时电池总反应知,充电时锂离子得电子生成Li C ,此时才能
a 6
从石墨电极中回收金属锂,D项错误。
答案 D
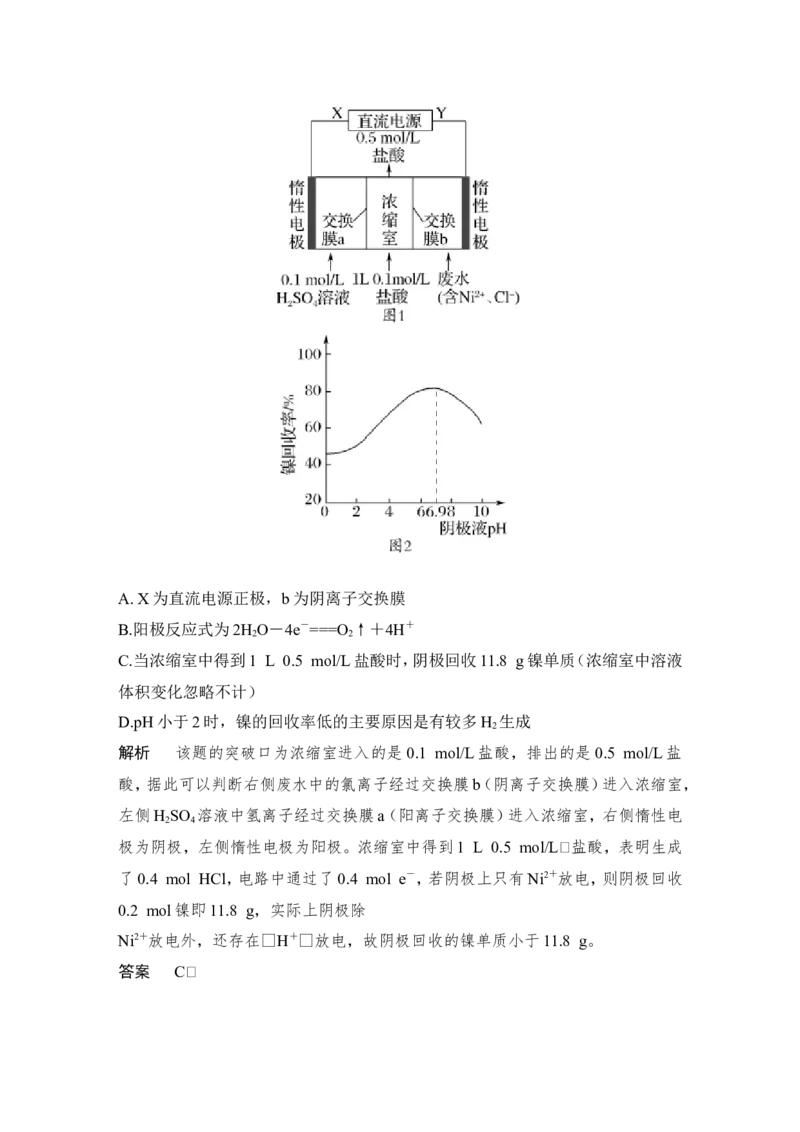
10.[ZK(]某镍冶炼车间排放的废水中含有一定浓度的Ni2+和Cl-,图1是双膜三室
电沉积法回收废水中Ni2+的示意图,图2所示的是实验中阴极液pH与镍回收率
间的关系。下列说法不正确的是(Ni的相对原子质量为59) ( )A. X为直流电源正极,b为阴离子交换膜
B.阳极反应式为2H O-4e-===O ↑+4H+
2 2
C.当浓缩室中得到1 L 0.5 mol/L盐酸时,阴极回收11.8 g镍单质(浓缩室中溶液
体积变化忽略不计)
D.pH小于2时,镍的回收率低的主要原因是有较多H 生成
2
解析 该题的突破口为浓缩室进入的是 0.1 mol/L盐酸,排出的是0.5 mol/L盐
酸,据此可以判断右侧废水中的氯离子经过交换膜b(阴离子交换膜)进入浓缩室,
左侧H SO 溶液中氢离子经过交换膜a(阳离子交换膜)进入浓缩室,右侧惰性电
2 4
极为阴极,左侧惰性电极为阳极。浓缩室中得到1 L 0.5 mol/L盐酸,表明生成
了0.4 mol HCl,电路中通过了0.4 mol e-,若阴极上只有Ni2+放电,则阴极回收
0.2 mol镍即11.8 g,实际上阴极除
Ni2+放电外,还存在H+放电,故阴极回收的镍单质小于11.8 g。
答案 C