文档内容
选择题突破四
题组一 元素推断与“位—构—性”的关系
1.(2024·北京丰台区一模)我国研究人员开发出的铝/镁/铝层压板,质量轻、耐腐蚀。下列说法不正确
的是 ( )
A.原子半径:Mg>Al
B.第一电离能:MgAl(OH)
2 3
D.氧化性:Mg2+Y>Z>W
B.原子半径:XZ
B.电负性:W>Z>X
C.配体ZW中配位原子为Z
D.Y的最高价氧化物为碱性氧化物
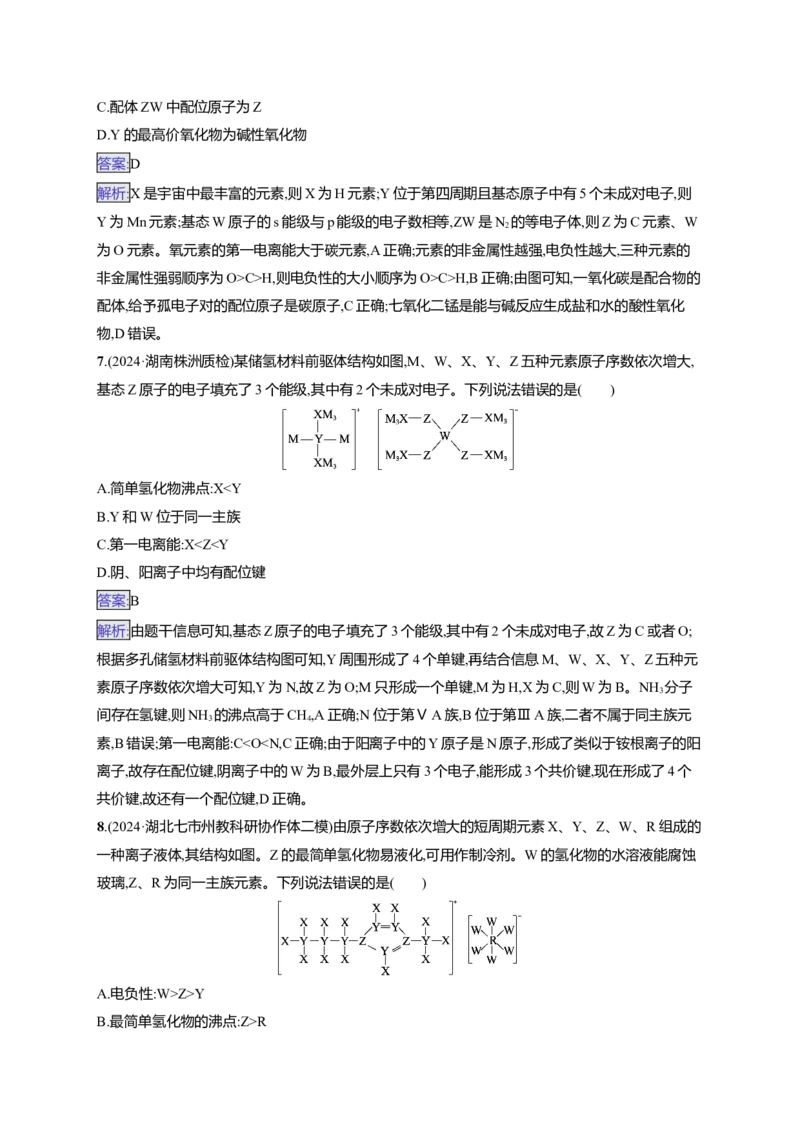
7.(2024·湖南株洲质检)某储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,
基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法错误的是( )
A.简单氢化物沸点:XZ>Y
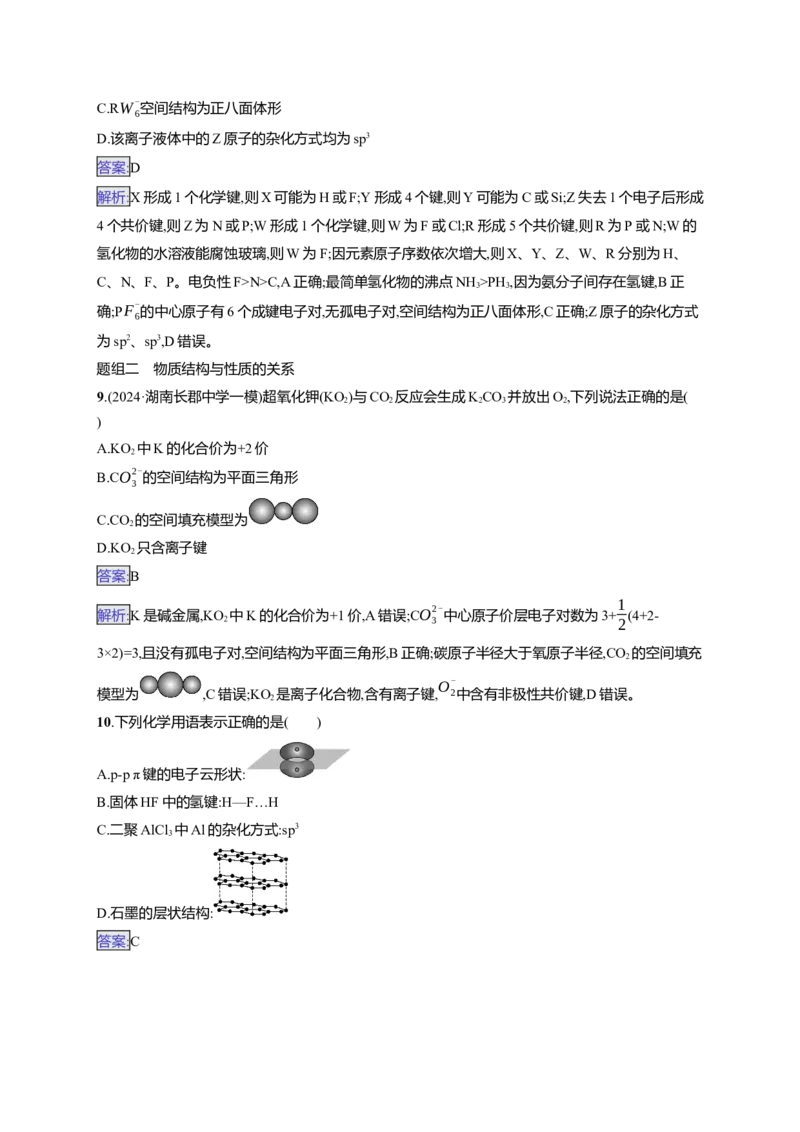
B.最简单氢化物的沸点:Z>R
C.RW-
空间结构为正八面体形
6
D.该离子液体中的Z原子的杂化方式均为sp3
题组二 物质结构与性质的关系
9.(2024·湖南长郡中学一模)超氧化钾(KO )与CO 反应会生成KCO 并放出O,下列说法正确的是(
2 2 2 3 2
)
A.KO 中K的化合价为+2价
2
B.CO2-
的空间结构为平面三角形
3C.CO 的空间填充模型为
2
D.KO 只含离子键
2
10.下列化学用语表示正确的是( )
A.p-p π键的电子云形状:
B.固体HF中的氢键:H—F…H
C.二聚AlCl 中Al的杂化方式:sp3
3
D.石墨的层状结构:
11.(2024·湖北卷)结构决定性质,性质决定用途。下列事实解释错误的是( )
选项 事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
12.(2024·湖南卷)下列有关化学概念或性质的判断错误的是( )
A.CH 分子是正四面体结构,则CHCl 没有同分异构体
4 2 2
B.环己烷与苯分子中C—H的键能相等
C.甲苯的质谱图中,质荷比为92的峰归属于
D.由R
N+与PF-
组成的离子液体常温下呈液态,与其离子的体积较大有关
4 6
13.(2024·湖南卷)Li CN 是一种高活性的人工固氮产物,其合成反应为2LiH+C+N LiCN+H ,晶
2 2 2 2 2 2
胞如图所示,下列说法错误的是( )
A.合成反应中,还原剂是LiH和C
B.晶胞中含有的Li+个数为4
C.每个CN2-
周围与它最近且距离相等的Li+有8个
2D.CN2-
为V形结构
2
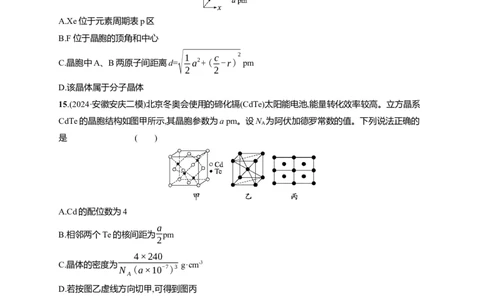
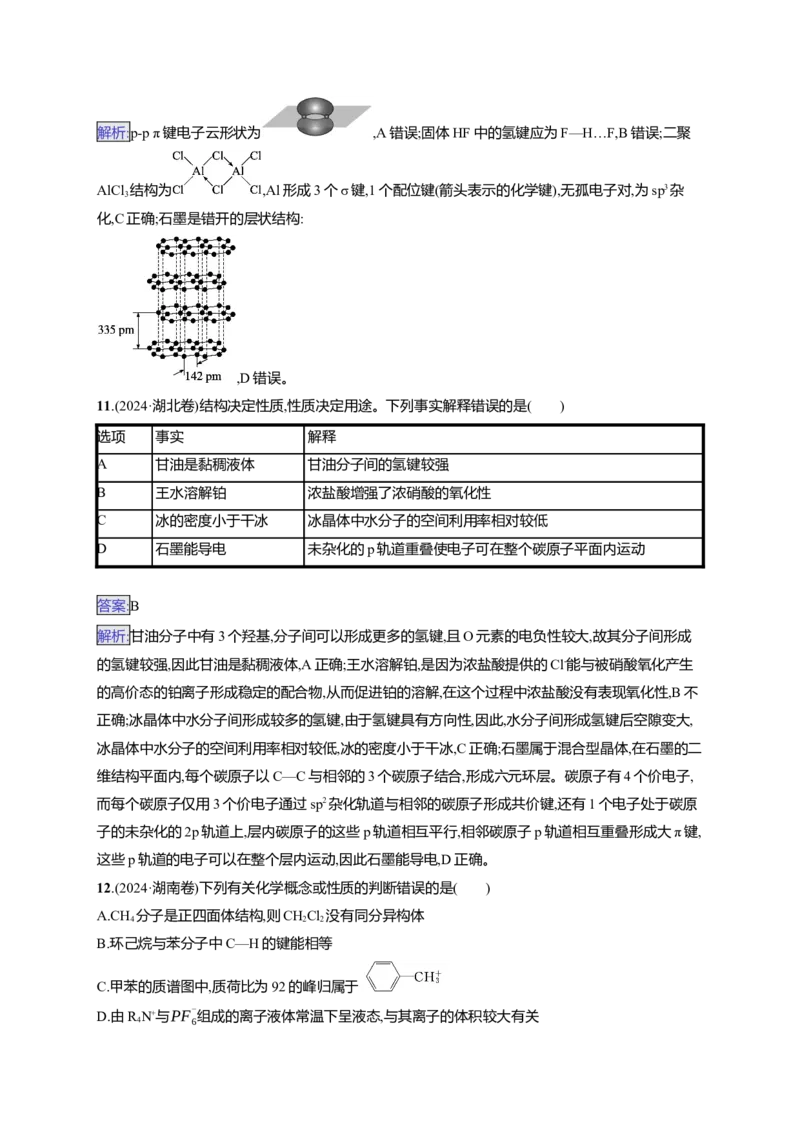
14.(2024·广东广州黄埔区二模)二氟化氙(XeF )是一种选择性良好的氟化试剂,在室温下易升华,它的
2
晶体属四方晶系,晶胞棱边夹角均为90°,晶胞参数如图所示,其中B原子的分数坐标为(0,0,r),下列说
法不正确的是( )
A.Xe位于元素周期表p区
B.F位于晶胞的顶角和中心
√1 c 2
C.晶胞中A、B两原子间距离d= a2+( -r) pm
2 2
D.该晶体属于分子晶体
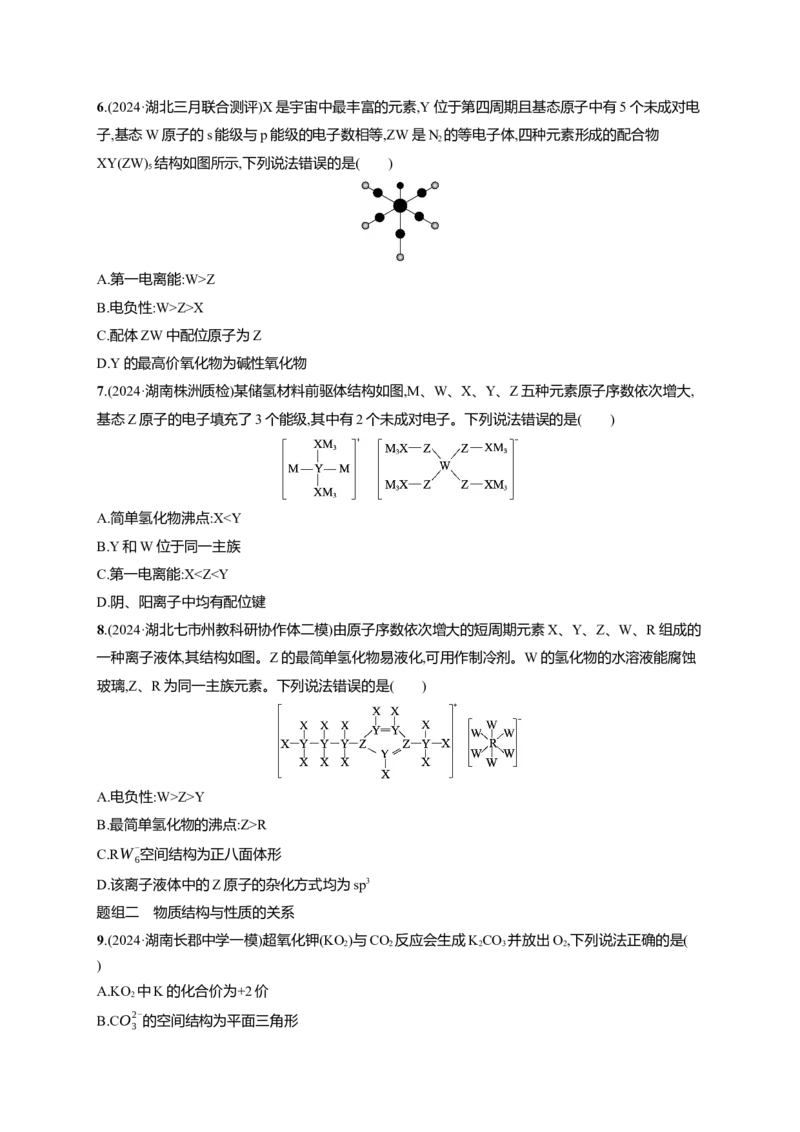
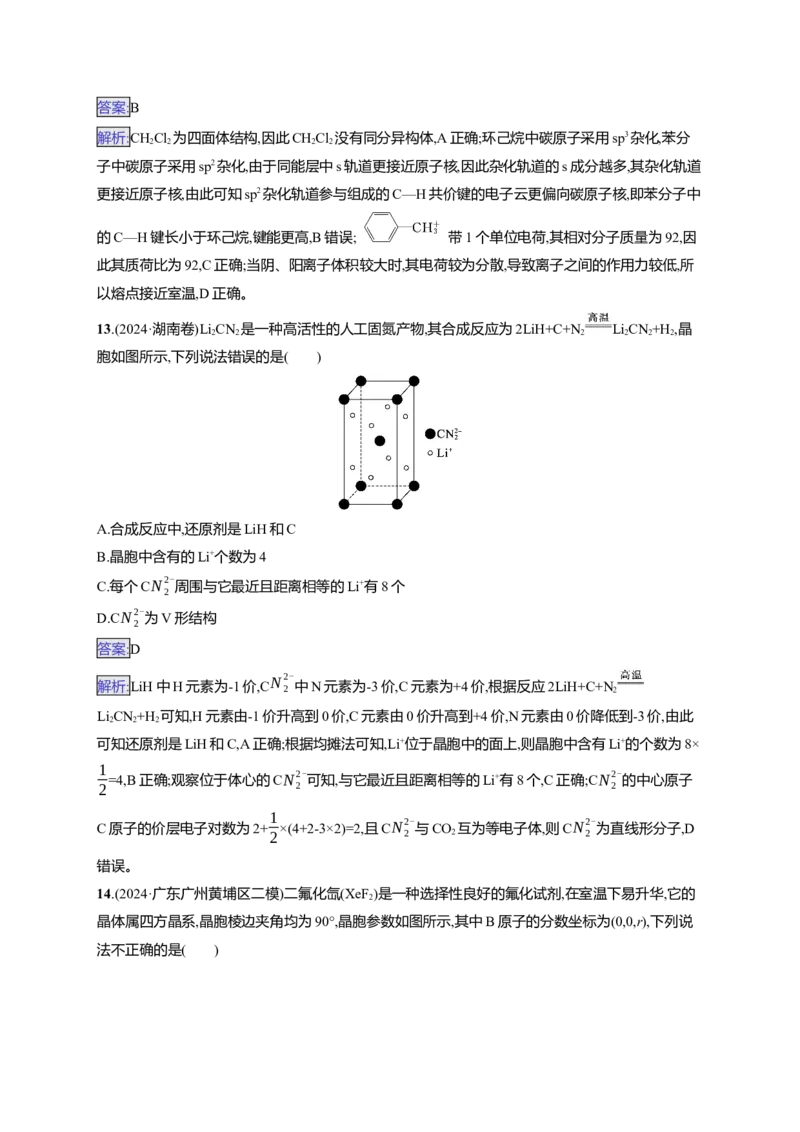
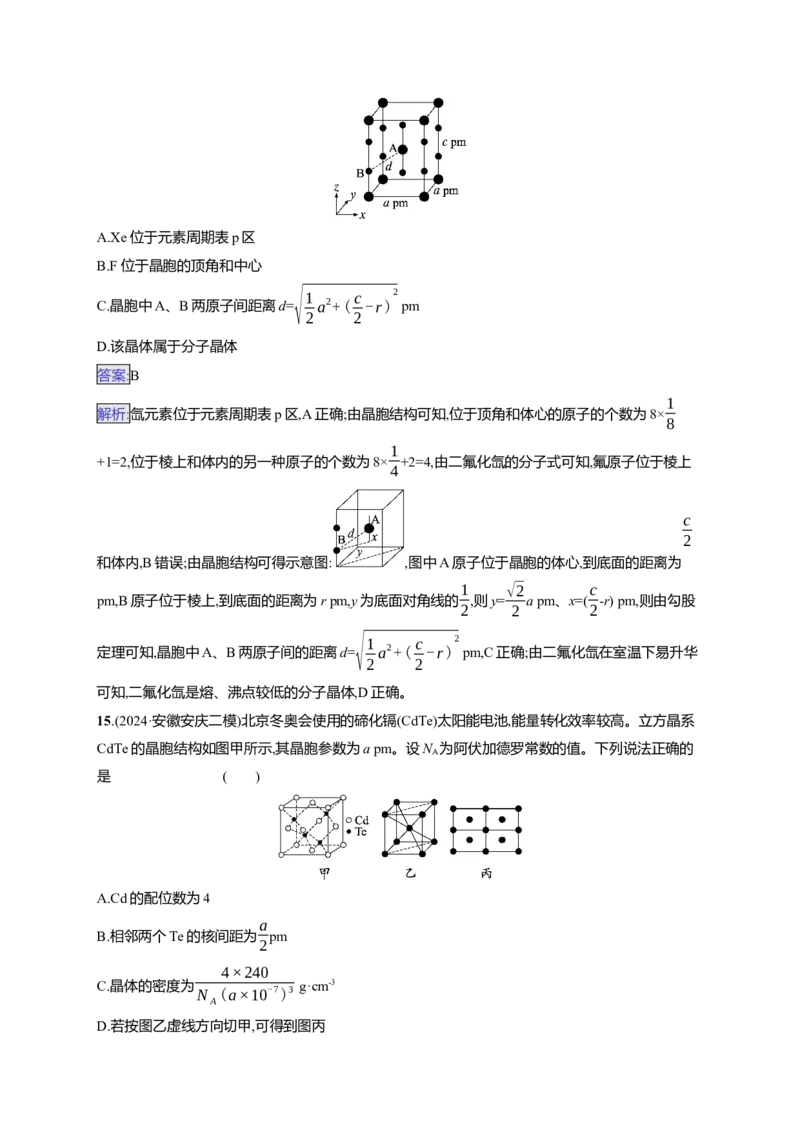
15.(2024·安徽安庆二模)北京冬奥会使用的碲化镉(CdTe)太阳能电池,能量转化效率较高。立方晶系
CdTe的晶胞结构如图甲所示,其晶胞参数为a pm。设N 为阿伏加德罗常数的值。下列说法正确的
A
是 ( )
A.Cd的配位数为4
a
B.相邻两个Te的核间距为 pm
2
4×240
C.晶体的密度为
N (a×10-7)3
g·cm-3
A
D.若按图乙虚线方向切甲,可得到图丙
选择题突破四
题组一 元素推断与“位—构—性”的关系
1.(2024·北京丰台区一模)我国研究人员开发出的铝/镁/铝层压板,质量轻、耐腐蚀。下列说法不正确
的是 ( )
A.原子半径:Mg>Al
B.第一电离能:MgAl(OH)
2 3D.氧化性:Mg2+Al,A正确;同周期元素从左到右,第一
电离能呈增大趋势,但Mg的最外层s能级为全充满状态,第一电离能:Mg>Al,B错误;同周期元素从左
到右,元素的金属性逐渐减弱,对应的最高价氧化物的水化物的碱性减弱,金属性:Mg>Al,则碱
性:Mg(OH) >Al(OH) ,C正确;金属性:Mg>Al,金属的还原性越强,对应离子的氧化性越弱,则氧化
2 3
性:Mg2+Y>Z>W
B.原子半径:XO>P>Ca,A错误;原子半径:FZ
B.电负性:W>Z>XC.配体ZW中配位原子为Z
D.Y的最高价氧化物为碱性氧化物
答案:D
解析:X是宇宙中最丰富的元素,则X为H元素;Y位于第四周期且基态原子中有5个未成对电子,则
Y为Mn元素;基态W原子的s能级与p能级的电子数相等,ZW是N 的等电子体,则Z为C元素、W
2
为O元素。氧元素的第一电离能大于碳元素,A正确;元素的非金属性越强,电负性越大,三种元素的
非金属性强弱顺序为O>C>H,则电负性的大小顺序为O>C>H,B正确;由图可知,一氧化碳是配合物的
配体,给予孤电子对的配位原子是碳原子,C正确;七氧化二锰是能与碱反应生成盐和水的酸性氧化
物,D错误。
7.(2024·湖南株洲质检)某储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,
基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法错误的是( )
A.简单氢化物沸点:XZ>Y
B.最简单氢化物的沸点:Z>RC.RW-
空间结构为正八面体形
6
D.该离子液体中的Z原子的杂化方式均为sp3
答案:D
解析:X形成1个化学键,则X可能为H或F;Y形成4个键,则Y可能为C或Si;Z失去1个电子后形成
4个共价键,则Z为N或P;W形成1个化学键,则W为F或Cl;R形成5个共价键,则R为P或N;W的
氢化物的水溶液能腐蚀玻璃,则W为F;因元素原子序数依次增大,则X、Y、Z、W、R分别为H、
C、N、F、P。电负性F>N>C,A正确;最简单氢化物的沸点NH >PH,因为氨分子间存在氢键,B正
3 3
确;PF-
的中心原子有6个成键电子对,无孤电子对,空间结构为正八面体形,C正确;Z原子的杂化方式
6
为sp2、sp3,D错误。
题组二 物质结构与性质的关系
9.(2024·湖南长郡中学一模)超氧化钾(KO )与CO 反应会生成KCO 并放出O,下列说法正确的是(
2 2 2 3 2
)
A.KO 中K的化合价为+2价
2
B.CO2-
的空间结构为平面三角形
3
C.CO 的空间填充模型为
2
D.KO 只含离子键
2
答案:B
1
解析:K是碱金属,KO
中K的化合价为+1价,A错误;CO2-
中心原子价层电子对数为3+ (4+2-
2 3 2
3×2)=3,且没有孤电子对,空间结构为平面三角形,B正确;碳原子半径大于氧原子半径,CO 的空间填充
2
O-
模型为 ,C错误;KO 是离子化合物,含有离子键, 2中含有非极性共价键,D错误。
2
10.下列化学用语表示正确的是( )
A.p-p π键的电子云形状:
B.固体HF中的氢键:H—F…H
C.二聚AlCl 中Al的杂化方式:sp3
3
D.石墨的层状结构:
答案:C解析:p-p π键电子云形状为 ,A错误;固体HF中的氢键应为F—H…F,B错误;二聚
AlCl 结构为 ,Al形成3个σ键,1个配位键(箭头表示的化学键),无孤电子对,为sp3杂
3
化,C正确;石墨是错开的层状结构:
,D错误。
11.(2024·湖北卷)结构决定性质,性质决定用途。下列事实解释错误的是( )
选项 事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
答案:B
解析:甘油分子中有3个羟基,分子间可以形成更多的氢键,且O元素的电负性较大,故其分子间形成
的氢键较强,因此甘油是黏稠液体,A正确;王水溶解铂,是因为浓盐酸提供的Cl-能与被硝酸氧化产生
的高价态的铂离子形成稳定的配合物,从而促进铂的溶解,在这个过程中浓盐酸没有表现氧化性,B不
正确;冰晶体中水分子间形成较多的氢键,由于氢键具有方向性,因此,水分子间形成氢键后空隙变大,
冰晶体中水分子的空间利用率相对较低,冰的密度小于干冰,C正确;石墨属于混合型晶体,在石墨的二
维结构平面内,每个碳原子以C—C与相邻的3个碳原子结合,形成六元环层。碳原子有4个价电子,
而每个碳原子仅用3个价电子通过sp2杂化轨道与相邻的碳原子形成共价键,还有1个电子处于碳原
子的未杂化的2p轨道上,层内碳原子的这些p轨道相互平行,相邻碳原子p轨道相互重叠形成大π键,
这些p轨道的电子可以在整个层内运动,因此石墨能导电,D正确。
12.(2024·湖南卷)下列有关化学概念或性质的判断错误的是( )
A.CH 分子是正四面体结构,则CHCl 没有同分异构体
4 2 2
B.环己烷与苯分子中C—H的键能相等
C.甲苯的质谱图中,质荷比为92的峰归属于
D.由R
N+与PF-
组成的离子液体常温下呈液态,与其离子的体积较大有关
4 6答案:B
解析:CHCl 为四面体结构,因此CHCl 没有同分异构体,A正确;环己烷中碳原子采用sp3杂化,苯分
2 2 2 2
子中碳原子采用sp2杂化,由于同能层中s轨道更接近原子核,因此杂化轨道的s成分越多,其杂化轨道
更接近原子核,由此可知sp2杂化轨道参与组成的C—H共价键的电子云更偏向碳原子核,即苯分子中
的C—H键长小于环己烷,键能更高,B错误; 带1个单位电荷,其相对分子质量为92,因
此其质荷比为92,C正确;当阴、阳离子体积较大时,其电荷较为分散,导致离子之间的作用力较低,所
以熔点接近室温,D正确。
13.(2024·湖南卷)Li CN 是一种高活性的人工固氮产物,其合成反应为2LiH+C+N LiCN+H ,晶
2 2 2 2 2 2
胞如图所示,下列说法错误的是( )
A.合成反应中,还原剂是LiH和C
B.晶胞中含有的Li+个数为4
C.每个CN2-
周围与它最近且距离相等的Li+有8个
2
D.CN2-
为V形结构
2
答案:D
N2-
解析:LiH中H元素为-1价,C
2
中N元素为-3价,C元素为+4价,根据反应2LiH+C+N
2
LiCN+H 可知,H元素由-1价升高到0价,C元素由0价升高到+4价,N元素由0价降低到-3价,由此
2 2 2
可知还原剂是LiH和C,A正确;根据均摊法可知,Li+位于晶胞中的面上,则晶胞中含有Li+的个数为8×
1
=4,B正确;观察位于体心的CN2- 可知,与它最近且距离相等的Li+有8个,C正确;CN2-
的中心原子
2 2 2
1
C原子的价层电子对数为2+
×(4+2-3×2)=2,且CN2-
与CO
互为等电子体,则CN2-
为直线形分子,D
2 2 2 2
错误。
14.(2024·广东广州黄埔区二模)二氟化氙(XeF )是一种选择性良好的氟化试剂,在室温下易升华,它的
2
晶体属四方晶系,晶胞棱边夹角均为90°,晶胞参数如图所示,其中B原子的分数坐标为(0,0,r),下列说
法不正确的是( )A.Xe位于元素周期表p区
B.F位于晶胞的顶角和中心
√1 c 2
C.晶胞中A、B两原子间距离d= a2+( -r) pm
2 2
D.该晶体属于分子晶体
答案:B
1
解析:氙元素位于元素周期表p区,A正确;由晶胞结构可知,位于顶角和体心的原子的个数为8×
8
1
+1=2,位于棱上和体内的另一种原子的个数为8× +2=4,由二氟化氙的分子式可知,氟原子位于棱上
4
c
2
和体内,B错误;由晶胞结构可得示意图: ,图中A原子位于晶胞的体心,到底面的距离为
1 √2 c
pm,B原子位于棱上,到底面的距离为r pm,y为底面对角线的 ,则y= a pm、x=( -r) pm,则由勾股
2 2 2
√1 c 2
定理可知,晶胞中A、B两原子间的距离d= a2+( -r) pm,C正确;由二氟化氙在室温下易升华
2 2
可知,二氟化氙是熔、沸点较低的分子晶体,D正确。
15.(2024·安徽安庆二模)北京冬奥会使用的碲化镉(CdTe)太阳能电池,能量转化效率较高。立方晶系
CdTe的晶胞结构如图甲所示,其晶胞参数为a pm。设N 为阿伏加德罗常数的值。下列说法正确的
A
是 ( )
A.Cd的配位数为4
a
B.相邻两个Te的核间距为 pm
2
4×240
C.晶体的密度为
N (a×10-7)3
g·cm-3
A
D.若按图乙虚线方向切甲,可得到图丙答案:A
解析:由图甲所示信息可知,Cd位于晶胞8个顶角和6个面心,Te位于晶胞体内,故Cd的配位数即离
某个Cd原子距离相等且最近的Te原子个数为4,A正确;由图甲可知,相邻两个Te的核间距为面对角
√2 1 1
线的一半即为 a pm,B错误;由图甲可知,一个晶胞中含有Cd的数目为8× +6× =4,含有Te原子
2 8 2
4×(112+128)
的数目为4,故一个晶胞的质量为 g,晶胞参数为a pm,则一个晶胞的体积为(a×10-10)3
N
A
4×240
cm3,故晶体的密度为
N (a×10-10)3
g·cm-3,C错误;若按图乙虚线方向切甲,由于体心没有原子,不
A
能得到图丙,D错误。