文档内容
10.多平衡体系图像及分析
1.(2024·浙江温州一模)已知HCOOH水溶液在密封石英管中的分解反应:
Ⅰ.HCOOH CO+HO K
2 1
Ⅱ.HCOOH CO+H K
2 2 2
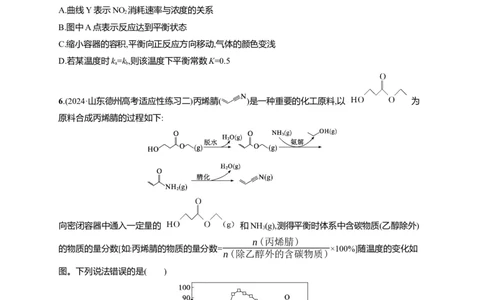
T温度下,在密封石英管内完全充满1.0 mol·L-1 HCOOH水溶液,使HCOOH分解,分解产物均完全溶
于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列有关说法
不正确的是( )
A.混合体系达平衡后:c(CO)·c(H )>c(CO)
2 2
B.活化能:反应Ⅰ<反应Ⅱ
C.c(CO)浓度变小的原因是CO 的生成导致反应Ⅰ平衡逆向移动
2
D.c(HCOOH)可降为0
2.(2024·江苏泰州一模调研)二甲醚和水蒸气制氢气可作为燃料电池的氢能源,发生的主要反应如下:
反应Ⅰ CHOCH (g)+HO(g) 2CHOH(g) ΔH>0
3 3 2 3 1
反应Ⅱ CHOH+H O(g) CO(g)+3H(g) ΔH>0
3 2 2 2 2
反应Ⅲ CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2 3
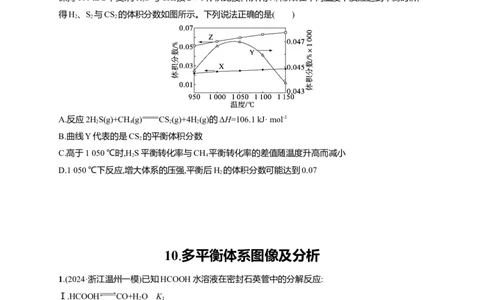
在恒压下,将一定比例的二甲醚和水蒸气混合后,以一定流速通过装有催化剂的反应器,反应相同时间
测得的CHOCH 实际转化率、CO 实际选择性与CO 平衡选择性随温度的变化如图所示。CO 的选
3 3 2 2 2
n (CO )
生成 2
择性= ×100%。下列说法不正确的是( )
2n (CH OCH )
反应 3 3
A.曲线a表示CHOCH 实际转化率随温度的变化
3 3
B.200 ℃时,反应Ⅱ的速率大于反应Ⅲ的速率
n (H O)
起始 2
C.适当增加 ,有利于提高H 的产率
n (CH OCH ) 2
起始 3 3D.一定温度下,若增大压强,CO的平衡产量不变
3.(2024·黑龙江大庆实验中学模拟)某温度下,向V L恒容密闭容器中通入4 mol X(g),发生反应:
①2X(g) Y(g)+4Z(g),②2Z(g) M(g)。反应体系中X、Y、Z的物质的量随时间t的变化曲线
如图所示。下列说法错误的是( )
A.25 min时,生成了3.2 mol M
0.32
B.0~10 min内,气体X的平均反应速率为 mol·L-1· min-1
V
C.该温度下,反应②的平衡常数K=2V
D.25 min时保持其他条件不变,再向体系中通入1 mol Y(g)后,反应②的平衡不移动
4.(2024·江苏盐城一模)CHOH可作大型船舶的绿色燃料。工业上用CO 制备CHOH的原理如下:
3 2 3
反应1:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49.5 kJ·mol-1
2 2 3 2 1
反应2:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2 2
分别在3 MPa、5 MPa下,将n (CO)∶n (H )=1∶3的混合气体置于密闭容器中,若仅考虑上述反
起始 2 起始 2
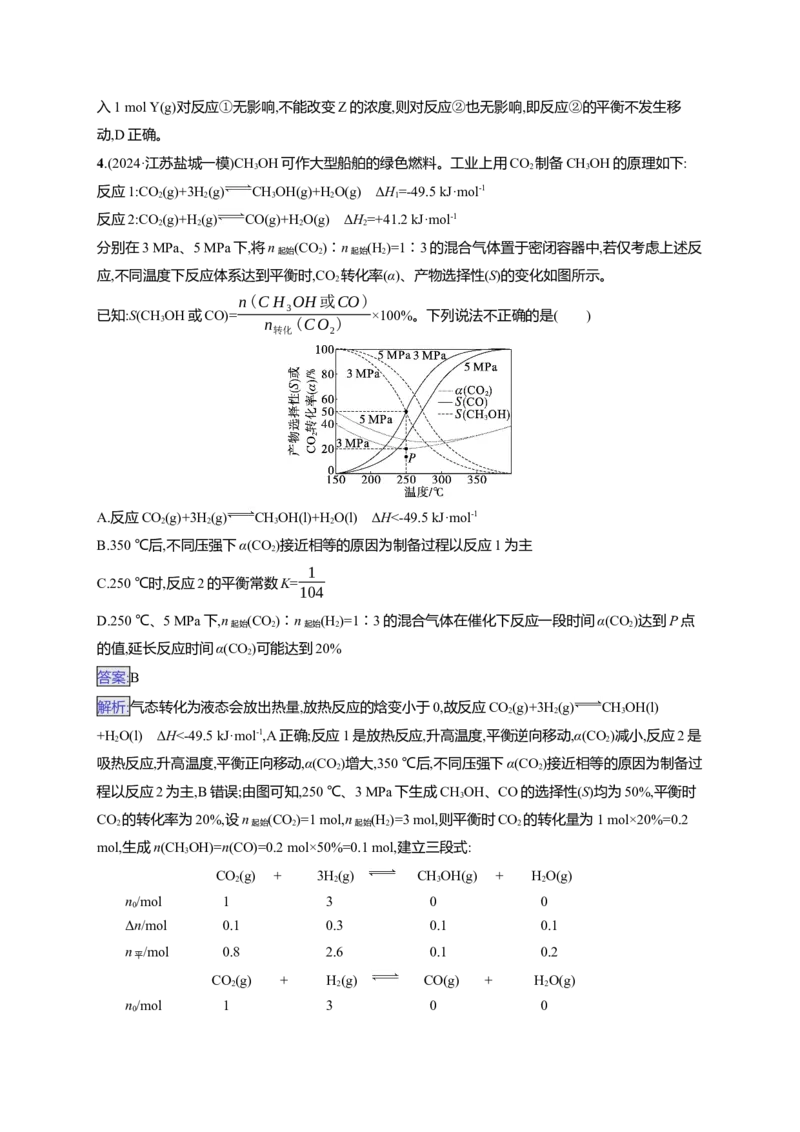
应,不同温度下反应体系达到平衡时,CO 转化率(α)、产物选择性(S)的变化如图所示。
2
n(CH OH或CO)
3
已知:S(CHOH或CO)= ×100%。下列说法不正确的是( )
3 n (CO )
转化 2
A.反应CO(g)+3H(g) CHOH(l)+H O(l) ΔH<-49.5 kJ·mol-1
2 2 3 2
B.350 ℃后,不同压强下α(CO)接近相等的原因为制备过程以反应1为主
2
1
C.250 ℃时,反应2的平衡常数K=
104
D.250 ℃、5 MPa下,n (CO)∶n (H )=1∶3的混合气体在催化下反应一段时间α(CO)达到P点
起始 2 起始 2 2
的值,延长反应时间α(CO)可能达到20%
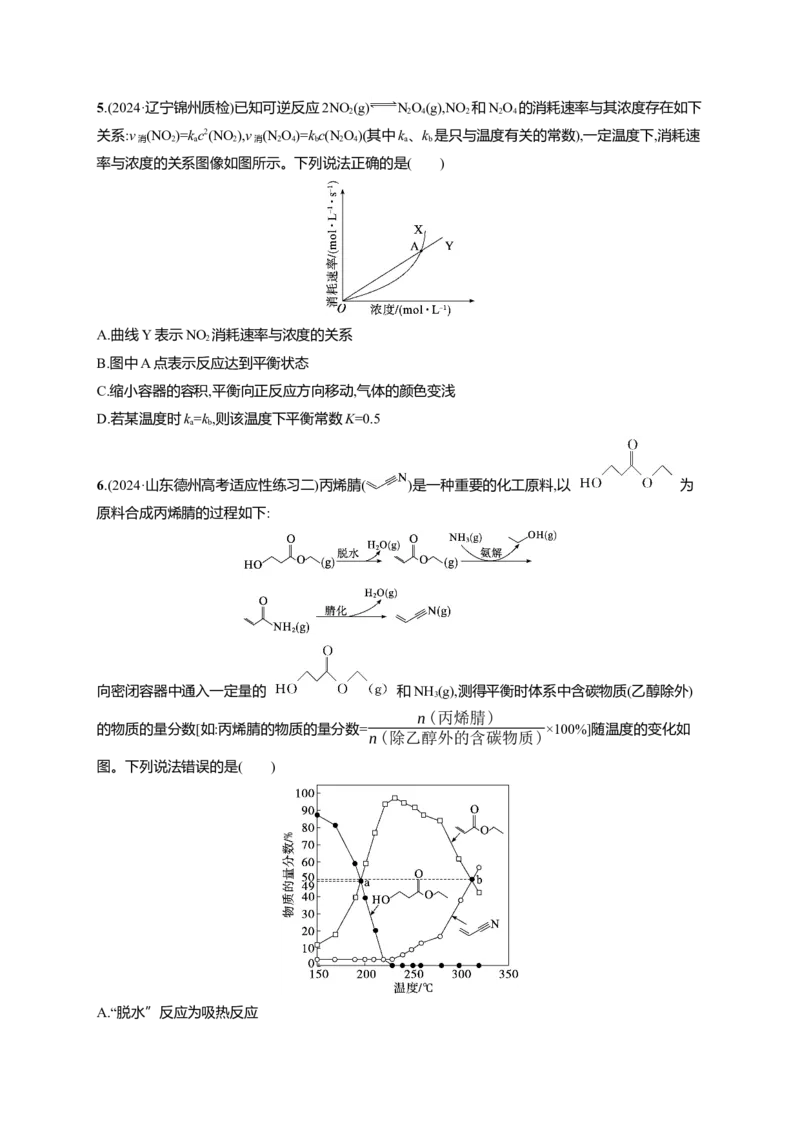
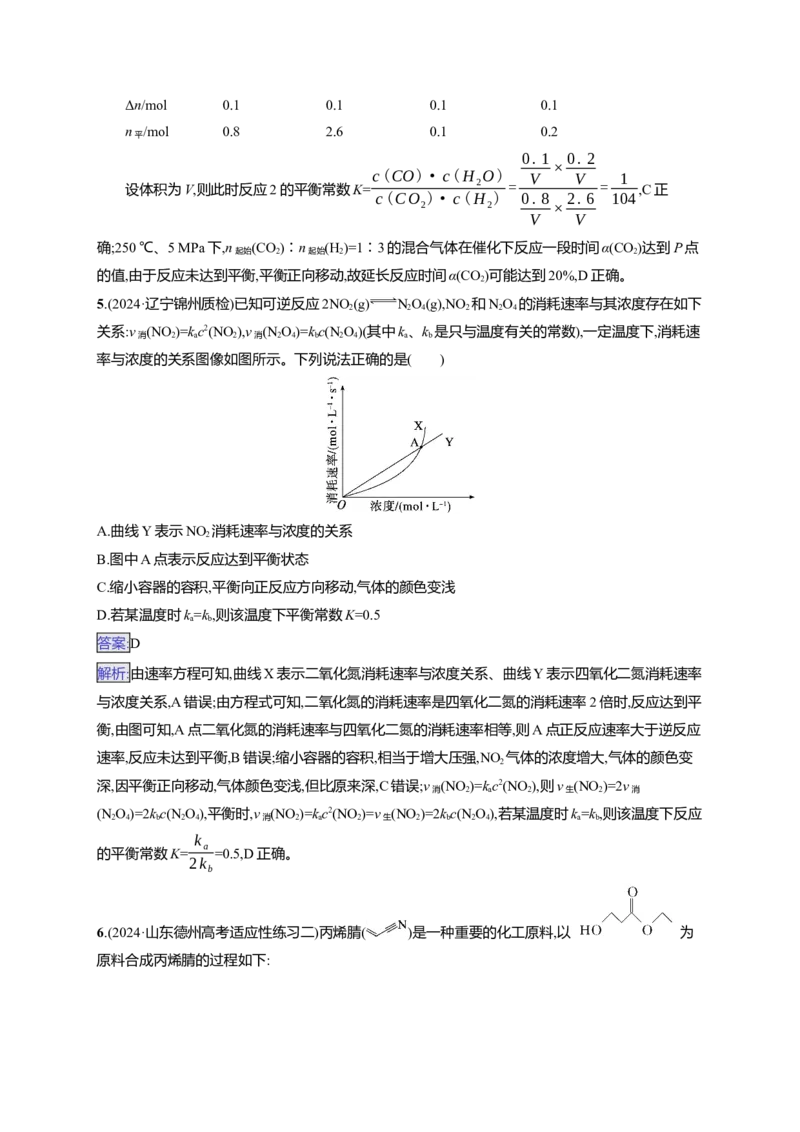
25.(2024·辽宁锦州质检)已知可逆反应2NO (g) NO(g),NO 和NO 的消耗速率与其浓度存在如下
2 2 4 2 2 4
关系:v (NO )=kc2(NO ),v (N O)=kc(N O)(其中k、k 是只与温度有关的常数),一定温度下,消耗速
消 2 a 2 消 2 4 b 2 4 a b
率与浓度的关系图像如图所示。下列说法正确的是( )
A.曲线Y表示NO 消耗速率与浓度的关系
2
B.图中A点表示反应达到平衡状态
C.缩小容器的容积,平衡向正反应方向移动,气体的颜色变浅
D.若某温度时k=k,则该温度下平衡常数K=0.5
a b
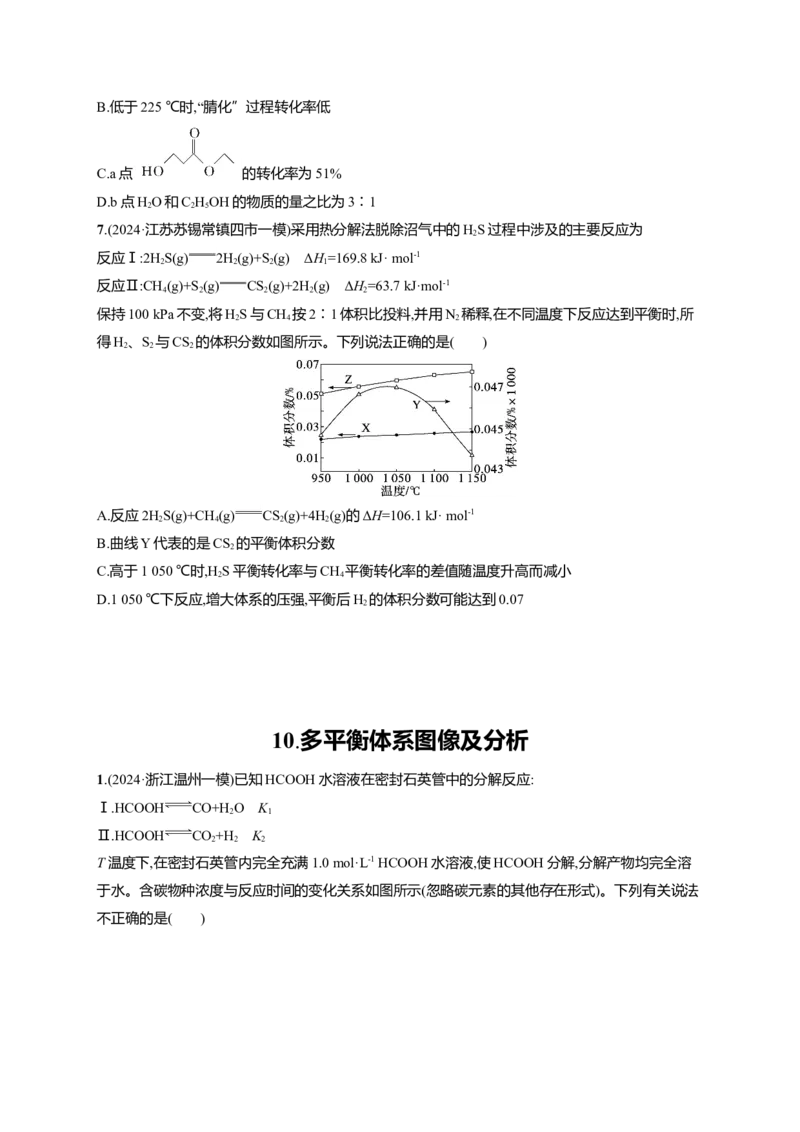
6.(2024·山东德州高考适应性练习二)丙烯腈( )是一种重要的化工原料,以 为
原料合成丙烯腈的过程如下:
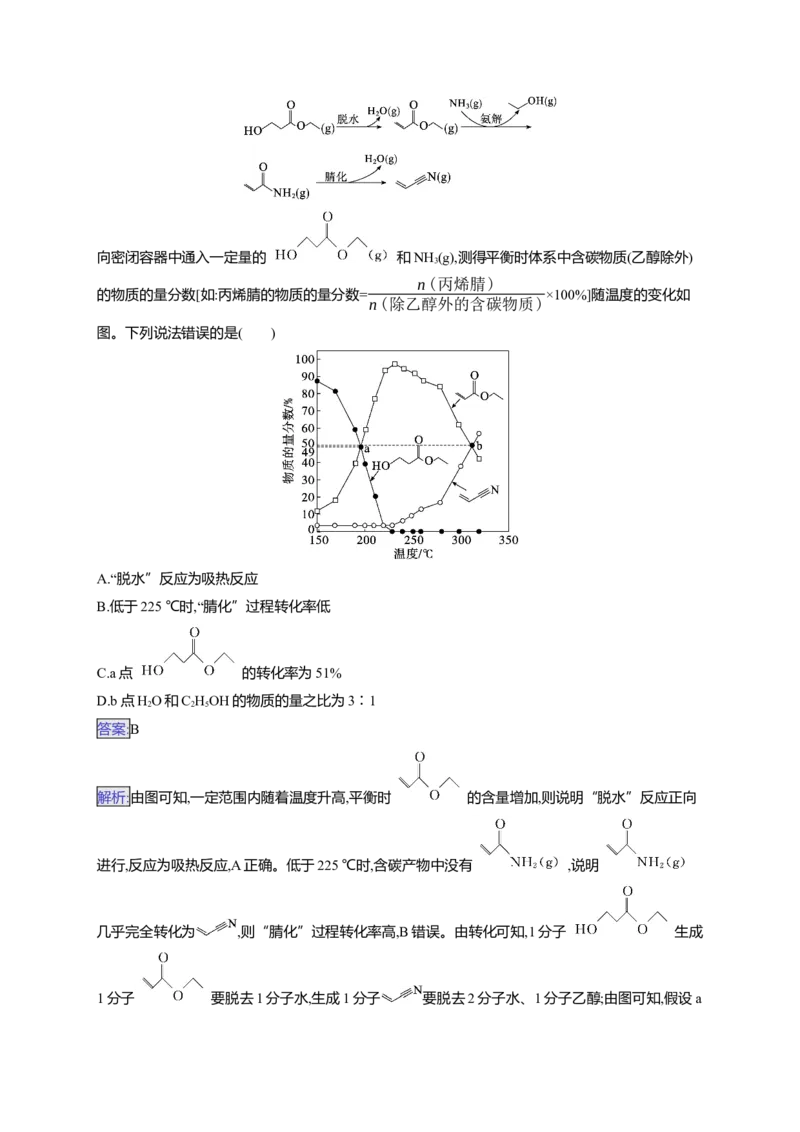
向密闭容器中通入一定量的 和NH (g),测得平衡时体系中含碳物质(乙醇除外)
3
n(丙烯腈)
的物质的量分数[如:丙烯腈的物质的量分数= ×100%]随温度的变化如
n(除乙醇外的含碳物质)
图。下列说法错误的是( )
A.“脱水”反应为吸热反应B.低于225 ℃时,“腈化”过程转化率低
C.a点 的转化率为51%
D.b点HO和C HOH的物质的量之比为3∶1
2 2 5
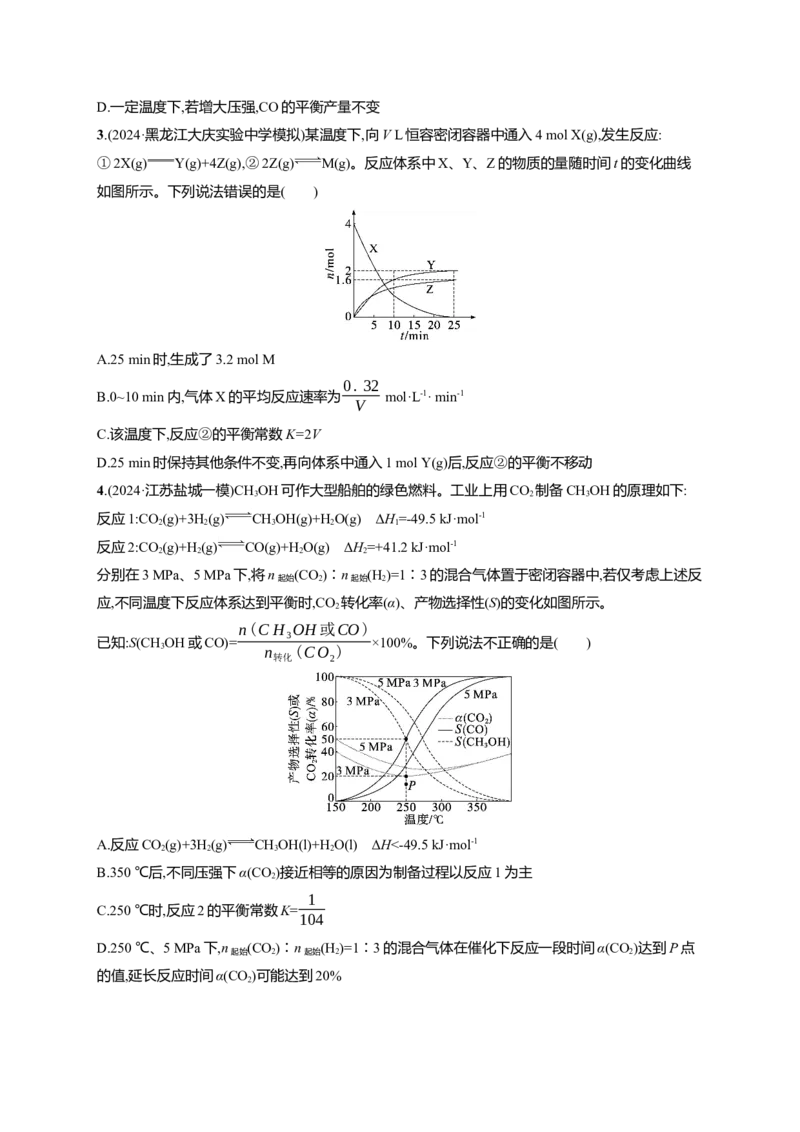
7.(2024·江苏苏锡常镇四市一模)采用热分解法脱除沼气中的HS过程中涉及的主要反应为
2
反应Ⅰ:2H S(g) 2H(g)+S (g) ΔH=169.8 kJ· mol-1
2 2 2 1
反应Ⅱ:CH (g)+S (g) CS(g)+2H(g) ΔH=63.7 kJ·mol-1
4 2 2 2 2
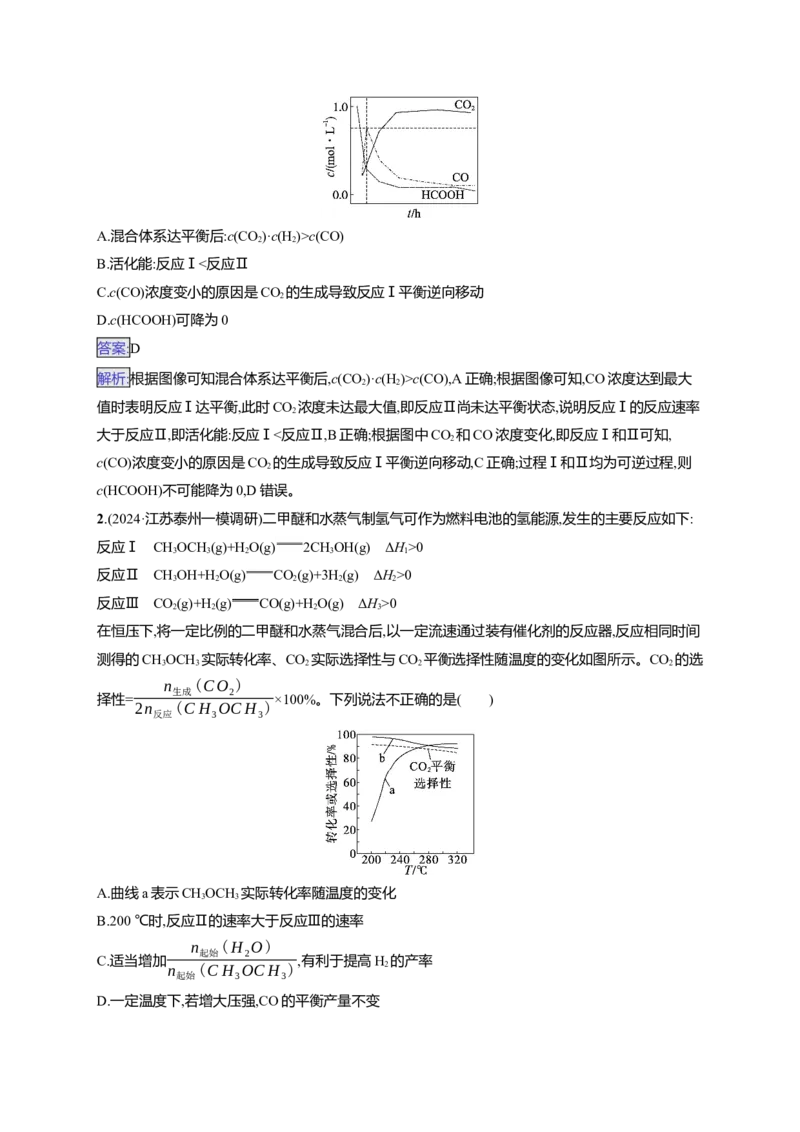
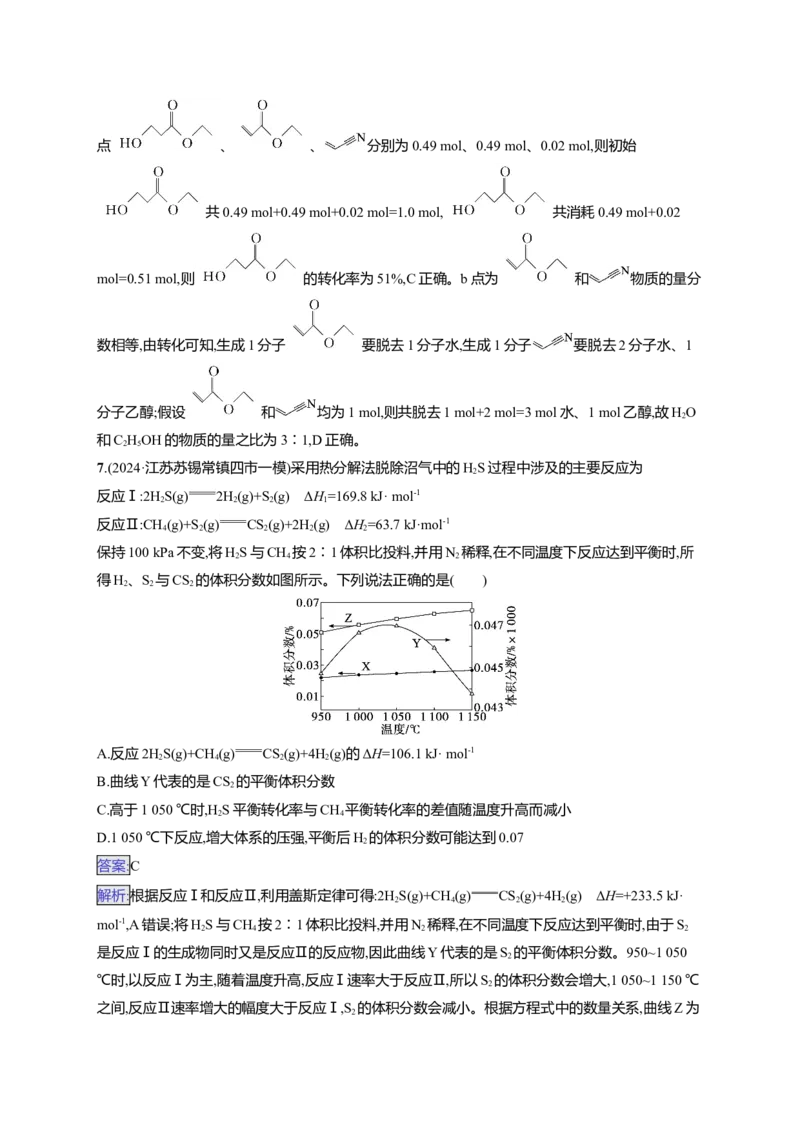
保持100 kPa不变,将HS与CH 按2∶1体积比投料,并用N 稀释,在不同温度下反应达到平衡时,所
2 4 2
得H、S 与CS 的体积分数如图所示。下列说法正确的是( )
2 2 2
A.反应2HS(g)+CH(g) CS(g)+4H(g)的ΔH=106.1 kJ· mol-1
2 4 2 2
B.曲线Y代表的是CS 的平衡体积分数
2
C.高于1 050 ℃时,H S平衡转化率与CH 平衡转化率的差值随温度升高而减小
2 4
D.1 050 ℃下反应,增大体系的压强,平衡后H 的体积分数可能达到0.07
2
10.多平衡体系图像及分析
1.(2024·浙江温州一模)已知HCOOH水溶液在密封石英管中的分解反应:
Ⅰ.HCOOH CO+HO K
2 1
Ⅱ.HCOOH CO+H K
2 2 2
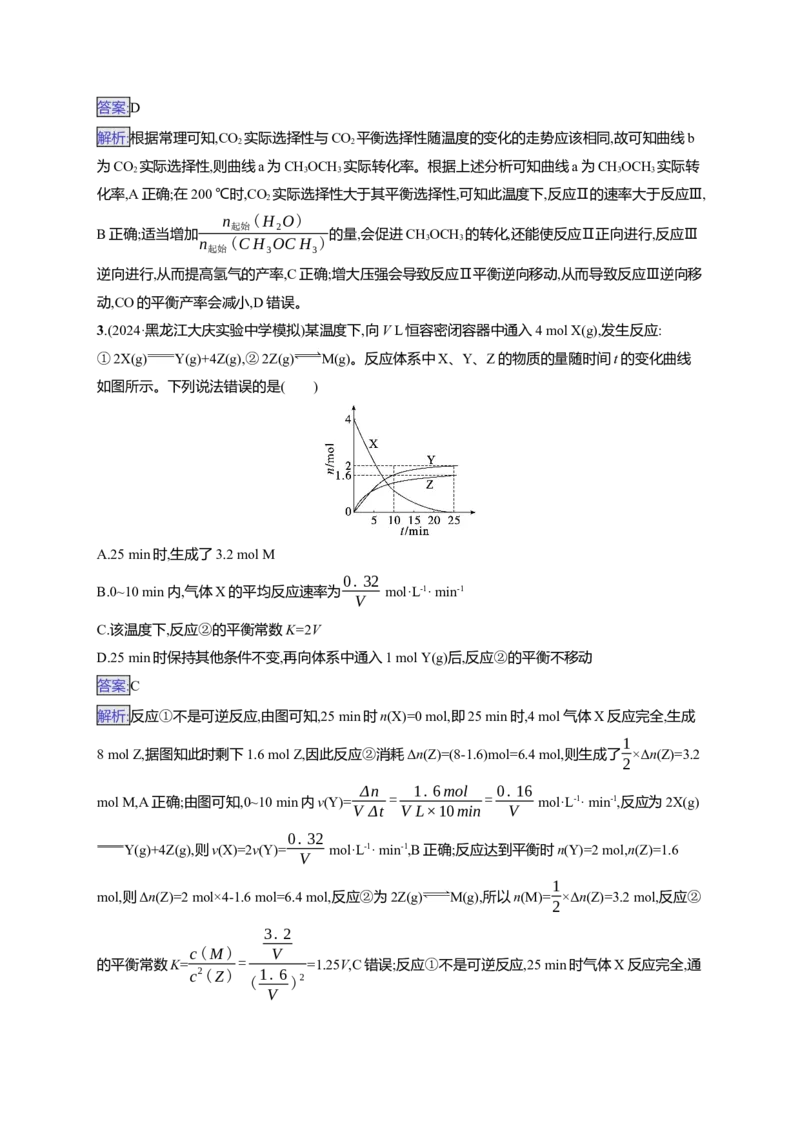
T温度下,在密封石英管内完全充满1.0 mol·L-1 HCOOH水溶液,使HCOOH分解,分解产物均完全溶
于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列有关说法
不正确的是( )A.混合体系达平衡后:c(CO)·c(H )>c(CO)
2 2
B.活化能:反应Ⅰ<反应Ⅱ
C.c(CO)浓度变小的原因是CO 的生成导致反应Ⅰ平衡逆向移动
2
D.c(HCOOH)可降为0
答案:D
解析:根据图像可知混合体系达平衡后,c(CO)·c(H )>c(CO),A正确;根据图像可知,CO浓度达到最大
2 2
值时表明反应Ⅰ达平衡,此时CO 浓度未达最大值,即反应Ⅱ尚未达平衡状态,说明反应Ⅰ的反应速率
2
大于反应Ⅱ,即活化能:反应Ⅰ<反应Ⅱ,B正确;根据图中CO 和CO浓度变化,即反应Ⅰ和Ⅱ可知,
2
c(CO)浓度变小的原因是CO 的生成导致反应Ⅰ平衡逆向移动,C正确;过程Ⅰ和Ⅱ均为可逆过程,则
2
c(HCOOH)不可能降为0,D错误。
2.(2024·江苏泰州一模调研)二甲醚和水蒸气制氢气可作为燃料电池的氢能源,发生的主要反应如下:
反应Ⅰ CHOCH (g)+HO(g) 2CHOH(g) ΔH>0
3 3 2 3 1
反应Ⅱ CHOH+H O(g) CO(g)+3H(g) ΔH>0
3 2 2 2 2
反应Ⅲ CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2 3
在恒压下,将一定比例的二甲醚和水蒸气混合后,以一定流速通过装有催化剂的反应器,反应相同时间
测得的CHOCH 实际转化率、CO 实际选择性与CO 平衡选择性随温度的变化如图所示。CO 的选
3 3 2 2 2
n (CO )
生成 2
择性= ×100%。下列说法不正确的是( )
2n (CH OCH )
反应 3 3
A.曲线a表示CHOCH 实际转化率随温度的变化
3 3
B.200 ℃时,反应Ⅱ的速率大于反应Ⅲ的速率
n (H O)
起始 2
C.适当增加 ,有利于提高H 的产率
n (CH OCH ) 2
起始 3 3
D.一定温度下,若增大压强,CO的平衡产量不变答案:D
解析:根据常理可知,CO 实际选择性与CO 平衡选择性随温度的变化的走势应该相同,故可知曲线b
2 2
为CO 实际选择性,则曲线a为CHOCH 实际转化率。根据上述分析可知曲线a为CHOCH 实际转
2 3 3 3 3
化率,A正确;在200 ℃时,CO 实际选择性大于其平衡选择性,可知此温度下,反应Ⅱ的速率大于反应Ⅲ,
2
n (H O)
起始 2
B正确;适当增加 的量,会促进CHOCH 的转化,还能使反应Ⅱ正向进行,反应Ⅲ
n (CH OCH ) 3 3
起始 3 3
逆向进行,从而提高氢气的产率,C正确;增大压强会导致反应Ⅱ平衡逆向移动,从而导致反应Ⅲ逆向移
动,CO的平衡产率会减小,D错误。
3.(2024·黑龙江大庆实验中学模拟)某温度下,向V L恒容密闭容器中通入4 mol X(g),发生反应:
①2X(g) Y(g)+4Z(g),②2Z(g) M(g)。反应体系中X、Y、Z的物质的量随时间t的变化曲线
如图所示。下列说法错误的是( )
A.25 min时,生成了3.2 mol M
0.32
B.0~10 min内,气体X的平均反应速率为 mol·L-1· min-1
V
C.该温度下,反应②的平衡常数K=2V
D.25 min时保持其他条件不变,再向体系中通入1 mol Y(g)后,反应②的平衡不移动
答案:C
解析:反应①不是可逆反应,由图可知,25 min时n(X)=0 mol,即25 min时,4 mol气体X反应完全,生成
1
8 mol Z,据图知此时剩下1.6 mol Z,因此反应②消耗Δn(Z)=(8-1.6)mol=6.4 mol,则生成了 ×Δn(Z)=3.2
2
Δn 1.6mol 0.16
mol M,A正确;由图可知,0~10 min内v(Y)= = = mol·L-1· min-1,反应为2X(g)
V Δt V L×10min V
0.32
Y(g)+4Z(g),则v(X)=2v(Y)= mol·L-1· min-1,B正确;反应达到平衡时n(Y)=2 mol,n(Z)=1.6
V
1
mol,则Δn(Z)=2 mol×4-1.6 mol=6.4 mol,反应②为2Z(g) M(g),所以n(M)= ×Δn(Z)=3.2 mol,反应②
2
3.2
c(M) V
的平衡常数K= = =1.25V,C错误;反应①不是可逆反应,25 min时气体X反应完全,通
c2(Z)
(
1.6
)2
V入1 mol Y(g)对反应①无影响,不能改变Z的浓度,则对反应②也无影响,即反应②的平衡不发生移
动,D正确。
4.(2024·江苏盐城一模)CHOH可作大型船舶的绿色燃料。工业上用CO 制备CHOH的原理如下:
3 2 3
反应1:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49.5 kJ·mol-1
2 2 3 2 1
反应2:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2 2
分别在3 MPa、5 MPa下,将n (CO)∶n (H )=1∶3的混合气体置于密闭容器中,若仅考虑上述反
起始 2 起始 2
应,不同温度下反应体系达到平衡时,CO 转化率(α)、产物选择性(S)的变化如图所示。
2
n(CH OH或CO)
3
已知:S(CHOH或CO)= ×100%。下列说法不正确的是( )
3 n (CO )
转化 2
A.反应CO(g)+3H(g) CHOH(l)+H O(l) ΔH<-49.5 kJ·mol-1
2 2 3 2
B.350 ℃后,不同压强下α(CO)接近相等的原因为制备过程以反应1为主
2
1
C.250 ℃时,反应2的平衡常数K=
104
D.250 ℃、5 MPa下,n (CO)∶n (H )=1∶3的混合气体在催化下反应一段时间α(CO)达到P点
起始 2 起始 2 2
的值,延长反应时间α(CO)可能达到20%
2
答案:B
解析:气态转化为液态会放出热量,放热反应的焓变小于0,故反应CO(g)+3H(g) CHOH(l)
2 2 3
+H O(l) ΔH<-49.5 kJ·mol-1,A正确;反应1是放热反应,升高温度,平衡逆向移动,α(CO)减小,反应2是
2 2
吸热反应,升高温度,平衡正向移动,α(CO)增大,350 ℃后,不同压强下α(CO)接近相等的原因为制备过
2 2
程以反应2为主,B错误;由图可知,250 ℃、3 MPa下生成CHOH、CO的选择性(S)均为50%,平衡时
3
CO 的转化率为20%,设n (CO)=1 mol,n (H )=3 mol,则平衡时CO 的转化量为1 mol×20%=0.2
2 起始 2 起始 2 2
mol,生成n(CHOH)=n(CO)=0.2 mol×50%=0.1 mol,建立三段式:
3
CO(g) + 3H (g) CH OH(g) + H O(g)
2 2 3 2
n/mol 1 3 0 0
0
Δn/mol 0.1 0.3 0.1 0.1
n /mol 0.8 2.6 0.1 0.2
平
CO(g) + H (g) CO(g) + H O(g)
2 2 2
n/mol 1 3 0 0
0Δn/mol 0.1 0.1 0.1 0.1
n /mol 0.8 2.6 0.1 0.2
平
0.1 0.2
×
c(CO)·c(H O) V V 1
设体积为V,则此时反应2的平衡常数K= 2 = = ,C正
c(CO )·c(H ) 0.8 2.6 104
2 2 ×
V V
确;250 ℃、5 MPa下,n (CO)∶n (H )=1∶3的混合气体在催化下反应一段时间α(CO)达到P点
起始 2 起始 2 2
的值,由于反应未达到平衡,平衡正向移动,故延长反应时间α(CO)可能达到20%,D正确。
2
5.(2024·辽宁锦州质检)已知可逆反应2NO (g) NO(g),NO 和NO 的消耗速率与其浓度存在如下
2 2 4 2 2 4
关系:v (NO )=kc2(NO ),v (N O)=kc(N O)(其中k、k 是只与温度有关的常数),一定温度下,消耗速
消 2 a 2 消 2 4 b 2 4 a b
率与浓度的关系图像如图所示。下列说法正确的是( )
A.曲线Y表示NO 消耗速率与浓度的关系
2
B.图中A点表示反应达到平衡状态
C.缩小容器的容积,平衡向正反应方向移动,气体的颜色变浅
D.若某温度时k=k,则该温度下平衡常数K=0.5
a b
答案:D
解析:由速率方程可知,曲线X表示二氧化氮消耗速率与浓度关系、曲线Y表示四氧化二氮消耗速率
与浓度关系,A错误;由方程式可知,二氧化氮的消耗速率是四氧化二氮的消耗速率2倍时,反应达到平
衡,由图可知,A点二氧化氮的消耗速率与四氧化二氮的消耗速率相等,则A点正反应速率大于逆反应
速率,反应未达到平衡,B错误;缩小容器的容积,相当于增大压强,NO 气体的浓度增大,气体的颜色变
2
深,因平衡正向移动,气体颜色变浅,但比原来深,C错误;v (NO )=kc2(NO ),则v (NO )=2v
消 2 a 2 生 2 消
(N O)=2kc(N O),平衡时,v (NO )=kc2(NO )=v (NO )=2kc(N O),若某温度时k=k,则该温度下反应
2 4 b 2 4 消 2 a 2 生 2 b 2 4 a b
k
a
的平衡常数K= =0.5,D正确。
2k
b
6.(2024·山东德州高考适应性练习二)丙烯腈( )是一种重要的化工原料,以 为
原料合成丙烯腈的过程如下:向密闭容器中通入一定量的 和NH (g),测得平衡时体系中含碳物质(乙醇除外)
3
n(丙烯腈)
的物质的量分数[如:丙烯腈的物质的量分数= ×100%]随温度的变化如
n(除乙醇外的含碳物质)
图。下列说法错误的是( )
A.“脱水”反应为吸热反应
B.低于225 ℃时,“腈化”过程转化率低
C.a点 的转化率为51%
D.b点HO和C HOH的物质的量之比为3∶1
2 2 5
答案:B
解析:由图可知,一定范围内随着温度升高,平衡时 的含量增加,则说明“脱水”反应正向
进行,反应为吸热反应,A正确。低于225 ℃时,含碳产物中没有 ,说明
几乎完全转化为 ,则“腈化”过程转化率高,B错误。由转化可知,1分子 生成
1分子 要脱去1分子水,生成1分子 要脱去2分子水、1分子乙醇;由图可知,假设a点 、 、 分别为0.49 mol、0.49 mol、0.02 mol,则初始
共0.49 mol+0.49 mol+0.02 mol=1.0 mol, 共消耗0.49 mol+0.02
mol=0.51 mol,则 的转化率为51%,C正确。b点为 和 物质的量分
数相等,由转化可知,生成1分子 要脱去1分子水,生成1分子 要脱去2分子水、1
分子乙醇;假设 和 均为1 mol,则共脱去1 mol+2 mol=3 mol水、1 mol乙醇,故HO
2
和C HOH的物质的量之比为3∶1,D正确。
2 5
7.(2024·江苏苏锡常镇四市一模)采用热分解法脱除沼气中的HS过程中涉及的主要反应为
2
反应Ⅰ:2H S(g) 2H(g)+S (g) ΔH=169.8 kJ· mol-1
2 2 2 1
反应Ⅱ:CH (g)+S (g) CS(g)+2H(g) ΔH=63.7 kJ·mol-1
4 2 2 2 2
保持100 kPa不变,将HS与CH 按2∶1体积比投料,并用N 稀释,在不同温度下反应达到平衡时,所
2 4 2
得H、S 与CS 的体积分数如图所示。下列说法正确的是( )
2 2 2
A.反应2HS(g)+CH(g) CS(g)+4H(g)的ΔH=106.1 kJ· mol-1
2 4 2 2
B.曲线Y代表的是CS 的平衡体积分数
2
C.高于1 050 ℃时,H S平衡转化率与CH 平衡转化率的差值随温度升高而减小
2 4
D.1 050 ℃下反应,增大体系的压强,平衡后H 的体积分数可能达到0.07
2
答案:C
解析:根据反应Ⅰ和反应Ⅱ,利用盖斯定律可得:2H S(g)+CH(g) CS(g)+4H(g) ΔH=+233.5 kJ·
2 4 2 2
mol-1,A错误;将HS与CH 按2∶1体积比投料,并用N 稀释,在不同温度下反应达到平衡时,由于S
2 4 2 2
是反应Ⅰ的生成物同时又是反应Ⅱ的反应物,因此曲线Y代表的是S 的平衡体积分数。950~1 050
2
℃时,以反应Ⅰ为主,随着温度升高,反应Ⅰ速率大于反应Ⅱ,所以S 的体积分数会增大,1 050~1 150 ℃
2
之间,反应Ⅱ速率增大的幅度大于反应Ⅰ,S 的体积分数会减小。根据方程式中的数量关系,曲线Z为
2H,曲线X为CS,B错误;1 050~1 150 ℃之间,S 与CS 的体积分数差值越来越小,所以HS平衡转化
2 2 2 2 2
率与CH 平衡转化率的差值随温度升高而减小,C正确;1 050 ℃下反应,反应Ⅰ和反应Ⅱ都是气体体
4
积增大的反应,增大体系的压强,平衡会逆向移动,平衡后H 的体积分数小于0.07,D错误。
2