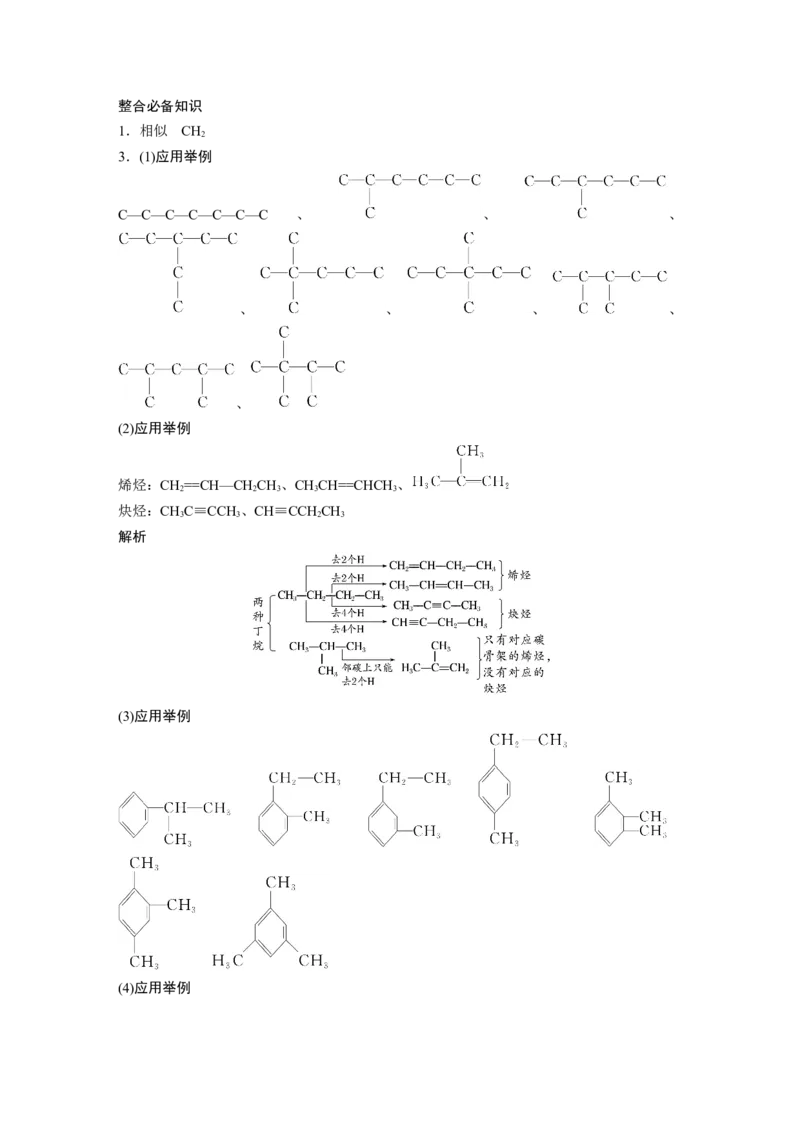
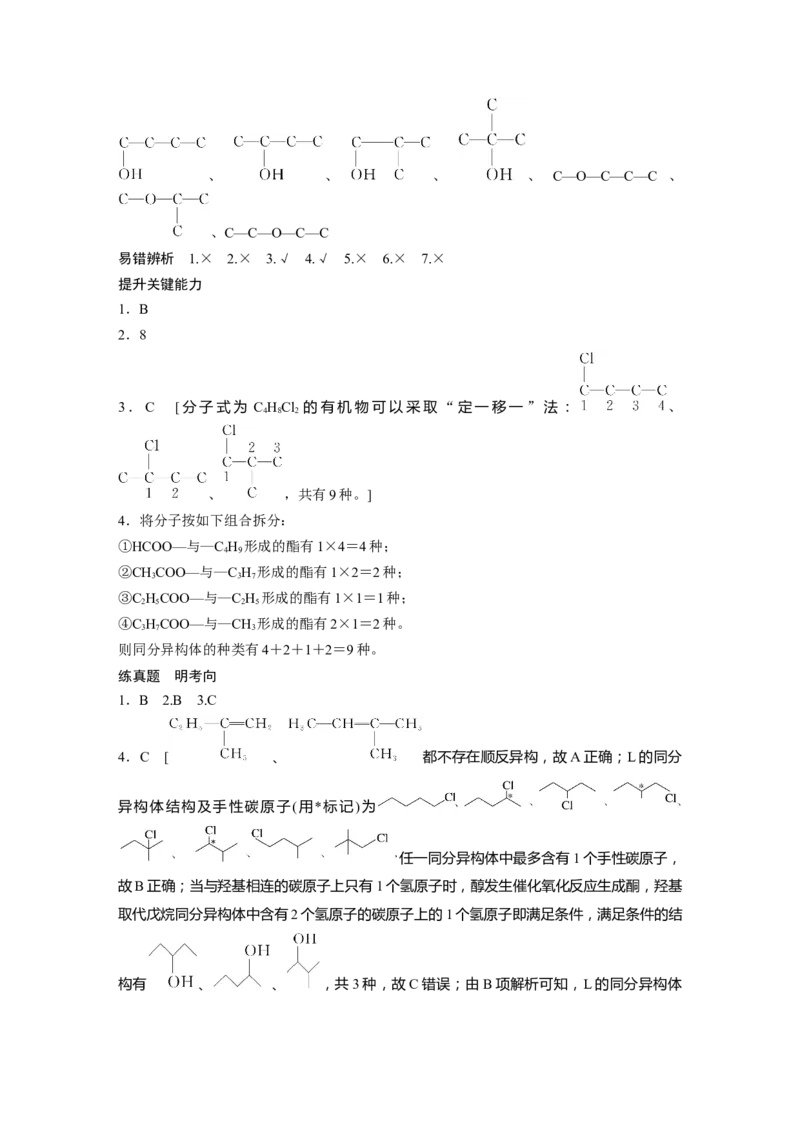
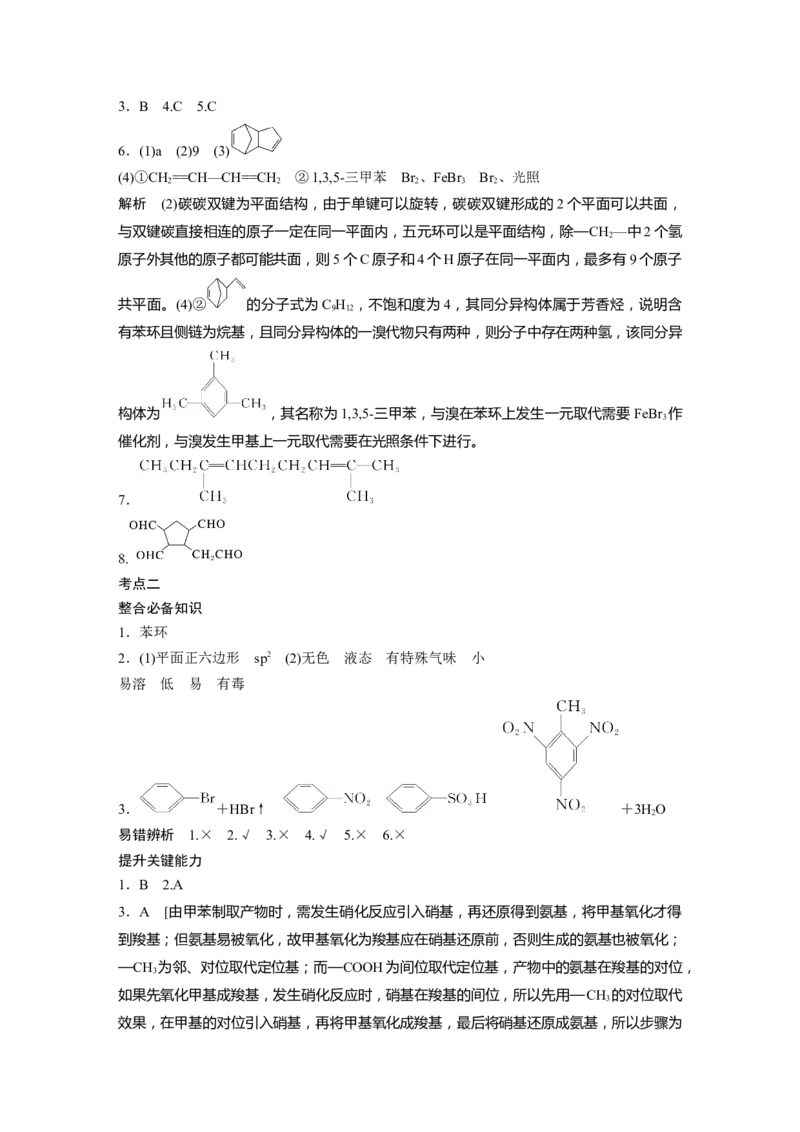
文档内容
复习讲义答案精析
第一章 化学物质及其变化
第 1 讲 物质的组成、性质和转化
考点一
整合必备知识
1.(1)游离 原子 分子 化合 原子 分子 离子
(2)①几种性质不同的单质 ②化学 ③O、O 金刚石、石墨、C 白磷、红磷
2 3 60
2.应用举例
①⑧⑨⑩⑭⑮⑰⑲ ②③④⑤⑥⑦⑪⑫⑬⑯ ⑱
3.树状 交叉 (1)① ②⑨ ③⑦ ④⑤ ⑥ ⑧ ⑩ ⑪
(2)
易错辨析 1.× 2.× 3.× 4.√ 5.√ 6.×
提升关键能力
1.②③⑤ ①④⑥ ①②⑥ ③④ ⑤ ①②③ ④⑤⑥ ③⑤ ①②④⑥ ⑦⑩ ⑧
⑨
2.B A
3.C
考点二
整合必备知识
1.(1)①③④⑨⑩⑬ ②⑤⑥⑦⑧⑪⑫⑭⑮
(2)宏观 有新物质生成的是化学变化,反之是物理变化
有旧化学键断裂,同时有新化学键形成的是化学变化,本质是原子的重
微观
新组合
易错辨析
1.× 2.× 3.× 4.√ 5.①× ②√ ③× ④√
提升关键能力
1.① CO +2Mg=====2MgO+C ② C+O=====CO ③ 2C+O=====2CO ⑤ 2CO+
2 2 2 2
O=====2CO ⑥ NaCO +2HCl===2NaCl+CO↑+HO ⑦ CO +2NaOH===NaCO +
2 2 2 3 2 2 2 2 3
HO
2
2.(1)盐、铜盐、碱式盐(或碳酸盐) (2)Cu (OH) CO +4HCl===2CuCl +3HO+CO↑
2 2 3 2 2 2
(3)Cu(OH) =====CuO+HO CuO+H=====Cu+HO (4)① ②③ ④
2 2 2 2
3.HPO +NaOH===NaH PO +HO
3 2 2 2 2
4.(1)Be(OH) +2NaOH===NaBeO+2HO
2 2 2 2
(2)Be(OH) +2HCl===BeCl +2HO
2 2 2
考点三
整合必备知识
1.(1)分散质 分散剂 (2)分散质粒子直径 溶液 胶体 浊液
2.(1)②④⑥ ①⑤ ③⑦ (2)胶体 溶液
3.<1 nm 1~100 nm >100 nm 均一、透明 均一、透明
不均一、不透明 无丁达尔效应 有丁达尔效应 静置沉淀或分层
易错辨析 1.× 2.√ 3.√ 4.√
提升关键能力
(1)饱和FeCl 溶液 红褐色 (2)FeCl +3HO=====Fe(OH) (胶体)+3HCl (3)A (4)①丁达
3 3 2 3
尔效应 ②生成红褐色沉淀 自来水中含有电解质,使胶体发生聚沉 生成红褐色沉淀 长
时间加热使胶体发生聚沉
练真题 明考向
1.C 2.D 3.A
4.B [明矾净水的原理为Al3++3HOAl(OH) (胶体)+3H+,Al(OH) 胶体具有吸附性,
2 3 3
可以使泥水变澄清,涉及化学变化,A错误;水快速制冰为物理变化,B正确;炖排骨汤时
放点醋,可使骨头中的钙、磷、铁等矿物质溶解出来,此外,醋还可以防止食物中的维生素
被破坏,涉及化学变化,C错误;茄子中存在一类叫“酚氧化酶”的物质,遇到氧气之后,
发生化学反应产生一些有色的物质,反应时间越长,颜色越深,涉及化学变化,D错误。]第 2 讲 离子反应 离子方程式
考点一
整合必备知识
1.(1)水溶液里 熔融状态下 (2)完全电离 部分电离
应用举例 (1)①③⑦ (2)⑤⑥⑨⑪ (3)②⑥⑩⑪ (4)④⑧ (5)⑤⑥⑨○⑪ (6)②
2.应用举例 ①Ba(OH) ===Ba2++2OH-
2
②KAl(SO )===K++Al3++2SO
4 2
③CHCOOHCHCOO-+H+
3 3
④HCOH++HCO、HCOH++CO
2 3
⑤Cu(OH) Cu2++2OH-
2
⑥NaHSO===Na++H++SO
4
⑦NaHSO(熔融)===Na++HSO
4
⑧NaHCO ===Na++HCO、HCOH++CO
3
提升关键能力
1.(6)(9)(11)
2.√ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √
× × ×
3.(1)①能 ②不能,H+、Fe2+、NO发生氧化还原反应 ③不能,HO 在酸性条件下氧化
2 2
Fe2+
(2)能 2S2-+SO+6H+===3S↓+3HO Cl-+ClO-+2H+===Cl↑+HO
2 2 2
4.(1)D (2)B (3)C (4)B (5)C (6)A
5.A [Ba(OH) 溶液和 HSO 、NaHSO 溶液反应的化学方程式分别为 HSO +
2 2 4 4 2 4
Ba(OH) ===BaSO↓+2HO,NaHSO +Ba(OH) ===BaSO↓+NaOH+HO、2NaHSO +
2 4 2 4 2 4 2 4
Ba(OH) ===BaSO↓+NaSO +2HO,溶液导电能力与离子浓度成正比,根据图知,曲线
2 4 2 4 2
①在a点溶液电导率接近0,说明该点溶液离子浓度最小,应该为Ba(OH) 和HSO 的反应,
2 2 4
则曲线②为Ba(OH) 和NaHSO 的反应。b→d反应为向NaOH溶液中继续滴加NaHSO 溶液,
2 4 4
实际上是酸碱中和反应,离子方程式为H++OH-===HO,故A项正确;d点时溶质为
2
NaSO ,根据化学式知,Na+与SO的物质的量之比为2∶1,故B项错误;c点,①中稀硫
2 4
酸过量,溶质为硫酸,②中溶质为NaOH、NaSO ,则该点两种溶液中氢氧根离子浓度不同,
2 4
故C项错误;a点液体为纯水,b点溶质为NaOH,所以a点呈中性,b点呈碱性,故D项错
误。]
考点二
整合必备知识
1.(1)实际参加反应的离子符号 (2)某个具体的化学反应 同一类型的离子反应2.(1)强酸 强碱 可溶性盐
提升关键能力
1.(1)①2NaO+2HO===4Na++4OH-+O↑
2 2 2 2
②Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
③Cl+HOH++Cl-+HClO
2 2
④HSO+H+===HO+SO ↑
2 2
(2)①OH-+H+===HO
2
②SO+2Ag+===Ag SO ↓
2 4
③NH+OH-=====NH ↑+HO
3 2
(3)①MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
②Cu+4H++2NO===Cu2++2NO ↑+2HO
2 2
2.(1)Ba2++2OH-+2H++SO===BaSO↓+2HO
4 2
(2)Ba2++2OH-+2NH+SO===BaSO↓+2NH ·H O
4 3 2
(3)Cu2++SO+Ba2++2OH-===Cu(OH) ↓+BaSO↓
2 4
3.(1)①× ②× ③√ ④√ ⑤× ⑥× (2)①√ ②× ③√ ④√ ⑤× (3)①√
②× ③× ④√ ⑤× ⑥× (4)①√ ②√ ③× ④×
热点强化1
1.(1)①CO+2OH-===CO+HO
2 2
②CO+OH-===HCO
2
(2)①CO+H+===HCO
②CO+2H+===CO↑+HO
2 2
(3)①AlO+H++HO===Al(OH) ↓
2 3
②AlO+4H+===Al3++2HO
2
(4)①2AlO+CO+3HO===2Al(OH) ↓+CO
2 2 3
②AlO+CO+2HO===Al(OH) ↓+HCO
2 2 3
(5)①Al3++3OH-===Al(OH) ↓
3
②Al3++4OH-===AlO+2HO
2
(6)①Fe+NO+4H+===Fe3++NO↑+2HO
2
②3Fe+2NO+8H+===3Fe2++2NO↑+4HO
2
2.(1)①Ca2++HCO+OH-===CaCO ↓+HO
3 2
②Ca2++2HCO+2OH-===CaCO ↓+2HO+CO
3 2
(2)①HCO+OH-+Ca2+===CaCO ↓+HO
3 2
②Ca2++2OH-+2HCO===CaCO ↓+CO+2HO
3 2
(3)①Ba2++OH-+H++SO===BaSO↓+HO 碱
4 2
②Ba2++2OH-+2H++SO===BaSO↓+2HO 中 SO+Ba2+===BaSO↓
4 2 4(4)①3Ba2++3SO+2Al3++6OH-===3BaSO↓+2Al(OH) ↓
4 3
②NH+Al3++2SO+2Ba2++4OH-===NH ·H O+Al(OH) ↓+2BaSO↓
3 2 3 4
3.(1)H++OH-===HO
2
NH+H++2OH-===NH ·H O+HO
3 2 2
(2)H++OH-===HO
2
Al3++3OH-===Al(OH) ↓
3
NH+OH-===NH ·H O
3 2
Al(OH) +OH-===AlO+2HO
3 2
(3)OH-+H+===HO
2
AlO+H++HO===Al(OH) ↓
2 3
CO+H+===HCO、HCO+H+===CO↑+HO
2 2
Al(OH) +3H+===Al3++3HO
3 2
(4)Cl +2Fe2+===2Fe3++2Cl-
2
2Fe2++2Br-+2Cl===2Fe3++Br +4Cl-
2 2
2Fe2++4Br-+3Cl===2Fe3++2Br +6Cl-
2 2
第 3 讲 氧化还原反应的概念和规律
考点一
整合必备知识
1.(1)化合价 (2)电子转移
2.得 降低 失 升高
3.(1)同一元素 (2)不同元素
应用举例 (1)
(浓)=====MnCl +Cl↑+2HO
2 2 2
(2)2N (或1.204×1024) 2
A
4.(1)Cl- SO NO或NO Mn2+ Fe2+或Fe Cr3+
2 2
(2)Zn2+ HO CO Fe3+ S I
2 2 2
(3)Fe S HO Fe3+ SO O 还原 氧化
2 25.D B C A
易错辨析 1.× 2.√ 3.× 4.× 5.× 6.×
提升关键能力
1.B
2.(1)氧 (2)KMnO (3)5∶2 (4)0.25N
4 A
3.(1)H O NaBH
2 4
(2) ===NaBO +4H↑ 1∶1 (3)0.2 mol
2 2
考点二
整合必备知识
1.得电子 失电子
2.难易 多少
提升关键能力
1.①Cl>Br >I >S ②Na+Fe>Cu>Ag ②Br-Cl->OH->SO
3.>
4.(1)①③⑥⑦ (2)⑤⑥⑦⑧ (3)②④
5.Tl3+>Ag+>Fe2+
6.D
热点强化2
2.(1)Fe2+ Br- Fe2+ 2Fe2++Cl===2Fe3++2Cl- 2Fe2++4Br-+3Cl===2Fe3++2Br +
2 2 2
6Cl-
热点专练
1.G、Y、Q、Z、X
2.A 3.D
4.B [根据还原性:Br-<Fe2+<I-,线段AB代表I-物质的量的变化情况,线段BC代表
Fe3+物质的量的变化情况,线段DE代表Br-物质的量的变化情况,A项正确;溶液体积未
知,无法计算浓度,B项错误;根据三段消耗氯气的量可知,原溶液中n(Fe2+)∶n(I-)∶n(Br
-)=2∶1∶3,D项正确。]
练真题 明考向
1.C
2.A [由方程式可知,反应生成1 mol一氧化二氮,转移4 mol电子,故A正确;该反应
中H、O元素化合价不变,HO既不是氧化产物,也不是还原产物,还原产物为 Fe2+,故B
2
错误;由方程式可知,反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,铁元
2
素的化合价降低被还原,铁离子是反应的氧化剂,故C错误;由方程式可知,反应中铁元
素的化合价降低被还原,铁离子是反应的氧化剂,若设计成原电池,铁离子在正极得到电子发生还原反应生成亚铁离子,亚铁离子为正极产物,故D错误。]
3.BD
4.CoCl >Cl>FeCl
3 2 3
第 4 讲 氧化还原反应方程式的配平及计算
考点一
整合必备知识
1.氧化剂 还原剂 升高 种类 个数 总数
2.化合价 相等 质量 电荷 电子
提升关键能力
1.(1)3 8 3 2 4 (2)5 1 3 3 3 3 (3)2 16 10 2 5 8
2.(1)3 6 5 1 3 (2)3 6 2 1 3 (3)2 9 3 3 5
3.(1)2x 2 2x 1 (2) 2 (-1) 1 1 (3)1 (3x+1) (2x-2) x (3x+1) (x-1)
4.(1)2 1 2 2 2 2 2
(2)5 12 18 6 12 10 28
(3)3 2 8 2 2 3 11
5.(1)3 2 4OH- 3 2 5
(2)2 5 6H+ 2 5 8
(3)AlO 3C N 2 3CO
2 3 2
(4)5 2 14 H+ 5 5 2 MnO 7 HO
2
考点二
提升关键能力
1.+3
2.5
3.1.5 2.2
解析 设7.5 mol CuSO 可氧化P的物质的量为x,生成1 mol Cu P时,被氧化的P的物质的
4 3
量为y;根据得失电子守恒:7.5 mol×(2-1)=x×(5-0),解得x=1.5 mol;1 mol×3×(2-
1)+1 mol×[0-(-3)]=y×(5-0),解得y=1.2 mol,所以生成1 mol Cu P时,参加反应的P
3
的物质的量为1.2 mol+1 mol=2.2 mol。
4.9.20
5.60
6. mol·L-1
解析 Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO,5Fe2++MnO+8H+===5Fe3++Mn2++
2 2
4HO。根据得失电子守恒列等式:c mol·L-1×V mL×10-3 L ·mL-1=20 mL×10-3 L·mL-
2 1 11
×6c(CrO)+5c mol·L-1×V mL×10-3 L·mL-1,解得c(CrO)= mol·L-1。
2 2 2 2
热点强化3
热点专练
1.(1)6Co(OH) +O=====2Co O+6HO
2 2 3 4 2
(2)4K+2F+CuCl ===KCuF+2KCl
2 2 2 4
(3)CO+2[Ag(NH)]OH===2Ag↓+(NH )CO+2NH
3 2 4 2 3 3
2.(1)4Co(OH) +O===4CoO(OH)+2HO
2 2 2
(2)Mn2++HSO+HO===MnO ↓+SO+3H+
2 2
3.2CeO+HO+6H+===2Ce3++O↑+4HO
2 2 2 2 2
4.(1)①4Fe(NO)2++O+4H+===4Fe3++4NO+2HO
2 2
②14Fe3++FeS+8HO===15Fe2++2SO+16H+
2 2
(2)作催化剂
5.2NH +3NaClO===N+3HO+3NaCl
3 2 2
第二章 物质的量
第 5 讲 物质的量 气体摩尔体积
考点一
整合必备知识
1.粒子 摩尔(mol)
2.g·mol-1(或g/mol) g·mol-1
易错辨析 1.× 2.√ 3.× 4.× 5.×
提升关键能力
1.160 g·mol-1 8
2.0.33N 0.26
A
考点二
整合必备知识
1.L·mol-1(或L/mol) 22.4 L·mol-1
2.(1)分子数 物质的量 (2)N ∶N ρ∶ρ n∶n
1 2 1 2 1 2
易错辨析 1.× 2.× 3.√ 4.× 5.√
提升关键能力
1.(1)6.72 13.44 (2)22.4 L (3)4.5 15 33.6 (4)
2.(1)64 SO (2)①1.61 ②36
23.(1) mol 6d g·mol-1 (2)22.4ρ g·mol-1
(3)17a%+44b%+18c%
解析 (1)NH HCO =====NH ↑+HO↑+CO↑,假设NH HCO 的摩尔质量为M,混合气
4 3 3 2 2 4 3
体的平均摩尔质量(混)==。同温同压下,==d,则(混)=2d g·mol-1=,所以M=6d
g·mol-1。混合气体的物质的量n(混)== mol。
(2)(混)=ρ·V =22.4ρ g·mol-1。
m
(3)(混)=M(NH )·φ(NH )+M(CO)·φ(CO)+M(H O)·φ(H O)=17a%+44b%+18c%。
r r 3 3 r 2 2 r 2 2
4.(1)Z (2)X (3)4∶1
5.(1)ρ(O )>ρ(Ne)>ρ(H ) (2)p(H )>p(Ne)>p(O )
2 2 2 2
(3)V(H )>V(Ne)>V(O ) (4)m(O )>m(Ne)>m(H )
2 2 2 2
练真题 明考向
1.A 2.C
3.(1)N (2)5N (3)14N (4)1.5N (5)0.1N (6)3N
A A A A A A
4.A [氩气( Ar)是单原子分子,标况下22.4 L氩气是1 mol,其中含有的质子数是18N ,
18 A
A正确;同温同压下,=,所以=,不相同,B错误;标况下,乙醇为非气体,C错误;标
况下,22.4 L(即1 mol) N 分子中含中子数为(14-7)×2N =14N ,D错误。]
2 A A
第 6 讲 物质的量浓度
考点一
整合必备知识
1.单位体积的溶液 c 溶质 溶液 百分数 mol·L-1
B
2.(1)①NaOH HCO HSO HSO ②NH ·H O ③CuSO NaCO
2 3 2 3 2 4 3 2 4 2 3
易错辨析 1.√ 2.× 3.× 4.× 5.× 6.× 7.×
提升关键能力
1.A
2.(1) mol·L-1 (2) mol·L-1 (3)×100% (4) g
3.A [ mL溶液中Al3+的物质的量为= mol,稀释后溶液中Al3+的物质的量浓度为c(Al3
+)== mol·L-1,c(SO)=c(Al3+)=× mol·L-1= mol·L-1。]
4.0.4 mol·L-1
考点二
整合必备知识
1.(1)刻度线易错辨析 1.× 2.√ 3.× 4.× 5.×
提升关键能力
1.(1)胶头滴管 500 mL容量瓶 (2)10.0 g
(3)①左盘 ②小于 32.6 g
(4)搅拌,加速溶解
(5)玻璃棒 保证溶质全部转移至容量瓶中
(6)向容量瓶中加入蒸馏水至距刻度线1~2 cm时,改用胶头滴管滴加蒸馏水至溶液的凹液
面与刻度线相切
2.(1)偏小 (2)偏小 (3)偏小 (4)偏大 (5)偏小 (6)偏小
3.(1)偏大 (2)偏小 (3)偏小 (4)无影响 (5)无影响
练真题 明考向
1.D
2.分液漏斗、球形冷凝管
3.C
4.11.5
热点强化4
1.(1)× (2)× (3)√ (4)× (5)√ (6)× (7)√
2.(1)× (2)× (3)× (4)× (5)× (6)× (7)√ (8)×
3.(1)× (2)× (3)√ (4)× (5)× (6)√ (7)× (8)√ (9)√
4.(1)× 该反应为 NaO 中-1 价氧元素的歧化反应,0.1 mol CO 反应消耗 0.1 mol
2 2 2
NaO,转移0.1 mol电子
2 2
(2)√ 0.1 mol Fe和0.1 mol Cu均能完全使0.1 mol Cl 转化为0.2 mol Cl-,转移0.2 mol电子
2
(3)× 没有给出硝酸的量,不能判断最终产物中铁元素的价态,故不能判断转移电子的数
目
(4)× 该反应的产物为Cu S,0.1 mol Cu只能失去0.1 mol电子
2
(5)× 还原性:Fe2+>Br-,Cl 首先氧化Fe2+,Cl 的量不确定,无法确定Br-被氧化的量,
2 2
转移的电子数在N ~3N 之间
A A
热点专练
1.A 2.D 3.A
4.C [25 ℃、101 kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,
故A错误;Al3+在溶液中会发生水解生成Al(OH) ,因此2.0 L 1.0 mol·L-1的AlCl 溶液中
3 3
Al3+数目小于2.0N ,故B错误;苯甲酸完全燃烧的化学方程式为C HCOOH+O――→7CO
A 6 5 2 2
+3HO,1 mol苯甲酸完全燃烧生成7 mol CO ,则0.20 mol苯甲酸完全燃烧生成1.4 mol
2 2
CO ,数目为1.4N ,故C正确;电解熔融CuCl 时,阳极反应为2Cl--2e-===Cl↑,阴极
2 A 2 2
反应为Cu2++2e-===Cu,阴极增加的重量为Cu的质量,6.4 g Cu的物质的量为0.10 mol,根据阴极反应可知,外电路中通过电子的物质的量为 0.20 mol,数目为0.20N ,故D错
A
误。]
5.A 6.C
7.A [Mn元素由+7价降低到+2价,C元素由0价升高到+4价,则1 mol [4MnO+
5HCHO]完全反应转移的电子数为20N ,A正确;电解精炼铜时,开始阶段阳极上比Cu活
A
泼的金属杂质也会放电,故电路中通过的电子数为 N 时,阳极上被氧化的Cu的质量小于
A
32 g,B错误;题目未指明pH=9的CHCOONa溶液的体积,无法确定水电离出的H+数,
3
C错误;1 L浓度为0.100 mol·L-1的NaCO 溶液中含有0.100 mol Na CO ,CO水解生成
2 3 2 3
HCO和OH-,阴离子数目增加,故溶液中阴离子数大于0.100N ,D错误。]
A
第 7 讲 化学计算的常用方法
类型一
整合必备知识
2.应用举例 样品加热发生的反应为
2NaHCO =====NaCO+HO+CO↑ Δm
3 2 3 2 2
168 106 62
m(NaHCO ) (w-w) g
3 1 2
样品中m(NaHCO )= g,
3
则样品中m(Na CO)=w g- g,
2 3 1
其质量分数为×100%=×100%=×100%。
提升关键能力
1.C 2.B
3.(1)× (2)√
4.NH Fe(SO )·12H O
4 4 2 2
5.①CaC O========CaCO +CO↑
2 4 3
②CaC O·H O热分解放出更多的气体,制得的CaO更加疏松多孔
2 4 2
解析 ①M(CaC O·H O)=146 g·mol-1,取1 mol CaC O·H O,质量为146 g,当剩余质量
2 4 2 2 4 2
为128 g时,质量减少了18 g,即减少1 mol H O,结合题图知,在400 ℃时,固体的化学
2
式为CaC O;当剩余质量为100 g时,质量又减少了28 g,即减少1 mol CO,CaC O 失去1
2 4 2 4
个CO后变成CaCO ,所以在400 ℃至600 ℃时发生的反应为 CaC O========CaCO +
3 2 4 3
CO↑。
6.Fe O ;设FeS 氧化成含有两种元素的固体产物化学式为FeO,M(FeS )=120 g·mol-1,
2 3 2 x 2
则M(FeO)=120 g·mol-1×66.7%=80.04 g·mol-1,则56+16x=80.04,x≈,即固体产物为
x
Fe O
2 3类型二
整合必备知识
2.应用举例 257.9 t
提升关键能力
1.90.36
2.45.0%
3.%
4.①m+m-2m ②%
3 1 2
解析 ②滴定时,根据题给三个离子方程式可得关系式:WO~2IO~6I~12SO,结合钨元
2 2
素的质量守恒可得关系式:WCl~12SO,则样品中 n(WCl )=n(S O)=×c mol·
6 2 6 2
L-1×V×10-3L,m(WCl )=×c mol·L-1×V×10-3L×M g·mol-1= g,因此样品中WCl 的
6 6
质量分数为×100%=%。
类型三
提升关键能力
1.(1)9
计算过程:
2[Al(NO )·xHO]~Al O
3 3 2 2 3
2(213+18x)g 102 g
7.50 g 1.02 g
=
解得x=9 (2)0.010 0
2.84%
3.97.6%
4.酸性 4
5.D [由混合溶液中加入b mol BaCl ,恰好使溶液中的 SO完全沉淀,根据SO+Ba2+
2
===BaSO↓可知n(SO)=b mol;由加入足量强碱并加热可得到c mol NH ,根据NH+OH-
4 3
=====NH ↑+HO可知n(NH)=c mol,由于溶液不显电性,设原溶液中Al3+的物质的量为
3 2
x mol,由电荷守恒可知,3x+c=2b,所以x=,由于溶液的体积是a L,所以原溶液中Al3
+的物质的量浓度c(Al3+)== mol·L-1,故D正确。]
类型四
提升关键能力
1.CaCO ·FeCO[或CaFe(CO)] CaFe(CO)=====CaO+FeO+2CO↑
3 3 3 2 3 2 2
解析 X完全分解生成CO 的质量为10.80 g-6.40 g=4.40 g,其物质的量为0.10 mol,根据
2
CaCO =====CaO+CO↑、FeCO=====FeO+CO↑可得:n(FeO)+n(CaO)=0.1 mol,56 g·mol-
3 2 3 2
1
×n(CaO)+72 g·mol-1×n(FeO)=6.40 g,解以上两式可得:n(FeO)=n(CaO)=0.050 mol,则X的化学式为CaFe(CO)。
3 2
2.(1) (2)
第三章 化学实验基础知识
第 8 讲 化学实验基础知识和技能
考点一
整合必备知识
1.(1)①②③ ④⑤⑥⑦
(2)蒸发皿 坩埚 蒸馏烧瓶 三颈烧瓶
(3)泥三角 坩埚钳 陶土网
2.(1)①上部 ③没有
(2)①0.1 ②0.1 ③0.01 是否漏水 只有一条
3.(1)①搅拌 (2)普通 长颈 分液 恒压滴液 (3)直形 球形 冷凝回流 (4)球形干燥
管
易错辨析 1.× 2.√ 3.× 4.× 5.× 6.×
提升关键能力
1.(1)①烧杯 ②集气瓶 ③坩埚 ④烧杯
(2)①10 mL量筒 ②酸式滴定管 ③碱式滴定管 ④托盘天平 ⑤pH计 ⑥500 mL容量
瓶
(3)①分液漏斗 ②(普通)漏斗 ③(普通)漏斗 ④分液漏斗
2.(1)3.2 (2)D
3.(1)(球形)分液漏斗 向反应器中添加液体药品,并能控制加入液体的多少 锥形瓶 收
集气体 (2)长颈漏斗 防止气体逸出 U形管 球形干燥管 (3)漏斗 充分吸收氨气,防
倒吸 (4)坩埚 泥三角 蒸发皿 (5)直形冷凝管 球形冷凝管 冷凝后的液体容易残留在
球形区域内 防暴沸 (6)图6中温度计测定馏分的温度,图7中温度计测定反应体系的温度
考点二
整合必备知识
1.(1)①广口 细口 ②棕色 ③碱性 强酸性 强氧化性 ⑤铁屑 煤油 石蜡 水 棕
色 稀盐酸 NaOH溶液 橡胶 (2)①药匙 纸槽 托盘天平 胶头滴管 用试剂瓶倾倒
2.(1)定性 定量 Cl 等具有强氧化性 (2)①洁净的玻璃片或表面皿 玻璃棒蘸取待测液
2
体 中部 ②润湿
3.(2)②NH HCl (3)较大 较小
3
4.(1)①略向下 炸裂 ②均匀 固定 (2)①擦干 向上 ② (3)受热均匀,便于控制温度
5.(3)NaOH溶液或热的纯碱溶液 CS 或热的NaOH溶液 稀HNO 浓盐酸
2 3
6.(2)1% 牛奶、蛋清或豆浆 硫粉 湿抹布或沙土 酒精 沙土
易错辨析
1.√ 2.× 3.× 4.× 5.× 6.× 7.× 8.× 9.×
提升关键能力
1.(1)检查装置的气密性 (2)检验气体的纯度 (3)润湿试纸 (4)调天平平衡 (5)分液漏斗、
酸式滴定管、碱式滴定管、容量瓶
2.C
3.试管底易破裂 读数偏低 量筒内液体表面的水会飞溅(或量筒会炸裂)
4.(1)×,加热液体时,试管内液体不能超过其容积的
(2)×,加热结晶水合物时,试管口要略向下倾斜,防止生成的水倒流,导致试管炸裂
(3)×,取放蒸发皿要使用坩埚钳 (4)√
(5)×,蒸发或浓缩溶液时要使用蒸发皿 (6)√
练真题 明考向
1.A 2.D 3.A 4.高温灼烧 冷却干燥 A、C
热点强化5
一、
3.(1)A b a a (2)F 饱和食盐水 a (3)打开止水夹,向长颈漏斗中注入适量蒸馏水
(4)C D a B (5)a
4.冷凝、导气 冷凝回流
二、
2.(1)平衡气压,便于硫酸顺利滴下;减少加入硫酸占有体积带来的误差。 (2)待装置内气
体恢复到室温,将量气管上下移动,至左右管内液面平齐,然后读数。
(3)
热点专练
1.B 2.B
3.D [NaCO 固体受热不分解,所以该装置不能制备CO ,A错误;乙醇和乙酸互溶,不
2 3 2
能采用分液的方式分离,应采用蒸馏,B错误;二氧化硫通入品红溶液中,可以验证其漂白
性,不能验证其酸性,C错误。]
4.D 5.D 6.D
7.C [红磷使用前应用水洗涤,除去其表面的可溶性氧化物及氧化物的水化物,A正确;将红磷转入装置,抽真空后加热外管,除去红磷表面的水分,同时除去残余的少量氧气,B
正确;由仪器构造可知,应从b口通入冷凝水(类比直形冷凝管的“下口进上口出”,b口类
似于直形冷凝管的下口),C错误;通入冷凝水后P(g)在冷凝管外壁凝华,冷却后在氮气氛
4
围下收集,防止产品变质,D正确。]
答题规范(1)
例 (1)产生气泡 形成一段水柱
(2)高于 液面位置保持不变 高于 位置保持不变
(3)一段时间后,水柱的水位不会下降
(4)能回到原来的位置 上升 保持稳定
规范精练
1.(1)将e导管下端管口浸入盛水的烧杯中,关闭b的活塞,打开a处止水夹,微热d,若e
导管口有气泡冒出,冷却至室温后,又有一段水柱上升,证明气密性良好 (2)不可行 无
论气密性是否良好,b中的液体均能顺利滴下
2.(1)关闭活塞E,C中加水没过长导管口,加热A,C中长导管口有气泡冒出,撤去热源
后,长导管内有倒吸产生的液柱,且一段时间内高度保持不变,证明装置气密性良好
(2)三颈烧瓶 防倒吸 碱石灰(或NaOH等合理答案均可) (3)2H SO (浓)+Cu=====CuSO
2 4 4
+SO ↑+2HO
2 2
(4)打开活塞E,从E管口向A中鼓入大量空气
(5)白色固体溶解,溶液变为蓝色 反应后的混合液中含有浓硫酸,若将水加入浓硫酸中,
会放出大量热而使液体飞溅
第 9 讲 物质的分离与提纯
考点一
整合必备知识
1.除去 纯净物
易错辨析 1.× 2.× 3.× 4.× 5.× 6.× 7.×
提升关键能力
1.(1)饱和溶液
(2)降温、加入KNO 固体、加热蒸发再冷却至原来的温度
3
(3)蒸发结晶
(4)蒸发浓缩、冷却结晶、过滤
(5)将固体混合物加入热水,搅拌、趁热过滤(或将固体加水溶解,将溶液蒸发至有大量固体
析出,停止加热,趁热过滤)
(6)将固体加水溶解,将溶液蒸发浓缩至出现晶膜,停止加热,冷却后有固体析出,过滤
(7)加热浓缩溶液至有大量晶体析出,在高于34 ℃条件下趁热过滤2.(1)蒸发浓缩 过滤 ①③
(2)更换滤纸,重新过滤 滤纸破损、滤液超过滤纸边缘
(3)防止晶体失去结晶水,也防止可溶性杂质析出
(4)没有打开分液漏斗颈上的玻璃塞(或玻璃塞上的凹槽没有与漏斗上的小孔对齐)
3.(1)冷凝回流并导出馏分 c (2)H BO +3CHOHB(OCH ) +3HO (3)受热均匀,
3 3 3 3 3 2
便于控制温度
防止空气中的水蒸气进入锥形瓶,使硼酸三甲酯水解
(4)圆底烧瓶 (5)使用溶剂少,可连续萃取(萃取率高)
4.(1)[Cu(NH )]2++2RH===2NH+2NH ↑+CuR (2)提高铜离子的萃取率,提高原料利用
3 4 3 2
率 (3)稀硫酸 (4)①pH太小氧化亚铜会发生歧化反应,pH太大,氧化亚铜会溶解 ②真
空干燥
考点二
易错辨析 1.× 2.× 3.× 4.× 5.× 6.√
提升关键能力
1.灼热铜网 灼热氧化铜 NaOH溶液或碱石灰 洗气或用固体转化气体 饱和 NaHCO
3
溶液 饱和 NaHCO 溶液或酸性 KMnO 溶液 饱和 NaHSO 溶液 洗气 CO Cl
3 4 3 2 2
MgO、Mg(OH) 或MgCO 调pH转为沉淀,过滤 NaOH溶液 加过量NaOH溶液,过滤、
2 3
洗涤 NaOH溶液 加过量NaOH溶液,过滤、洗涤 精铜、CuSO 溶液 电解精炼
4
2.(1)变多 (2) (3)降低 (4)H++OH-===HO
2
3.(1)重结晶 (2)锆、铪配离子[MF ]2-与阴离子交换树脂的结合能力不同 (3)萃取
6
(4)3K ZrF +4Al=====6KF+4AlF+3Zr
2 6 3
答题规范(2)
规范精练
1.(1)向上层清液中再加入BaCl 溶液,若产生白色沉淀,说明SO未沉淀完全,反之则沉淀
2
完全。
(2)洗去可溶性杂质(Na+、Cl-等)。
(3)沿玻璃棒向漏斗中注入蒸馏水至浸没沉淀,待蒸馏水自然流下后,重复操作2~3次。
(4)取少许最后一次洗涤液于一洁净的试管中,滴加稀HNO 酸化的AgNO 溶液,若产生白
3 3
色沉淀,说明沉淀未洗净,反之已洗净。
2.(1)有利于析出更多的晶体 防止晶体见光分解 (2)减少洗涤过程中的溶解损耗
3.(1)SrCO +2H+===Sr2++HO+CO↑ (2)BaSO 、Fe(OH) BD (3)可减少氯化锶晶体
3 2 2 4 3
的溶解,提高产率 (4)A
练真题 明考向
1.D 2.A 3.D
4.⑥⑩③⑤ CCl
4解析 组装蒸馏装置对TiCl 、CCl 混合物进行蒸馏提纯,按由下而上、从左到右的顺序组
4 4
装,安装顺序为①⑨⑧,然后连接冷凝管,蒸馏装置中应选择直形冷凝管⑥,接着连接尾接
管⑩,TiCl 极易水解,为防止外界水蒸气进入,最后连接③⑤,安装顺序为
4
①⑨⑧⑥⑩③⑤;由于TiCl 、CCl 分子结构相似,TiCl 的相对分子质量大于CCl ,TiCl 分
4 4 4 4 4
子间的范德华力较大,TiCl 的沸点高于CCl ,故先蒸出的物质为CCl 。
4 4 4
热点强化6
热点专练
1.C 2.D
3.趁热过滤 用80~90 ℃的蒸馏水洗涤2~3次
4.防止因温度降低,CoCl 晶体析出
2
5.1.2 mol·L-1 蒸发浓缩、冷却结晶
6.(1)SO 静置,取上层清液加入BaCl ,若无白色沉淀,则SO已沉淀完全 (2)趁热过滤
2
第四章 金属及其化合物
第 10 讲 碱金属 钠及其氧化物
考点一
整合必备知识
1.锂(Li) 钠(Na) 钾(K) 铷(Rb) ns1 很强
2.(1)银白 (2)减小 (3)< > > 煤油 (4)降低 小于
3.(1)2R+2HO===2ROH+H↑
2 2
4.(1)物理 (2)黄 紫 蓝色钴玻璃
易错辨析 1.× 2.× 3.√ 4.× 5.×
提升关键能力
1.(1)锂可以与水反应 (2)B
2.(1) KH+HO===KOH+H↑ N (或6.02×1023)
2 2 A
(2)3NaH+Fe O===2Fe+3NaOH
2 3
(3)AlCl LiCl
3
考点二
整合必备知识
1.(1)①2Na+2HO===2NaOH+H↑ 2CHCHOH+2Na―→2CHCHONa+H↑ ②小
2 2 3 2 3 2 2
放 低 (2)4Na+O===2NaO 2Na+O=====NaO
2 2 2 2 2
3.2NaCl(熔融)=====2Na+Cl↑
2易错辨析 1.× 2.× 3.× 4.× 5.√
提升关键能力
1.c>a>b 钠与上述三种物质反应的实质都是钠与H+之间的置换反应,由三种物质电离出
H+的能力可知反应速率的大小顺序为c>a>b
2.(1)2Na+2HO+Cu2+===Cu(OH) ↓+2Na++H↑ (2)①③④⑥
2 2 2
3.(1)K NbF +5Na===Nb+5NaF+2KF (2)A
2 7
4.C [钠沉入液氨中说明钠的密度比液氨大,A正确;液氨中没有能导电的离子,而钠投
入液氨中生成蓝色的溶剂合电子,能导电,说明溶液的导电性增强,B正确;钠投入液氨中
先生成络合物,再反应得到H,故0.1 mol钠反应失去0.1 mol电子,C错误;反应中钠失去
2
电子,只能是氢元素得到电子,所以钠和液氨可以发生的反应为2NH +2Na===2NaNH +
3 2
H↑,D正确。]
2
考点三
整合必备知识
1.淡黄色 碱性 -2 -1 1∶2 1∶2 NaO+HO===2NaOH 2NaO +
2 2 2 2
2HO===4NaOH+O↑ NaO+CO===NaCO 2NaO +2CO===2NaCO +O NaO+
2 2 2 2 2 3 2 2 2 2 3 2 2
2HCl===2NaCl+HO 2NaO+4HCl===4NaCl+2HO+O↑
2 2 2 2 2
2.(1)Na SO NaSO +2NaOH S↓+2NaOH
2 4 2 4
易错辨析 1.√ 2.× 3.× 4.√ 5.√
提升关键能力
1.(1) NaO NaO O NaOH (2)0.2N (或1.204×1023)
2 2 2 2 2 A
2.A
3.(1)0.1 (2)14
解析 (1)Na O 和 NaO 的混合物溶于水发生反应:NaO+HO===2NaOH、2NaO +
2 2 2 2 2 2 2
2HO===4NaOH+O↑,气体B为氧气,其物质的量为0.05 mol,则NaO 的物质的量为0.1
2 2 2 2
mol,质量为7.8 g,NaO的质量为14 g-7.8 g=6.2 g,物质的量为0.1 mol。(2)溶液A中
2
NaOH的物质的量为0.1 mol×2+0.05 mol×4=0.4 mol,则稀释后溶液中c(OH-)=c(NaOH)
==1 mol·L-1,c(H+)=10-14 mol·L-1,溶液pH=14。
4.(1) 离子键、非极性共价键 -1
(2)2Na O +2HO===4NaOH+O↑ 反应生成的HO 具有漂白作用(或反应生成的HO 氧
2 2 2 2 2 2 2 2
化了酚酞)
(3)2MnO+5HO+6H+===2Mn2++5O↑+8HO
2 2 2 2
(4)Na O+2HO===2NaOH+HO 复分解反应
2 2 2 2 2
5.(1)两个氧原子之间都含有一对共用电子对(或都含有一个过氧键)
(2)2CaO+2HO===2Ca(OH) +O↑
2 2 2 2
2CaO+2CO===2CaCO +O
2 2 3 2
6.(1) (2)
7.(1)2
(2)4H O+Cr O+2H+===2CrO+5HO 不是
2 2 2 5 2
练真题 明考向
1.(1)√ (2)× (3)×
2.B 3.D 4.A
第 11 讲 碳酸钠和碳酸氢钠 钠及其化合物的相互转化
考点一
整合必备知识
纯碱 苏打 小苏打 放热 吸热 大于 碱 大于 >
易错辨析
1.× 2.× 3.√ 4.√ 5.× 6.√ 7.× 8.√
提升关键能力
1.(1)充分灼烧至恒重 2NaHCO =====NaCO+HO+CO↑
3 2 3 2 2
(2)通入足量CO NaCO+HO+CO===2NaHCO
2 2 3 2 2 3
(3)滴加适量NaOH 溶液 NaHCO +NaOH===NaCO+HO
3 2 3 2
2.(1)NaHCO (2)NaHCO NaCO (3)Na CO NaHCO
3 3 2 3 2 3 3
3.(1)Ⅱ (2)2NaHCO =====NaCO+HO+CO↑,CO+Ca(OH) ===CaCO ↓+HO D
3 2 3 2 2 2 2 3 2
(3)NaHCO
3
4.NaHCO NaCO NaCO NaHCO 相等
3 2 3 2 3 3
5.(1)NaHCO (2)Na CO CO+H+===HCO HCO+H+===HO+CO↑ (3)NaOH和
3 2 3 2 2
NaCO OH-+H+===HO、CO+H+===HCO HCO+H+===CO↑+HO (4)Na CO 和
2 3 2 2 2 2 3
NaHCO
3
6.(1)Na CO+HCl===NaCl+NaHCO 、NaHCO +HCl===NaCl+HO+CO↑
2 3 3 3 2 2
(2)NaHCO NaCl NaCO (3)0.05 mol·L-1 (4)0.112 L
3 2 3
考点二
构建知识网络
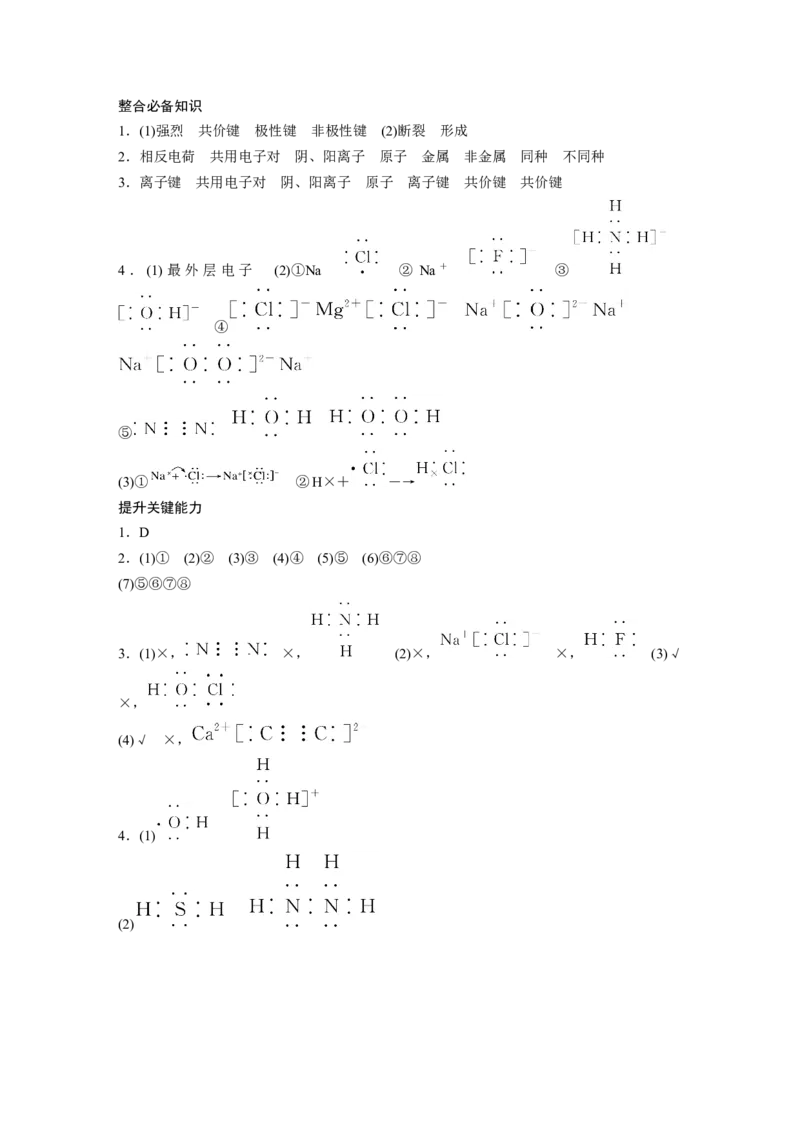
(1)2Na O +2HO===4NaOH+O ↑ 2NaO +2CO===2NaCO +O (2)①2NaCl(熔
2 2 2 2 2 2 2 2 3 2
融)=====2Na+Cl↑ ②2NaCl+2HO=====2NaOH+H↑+Cl↑ ③NH +NaCl+CO +
2 2 2 2 3 2HO===NaHCO ↓ + NH Cl 2NaHCO =====NaCO + HO + CO↑ (3)①2OH - +
2 3 4 3 2 3 2 2
CO===CO+HO ②OH-+CO===HCO (4)2Na++CO+CO+HO===2NaHCO ↓
2 2 2 2 2 3
拓展综合应用
1.B
2.(1)Na CO 溶液显碱性,也会使酚酞溶液变红
2 3
(2)Na CO 方案2的①中出现的白色沉淀是BaCO ,所以燃烧后的白色物质中有NaCO ,
2 3 3 2 3
②中滴加无色酚酞溶液无明显现象,说明燃烧后的白色物质中没有NaO
2
(3)4Na+3CO=====2NaCO+C
2 2 3
(4)不同意。因为反应物中无氢元素(或违背质量守恒定律)
3.(1)先通入NH ,然后通入CO
3 2
(2)NH CO 由于CO 在水中的溶解度比较小,而 NH 极易溶于水,为防止倒吸,通入
3 2 2 3
NH 的导气管的末端不能伸入到溶液中,为增加二氧化碳的吸收率,通入CO 的导气管的末
3 2
端应插入液面以下 (3)吸收氨气尾气,防止污染空气
4.D [饱和食盐水中通入氨气形成氨盐水,再通入二氧化碳反应生成碳酸氢钠沉淀和氯化
铵,碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,气体X为CO ,故A正确;氨盐水中
2
通入气体X后,反应生成碳酸氢钠沉淀,因此溶液中Na+大量减少,故B正确;悬浊液a经
过操作b得到滤渣和滤液,说明操作b为过滤,故C正确;悬浊液a中的不溶物主要是碳酸
氢钠晶体,故D错误。]
热点强化7
1.(1)2NaHCO =====NaCO+CO↑+HO 83.2%
3 2 3 2 2
(2)将样品分解产生的气体全部带出,使其被B、C装置完全吸收 ×100%
2.(1)①D ②取少量最后一次洗涤液于试管中,滴加NaSO 溶液,如无沉淀,则沉淀已洗
2 4
净,反之则未洗净 ③44.2%
(2)洗涤 (再)称量 ×100%
3.(1)防止空气中的CO 和HO进入装置D中产生误差
2 2
(2)④ ⑦ ⑥
(3)将反应产生的CO 全部赶入装置D中,减小误差
2
(4)38.7%
4.(1)酚酞 甲基橙 由黄色变橙色,且半分钟内不变色 (2)NaCl、NaHCO 、HCO
3 2 3
(3)3.56% (4)偏大
解析 (1)第一滴定终点为恰好生成NaHCO ,溶液呈碱性,应选用酚酞作指示剂;第二滴定
3
终点为HCl与碳酸氢钠恰好完全反应,溶液呈酸性,应选用甲基橙作指示剂。
(2)步骤③中,某时刻滴加盐酸使溶液呈中性,因碳酸氢钠与HCl反应生成的CO 溶于水生
2
成HCO,使溶液显酸性,溶液呈中性说明其中还有NaHCO 未反应完。
2 3 3
(3)第一次滴定发生反应:NaCO +HCl===NaHCO +NaCl,消耗盐酸V mL,平均值为
2 3 3 122.45 mL,第二次滴定发生反应:NaHCO +HCl===NaCl+HO+CO↑,消耗盐酸 V
3 2 2 2
mL,平均值为23.51 mL,原碳酸钠转化的碳酸氢钠,还要再消耗盐酸的体积为V mL,则
1
原溶液中含有的NaHCO 所消耗的盐酸体积为V mL-V mL=1.06 mL,产品中NaHCO 的
3 2 1 3
质量分数为×100%=×100%≈3.56%。
(4)第一次滴定终点时,俯视读数,导致V 偏小,则V -V 偏大,导致NaHCO 质量分数的
1 2 1 3
计算结果偏大。
练真题 明考向
1.(1)× (2)× (3)√ (4)× (5)√ (6)× (7)×
2.(1)
(2)作助熔剂,降低NaCl的熔点,节省能耗
(3) (4)c a (6)159
3.(1)aefbcgh (2)使氨盐水雾化,可增大与二氧化碳的接触面积,从而提高产率(或其他合
理答案)
(3)NH ·H O+NaCl+CO===NH Cl+NaHCO ↓
3 2 2 4 3
(4)②冷却结晶 过滤
第 12 讲 铁及其氧化物和氢氧化物
考点一
整合必备知识
1.四 化合态 陨铁 3d64s2 Ⅷ +2、+3
2.(1)银白 磁体 (2)+2 +3 3Fe+2O=====Fe O
2 3 4
2Fe+3Cl=====2FeCl Fe+S=====FeS Fe+I=====FeI 3Fe+4HO(g)=====Fe O +4H
2 3 2 2 2 3 4 2
Fe+2H+===Fe2++H↑ 钝化 +3 Fe+Cu2+===Fe2++Cu 2Fe3++Fe===3Fe2+
2
3.(1)黑色 红棕色 黑色 不溶于水 不溶于水 不溶于水 +2 +3 +2、+3
(2)①Fe O ② FeO+2H+===Fe2++HO Fe O +6H+===2Fe3++3HO ③ Fe O +
3 4 2 2 3 2 2 3
3CO=====2Fe+3CO Fe O+2Al=====2Fe+Al O
2 2 3 2 3
④3FeO+10HNO===3Fe(NO )+NO↑+5HO
3 3 3 2
⑤Fe O+2I-+6H+===2Fe2++I+3HO
2 3 2 2
易错辨析 1.× 2.× 3.× 4.× 5.× 6.√
提升关键能力
1.D 2.A
3.(1)提供水蒸气,使之与还原铁粉在高温下发生反应(2)3Fe+4HO(g)=====Fe O+4H
2 3 4 2
(3)集中火焰,产生高温 A 用水蒸气排尽装置中的空气
(4)收集气体
4.(1)常温下,铁在冷的浓硫酸或冷的浓硝酸中钝化,未看到铁片明显的溶解
(2)加热时,铁能溶于浓硫酸或浓硝酸,生成 Fe3+和 SO 或 Fe3+和 NO 2Fe+
2 2
6HSO (浓)=====Fe (SO )+3SO ↑+6HO、Fe+6HNO(浓)=====Fe(NO )+3NO ↑+3HO
2 4 2 4 3 2 2 3 3 3 2 2
(3)铁与稀硝酸反应生成Fe3+和NO:Fe+4HNO(稀)===Fe(NO ) +NO↑+2HO 铁与稀硫
3 3 3 2
酸反应生成Fe2+和H:Fe+2H+===Fe2++H↑
2 2
(4)过量铁粉与浓酸在加热条件下的反应:
①与浓硫酸:Fe+2HSO (浓)=====FeSO +SO ↑+2HO
2 4 4 2 2
②与浓硝酸:Fe+4HNO(浓)=====Fe(NO )+2NO ↑+2HO。
3 3 2 2 2
过量铁粉与稀酸的反应:
①与稀硫酸:Fe+HSO (稀)===FeSO +H↑
2 4 4 2
②与稀硝酸:3Fe+8HNO(稀)===3Fe(NO )+2NO↑+4HO。
3 3 2 2
5.FeO
6.Fe O
5 7
解析 n(HCl)=0.14 L×5.0 mol·L-1=0.7 mol,由氧化物和盐酸反应生成水可知,氧化物中
含有n(O)=0.5n(HCl)=0.35 mol,所得溶液还能吸收0.025 mol Cl ,恰好使其中的Fe2+全部
2
转变为Fe3+,反应后所得溶液为FeCl ,因n(Cl-)=0.7 mol+0.025 mol×2=0.75 mol,则
3
n(Fe3+)=n(Cl-)=0.25 mol,所以氧化物中n(Fe)∶n(O)=0.25∶0.35=5∶7,所以化学式为
Fe O。
5 7
考点二
整合必备知识
白 红 褐 Fe(OH) + 2H + ===Fe2 + + 2HO Fe(OH) + 3H + ===Fe3 + + 3HO
2 2 3 2
2Fe(OH) =====Fe O +3HO Fe2++2OH-===Fe(OH) ↓ Fe3++3OH-===Fe(OH) ↓ 白色
3 2 3 2 2 3
絮状沉淀迅速变成灰绿色 红褐色 4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
易错辨析 1.× 2.× 3.√ 4.× 5.×
提升关键能力
1.(1)稀HSO 、铁屑 (2)煮沸 (3)避免生成的Fe(OH) 沉淀接触O 而被氧化 苯(或煤油)
2 4 2 2
(4)打开 关闭 稀硫酸与铁粉反应产生的H 排出了装置中的空气
2
(5)①Fe Fe-2e-===Fe2+ ②BC ③隔绝空气,防止生成的Fe(OH) 被氧化 加热煮沸,
2
排出溶解的O 否 CCl 比FeSO 溶液的密度大,在下层,无法隔绝空气
2 4 4
(6)白色沉淀迅速变为灰绿色,最后变成红褐色
2.(1)除去水中溶解的氧气 分液漏斗
(2)①Zn + 2Cr3+===Zn2+ + 2Cr2+ ②排尽装置c中的空气
(3)冷却结晶 过滤(4)敞开体系,醋酸亚铬会与空气接触,且缺少氢气的处理装置
练真题 明考向
1.A 2.C
3.(1)分液漏斗 液封,防止空气进入装置4 (2)在装置2、3之间添加控制开关 (3)装置4
内的空气没有排尽
第 13 讲 铁盐、亚铁盐 铁及其化合物的转化
考点一
整合必备知识
1.(2)2Fe3++Cu===2Fe2++Cu2+ 2Fe3++HS===2Fe2++S↓+2H+ (3)①将氯化铁固体先
2
溶于较浓的盐酸中,然后再稀释至所需浓度 ③Fe O ④Fe(OH)
2 3 3
2.(1)绿 绿矾 (2)浅绿 ①Fe2++Zn===Zn2++Fe ②2Fe2++Cl===2Fe3++2Cl-
2
(3)铁屑(钉)
3.+6 杀菌 消毒
4.(1)变红 灰绿 红褐 K++Fe2++[Fe(CN) ]3-===KFe[Fe(CN) ]↓ (2)红 红褐色 紫
6 6
(3)Fe3+ Fe2+
易错辨析 1.√ 2.× 3.√ 4.× 5.×
提升关键能力
1.D 2.A
3.(1)加入过量铁粉 2Fe3++Fe===3Fe2+
(2)加入氯水(或通入Cl) 2Fe2++Cl===2Fe3++2Cl-
2 2
(3)滴加HO 2Fe2++HO+2H+===2HO+2Fe3+
2 2 2 2 2
(4)加入过量铁粉,过滤 Fe+Cu2+===Cu+Fe2+
(5)先向溶液中加入氧化剂(如HO 、氯水),然后向混合液中加入CuO或Cu(OH) ,调pH,
2 2 2
促进Fe3+水解生成Fe(OH) 沉淀,静置过滤
3
4.C
5.取固体粉末溶于适量稀硫酸,将溶液分成两份,一份滴加KSCN溶液,溶液变红,证明
含有Fe3+,另一份滴加酸性KMnO 溶液,KMnO 溶液紫红色褪去,证明含Fe2+。
4 4
考点二
构建知识网络
2.①2Fe2++Cl===2Fe3++2Cl-
2
②3Fe2++4H++NO===3Fe3++2HO+NO↑
2
③2Fe2++HO+2H+===2Fe3++2HO
2 2 2
④5Fe2++MnO+8H+===5Fe3++Mn2++4HO
2
⑤2Fe3++Fe===3Fe2+⑥Cu+2Fe3+===Cu2++2Fe2+
⑦2Fe3++HS===2Fe2++S↓+2H+
2
拓展综合应用
1.(1)①a ②d ③c (2)2∶1
2.C
3.(1)Fe O +6H+===2Fe3++3HO (2)2Fe3++Fe===3Fe2+、Fe+2H+===Fe2++H↑ (3)取
2 3 2 2
少量溶液B于试管中,滴加KSCN溶液,若溶液不变红色,说明溶液B中不存在Fe3+ (4)
防止被空气氧化
4.(1)2Fe+3Cl=====2FeCl
2 3
(2)在沉积的FeCl 固体下方加热 (3)②⑤
3
(4)冷凝、收集氯化铁 Fe3++3SCN-Fe(SCN)
3
(5)
(6)2Fe3++HS===2Fe2++S↓+2H+
2
5.B
6.(1)球形干燥管 饱和食盐水 C
(2)2MnO+16H++10Cl-===2Mn2++5Cl↑+8HO
2 2
(3)2Fe(OH) +3ClO-+4OH-===2FeO+3Cl-+5HO
3 2
(4)①ADEF ②90%
解析 (1)仪器D为球形干燥管;洗气瓶B中盛有的试剂是饱和食盐水,用来除去混合气体
中的氯化氢;因为实验中需要保持碱性环境,因此先向 Fe (SO ) 溶液中加入NaOH溶液,
2 4 3
然后再通入Cl ,所以先打开分液漏斗C的活塞。(3)结合化合价升降相等、原子守恒、电荷
2
守恒可写出制取NaFeO 的离子方程式:2Fe(OH) +3ClO-+4OH-===2FeO+3Cl-+5HO。
2 4 3 2
(4)①溶液配制需要胶头滴管、烧杯、50 mL容量瓶、玻璃棒。②n(BaCO )==0.001 8
3
mol,所以CN-的去除率为×100%=90%。
练真题 明考向
1.A
2.ABCD
3.C [图中所示铁元素不同化合价的物质:a为Fe,b为FeCl 、FeSO 、Fe(NO ) 等Fe(Ⅱ)
2 4 3 2
的盐类物质,c 为 Fe(OH) ,e 为 FeCl 、Fe (SO ) 、Fe(NO ) 等 Fe(Ⅲ)的盐类物质,d 为
2 3 2 4 3 3 3
Fe(OH) 。Fe 与 Fe(Ⅲ)的盐类物质可发生反应生成 Fe(Ⅱ)的盐类物质,如 Fe+
3
2FeCl ===3FeCl ,故A不选;Fe(Ⅱ)为铁元素的中间价态,既有还原性也有氧化性,因此既
3 2
可被氧化,也可被还原,故B不选;Fe(Ⅲ)的盐类物质与浓碱液反应生成Fe(OH) 沉淀,制
3
备Fe(OH) 胶体操作为向沸水中滴加饱和FeCl 溶液,继续煮沸至溶液呈红褐色,停止加热,
3 3故C选;b→c→d→e→b转化如FeCl ――→Fe(OH) ―――→Fe(OH) ――→FeCl ――→FeCl ,故D不
2 2 3 3 2
选。]
4.(1)不再有气泡产生 Fe、Cu在稀盐酸中形成原电池,加快反应速率 (2)漏斗、玻璃棒
(3)K [Fe(CN) ]溶液 (4)2Fe3++Fe===3Fe2+、2Fe2++Cl===2Fe3++2Cl- (5)在HCl气流中
3 6 2
蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到FeCl ·6H O晶体 (6)球形冷凝管 冷凝回流
3 2
SOCl 吸收SO 、HCl等尾气,防止污染 (7)碱石灰与SO 、HCl气体反应,失去干燥作用
2 2 2
(8)a
第 14 讲 铝、镁及其化合物
考点一
整合必备知识
1.最多 化合态
2.(1)银白 小 导电、导热和延展性
(2)①4Al+3O=====2Al O
2 2 3
②2Al+3Cl=====2AlCl
2 3
③钝化 2Al+6H+===2Al3++3H↑
2
④2Al+2OH-+2HO===2AlO+3H↑
2 2
⑤2Al+Fe O=====2Fe+Al O
2 3 2 3
3.Al O +6H+===2Al3++3HO Al O +2OH-===2AlO+HO 2Al O(熔融)=====4Al+
2 3 2 2 3 2 2 3
3O↑
2
4.(2)①2Al(OH) =====Al O+3HO
3 2 3 2
②Al(OH) +3H+===Al3++3HO
3 2
③Al(OH) +OH-===AlO+2HO
3 2
(3)①Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②AlO+CO+2HO===Al(OH) ↓+HCO
2 2 3
③Al3++3AlO+6HO===4Al(OH) ↓
2 3
5.(1)KAl(SO )·12H O (2)KAl(SO )===K++Al3++2SO Al(OH) 胶体
4 2 2 4 2 3
易错辨析 1.× 2.× 3.× 4.×
提升关键能力
1.(1)(4)
2.C
3.(1)H+、Al3+、NH、Al(OH)
3
(2)①H++OH-===HO
2
②Al3++3OH-===Al(OH) ↓,Mg2++2OH-===Mg(OH) ↓
3 2③NH+OH-===NH ·H O
3 2
④Al(OH) +OH-===AlO+2HO
3 2
4.(1)两性 Fe O Al O+2OH-===2AlO+HO
2 3 2 3 2
(2)氯化铝是共价化合物,熔融氯化铝以分子的形式存在
(3)Na AlF 降低Al O 熔融的温度
3 6 2 3
(4)2Al(OH) =====Al O+3HO 2Al O(熔融)=====4Al+3O↑
3 2 3 2 2 3 2
(5)石墨电极被阳极上产生的O 氧化 定期补充石墨
2
拓展应用
1.A
2.(1)AlO (2)Zn+2OH-===ZnO+H↑ (3)①③④
2
(4)Al3++3NH ·H O===Al(OH) ↓+3NH 可溶性锌盐与氨水反应产生的Zn(OH) 可溶于过
3 2 3 2
量氨水中,生成[Zn(NH )]2+,氨水的用量不易控制
3 4
考点二
整合必备知识
1.(1)2Mg+O=====2MgO
2
(2)3Mg+N=====MgN
2 3 2
(3)Mg+2H+===Mg2++H↑
2
(4)2Mg+CO=====2MgO+C
2
(5)Mg+Cu2+===Mg2++Cu
(6)Mg+2HO=====Mg(OH) +H↑
2 2 2
2.(1)难 碱性氧化物 MgO+2H+===Mg2++HO
2
(2)难 Mg(OH) +2H+===Mg2++2HO
2 2
提升关键能力
1.(1)CaCO=====CaO+CO↑ CaO+HO===Ca(OH) (2)Mg2++Ca(OH) ===Mg(OH) +
3 2 2 2 2 2
Ca2+ (3)Mg(OH) +2HCl===MgCl +2HO MgCl ·6H O=====MgCl +6HO (4)MgCl (熔
2 2 2 2 2 2 2 2
融)=====Mg+Cl↑
2
2.C
练真题 明考向
1.(1)√ (2)× (3)√ (4)√ (5)√ (6)×
2.D
3.C [陶瓷的成分中含有SiO ,SiO 能与HF发生反应,因此不宜用陶瓷作吸收塔内衬材
2 2
料,故A正确;采用溶液喷淋法可增大反应物的接触面积,提高吸收塔内烟气吸收效率,
故B正确;烟气(含HF)通入吸收塔,加入过量的碳酸钠,发生反应:NaCO+HF===NaF+
2 3
NaHCO ,向合成槽中通入NaAlO ,发生反应:6NaF+NaAlO +4NaHCO ===NaAlF↓+
3 2 2 3 3 6
4NaCO +2HO,过滤得到 NaAlF 和含有 NaCO 的滤液,所以合成槽内产物主要有
2 3 2 3 6 2 3
NaAlF 、NaCO 、HO,故C错误;滤液的主要成分为NaCO ,可进入吸收塔循环利用,
3 6 2 3 2 2 3故D正确。]
4.B
第 15 讲 铜 金属材料 金属冶炼
考点一
整合必备知识
2.(1)2Cu+O +CO +HO===Cu (OH) CO (3)醛基 (4)H O (5)继续溶解 (6)会产生污
2 2 2 2 2 3 2
染性气体SO 且HSO 的利用率低
2 2 4
易错辨析 1.× 2.√ 3.× 4.× 5.×
提升关键能力
1.D 2.B
3.(1)Fe O、CuO 将固体A粉碎(或升高温度或增大盐酸浓度等)
2 3
(2)调节溶液pH,使Fe3+形成Fe(OH) 沉淀而除去 2FeCl +Cu===2FeCl +CuCl
3 3 2 2
(3)2Cu2++SO+2Cl-+HO===2CuCl↓+SO+2H+
2
(4)有利于加快除去CuCl表面的水分,防止其水解氧化
考点二
整合必备知识
1.铁 铬
2.低 大
3.2Fe+3CO W+3HO 2Fe+Al O 4Al+3O↑ Mg+Cl↑ 2Na+Cl↑
2 2 2 3 2 2 2
易错辨析
1.× 2.√ 3.√ 4.× 5.× 6.× 7.√ 8.×
提升关键能力
1.C 2.B
3.(1)CuFeS +3FeCl ===CuCl+4FeCl +2S
2 3 2
(2)Fe O
2 3
(3)Cu2+
(4)HCl和CuCl 0.5 mol
2
(5)会产生污染环境的气体SO (或能耗高等)(答案合理即可)
2
练真题 明考向
1.D 2.C
3.(1)除去原料表面的油污 (2)SO (3)Cu+HO +HSO ===CuSO +2HO (4)胆矾晶体
2 2 2 2 4 4 2
易溶于水 (5)ⅰ.溶液 C 经步骤③加热浓缩后双氧水已完全分解 ⅱ.取滤液D,向其中加
入适量硫化钠,使铜离子恰好完全沉淀,静置后,向上层清液中再加入KI溶液,溶液不变
色,I-不能被氧化解析 (1)原料表面含有少量的油污,NaCO 溶液呈碱性,可以除去原料表面的油污。(2)在
2 3
加热的条件下,铜可以与浓硫酸发生反应生成 CuSO 、SO 和HO,二氧化硫是一种大气污
4 2 2
染物,步骤②中,若仅用浓HSO 溶解固体B,将生成SO 污染环境。(3)步骤②中,在HO
2 4 2 2 2
存在下 Cu 溶于稀 HSO ,生成 CuSO 和 HO,该反应的化学方程式为 Cu+ HO +
2 4 4 2 2 2
HSO ===CuSO +2HO。(4)胆矾是一种易溶于水的晶体,因此,经步骤④得到的胆矾,不
2 4 4 2
能用水洗涤。(5)ⅰ.H O 常温下即能发生分解反应,在加热的条件下,其分解更快,因此,
2 2
甲同学认为不可能是步骤②中过量HO 将I-氧化为I 。ⅱ.I-氧化为I 时溶液的颜色会发生
2 2 2 2
变化;滤液D中含有CuSO 和HSO ,乙同学通过实验证实,只能是Cu2+将I-氧化为I ,
4 2 4 2
较简单的方案是除去溶液中的Cu2+,然后再向其中加入含有I-的溶液,观察溶液是否变色。
第五章 非金属及其化合物
第 16 讲 氯及其重要化合物
考点一
整合必备知识
1.(1)黄绿 刺激性 大 易 (2)①棕红 棕黄 苍白 Cl+2KI===2KCl+I Cl+SO +
2 2 2 2
2HO===HSO +2HCl Cl+2FeCl ===2FeCl
2 2 4 2 2 3
②氧化 还原 与水反应:Cl+HOHCl+HClO
2 2
(3)①2
2.(1)弱 2HClO=====2HCl+O↑ 棕色 (2)NaClO 2NaOH+Cl===NaCl+NaClO+HO
2 2 2
NaClO + CO + HO===NaHCO + HClO (3)CaCl 和 Ca(ClO) Ca(ClO) 2Cl +
2 2 3 2 2 2 2
2Ca(OH) ===CaCl +Ca(ClO) +2HO 碱 氧化 Ca(ClO) +CO +HO===CaCO +2HClO
2 2 2 2 2 2 2 3
Ca(ClO) +CO+HO===CaCO +2HClO,2HClO=====2HCl+O↑
2 2 2 3 2
易错辨析
1.√ 2.√ 3.× 4.× 5.× 6.× 7.√ 8.× 9.×
提升关键能力
1.B
2.Cl Cl- H+ H+、HClO
2
3.(1)干燥的红色布条不褪色,湿润的红色布条褪色 Cl 无漂白性,Cl 与水反应生成的
2 2
HClO有漂白性 (2)Cl +HOH++Cl-+HClO (3)溶液先变红后褪色 (4)H O+SO+
2 2 2Cl===2H++SO+2Cl- (5)2Fe2++Cl===2Fe3++2Cl- (6)吸收氯气,防止污染环境
2 2
4.(1)溶液先变红后褪色
(2)次氯酸钠溶液中存在水解平衡:ClO-+HOHClO+OH-,调节pH在12左右,可以
2
抑制ClO-的水解,减少生成不稳定的HClO
(3)CO +ClO-+HO===HClO+HCO
2 2
(4)2H++Cl-+ClO-===Cl↑+HO,氯气逸出,导致Ca(ClO) 失效
2 2 2
5.NaClO:×35.5≈0.95
ClO :×35.5≈2.63
2
NaClO:×35.5≈1.57
2
6.ClO Cl NaFeO
2 2 2 4
考点二
整合必备知识
1.(1)MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
(2)①分液漏斗 圆底烧瓶 ②除去Cl 中少量的HCl气体
2
③干燥氯气(或除去氯气中的水蒸气)
(3)①上 ②饱和食盐水
(4)NaOH溶液 吸收过量的氯气,防止污染环境
2.(1)ClO-+Cl-+2H+===Cl↑+HO
2 2
(2)ClO+5Cl-+6H+===3Cl↑+3HO
2 2
(3)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO
2 2
提升关键能力
1.D
2.(1)观察集气瓶中气体颜色的变化,若集气瓶上部充满黄绿色气体,则证明Cl 已收集满。
2
(2)饱和食盐水中Cl-浓度较大,抑制了Cl 与水的反应,Cl 在饱和食盐水中的溶解度很小,
2 2
因此可用排饱和食盐水法收集氯气,且用此法可除去实验过程中挥发产生的HCl气体。
3.(1)浓盐酸具有挥发性,加热时大量HCl挥发;随反应进行,浓盐酸变为稀盐酸,稀盐酸
不再与MnO 反应产生Cl
2 2
(2)MnO Cl- 一 NaCl 加入MnSO 固体和NaCl固体(或加入浓HSO 和MnSO 固体)
2 4 2 4 4
练真题 明考向
1.(1)√ (2)√ (3)√ (4)×
2.Cl +2OH-===ClO-+Cl-+HO NaClO溶液吸收空气中的CO 后产生HClO,HClO见
2 2 2
光分解
3.(1)MnO +4HCl(浓)=====MnCl +Cl↑+2HO (2)c→d→b→a→e (3)HClO 向溶液中
2 2 2 2
加入过量稀硝酸,再加入少量AgNO 溶液,若有白色沉淀生成,则证明此久置氯水中含有
3
Cl-第 17 讲 氯及其重要化合物的转化关系
构建知识网络
1.(从上到下,从左到右)HClO NaClO Ca(ClO) Cl HCl NaCl
2 2
2.①MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
②Cl+HOHCl+HClO
2 2
③2Cl+2Ca(OH) ===CaCl +Ca(ClO) +2HO
2 2 2 2 2
④NaClO+2HCl===NaCl+Cl↑+HO
2 2
⑤2HClO=====2HCl+O↑
2
⑥2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
⑦2Fe+3Cl=====2FeCl
2 3
⑧2FeCl +Cl===2FeCl
2 2 3
拓展综合应用
1.(1)圆底烧瓶 饱和食盐水
(2)水浴加热 Cl +2OH-===ClO-+Cl-+HO 避免生成NaClO (3)吸收尾气(Cl ) AC
2 2 3 2
(4)过滤 少量(冷)水洗涤
2.C
3.(1)蒸馏烧瓶 (2)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO (3)丁装置内充满黄绿
2 2
色气体 使 SnCl 汽化,利于从混合物中分离出来 (4)Sn+2HCl===SnCl +H↑ AC
4 2 2
(5)BD (6)91.2%
解析 (3)整个装置中充满氯气,即丁装置充满黄绿色气体时,再加热熔化锡粒生成SnCl ,
4
继续加热丁装置,促进氯气与锡反应,使生成的SnCl 汽化,有利于从混合物中分离出来,
4
便于在戊装置处冷却收集。(4)碱石灰能吸收二氧化碳,但二氧化碳对反应没有影响,故B
不符合;即使有O 进入,O 能氧化丁中生成的副产物SnCl ,但不会氧化戊装置试管中的产
2 2 2
物SnCl ,故D不符合。(5)H O 溶液能氧化SnCl ,同时双氧水被还原生成水,但是没有明
4 2 2 2
显现象,无法检验,故A错误;FeCl 溶液(滴有KSCN)呈红色,氯化铁氧化SnCl ,铁离子
3 2
被还原生成亚铁离子,溶液褪色,可以检验,故B正确;AgNO 溶液能检验氯离子,但是
3
不能检验Sn2+,故C错误;溴水氧化SnCl ,溴被还原生成溴离子,溶液褪色,可以检验,
2
故D正确。(6)用去锡粒1.19 g,其物质的量为=0.01 mol,根据Sn原子守恒可知生成SnCl
4
0.01 mol,则SnCl 的产率为×100%≈91.2%。
4
第 18 讲 卤族元素 溴、碘单质的提取
考点整合必备知识
2.深红棕 紫黑 固体 挥发 升华 变蓝
3.HX+HXO 易 难 NaX+NaXO+HO > > < < 易 难
2
4.(2)2H O+2F===4HF+O
2 2 2
5.(1)白 浅黄 黄 (2)Br- I- (3)蓝
应用举例 ②④⑤
易错辨析 1.× 2.× 3.× 4.√ 5.√ 6.× 7.×
提升关键能力
1.A 2.B
3.(1)
(2)(CN) +2NaOH===NaCN+NaCNO+HO
2 2
(3)2I-+Cl===I+2Cl-
2 2
4.(1)HCl、HIO (2)ICl+2OH-===Cl-+IO-+HO 否
2 2
5.(1) (2)湿润的淀粉-KI试纸变蓝 (3)Cl +2Br-===Br +2Cl- (4)打开活塞
2 2
b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后CCl 层变为紫红色
4
(5)确认C中的黄色溶液中无Cl,排除Cl 对溴置换碘实验的干扰 (6)原子半径逐渐增大
2 2
热点强化8
1.(2)①2NaBr+Cl===Br +2NaCl
2 2
②Br +SO +2HO===2HBr+HSO
2 2 2 2 4
③2HBr+Cl===2HCl+Br
2 2
2.(2)Cl +2I-===I+2Cl-
2 2
热点专练
1.C
2.(1)富集溴元素 A (2)3Br +3CO===BrO+5Br-+3CO↑ (3)BrO+5Br-+6H+===3Br
2 2 2
+3HO
2
3.(1)2I-+2H++HO===I+2HO (2)下口放出 (3)3I +6NaOH===5NaI+NaIO +3HO
2 2 2 2 2 3 2
(4)5I-+IO+6H+===3I↓+3HO (5)过滤
2 2
4.(1)2NO+4H++2I-===2NO↑+I↓+2HO (2)氯气、浓硝酸、酸性高锰酸钾氧化性太
2 2
强,还能继续氧化I (3)碘在水中溶解度不大,且易升华 (4)富集碘元素
2
5.(1)BC (2)2I-+HO+2H+===I+2HO 否 HO 会将I-全部氧化生成I,无法进行反
2 2 2 2 2 2 2
应I+I-I,从而导致后续反应无法进行
2
练真题 明考向
1.B
2.①2AgI+Fe===2Ag+Fe2++2I- AgNO
3
②FeI+Cl===I+FeCl I、FeCl I 被过量的Cl 进一步氧化
2 2 2 2 2 3 2 2解析 ①由流程图可知悬浊液中含AgI,AgI可与Fe反应生成FeI 和Ag,FeI 易溶于水,在
2 2
离子方程式中能拆,故加入Fe粉进行转化反应的离子方程式为2AgI+Fe===2Ag+Fe2++2I
-,生成的银能与硝酸反应生成硝酸银参与循环。
②通入Cl 的过程中,因I-还原性强于Fe2+,Cl 先氧化还原性强的I-,若氧化产物只有一
2 2
种,则该氧化产物只能是I ,故反应的化学方程式为FeI +Cl===I +FeCl ;若反应物用量
2 2 2 2 2
比=1.5时,先氧化完全部I-再氧化Fe2+,恰好将全部I-和Fe2+氧化,故氧化产物为I 、
2
FeCl ;当>1.5即Cl 过量,多余的氯气会与生成的单质碘以及水继续发生氧化还原反应,单
3 2
质碘的收率会降低。
3.(1)碘酸钾 (2)加热 KCl KH(IO)+KOH===2KIO +HO
3 2 3 2
第 19 讲 硫及其氧化物
考点一
整合必备知识
1.硫化物 硫酸盐
2.黄色 难溶 易溶
思考 (1)S 、S 、S 、S 属于同一元素的不同种单质,它们互为同素异形体,S 转化为S 、
2 4 6 8 8 6
S、S 属于化学变化。
4 2
(2)硫单质、CS 均属于非极性分子,而HO属于极性分子,根据“相似相溶”规律,非极性
2 2
分子易溶于非极性分子形成的溶剂中。
3.Fe+S=====FeS 2Cu+S=====Cu S 低 H+S=====HS S+O=====SO
2 2 2 2 2
易错辨析 1.× 2.×
提升关键能力
1.A 2.D
3.A [由题干信息知,多硫离子S中S元素化合价为-价>-2价,而As S 中S元素为-2
2 3
价,是正常硫化物,A错误; As S 发生氧化反应生成氧化产物As S ,B正确;NaS 中阴、
2 3 2 5 2 2
阳离子分别为S、Na+,个数比为1∶2,C正确;久置NaS溶液被空气中氧气氧化后生成单
2
质硫,S与NaS溶液进一步反应生成多硫化物,多硫化物在酸性条件下易歧化,可能生成
2
单质硫,溶液变浑浊,D正确。]
考点二
整合必备知识
1.(1)无 有刺激性 有毒气体 大 易 40 (2)SO +HOHSO 2NaOH+
2 2 2 3
SO ===NaSO +HO 2SO +O2SO Cl +SO +2HO===2HCl+HSO 品红
2 2 3 2 2 2 3 2 2 2 2 4
(3)①NaSO +HSO ===NaSO +SO ↑+HO ② Cu+2HSO (浓)=====CuSO +SO ↑+
2 3 2 4 2 4 2 2 2 4 4 2
2HO
22.(1)液 固 (2)SO +HO===HSO CaO+SO ===CaSO SO +Ca(OH) ===CaSO +
3 2 2 4 3 4 3 2 4
HO
2
3.(1)石油和煤 含硫矿物 酸雨 5.6 脱硫 二氧化硫
易错辨析 1.× 2.× 3.× 4.× 5.×
提升关键能力
1.(1)Na SO +HSO (浓)===NaSO +SO ↑+HO
2 3 2 4 2 4 2 2
(2)溶液蓝色变浅直至褪色 无色溶液中出现黄色浑浊 还原性 氧化性 SO +2HO+
2 2
I===SO+2I-+4H+
2
(3)品红溶液褪色后,关闭分液漏斗的活塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH(答案合理即可)
2.(1)褪色 还原 (2)变红 (3)否 (4)BaSO (5)BaSO SO +2OH-===SO+HO、Ba2++
4 3 2 2
SO===BaSO↓
3
3.(1)品红溶液 检验SO
2
(2)酸性KMnO 溶液 除去SO 并检验SO 是否除尽
4 2 2
(3)澄清石灰水 检验CO
2
(4)酸性KMnO 溶液的颜色变浅但不褪成无色
4
热点强化9
1.(1)①增大接触面积,加快吸收速率,使SO 被充分吸收
2
②SO +I+2HO===HSO +2HI ③
2 2 2 2 4
(2)①AC ②×100%
2.(1)2NH +SO +HO===(NH )SO (NH )SO +SO +HO===2NH HSO
3 2 2 4 2 3 4 2 3 2 2 4 3
(2)AC (3)燃煤烟气中大量的CO 虽然能被氨水吸收生成NH HCO ,但由于亚硫酸的酸性
2 4 3
强于碳酸,故SO 会与NH HCO 反应生成NH HSO ,离子方程式为HCO+SO ===CO +
2 4 3 4 3 2 2
HSO
(4)2CO+SO =====S+2CO 2H+SO =====S+2HO
2 2 2 2 2
(5)2NaHSO=====NaSO +SO ↑+HO
3 2 3 2 2
3.(1)SO +CaCO ===CO+CaSO 2CaSO+O===2CaSO CaSO+2HO===CaSO·2H O
2 3 2 3 3 2 4 4 2 4 2
(2)①pH增大,石灰石的溶解度减小,减慢了与SO 的反应
2
②温度升高,SO 的溶解度减小
2
练真题 明考向
1.(1)√ (2)× (3)× (4)× (5)√ (6)×
2.C 3.C
4.C [锥形瓶内发生反应:NaSO +HSO ===NaSO +SO ↑+HO ,产生的SO 进入到
2 3 2 4 2 4 2 2 2
试管中,CCl 层溶液褪色,发生反应:SO +Br +2HO===HSO +2HBr,证明Br 具有氧
4 2 2 2 2 4 2
化性,A项正确;试管中花瓣褪色,说明SO 可以漂白花瓣中的有色物质,证明SO 具有漂
2 2
白性,B项正确;试管中产生大量气泡是锥形瓶中产生的SO 进入到试管中引起的,NaSO
2 2 3与HSO 发生复分解反应,C项错误;试管中Br 可将SO 氧化,生成HSO 和HBr,SO 可
2 4 2 2 2 4
以和Ba2+结合生成不溶于酸的白色沉淀,D项正确。]
第 20 讲 硫酸 硫酸盐
考点一
整合必备知识
1.将浓HSO 沿烧杯内壁缓缓倒入水中并用玻璃棒不断搅拌
2 4
2.钝化 Cu+2HSO (浓)=====CuSO +SO ↑+2HO C+2HSO (浓)=====CO↑+
2 4 4 2 2 2 4 2
2SO ↑+2HO
2 2
3.(1)①4FeS+11O=====2Fe O+8SO S+O=====SO ②2SO +O2SO
2 2 2 3 2 2 2 2 2 3
(2)①混合气中除含有二氧化硫外,还含有多种杂质。这些杂质有的使催化剂中毒、失效,
有的对反应设备有腐蚀作用,所以必须净化处理 ②常压下SO 的转化率已经很大,高压下
2
SO 转化率提高不多,但成本大大增加 ③用水吸收SO 会产生大量酸雾
2 3
易错辨析
1.× 2.√ 3.√ 4.√ 5.× 6.√ 7.× 8.×
提升关键能力
1.(1)浓硫酸的吸水性 (2)浓硫酸具有高沸点、难挥发性 (3)浓硫酸的强氧化性 (4)硫酸
的强酸性 (5)浓硫酸的酸性、强氧化性 (6)浓硫酸的脱水性 (7)浓硫酸的脱水性、强氧化
性
2.(1)(2)(3) (4)(5)(6)(7)
3.C
4.H 和SO 的混合气体 随着反应的进行,硫酸的浓度变小,铁与稀硫酸反应生成氢气
2 2
考点二
整合必备知识
1.BaSO CaSO·2H O CuSO ·5H O KAl(SO )·12H O
4 4 2 4 2 4 2 2
2.排除CO、SO、Ag+等离子的干扰 CO+2H+===CO↑+HO SO+2H+===SO ↑+
2 2 2
HO Ag++Cl-===AgCl↓ Ba2++SO===BaSO↓
2 4
提升关键能力
1.C
2.取样品溶液于试管中,加入过量BaCl 溶液,过滤,然后向沉淀中滴入过量稀盐酸,若
2
沉淀全部溶解,则NaSO 未被氧化;若沉淀部分溶解,则NaSO 部分被氧化;若沉淀一点
2 3 2 3
也不溶解,则NaSO 全部被氧化。
2 3
3.(1)SO+2H+===SO ↑+HO(或HSO+H+===SO ↑+HO) NaS和NaCO 的混合溶液
2 2 2 2 2 2 3
(2)S (3)NaOH溶液(合理即可) (4)控制反应温度、调节酸的滴加速率(或调节酸的浓度等)
(5)若SO 过量,溶液显酸性,产物分解
24.(1)2NaHSO===NaSO+HO
3 2 2 5 2
(2)①NaHSO ②得到NaHSO 过饱和溶液
3 3
5.(1)NaHSO 、NaHSO (2)① 增大锌的表面积,加快化学反应速率 ② Zn+
3 4
2SO ===ZnS O
2 2 4
③减少NaSO 的溶解损失,易于干燥 NaCO 为碱性物质,保险粉在碱性介质中较稳定
2 2 4 2 3
(3)HCOO-+OH-+2SO ===SO+CO+HO
2 2 2 2
练真题 明考向
1.(1)√ (2)× (3)√ (4)√ (5)×
2.B
3.B [铜和浓硫酸反应生成CuSO ,体现浓硫酸的酸性,生成SO ,体现浓硫酸的强氧化
4 2
性,故A错误;a处的紫色石蕊变红,其原因是SO 溶于水生成了酸,可说明SO 是酸性氧
2 2
化物,故B正确;b处品红褪色,其原因是SO 具有漂白性,而c处酸性高锰酸钾褪色,其
2
原因是SO 和酸性KMnO 发生氧化还原反应,SO 体现还原性,故C错误;实验过程中试
2 4 2
管底部出现白色固体,其原因是浓硫酸具有吸水性,将反应生成的HO吸收,故D错误。]
2
4.(1)浓硫酸吸水且放热,导致HCl挥发
(2)HCl气体会将HSO 带出,与Ba(NO ) 作用生成BaSO 白色沉淀
2 4 3 2 4
第 21 讲 硫及其化合物的相互转化
构建知识网络
1.(从上到下,从左到右)SO HSO SO NaHSO NaSO S FeS
3 2 4 2 3 2 3
2.①SO +Cl+2HO===HSO +2HCl(或SO +HO===HSO )
2 2 2 2 4 2 2 2 2 4
②2HSO (浓)+Cu=====CuSO +SO ↑+2HO
2 4 4 2 2
③SO +2NaOH===NaSO +HO
2 2 3 2
④NaSO +HSO ===NaSO +SO ↑+HO
2 3 2 4 2 4 2 2
⑤NaHSO+NaOH===NaSO +HO(或NaHSO+NaCO===NaSO +NaHCO )
3 2 3 2 3 2 3 2 3 3
⑥NaSO +SO +HO===2NaHSO
2 3 2 2 3
⑦2NaSO +O===2NaSO
2 3 2 2 4
⑧4FeS+11O=====2Fe O+8SO
2 2 2 3 2
⑨CuO+HSO ===CuSO +HO
2 4 4 2
⑩Fe+S=====FeS
⑪2SO +O2SO
2 2 3
⑫SO +2HS===3S+2HO
2 2 2
拓展综合应用
1.B 2.C 3.C4.(1)⑤ 酸性KMnO 溶液褪色 还原
4
(2)+4(或-2) 0 (3)Cu+2HSO (浓)=====CuSO +SO ↑+2HO 将产生的气体通入品红
2 4 4 2 2
溶液,品红溶液褪色
5.(1)S+SO +2NaHCO ===NaSO+HO+2CO
2 3 2 2 3 2 2
(2) 亚硫酸钠
(3)①BrO+6I- +6H+===3I↓+Br-+3HO ②淀粉溶液
2 2
解析 (1)Cu S在空气中煅烧可以发生两种反应,①Cu S+O=====2CuO+S,②Cu S+
2 2 2 2
2O=====SO +2CuO;则可推断产生的黄色固体为S,反应釜中S和SO 与过量NaHCO 反
2 2 2 3
应,化学方程式为 S+SO +2NaHCO ===NaSO +HO+2CO 。(2)由 S+SO +
2 3 2 2 3 2 2 2
2NaHCO ===NaSO+HO+2CO 可知,n(S)∶n(SO )为1∶1时,固体A与气体B的利用率
3 2 2 3 2 2 2
最高,①+②可得:2Cu S+3O=====4CuO+S+SO ,当=时,利用率最高,若高于此值,
2 2 2
二氧化硫会与碳酸氢钠反应生成亚硫酸钠。(3)②滴定过程中所用指示剂为淀粉溶液,因为
淀粉遇碘变蓝,消耗NaSO 的物质的量为c mol·L-1×V×10-3 L=cV×10-3 mol,根据关
2 2 3
系式:KBrO ~3I ~6SO,25 mL溶液中KBrO 的物质的量为×cV×10-3 mol,则250 mL
3 2 2 3
溶液中KBrO 的物质的量为×cV×10-2 mol,纯度为×100%=%。
3
练真题 明考向
1.C
2.B [根据流程图分析可知,吸收过程中有二氧化碳生成,A正确;结晶后母液中含饱和
NaHSO 和过量的二氧化硫形成的亚硫酸,没有NaHCO ,B错误;NaHSO 高温时易分解变
3 3 3
质,所以气流干燥过程中温度不宜过高,C正确;结合上述分析可知,中和后溶液中含
NaSO 和NaHCO ,D正确。]
2 3 3
3.(1)ABD
(2)SO 遇品红溶液生成不稳定无色物质,受热释放SO ,溶液恢复红色;温度降低,SO 在
2 2 2
品红溶液中溶解度增大,溶液颜色变浅
第 22 讲 氮及其氧化物 硝酸
考点一
整合必备知识
1.游离 人工 化合
2.(1)无 无 难 (3)①N 的稳定性 ②N 的氧化性 ③N 的还原性 ④N 的沸点低,液
2 2 2 2
氮易汽化,且汽化吸收热量
3.(1)NO NO NO (2)红棕色、有刺激性气味的气体 不 易 2NO+O===2NO
2 4 2 5 2 2
思考 方案一 将气体分别溶于盛有少量有机溶剂(如苯、四氯化碳)的试管中,溶液变橙红
色的是溴蒸气,无变化的是NO 。
2方案二 将气体分别通入盛有少量水的试管中,溶液变黄的是溴蒸气,无明显现象的是
NO 。
2
方案三 将气体分别通入盛有少量硝酸银溶液的试管中,产生淡黄色沉淀的是溴蒸气,无明
显现象的是NO 。
2
4.光化学烟雾
易错辨析
1.√ 2.× 3.× 4.× 5.× 6.× 7.× 8.×
提升关键能力
1.C
2.D [反应①将N 转化为NO,属于氮的固定,反应②属于植物固氮,A正确;由图示知,
2
氮循环过程中涉及氢、氧元素,B正确;反应④是O 将NH 氧化为NO,N元素化合价由-
2 3
3价升高到+5价,即生成1 mol NO失去8 mol电子,根据得失电子守恒可知每生成1 mol
NO需要消耗2 mol O ,C正确;反应③中NO被氧化为NO,反应⑤中NO被还原为N ,D
2 2
错误。]
3.(1)①2NO+O===2NO ②3NO +HO===2HNO+NO
2 2 2 2 3
(2)4NO+3O+2HO===4HNO 4NO +O+2HO===4HNO
2 2 3 2 2 2 3
(3)①O 8 mL、4 mL ②NO 10.8 mL、1.2 mL
2
4.(1)2CO+2NO=====N+2CO
2 2
(2)8NH +6NO =====7N+12HO 4∶3
3 2 2 2
(3)①2NO +2NaOH===NaNO +NaNO +HO
2 3 2 2
②NaNO ③≥ 补充适量空气
2
5.(1)NO+NO +Ca(OH) ===Ca(NO )+HO
2 2 2 2 2
(2)使NO、NO 与石灰乳充分接触,加快吸收速率,提高吸收效率
2
(3)产品中含有Ca(NO ) NO不能完全吸收,污染空气
3 2
(4)3NO+2H+===NO+2NO↑+HO
2
考点二
整合必备知识
1.无 易 有刺激性
2.(1)4HNO=====2HO+4NO ↑+O↑
3 2 2 2
(2)①3Cu+8HNO(稀)===3Cu(NO ) +2NO↑+4HO Cu+4HNO(浓)===Cu(NO ) +
3 3 2 2 3 3 2
2NO ↑+2HO
2 2
②C+4HNO(浓)=====CO↑+4NO ↑+2HO
3 2 2 2
③3Fe2++4H++NO===3Fe3++NO↑+2HO
2
(3)① +HNO――→ +HO ②黄
3 2
易错辨析1.√ 2.× 3.× 4.√ 5.√ 6.× 7.√ 8.√
提升关键能力
1.D 2.D
3.(1)红棕 Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
(2)3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
(3)被还原的 n(HNO)==0.05 mol;反应生成 n[Cu(NO )]==0.03 mol,所以反应消耗
3 3 2
n(HNO)=0.03 mol×2+0.05 mol=0.11 mol
3
(4)加入稀硫酸后,氢离子与原溶液中的硝酸根离子构成HNO,又能与过量的铜反应
3
4.(1)Fe+NO+4H+===Fe3++NO↑+2HO (2)Fe2+ (3)0.1 0.2 (4)3.36
2
练真题 明考向
1.(1)× (2)× (3)× (4)×
2.D [实验室配制AlCl 溶液时向其中加入少量的稀盐酸以抑制Al3+水解,A不符合题意;
3
蔗糖和淀粉水解时常采用稀硫酸作催化剂,B不符合题意;清洗附有银镜的试管用稀硝酸,
反应原理为3Ag+4HNO(稀)===3AgNO +NO↑+2HO,C不符合题意;苯的磺化是苯和
3 3 2
浓硫酸共热生成苯磺酸的反应,故不需要用到浓硫酸和浓硝酸的混合溶液,D符合题意。]
3.A
4.NaNO NO
3
第 23 讲 氨 铵盐
考点一
整合必备知识
2.刺激性 小 液化 制冷 喷泉
思考 NH 、HO均为极性分子,NH 与HO之间可形成分子间氢键,并且NH 和HO反应。
3 2 3 2 3 2
3.(1)非金属性强 键能大 (2)3 Al(OH) ↓+3NH (3)Cu(OH) +4NH ===[Cu(NH )]2++
3 2 3 3 4
2OH- (4)4NH +5O=====4NO+6HO
3 2 2
易错辨析 1.× 2.× 3.× 4.√ 5.√ 6.× 7.×
提升关键能力
1.(1)2NH +3CuO=====3Cu+3HO+N
3 2 2
(2)8NH +3Cl===N+6NH Cl
3 2 2 4
(3)①4NH +5O=====4NO+6HO
3 2 2
②2NO+O===2NO
2 2
③3NO +HO===2HNO+NO
2 2 3
2.A3.(1) -2 (2)N H +HONH+OH- NH(HSO ) (3)2NH +
2 4 2 2 2 6 4 2 3
NaClO===NH+NaCl+HO 联氨和NO 反应放出大量热且产生大量气体
2 4 2 2 4
考点二
整合必备知识
1.(1)白 (2)2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO NH+OH-=====NH ↑+HO
4 2 2 3 2 3 2
2.蓝色
易错辨析 1.× 2.√ 3.√ 4.× 5.√
提升关键能力
1.A
2.(1)Ca(OH) +2NH Cl=====2NH ↑+CaCl +2HO (2)丙 (3)将湿润的红色石蕊试纸放在
2 4 3 2 2
试管口,若试纸变蓝,则证明氨气已收集满[或用玻璃棒蘸取浓盐酸(或浓硝酸)放在试管口,
若产生白烟,则证明氨气已收集满] (4)乙 2NH +HSO ===(NH )SO (或NH +HSO
3 2 4 4 2 4 3 2 4
===NH HSO ) (5)C
4 4
热点强化10
1.(1)①打开止水夹,挤出胶头滴管中的水
②氨极易溶于水,使烧瓶内的压强迅速减小
(2)①玻璃管中有空气,氨与水不接触,不能被水吸收,烧瓶内压强不减小,故不能产生倒
吸现象
②打开止水夹,用手(或热毛巾等)将烧瓶捂热,使烧瓶内氨膨胀,将导管中的空气排出,使
氨与烧杯中的水接触
(3)NaOH溶液 水 NaOH溶液 水 水 水
2.B
3.(1) (进气管短,出气管长)
(2)观察气泡的速率,控制混合气体的比例
(3)0.036
练真题 明考向
1.(1)× (2)√ (3)× (4)×
2.B
3.(1) A、C、G (2)①产生白色的烟 氯化氢与氨气反应生成了氯化铵小颗粒,氯化铵小
颗粒形成白烟 ②烧杯中的石蕊溶液会倒流进入到B瓶中且呈红色第 24 讲 氮及其化合物的转化关系
构建知识网络
1.(从上到下,从左到右)HNO Cu(NO ) NO NO NO N NH ·H O NH NH Cl
3 3 2 2 2 4 2 3 2 3 4
2.①N+O========2NO
2 2
②4NH +5O=====4NO+6HO
3 2 2
③3NO +HO===2HNO+NO
2 2 3
④3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
⑤Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
⑥NH +HCl===NH Cl
3 4
⑦2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO
4 2 2 3 2
⑧CuO+2HNO===Cu(NO )+HO
3 3 2 2
⑨N+3H2NH
2 2 3
⑩8NH +3Cl===6NH Cl+N
3 2 4 2
3.(1)4NH +5O=====4NO+6HO
3 2 2
(2)Fe(NO ) (3) (4)治疗胃酸过多、作发酵粉、用于泡沫灭火器等(任答其中一
3 3
种即可)
拓展综合应用
1.B 2.C
3.(1)①A 2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑(或 B NH ·H O=====NH ↑+
4 2 2 2 3 3 2 3
HO) ②dcfedci
2
(2)①红棕色气体颜色慢慢变浅 ②6NO +8NH =====7N +12HO ③Z中NaOH溶液产生
2 3 2 2
倒吸现象 ④反应后气体分子数减少,Y管中压强小于外界压强
解析 (1)②氨气是碱性气体,可用碱石灰干燥,其密度小于空气,应采用向下排空气法收
集,氨气极易溶于水,尾气处理时应防止倒吸,则要收集一瓶干燥的氨气,仪器的连接顺序
为发生装置→dcfedci。
(2)打开K ,推动注射器活塞将氨气缓慢通入Y管中,在一定温度和催化剂的作用下发生反
1
应:6NO +8NH =====7N +12HO,随着反应的发生Y管中红棕色气体颜色变浅;反应生
2 3 2 2
成的水蒸气液化后,NO 和NH 反应后气体的物质的量减小,反应容器中的压强减小,打开
2 3
K,Z中的溶液倒吸入Y管中。
2第 25 讲 碳、硅 无机非金属材料
考点一
整合必备知识
1.(1)ns2np2 (2)同素异形体
2.小 能
3.(2)③Ca(HCO )
3 2
易错辨析
1.√ 2.√ 3.× 4.√ 5.× 6.× 7.× 8.√
提升关键能力
1.B 2.B
考点二
整合必备知识
1.化合态 氧 氧化物 硅酸盐
2.(1)Si+2F===SiF Si+4HF===SiF↑+2H↑ Si+2NaOH+HO===NaSiO+2H↑
2 4 4 2 2 2 3 2
(3)SiO+2C=====Si(粗)+2CO↑
2
3.(1)大 高
(2)①SiO +2NaOH===NaSiO +HO ② SiO +CaCO =====CaSiO +CO↑ ③ SiO +
2 2 3 2 2 3 3 2 2
CaO=====CaSiO ④SiO+4HF===SiF↑+2HO
3 2 4 2
(3)光导纤维
4.不 弱 NaCO +HSiO↓ HSiO=====SiO +HO NaSiO +2HCl===2NaCl+
2 3 2 3 2 3 2 2 2 3
HSiO↓
2 3
5.(3)CaO·3MgO·4SiO
2
易错辨析
1.× 2.√ 3.× 4.√ 5.√ 6.√ 7.× 8.× 9.×
提升关键能力
1.Si SiF SiO HSiO NaSiO
4 2 2 3 2 3
2.①SiO+2C=====Si+2CO↑
2
②Si+3HCl=====SiHCl +H
3 2
③SiHCl +H=====Si+3HCl
3 2
④SiO+4HF===SiF↑+2HO
2 4 2
⑤HSiO=====HO+SiO
2 3 2 2
⑥SiO+2NaOH===NaSiO+HO(或SiO+NaCO=====NaSiO+CO↑)
2 2 3 2 2 2 3 2 3 2
⑦NaSiO+CO+HO===NaCO+HSiO↓(或NaSiO+2HCl===2NaCl+HSiO↓)
2 3 2 2 2 3 2 3 2 3 2 3
⑧SiO+CaO=====CaSiO (或SiO+CaCO =====CaSiO +CO↑)
2 3 2 3 3 2
⑨Si+2NaOH+HO===NaSiO+2H↑
2 2 3 23.C
4.(1)蒸馏 (2)①排出装置内的空气,以防爆炸 ②水浴加热
5.B
6.(1)Si O (2)Si O (3)Be Al Si O (或3BeO·Al O·6SiO)
3 n 3 2 6 18 2 3 2
解析 (1)b含有氧原子个数为9,含有3个四面体结构,则含有硅原子个数为3,根据化合
物中Si的化合价为+4、氧元素化合价为-2可知,b的化学式为Si O。(2)c中含有6个四面
3
体结构,所以含有6个Si原子,含有的氧原子数为18,含有氧原子数比6个硅酸根离子少6
个O,带有的电荷为6×(-2)=-12;根据图示可知:若一个单环状离子中 Si原子数为
n(n≥3),则含有n个四面体结构,含有的氧原子比n个硅酸根离子恰好少n个O原子,即含
有n个Si,则含有3n个O,带有的负电荷为n×(-2)=-2n,其化学式为Si O。 (3)根据
n
Si O可知,含有6个硅原子,该硅酸盐所带的负电荷为-12,设铍的个数为x,铝的个数为
n
y,则2x+3y=12,讨论可得x=3、y=2,其化学式为Be Al Si O 或3BeO·Al O·6SiO。
3 2 6 18 2 3 2
考点三
整合必备知识
1.石灰石、黏土 纯碱、石灰石、石英砂 NaSiO+CO↑ CaSiO +CO↑
2 3 2 3 2
易错辨析 1.× 2.√ 3.√ 4.× 5.√
提升关键能力
1.A
2.(1)2Al+2NaOH+2HO===2NaAlO +3H↑ SiO+4HF===SiF↑+2HO
2 2 2 2 4 2
(2)石灰石 SiO +NaCO=====NaSiO +CO↑(或 SiO +CaCO =====CaSiO +CO↑)
2 2 3 2 3 2 2 3 3 2
(3)SiO (4)D
2
3.D
4.(1)SiO+2NaOH===NaSiO+HO
2 2 3 2
(2)①② (3)Si N
3 4
(4)3SiCl +2N+6H=====Si N+12HCl
4 2 2 3 4
练真题 明考向
1.(1)× (2)√ (3)√ (4)×
2.C
第六章 元素及其化合物综合应用
第 26 讲 化学与 STSE 化学与中华文明
考点一提升关键能力
1.B 2.D
3.D [A错误,铅笔芯是用石墨和黏土等制作而成的;B错误,青铜和黄铜都是铜合金;C
错误,硅可制作光感电池;D正确,铝合金硬度大、密度小,可用于高铁建设。]
4.B [高温多雨时施用化肥易使肥料分解损失或随雨水流失,A错误;石灰硫黄合剂与硫
酸混合施用,会因石灰、硫酸发生化学反应而失去相应的功效,C错误;硝酸铵受热或经撞
击易发生爆炸,所以不可直接施用,必须经过改性处理后才能施用,D错误。]
5.B
考点二
提升关键能力
1.C 2.C 3.C
4.C [Xe在元素周期表中位于第五周期0族,故A错误;赤铁矿的主要成分是Fe O ,故
2 3
B错误;2H与3H具有相同的质子数,不同的中子数,互为同位素,故C正确;金刚石是共
价晶体,故D错误。]
5.D
热点强化11
热点专练
1.A 2.A 3.C 4.B
5.D [O 具有强氧化性,A错误;臭氧污染是排放到空气中的氮氧化物引起的二次污染,
3
O 不是工业生产中直接排放的污染物,B错误;夏季太阳辐射强,温度高,有利于NO 光
3 2
解为NO和O,O与O 结合生成O,所以夏季大气中O 的浓度更大,C错误。]
2 3 3
6.D [光化学烟雾中的臭氧、NO 、过氧乙酰硝酸酯都有强氧化性,故A正确;光化学烟
2
雾成分中含有碳氢化合物和醛、酮、过氧乙酰硝酸酯,碳氢化合物即烃类,醛、酮、过氧乙
酰硝酸酯属于烃的衍生物,故C正确;NO 是红棕色气体,光化学烟雾呈现淡蓝色是由于光
2
的折射和反射,故D错误。]
7.C
8.(1)N 排尽装置中的空气,防止NO被O 氧化
2 2
(2)24ClO+C H O+24H+===24ClO ↑+6CO↑+18HO C
6 12 6 2 2 2
(3)40 NH Cl[或(NH )SO 或NH NO ] 作氮肥
4 4 2 4 4 3
(4)4NH ·H O+6NO=====5N+10HO
3 2 2 2
第 27 讲 常见物质(离子)的检验与推断
考点一
整合必备知识1.焰色试验 铂丝用盐酸洗涤后在火焰上灼烧至原火焰颜色
蘸取溶液,放在火焰上灼烧,观察火焰颜色 火焰呈紫色(通过蓝色钴玻璃观察) 火焰呈黄
色 NaOH溶液(浓) 取少量待测溶液于试管中,加入NaOH浓溶液并加热,将湿润红色石
蕊试纸置于试管口 生成有刺激性气味、能使湿润红色石蕊试纸变蓝的气体 KSCN溶液
取少量待测溶液于试管中,加入KSCN溶液 变为红色溶液 NaOH溶液 取少量待测溶液
于试管中,滴加NaOH溶液 产生红褐色沉淀 KSCN溶液、新制的氯水 取少量待测溶液
于试管中,先加入KSCN溶液,再加入新制的氯水 加入KSCN溶液不显红色,加入少量
新制的氯水后,立即显红色 NaOH溶液 取少量待测溶液于试管中,加入NaOH溶液并露
置在空气中 开始时生成白色沉淀,迅速变成灰绿色,最后变成红褐色沉淀 酸性KMnO
4
溶液 取少量待测溶液于试管中,加入酸性KMnO 溶液 溶液紫红色褪去 K[Fe(CN) ]溶
4 3 6
液 取少量待测溶液于试管中,加入K[Fe(CN) ]溶液 生成蓝色沉淀
3 6
2.白色 淡黄色 橙红 黄色 紫红 溶液变蓝 先加入稀盐酸,再加入 BaCl 溶液 白
2
色
3.点燃(纯氢) 火焰呈浅蓝色,干冷的烧杯罩在火焰上方,烧杯内壁有水雾产生 带火星
的木条 木条复燃 湿润的淀粉-KI试纸 试纸变蓝 通入澄清石灰水中 澄清石灰水变浑
浊(通入过量二氧化碳后又变澄清) 通入品红溶液中 品红溶液褪色,加热后又恢复红色
湿润的红色石蕊试纸 试纸变蓝 点燃 火焰呈蓝色,干冷的烧杯罩在火焰上方,烧杯内壁
有水雾产生,加澄清石灰水振荡变浑浊 通入溴的四氯化碳溶液(或酸性KMnO 溶液) 溶
4
液褪色 通入溴的四氯化碳溶液(或酸性KMnO 溶液) 溶液褪色
4
提升关键能力
1.C 2.C
3.D [MgCl 溶液中滴加NaOH溶液至过量,两者发生反应产生白色沉淀,白色沉淀为氢
2
氧化镁,氢氧化镁为中强碱,其不与过量的NaOH溶液发生反应,因此沉淀不消失,A不正
确;FeCl 溶液中滴加KSCN溶液,溶液不变色,B不正确;AgI的溶解度远远小于AgCl,
2
因此,向AgI悬浊液中滴加NaCl溶液至过量,黄色沉淀不可能全部转化为白色沉淀,C不
正确;酸性KMnO 溶液呈紫红色,其具有强氧化性,而乙醇具有较强的还原性,因此,酸
4
性KMnO 溶液中滴加乙醇至过量后溶液紫红色褪色,D正确。]
4
考点二
提升关键能力
1.B 2.A 3.A
4.A [根据实验①可以直接确定没有难溶物PbSO 存在;因为实验①使用了稀硫酸溶解固
4
体,引入了SO,故实验②无法确定Fe (SO ) 的存在;根据实验③可以确定该固体中存在Fe
2 4 3
元素,但是无法确定Fe元素来自Fe (SO ) 还是FeCl ,故只能确定二者之中至少有一个;根
2 4 3 2
据实验④可以确定含有Na元素,则含有NaCl,实验室可用无锈铁丝做焰色试验,说明铁元
素不会干扰Na元素的焰色试验。综上所述,A正确,B、C、D错误。]
5.(1)CO Na+、H+、Al3+、Mg2+、NH(2)NH+OH-===NH ·H O
3 2
(3)2∶1 10.7 (4)存在 0.08
答题规范(3)
规范精练
1.从水层取少量溶液,加入1~2 mL淀粉溶液,加稀盐酸酸化,滴加FeCl 溶液,若溶液
3
变蓝,说明废水中含有I-。另从水层取少量溶液,加入1~2 mL淀粉溶液,加稀盐酸酸化,
滴加NaSO 溶液,若溶液变蓝,说明废水中含有IO
2 3
2.(1)取少量产品溶于足量稀盐酸,静置,取上层清液(或过滤,取滤液)于一试管中,滴加
BaCl 溶液,若产生白色沉淀,则说明含有NaSO 杂质(合理即可)
2 2 4
(2)取矿石少许,加稀硫酸充分溶解后,向其中滴加酸性高锰酸钾溶液,若紫色褪去,证明
矿石中含有FeO(不能加盐酸溶解)
3.取少量装置D内溶液于试管中,滴加BaCl 溶液,生成白色沉淀,加入足量稀盐酸后,
2
沉淀完全溶解,放出无色有刺激性气味的气体
第 28 讲 常见气体的实验室制备、净化和收集
整合必备知识
2.(1)O NH
2 3
4.(2)Cu粉
提升关键能力
1.C 2.A 3.B
4 . (1) 甲 ( 或 乙 ) MnO + 4HCl( 浓 )=====MnCl + Cl↑ + 2HO[ 或 2KMnO +
2 2 2 2 4
16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO] (2)长颈漏斗 贮存少量气体[或平衡气压(安
2 2 2
全瓶)或防倒吸] (3)NaClO、NaOH
5.(1)打开装置Ⅰ的弹簧夹,通入N 排出装置中的空气,然后关闭弹簧夹 (2)饱和亚硫酸
2
氢钠溶液 通过观察气泡调控SO 的生成速率;作安全瓶 (3)bd
2
6.D 7.A
8.D [A装置是氯气发生装置,B为除去氯气中的氯化氢,C为干燥装置,D为氯气与铁
的反应装置,E为氯化铁的收集装置,氯化铁易水解,故F装置是尾气吸收装置并防止空气
中的水蒸气进入收集器,A正确;FeCl 蒸气遇冷变为固体,若导管较细,容易堵塞,所以
3
硬质玻璃管直接连接收集器,B正确;FeCl 固体溶于水发生水解,配制FeCl 溶液时应先将
3 3
FeCl 固体溶于少量盐酸,抑制水解,再加水稀释,C正确;实验开始时,应先点燃A处酒
3
精灯,至装置中充满氯气后,再点燃D处酒精灯,D错误。]
9.(1)分液漏斗、锥形瓶
(2)刚好没过MnO 固体 试管内的HO 溶液被压入长颈漏斗中,与MnO 分离
2 2 2 2(3)液面上升 打开弹簧夹K (4)ab
2
解析 (2)乙装置是启普发生器的简易装置,可以随时控制反应的发生和停止。用粘合剂将
MnO 制成团,放在多孔塑料片上,连接好装置,气密性良好后打开活塞 K ,经长颈漏斗向
2 1
试管中缓慢加入3% H O 溶液至刚好没过MnO 固体,此时可以产生氧气,氧气通过导管导
2 2 2
出。欲使反应停止,关闭活塞K ,此时由于气体还在产生,使容器内压强增大,可观察到
1
试管内的HO 溶液被压入长颈漏斗中,与MnO 分离。(3)丙装置用圆底烧瓶盛装HO 溶液,
2 2 2 2 2
可用于制备较多O ,催化剂铂丝可上下移动,可以控制反应速率。制备过程中如果体系内
2
压强过大,HO 溶液会被压入安全管中,可观察到安全管中液面上升,圆底烧瓶中液面下
2 2
降。此时可以将铂丝抽离HO 溶液,使反应速率减慢,还可以打开弹簧夹K ,使烧瓶内压
2 2 2
强降低。(4)催化剂铂丝可上下移动,可以控制制备反应的开始和结束,a正确;催化剂与液
体接触的面积越大,反应速率越快,可通过调节催化剂与液体接触的面积来控制反应的速率,
b正确;丙装置用圆底烧瓶盛装HO 溶液,与乙装置相比,可用于制备较多O ,但产物中
2 2 2
的O 含量和杂质种类和乙中没有区别,c错误。
2
10.(1)恒压滴液漏斗 平衡气压,便于硫酸顺利滴下 (2)防止倒吸 (3)SO +
2
MnO ===MnSO 增大反应物的接触面积,加快反应速率,增大二氧化硫的吸收效率 (4)
2 4
氢氧化钠溶液 防止倒吸
热点强化12
1.(1)× (2)× (3)× (4)×
2.(1)× (2)× (3)× (4)×
3.(1)× (2)√ (3)√ (4)√ (5)√ (6)√ (7)√ (8)× (9)√ (10)√ (11)√ (12)×
(13)× (14)× (15)× (16)× (17)√ (18)× (19)√ (20)×
第 29 讲 非金属及其化合物拓展创新
考点一
拓展综合应用
1.(1)4s24p4 硫、碲 (2)亚硒酸钠 (3)粉碎 过滤 (4)Na SeO
2 4
+4C=====NaSe+4CO↑ (5)2Se2-+O +2CO===2Se↓+2CO(或 2Se2-+O +4CO +
2 2 2 2 2
2HO===2Se↓+4HCO)
2
2.(1)CuSO (2)过滤 加稀硝酸充分反应,过滤、洗涤、干燥
4
(3)Cu2++2e-===Cu (4)①80 ℃,2.0 h ②SO 的溶解度随着温度的升高而降低,SO 浓度
2 2
降低,粗碲的产率会降低 ③TeO2++2SO +3HO===Te↓+2SO+6H+
2 2
考点二
拓展综合应用1.A 2.D
3.(P O )(n+2)-
n 3n+1
解析 由三磷酸根离子的结构可知,中间P原子连接的4个O原子中,2个O原子完全属于
该P原子,另外2个O原子分别属于另外2个P原子,故属于该P原子的O原子数为2+
2×=3,属于左、右两边的2个P原子的O原子数为3×2+×2=7,故若这类磷酸根离子
中含n个P原子,则O原子个数为3n+1,又O元素的化合价为-2,P元素的化合价为+
5,故该离子所带电荷为-2×(3n+1)+5n=-n-2,这类磷酸根离子的化学式可用通式表
示为(P O )(n+2)-。
n 3n+1
4.(1)①-2 4H++2Sn2++2As S===2HS↑+2Sn4++As S
2 3 2 4 4
②SO As O+2HO+HO===2HAsO
2 2 3 2 2 2 3 4
(2)2AsH(g)+3O(g)===As O(s)+3HO(l) ΔH=-5b kJ·mol-1
3 2 2 3 2
第 30 讲 陌生过渡金属及其化合物的制备流程分析
拓展综合应用
1.C
2.B [酸浸时采用高温可以使反应速率加快,而沉锰时如果温度过高,氨水和NH HCO 受
4 3
热分解,MnCO 溶解度增大,导致沉锰效率降低,因此应该在低温下进行沉锰,A错误;
3
SiO 、生成的S均不溶于稀硫酸,因此用稀硫酸溶解后的滤渣1的成分中含有S和SiO ,B
2 2
正确;调pH的目的是使溶液中的Fe3+、Al3+转化为Fe(OH) 、Al(OH) 沉淀,从而达到除去
3 3
Fe3+、Al3+的目的,C错误;沉锰操作中加入NH ·H O和NH HCO ,反应的离子方程式为
3 2 4 3
2HCO+Mn2++2NH ·H O===MnCO ↓+CO+2NH+2HO,D错误。]
3 2 3 2
3.B
4.(1)SiO(或不溶性硅酸盐) MnO +MnS+2HSO ===2MnSO +S+2HO (2)将Fe2+氧化
2 2 2 4 4 2
为Fe3+ (3)4.7 (4)NiS和ZnS (5)F-与H+结合生成弱电解HF,导致MgF (s)Mg2+(aq)
2
+2F-(aq)平衡向右移动
5.(1)将矿石粉碎或增大空气的量等(任选一条) (2)+3 4FeCr O +7O +
2 4 2
8NaCO=====2Fe O+8NaCrO+8CO
2 3 2 3 2 4 2
(3)2CrO+2H+Cr O+HO 4×1014 (4)pH高于10时,AlO不能完全转化为氢氧化铝,
2 2
pH低于6时,氢氧化铝会继续溶解转化为铝离子,故需控制pH在6~10的范围,让AlO中
铝以氢氧化铝形式存在而过滤除去 (5)2-a
6.(1)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO (2)碱石灰 吸收未反应完的Cl,防
2 2 2
止空气中的水蒸气进入D装置使CoCl 潮解 (3)250 mL容量瓶 胶头滴管 大于 (4)防止
2
温度过高使HO 和NH ·H O分解
2 2 3 2
(5)2CoCl +2NH Cl+10NH ·H O+HO=====2[Co(NH )]Cl +12HO (6)趁热过滤 冷却结
2 4 3 2 2 2 3 6 3 2晶
第七章 原子结构与性质
第 31 讲 原子结构 核外电子排布规律
考点一
整合必备知识
1.(1)核素 元素 化学 (2)中子 质子 ①质子数 ②质子数 (3)质量数 质子数
2.(1)质子数 质子 中子 质子 中子
(2)①中子数 质子数 几乎完全相同 差异较大
(3)氕 D 氘 T 氚
易错辨析 1.√ 2.× 3.× 4.× 5.× 6.√
提升关键能力
1.B
2.(1)核素 同位素 (2)O、O
2 3
(3)30 24 (4)7 5
3.B 4.A
考点二
整合必备知识
1.(1)K L M N 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 1 1 3 1 3 5 1 3
5 7 1 4 9 16 2 8 18 32 (2)球 哑铃 3 (3)25,50 (4)①1s<2s<2p<3s<3p<3d
②2s<2p=2p=2p
x y z
2.(1)最低能量状态 跃迁 (2)吸收 释放 吸收 发射
3.(1)①能量最低原理 ②泡利原理 2 相反 ③洪特规则
易错辨析 1.√ 2.× 3.× 4.× 5.√ 6.√
提升关键能力
1.(1) (2)K+和P3- (3)发射光谱
2.D C
3.电子由较高能量的激发态跃迁到较低能量的激发态或基态时,以光的形式释放能量
4.(1)9 (2)3d24s2 12 22 (3)4 洪特规则 (4)15
5.(1)1 4d25s2 3 (2)4 (3)3∶1 (4)6.(1)S Cl K Ca (2)①N ② Fe 1s22s22p63s23p63d64s2(或
[Ar]3d64s2)
练真题 明考向
1.A
2.(1)①2s22p3 ②× (2)3s23p4 (3) (4)5s25p3
3.(1)A (2)4∶5
第 32 讲 元素周期表 元素的性质
考点一
整合必备知识
1.
2.(1)ns1~2 ns2np1~5 ns2np6 (n-1)d10ns1~2 (n-1)d1~5ns1~2 (n-1)d6~9ns1~2
易错辨析 1.× 2.√ 3.× 4.√
提升关键能力
1.(1)第三周期第ⅢA族 (2)a+1或a+11
2.A
3.O、P、Cl
4.A:Na 11 s 三 ⅠA
B:Fe 26 d 四 Ⅷ
C:Cu 29 ds 四 ⅠB
D:S 16 p 三 ⅥAE:Cl 17 p 三 ⅦA
考点二
整合必备知识
1.原子序数 原子的核外电子排布
2.相同 依次增加 相同 逐渐减小 逐渐增大 逐渐减弱 逐渐增强 逐渐增强 逐渐
减弱 主族序数-8 主族序数 逐渐增强 逐渐减弱 逐渐减弱 逐渐增强 逐渐增强
逐渐减弱
3.(1)同周期元素从左到右,元素第一电离能呈增大趋势,原因是同周期元素从左到右,核
电荷数增大,原子半径减小,原子失去电子越来越困难。同一主族元素从上到下,元素第一
电离能逐渐减小。
(2)Be:2s2、N:2s22p3、Mg:3s2、P:3s23p3。发生该现象的原因是它们原子核外价层电子
排布处于半充满或全空的稳定状态,失去电子较为困难,故第一电离能比相邻元素的第一电
离能大。
(3)X、Y、Z三种元素最外层电子数分别是2、3、1;这三种元素分别是Mg、Al、Na。
4.吸引力 越大 4.0 1.0 增大 减小
易错辨析 1.× 2.× 3.× 4.× 5.×
提升关键能力
1.(1)> > (2)< < (3)> > (4)< < (5)> > (6)> >
2.(1)> > > > (2)< < (3)> > (4)< < (5)> < (6)> >
3.C
4.C [由表中数据可知,R元素的第三电离能与第二电离能的差距较大,故最外层有 2个
电子,最高正价为+2价,位于第ⅡA族,可能为Be或Mg元素,故A、B、D错误;短周
期第ⅡA族(ns2np0)的元素,因np轨道处于全空状态,比较稳定,故其第一电离能大于同周
期相邻主族元素,C正确。]
5.(1)N (2)镧
6.(1)0.9~1.5
(2)非金属性越强,电负性越大;金属性越强,电负性越小
(3)离子化合物 共价化合物 共价化合物
(4)负 Cl的电负性大于P,Cl对键合电子的吸引能力强
答题规范(4)
规范精练
1.I(O)>I(S),氧原子半径小,原子核对最外层电子的吸引力大,不易失去一个电子
1 1
2.Cu Cu的第一电离能失去的是4s1电子,第二电离能失去的是3d10的电子,Zn的第一电
离能失去的是4s2电子,第二电离能失去的是4s1的电子,失去2个电子后Zn2+的3d10电子处
于全充满状态
练真题 明考向
1.C 2.D3.A [核外电子排布相同时,核电荷数越大,离子半径越小,故半径大小为r(Al3+) 中心原子的电负性A强于B,中心原子的电负性越大,成键电子对离中心原子越
近,斥力越大,键角也越大
例4 < 电负性:B>A>C,在AB 中成键电子对离中心原子较远,斥力较小,因而键角
3
较小
变式训练4 ①> 中心原子的电负性N强于P,中心原子的电负性越大,成键电子对离中
心原子越近,斥力越大,键角也越大 ②< F的电负性比H大,NF 中成键电子对离中心
3
原子较远,斥力较小,因而键角也较小
规范精练
1.大于 HBO 分子中的B采取sp2杂化,而BH中的B采取sp3杂化,sp2杂化形成的键角
3 3
大于sp3杂化
2.> N原子上有孤电子对,由于孤电子对与成键电子对的排斥力更大,使得Si—N—Si键
角较小
3.小 SeO中中心Se原子采取sp3杂化,键角为109°28′,SeO 中中心Se原子采取sp2杂
3
化,键角为120°
热点强化14
(一)
1.0 sp 直线形 1 sp2 V形 2 sp3 V形 0 sp2 平面三角形 1 sp3 三角锥形
0 sp3 四面体形
热点专练
1.A 2.D
3.C [硝酸根离子中,成键电子对为3,孤电子对数为×(5+1-3×2)=0,因此其空间结
构为平面三角形,A错误;硝酸盐易溶于水,B错误;五元环为平面结构,可知该化合物中
五元环上的5个原子均为sp2杂化,它们的杂化方式相同,C正确;该化合物受热迅速生成
N,化学性质不稳定,D错误。]
2
4.(1)正四面体形 4 sp3 (2)正四面体 sp3
5.(1)平面三角形 sp2、sp3 8
(2)KCl,C—F的极性大于C—Cl的极性,导致氟乙酸羧基中的羟基的极性更大,
更易电离出H+,故氟乙酸的酸性大于氯乙酸的酸性
3.烷基(R—)是推电子基团,烷基越长推电子效应越大,使羧基中的羟基的极性越小,羧酸
的酸性越弱
4.NO、HO 、NO 、SO 、CHCl 、HCN、HCHO、PCl P 、C 、Cl 、CS 、C H 、
2 2 2 2 2 2 3 4 60 2 2 2 2
SO 、BF、PCl
3 3 5
考点二
整合必备知识
1.(1)无 有 氢键 范德华力 越大 越大
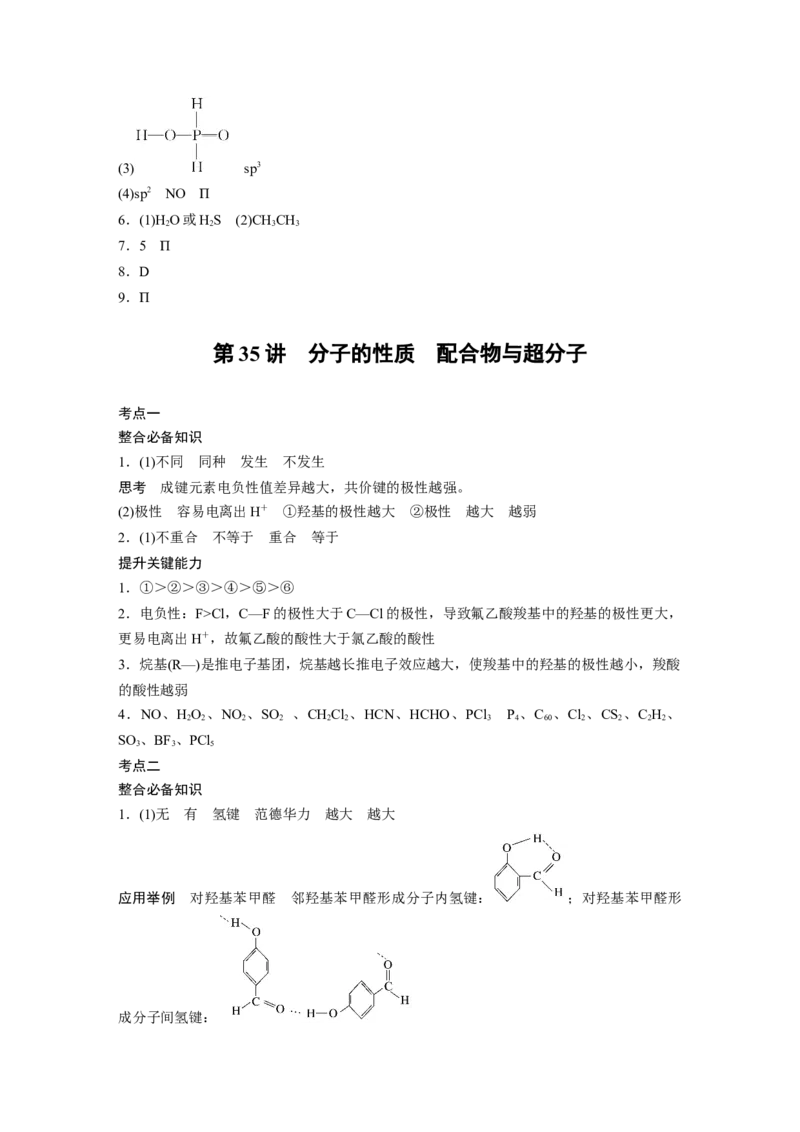
应用举例 对羟基苯甲醛 邻羟基苯甲醛形成分子内氢键: ;对羟基苯甲醛形
成分子间氢键:2.(1)①非极性 极性 (2)增大
3.(1)镜像 不能叠合 (2)手性异构体 (3)四个不同基团或原子
易错辨析 1.× 2.× 3.√ 4.× 5.×
提升关键能力
1.C 2.C
3.(1)H O 为极性分子,而CS 为非极性溶剂,根据“相似相溶”规律,HO 难溶于CS
2 2 2 2 2 2
(2)NH 、CHCHOH、CHCHO都是极性分子,且都能与HO形成氢键
3 3 2 3 2
4.(1)A A易形成分子内氢键,B易形成分子间氢键,所以B的沸点比A的高 (2)苯胺分
子间存在氢键
(3)S 相对分子质量大,分子间范德华力大
8
(4)H O>CHOH>CO >H HO与CHOH均为极性分子,HO中氢键比甲醇多;CO 与
2 3 2 2 2 3 2 2
H 均为非极性分子,CO 相对分子质量较大,范德华力较大
2 2
5.
考点三
整合必备知识
1.(1)孤电子对 配位键 (2)→ 相同
2.(1)分子或离子 配位键 配位原子 配位体 配位数
3.(1)两种或两种以上 分子间相互作用 (3)分子识别 自组装
易错辨析 1.√ 2.√ 3.× 4.× 5.× 6.√
提升关键能力
1.C 2.A
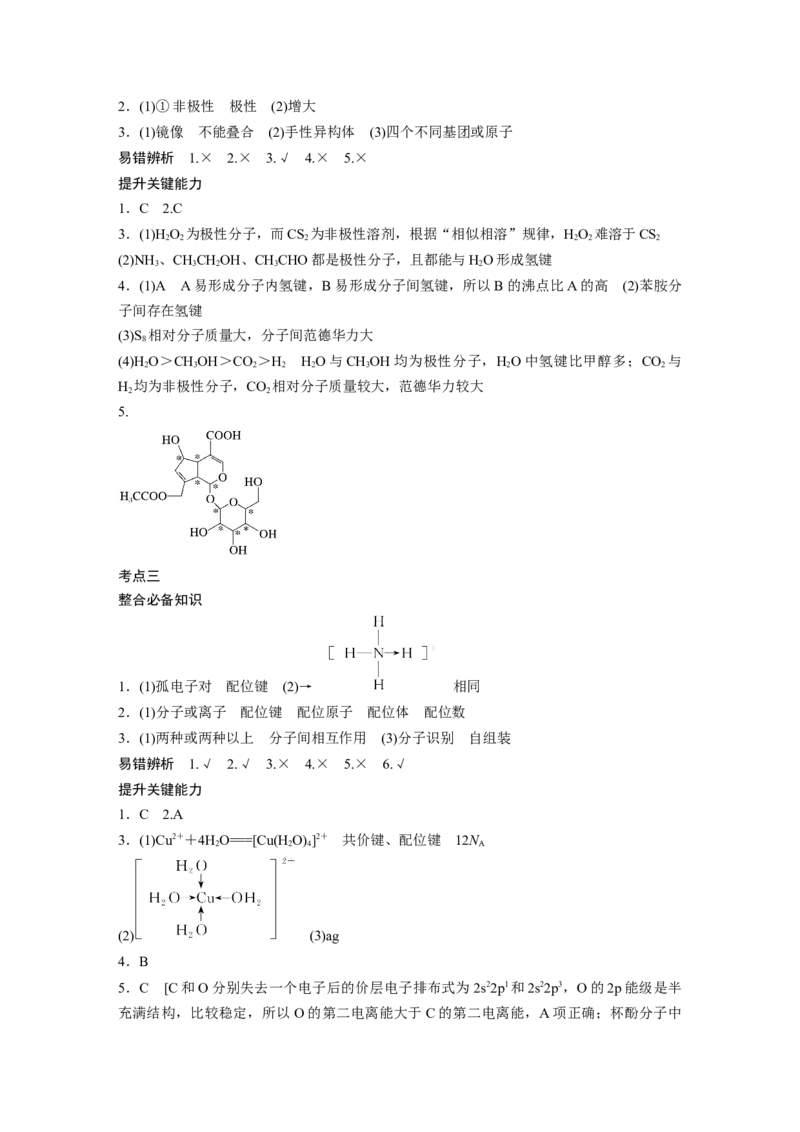
3.(1)Cu2++4HO===[Cu(H O) ]2+ 共价键、配位键 12N
2 2 4 A
(2) (3)ag
4.B
5.C [C和O分别失去一个电子后的价层电子排布式为2s22p1和2s22p3,O的2p能级是半
充满结构,比较稳定,所以O的第二电离能大于C的第二电离能,A项正确;杯酚分子中含有苯环结构,具有大π键,B项正确;C 中只含有C元素,无法形成氢键,C项错误;
60
金刚石是共价晶体,C 为分子晶体,D项正确。]
60
练真题 明考向
1.B
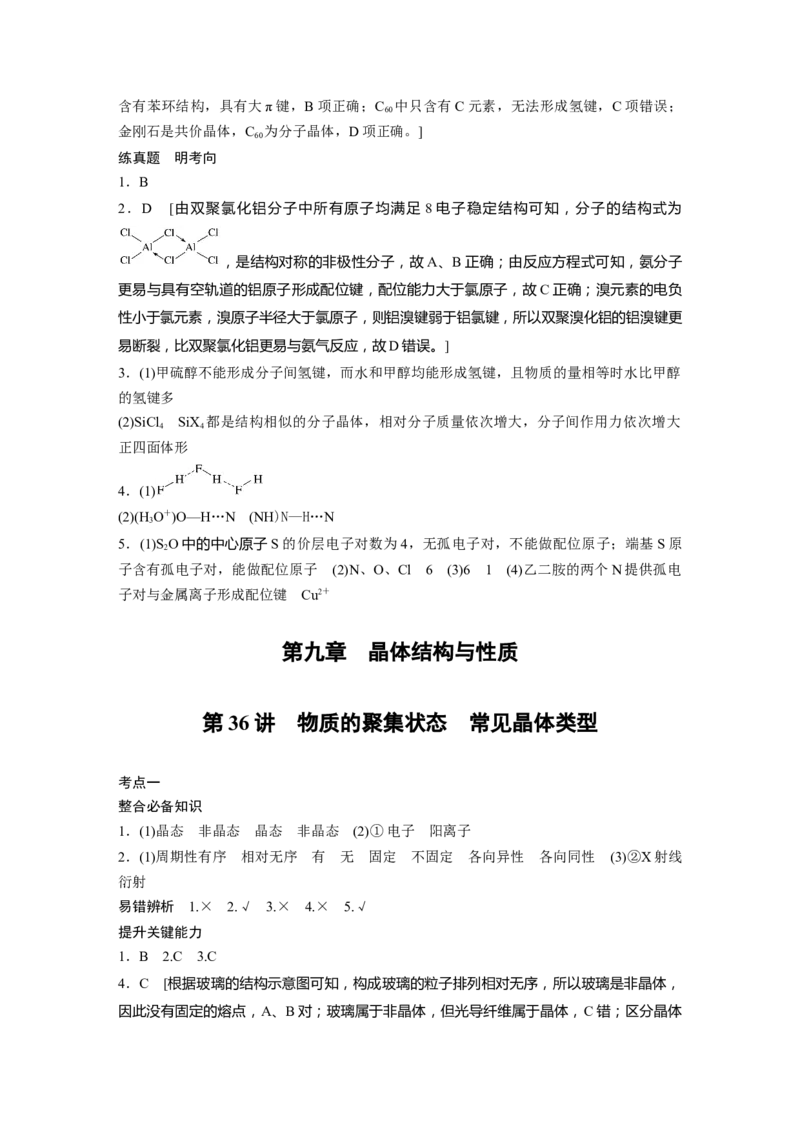
2.D [由双聚氯化铝分子中所有原子均满足 8 电子稳定结构可知,分子的结构式为
,是结构对称的非极性分子,故A、B正确;由反应方程式可知,氨分子
更易与具有空轨道的铝原子形成配位键,配位能力大于氯原子,故C正确;溴元素的电负
性小于氯元素,溴原子半径大于氯原子,则铝溴键弱于铝氯键,所以双聚溴化铝的铝溴键更
易断裂,比双聚氯化铝更易与氨气反应,故D错误。]
3.(1)甲硫醇不能形成分子间氢键,而水和甲醇均能形成氢键,且物质的量相等时水比甲醇
的氢键多
(2)SiCl SiX 都是结构相似的分子晶体,相对分子质量依次增大,分子间作用力依次增大
4 4
正四面体形
4.(1)
(2)(H O+)O—H…N (NH)N—H…N
3
5.(1)S O中的中心原子S的价层电子对数为4,无孤电子对,不能做配位原子;端基S原
2
子含有孤电子对,能做配位原子 (2)N、O、Cl 6 (3)6 1 (4)乙二胺的两个N提供孤电
子对与金属离子形成配位键 Cu2+
第九章 晶体结构与性质
第 36 讲 物质的聚集状态 常见晶体类型
考点一
整合必备知识
1.(1)晶态 非晶态 晶态 非晶态 (2)①电子 阳离子
2.(1)周期性有序 相对无序 有 无 固定 不固定 各向异性 各向同性 (3)②X射线
衍射
易错辨析 1.× 2.√ 3.× 4.× 5.√
提升关键能力
1.B 2.C 3.C
4.C [根据玻璃的结构示意图可知,构成玻璃的粒子排列相对无序,所以玻璃是非晶体,
因此没有固定的熔点,A、B对;玻璃属于非晶体,但光导纤维属于晶体,C错;区分晶体与非晶体最科学的方法是对固体进行X射线衍射实验,D对。]
考点二
整合必备知识
1.分子 原子 阴、阳离子 范德华力 共价键 金属键 离子键 很大 较大 很高
2.(1)①12 ②4 2 (2)②sp3 109°28′ 正四面体 6 12 顶点 面心 4 8 4 2
1∶2 12 6 6 4N 8 6 4 16 8 16 (3)①6 6 6 4 4 ②8 8 8 ③8 4
A
4 8 (4)②范德华力 2 sp2
易错辨析 1.× 2.× 3.× 4.× 5.× 6.×
提升关键能力
1.(1)NaCl、NaS (2)NaOH、(NH )S (3)(NH )S (4)Na S (5)H O 、CO 、CCl 、
2 4 2 4 2 2 2 2 2 2 4
C H、晶体氩 (6)SiO、SiC
2 2 2
2.D 3.A 4.D
练真题 明考向
1.C 2.A 3.A
4.B [石墨晶体中每个碳原子上未参与杂化的1个2p轨道上电子在层内离域运动,故石墨
晶体能导电,而(CF) 中没有未参与杂化的2p轨道上的电子,故与石墨相比,(CF) 导电性减
x x
弱,A错误;石墨层间插入F后形成的C—F键长短,键能极大,分子结构稳定性增强,抗
氧化性增强,B正确,C错误;由题干结构示意图可知,在(CF) 中每个C与周围的3个碳原
x
子、1个F原子形成共价键,每个C—C被2个碳原子共用,即1 mol (CF) 中含有2.5x mol
x
共价单键,D错误。]
5.共价晶体中,原子半径越小,共价键键能越大,熔点越高,原子半径:C<Si(或键长:
C—C<Si—Si),键能:C—C>Si—Si
答题规范(6)
例1 (1)金刚石是共价晶体,而NaCl是离子晶体 (2)SiO 是共价晶体,而CO 是分子晶体
2 2
例2 (1)同为分子晶体,NH 分子间存在较强的氢键,而PH 分子间仅有较弱的范德华力
3 3
(2)同为分子晶体,CS 的相对分子质量大,范德华力强,熔、沸点高 (3)同为分子晶体,两
2
者相对分子质量相同,CO的极性大,熔、沸点高
(4) 形成分子内氢键,而 形成分子间氢键,分子间氢键
会使沸点升高
例3 晶体硅与SiC均属于共价晶体,晶体硅中的Si—Si比SiC中Si—C的键长长,键能低,
所以熔点低
例4 (1)ZnO和ZnS同属于离子晶体,O2-半径小于S2-,故ZnO离子键强(或晶格能大),
熔点高 (2)同为离子晶体,Fe2+半径比Fe3+大,所带电荷数也小于Fe3+,FeO的离子键(或
晶格能)比Fe O 弱(或小)
2 3规范精练
1.离子键 FeF 为离子晶体,FeBr 属于分子晶体
3 3
2.离子晶体 K+的半径大于Na+,KO的离子键弱于NaO
2 2
3.联氨分子间形成氢键的数目多于氨分子形成的氢键
4.BN 两种晶体均为共价晶体,N和B原子半径较小,键能较大,熔点较高
5.(1)两者均为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高
(2)MnS中阴阳离子所带电荷数比NaCl的多,离子键强度更大
第 37 讲 晶胞结构分析与计算
考点一
整合必备知识
1.(2)任何间隙 平行 取向
提升关键能力
1.1∶1 KFe (CN)
2 6
2.4∶1∶2∶1
3.共价晶体 SiP
2
4.BO[或(BO)]
2
5.8
6.12
考点二
提升关键能力
1.CsPbI
3
2.4 ×1021
3.①KSeBr ②××107
2 6
4.①O MgGeO ②×1021
2 4
解析 ①由晶胞结构可知,晶胞中位于顶点、面上、棱上和体内的 X原子数为8×+6×+
4×+3=8,位于体内的Y原子数和Z原子数分别为4和16,由Ge和O原子的个数比为
1∶4可知,X为Mg原子、Y为Ge原子、Z为O原子,则该化合物的化学式为MgGeO 。
2 4
②由晶胞的质量公式可得 g=abc×10-21 cm3×ρ,解得ρ=×1021 g·cm-3。
热点强化15
(一)
例 (,,) (,,)
对点训练
1.(,,0) (0,0,)
2.(1)BiLi (2)(0.25,0.75,0.25)
33.C (1,,)
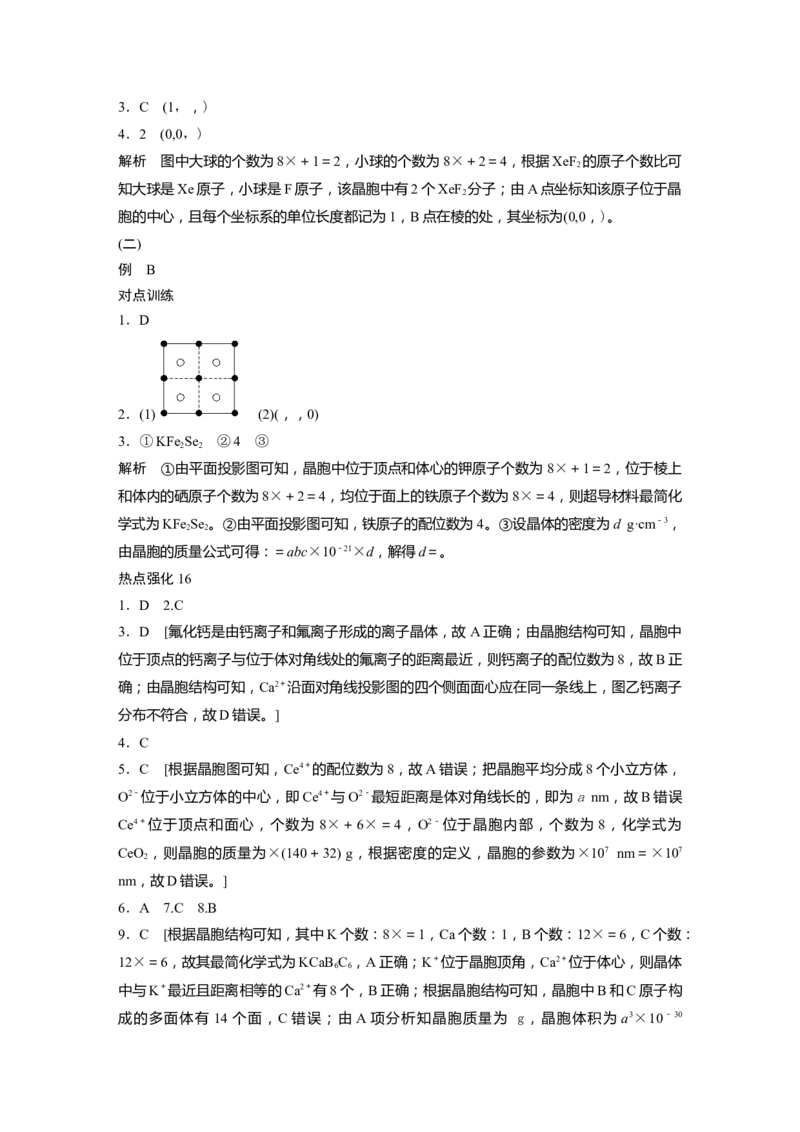
4.2 (0,0,)
解析 图中大球的个数为8×+1=2,小球的个数为8×+2=4,根据XeF 的原子个数比可
2
知大球是Xe原子,小球是F原子,该晶胞中有2个XeF 分子;由A点坐标知该原子位于晶
2
胞的中心,且每个坐标系的单位长度都记为1,B点在棱的处,其坐标为(0,0,)。
(二)
例 B
对点训练
1.D
2.(1) (2)(,,0)
3.①KFe Se ②4 ③
2 2
解析 ①由平面投影图可知,晶胞中位于顶点和体心的钾原子个数为8×+1=2,位于棱上
和体内的硒原子个数为8×+2=4,均位于面上的铁原子个数为8×=4,则超导材料最简化
学式为KFeSe 。②由平面投影图可知,铁原子的配位数为4。③设晶体的密度为d g·cm-3,
2 2
由晶胞的质量公式可得:=abc×10-21×d,解得d=。
热点强化16
1.D 2.C
3.D [氟化钙是由钙离子和氟离子形成的离子晶体,故A正确;由晶胞结构可知,晶胞中
位于顶点的钙离子与位于体对角线处的氟离子的距离最近,则钙离子的配位数为8,故B正
确;由晶胞结构可知,Ca2+沿面对角线投影图的四个侧面面心应在同一条线上,图乙钙离子
分布不符合,故D错误。]
4.C
5.C [根据晶胞图可知,Ce4+的配位数为8,故A错误;把晶胞平均分成8个小立方体,
O2-位于小立方体的中心,即Ce4+与O2-最短距离是体对角线长的,即为a nm,故B错误
Ce4+位于顶点和面心,个数为 8×+6×=4,O2-位于晶胞内部,个数为 8,化学式为
CeO ,则晶胞的质量为×(140+32) g,根据密度的定义,晶胞的参数为×107 nm=×107
2
nm,故D错误。]
6.A 7.C 8.B
9.C [根据晶胞结构可知,其中K个数:8×=1,Ca个数:1,B个数:12×=6,C个数:
12×=6,故其最简化学式为KCaB C ,A正确;K+位于晶胞顶角,Ca2+位于体心,则晶体
6 6
中与K+最近且距离相等的Ca2+有8个,B正确;根据晶胞结构可知,晶胞中B和C原子构
成的多面体有 14 个面,C 错误;由 A 项分析知晶胞质量为 g,晶胞体积为 a3×10-30cm3,则其密度为 g·cm-3,D正确。]
10.D 11.C 12.A
13.C [Ti是22号元素,位于元素周期表第四周期第ⅣB族,故A错误;由晶胞结构图可
知,i原子与q原子处于中心对称位置,所以i的原子坐标为(0.81a,0.19a,0.5c),故C正确;
由晶胞结构图可知,该晶胞中有2个Ti原子,4个O原子,相当于有2个TiO,所以晶体密
2
度为 g·cm-3= g·cm-3,故D错误。]
14.D
15.A [根据均摊法,普鲁士蓝晶胞中含Fe:8×+6×+12×+1=8、含CN-:24×+
24×+6=24、含Na+:4,根据各元素化合价代数和等于 0,可知Fe2+ 与Fe3+个数比为
1∶1,A错误;根据晶胞图,格林绿晶体中Fe3+周围等距且最近的Fe3+数为6,B正确;每
个Fe(CN) 晶胞有8个Fe3+完全转化为NaFe(CN) 晶胞,转移8个e-,C正确;根据均摊法,
3 3
普鲁士白晶胞中含Fe:8×+6×+12×+1=8、含CN-:24×+24×+6=24、含Na+:
8,若普鲁士白的晶胞棱长为a pm ,则其晶体的密度为 g·cm-3=×1030 g·cm-3,D正
确。]
第十章 化学反应与能量
第 38 讲 反应热 热化学方程式
考点一
整合必备知识
1.(2)等于
2.③⑥⑦⑧⑨ ①②④⑤
3.(1)吸热 > < 放热
易错辨析 1.× 2.× 3.× 4.×
提升关键能力
1.(1)d (2)确保盐酸被完全中和 (3)-51.8 kJ·mol-1 (4)①偏低 弱酸或弱碱在溶液中部
分电离,在反应过程中,弱酸或弱碱会继续电离,而电离是吸热的过程 ②不相等 相等
中和反应反应热是以生成1 mol液态水为标准的,与反应物的用量无关
2.(1)< (2)吸热 放热
(3)E E E+|ΔH| E+|ΔH|
1 2
3.(1)Bi O 由图可知,使用BiO 催化剂时,相对能量减小得多,趋于更稳定状态 (2)<
2 3 2 3
(3)0.38 eV 0.32 eV
(4)*CO+HCO+e-===*CO+*HCOO-4.+124 kJ·mol-1
解析 ΔH=E(C—C)+6E(C—H)-E(C==C)-4E(C—H)-E(H—H)=(347+6×414-615-
4×414-436) kJ·mol-1=+124 kJ·mol-1。
5.460
考点二
整合必备知识
2.物质 能量 2 mol H (g)与1 mol O (g)反应生成2 mol液态水时放出的热量为571.6 kJ
2 2
提升关键能力
1.(1)× 物质未标明聚集状态。
(2)× ΔH单位为kJ·mol-1。
(3)√
(4)× SO 与O 的反应为可逆反应,1 mol SO 、0.5 mol O 混合反应,消耗的SO 物质的量
2 2 2 2 2
小于1 mol。
(5)× 同素异形体应指明名称。
(6)× 液态肼的燃烧为放热反应,ΔH应为“-”号。
2.(1)N H(g)+O(g)===N(g)+2HO(g) ΔH=-534.4 kJ·mol-1
2 4 2 2 2
(2)4CuCl(s)+O(g)===2CuCl (s)+2CuO(s) ΔH=-177.6 kJ·mol-1
2 2
(3)2NH (g)N(g)+3H(g) ΔH=+92 kJ·mol-1
3 2 2
3.(1)NO (g)+CO(g)===NO(g)+CO(g) ΔH=-234 kJ·mol-1
2 2
(2)M(s)+CO(g)===N(s) ΔH=-48.96 kJ·mol-1
2
(3)①ClO ②3ClO-(aq)===ClO(aq)+2Cl-(aq) ΔH=-117 kJ·mol-1
考点三
整合必备知识
1.(1)1 完全燃烧
2.(2)煤 石油 天然气
易错辨析 1.√ 2.√ 3.× 4.√ 5.√ 6.× 7.×
提升关键能力
1.(1)S (s)+8O(g)===8SO (g) ΔH=-8a kJ·mol-1 (2)SO (g)===SO (g)+O(g) ΔH=+b
8 2 2 3 2 2
kJ·mol-1
2.(1) (2)426 NH(g)+O(g)===N(g)+2HO(g) ΔH=-577 kJ·mol-1
2 4 2 2 2
(3)N H+2HO===N↑+4HO↑ (4)816 kJ (5)H O 高温下稳定,且更容易液化储存
2 4 2 2 2 2 2 2
练真题 明考向
1.A
2.ab
3.C [根据表格中的数据可知,H 的键能为218 kJ·mol-1×2=436 kJ·mol-1,A正确;由
2表格中的数据可知O 的键能为249 kJ·mol-1×2=498 kJ·mol-1,由题中信息可知HO 中氧
2 2 2
氧单键的键能为214 kJ·mol-1,则O 的键能大于HO 中氧氧单键的键能的两倍,B正确;
2 2 2
由表格中的数据可知HOO===HO+O,解离其中氧氧单键需要的能量为249 kJ·mol-1+39
kJ·
mol-1-10 kJ·mol-1=278 kJ·mol-1,HO 中氧氧单键的键能为214 kJ·mol-1,C错误;由表
2 2
中的数据可知HO(g)+O(g)===HO(g)的ΔH=-136 kJ·mol-1-(-242 kJ·mol-1)-249 kJ·
2 2 2
mol-1=-143 kJ·mol-1,D正确。]
4.(1)H (g)+O(g)===HO(l) ΔH=-286 kJ·mol-1
2 2 2
(2)6CO (g)+6HO(l)===C H O(s)+6O(g) ΔH=+2 804 kJ·mol-1
2 2 6 12 6 2
(3)N (g)+3H(g)2NH (g) ΔH=-(a-b) kJ·mol-1 降低反应的活化能
2 2 3
第 39 讲 盖斯定律及应用
考点一
整合必备知识
1.始态和终态 反应的途径
3.aΔH -ΔH ΔH+ΔH
2 2 1 2
提升关键能力
1.C
2.3SO (g)+2HO(g)===2HSO (l)+S(s) ΔH=-254 kJ·mol-1
2 2 2 4 2
3.ΔH-ΔH
2 1
4.(a+c-2b)
5.+118
考点二
提升关键能力
1.ΔH<ΔH
1 2
2.ΔH<ΔH
2 1
3.由反应①-反应②可得2Al(s)+Fe O(s)===2Fe(s)+Al O(s) ΔH=ΔH -ΔH ,已知铝热
2 3 2 3 1 2
反应为放热反应,故ΔH<0,ΔH<ΔH。
1 2
4.B
第 40 讲 原电池 常见化学电源
考点一
整合必备知识1.化学 电
3.(2)形成闭合回路 平衡电荷 (3)负极 正极
易错辨析 1.× 2.√ 3.× 4.√ 5.√ 6.√ 7.×
提升关键能力
1.(1)负 Ag-e-===Ag+ (2)正 Ag++e-===Ag (3)A
(4)浓度
2.(1)负极 氧化反应 还原 Fe3++e-===Fe2+
(2)正 I+2e-===2I-
2
3.A
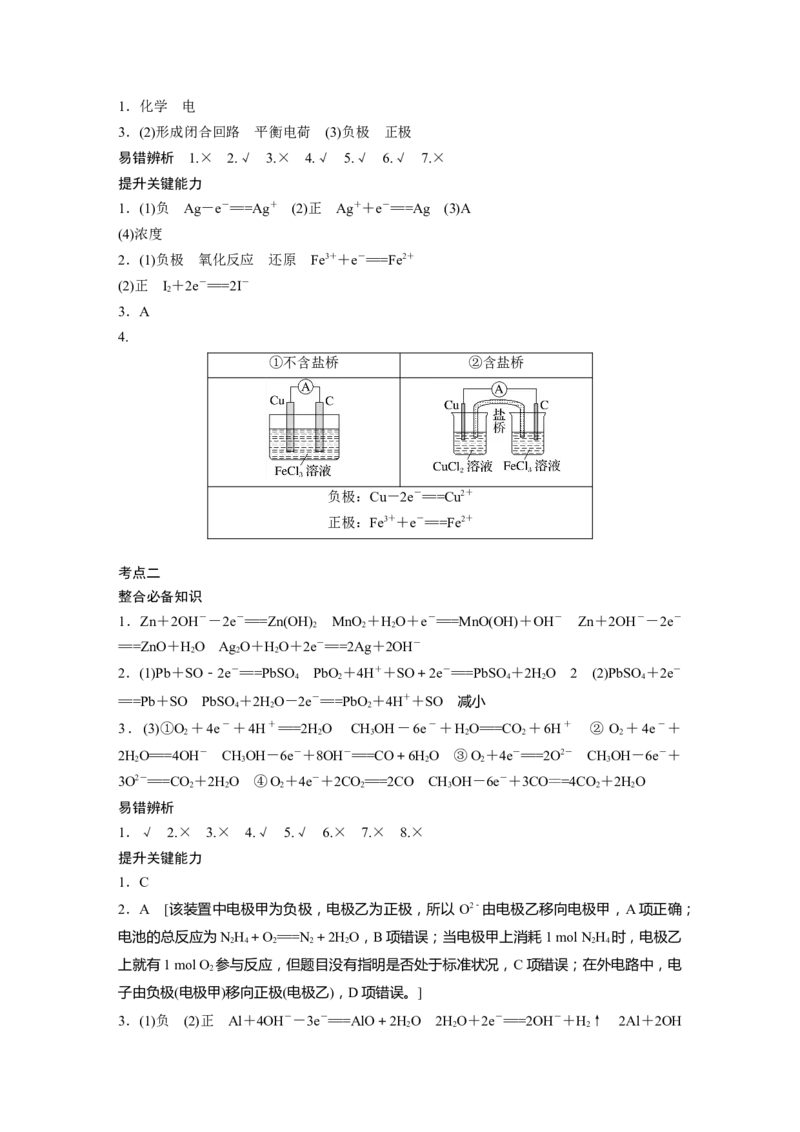
4.
①不含盐桥 ②含盐桥
负极:Cu-2e-===Cu2+
正极:Fe3++e-===Fe2+
考点二
整合必备知识
1.Zn+2OH--2e-===Zn(OH) MnO +HO+e-===MnO(OH)+OH- Zn+2OH--2e-
2 2 2
===ZnO+HO Ag O+HO+2e-===2Ag+2OH-
2 2 2
2.(1)Pb+SO-2e-===PbSO PbO +4H++SO+2e-===PbSO +2HO 2 (2)PbSO +2e-
4 2 4 2 4
===Pb+SO PbSO +2HO-2e-===PbO +4H++SO 减小
4 2 2
3.(3)①O +4e-+4H+===2HO CHOH-6e-+HO===CO +6H+ ② O +4e-+
2 2 3 2 2 2
2HO===4OH- CHOH-6e-+8OH-===CO+6HO ③O +4e-===2O2- CHOH-6e-+
2 3 2 2 3
3O2-===CO+2HO ④O+4e-+2CO===2CO CHOH-6e-+3CO===4CO+2HO
2 2 2 2 3 2 2
易错辨析
1.√ 2.× 3.× 4.√ 5.√ 6.× 7.× 8.×
提升关键能力
1.C
2.A [该装置中电极甲为负极,电极乙为正极,所以 O2-由电极乙移向电极甲,A项正确;
电池的总反应为NH +O===N +2HO,B项错误;当电极甲上消耗1 mol N H 时,电极乙
2 4 2 2 2 2 4
上就有1 mol O 参与反应,但题目没有指明是否处于标准状况,C项错误;在外电路中,电
2
子由负极(电极甲)移向正极(电极乙),D项错误。]
3.(1)负 (2)正 Al+4OH--3e-===AlO+2HO 2HO+2e-===2OH-+H↑ 2Al+2OH
2 2 2-+2HO===2AlO+3H↑ (3)正 Cu-2e-===Cu2+ NO+2H++e-===NO ↑+HO Cu
2 2 2 2
+4HNO(浓)===Cu(NO )+2NO ↑+2HO (4)能 Cu O+4e-+2HO===4OH-
3 3 2 2 2 2 2
4.(1)Zn-2e-+2OH-===Zn(OH) FeO+4HO+3e-===Fe(OH) +5OH-
2 2 3
(2)LiC -e-===Li++C CoO+Li++e-===LiCoO
6 6 2 2
(3)Mg-2e-===Mg2+ AgCl+e-===Ag+Cl-
练真题 明考向
1.A
2.B [由题图分析可知,Cl-在Ag极失去电子发生氧化反应,Ag为负极,A错误;电子由
负极Ag经活性炭流向正极Pt,B正确;溶液为酸性,故Pt表面发生的电极反应为O +4H+
2
+4e-===2HO,C错误;每消耗标准状况下11.2 L的O,转移2 mol电子,最多去除2 mol Cl
2 2
-,D错误。]
3.B 4.B
第 41 讲 新型化学电源分类突破
1.B 2.B 3.C
4.C [如果玻璃薄膜球内电极的电势低,则该电极为负极,负极发生氧化反应而不是还原
反应,A错误;pH与电池的电动势E存在关系:pH=,则玻璃膜内外氢离子浓度的差异会
引起电动势的变化,B错误;pH与电池的电动势E存在关系:pH=,则分别测定含已知pH
的标准溶液和未知溶液的电池的电动势,可得出未知溶液的 pH,C正确;pH计工作时,利
用原电池原理,则化学能转化为电能,D错误。]
5.B 6.B
7.D [该装置发生的有关反应为 HS+2Fe3+===2H++S+2Fe2+(a 极区)、2Fe2+-2e-
2
===2Fe3+(a极)、2H++2e-===H(b极),结合反应条件得到总反应:HS=====H +S,A、C
2 2 2
正确;该制氢工艺中光能转化为电能,最终转化为化学能,B正确;a极区涉及两步反应,
第一步利用氧化性强的Fe3+高效捕获HS得到硫和还原性的Fe2+,第二步是还原性的Fe2+
2
在a极表面失去电子生成氧化性强的Fe3+,这两步反应反复循环进行,所以a极区无需补充
含Fe3+和Fe2+的溶液,D错误。]
8.D 9.A
第 42 讲 电解池 金属的腐蚀与防护
考点一
整合必备知识1.电解质溶液(或熔融电解质) 氧化还原反应 电 化学 直流电源 电解质 熔融电解
质 闭合回路
3.(3)①2H++2e-===H↑ 2HO-4e-===4H++O↑ 2HO=====2H↑+O↑ 增大 加
2 2 2 2 2 2
水 ②2H++2e-===H↑ 2Cl--2e-===Cl↑ 2HCl=====H↑+Cl↑ Cu2++2e-===Cu
2 2 2 2
2Cl--2e-===Cl↑ CuCl =====Cu+Cl↑ 减小 通入HCl 加CuCl 固体 ③2Cl--2e-
2 2 2 2
===Cl↑ 2HO+2e-===H↑+2OH- 2Cl-+2HO=====Cl↑+H↑+2OH- 通入HCl
2 2 2 2 2 2
2HO-4e-===4H++O↑ Cu2++2e-===Cu 2Cu2++2HO=====2Cu+O↑+4H+ 减小
2 2 2 2
并生成新电解质 加CuO
提升关键能力
1.D 2.D
3.(1)1 0.4 CuO(或0.62 CuCO) (2)水(或HO) 0.02 (3)0.015
3 2
解析 (1)阳极生成 O 56 mL(标准状况)即 0.002 5 mol,依据总反应式:2CuSO +
2 4
2HO=====2Cu+O↑+2HSO ,溶液中生成0.01 mol H+,c(H+)=0.1 mol·L-1,pH=1;电
2 2 2 4
解生成0.002 5 mol O 和0.005 mol Cu,故要使溶液复原可加0.005 mol CuO,质量为0.4
2
g,或加0.005 mol CuCO ,质量为0.62 g。(2)继续通电电解,电解质溶液为HSO 溶液,故
3 2 4
实际被电解的物质为HO;加入 0.005 mol Cu(OH) 可使溶液复原,相当于加入0.005 mol
2 2
CuO和0.005 mol H O,故转移电子为(0.005×2+0.005×2) mol=0.02 mol。(3)Cu (OH) CO
2 2 2 3
相当于2CuO·H O·CO ,故转移的电子为0.005 mol×2+0.002 5 mol×2=0.015 mol。
2 2
4.(1)2Cl--2e-===Cl↑ Mg2++2HO+2e-===H↑+Mg(OH) ↓ Mg2++2Cl-+
2 2 2 2
2HO=====Mg(OH) ↓+Cl↑+H↑
2 2 2 2
(2)2Al-6e-+3HO===Al O+6H+ 2H++2e-===H↑ 2Al+3HO=====Al O+3H↑
2 2 3 2 2 2 3 2
(3)Mn2++2HO-2e-===MnO ↓+4H+
2 2
5.4CO+2HO-4e-===4HCO+O↑ H
2 2 2
6.(4)从右往左 (5)2NH -6e-+6OH-===N+6HO
3 2 2
考点二
整合必备知识
1.(1)2Cl--2e-===Cl↑ 氧化 2HO+2e-===H↑+2OH- 还原 2NaCl+
2 2 2
2HO=====2NaOH+H↑+Cl↑
2 2 2
2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2
(2)精制饱和NaCl溶液 HO(含少量NaOH) 淡盐水 NaOH溶液 Cl H (3)OH-
2 2 2
2.(1)②镀层金属 镀件 含有镀层金属离子 Cu-2e-===Cu2+ Cu2++2e-===Cu (2)粗
铜 纯铜 硫酸铜溶液 Cu-2e-===Cu2+、Zn-2e-===Zn2+、Ni-2e-===Ni2+ Cu2++2e
-===Cu 阳极泥 电解质溶液 有所下降
3.2NaCl(熔融)=====2Na+Cl↑ 2Cl--2e-===Cl↑ Na++e-===Na MgCl (熔
2 2 2
融)=====Mg+Cl↑ 2Cl--2e-===Cl↑ Mg2++2e-===Mg 2Al O(熔融)=====4Al+
2 2 2 3
3O↑ 2O2--4e-===O↑ Al3++3e-===Al
2 2易错辨析 1.× 2.× 3.× 4.×
提升关键能力
1.C 2.B
3.D [电解时,阳极Zn、Fe、Ni失去电子,发生氧化反应,A项错误;因氧化性:Ni2+>
Fe2+>Zn2+,故阴极的电极反应式为Ni2++2e-===Ni,阳极质量减少是因为Zn、Fe、Ni溶
解,而阴极质量增加是因为Ni析出,二者质量不相等,B项错误;电解后溶液中的阳离子
除Fe2+和Zn2+外,还有Ni2+和H+,C项错误。]
4.负 4Al Cl+3e-===Al+7AlCl H
2 2
5.A 6.B
考点三
整合必备知识
1.氧化
2.(2)2H++2e-===H↑ O +2HO+4e-===4OH- Fe+2H+===Fe2++H↑ 2Fe+O +
2 2 2 2 2
2HO===2Fe(OH) 吸氧腐蚀
2 2
3.应用举例 ⑤④②①③⑥
4.负 正 阴 阳
易错辨析 1.× 2.√ 3.× 4.× 5.×
提升关键能力
1.(1)吸氧 (2)B
2.(1)析氢 2H++2e-===H↑ 有气泡冒出 (2)吸氧 O +4e-+2HO===4OH- 导管内
2 2 2
液面上升
3.吸氧 Fe-2e-===Fe2+ 2HO+O+4e-===4OH- 4Fe(OH) +O+2HO===4Fe(OH) 、
2 2 2 2 2 3
2Fe(OH) ===Fe O·xHO+(3-x)H O
3 2 3 2 2
4.C 5.B
练真题 明考向
1.C 2.A
3.B [电极A是氯离子变为氯气,化合价升高,失去电子,是电解池阳极,因此电极A接
电源正极,发生氧化反应,故A正确;电极B为阴极,通入的氧气得到电子,其电极反应
式为2HO+4e-+O===4OH-,故B错误;右室生成氢氧根离子,应选用阳离子交换膜,
2 2
左室的钠离子进入到右室,在右室获得浓度较高的NaOH溶液,故C正确;改进设计中增
大了氧气的量,提高了电极B处的氧化性,从而降低电解电压,减少能耗,故D正确。]
4.D 5.C
热点强化17
热点专练
1.C 2.C 3.A
4.(1)NO+2HO-3e-===NO+4H+ (2)阳 5SO +2NO+8HO=====2NH+5SO+8H+
2 2 2(3)阴 减小18 g (4)15.68
解析 (1)甲池在放电过程中,负极上一氧化氮失去电子发生氧化反应生成硝酸根离子,反
应为NO+2HO-3e-===NO+4H+。(2)乙池中通入废气SO 的电极连接电源的正极,为阳
2 2
极;阳极二氧化硫发生氧化反应生成硫酸根离子,阴极一氧化氮发生还原反应生成铵根离子,
电池总反应的离子方程式为5SO +2NO+8HO=====2NH+5SO+8H+。(3)丙中阳极上水放
2 2
电发生氧化反应生成氧气和氢离子,氢离子从M室通过a膜进入浓缩室;N室中氯离子通
过b膜进入浓缩室,最终得到较浓的盐酸,故b为阴离子交换膜。当浓缩室得到4 L浓度
为0.6 mol·L-1盐酸时,迁移过来的氢离子为4 L×(0.6 mol·L-1-0.1 mol·L-1)=2 mol;2HO
2
-4e-===4H++O↑,则反应1 mol水,M室中溶液的质量变化为减少1 mol×18 g·mol-1=
2
18 g。(4)乙池中SO 转化为硫酸根离子、NO转化为铵根离子;若标准状况下,甲池有5.6 L
2
O(为0.25 mol)参加反应,根据得失电子守恒可知,O ~4e-~2SO ~NO,则乙池中处理废
2 2 2
气(SO 和NO)共0.7 mol,总体积为15.68 L。
2
第 43 讲 电解原理应用新拓展
1.C 2.C
3.D [石墨电极为阳极,对应的电极反应式为 P +8CN--4e-===4[P(CN) ]-,则生成1
4 2
mol Li[P(CN) ],理论上外电路需要转移1 mol电子,A错误;阴极上发生还原反应,应该得
2
电子,电极反应式为2HCN+2e-===H↑+2CN-,B错误;石墨电极为阳极,铂电极为阴
2
极,CN-应该向阳极移动,即移向石墨电极,C错误;由所给图示可知HCN在阴极放电,
产生CN-和H ,而HCN中的H来自于LiOH,则电解产生的H 中的氢元素来自于LiOH,
2 2
D正确。]
4.C [据图可知与电源y连接的电极上HS发生氧化反应转化为S,所以y为电源正极,x
2
为电源负极,阴极发生还原反应,电极反应式为 2HO+2e-===2OH-+H↑,所以阴极区
2 2
溶液的pH增大,A正确;阳极发生氧化反应,电极反应式为 HS+2CO-2e-===S↓+
2
2HCO,C 错误;通电一段时间后,阴极区得到氢氧化钠溶液,阳极区得到 NaHCO ,
3
NaHCO 溶液与NaOH溶液反应生成NaCO ,所以将阴极区溶液补充到阳极区可实现电解
3 2 3
液的再生,D正确。]
5.D 6.C
热点强化18
热点专练
1.A 2.D 3.C
4.C [由甲池放出O 知,乙池电极为电解池的阴极,和电源负极连接,溶液中水电离出的
2
氢离子放电生成氢气,A项错误;电解池中阳离子移向阴极,B项错误;阴极附近水电离出的氢离子放电破坏了水的电离平衡,电极附近氢氧根离子浓度增大,NaOH溶液Y的浓度比
NaOH溶液Z的大,C项正确;甲池电极为阳极,电解质溶液中水电离出的氢氧根离子放电
生成氧气,氢离子浓度增大,碳酸根离子结合氢离子生成碳酸氢根离子,出口为碳酸氢钠溶
液,则电极反应式为4CO+2HO-4e-===4HCO+O↑,D项错误。]
2 2
5.D 6.C
7.B [根据题干信息确定该装置为电解池,阴离子向阳极移动,阳离子向阴极移动,所以
电极a为阳极,连接电源的正极,A项正确;水在双极膜A解离后,H+吸引阴离子透过B
膜到左侧形成酸,B为阴离子交换膜,B项错误;电解质溶液采用NaSO 溶液,电解时生
2 4
成H 和O ,可避免有害气体的产生,C项正确;海水中的阴、阳离子透过两侧交换膜向两
2 2
侧移动,淡水从Ⅱ口排出,D项正确。]
第十一章 化学反应速率与化学平衡
第 44 讲 化学反应速率及影响因素
考点一
整合必备知识
1.(1)单位时间内反应物浓度的减小 生成物浓度的增大 mol·L-1·s-1[或mol/(L·s)]
(2)化学计量数 m∶n∶p∶q
2. b- c+ mol·L-1·s-1
mol·L-1·s-1 mol·L-1·s-1
应用举例
1.(1)X (2)0~8 min,v(H )==0.011 25 mol·L-1·min-1。 (3)10~12 min,v(NH )==
2 3
5.0×10-3 mol·L-1·min-1,v(N )==2.5×10-3 mol·L-1·min-1。
2
2.③>①>②>⑤>④
易错辨析 1.× 2.× 3.× 4.×
提升关键能力
1.30
2.0.48 kPa·s-1
3.(1-α)
4.30.0 6.0×10-2
解析 由方程式 2NO(g)===4NO (g)+O(g)可知,62 min 时, =2.9 kPa,则减小的
2 5 2 2
NO 为 5.8 kPa,此时 =35.8 kPa-5.8 kPa=30.0 kPa,则 v(N O)=2×10-3×30.0
2 5 2 5kPa·min-1=6.0×10-2 kPa·min-1。
考点二
整合必备知识
1.本身的性质 >
2.增大 减小 不变 增大 减小 气体 增大 减小 增大 相同 比表面积
应用举例 ①④⑥⑦
3.(1)化学反应 足够的能量 合适的取向 (2)能量 有效碰撞 (3)增加 增加 不变 增
加 增大 增加 增加 不变 增加 增大 不变 增加 增加 增加 增大 不变 增加
增加 增加 增大
易错辨析 1.× 2.× 3.× 4.× 5.×
提升关键能力
1.(1)增大 单位体积内,活化分子数目增加,有效碰撞的次数增多 (2)增大 (3)不变 单
位体积内活化分子数不变 (4)减小
2.增大反应物接触面积,提高反应速率和原料利用率
3.降低 CaO+CO===CaCO ,CaCO 覆盖在CaO表面,减少了CO 与CaO的接触面积
2 3 3 2
4.(1)硫酸 2MnO+5HC O +6H+===2Mn2++10CO↑+8HO (2)温度 催化剂 (3)0.5
2 2 4 2 2
酸性KMnO 溶液褪色所用时间
4
练真题 明考向
1.C 2.B
3.D [由图可知,无催化剂时,随反应进行,生成物的浓度也在增加,说明反应也在进行,
故A错误;由图可知,催化剂Ⅰ比催化剂Ⅱ催化效果好,反应速率大,说明催化剂Ⅰ使反
应活化能更低,故B错误;由图可知,使用催化剂Ⅱ时,在0~2 min内Y的浓度变化了2.0
mol·L-1,而a曲线表示的X的浓度变化了2.0 mol·L-1,二者变化量之比不等于化学计量数
之比,所以a曲线不表示使用催化剂Ⅱ时X的浓度随时间t的变化,故C错误;使用催化剂
Ⅰ时,在0~2 min内,Y的浓度变化了4.0 mol·L-1,则v(Y)==2.0 mol·L-1·min-1,v(X)=
v(Y)=×2.0 mol·L-1·min-1=1.0 mol·L-1·min-1,故D正确。]
4.①4.0 6.0 ②2
第 45 讲 过渡态理论 催化剂对化学反应的影响
考点一
整合必备知识
1.(1)每一步反应
3.应用举例 (1)E (2)E (3)E -E (4)小
a1 a2 a1 a2
提升关键能力
1.D2.Cu/Zn*+CO+2H===Cu/ZnO*+CHOH
2 2 3
3.D [根据表中数据分析,该反应的速率始终不变,NO的消耗是匀速的,说明反应速率
2
与c(N O)无关,故速率方程中n=0,每10 min一氧化二氮浓度减小0.02 mol·L-1,则c =
2 1
0.06>c =c =0,A、C错误;t=10 min 时瞬时速率等于平均速率 v(N O)==2.0×10-3
2 3 2
mol·L-1· min-1,B错误;保持其他条件不变,该反应的反应速率不变,即为 2.0×10-3
mol·L-1· min-1,若起始浓度0.200 mol·L-1,减至一半时所耗时间为=50 min,D正确。]
4.2 4×10-8 L·mol-1·s-1
5.C 6.B
考点二
提升关键能力
1.D [根据图示中各微粒的构造可知,该过程有HO参与,故A正确;根据图示的转化过
2
程,NO 转化为HNO ,N元素的化合价由+4变为+3,得电子被还原,作氧化剂,故B正
2 2
确;硫酸盐(含SO、HSO)气溶胶中含有HSO,转化过程有水参与,则HSO在水中可电离生
成H+和SO,则硫酸盐气溶胶呈酸性,故 C正确;根据图示转化过程中,由 SO转化为
HSO,有硫氧键生成,故D错误。]
2.D
3.C [由图可知,NH 吸附在催化剂表面后,经过一定的反应形成了 NH NO,NH NO又
3 2 2
经过反应得到N 和HO,所以NH NO是脱硝反应的活性中间体,B说法正确;始态相对能
2 2 2
量高于终态,说明这是一个放热反应,升高温度平衡逆向移动,脱硝反应的正反应速率的增
大程度小于其逆反应速率的增大程度,C说法错误;由图可知,全过程只有H的移除过程势
能升高,其速率是全过程几个反应中最慢的,是总反应的控速步骤,D说法正确。]
4.C
5.升高温度,消耗一氧化氮的反应速率增大,但催化剂的活性下降,消耗一氧化氮的反应
速率减小,前者的影响比后者的大
练真题 明考向
1.C [由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,
A正确;该反应是放热反应,升高温度平衡向左移动,R的浓度增大,B正确;由图可知Ⅰ
的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平衡,
C错误;在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高
反应速率较慢,所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确。]
2.B
3.C [由题中图2信息可知,t ~t ,n(H )比n(CO)多,且生成H 的速率不变,且反应过程
1 3 2 2
中始终未检测到CO ,在催化剂上有积碳,故可能发生副反应:CH=====C+2H ,B正确;
2 4 2
由反应②的化学方程式可知,H 和CO的反应速率相等,而t 时,H 的反应速率未变,仍然
2 2 2
为2 mmol·min-1,而CO的反应速率为1~2 mmol·min-1,故能够说明副反应生成H 的速率
2小于反应②生成H 速率,C错误;由图2可知,t 之后,CO的速率为0,CH 的速率逐渐增
2 3 4
大至1 mmol·min-1,说明反应②不再发生,而后副反应逐渐停止,D正确。]
4.(ⅰ)Ⅰ (ⅱ)c (ⅲ)< 2
第 46 讲 化学平衡状态与化学平衡常数
考点一
整合必备知识
1.(1)正反应方向 逆反应方向
应用举例
(1)①不正确,两个反应发生的条件不同。②正确。③正确。
(2)存在于氧气、二氧化硫和三氧化硫3种物质中。
2.(1)可逆 相等 (3)可逆反应 动态平衡 v正 v逆 质量或浓度
易错辨析 1.× 2.× 3.√ 4.√ 5.× 6.×
提升关键能力
1.D
2.(1)①③④⑦ (2)⑤⑦ (3)①②③④⑦ (4)①②③ (5)②④⑦
3.(1)②③④⑦ (2)⑤⑦ (3)②③④⑦
考点二
整合必备知识
1.K
2.
应用举例 (1)c(CO) (2)
2
3.温度
4.(2)正 平衡 逆 (3)吸热 放热 放热 吸热
易错辨析 1.× 2.√ 3.× 4.× 5.× 6.×
提升关键能力
1.K =,K = ,K =。K = ,K =。
1 2 3 2 3
2.
3.
4.(1)K ·K (2)< (3)>
1 2
练真题 明考向
1.C2. (或)
3.2
4.5
解析 设充入HO(g)物质的量为x mol;在某温度、100 kPa下,向反应器中充入1 mol气态
2
乙苯发生已知反应。乙苯的平衡转化率为50%,可列三段式:
C HC H(g)C HCH==CH(g)+H(g)
6 5 2 5 6 5 2 2
n(起始)/mol 1 0 0
n(转化)/mol 0.5 0.5 0.5
n(平衡)/mol 0.5 0.5 0.5
此时平衡时混合气体总物质的量为1.5 mol,此时容器的体积为V;当乙苯的平衡转化率为
75%,可列三段式:
C HC H(g)C HCH==CH(g)+H(g)
6 5 2 5 6 5 2 2
n(起始)/mol 1 0 0
n(转化)/mol 0.75 0.75 0.75
n(平衡)/mol 0.25 0.75 0.75
此时乙苯、苯乙烯、H 物质的量之和为1.75 mol,混合气的总物质的量为(1.75+x)mol,在
2
恒温、恒压时,体积之比等于物质的量之比,此时容器的体积为V;两次平衡温度相同,则
平衡常数相等,则=,解得x=5。
第 47 讲 化学平衡常数的综合计算
考点一
整合必备知识
例
提升关键能力
1.C 2.C
3.40% 3.56×104
解析 设容器中起始加入I(g)和环戊烯的物质的量均为a mol,平衡时转化的环戊烯的物质
2
的量为x mol,列出三段式:
(g)+I(g) (g)+2HI(g)
2
起始/mol a a 0 0
转化/mol x x x 2x平衡/mol a-x a-x x 2x
根据平衡时总压增加了20%,且恒温恒容时,压强之比等于气体物质的量之比,得=,解
得x=0.4a,则环戊烯的转化率为×100%=40%,平衡时 (g)、I(g)、 (g)、HI(g)的
2
分压分别为、、、,则 K ==p ,根据 p =1.2×105 Pa,可得 K =×1.2×105
p 总 总 p
Pa≈3.56×104 Pa。
拓展应用
(1)C (2)70 (3)变小
考点二
1.(1)3 (2)B
2.5 0
3.(1) (2)2 120
4.(1)B (2)0.025 mol·L-1·min-1 0.75
解析 (1)该反应是放热反应,反应达到平衡后,仅降低温度,k 、k 均减小,平衡正向移
正 逆
动,正反应速率大于逆反应速率,因此k 减小的倍数更少。
正
(2) 2CH==CH(g)+O(g)2 (g)
2 2 2
开始/mol 1 1 0
转化/mol 2x x 2x
平衡/mol 1-2x 1-x 2x
=0.875,x=0.25,则 0~10 min 内 v(O )==0.025 mol·L-1·min-1,k ·c2( )=k
2 逆
·c2(CH==CH)·c(O ),==0.75。
正 2 2 2
热点强化19
热点专练
1. 0.43
2.
解析 由题给反应的化学方程式可知,对于反应Ⅰ,每生成1 mol甲醇的同时生成1 mol水;
对于反应Ⅲ,每生成1 mol一氧化碳的同时生成1 mol水;对于反应Ⅱ,每消耗1 mol一氧
化碳的同时生成1 mol甲醇;由此可知,生成的水的物质的量等于生成的甲醇和一氧化碳的
物质的量之和,即生成水的物质的量为(a+b) mol,即水的浓度为 mol·L-1。由C原子个数
守恒可知,平衡时混合气体中CO 的物质的量为(1-a-b) mol,由H原子个数守恒可知,
2
平衡时混合气体中H 的物质的量为[3-2a-(a+b)] mol,因此平衡常数K=。
2
3.(b+)b
4.A
5.(1)0.8 mol·L-1·min-1 (2)80% 1.25解析 (1)设平衡时CO为x mol,H 为y mol,CHOH为z mol,则CHOCH 为2z mol,
2 3 3 3
HO为2z mol,根据:
2
C守恒:x+z+2×2z=4
H守恒:2y+4z+6×2z+2×2z=2×8
O守恒:x+z+2z+2z=4
CO的转化率为=80%,解得x=0.8,y=1.6,z=0.64,v(H )==0.8 mol·L-1·min-1。(2)反应Ⅰ
2
中CO的转化率为80%,则生成的CHOH的物质的量为4 mol×80%=3.2 mol,反应Ⅱ生成
3
的CHOCH 的物质的量为2z mol即2×0.64 mol=1.28 mol,则反应Ⅱ转化的CHOH的物
3 3 3
质的量为2×1.28 mol=2.56 mol,则反应Ⅱ中CHOH的转化率α=×100%=80%。根据之
3
前所解方程,可得平衡时:CHOH、H 、CO的浓度分别为0.32 mol·L-1、0.8 mol·L-1、0.4
3 2
mol·L-1,反应Ⅰ的平衡常数K==1.25。
6.(1)0.9α (2)逆向移动 1∶10
练真题 明考向
1.(1)①-223 1.2×1014 (2)①7.2×105
2.(3)3.0 2.25 增大
(4) 46.26
3.吸收 31.2 0.02 MPa
解析 反应达到平衡时,HO(g)的转化率为50%,则水的变化量为0.5 mol,水的平衡量也
2
是0.5 mol,由于CO的物质的量为0.1 mol,CO和CO 中的O均来自HO中,则根据O原
2 2
子守恒可知CO 的物质的量为0.2 mol,生成0.2 mol CO 时消耗了0.2 mol CO,故在反应Ⅰ
2 2
实际生成了0.3 mol CO。根据相关反应的热化学方程式可知,整个体系的热量变化为+
131.4 kJ·
mol-1×0.3 mol-41.1 kJ·mol-1×0.2 mol=39.42 kJ-8.22 kJ=31.2 kJ;由H原子守恒可知,
平衡时H 的物质的量为0.5 mol,CO的物质的量为0.1 mol,CO 的物质的量为0.2 mol,水
2 2
的物质的量为0.5 mol,则平衡时气体的总物质的量为0.5 mol+0.1 mol+0.2 mol+0.5 mol=
1.3 mol,在同温同体积条件下,气体的总压之比等于气体的总物质的量之比,则平衡体系
的总压为 0.2 MPa×1.3=0.26 MPa,反应Ⅰ的平衡常数K ==×p =×0.26 MPa=0.02
p 总
MPa。
第 48 讲 影响化学平衡的因素
考点一整合必备知识
1.(2)①> ②< ③=
2.(1)实验一:①加入较浓的FeCl 溶液或KSCN溶液,红色加深,平衡正向移动。②加入
3
少量Fe粉,红色变浅,平衡逆向移动。③加入少量KCl固体,红色几乎不变,平衡不移动。
实验二:①滴加NaOH溶液,溶液由橙色变为黄色,平衡正向移动。②滴加HSO 溶液,溶
2 4
液橙色加深,平衡逆向移动。
(2)气体的颜色先变深后变浅,最终还是比最初的颜色深。增大压强,平衡向生成 NO 的方
2 4
向(气体体积减小的方向)移动。
(3)溶液由蓝色变为绿色 在其他条件不变时,升高温度,平衡向正反应(吸热)方向移动 溶
液恢复蓝色 在其他条件不变时,降低温度,平衡向逆反应(放热)方向移动
思考 因为加热时,平衡正向移动,[Cu(H O) ]2+有部分转化为[CuCl ]2-,[Cu(H O) ]2+显蓝
2 4 4 2 4
色,[CuCl ]2-显黄色,而二者的混合色为绿色,故看不到黄色。
4
3.减弱
提升关键能力
1.(1)①增大 不变 正向移动 ②减小 不变 逆向移动 ③不变 增大 逆向移动 ④
不变 减小 正向移动
(2)①增大 增大 向气体体积减小的方向移动 ②减小 减小 向气体体积增大的方向移
动 (3)①增大 增大 向吸热反应方向移动 ②减小 减小 向放热反应方向移动 (4)增
大 增大 不移动
2.C
3.(1)
(2)
4.一定量的A和B 向容器中加入C
考点二
1.(1)正反应 减小 增大
(2)正反应 不变 不变
(3)正反应 增大 减小
(4)正向 增大 减小 不变 减小 增大
2.B 3.D4.BC
5.BD
解析 在恒温恒容条件下,平衡时向容器中充入惰性气体不能改变各组分的浓度,因此反应
Ⅰ的平衡不移动,A说法不正确;在反应中固体C转化为气体,气体的质量增加,而容器的
体积不变,因此气体的密度在反应过程中不断增大,当混合气体的密度保持不变时,说明反
应体系已达到平衡,B说法正确;若C(s)和HO(g)完全反应全部转化为CO(g)和H(g),由
2 2 2
C(s)+2HO(g)CO(g)+2H(g)可知,H 的体积分数的极值为,由于可逆反应有一定的限
2 2 2 2
度,因此,平衡时H 的体积分数不可能大于,C说法不正确;将炭块粉碎可以增大其与
2
HO(g)的接触面积,因此可加快反应速率,D说法正确。
2
练真题 明考向
1.B 2.C
3.①p <p <p 合成氨的反应为气体分子数减少的反应,压强越大平衡时氨的摩尔分数
1 2 3
越大 ②图2 ③33.33%
解析 ①合成氨的反应中,压强越大平衡时氨的摩尔分数越大。由图中信息可知,在相同温
度下,反应达平衡时氨的摩尔分数:p <p <p ,因此,图中压强由小到大的顺序为p <p
1 2 3 1 2
<p 。②该反应为气体分子数减小的反应,在相同温度和相同压强下,惰性气体Ar不利于
3
合成氨,进料组成中含有惰性气体Ar的图是图2。③图1中,进料组成为 =0.75、
=0.25,两者物质的量之比为 3∶1。假设进料中氢气和氮气的物质的量分别为 3 mol和1
mol,达到平衡时氮气的变化量为x mol,则有:
N(g)+3H(g)2NH (g)
2 2 3
始/mol 1 3 0
变/mol x 3x 2x
平/mol 1-x 3-3x 2x
当p =20 MPa、 =0.20时, ==0.20,解得x=,则氮气的转化率α=≈33.33%,
2
平衡时N 、H 、NH 的物质的量分别为 mol、2 mol、 mol,其物质的量分数分别为、、,
2 2 3
则该温度下K′ ==(MPa)-2,因此,该温度时反应N(g)+H(g)NH (g)的平衡常数K =
p 2 2 3 p
=(MPa)-1。
第 49 讲 化学反应的方向与调控
考点一
整合必备知识
2.(1)S > > (2)自发进行3.能 平衡 不能
易错辨析 1.× 2.√ 3.× 4.× 5.× 6.√ 7.√
提升关键能力
1.D
2.(1)不能实现,因为该反应的ΔH>0,ΔS<0,ΔG>0,反应不可能自发进行 (2)< 该反
应的ΔS<0,因该反应能自发进行,根据ΔG=ΔH-TΔS<0可知ΔH<0 (3)高温
3.C
考点二
提升关键能力
1.(1)升高温度、增大压强、增大反应物的浓度、使用催化剂等,都可以使合成氨的反应速
率增大;降低温度、增大压强、增大反应物浓度或减小生成物浓度等有利于提高氮气或氢气
的转化率。
(2)①使用铁触媒作催化剂改变了反应历程,降低了反应的活化能,提高了活化分子的百分
数,有效碰撞次数增加,反应速率加快。
②不能。因为催化剂对化学平衡无影响。
③能。因为实际合成氨过程为非平衡状态下进行,反应速率大,单位时间里生产的氨气的量
多。
(3)考虑速率因素,500 ℃时催化剂的催化活性最好。
(4)合成氨时增大压强尽管可以同时提高反应速率和反应物的转化率。但是,压强越大,对
材料的强度和设备的要求也越高,增加生产投资将降低综合经济效益。
(5)使氨气冷却成液氨并及时分离,分离后的原料气循环使用。
2.(1)770 ℃ 890 ℃ (2)降低压强或移去钾蒸气、适当升高温度 (3)K=
3.(1)-41.2 (2)①b c B=C>A ② (3)放热 高温时,积碳反应主要发生CH 裂解,
4
导致催化剂积碳,活性降低
解析 (1)根据盖斯定律知,反应 Ⅱ =反应 Ⅰ-反应 Ⅲ,ΔH =ΔH -ΔH =-206.2 kJ·mol
2 1 3
-1-(-165.0 kJ·mol-1)=-41.2 kJ·mol-1。
(2)①结合反应,越大,CO转化率越大,直到接近100%,故b表示CO转化率变化的曲线;
随着的增大,CO接近完全转化,CH 产率逐渐增大,直到接近100%,故c表示CH 产率变
4 4
化的曲线;b表示CO转化率变化的曲线,B、C均在曲线b上,温度:B=C,结合反应 Ⅰ、
Ⅱ,两反应均为放热反应,则温度越低CO转化率越高,A点转化率高于C,故温度:B=
C>A。
②设起始投料n(CO)=n mol,则n(H )=3n mol,列出反应 Ⅰ 三段式:
2
CO(g)+3H(g)CH(g)+HO(g)
2 4 2
起始/mol n 3n 0 0
转化/mol x 3x x x
平衡/mol n-x 3n-3x x x反应Ⅱ前后气体体积不变,反应Ⅰ前后总物质的量减少2x mol,根据初始压强为p ,达到
0
平衡时总压为,则=,解得x=0.5n;CO的平衡转化率为a,列出反应Ⅱ三段式:
CO(g) + HO(g) CO(g) + H(g)
2 2 2
起始/mol 0.5n 0.5n 0 1.5n
转化/mol na-0.5n na-0.5n na-0.5n na-0.5n
平衡/mol n(1-a) n(1-a) n(a-0.5) n(1+a)
则CH 的选择性=×100%=%;平衡时,CO的分压为×p=、H 的分压为×p=、CH 的分
4 0 2 0 4
压为×p=、HO的分压为×p=,反应Ⅰ的K ==。
0 2 0 p
第 50 讲 化学反应速率与化学平衡图像分类突破
提升关键能力
1.(1)ACDF (2)C E B (3)A
(4)
2.(1)< 放热 (2)< 增大 (3)a =
3.
4.(1)22 0.02 (2)及时移去产物 改进催化剂 提高反应物压强 (3)大于 1.3
5.> > > >
6.A [由图像可知,压强一定时,温度越高,CH 的平衡转化率越高,故正反应为吸热反
4
应,ΔH>0,A项错误;该反应为气体分子总数增加的反应,压强越大,甲烷的平衡转化率
越小,故压强:p>p>p>p ,B项正确;压强为p 、温度为1 100 ℃时,甲烷的平衡转化率
4 3 2 1 4
为80.00%,故平衡时各物质的浓度分别为c(CH)=0.02 mol·L-1,c(CO)=0.02 mol·L-1,
4 2
c(CO)=0.16 mol·L-1,c(H )=0.16 mol·L-1,平衡常数K=≈1.64,C项正确;压强为p 时,y点未达到平衡,
2 4
此时v >v ,D项正确。]
正 逆
7.D
8.2.0
9.(5)在反应过程中,断裂和形成的化学键相同 (6)a
10.①大于 ② K ·K 大于 设 T′>T,即<,由图可知:lg K (T′)-lg K (T)>|lg
p1 p2 p2 p2
K (T′)-lg K (T)|=lg K (T)-lg K (T′),则:lg[K (T′)·K (T′)]>lg[K (T)·K (T)],即
p1 p1 p1 p1 p2 p1 p2 p1
K(T′)>K(T),因此该反应正反应为吸热反应,即ΔH大于0
11.C [由盖斯定律知:反应Ⅱ×2+Ⅲ得反应:2CO(g)+6H(g)CHOCH (g)+3HO(g)
2 2 3 3 2
ΔH=2×(-49.5 kJ·mol-1)+(-23.5 kJ·mol-1)=-122.5 kJ·mol-1,A错误;升高温度,反
应Ⅰ正向进行,则CO的平衡体积分数应增大,故Y表示CO,B错误;由图可知,温度从
553 K上升至573 K时,反应Ⅰ消耗的CO 大于反应Ⅱ生成的CO,D错误。]
2 2
热点强化20
热点专练
1.(1)< (2)K >K>K (3)T ~T 温度区间,化学反应已达到平衡,由于正反应是放热反
b c d 3 4
应,温度升高平衡向逆反应方向移动,不利于CO 的捕获
2
2.①该反应为放热反应,温度升高,平衡逆向移动(或平衡常数减小) ②分子筛膜从反应
体系中不断分离出HO,有利于反应正向进行,甲醇产率升高 ③210
2
3.乙 p >p >p T 时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡没有
1 2 3 1
影响
4.p>p>p>p 该反应正向是气体分子数减小的反应,相同温度下,压强升高乙烯平衡转
4 3 2 1
化率升高
5.反应为放热反应,温度升高平衡左移 温度高于1 030 ℃时,x(O )大于21%,载氧体无
2
法载氧
6.(1)870 K(860~880 K范围内都可以)
(2)该反应放热,升高温度,反应向逆反应方向进行
(3)加入的CO会与NO的分解产物O 发生反应,促进NO分解平衡向生成N 的方向移动,
2 2
导致NO的转化率增大
7.Mn 200 ℃ b~a段,开始温度较低,催化剂活性较低,脱氮反应速率较慢,反应还
没达到化学平衡,随着温度升高反应速率变大,一定时间参与反应的氮氧化物变多,导致脱
氮率逐渐增大第十二章 水溶液中的离子反应与平衡
第 51 讲 弱电解质的电离平衡
考点一
整合必备知识
2.(1)小 (2)越大 (3)结合成弱电解质分子 (4)电离
易错辨析 1.√ 2.√ 3.× 4.× 5.√ 6.× 7.×
提升关键能力
1.向右 增大 减小 减弱 向右 增大 增大 增强 向左 增大 增大 增强 向右
减小 减小 增强 向左 减小 减小 增强 向右 增大 增大 增强
2.C 3.D
4.A [25 ℃时,若测得0.01 mol·L-1 HR溶液pH>2,说明HR在水溶液中部分电离,溶液
中存在电离平衡,则HR是弱酸,故A正确;25 ℃时,若测得0.01 mol·L-1和0.1 mol·L-1
HR溶液的pH差值等于1,说明稀释十倍,H+的物质的量没有变化,HR完全电离,是强酸,
故B错误;25 ℃时,若测得0.01 mol·L-1 NaR溶液pH=7,说明溶液呈中性,NaR为强酸
强碱盐,HR为强酸,故C错误;若HR为强酸,NaR溶液呈中性,升高温度,促进水的电
离,pH减小,则a>b,若HR是弱酸,R-水解溶液呈碱性,加热,促进盐的水解,碱性增
强,则a
2.(1)越小 越大 (2)增大
3.(2)第一步电离
易错辨析 1.× 2.× 3.× 4.×
提升关键能力
1.D 2.D
3.(1)HCOOH>HCO>HS>HClO
2 3 2
(2)S2->CO>ClO->HS->HCO>HCOO-
(3)①②④
4.(1)变小 (2)变大 (3)变小 (4)不变 (5)不变
热点强化21
1.(3)①小 ②大
2. HA H+ +A-起始 c 0 0
转化 c·α c·α c·α
平衡 c·(1-α) c·α c·α
K==,α很小,可认为1-α≈1,则K=c·α2。
a a
热点专练
1.B [HA电离出的c(H+)为0.1 mol·L-1×0.1%=10-4 mol·L-1,则pH=4,故A正确;温
度升高促进弱酸的电离,氢离子浓度变大,则pH变小,故B错误;由HAH++A-,c(H
+)=c(A-)=0.1 mol·L-1×0.1%=10-4 mol·L-1,则电离平衡常数为≈10-7,故C正确;HA
电离出的c(H+)为10-4 mol·L-1,水电离产生的氢离子浓度为 mol·L-1=10-10 mol·L-1,则
由HA电离出的c(H+)约为水电离出的c(H+)的106倍,故D正确。]
2.4.2×10-7
3.
4.(1)在M点时,溶液中c(OH-)=10-10 mol·L-1,则常温时0.010 mol·L-1的HA溶液中c(H
+)=10-4 mol·L-1,HA为一元弱酸。
(2)在相同温度下,M、P点的电离常数相同,用M点计算电离常数。HAH++A-,c(H
+)≈c(A-),
常温下,K(HA)=≈=1.0×10-6。
a
5.(1)由图像可知:
pH=1.2时,c(HC O)=c(H C O),K (H C O)==10-1.2。
2 2 2 4 a1 2 2 4
pH=4.2时,c(HC O)=c(C O),K ( H C O)==10-4.2。
2 2 a2 2 2 4
(2)1 000
6.(1)H PO HPO+H+ HPOHPO+H+
3 3 2 2
(2)Ⅰ (3)10-1.4
解析 K =,K =,且K >K ,由图像可知,在相同或时,Ⅱ对应的c(H+)较大,为第一
a1 a2 a1 a2
步电离, Ⅰ 对应的c(H+)较小,为第二步电离,选用Ⅱ中的特殊点B计算K ,K ==
a1 a1
10×10-2.4=10-1.4。
练真题 明考向
1.C 2.B
3.1012·K 1024·K ·K
a1 a1 a2
解析 HCO 是二元弱酸,分步发生电离:HCOHCO+H+、HCOCO+H+,则有
2 3 2 3
K =、K =,从而可得K ·K =。当溶液pH=12时,c(H+)=10-12 mol·L-1,代入K 、
a1 a2 a1 a2 a1
K ·K 可得c(H CO)∶c(HCO)=1∶(1012·K ),c(H CO)∶c(CO)=1∶(1024·K ·K ),综合可
a1 a2 2 3 a1 2 3 a1 a2
得c(H CO)∶c(HCO)∶c(CO)=1∶(1012·K )∶(1024·K ·K )。
2 3 a1 a1 a2第 52 讲 水的电离和溶液的 pH
考点一
整合必备知识
1.HOH++OH- c(H+)·c(OH-) 1×10-14 不变 增大 稀的电解质
2
2.逆 不变 减小 减小 增大 逆 不变 减小 增大 减小 正 不变 增大 增大
减小 正 不变 增大 减小 增大 逆 不变 减小 减小 增大 正 增大 增大 增
大 增大
3.(3)①1×10-12 mol·L-1 ②1×10-10 mol·L-1 ③1×10-10 mol·L-1 ④1×10-4 mol·L-
1 ⑤1×10-4 mol·L-1
易错辨析 1.√ 2.√ 3.× 4.× 5.√ 6.×
提升关键能力
1.D
2.(1)B>C>A=D=E (2)D (3)碱
(4)1×10-10
考点二
整合必备知识
1.> < = = < >
2.(1)-lg c(H+) (3)玻璃片 表面皿 标准比色卡
(4)①-lg c(OH-) ②14
易错辨析
1.√ 2.√ 3.× 4.√ 5.× 6.× 7.× 8.√ 9.×
提升关键能力
1.C 2.C 3.B 4.C
5.(1)中性 (2)碱性 (3)酸性 (4)中性 (5)酸性 (6)碱性 (7)酸性 (8)碱性
6.(1)10 (2)1∶4 (3)10
解析 (1)pH=3的硝酸溶液中c(H+)=10-3 mol·L-1,pH=12的Ba(OH) 溶液中c(OH-)=
2
mol·
L-1=10-2 mol·L-1,二者以体积比9∶1混合,Ba(OH) 过量,溶液呈碱性,混合溶液中c(OH
2
-)==1×10-4 mol·L-1,则混合后c(H+)== mol·
L-1=1×10-10 mol·L-1,故pH=10。
(2)设氢氧化钡溶液的体积为V L,硫酸氢钠溶液的体积为V L,依题意知,n(Ba2+)=
1 2
n(SO),由Ba(OH) +NaHSO===BaSO↓+NaOH+HO知,生成的氢氧化钠的物质的量为
2 4 4 2
n(NaOH)=n[Ba(OH) ]=5×10-3V mol,=1×10-3 mol·L-1,则V∶V=1∶4。
2 1 1 2
(3)pH=a的NaOH溶液中c(OH-)=10a-14 mol·L-1,pH=b的稀盐酸中c(H+)=10-b mol·L-1,根据中和反应H++OH-===H O,知c(OH-)·V=c(H+)·V ,===1014-(a+b),a+b=
2 a b
13,则=10。
练真题 明考向
1.D 2.C
3.C [根据HNO 和CHCOOH的电离常数,可知酸性:HNO>CH COOH,相同pH的两
2 3 2 3
种酸溶液,稀释相同倍数时,弱酸的pH变化较小,故曲线 Ⅰ 代表CHCOOH溶液,A项
3
错误;两种酸溶液中水的电离受到抑制,b点溶液pH小于c点溶液pH,则b点对应酸电离
出的c(H+)大,对水的电离抑制程度大,故水的电离程度:b点c(HNO),故n(CHCOOH)>n(HNO),因此与NaOH恰好中和后,溶液中n(Na
3 2 3 2
+)不同,D项错误。]
第 53 讲 酸碱中和滴定及拓展应用
考点一
整合必备知识
1.
2.(1)红 蓝 红 黄 无 浅红 红
3.(1)①上 ②0.01 ③酸式 碱性 碱式 酸性 强氧化性 (2)查漏 润洗 (3)滴定管
的活塞 锥形瓶内溶液颜色 锥形瓶 (5)2~3 平均值
易错辨析 1.× 2.× 3.× 4.× 5.√
提升关键能力
1.(1)酸 0.30 24.90 大于 酚酞或甲基橙
(2)丙 (3)①滴入最后半滴标准盐酸时,溶液由红色变为无色,且在半分钟内不恢复红色
②第三次数据明显与前两次数据差别较大,应舍弃,将第一次滴定所得数据代入,得:
c(NaOH)===0.100 1 mol·L-1;同理可得:c(NaOH)=0.099 9 mol·L-1,则c(NaOH)==
1 2
0.100 0 mol·L-1
二、偏大 偏小
2.偏高 偏高 偏低 无影响 偏低 偏低 偏高 偏低 无影响 偏低 偏高
考点二
提升关键能力
1.C 2.C
3.A [NaOH溶液滴定HX,恰好完全反应时溶液显碱性,甲基橙在酸性时就变色,故
NaOH消耗量会减小,测定结果偏低,故A正确;0.100 0 mol·L-1 NaOH与20 mL酸恰好反
应时消耗的碱的体积为20.00 mL,所以酸的浓度都是0.100 0 mol·L-1,根据图像纵坐标可知,HX为弱酸,HY为强酸,故B、C错误;a点对应溶质是NaX和HX,HX为弱电解质,b点
对应溶质是NaY和HY,HY是强电解质,虽然各物质的浓度都相同,但是溶液中离子浓度
不相同,故导电性不同,故D错误。]
4.D
热点强化22
热点专练
1.B
2.(1)5NO+2MnO+6H+===5NO+2Mn2++3HO % (2)偏小
2
3.(1)×104 (2)偏高
解析 (1)根据关系式:Cr O~6Fe2+,求得 KCr O 标准溶液消耗 n(Fe2+)=6cV×10-3
2 2 2 7 2 2
mol;则NO消耗n(Fe2+)=(cV -6cV)×10-3 mol,根据关系式3Fe2+~NO得n(NO)=
1 1 2 2
(cV -6cV)×10-3 mol,n(NO)=n(NO )=n(NO)=(cV -6cV)×10-3 mol,V L气样中
1 1 2 2 x 2 1 1 2 2
含m(NO )=(cV-6cV)×46× mg,所以气样中NO 的含量为 mg·
2 1 1 2 2 2
m-3=×104 mg·m-3。
答题规范(7)
规范精练
1.当滴入最后半滴标准液后,溶液由红色变为无色,且半分钟内不恢复红色 当滴入最后
半滴标准液后,溶液由黄色变为橙色,且半分钟内不恢复黄色
2.淀粉溶液 当滴入最后半滴标准液后,溶液由无色变为蓝色,且半分钟内不褪色
3.否 当滴入最后半滴酸性KMnO 溶液后,溶液由无色变为浅红色,且半分钟内不褪色
4
4.Ti3++Fe3+===Ti4++Fe2+ 当滴入最后半滴标准液后,溶液变成红色,且半分钟内不褪
色
5.KSCN溶液 当滴入最后半滴标准KI溶液后,溶液的红色褪去,且半分钟内不恢复红色
练真题 明考向
1.(1)√ (2)× (3)√ (4)×
2.(1)C
(2)A [ 用 c mol·L - 1 NaOH- 甲 醇 标 准 溶 液 进 行 滴 定 , 根 据 反 应 CHCOOH +
3
NaOH===CHCOONa+HO,结合步骤④可得关系式:乙酸酐[(CH CO) O]~2CHCOOH~
3 2 3 2 3
2NaOH,则 n(乙酸酐)=0.5cV×10-3 mol,根据反应(CHCO) O+ROH―→CHCOOR+
2 3 2 3
CHCOOH,结合步骤②,设样品中ROH为x mol,则x+2(0.5cV×10-3-x)=cV×10-3,
3 2 1
解得x=c(V -V)×10-3,又因ROH样品的质量为m g,则ROH样品中羟基的质量分数为
2 1
×100%,A正确。]
(3)B3.0.110 4
4.从左侧滴定管中放出一定体积的待测Ce4+溶液,加入指示剂苯代邻氨基苯甲酸,用
0.020 00 mol·L-1(NH )Fe(SO ) 溶液来滴定,当滴入最后半滴标准液时,溶液由紫红色变为
4 2 4 2
亮黄色,且半分钟内不变色,即达到滴定终点,重复上述操作2~3次,记录标准液的体积
第 54 讲 盐类的水解
考点一
整合必备知识
1.水电离出来的H+或OH-结合生成弱电解质
2.右
3.(2)酸碱中和
4.否 中性 是 NH、Cu2+ 酸性 是 CHCOO-、CO 碱性
3
5.应用举例
(1)NH+HONH ·H O+H+ (2)CO+HOHCO+OH- HCO+HOHCO +OH-
2 3 2 2 2 2 3
(3)Fe3++3HOFe(OH) +3H+ (4)CH COO-+NH+HOCHCOOH+NH ·H O
2 3 3 2 3 3 2
(5)2Al3++3S2-+6HO===2Al(OH) ↓+3HS↑ (6)Al3++3HCO===Al(OH) ↓+3CO↑
2 3 2 3 2
易错辨析 1.× 2.× 3.× 4.× 5.×
提升关键能力
1.A
2.(1)②>④>③>① ②>④>③>①
(2)①>③>④>② (3)c(Na+)>c(CN-)>c(HCN)
(4)中 碱
3.B
4.(1)TiO2++2HOTiO(OH) +2H+
2 2
(2)TiO2++CO+HO===TiO(OH) ↓+CO↑
2 2 2
5.SOCl +HO===SO ↑+2HCl↑
2 2 2
考点二
整合必备知识
1.吸热
2.(1)增大 (2)减小应用举例 向右 增多 减小 颜色变深 向左 增多 减小 颜色变浅 向右 增多 增
大 颜色变浅 向右 减少 增大 生成红褐色沉淀,放出气体
易错辨析 1.× 2.× 3.× 4.× 5.× 6.√
提升关键能力
1.B 2.B
3.⑤>④>③>①>②
4.(1)③>②>④>① (2)②>①>③ (3)④>②>③>①
答题规范(8)
规范精练
1.(1)变小 水的电离为吸热过程,升高温度,平衡向电离方向移动,水中c(H+)增大,故
pH变小 (2)温度升高,CHCOO-水解程度增大,OH-浓度增大,而K 增大,综合作用结
3 w
果使H+浓度增大,pH减小 (3)升高温度,促进水的电离,故c(H+)增大;升高温度,促进
铜离子水解,故c(H+)增大,两者共同作用使pH发生变化
2.取NaCO 溶液,滴加酚酞,溶液呈红色,然后分成两份,加热其中一份,若红色变深,
2 3
则盐类水解吸热
3.在NH Cl溶液中存在水解平衡:NH+HONH ·H O+H+,加入Mg粉,Mg与H+反
4 2 3 2
应放出H,使溶液中c(H+)降低,水解平衡向右移动,使Mg粉不断溶解。
2
练真题 明考向
1.C
2.A [a点、c点的pH相同,即c(H+)相同,但是c点的温度高,K 大,所以a点溶液的
w
c(OH-)比c点溶液的小,A正确;NaHCO 溶液中存在电离平衡和水解平衡,根据图示可知,
3
NaHCO 溶 液 显 碱 性 , 水 解 过 程 大 于 电 离 过 程 , K = > K , 所 以 K >
3 h a2 w
K (H CO)·K (H CO),B错误;b点溶液显碱性,溶液中存在电荷守恒:c(Na+)+c(H+)=
a1 2 3 a2 2 3
c(HCO)+2c(CO)+c(OH-),由于c(H+)c(HCO)>c(H CO)>c(CO)
2 3
2.c(Na+)>c(HC O)>c(C O)>c(H C O)
2 2 2 2 4
3.(1)③<②<① (2)< (3)碱 NaHPO 的水解常数K ===≈1.6×10-7,K >K ,即
2 4 h h a3
HPO的水解程度大于其电离程度,因而NaHPO 溶液显碱性
2 4
4.(1)NH水解使溶液显酸性,其水解常数为K (NH)==≈5.6×10-10,HCO水解使溶液显
h
碱性,其水解常数为K (HCO)==≈2.3×10-8,HCO的水解程度大于NH的水解程度,溶
h
液显碱性
(2)c(NH)>c(HCO)>c(H CO)>c(NH ·H O)
2 3 3 2
5.D [CN-的水解常数K =1.6×10-5,则HCN的电离常数为K ===6.25×10-10,K >
h a h
K,所以水解程度更大,溶液显碱性,pH>7,A项错误;CN-的水解程度大于HCN的电
a
离程度,所以c(HCN)>c(Na+)>c(CN-),C项错误;c mol·L-1盐酸与0.6 mol·L-1 NaCN溶
液等体积混合后溶液中存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c(CN-)+c(Cl-),溶液显中性,所以c(CN-)=c(Na+)-c(Cl-)= mol·L-1,溶液中还存在元素守恒:c(HCN)+c(CN-)
=c(Na+),所以c(HCN)=c(Na+)-c(CN-)= mol·L-1,所以有K===6.25×10-10,解得
a
c=,D项正确。]
6.(1)CH COONa的水解常数K ==≈5.9×10-10c(Na+)>c(CHCOOH)>c(H+)
3 3
考点三
提升关键能力
1.(1)①c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
②c(H+)+c(Na+)=c(CHCOO-)+c(OH-)
3
③c(H+)+c(CHCOOH)=c(OH-)
3
(2)①c(Na+)=2[c(CO)+c(HCO)+c(H CO)]
2 3
②c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)
③c(OH-)=c(H+)+2c(H CO)+c(HCO)
2 3
(3)①c(Na+)=c(HCO)+c(H CO)+c(CO)
2 3
②c(Na+)+c(H+)=c(OH-)+c(HCO)+2c(CO)
③c(OH-)+c(CO)=c(H+)+c(H CO)
2 3
2.(1)①c(NH)+c(H+)=c(Cl-)+c(OH-)
②2c(Cl-)=c(NH)+c(NH ·H O)
3 2
(2)①c(Na+)+c(H+)=c(CHCOO-)+c(OH-)+c(Cl-)
3
②c(Na+)=c(CHCOO-)+c(CHCOOH)=c(Cl-)
3 3
(3)①c(Na+)+c(H+)=c(OH-)+2c(CO)+c(HCO)
②2c(Na+)=3c(CO)+3c(HCO)+3c(H CO)
2 3
练真题 明考向
1.B 2.B 3.A
4.D [经过步骤①,100 mL 0.1 mol·L-1CaCl 水溶液和0.01 mol Na SO 反应的化学方程式
2 2 4
为CaCl + NaSO ===2NaCl+CaSO↓,生成0.02 mol NaCl和0.01 mol CaSO ,CaSO 微溶,
2 2 4 4 4 4
则溶液中含有SO和Ca2+,则c(Ca2+)+c(Na+)>c(Cl-),故A错误;步骤②中,CaSO(s)+
4
NaCO(aq)===CaCO (s)+NaSO (aq),步骤②中反应完全,则反应后的溶质为 0.01 mol
2 3 3 2 4
NaSO 、0.01 mol Na CO 和0.02 mol NaCl,则c(Na+)=6c(SO),故B错误;由B项分析可
2 4 2 3
知,存在元素守恒:c(Cl-)=2c(CO)+2c(HCO)+2c(H CO),故C错误;步骤③中,CaCO
2 3 3
+2CHCOOH===(CHCOO) Ca+HO+CO↑,反应后的溶液中含有 0.02 mol NaCl、0.01
3 3 2 2 2
mol (CHCOO) Ca,则c(CHCOOH)+c(CHCOO-)=c(Cl-),故D正确。]
3 2 3 3
5.(1)SbCl +HOSbOCl↓+2HCl(“”写成“===”亦可) 加盐酸,抑制水解
3 2
(2)10(3)c(CHCOO-)=c(NH)>c(H+)=c(OH-)
3
第 56 讲 溶液中的粒子平衡曲线分类突破
类型一
(1)CH COOH c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-) (2)CH COOH CHCOONa
3 3 3 3 3
c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+)>c(OH-) 2c(Na+) (3)CH COONa
3 3 3
CHCOOH c(Na+)=c(CHCOO-)>c(H+)=c(OH-) (4)CH COONa c(Na+)>c(CHCOO-)
3 3 3 3
>c(OH-)>c(H+) (5)CH COONa NaOH c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
3 3
对点训练
1.C 2.A
3 . D [ 滴 定 过 程 中 发 生 反 应 : NaOH + HSO ===NaHSO + HO 、 NaHSO +
2 3 3 2 3
NaOH===NaSO +HO。a 点溶液中的溶质为 NaHSO 和 HSO ,根据元素守恒得出,
2 3 2 3 2 3
c(H SO )+c(HSO)+c(SO)<0.1 mol·L-1,根据电离常数K =,此时溶液的pH=1.85,可
2 3 a1
推出c(HSO)=c(H SO ),代入上式得出,2c(H SO )+c(SO)<0.1 mol·L-1,故A正确;b
2 3 2 3
点加入20 mL NaOH溶液,NaOH和HSO 恰好完全反应生成NaHSO ,即溶质为NaHSO ,
2 3 3 3
根据质子守恒得 c(H SO )+c(H+)=c(SO)+c(OH-),故 B 正确;c 点溶质为 NaSO 和
2 3 2 3
NaHSO ,溶液显碱性,SO+HOHSO+OH-,根据水解平衡常数K (SO)==,c(OH-)
3 2 h
=,推出c(HSO)=c(SO)①,根据电荷守恒:c(Na+)+c(H+)=2c(SO)+c(HSO)+c(OH
-)②,将①代入②得c(Na+)+c(H+)=3c(HSO)+c(OH-),c点溶液显碱性,c(OH-)>c(H+),
显然:c(Na+)>3c(HSO),故 C 正确;d 点溶质为 NaSO ,溶液中离子浓度 c(Na
2 3
+)>c(SO)>c(HSO),故D错误。]
类型二
思考 HC OH++HC O,HC OH++C O,K ·K =,由于交点O时,c(H C O)=
2 2 4 2 2 2 a1 a2 2 2 4
c(C O),c2(H+)=K ·K = ,两边取负对数,即可得,pH=。
2 a1 a2 3
对点训练
1.B
2.D [NH CHCOOH中存在—COOH和—NH ,所以甘氨酸既有酸性又有碱性,故 A正
2 2 2
确;氨基具有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧根离
子反应,故曲线a表示NHCHCOOH的分布分数随溶液pH的变化,曲线b表示NHCHCOO-
2 2
的分布分数随溶液pH的变化,曲线c表示NH CHCOO-的分布分数随溶液pH的变化,故
2 2
B正确;NHCHCOO-+HONHCHCOOH+OH-的平衡常数K=,25 ℃时,根据a、b曲
2 2 2
线交点坐标(2.35,0.50)可知,pH=2.35时,c(NHCHCOO-)=c(NHCHCOOH),则K==10-
2 2
11.65,故C正确;由C项分析可知,=,根据b、c曲线交点坐标(9.78,0.50)分析可得电离平衡 NHCHCOO-NH CHCOO-+H+的电离常数 K=10-9.78,=,则×=×<1,即
2 2 2
c2(NHCHCOO-)>c(NHCHCOOH)·c(NH CHCOO-),故D错误。]
2 2 2 2
3.D
类型三
对点训练
1.C
2.D [横坐标取0时,曲线M对应pH约为5.4,曲线N对应pH约为4.4,因为是NaOH滴
定HX溶液,所以在酸性较强的溶液中会存在c(HX-)=c(H X),所以曲线N表示pH与lg
2 2
的变化关系,B正确;=1时,即lg=0,pH≈5.4,c(H+)=1×10-5.4 mol·L-1,K ==1×10
a2
-5.4,A正确;NaHX溶液中,c(HX-)>c(X2-),即<1,lg<0,此时溶液呈酸性,C正确;当
溶液呈中性时,由曲线M可知lg>0,>1,即c(X2-)>c(HX-),D错误。]
热点强化23
热点专练
1.C 2.C 3.C
4.C [x 时,氨的去除率为100%、总氮残余率为5%,n(NH )=0.006 mol·L-1×1 L=0.006
1 3
mol,
95%的氨气参与反应①,5%的氨气参与反应②,反应①消耗n(ClO-)=×3=0.008 55 mol,
1
反应②消耗n(ClO-)=4×0.006 mol×5%=0.001 2 mol,x =0.008 55 mol+0.001 2 mol=
2 1
0.009 75 mol,A错误;x>x 时,反应①也生成氯离子,所以c(Cl-)>4c(NO),B错误;x>x
1 1
时,氨去除率不变,x越大,总氮残余率越大,说明生成的硝酸根离子越多,生成N 的量越
2
少,C正确;x=x 时,氨的去除率为100%,溶液中没有NH和ClO-,含有Na+、H+、
1
NO、Cl-和OH-,根据电荷守恒得c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(NO),D错误。]
5.C 6.D
7.C [由图可知,pH=1,即c(H+)=0.1 mol·L-1时c([FeL]+)=1.0×10-4 mol·L-1,又
c(H L)=5.0×10-3 mol·L-1,根据 Fe3++HL[FeL]++2H+知,此时 c(H L)=(5.0-
0 2 2 2
0.1)×10-3 mol·
L-1=4.9×10-3 mol·L-1,结合K ==10-7.46知,此时c(HL-)=10-7.46×4.9×10-3×
a1
10 mol·L-1=4.9×10-9.46 mol·L-1,又pH=1时,c(OH-)=10-13 mol·L-1,故A错误;pH
在9.5~10.5之间时c([FeL ]3-)=c([FeL (OH)]2-)=10-4 mol·L-1,其中两种离子共含c(L2-)
3 2
=3×10-4 mol·L-1+2×10-4 mol·L-1=5×10-4 mol·L-1,当pH=10时,c(H+)=10-10
mol·L-1,根据K ===10-7.46,c(HL-)=102.54c(H L),即c(HL-)>c(H L),由K ==10-
a1 2 2 a2
12.4,得c(HL-)=102.4c(L2-),即c(HL-)>c(L2-),B、D错误;该反应的平衡常数K=,由题
图知,当c([FeL ]-)=c([FeL]+)时,pH=4,由K ·K =10-19.86=,得①式:10-19.86×c(H L)
2 a1 a2 2
=10-8c(L2-),此时c(H L)=5.0×10-3 mol·
2L-1-3×10-4 mol·L-1=4.7×10-3 mol·L-1,代入①式,c(L2-)= mol·L-1=4.7×10-14.86
mol·L-1,则K=≈2×1013.86,故lg K=13.86+lg 2≈14,C正确。]
第 57 讲 难溶电解质的沉淀溶解平衡
考点一
整合必备知识
2.(1)> = < (3)②右移 增大 右移 不变 左移 增大 右移 减小 左移 减
小 右移 减小
应用举例 ③>④>①>②
3.(1)cm(An+)·cn(Bm-) cm(An+)·cn(Bm-) 沉淀 平衡
未饱和 (2)①越小 越小 ②温度
应用举例
(1)能。溶解能力由大到小:AgCl>AgBr>AgI。
(2)K (AgCl)=c(Ag+)·c(Cl-)=c2(Ag+)=1.8×10-10,c(Ag+)≈1.34×10-5 mol·L-1,即AgCl
sp
的溶解浓度为1.34×10-5 mol·L-1;K [Mg(OH) ]=c(Mg2+)·c2(OH-)=4c3(Mg2+)=5.6×10-
sp 2
12,c(Mg2+)≈1.12×10-4 mol·L-1,即Mg(OH) 的溶解浓度为1.12×10-4 mol·L-1,则AgCl
2
更难溶。
提升关键能力
1.②③④⑤⑦
2.D
3.c(Ag+)==0.02 mol·L-1,c(Cl-)==0.04 mol·
L-1,Q=c(Ag+)·c(Cl-)=0.02×0.04=8.0×10-4>K ,所以有AgCl沉淀生成。
sp
4.(1)5 (2)6
5.三种阴离子浓度均为0.01 mol·L-1时,分别产生AgCl、AgBr和Ag CrO 沉淀,所需要
2 4
Ag+浓度依次为
c(Ag+)== mol·L-1=1.56×10-8 mol·L-1,
1
c(Ag+)== mol·L-1=7.7×10-11 mol·L-1,
2
c(Ag+)== mol·L-1=3×10-5 mol·L-1,沉淀时Ag+浓度最小的优先沉淀,因而沉淀的顺
3
序为Br-、Cl-、CrO。
考点二
整合必备知识
1.(3)CuO[或 Cu(OH) 或 CuCO 或 Cu (OH) CO] CuO 与 H+反应,促进 Fe3+水解生成
2 3 2 2 3
Fe(OH) 沉淀 氨水 Fe3+与NH ·H O反应生成Fe(OH) 沉淀 NaS NaS与Cu2+、Hg2+反
3 3 2 3 2 2
应生成沉淀2.(1)< 沉淀溶解的方向 (2)①Mg(OH) +2H+===Mg2++2HO Mg(OH) +2NH===Mg2+
2 2 2
+2NH ·H O
3 2
②PbSO (s)Pb2+(aq)+SO(aq),当加入CHCOONH 溶液时,Pb2+与CHCOO-结合生成
4 3 4 3
更难电离的(CHCOO) Pb,c(Pb2+)减小,Q(PbSO ) ②<
(3)①CaSO(s)+CO(aq)CaCO (s)+SO(aq)
4 3
②ZnS(s)+Cu2+(aq)CuS(s)+Zn2+(aq) PbS(s)+Cu2+(aq)CuS(s)+Pb2+(aq)
提升关键能力
1.B
2.C [向PbI 饱和溶液加入KI溶液,I-浓度增大,平衡PbI Pb2++2I-逆向移动,①②
2 2
中产生PbI 固体,A正确;b到c过程中加水稀释沉淀溶解平衡正向移动,①中固体质量减
2
小,B正确;向①中加水稀释c(I-)减小,则c(Pb2+)增大,c点时溶液中c(Pb2+):①>②,C
错误;b点为试管①加入蒸馏水稀释促进PbI 溶解,平衡正向移动,此时离子积小于溶度积,
2
则Q=c(Pb2+)·c2(I-)
3.①Fe(OH) ②2×10-7
3
4.(1)PbSO (s)+CO(aq)PbCO (s)+SO(aq) 反应 PbSO (s)+CO(aq)PbCO (s)+
4 3 4 3
SO(aq)的平衡常数K===≈3.4×105>105,PbSO 可以比较彻底的转化为PbCO
4 3
(2)反应BaSO(s)+CO(aq)BaCO (s)+SO(aq)的平衡常数K===≈0.04≪105,反应正向
4 3
进行的程度有限
第 58 讲 沉淀溶解平衡图像的分析
类型一对点训练
1.A 2.B
类型二
对点训练
1.B [K (Ag CrO)=c2(Ag+)·c(CrO)=(10-3)2×10-6=10-12,A 错误;在 T ℃时,
sp 2 4
Ag CrO(s)+2Cl-(aq)2AgCl(s)+CrO(aq)的平衡常数K=====2.5×107,B正确;开
2 4
始生成AgCl沉淀时所需c(Ag+)== mol·L-1=2×10-8 mol·L-1,开始生成Ag CrO 沉淀
2 4
时所需c(Ag+)==mol·L-1=10-5 mol·L-1,故先析出氯化银沉淀,C错误;在Ag CrO 饱
2 4
和溶液中加入KCrO 固体,可使沉淀溶解平衡逆向移动,则溶液中c(CrO)增大,c(Ag+)减
2 4
小,不可能由Y点到X点,D错误。]
2.D
类型三
2.(1)10-10 (2)= (3)a (4)b
对点训练
1.D
2.C [根据三种沉淀的溶度积常数,三种离子沉淀的先后顺序为I-、Br-、Cl-,根据滴定
图示,当滴入4.50 mL硝酸银溶液时,Cl-恰好沉淀完全,此时共消耗硝酸银的物质的量为
4.50×10-3 L×0.100 mol·L-1=4.5×10-4 mol,所以Cl-、Br-和I-均为1.5×10-4 mol。I-
先沉淀,所以a点有黄色沉淀AgI生成,原溶液中I-的浓度为=0.010 mol·L-1,故A、B错
误;当Br-沉淀完全时(Br-浓度为1.0×10-5 mol·L-1),溶液中的c(Ag+)== mol·L-1=
5.4×10-8 mol·L-1,则此时溶液中的c(Cl-)== mol·
L-1≈3.3×10-3 mol·L-1,原溶液中的c(Cl-)=c(I-)=0.010 mol·L-1,则已经有部分Cl-沉淀,
故C正确;b点加入了过量的硝酸银溶液,Ag+浓度最大,故D错误。]
类型四
2.(2)①减小 ②饱和 等于 ③饱和 大于 ④不饱和 小于
对点训练
1.C
2 . C [a 点 在 两 曲 线 右 上 方 , 对 应 的 c(Ag + )·c(Cl - )