文档内容
第 4 讲 氧化还原反应方程式的配平及计算
[复习目标] 1.掌握氧化还原反应方程式的配平方法及技巧。2.了解电子守恒法在化学计算
中的应用。
考点一 氧化还原反应方程式的配平
1.氧化还原反应方程式配平的基本原则
2.氧化还原反应方程式配平的一般步骤
1.正向配平
(1)______Cu+______HNO(稀)===______Cu(NO )+______NO↑+______HO
3 3 2 2
(2)______KI+______KIO +______HSO ===______I+______KSO +______HO
3 2 4 2 2 4 2
(3)______MnO+______H++______Cl-===______Mn2++______Cl↑+______HO
2 2
答案 (1)3 8 3 2 4 (2)5 1 3 3 3 3 (3)2 16 10 2 5 8
2.逆向配平
(1)______I +______NaOH===______NaI+______NaIO +______HO
2 3 2(2)______S+______KOH===______KS+______KSO +______HO
2 2 3 2
(3)______P +______KOH+______HO===______KPO +______PH ↑
4 2 3 4 3
答案 (1)3 6 5 1 3 (2)3 6 2 1 3 (3)2 9 3 3 5
3.含有未知数的配平
(1)______CO+______NO===______CO+______N
x 2 2
(2)______FeS+______HCl===__________S+______FeCl +______HS
x 2 2
(3)______Na S+______NaClO+______NaOH===______NaSO +______NaCl+______HO
2 x 2 4 2
答案 (1)2x 2 2x 1 (2) 2 (-1) 1 1 (3)1 (3x+1) (2x-2) x (3x+1) (x-1)
4.有机物参与的氧化还原反应方程式的配平
(1)______KClO + ______HC O + ______HSO ===______ClO ↑ + ______CO↑ +
3 2 2 4 2 4 2 2
______KHSO+______HO
4 2
(2)______CH ==CH + ______KMnO + ______HSO ===______KSO + ______MnSO +
2 2 4 2 4 2 4 4
______CO+______HO
2 2
(3)______C HOH + ______KCr O + ______HSO ===______KSO + ______Cr (SO ) +
2 5 2 2 7 2 4 2 4 2 4 3
______CHCOOH+______HO
3 2
答案 (1)2 1 2 2 2 2 2
(2)5 12 18 6 12 10 28
(3)3 2 8 2 2 3 11
5.缺项配平
(1)______ClO-+______Fe(OH) +________===______Cl-+______FeO+______HO
3 2
(2)______MnO+______HO+________===______Mn2++______O↑+______HO
2 2 2 2
(3)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有Al O、C、N、CO。
2 3 2
请将AlN之外的反应物与生成物分别填入以下空格内,并配平。
++=====AlN+
(4)将NaBiO 固体(黄色,微溶)加入MnSO 和HSO 的混合溶液里,加热,溶液显紫色(Bi3+
3 4 2 4
无色)。配平该反应的离子方程式:
NaBiO+Mn2++____===Na++Bi3++____+____
3
答案 (1)3 2 4OH- 3 2 5
(2)2 5 6H+ 2 5 8
(3)AlO 3C N 2 3CO
2 3 2
(4)5 2 14 H+ 5 5 2 MnO 7 HO
2
解析 (3)根据氮元素、碳元素的化合价变化,N 是氧化剂,C是还原剂,AlN为还原产物,
2
CO为氧化产物。
“三步法”突破缺项型氧化还原反应方程式的配平缺项方程式是指某些反应物或生成物在方程式中没有写出来,它们一般为水、酸(H+)或碱
(OH-),其配平一般规律为
条件 补项原则
酸性条件下 缺H或多O补H+,少O补HO
2
碱性条件下 缺H或多O补HO,少O补OH-
2
考点二 电子守恒法计算及应用
1.电子守恒法计算的原理
氧化剂得电子总数=还原剂失电子总数。
2.电子守恒法计算的流程
(1)找出氧化剂、还原剂及相应的还原产物和氧化产物。
(2)找准一个原子或离子得失电子数(注意化学式中粒子的个数)。
(3)根据题中物质的物质的量和得失电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值(高价-低价)=n(还原剂)×变价原子个数×化合价
变化值(高价-低价)。
一、利用电子守恒确定元素价态或物质组成
1.现有24 mL 0.05 mol·L-1的NaSO 溶液与20 mL 0.02 mol·L-1的KCr O 溶液恰好完全反
2 3 2 2 7
应。已知NaSO 可被KCr O 氧化为NaSO ,则元素Cr在还原产物中的化合价为________。
2 3 2 2 7 2 4
答案 +3
解析 根据氧化还原反应中得失电子守恒:0.05 mol·L-1×0.024 L×(6-4)=0.02 mol·L-1×0.020
L×2×(6-n),解得n=3。
2.NaS 在碱性溶液中可被 NaClO氧化为NaSO ,而NaClO被还原为NaCl,若反应中
2 x 2 4
NaS 与NaClO的物质的量之比为1∶16,则x的值为________。
2 x
答案 5
解析 ―→xNaSO,NaClO―→NaCl,
2 4
得关系式1×·x=16×2,解得x=5。
二、电子守恒在未配平方程式中的应用
3.在P+CuSO +HO―→Cu P+HPO +HSO (未配平)反应中,7.5 mol CuSO 可氧化P的
4 2 3 3 4 2 4 4
物质的量为________mol。生成1 mol Cu P时,参加反应的P的物质的量为________mol。
3答案 1.5 2.2
解析 设7.5 mol CuSO 可氧化P的物质的量为x,生成1 mol Cu P时,被氧化的P的物质的
4 3
量为y;根据得失电子守恒:7.5 mol×(2-1)=x×(5-0),解得x=1.5 mol;1 mol×3×(2-
1)+1 mol×[0-(-3)]=y×(5-0),解得y=1.2 mol,所以生成1 mol Cu P时,参加反应的P
3
的物质的量为1.2 mol+1 mol=2.2 mol。
三、多步反应得失电子守恒问题
4.取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生 8 960 mL的NO 气体
2
和672 mL的NO 气体(均已折算为标准状况),在反应后的溶液中加入足量的氢氧化钠溶液,
2 4
生 成 沉 淀 的 质 量 为 17.02 g 。 则 x 等 于
________________________________________________。
答案 9.20
解析 反应流程为
――→
x g=17.02 g-m(OH-),而OH-的物质的量等于镁、铜失去电子的物质的量,等于浓 HNO
3
得到电子的物质的量,即:n(OH-)=×1+×2×1=0.46 mol,所以x g=17.02 g-0.46
mol×17 g·mol-1=9.20 g。
5.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO 、NO 、NO的混合气体,将这些
2 2 4
气体与1.68 L O (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝
2
酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
________mL。
答案 60
解析 由题意可知,HNO,则Cu失去电子的物质的量与O 得到电子的物质的量相
3 2
等,即n(Cu)=2n(O )=2×=0.15 mol。根据元素守恒及NaOH和Cu(NO ) 的反应可得关系
2 3 2
式:n(NaOH)=2n[Cu(NO )]=2n(Cu)=0.3 mol,则V(NaOH)==0.06 L=60 mL。
3 2
四、电子守恒在氧化还原滴定中的应用
6.某废水中含有Cr O,为了处理有毒的Cr O,需要先测定其浓度:取20 mL废水,加入适
2 2
量稀硫酸,再加入过量的V mL c mol·L-1 (NH )Fe(SO ) 溶液,充分反应(还原产物为Cr3
1 1 4 2 4 2
+)。用c mol ·L-1 KMnO 溶液滴定过量的Fe2+至终点,消耗KMnO 溶液V mL。则原废
2 4 4 2
水中c(CrO)为_______________________________________________________________。
2
答案 mol·L-1
解析 Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO,5Fe2++MnO+8H+===5Fe3++Mn2++
2 2
4HO。根据得失电子守恒列等式:c mol·L-1×V mL×10-3 L ·mL-1=20 mL×10-3 L·mL-
2 1 1
1×6c(CrO)+5c mol·L-1×V mL×10-3 L·mL-1,解得c(CrO)= mol·L-1。
2 2 2 2课时精练
1.一定条件下,硝酸铵受热分解的化学方程式(未配平)为NH NO ―→HNO+N↑+HO,
4 3 3 2 2
下列说法错误的是( )
A.配平后HO的化学计量数为6
2
B.NH NO 既是氧化剂又是还原剂
4 3
C.该反应既是分解反应也是氧化还原反应
D.氧化产物和还原产物的物质的量之比为5∶3
答案 A
解析 5NH NO ===2HNO +4N↑+9HO,A错误;NH NO 中NH所含N元素价态升高,
4 3 3 2 2 4 3
部分NO所含N元素价态降低,则NH NO 既是氧化剂又是还原剂,B正确;该反应中反应
4 3
物只有一种,则属于分解反应,该反应中含有变价元素,则属于氧化还原反应,C正确;氧
化产物(5NH→N)和还原产物(3NO→N)的物质的量之比为∶=5∶3,D正确。
2 2
2.把图2中的物质补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平)。
对该氧化还原反应的离子方程式,下列说法不正确的是( )
A.IO是氧化剂,具有氧化性
B.氧化性:MnO>IO
C.氧化剂和还原剂的物质的量之比为5∶2
D.若有2个Mn2+参加反应,则转移10个电子
答案 B
解析 由题干信息得到该离子方程式为5IO+2Mn2++3HO===2MnO+5IO+6H+,IO中的
2
碘元素在反应中化合价降低,得电子,作氧化剂,具有氧化性,故 A正确;根据反应方程
式可知,该反应的氧化剂是IO,氧化产物是MnO,则氧化性强弱顺序是IO>MnO,故B错
误;根据方程式可知:氧化剂碘酸根离子和还原剂锰离子的物质的量之比为5∶2,故C正
确;根据离子方程式可知,有2个 Mn2+参加反应时,转移电子的个数是10个,故D正确。
3.已知反应:①SO +2Fe3++2HO===SO+2Fe2++W;
2 2
②Cr O+aFe2++bH+―→Cr3++Fe3++HO (未配平)
2 2
下列有关说法正确的是( )
A.方程式①中W为4OH-
B.还原性强弱:SO >Fe2+
2C.a=6,b=7
D.反应Cr O+3SO +2H+===2Cr3++3SO+HO不能发生
2 2 2
答案 B
解析 根据原子守恒并结合离子方程式两边离子所带电荷总数相等可知,反应①为SO +2Fe3
2
++2HO===SO+2Fe2++4H+,W为4H+,A错误;由反应①可知,还原性:SO >Fe2+,B
2 2
正确;反应②中,根据得失电子守恒可得,Cr O和Cr3+对应的化学计量数分别为1、2,Fe2
2
+和Fe3+对应的化学计量数均为6,则a=6,再结合离子方程式两边离子所带电荷总数相等
可得,b=14,C错误;Cr O具有强氧化性,SO 具有还原性,且由①、②可知氧化性:
2 2
Cr O>SO,则Cr O能将SO 氧化为SO,即反应Cr O+3SO +2H+===2Cr3++3SO+HO能
2 2 2 2 2 2
发生,D错误。
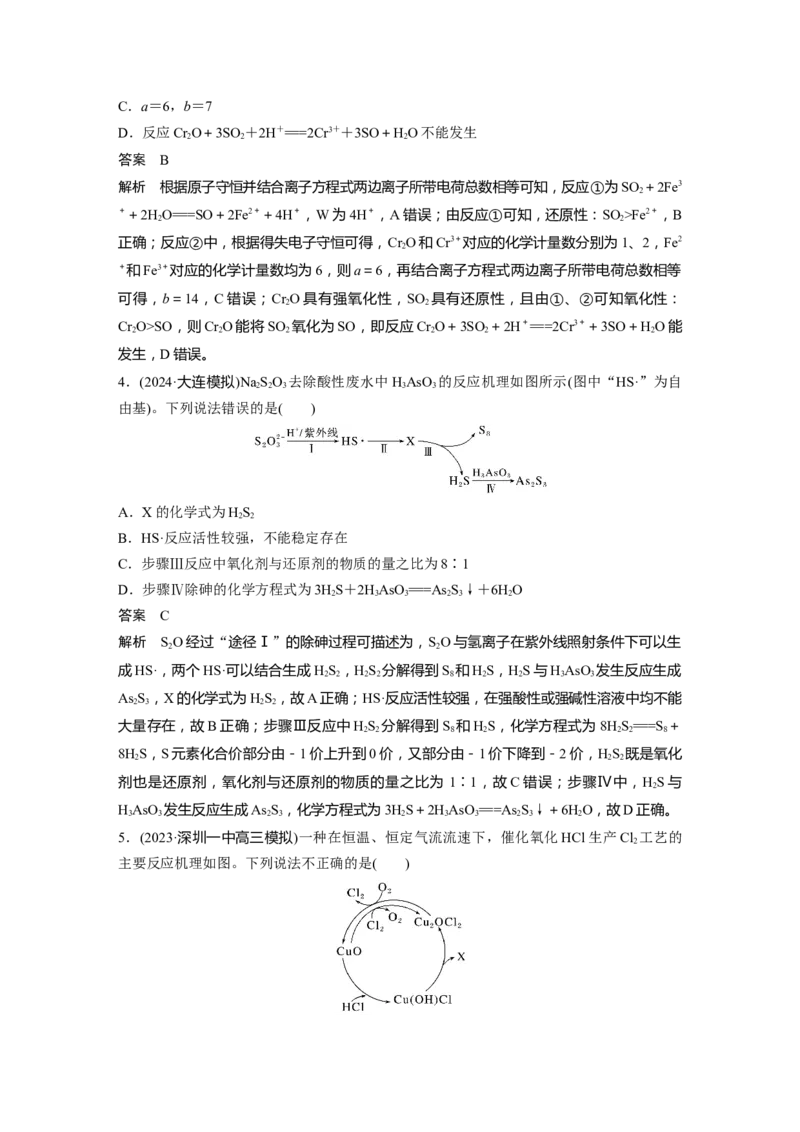
4.(2024·大连模拟)NaSO 去除酸性废水中HAsO 的反应机理如图所示(图中“HS·”为自
2 2 3 3 3
由基)。下列说法错误的是( )
A.X的化学式为HS
2 2
B.HS·反应活性较强,不能稳定存在
C.步骤Ⅲ反应中氧化剂与还原剂的物质的量之比为8∶1
D.步骤Ⅳ除砷的化学方程式为3HS+2HAsO ===As S↓+6HO
2 3 3 2 3 2
答案 C
解析 SO经过“途径Ⅰ”的除砷过程可描述为,SO与氢离子在紫外线照射条件下可以生
2 2
成HS·,两个HS·可以结合生成HS ,HS 分解得到S 和HS,HS与HAsO 发生反应生成
2 2 2 2 8 2 2 3 3
As S,X的化学式为HS,故A正确;HS·反应活性较强,在强酸性或强碱性溶液中均不能
2 3 2 2
大量存在,故B正确;步骤Ⅲ反应中HS 分解得到S 和HS,化学方程式为8HS===S +
2 2 8 2 2 2 8
8HS,S元素化合价部分由-1价上升到0价,又部分由-1价下降到-2价,HS 既是氧化
2 2 2
剂也是还原剂,氧化剂与还原剂的物质的量之比为 1∶1,故C错误;步骤Ⅳ中,HS与
2
HAsO 发生反应生成As S,化学方程式为3HS+2HAsO ===As S↓+6HO,故D正确。
3 3 2 3 2 3 3 2 3 2
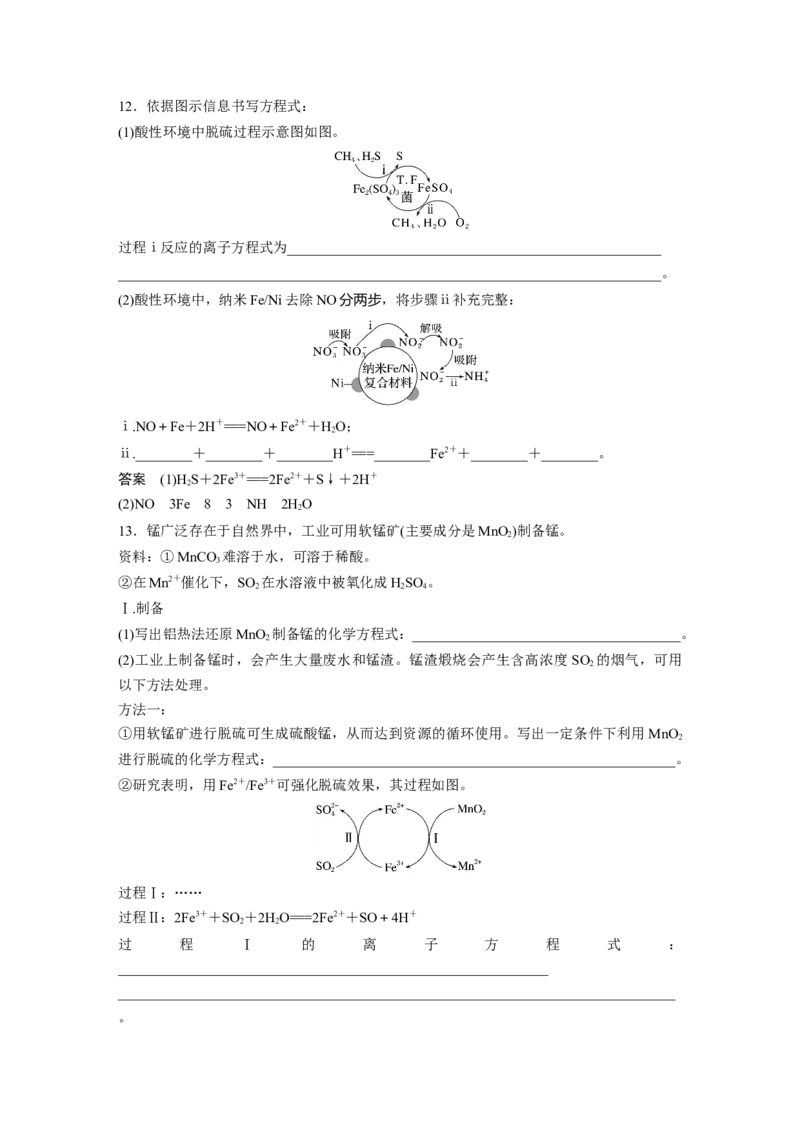
5.(2023·深圳一中高三模拟)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl 工艺的
2
主要反应机理如图。下列说法不正确的是( )A.该过程中Cu元素的化合价发生变化
B.Cu(OH)Cl、Cu OCl 均为中间产物
2 2
C.Cu(OH)Cl分解生成两种产物,物质X为HO
2
D.该过程涉及反应:2Cu OCl +O2Cl+4CuO
2 2 2 2
答案 A
解析 由反应历程图可知,该过程中含 Cu化合物CuO、Cu(OH)Cl、Cu OCl 中Cu元素的
2 2
化合价均为+2价,即保持不变,A项不正确;由反应历程图可知,反应前加入了 CuO,
CuO与HCl反应转化为Cu(OH)Cl,然后Cu(OH)Cl分解为Cu OCl 和HO,Cu OCl 与O 反
2 2 2 2 2 2
应又生成了CuO,则CuO为催化剂,Cu(OH)Cl、Cu OCl 均为中间产物,B、C项正确;由
2 2
反应历程图可知,该过程涉及Cu OCl 与O 反应生成CuO和Cl 的反应,根据氧化还原反应
2 2 2 2
配平可得2Cu OCl +O2Cl+4CuO,D项正确。
2 2 2 2
6.配平下列离子方程式:
(1)____NO+____Fe2++____H+===____NO↑+____Fe3++____HO
2
(2)____Mn2++____HO+____OH-===____MnO ↓+____HO
2 2 2 2
(3)____MnO +____SO+____H+===____Mn2++____SO+____HO
2 2
答案 (1)1 1 2 1 1 1 (2)1 1 2 1 2 (3)1 1 2 1 1 1
7.配平下列反应。
(1)____Li CO + ____C H O + ____FePO ===____LiFePO + ____CO↑ + ____HO +
2 3 6 12 6 4 4 2
____CO↑
2
(2)____(NH )MoO +____H=====____Mo+____NH +____HO
4 2 4 13 2 3 2
(3)____H S+____NO===____S+____HO+____N
2 x 2 2
(4)____FeCl ·6H O+____SOCl =====____FeCl +____SO ↑+____HCl↑
3 2 2 3 2
答案 (1)6 1 12 12 6 6 6 (2)1 12 4 2 13 (3)2x 2 2x 2x 1 (4)1 6 1
6 12
8.(1)[2022·全国甲卷,27(1)]工业上常用芒硝(Na SO ·10H O)和煤粉在高温下生产硫化钠,
2 4 2
同 时 生 成 CO , 该 反 应 的 化 学 方 程 式 为
_______________________________________________
_______________________________________________________________________________
。
(2)[2022·江苏,14(1)①]在弱碱性溶液中,FeS与CrO反应生成Fe(OH) 、Cr(OH) 和单质
3 3
S , 其 离 子 方 程 式 为
_________________________________________________________________。
答案 (1)Na SO ·10H O+4C=====NaS+4CO↑+10HO
2 4 2 2 2
(2)FeS+CrO+4HO===Fe(OH) +Cr(OH) +S+2OH-
2 3 3
9.[2021·全国甲卷,26(2)]以NaIO 为原料制备I 的方法是先向NaIO 溶液中加入计量的
3 2 3
NaHSO ,生成碘化物;再向混合溶液中加入NaIO 溶液,反应得到I 。上述制备I 的总反
3 3 2 2应的离子方程式为________________________________________________________________。
答案 2IO+5HSO===I+5SO+3H++HO
2 2
10.现代工业上用氧化锌烟灰(主要成分为ZnO,含少量Pb、CuO和As O)制取高纯锌的部
2 3
分工艺流程如图所示。
(1)已知:“溶浸”后浸出液中含[Zn(NH )]2+、[Cu(NH )]2+、AsCl等。写出该过程中生成
3 4 3 4
[Zn(NH )]2 + 的 相 关 离 子 方 程 式 :
3 4
____________________________________________________
_______________________________________________________________________________
。
(2)“氧化除杂”的目的是将“AsCl”转化为As O 胶体,再经吸附聚沉除去。写出氧化反应
2 5
的离子方程式:_______________________________________________________________
_______________________________________________________________________________
。
答 案 (1)ZnO + 2NH ·H O + 2NH===[Zn(NH )]2 + + 3HO (2)2AsCl + 2HO +
3 2 3 4 2 2 2
6NH ·H O===As O(胶体)+10Cl-+6NH+5HO
3 2 2 5 2
11.写出下列方程式。
(1)[2022·全国乙卷,26(3)(ⅱ)]在“酸浸”中,除加入醋酸(HAc),还要加入HO 。HO 促进
2 2 2 2
了 金 属 Pb 在 醋 酸 中 转 化 为 Pb(Ac) , 其 化 学 方 程 式 为
2
___________________________________
_______________________________________________________________________________
。
(2)[2022·湖南,17(2)①]TiO 与C、Cl ,在600 ℃的沸腾炉中充分反应后,混合气体中各组
2 2
分的分压如下表:
物质 TiCl CO CO Cl
4 2 2
分压/ MPa 4.59×10-2 1.84×10-2 3.70×10-2 5.98×10-9
该温度下,TiO 与C、Cl 反应的总化学方程式为____________________________________。
2 2
答案 (1)Pb+HO+2HAc===Pb(Ac) +2HO
2 2 2 2
(2)5TiO+6C+10Cl=====5TiCl +2CO+4CO
2 2 4 2
解析 (2)根据表中数据可知,该温度下C主要生成CO和CO,根据同温同体积下气体的压
2
强之比等于物质的量之比可知TiCl 、CO和CO 的物质的量之比约是5∶2∶4,所以TiO 与
4 2 2
C、Cl 反应的总化学方程式为5TiO+6C+10Cl=====5TiCl +2CO+4CO。
2 2 2 4 212.依据图示信息书写方程式:
(1)酸性环境中脱硫过程示意图如图。
过程ⅰ反应的离子方程式为_____________________________________________________
_____________________________________________________________________________。
(2)酸性环境中,纳米Fe/Ni去除NO分两步,将步骤ⅱ补充完整:
ⅰ.NO+Fe+2H+===NO+Fe2++HO;
2
ⅱ.________+________+________H+===________Fe2++________+________。
答案 (1)H S+2Fe3+===2Fe2++S↓+2H+
2
(2)NO 3Fe 8 3 NH 2HO
2
13.锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO )制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4
Ⅰ.制备
(1)写出铝热法还原MnO 制备锰的化学方程式:______________________________________。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度 SO 的烟气,可用
2
以下方法处理。
方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO
2
进行脱硫的化学方程式:_________________________________________________________。
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如图。
过程Ⅰ:……
过程Ⅱ:2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
过 程 Ⅰ 的 离 子 方 程 式 :
_____________________________________________________________
_______________________________________________________________________________
。方法二:
③ 用 MnCO 进 行 脱 硫 , 可 提 高 脱 硫 率 。 结 合 化 学 用 语 解 释 原 因 :
3
_________________________
________________________________________________________________________________
_______________________________________________________________________________
。
Ⅱ.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO ,将溶液中的Mn2+氧化为Mn3+,
4
用c mol·L-1 (NH ) Fe(SO ) 溶液进行滴定,达到滴定终点时,滴定管刻度由 V mL变为V
4 2 4 2 0 1
mL,废水中锰的含量为_______________________________________________________
g·mL-1。
答案 (1)4Al+3MnO =====3Mn+2Al O (2)①MnO +SO =====MnSO ②2Fe2++MnO
2 2 3 2 2 4 2
+4H+===Mn2++2Fe3++2HO ③溶液中存在平衡:MnCO (s)Mn2+(aq)+CO(aq),CO
2 3
消耗溶液中的H+,促进SO 溶解:SO +HOHSO H++HSO,Mn2+有催化作用,可
2 2 2 2 3
促进反应2SO +O+2HO=====2HSO 发生 (3)55c(V-V)×10-3
2 2 2 2 4 1 0
解析 (2)②据图可知过程Ⅰ中MnO 被Fe2+还原生成Mn2+,Fe2+被氧化为Fe3+,根据电子
2
守恒和元素守恒可得离子方程式为2Fe2++MnO +4H+===Mn2++2Fe3++2HO。(3)滴定时
2 2
发生反应Fe2++Mn3+===Fe3++Mn2+,所以n(Mn)=n(Mn3+)=n(Fe2+)=c(V -V)×10-3
1 0
mol,所取废水为1 mL,所以废水中锰的含量为55c(V-V)×10-3 g·mL-1。
1 0
14.(2023·北京,18节选)以银锰精矿(主要含Ag S、MnS、FeS)和氧化锰矿(主要含MnO )
2 2 2
为原料联合提取银和锰的一种流程示意图如下。
已知:酸性条件下,MnO 的氧化性强于Fe3+。
2
(1)“浸锰”过程是在HSO 溶液中使矿石中的锰元素浸出,同时去除FeS ,有利于后续银
2 4 2
的浸出;矿石中的银以Ag S的形式残留于浸锰渣中。
2
②在HSO 溶液中,银锰精矿中的FeS 和氧化锰矿中的MnO 发生反应,则浸锰液中主要的
2 4 2 2
金属阳离子有___________________________________________________________________。
(2)“浸银”时,使用过量 FeCl 、HCl 和 CaCl 的混合液作为浸出剂,将 AgS 中的银以
3 2 2
[AgCl ]-形式浸出。
2
①将“浸银”反应的离子方程式补充完整:
Fe3++Ag S+______________________+2[AgCl ]-+S
2 2
(3)“沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有______________________________________________________。
答案 (1)②Fe3+、Mn2+ (2)①2 4 Cl- 2 Fe2+ (3)①2[AgCl ]-+Fe===Fe2++2Ag+4Cl
2-、2Fe3++Fe===3Fe2+
解析 (1)②根据信息,在HSO 溶液中二氧化锰可将Fe2+氧化为Fe3+,自身被还原为Mn2
2 4
+,则浸锰液中主要的金属阳离子有Fe3+、Mn2+。(3)①铁粉可将[AgCl ]-还原为单质银,过
2
量的铁粉还可以与铁离子发生反应,因此离子方程式为2[AgCl ]-+Fe===Fe2++2Ag+4Cl
2
-、2Fe3++Fe===3Fe2+。