文档内容
第 8 讲 化学实验基础知识和技能
[复习目标] 1.了解化学实验室常用仪器的主要用途和使用方法。2.掌握化学实验的基本操
作。3.能识别常用危险化学品标识;了解实验室一般事故的预防和处理方法。
考点一 常用化学仪器及使用
1.可加热的仪器
(1)上述仪器中可直接加热的有____________________________________________________,
可间接(垫陶土网)加热的有__________。
答案 ①②③ ④⑤⑥⑦
(2)上述仪器中②、③、④B、⑦的名称分别为____、________、________、________。
答案 蒸发皿 坩埚 蒸馏烧瓶 三颈烧瓶
(3)实验室灼烧固体物质用坩埚,使用时注意:把坩埚放在三脚架上的泥三角上加热,取放
坩埚必须使用坩埚钳,加热完的坩埚应放在陶土网上冷却。
2.常用计量仪器
(1)实验仪器的“0”刻度①滴定管的“0”刻度在________。
②托盘天平的“0”刻度在标尺的最左边。
③量筒________“0”刻度。
(2)实验仪器的精确度
①托盘天平的精确度为________g。
②量筒的精确度为________mL。
③滴定管的精确度为________mL。
容量瓶、滴定管、量筒都属于玻璃计量仪器,都是在 20 ℃时标定的相应容积的刻度线,故
在20 ℃左右读数才准确;容量瓶、滴定管使用前必须检查________;容量瓶________刻度
线。
答案 (1)①上部 ③没有
(2)①0.1 ②0.1 ③0.01 是否漏水 只有一条
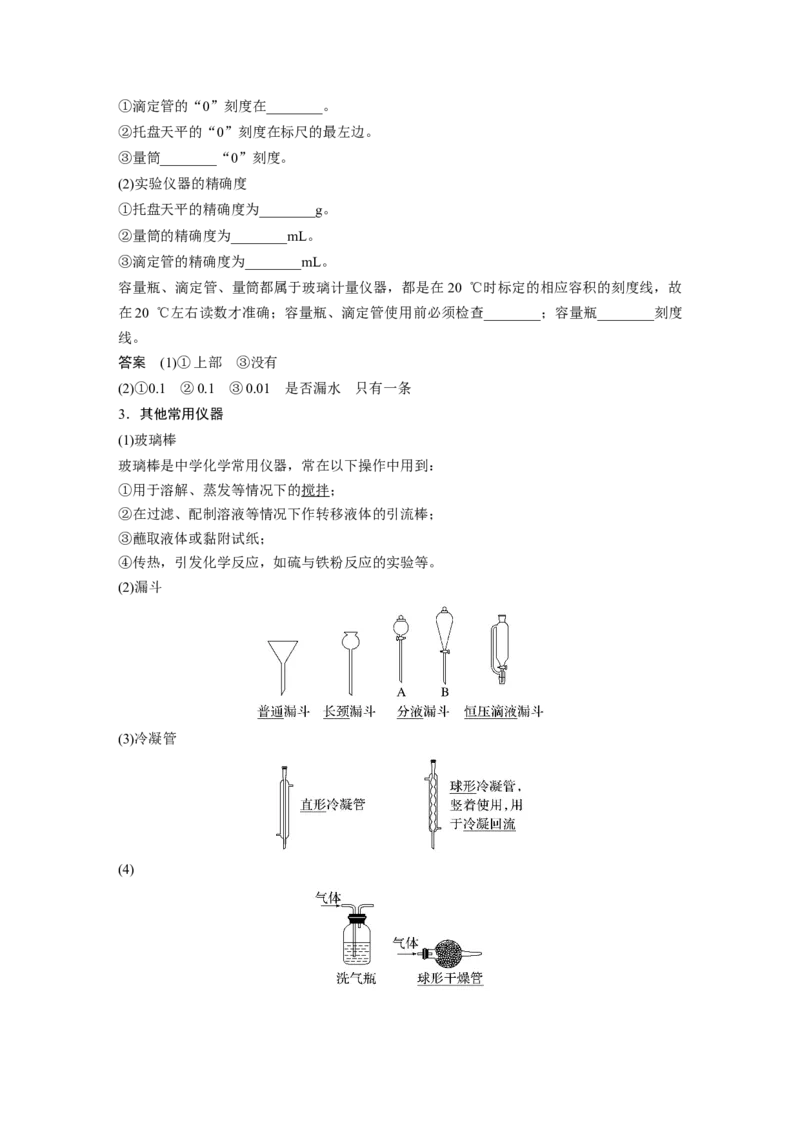
3.其他常用仪器
(1)玻璃棒
玻璃棒是中学化学常用仪器,常在以下操作中用到:
①用于溶解、蒸发等情况下的搅拌;
②在过滤、配制溶液等情况下作转移液体的引流棒;
③蘸取液体或黏附试纸;
④传热,引发化学反应,如硫与铁粉反应的实验等。
(2)漏斗
(3)冷凝管
(4)1.量筒、容量瓶、锥形瓶都是不能加热的玻璃仪器( )
2.容量瓶、滴定管使用前均需要检漏( )
3.用蒸发皿加热蒸发浓缩溶液时,必须垫上陶土网( )
4.用托盘天平称取11.75 g食盐( )
5.滴定管的“0”刻度在上端,量筒的“0”刻度在下端( )
6.选用瓷坩埚高温熔融NaCO 固体( )
2 3
答案 1.× 2.√ 3.× 4.× 5.× 6.×
一、仪器的选用与精确度
1.仪器的选用
(1)根据要求写出下列反应通常选用的反应器。
①较多量的金属钠与水反应(确保安全):____________________________________________。
②铁丝在氯气中燃烧:____________。
③灼烧氢氧化铁使之完全分解:____________________________________________________。
④用氢氧化钠溶液吸收尾气——氯气:_____________________________________________。
(2)下列实验应选用哪一种测量仪器(填名称)?
①量取6.5 mL水:__________________。
②量取6.50 mL盐酸:__________________。
③量取8.50 mL氢氧化钠溶液:__________________________________________________。
④称取6.5 g氯化钠粉末:_______________________________________________________。
⑤准确测定溶液的pH:__________________。
⑥配制500 mL一定物质的量浓度的溶液:__________________________________________。
(3)下列情况应选用哪一种漏斗(填名称)?
①制取氧气时向反应器中加双氧水:_______________________________________________。
②向酒精灯中添加酒精:____________。
③分离结晶出来的硝酸钾晶体:____________。
④将乙酸乙酯与饱和碳酸钠溶液分离:____________________________________________。
答案 (1)①烧杯 ②集气瓶 ③坩埚 ④烧杯
(2)①10 mL量筒 ②酸式滴定管 ③碱式滴定管 ④托盘天平 ⑤pH计 ⑥500 mL容量
瓶
(3)①分液漏斗 ②(普通)漏斗 ③(普通)漏斗 ④分液漏斗
2.量筒和滴定管的读数
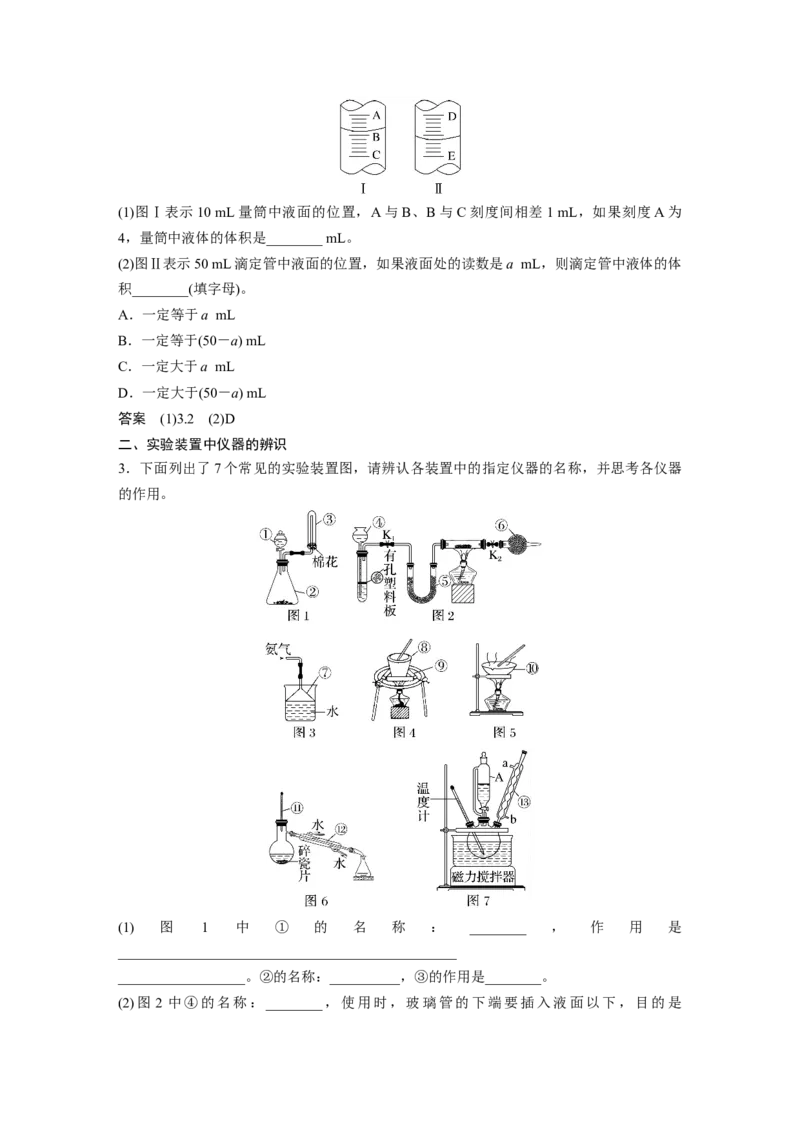
量筒和滴定管的构造、精确度都不同,都有不同的规格。(1)图Ⅰ表示10 mL量筒中液面的位置,A与B、B与C刻度间相差1 mL,如果刻度A为
4,量筒中液体的体积是________ mL。
(2)图Ⅱ表示50 mL滴定管中液面的位置,如果液面处的读数是a mL,则滴定管中液体的体
积________(填字母)。
A.一定等于a mL
B.一定等于(50-a) mL
C.一定大于a mL
D.一定大于(50-a) mL
答案 (1)3.2 (2)D
二、实验装置中仪器的辨识
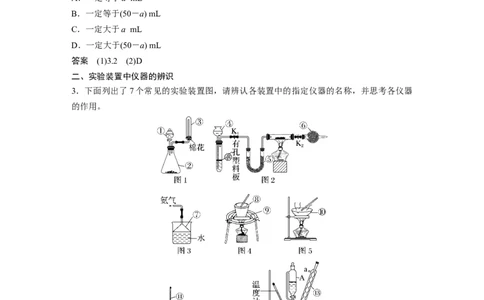
3.下面列出了7个常见的实验装置图,请辨认各装置中的指定仪器的名称,并思考各仪器
的作用。
(1) 图 1 中 ① 的 名 称 : ________ , 作 用 是
________________________________________________
__________________。②的名称:__________,③的作用是________。
(2)图 2 中④的名称:________,使用时,玻璃管的下端要插入液面以下,目的是__________。⑤的名称:________,⑥的名称:________。
(3)图3中仪器⑦的名称:________,其作用是__________________。
(4)图4中仪器⑧的名称:________,仪器⑨的名称:________,图5中仪器⑩的名称:
_______________________________________________________________________________。
(5)图6中仪器⑫的名称:________,图7中仪器⑬的名称:________________,仪器⑫不
能 换 成 仪 器 ⑬ 的 原 因 是
_____________________________________________________________。
图6中碎瓷片的作用是________________。
(6) 图 6 、 图 7 中 的 温 度 计 的 作 用 有 何 不 同 :
____________________________________________
____________。
答案 (1)(球形)分液漏斗 向反应器中添加液体药品,并能控制加入液体的多少 锥形瓶
收集气体 (2)长颈漏斗 防止气体逸出 U形管 球形干燥管 (3)漏斗 充分吸收氨气,
防倒吸 (4)坩埚 泥三角 蒸发皿 (5)直形冷凝管 球形冷凝管 冷凝后的液体容易残留
在球形区域内 防暴沸 (6)图6中温度计测定馏分的温度,图7中温度计测定反应体系的温
度
(1)若是加热仪器,蒸发或浓缩溶液用蒸发皿,灼烧固体用坩埚(莫忘玻璃棒搅拌)。
(2)若是量器,首先注意量程和精确度,粗量器(托盘天平和量筒)读出的数据为小数点后一位,
精量器(滴定管)读出的数据为小数点后两位。
(3)若是分离仪器,过滤用普通漏斗,分液用分液漏斗,蒸馏用蒸馏烧瓶。
考点二 化学实验基本操作与安全
1.试剂、药品的保存与取用
(1)根据物质的性质,选择试剂的保存方法
①根据药品状态
②根据见光是否分解
③根据酸碱性
④对于易变质、易挥发或有危险性的化学试剂,还应根据性质采取特殊的保存方法。
⑤常见试剂的保存方法总结
保存依据 保存方法 典型实例
防氧化 ①密封或用后立即盖好; ①NaSO 、NaS、KI溶液等用后立即盖好;
2 3 2②加入还原剂; ②向FeSO 溶液中加少量铁屑;
4
③隔绝空气 ③K、Na保存在煤油中,Li保存在石蜡中
防与CO NaOH、NaCO 溶液、石灰水、NaO 固体等密
2 2 3 2 2
密封保存,减少暴露时间
反应 封保存
①密封,置于阴凉处; ①浓盐酸、浓氨水等置于阴凉处;
防挥发
②液封 ②液溴用水封
置于冷暗处,不与氧化剂混
防燃烧 苯、汽油、酒精等
合贮存,严禁火种
保存在棕色瓶中,并置于阴
防分解 浓HNO、KMnO 溶液、AgNO 溶液、氯水等
3 4 3
暗处
向FeCl 溶液中加稀盐酸;
3
防水解 加入酸(碱)抑制水解
向NaS溶液中加 NaOH 溶液
2
①腐蚀橡胶的物质用玻璃塞
①浓HNO、酸性KMnO 溶液、氯水、溴水等腐
3 4
或塑料塞;
防腐蚀 蚀橡胶;
②腐蚀玻璃的物质用塑料容
②氢氟酸保存在塑料瓶中
器
防黏结 碱性溶液用橡胶塞 NaOH、NaCO、NaSiO 溶液等
2 3 2 3
(2)药品的取用
①根据药品的性状和用量选择取用方法
固体药品 液体药品
取用药品
粉末 块状 一定量 少量 多量 一定量
用托盘天 用试剂瓶 用量筒、滴定管
使用仪器 药匙或纸槽 镊子 胶头滴管
平称量 倾倒 或移液管量取
②向仪器中加入药品的操作方法
a.向容器内加固体药品
b.向容器内加液体药品
2.试纸的使用
(1)常用试纸类型及其作用
——定性检验溶液的酸碱性|
——定量检测酸碱性强弱(粗测)
|
——检验Cl 等具有强氧化性的物质
2
(2)使用方法
①检验溶液:取一小块试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液体,点在试
纸中部,观察试纸的颜色变化(若是测定pH,等试纸变色后,与标准比色卡对照读数)。
②检验气体:先用蒸馏水把试纸润湿,再用镊子夹取或粘在玻璃棒的一端,然后放在集气瓶
口或导管口处,观察试纸的颜色变化。
pH试纸使用时的注意事项
(1)不能直接将pH试纸浸入待测液中,否则会导致溶液受到污染。
(2)测溶液的酸碱度时,不能先用蒸馏水将pH试纸润湿,再向试纸上点滴待测液。如果是测
定气体的酸碱性,则需要把pH试纸先润湿,然后再测定。
(3)广泛pH试纸只能读出整数,比较粗略。
(4)不能用pH试纸测定具有漂白性、强氧化性试剂的pH。
3.物质的溶解
(1)固体物质的溶解
一般在烧杯或试管里进行,为了加速溶解,常采用玻璃棒搅拌、粉碎、振荡或加热等措施,
但FeCl 、AlCl 等易水解的固体溶解时不能加热。
3 3
(2)气体物质的溶解或吸收
①溶解度不大的气体,如CO、Cl、HS等,用图a所示装置。
2 2 2
②极易溶于水的气体,如NH 、HCl 等,用图b所示装置。
3
(3)液体物质的溶解(稀释)
一般把密度较大的液体加入密度较小的液体中,如浓硫酸的稀释、浓硫酸与浓硝酸的混合。
4.物质的加热
(1)固体的加热
①试管口要略向下倾斜,防止生成的水倒流,引起试管炸裂。
②先给试管均匀加热,受热均匀后再固定在药品部位加热。
(2)液体的加热①加热前,先把玻璃容器外壁上的水擦干,以免容器炸裂;试管夹夹在距离试管口的处,管
口向上倾斜,不得对人,以防液体沸腾时溅出烫伤人。
②试管内液体的体积不超过试管容积的。
(3)加热方式
加热方式 适用范围
直接加热 瓷制、金属制或小而薄的玻璃仪器(如试管)等
隔陶土网加热 较大的玻璃反应器(如烧杯、烧瓶等)
①需严格控制温度(如硝基苯的制备);
浴热(水浴、油浴、沙浴等)
②需反应混合液静置(如银镜反应);
优点:受热均匀,便于控制温度
③蒸馏沸点差较小的混合液
5.玻璃仪器的洗涤
(1)洗净的标准:玻璃仪器内壁附着均匀的水膜,既不聚集成滴,也不成股流下。
(2)洗涤方法:使用毛刷,用特殊试剂或蒸馏水冲洗。
(3)常见残留物的洗涤
残留物 洗涤剂
容器里附有的油污 NaOH 溶液或热的纯碱溶液
容器壁上附着的硫 CS 或热的 NaOH 溶液
2
试管壁上附着的银镜 稀 HNO
3
AgCl 氨水
容器内残留的MnO 热的浓盐酸
2
6.实验安全问题
(1)常用危险化学药品的标识
(2)常见实验事故的处理
实验事故 处理方法
碱液洒在皮肤上 立即用大量水冲洗,然后涂上1%的硼酸
酸液洒在皮肤上 立即用大量水冲洗,然后用3%~5% NaHCO 溶液冲洗
3误食重金属盐 服用大量牛奶、蛋清或豆浆
水银洒在桌面上 尽量回收,再用硫粉覆盖
酸液溅到眼中 立即用大量水冲洗,边洗边眨眼睛
酒精等有机物在实验台上着火 用湿抹布或沙土盖灭
液溴、苯酚沾在皮肤上 立即用酒精擦洗
金属钠、钾等着火 不能用泡沫灭火器、干粉灭火器和水扑灭,要用沙土盖灭
1.氯水或硝酸银溶液存放在配有磨口塞的棕色试剂瓶中( )
2.配制王水时,应将浓硝酸沿玻璃棒缓慢注入浓硫酸中( )
3.检查容量瓶是否漏水的方法是往瓶中注入适量的水,倒转检查是否漏水即可( )
4.用洁净干燥的玻璃棒蘸取漂白粉溶液,滴到放在表面皿上的pH试纸上测pH( )
5.用湿润的淀粉-KI试纸鉴别Br (g)和NO ( )
2 2
6.金属钙失火应使用泡沫灭火器来灭火( )
7.配制氯化铁溶液时,将FeCl 溶于蒸馏水,再加入一定量的铁粉( )
3
8.用氟化氢清洗做过硅酸分解实验的瓷坩埚( )
9.氯酸钾、高锰酸钾结块时,可放在研钵中先敲击成小块,再研碎( )
答案 1.√ 2.× 3.× 4.× 5.× 6.× 7.× 8.× 9.×
一、仪器使用或实验的第一步操作
1.指出下列仪器使用或实验的第一步操作。
(1) 气 体 的 制 取 与 性 质 探 究 实 验 :
____________________________________________________
______________。
(2) 点 燃 氢 气 或 甲 烷 等 可 燃 性 气 体 :
__________________________________________________
______________。
(3)用淀粉碘化钾试纸检验氯气:___________________________________________________。
(4)用托盘天平称量烧碱固体:_____________________________________________________。
(5)使用时第一步操作必须检查是否漏水的常见仪器有:_____________________________。
答案 (1)检查装置的气密性 (2)检验气体的纯度 (3)润湿试纸 (4)调天平平衡 (5)分液漏
斗、酸式滴定管、碱式滴定管、容量瓶
二、化学试剂的分类保存2.(2022·山东,2)下列试剂实验室保存方法错误的是( )
A.浓硝酸保存在棕色细口瓶中
B.氢氧化钠固体保存在广口塑料瓶中
C.四氯化碳保存在广口塑料瓶中
D.高锰酸钾固体保存在棕色广口瓶中
答案 C
解析 四氯化碳是一种有机溶剂,易挥发,且能够溶解塑料,故其不能保存在广口塑料瓶中,
应该保存在细口玻璃瓶中,C错误。
三、实验操作的正误判断及错因分析
3.请将下列实验中的错误操作可能会引起的不良后果填在表格中。
实验 向试管中加锌粒 对量筒中液体读数 稀释浓HSO
2 4
错误操作
不良后果
答案 试管底易破裂 读数偏低 量筒内液体表面的水会飞溅(或量筒会炸裂)
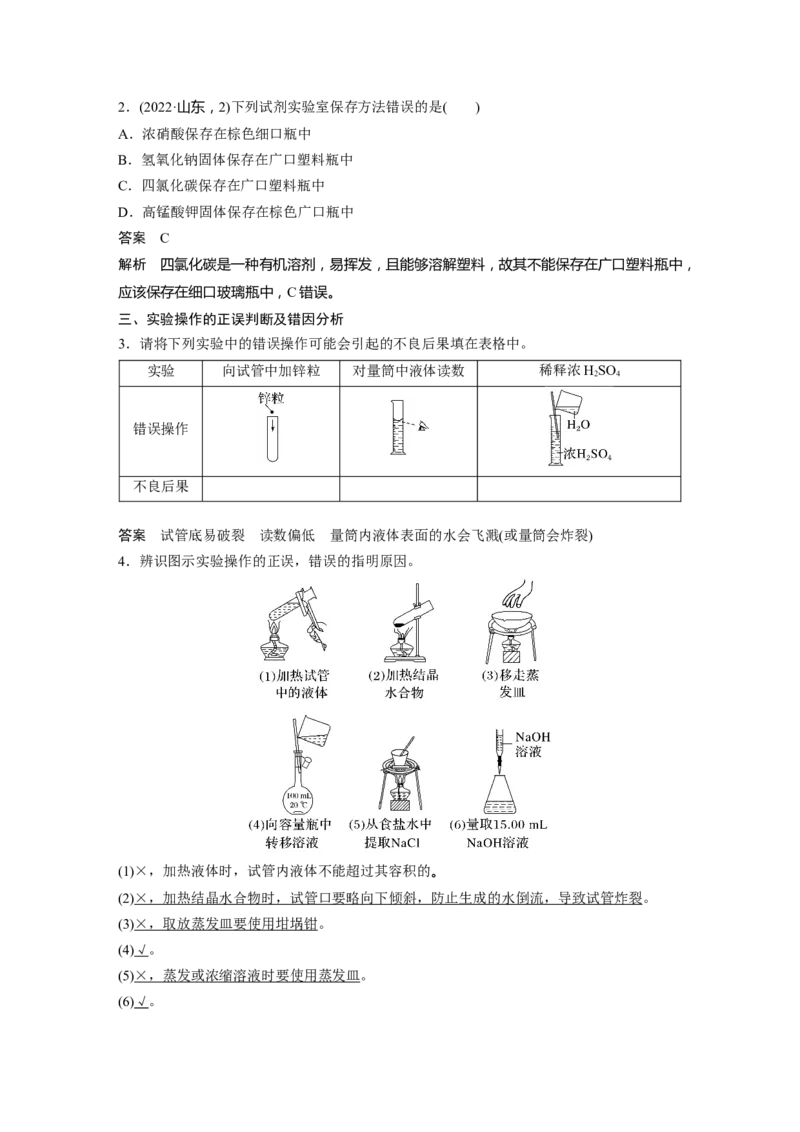
4.辨识图示实验操作的正误,错误的指明原因。
(1)×,加热液体时,试管内液体不能超过其容积的。
(2) × ,加热结晶水合物时,试管口要略向下倾斜,防止生成的水倒流,导致试管炸裂 。
(3) × ,取放蒸发皿要使用坩埚钳 。
(4)√。
(5) × ,蒸发或浓缩溶液时要使用蒸发皿 。
(6)√。1.(2023·山东,4)实验室安全至关重要,下列实验室事故处理方法错误的是( )
A.眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗
B.皮肤溅上碱液,先用大量水冲洗,再用2%的硼酸溶液冲洗
C.电器起火,先切断电源,再用二氧化碳灭火器灭火
D.活泼金属燃烧起火,用灭火毯(石棉布)灭火
答案 A
解析 眼睛溅进酸液,先用大量水冲洗,边洗边眨眼睛,并及时就医,故 A错误;活泼金
属会与水反应,所以其燃烧起火时,用灭火毯(石棉布)灭火,故D正确。
2.(2022·浙江6月选考,3)名称为“吸滤瓶”的仪器是( )
答案 D
解析 图示实验仪器A、B、C、D依次为蒸馏烧瓶、分液漏斗、容量瓶、吸滤瓶。
3.(2023·湖南,3)下列玻璃仪器在相应实验中选用不合理的是( )
A.重结晶法提纯苯甲酸:①②③
B.蒸馏法分离CHCl 和CCl :③⑤⑥
2 2 4
C.浓硫酸催化乙醇制备乙烯:③⑤
D.酸碱滴定法测定NaOH溶液浓度:④⑥
答案 A
解析 利用重结晶法来提纯苯甲酸,具体操作为加热溶解、趁热过滤和冷却结晶,此时用到
的玻璃仪器有漏斗、烧杯、玻璃棒,A选项不合理。
4.[2023·山东,18(3)]采用如下方法测定溶有少量HCl的SiHCl 纯度。
3
m g 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:
1
①____________,②____________(填操作名称),③称量等操作,测得所得固体氧化物质量
为m g,从下列仪器中选出①、②中需使用的仪器,依次为____________(填标号)。
2答案 高温灼烧 冷却干燥 A、C
解析 m g样品经水解、干燥等预处理过程得到硅酸水合物后,高温灼烧,在干燥器中冷
1
却干燥后,称量,所用仪器包括坩埚和干燥器。
课时精练
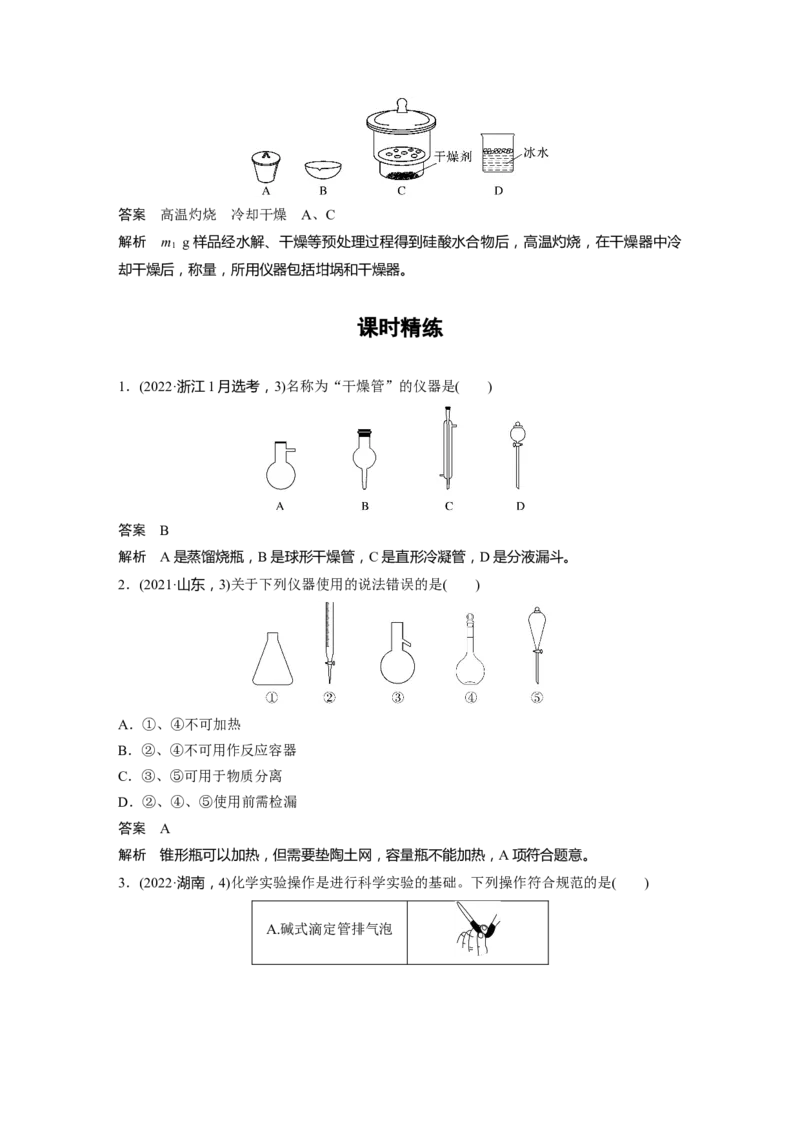
1.(2022·浙江1月选考,3)名称为“干燥管”的仪器是( )
答案 B
解析 A是蒸馏烧瓶,B是球形干燥管,C是直形冷凝管,D是分液漏斗。
2.(2021·山东,3)关于下列仪器使用的说法错误的是( )
A.①、④不可加热
B.②、④不可用作反应容器
C.③、⑤可用于物质分离
D.②、④、⑤使用前需检漏
答案 A
解析 锥形瓶可以加热,但需要垫陶土网,容量瓶不能加热,A项符合题意。
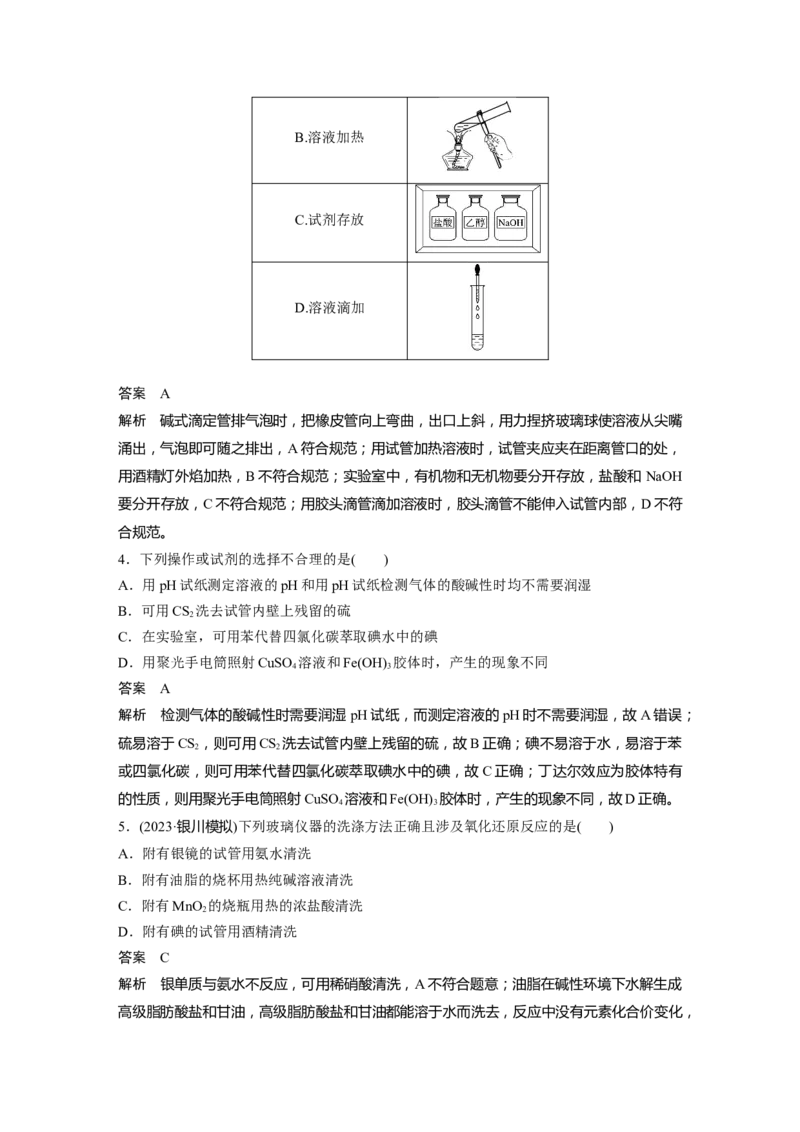
3.(2022·湖南,4)化学实验操作是进行科学实验的基础。下列操作符合规范的是( )
A.碱式滴定管排气泡B.溶液加热
C.试剂存放
D.溶液滴加
答案 A
解析 碱式滴定管排气泡时,把橡皮管向上弯曲,出口上斜,用力捏挤玻璃球使溶液从尖嘴
涌出,气泡即可随之排出,A符合规范;用试管加热溶液时,试管夹应夹在距离管口的处,
用酒精灯外焰加热,B不符合规范;实验室中,有机物和无机物要分开存放,盐酸和 NaOH
要分开存放,C不符合规范;用胶头滴管滴加溶液时,胶头滴管不能伸入试管内部,D不符
合规范。
4.下列操作或试剂的选择不合理的是( )
A.用pH试纸测定溶液的pH和用pH试纸检测气体的酸碱性时均不需要润湿
B.可用CS 洗去试管内壁上残留的硫
2
C.在实验室,可用苯代替四氯化碳萃取碘水中的碘
D.用聚光手电筒照射CuSO 溶液和Fe(OH) 胶体时,产生的现象不同
4 3
答案 A
解析 检测气体的酸碱性时需要润湿pH试纸,而测定溶液的pH时不需要润湿,故A错误;
硫易溶于CS ,则可用CS 洗去试管内壁上残留的硫,故B正确;碘不易溶于水,易溶于苯
2 2
或四氯化碳,则可用苯代替四氯化碳萃取碘水中的碘,故C正确;丁达尔效应为胶体特有
的性质,则用聚光手电筒照射CuSO 溶液和Fe(OH) 胶体时,产生的现象不同,故D正确。
4 3
5.(2023·银川模拟)下列玻璃仪器的洗涤方法正确且涉及氧化还原反应的是( )
A.附有银镜的试管用氨水清洗
B.附有油脂的烧杯用热纯碱溶液清洗
C.附有MnO 的烧瓶用热的浓盐酸清洗
2
D.附有碘的试管用酒精清洗
答案 C
解析 银单质与氨水不反应,可用稀硝酸清洗,A不符合题意;油脂在碱性环境下水解生成
高级脂肪酸盐和甘油,高级脂肪酸盐和甘油都能溶于水而洗去,反应中没有元素化合价变化,不属于氧化还原反应,B不符合题意;二氧化锰与热的浓盐酸反应生成氯气、氯化锰和水,
不溶性的二氧化锰转化为可溶性的氯化锰而洗去,反应中氯元素、锰元素的化合价发生变化,
属于氧化还原反应,C符合题意;碘能溶于酒精形成溶液,因此附有碘的试管用酒精清洗,
但属于物理变化,D不符合题意。
6.(2022·山东,6)实验室用基准NaCO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示
2 3
剂,并以盐酸滴定NaCO 标准溶液。下列说法错误的是( )
2 3
A.可用量筒量取25.00 mL Na CO 标准溶液置于锥形瓶中
2 3
B.应选用配带塑料塞的容量瓶配制NaCO 标准溶液
2 3
C.应选用烧杯而非称量纸称量NaCO 固体
2 3
D.达到滴定终点时溶液显橙色
答案 A
解析 量筒的精确度为0.1 mL,应该用碱式滴定管或移液管量取25.00 mL Na CO 标准溶液
2 3
置于锥形瓶中,A说法错误;NaCO 溶液显碱性,盛放NaCO 溶液的容器不能用玻璃塞,
2 3 2 3
以防碱性溶液腐蚀玻璃产生有黏性的硅酸钠而将瓶塞黏住,故应选用配带塑料塞的容量瓶配
制NaCO 标准溶液,B说法正确;NaCO 有吸水性且有一定的腐蚀性,故应选用烧杯而非
2 3 2 3
称量纸称量NaCO 固体,C说法正确;NaCO 溶液显碱性,甲基橙滴入NaCO 溶液中显黄
2 3 2 3 2 3
色,当滴入最后半滴盐酸时,溶液由黄色突变为橙色且半分钟内不变色即为滴定终点,D说
法正确。
7.洗涤玻璃仪器时,下列注意事项不正确的是( )
A.凡是已洗净的仪器,要用干布或纸擦干
B.灼热的玻璃仪器应冷却至室温后再洗涤,以防炸裂
C.洗涤时一般是先用水冲洗,若达不到要求再用其他方法洗涤
D.玻璃仪器洗净的标准是附着在玻璃仪器内壁上的水既不聚成水滴,也不成股流下
答案 A
解析 如果用干布或纸擦干仪器,则已洗净的仪器会重新附着其他杂质,故 A错误;温度
高的玻璃仪器遇水会发生炸裂,故B正确;洗涤时一般是先用水冲洗,洗不掉再用其他方
法洗涤,故C正确;洗过的玻璃仪器内壁附着的水既不聚成水滴也不成股流下时,表示仪
器已洗净,故D正确。
8.(2022·重庆,7)下列实验装置(夹持装置略)及操作正确的是( )
A.装置甲气体干燥 B.装置乙固液分离C.装置丙Cl 制备 D.装置丁pH测试
2
答案 A
解析 装置乙固液分离的过滤操作中缺少玻璃棒引流,且漏斗下端管口尖嘴处要紧贴烧杯内
壁,故B错误;二氧化锰与浓盐酸共热反应制备氯气,装置丙中缺少酒精灯加热,且反应
装置应选用圆底烧瓶,故C错误;测定溶液pH时,应将溶液滴在pH试纸中央,pH试纸不
能插入溶液中,故D错误。
9.下列关于实验中“先与后”的说法正确的是( )
①加热试管时,先均匀加热,后局部加热
②用排水法收集气体时,先移出导管,后熄灭酒精灯
③制取某气体时,先检查装置的气密性,后加试剂
④使用容量瓶、分液漏斗、滴定管前先检查是否漏液,后洗涤
⑤使用滴定管前,先用标准液润洗,后盛装标准液
A.除②外 B.除④外
C.除⑤外 D.全部正确
答案 D
解析 ①可防止试管因局部过热而炸裂,正确;②可防止仪器因液体倒流而炸裂,正确;⑤
如果不用标准液润洗,会造成误差,正确。
10.下列试剂保存方法的原因解释错误的是( )
选项 试剂 保存方法 原因
A NaH、CaC 均密封于广口瓶中 防止与空气中的水蒸气反应
2
B 液溴、少量白磷 均加水液封 防止挥发
C FeCl 溶液 加入少量铁屑和稀盐酸 防止氧化和水解
2
D HF溶液、NaF溶液 均用塑料瓶盛装 防止腐蚀
答案 B
解析 NaH、CaC 均易与水反应,所以应密封保存,A正确;液溴和少量白磷保存时均加水
2
液封,前者是为了防止液溴挥发,后者是为了防止白磷与空气中的氧气反应,B错误;
FeCl 中的Fe2+易被氧化、易水解,保存时,加入铁屑可防止Fe2+被氧化,加入稀盐酸可抑制
2
Fe2+水解,C正确;NaF水解可产生HF,HF易与玻璃中的SiO 反应,所以HF溶液和NaF
2
溶液都应用塑料瓶盛装,D正确。
11.(2023·济南一中模拟)某实验小组用如下实验用品检验黑木耳中铁元素。下列说法错误的
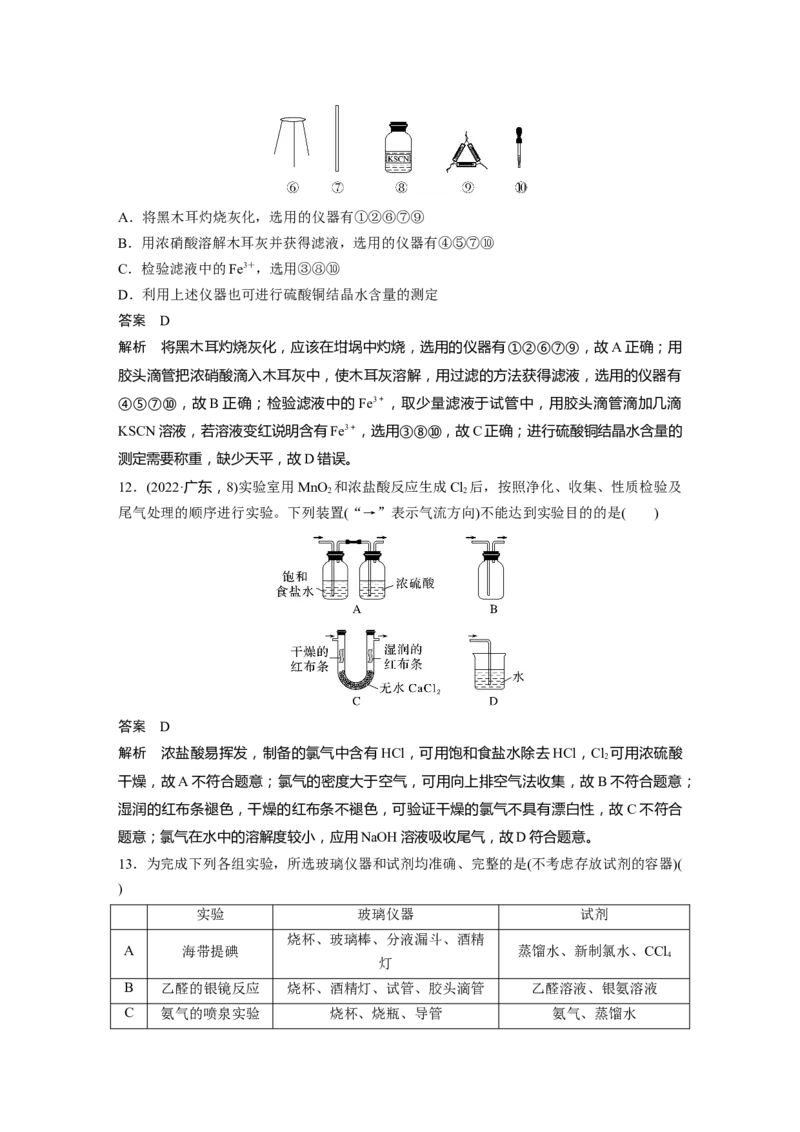
是( )A.将黑木耳灼烧灰化,选用的仪器有①②⑥⑦⑨
B.用浓硝酸溶解木耳灰并获得滤液,选用的仪器有④⑤⑦⑩
C.检验滤液中的Fe3+,选用③⑧⑩
D.利用上述仪器也可进行硫酸铜结晶水含量的测定
答案 D
解析 将黑木耳灼烧灰化,应该在坩埚中灼烧,选用的仪器有①②⑥⑦⑨,故A正确;用
胶头滴管把浓硝酸滴入木耳灰中,使木耳灰溶解,用过滤的方法获得滤液,选用的仪器有
④⑤⑦⑩,故B正确;检验滤液中的Fe3+,取少量滤液于试管中,用胶头滴管滴加几滴
KSCN溶液,若溶液变红说明含有Fe3+,选用③⑧⑩,故C正确;进行硫酸铜结晶水含量的
测定需要称重,缺少天平,故D错误。
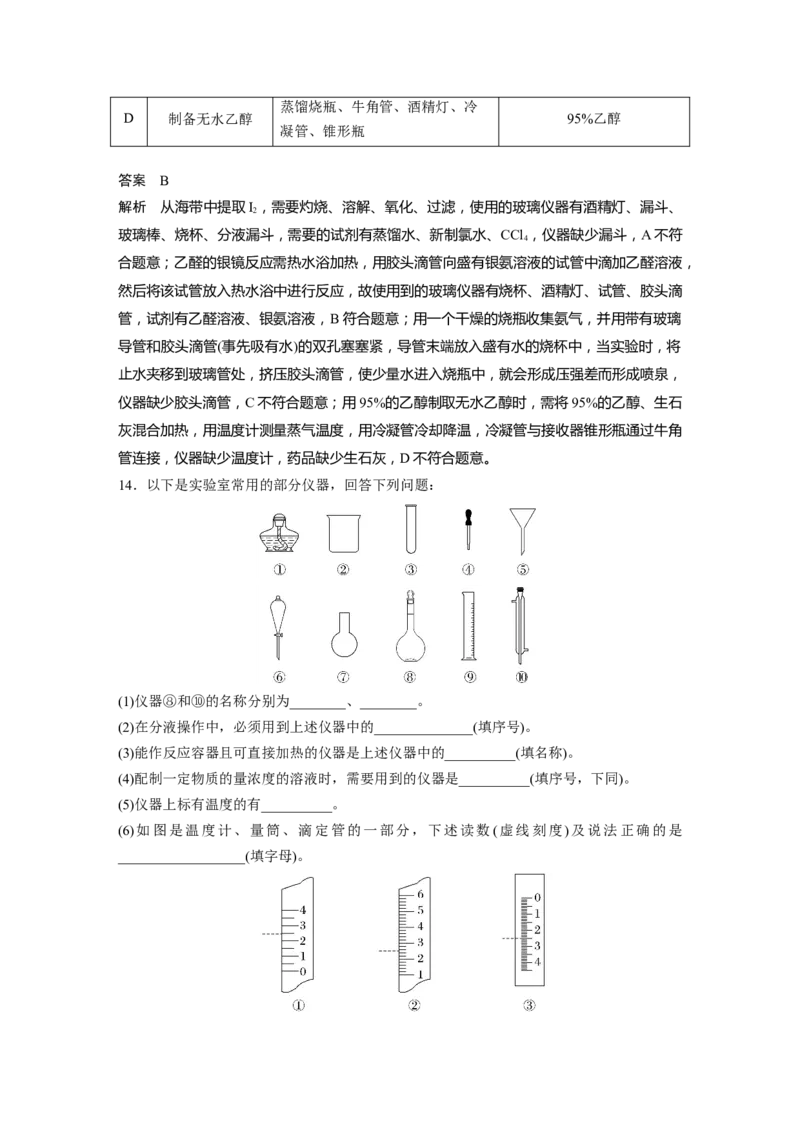
12.(2022·广东,8)实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验及
2 2
尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
答案 D
解析 浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用浓硫酸
2
干燥,故A不符合题意;氯气的密度大于空气,可用向上排空气法收集,故B不符合题意;
湿润的红布条褪色,干燥的红布条不褪色,可验证干燥的氯气不具有漂白性,故C不符合
题意;氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,故D符合题意。
13.为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂的容器)(
)
实验 玻璃仪器 试剂
烧杯、玻璃棒、分液漏斗、酒精
A 海带提碘 蒸馏水、新制氯水、CCl
4
灯
B 乙醛的银镜反应 烧杯、酒精灯、试管、胶头滴管 乙醛溶液、银氨溶液
C 氨气的喷泉实验 烧杯、烧瓶、导管 氨气、蒸馏水蒸馏烧瓶、牛角管、酒精灯、冷
D 制备无水乙醇 95%乙醇
凝管、锥形瓶
答案 B
解析 从海带中提取I ,需要灼烧、溶解、氧化、过滤,使用的玻璃仪器有酒精灯、漏斗、
2
玻璃棒、烧杯、分液漏斗,需要的试剂有蒸馏水、新制氯水、CCl ,仪器缺少漏斗,A不符
4
合题意;乙醛的银镜反应需热水浴加热,用胶头滴管向盛有银氨溶液的试管中滴加乙醛溶液,
然后将该试管放入热水浴中进行反应,故使用到的玻璃仪器有烧杯、酒精灯、试管、胶头滴
管,试剂有乙醛溶液、银氨溶液,B符合题意;用一个干燥的烧瓶收集氨气,并用带有玻璃
导管和胶头滴管(事先吸有水)的双孔塞塞紧,导管末端放入盛有水的烧杯中,当实验时,将
止水夹移到玻璃管处,挤压胶头滴管,使少量水进入烧瓶中,就会形成压强差而形成喷泉,
仪器缺少胶头滴管,C不符合题意;用95%的乙醇制取无水乙醇时,需将95%的乙醇、生石
灰混合加热,用温度计测量蒸气温度,用冷凝管冷却降温,冷凝管与接收器锥形瓶通过牛角
管连接,仪器缺少温度计,药品缺少生石灰,D不符合题意。
14.以下是实验室常用的部分仪器,回答下列问题:
(1)仪器⑧和⑩的名称分别为________、________。
(2)在分液操作中,必须用到上述仪器中的______________(填序号)。
(3)能作反应容器且可直接加热的仪器是上述仪器中的__________(填名称)。
(4)配制一定物质的量浓度的溶液时,需要用到的仪器是__________(填序号,下同)。
(5)仪器上标有温度的有__________。
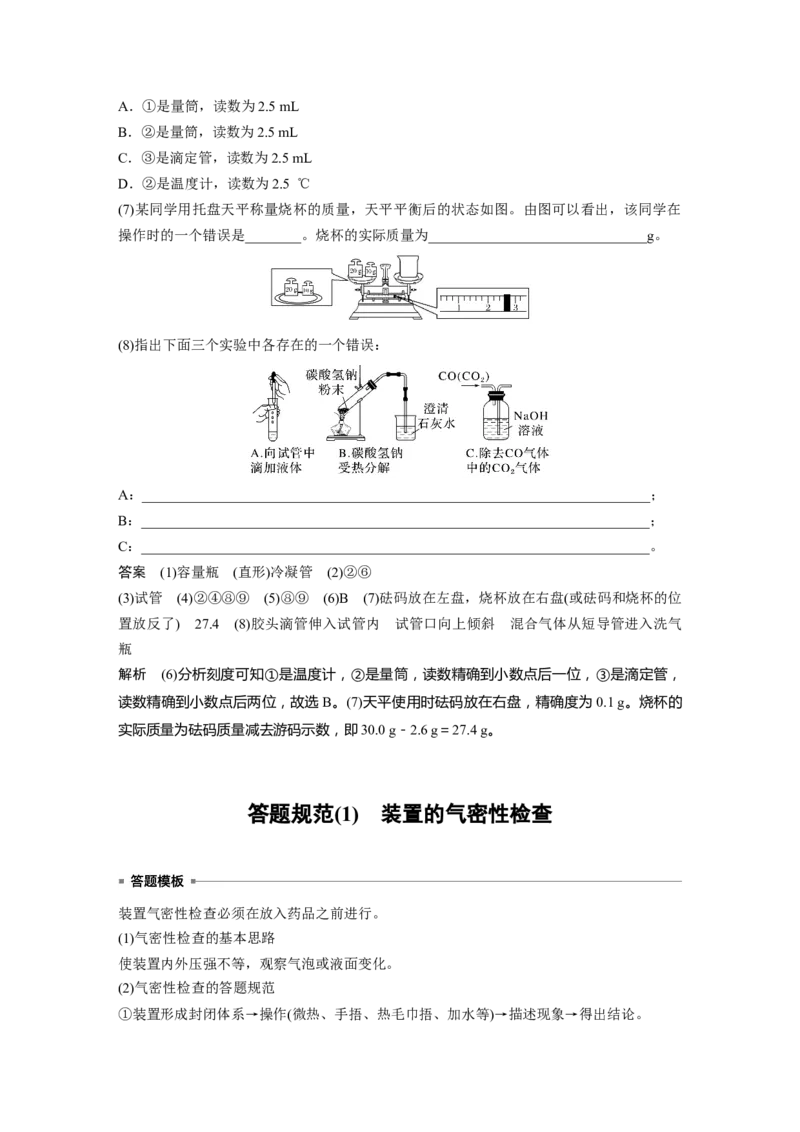
(6)如图是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是
__________________(填字母)。A.①是量筒,读数为2.5 mL
B.②是量筒,读数为2.5 mL
C.③是滴定管,读数为2.5 mL
D.②是温度计,读数为2.5 ℃
(7)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图。由图可以看出,该同学在
操作时的一个错误是________。烧杯的实际质量为_______________________________g。
(8)指出下面三个实验中各存在的一个错误:
A:________________________________________________________________________;
B:________________________________________________________________________;
C:________________________________________________________________________。
答案 (1)容量瓶 (直形)冷凝管 (2)②⑥
(3)试管 (4)②④⑧⑨ (5)⑧⑨ (6)B (7)砝码放在左盘,烧杯放在右盘(或砝码和烧杯的位
置放反了) 27.4 (8)胶头滴管伸入试管内 试管口向上倾斜 混合气体从短导管进入洗气
瓶
解析 (6)分析刻度可知①是温度计,②是量筒,读数精确到小数点后一位,③是滴定管,
读数精确到小数点后两位,故选B。(7)天平使用时砝码放在右盘,精确度为0.1 g。烧杯的
实际质量为砝码质量减去游码示数,即30.0 g-2.6 g=27.4 g。
答题规范(1) 装置的气密性检查
装置气密性检查必须在放入药品之前进行。
(1)气密性检查的基本思路
使装置内外压强不等,观察气泡或液面变化。
(2)气密性检查的答题规范
①装置形成封闭体系→操作(微热、手捂、热毛巾捂、加水等)→描述现象→得出结论。②微热法检查的关键词是封闭、微热、气泡、水柱。
③液差(封)法的关键词是封闭、液差。
④答题时易忽略的几句关键性的文字叙述:
a.将导管末端浸入水中;
b.关闭或者开启某些气体通道的活塞或弹簧夹;
c.加水至“将长颈漏斗下口浸没”。
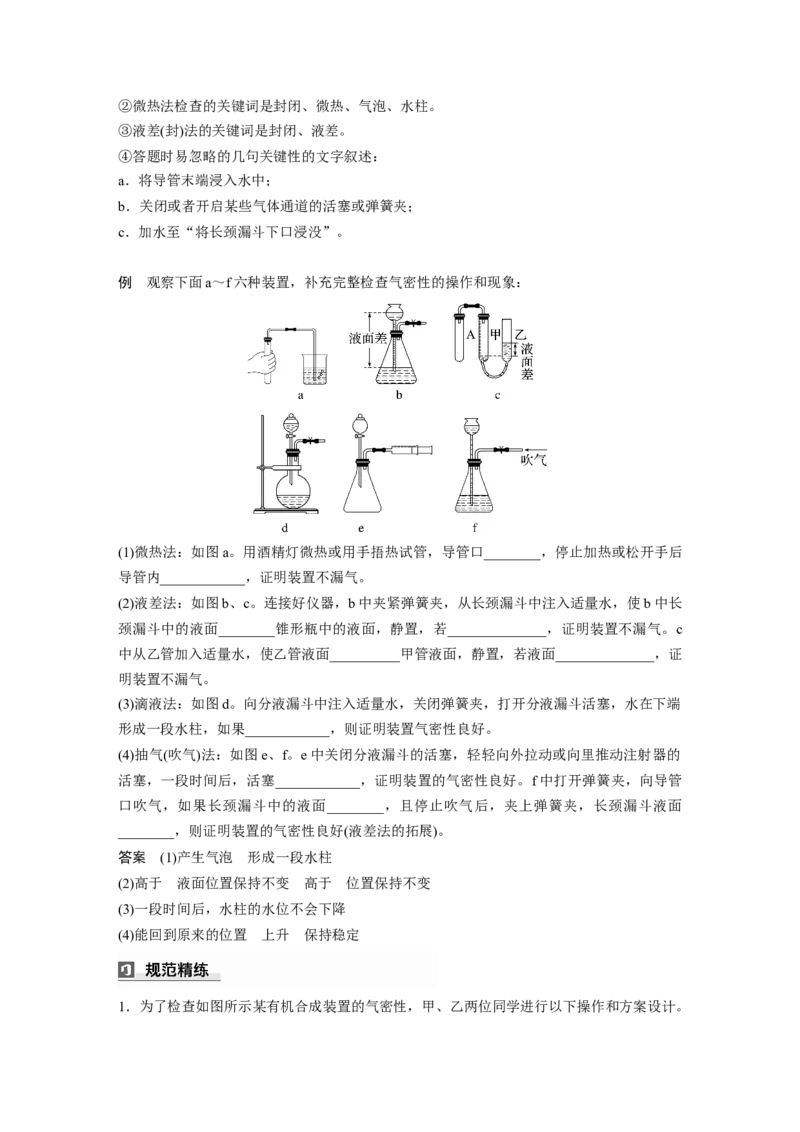
例 观察下面a~f六种装置,补充完整检查气密性的操作和现象:
(1)微热法:如图a。用酒精灯微热或用手捂热试管,导管口________,停止加热或松开手后
导管内____________,证明装置不漏气。
(2)液差法:如图b、c。连接好仪器,b中夹紧弹簧夹,从长颈漏斗中注入适量水,使b中长
颈漏斗中的液面________锥形瓶中的液面,静置,若______________,证明装置不漏气。c
中从乙管加入适量水,使乙管液面__________甲管液面,静置,若液面______________,证
明装置不漏气。
(3)滴液法:如图d。向分液漏斗中注入适量水,关闭弹簧夹,打开分液漏斗活塞,水在下端
形成一段水柱,如果____________,则证明装置气密性良好。
(4)抽气(吹气)法:如图e、f。e中关闭分液漏斗的活塞,轻轻向外拉动或向里推动注射器的
活塞,一段时间后,活塞____________,证明装置的气密性良好。f中打开弹簧夹,向导管
口吹气,如果长颈漏斗中的液面________,且停止吹气后,夹上弹簧夹,长颈漏斗液面
________,则证明装置的气密性良好(液差法的拓展)。
答案 (1)产生气泡 形成一段水柱
(2)高于 液面位置保持不变 高于 位置保持不变
(3)一段时间后,水柱的水位不会下降
(4)能回到原来的位置 上升 保持稳定
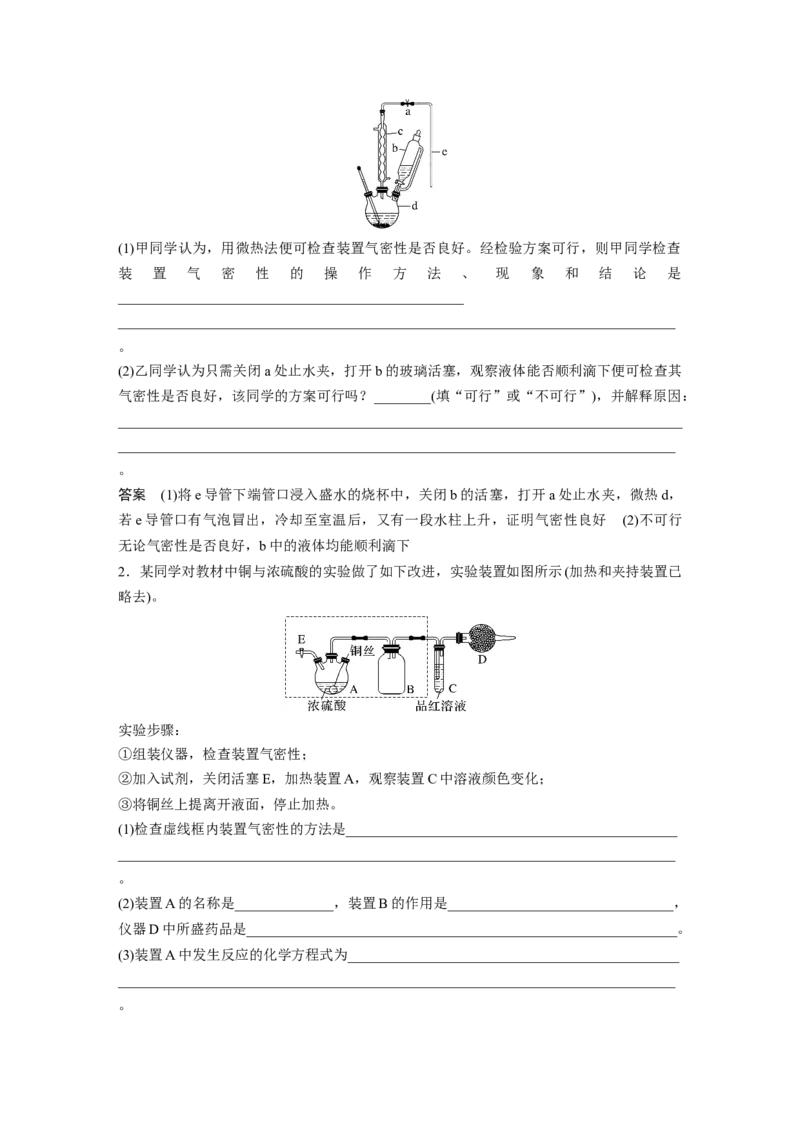
1.为了检查如图所示某有机合成装置的气密性,甲、乙两位同学进行以下操作和方案设计。(1)甲同学认为,用微热法便可检查装置气密性是否良好。经检验方案可行,则甲同学检查
装 置 气 密 性 的 操 作 方 法 、 现 象 和 结 论 是
_________________________________________________
_______________________________________________________________________________
。
(2)乙同学认为只需关闭a处止水夹,打开b的玻璃活塞,观察液体能否顺利滴下便可检查其
气密性是否良好,该同学的方案可行吗?________(填“可行”或“不可行”),并解释原因:
________________________________________________________________________________
_______________________________________________________________________________
。
答案 (1)将e导管下端管口浸入盛水的烧杯中,关闭b的活塞,打开a处止水夹,微热d,
若e导管口有气泡冒出,冷却至室温后,又有一段水柱上升,证明气密性良好 (2)不可行
无论气密性是否良好,b中的液体均能顺利滴下
2.某同学对教材中铜与浓硫酸的实验做了如下改进,实验装置如图所示(加热和夹持装置已
略去)。
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭活塞E,加热装置A,观察装置C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检查虚线框内装置气密性的方法是_______________________________________________
_______________________________________________________________________________
。
(2)装置A的名称是______________,装置B的作用是________________________________,
仪器D中所盛药品是_____________________________________________________________。
(3)装置A中发生反应的化学方程式为_______________________________________________
_______________________________________________________________________________
。(4) 实 验 后 , 拆 除 装 置 前 , 为 避 免 有 害 气 体 的 泄 漏 , 应 当 采 取 的 操 作 是
________________________________________________________________________________
_______________________________________________________________________________
。
(5)实验后装置A中有白色固体产生,将装置A中固液混合物缓慢转移至盛有少量水的烧杯
中,可观察到的现象是___________________________________________________________。
不 可 直 接 向 装 置 A 中 加 水 的 原 因 是
__________________________________________________
_______________________________________________________________________________
。
答案 (1)关闭活塞E,C中加水没过长导管口,加热A,C中长导管口有气泡冒出,撤去热
源后,长导管内有倒吸产生的液柱,且一段时间内高度保持不变,证明装置气密性良好
(2)三颈烧瓶 防倒吸 碱石灰(或NaOH等合理答案均可)
(3)2H SO (浓)+Cu=====CuSO +SO ↑+2HO
2 4 4 2 2
(4)打开活塞E,从E管口向A中鼓入大量空气
(5)白色固体溶解,溶液变为蓝色 反应后的混合液中含有浓硫酸,若将水加入浓硫酸中,
会放出大量热而使液体飞溅